一种普芦卡必利中间体的制备方法与流程
1.本发明属于药物合成技术领域,具体涉及一种普芦卡必利中间体4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的制备方法。
背景技术:
2.琥珀酸普芦卡必利(prucalopride succinate),化学名为4-氨基-5-氯-2,3-二氢-n-[1-(3-甲氧基丙基)-4-哌啶基]-7-苯并呋喃甲酰胺丁二酸盐,是比利时movetis公司开发的新一代高选择性、高亲和力的5-羟色胺4(5-ht4)受体激动药,它通过对肠道壁的直接作用恢复受损的肠道活动能力。2009年10月欧盟批准其用于治疗慢性便秘,2010年1月在德国上市,同年3月在英国上市,2012年10月经fda批准上市,临床研究表明该药对严重慢性便秘患者疗效恒定且安全,其化学结构式如下:
[0003][0004]
目前关于普芦卡必利的制备公开的方法较多,其中多数(如文献普卡必利的合成,药学与临床研究,2011,aug;19(4):306-307及专利cn1164233a(cn1071332c)、cn103664912b等)涉及4-氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸即式ii的合成,然后中间体ii与1-(3-甲氧基丙基)-4-哌啶胺经酰胺化反应制得终产物普芦卡必利。
[0005][0006]
由上可知,4-氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸即式ii作为制备普芦卡必利的关键中间体,直接影响该药品的生产、市场供应和质量问题。相关化学结构式如下:
[0007][0008]
目前关于4-氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸的合成主要有以下方法:
[0009]
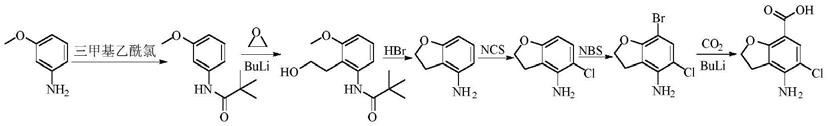
专利us5374637(cn1045781,ep389037)及文献j.het.chem.,1980,17(6):1333-1335以间甲氧基苯胺为原料,经特戊酰基保护,在丁基锂作用下羟乙基化、环合、氯代、溴代,最后在丁基锂作用下与二氧化碳反应得到,收率约18%,该路线两次使用丁基锂和气体反应物质(环氧乙烷、二氧化碳),需要-78℃低温非均相反应,并且其己烷溶液易燃,价格也比较昂贵,且氯代产生的异构体需经柱色谱分离,不适合工业放大。
[0010][0011]
文献chem.pharm.bull.,1998,46(1),42-52和普卡必利的合成,药学与临床研究,2011,(4),306-307及专利cn104016949a则以4-乙酰氨基-2-羟基苯甲酸甲酯为起始物料与3-溴丙-1-烯反应后,经fries重排反应、oso4/naio4氧化反应、nabh4还原反应、mitsunobu反应扣环、氯代反应、水解反应制得目标产品。但是该合成路线氧化步骤中需要使用剧毒、昂贵的四氧化锇试剂,同时在环化步骤中使用有毒的三苯基膦,产物须经柱层析提纯,且产率较低,不适合工业大规模生产。
[0012][0013]
专利cn103012337a则对上述工艺进行了改进,采用臭氧代替四氧化锇进行氧化,同时环化反应前引入磺酸酯作为离去基团,但是该方法步骤较长,操作繁琐,起始化合物价格昂贵,难以获得,且需要使用具有腐蚀性、刺激性以及基因毒性的烷基磺酰氯,整体收率较低,难于工业化放大生产。
[0014][0015]
专利cn102942542a采用相同策略制备目标产品,以三氯化钌或其水合物/高碘酸盐复合催化剂氧化制备醛基,同时环化反应前以卤素、对甲苯磺酰氧基、三氟甲基磺酰氧基、甲磺酰氧基或苯磺酰氧基作为离去基团。
[0016]
专利cn104529960a则采用4-氨基-2-羟基苯甲酸甲酯为起始物料,先用三氟乙酰基保护氨基,再与经friedel-crafts酰基化反应引入氯乙酰基,然后依次经环化、还原、氯代、水解等反应制得目标产品。但是该工艺采用价格较高的三氟乙酸酐引入保护基团,同时采用毒性、危险性较大的raney ni作为催化剂,难于工业化放大生产。
[0017][0018]
专利cn106316998a则对上述工艺进行了改进,该工艺以2-甲氧基-4-乙酰氨基-5-氯苯甲酸甲酯为起始物料来制备目标产品。但是采用剧毒物质水合肼进行还原,操作危险性较大,同时由于水合肼碱性较强,使得底物结构中的酯键和酰胺键极易胺解,同样不具备放大条件。
[0019][0020]
chemical process research,vol.870,chapter 8,washington:american chemical society,2003,125-139则以4-乙酰氨基-5-氯水杨酸甲酯(4-乙酰胺基-2-羟基-5-氯苯甲酸甲酯)为原料,经溴代、溴乙基化、环合及水解反应得到,反应条件温和,收率29%。该工艺在最后的水解反应存在较多问题,例如:1.该步水解反应的时间长,需要15小时以上,且原料反应不完全;2.按照文献方法所制得的底物(4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯)纯度差,若不经纯化直接水解2个保护基将产生很多杂质,使得目标产品的质量难以保证,同时增加其纯化的难度,进而影响终产品达到药品标准。
[0021][0022]
专利cn107337658a及文献琥珀酸普卡必利的合成,中国医药工业杂志,2012,43(1),5-8以对氨基水杨酸为起始物料,通过多步反应制得目标产品。但该工艺采用溴素进行溴代反应,毒性大,同时应用腐蚀性较强的磺酰氯进行氯代反应,此外大量使用锌粉,污染严重。
[0023][0024]
文献普芦卡必利关键中间体4-氨基-5-氯-2,3-二氢-7-苯并呋喃苯甲酸的合成工艺研究,中国药业,2016,25(2),38-40以2-甲氧基-4-乙酰氨基-5-氯苯甲酸甲酯为起始物料,通过多步反应制得目标产品。该工艺除应用毒性较大的溴素进行溴代外,还采用金属钠进行脱卤素偶联,使得步骤延长,难于放大生产。
[0025][0026]
文献synlett,1993,(4):269-270则以4-乙酰胺基-2-羟基苯甲酸甲酯为原料,经氯代、碘代、三甲基硅乙炔化后环合,在铑催化下氢化还原,最后水解得到,总收率38%。路线中用到价昂的硅试剂及铑试剂,不适于大量制备。
[0027][0028]
文献j.am.chem.soc.,1978,100(15):4842-4852以2-甲氧基-4-氨基-5-氯苯甲酸甲酯为原料,经houben-hoesch反应、环合、还原及水解反应得到目标产物。文献未报道收
率,还原反应同样要用到价格昂贵的铑催化剂。
[0029]
综上可知,目前4-氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸的制备方法存在诸多问题,而大多数工艺都通过各种途径制得4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯后再水解得到目标产物,因此4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯即式i同样作为制备普芦卡必利的关键中间体,直接影响该药品的生产、市场供应和质量问题。
[0030][0031]
鉴于目前制备4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯时存在许多不足,因此,研究寻找一条操作简便、反应条件温和、操作过程安全,产品收率高、纯度高的适合工业化生产4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的制备工艺仍是目前需要解决的问题。
技术实现要素:
[0032]
针对目前制备普芦卡必利相关中间体4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯时存在的诸多问题,本发明提供了一种4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的制备方法。该方法反应条件温和,操作过程安全、简便,所制得的目标产品具有较高的纯度和收率。
[0033]
本发明具体通过如下技术方案实现:
[0034]
一种普芦卡必利中间体4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的制备方法,以4-乙酰氨基-5-氯水杨酸甲酯(4-乙酰胺基-2-羟基-5-氯苯甲酸甲酯)即sm-1为反应原料,在有机溶剂中,在缚酸剂作用下与1,2-二溴乙烷反应制得中间体i-1,中间体i-1经催化剂催化反应制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,反应式如下:
[0035][0036]
一种如式i所示的普芦卡必利中间体4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的制备方法,具体包括以下步骤:
[0037]
步骤1.将4-乙酰氨基-5-氯水杨酸甲酯即sm-1、缚酸剂加入有机溶剂a中,控温搅拌均匀后,缓慢滴加1,2-二溴乙烷,继续反应至tlc检测反应完全,经后处理制得中间体i-1;
[0038]
步骤2.将alcl3加入无水有机溶剂b中,加毕搅拌均匀,控温加入中间体i-1的无水有机溶剂b溶液,升温继续反应至tlc检测反应完全,经后处理制得化合物i。
[0039]
优选地,步骤1中所述的缚酸剂选自na2co3,nahco3,k2co3,khco3中的一种或其组合,优选na2co3。
[0040]
优选地,步骤1中所述的有机溶剂a选自n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、乙腈、丙酮中的一种或其组合,优选n,n-二甲基甲酰胺。
[0041]
优选地,步骤1中所述的sm-1与缚酸剂的反应摩尔比为1:1.0~1.5,优选1:1.2。
[0042]
优选地,步骤1中所述的sm-1与1,2-二溴乙烷的反应摩尔比为1:1.3~2.2,优选1:1.7。
[0043]
优选地,步骤1中所述的反应温度为40~90℃,优选50~55℃。
[0044]
在一优选方案中,步骤1中所述后处理步骤为:将反应液倾入温水中搅拌,自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1;优选地,所述温水的温度为40~55℃。
[0045]
优选地,步骤2中所述的有机溶剂b选自二氯甲烷、1,2-二氯乙烷、氯仿、四氯化碳、二硫化碳、硝基甲烷、硝基苯中的一种或其组合,优选二氯甲烷。
[0046]
优选地,步骤2中所述的i-1与alcl3的投料摩尔比为1:0.1~1.0,优选1:0.3。
[0047]
优选地,步骤2中所述的加入i-1溶液时控制的温度为-5~10℃;反应温度为15~30℃,优选20~25℃。
[0048]
在一优选方案中,步骤2中所述后处理步骤为:控温加入稀盐酸,分液取有机相,水相以二氯甲烷萃取,合并有机相,纯化水洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物i;优选地,加入稀盐酸时控制的温度为-5~5℃。
[0049]
本发明的有益效果:
[0050]
本发明提供了一种简便高效的制备普芦卡必利中间体4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯的方法。本发明采用alcl3作为催化剂,直接进行苯环上的烷基化反应构建苯并四氢呋喃环,相较现有技术中的脱卤偶联方法以及采用氯乙酰氯进行酰基化反应后再还原的方法可有效缩短反应路线,并且操作更安全。整个合成方法操作简单,制得的目标产品收率及纯度均较高,适合工业化生产。
具体实施方式
[0051]
下面通过实施例来进一步说明本发明,应该正确理解的是:本发明的实施例仅仅是用于说明本发明,而不是对本发明的限制,所以,在本发明的方法前提下对本发明的简单改进均属于本发明要求保护的范围。
[0052]
以下各实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。
[0053]
i-1的合成:
[0054]
实施例1
[0055]
将1,2-二溴乙烷(31.94g,0.17mol),na2co3(12.72g,0.12mol)加入n,n-二甲基甲酰胺(200ml)中,控温50~55℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(4-乙酰胺基-2-羟基-5-氯苯甲酸甲酯,sm-1,24.36g,0.10mol)的n,n-二甲基甲酰胺(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后制得中间体i-1,收率95.7%,纯度99.0%。
[0056]
实施例2
[0057]
将1,2-二溴乙烷(41.33g,0.22mol),khco3(12.01g,0.12mol)加入n,n-二甲基甲
酰胺(200ml)中,控温50~55℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.35g,0.10mol)的n,n-二甲基甲酰胺(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率94.4%,纯度97.3%。
[0058]
实施例3
[0059]
将1,2-二溴乙烷(43.21g,0.23mol),k2co3(16.58g,0.12mol)加入n,n-二甲基甲酰胺(200ml)中,控温50~55℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.38g,0.10mol)的n,n-二甲基甲酰胺(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率90.1%,纯度97.1%。
[0060]
实施例4
[0061]
将1,2-二溴乙烷(24.42g,0.13mol),nahco3(10.08g,0.12mol)加入n,n-二甲基乙酰胺(200ml)中,控温60~65℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.36g,0.10mol)的n,n-二甲基乙酰胺(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率93.5%,纯度98.8%。
[0062]
实施例5
[0063]
将1,2-二溴乙烷(22.54g,0.12mol),na2co3(12.72g,0.12mol)加入n,n-二甲基甲酰胺(200ml)中,控温50~55℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.34g,0.10mol)的n,n-二甲基甲酰胺(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率89.7%,纯度99.1%。
[0064]
实施例6
[0065]
将1,2-二溴乙烷(31.94g,0.17mol),na2co3(15.90g,0.15mol)加入丙酮(200ml)中,控温45~50℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.37g,0.10mol)的丙酮(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率94.6%,纯度98.7%。
[0066]
实施例7
[0067]
将1,2-二溴乙烷(31.94g,0.17mol),na2co3(10.60g,0.10mol)加入乙腈(200ml)中,控温65~70℃搅拌均匀后,缓慢滴加4-乙酰氨基-5-氯水杨酸甲酯(24.36g,0.10mol)的乙腈(50ml)溶液,继续反应至tlc检测反应完全,将反应液倾入45~50℃的温水(600ml)中搅拌并自然冷却至室温,搅拌析晶,过滤,滤饼经甲苯重结晶后即为中间体i-1,收率93.4%,纯度99.0%。
[0068]
i的合成:
[0069]
实施例8
[0070]
将alcl3(2.00g,0.015mol)加入干燥的二氯甲烷(150ml)中,加毕搅拌均匀后,控温0~5℃加入4-乙酰氨基-2-(2-溴乙氧基)-5-氯苯甲酸甲酯(i-1,17.53g,0.05mol)的二氯甲烷(100ml)溶液,继续控温20~25℃至反应结束后,控温-5~5℃加入稀盐酸(ω=5%,
50ml),分液取有机相,水相以二氯甲烷(20ml
×
3)萃取,合并有机相,纯化水(40ml
×
3)洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,收率91.5%,纯度99.3%。
[0071]
实施例9
[0072]
将alcl3(0.67g,0.005mol)加入干燥的1,2-二氯乙烷(150ml)中,加毕搅拌均匀后,控温0~5℃加入4-乙酰氨基-2-(2-溴乙氧基)-5-氯苯甲酸甲酯(17.50g,0.05mol)的1,2-二氯乙烷(100ml)溶液,继续控温25~30℃至反应结束后,控温-5~5℃加入稀盐酸(ω=5%,50ml),分液取有机相,水相以二氯甲烷(20ml
×
3)萃取,合并有机相,纯化水(40ml
×
3)洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,收率89.3%,纯度99.0%。
[0073]
实施例10
[0074]
将alcl3(0.60g,0.0045mol)加入干燥的硝基甲烷(150ml)中,加毕搅拌均匀后,控温0~5℃加入4-乙酰氨基-2-(2-溴乙氧基)-5-氯苯甲酸甲酯(17.55g,0.05mol)的硝基甲烷(100ml)溶液,继续控温15~20℃至反应结束后,控温-5~5℃加入稀盐酸(ω=5%,50ml),分液取有机相,水相以二氯甲烷(20ml
×
3)萃取,合并有机相,纯化水(40ml
×
3)洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,收率85.7%,纯度98.7%。
[0075]
实施例11
[0076]
将alcl3(6.67g,0.05mol)加入干燥的四氯化碳(150ml)中,加毕搅拌均匀后,控温0~5℃加入4-乙酰氨基-2-(2-溴乙氧基)-5-氯苯甲酸甲酯(17.54g,0.05mol)的四氯化碳(100ml)溶液,继续控温20~25℃至反应结束后,控温-5~5℃加入稀盐酸(ω=5%,50ml),分液取有机相,水相以二氯甲烷(20ml
×
3)萃取,合并有机相,纯化水(40ml
×
3)洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,收率90.1%,纯度98.1%。
[0077]
实施例12
[0078]
将alcl3(8.00g,0.06mol)加入干燥的二氯甲烷(150ml)中,加毕搅拌均匀后,控温0~5℃加入4-乙酰氨基-2-(2-溴乙氧基)-5-氯苯甲酸甲酯(17.53g,0.05mol)的二氯甲烷(100ml)溶液,继续控温20~25℃至反应结束后,控温-5~5℃加入稀盐酸(ω=5%,50ml),分液取有机相,水相以二氯甲烷(20ml
×
3)萃取,合并有机相,纯化水(40ml
×
3)洗涤,干燥,过滤,滤液减压浓缩至干后,以石油醚/乙酸乙酯(v
石油醚
:v
乙酸乙酯
=2:1)的混合溶剂进行重结晶,制得化合物4-乙酰氨基-5-氯-2,3-二氢苯并呋喃-7-羧酸甲酯,收率87.4%,纯度97.8%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1