一种脂滴特异性标记的荧光探针及其合成方法和应用与流程
本发明属于生物医药技术领域,尤其涉及一种脂滴特异性标记的荧光探针及其合成方法和应用。
背景技术:
荧光成像为研究复杂生物结构和生理过程提供了一种直观且实时的观察方式。有机荧光探针作为荧光成像的重要载体,在研究细胞器和细胞生理进程中发挥了重要的作用。尽管目前已有许多靶向标记线粒体,溶酶体和内质网等细胞器的荧光探针实现了商业化,但脂滴成像荧光探针依旧较少。并且已经实现商品化的脂滴荧光探针的成像效果依旧难以令人满意。一方面,传统荧光探针由于光稳定性较差难以实现长时间成像观察。另一方面,信噪比更高的近红外发射荧光探针还有待进一步开发。
脂滴是一个复杂的、动态变化的多功能细胞器,在细胞内能量运输和信号传导等过程中起到非常重要的作用。并且动脉粥样硬化、脂肪肝和肥胖等也与脂滴的代谢异常息息相关。脂滴特异性荧光探针可以直观地观察脂滴在细胞内的含量以及脂滴的形态和变化过程,有助于研究脂滴相关疾病的发展历程。尽管目前已有部分脂滴荧光探针实现商业化,但特异性更好,光稳定性更优的脂滴特异性成像荧光探针仍有待进一步开发。开发在水中没有荧光,而在脂滴中荧光显著增强的脂滴特异性荧光探针具有重要的研究价值和产业化应用前景。
技术实现要素:
本发明的目的在于:针对上述现有技术中存在的不足,提供一种脂滴特异性标记的荧光探针及其合成方法和应用。
本发明采用的技术方案如下:
一种脂滴特异性标记的荧光探针,结构如下式ⅰ所示:
其中,r1为氢原子、甲基或甲氧基;r2为苯环或噻吩。
上述的脂滴特异性标记的荧光探针的合成方法,包括以下步骤:
式ⅱ的芳香醛类化合物与1,3-茚满二酮在催化剂的存在下,在有机溶剂中于50~140℃下反应0.1~300h,冷却至室温,再加入二氯甲烷,过滤,减压除去溶剂,分离纯化产物,干燥,即可。
本发明基于不同取代基的三苯胺和1,3-茚满二酮构建具有推拉电子结构的d-π-a型荧光分子,所得荧光探针在固体和溶液状态中没有荧光,而在油里具有很强的荧光,并能实现细胞内脂滴的特异性荧光成像。
进一步地,催化剂为三乙胺、哌啶和吡啶中的至少一种。
进一步地,有机溶剂为甲醇、乙醇、乙腈、四氢呋喃、二氯甲烷、三氯甲烷、乙醚、二甲基亚砜、苯、邻二氯苯、氯苯、甲苯、二甲苯、1,4-二氧六环、1,2-二氯乙烷、n,n-二甲基甲酰胺和n,n-二甲基乙酰胺中的至少一种。
进一步地,式ⅱ的芳香醛类化合物、1,3-茚满二酮和催化剂的摩尔比为0.001~100:0.001~100:0.0001~100。
进一步地,式ⅱ的芳香醛类化合物、1,3-茚满二酮和催化剂的的摩尔比为0.01~10:0.01~10:0.001~10。
进一步地,式ⅱ的芳香醛类化合物、1,3-茚满二酮和催化剂的的摩尔比为1:1:0.001。
进一步地,该反应在90~120℃下反应10~50h。
进一步地,该反应在100℃下反应24h。
上述的脂滴特异性标记的荧光探针在特异性标记脂滴方面的应用。
综上所述,由于采用了上述技术方案,本发明的有益效果是:
1、本发明通过不同取代基的三苯胺和1,3-茚满二酮构建具有推拉电子结构的d-π-a型荧光分子,所得荧光探针在常规溶剂和固体状态下几乎没有荧光,而在油脂中具有强烈的荧光,可以用于脂滴的细胞成像;
2、本发明的产物具有良好的脂滴特异性成像能力,在hela细胞中能特异性标记脂滴,能够实现活细胞中脂滴分布和形态的实时观察,为生物成像奠定坚实的基础;
3、本发明制备方法简单,操作简便,原料易得,易实现工业化生产。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
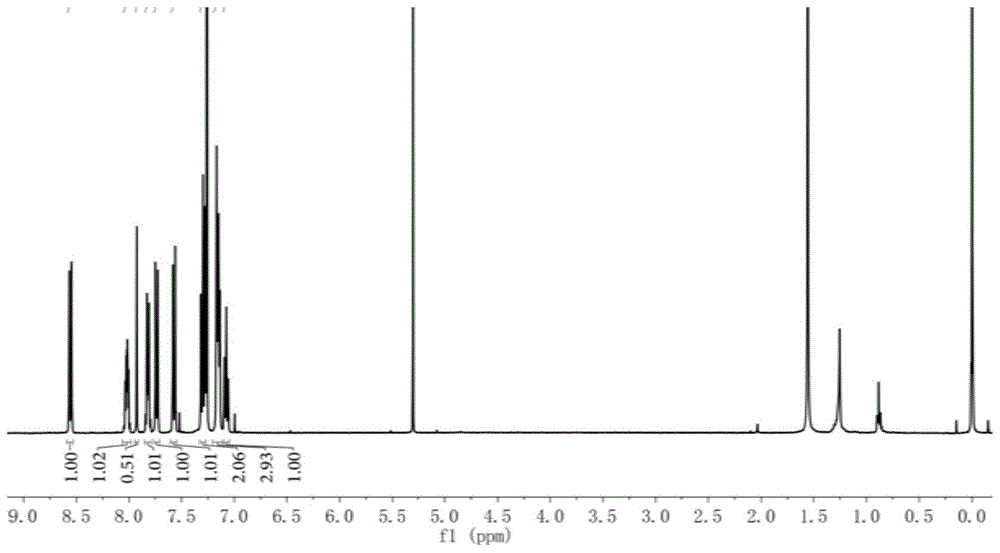
图1为实施例1产物核磁氢谱图;
图2为实施例2产物核磁氢谱图;
图3为实施例3产物核磁氢谱图;
图4为实施例4产物核磁氢谱图;
图5为实施例3产物在水里和油酸中荧光发射光谱图;
图6为实施例3产物对hela细胞中油脂的激光共聚焦成像图;标尺为25μm。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明,即所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本发明实施例的组件可以以各种不同的配置来布置和设计。
因此,以下对在附图中提供的本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明的是,术语“第一”和“第二”等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个……”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本发明较佳的实施例提供一种脂滴特异性标记的荧光探针的合成方法,具体步骤如下:
4'-(二苯氨基)联苯-4-甲醛(0.50g,1.43mmol),1,3-茚满二酮(0.23g,1.58mmol),溶解于5ml甲醇和5ml甲苯的混合溶液中,加入2滴哌啶,于100℃条件下反应,用薄层色谱法监测反应进程,反应结束后冷却至室温,浓缩,产物用硅胶柱层析分离提纯,得到0.56g红棕色固体化合物,产率为81.96%。1hnmr(400mhz,cdcl3):δ=7.05-7.11(t,2h),7.12-7.20(m,6h),7.27-7.33(m,4h),7.55-7.60(d,2h),7.71-7.76(d,2h),7.79-7.85(m,2h),7.92(s,1h),7.99-8.05(m,2h)ppm.
实施例2
本发明较佳的实施例提供一种脂滴特异性标记的荧光探针的合成方法,具体步骤如下:
5-(4-(二苯氨基)苯基)噻吩-2-甲醛(0.50g,1.41mmol),1,3-茚满二酮(0.22g,1.51mmol),溶解于5ml甲醇和5ml甲苯的混合溶液中,加入2滴哌啶,于120℃条件下反应,用薄层色谱法监测反应进程,反应结束后冷却至室温,浓缩,产物用硅胶柱层析分离提纯,得到0.58g红棕色固体化合物,产率为85.29%。1hnmr(400mhz,cdcl3):δ=6.97-7.02(m,2h),7.11-7.19(m,6h),7.35-7.42(t,4h),7.68-7.71(d,1h),7.74-7.79(m,2h),7.88-7.96(m,4h),8.05(s,1h),8.23-8.27(d,2h)ppm.
实施例3
本发明较佳的实施例提供一种脂滴特异性标记的荧光探针的合成方法,具体步骤如下:
5-(4-(二甲苯基氨基)苯基)噻吩-2-甲醛(0.60g,1.56mmol),1,3-茚满二酮(0.25g,1.72mmol),溶解于10ml甲苯中,加入2滴哌啶,于120℃条件下反应,用薄层色谱法监测反应进程,反应结束后冷却至室温,浓缩,产物用硅胶柱层析分离提纯,得到0.60g红棕色固体化合物,产率为75.01%。1hnmr(400mhz,dmso-d6):δ=2.30(s,6h),6.90-6.94(d,2h),7.01-7.06(d,4h),7.25-7.23(d,4h),7.64-7.68(d,1h),7.68-7.74(d,2h),7.87-7.97(m,4h),8.03(s,1h),8.22-8.26(d,2h)ppm.
实施例4
本发明较佳的实施例提供一种脂滴特异性标记的荧光探针的合成方法,具体步骤如下:
5-(4-(二甲氧基苯基氨基)苯基)噻吩-2-甲醛(0.60g,1.44mmol),1,3-茚满二酮(0.23g,1.59mmol),溶解于10ml甲苯中,加入2滴哌啶,于120℃条件下反应,用薄层色谱法监测反应进程,反应结束后冷却至室温,浓缩,产物用硅胶柱层析分离提纯,得到0.63g红棕色固体化合物,产率为80.25%。1hnmr(400mhz,dmso-d6):δ=3.77(s,6h),6.76-6.81(d,2h),6.95-7.00(m,4h),7.11-7.17(m,4h),7.62-7.64(d,1h),7.66-7.70(d,2h),7.88-7.94(m,4h),8.02(s,1h),8.21-8.23(d,1h)ppm.
实验例1
将实施例3的产物溶解在dmso中,配置成10mm的存储液。再用水或油酸稀释成5μm的测试溶液,然后进行荧光测试。
结果如图5,从图5结果可知,在水溶液中荧光探针基本没有荧光,而在油酸里荧光探针的荧光显著增强。图5结果说明本发明提供的荧光探针可以用于脂滴特异性荧光标记。
实验例2
将实施例3的产物溶解在dmso中,配置成10mm的存储液。用培养基将荧光探针稀释到10μm,用于hela细胞染色。细胞在培养箱中孵育1小时后用市售的脂滴荧光探针bodipy493/503进一步染色30分钟,用于研究所制备荧光探针的脂滴成像能力。细胞用pbs洗三次之后,用激光共聚焦显微镜进行观察拍照。共聚焦结果如图6所示。
由图6的结果可知,荧光探针的红色荧光可以很好地与bodipy493/503的绿色荧光重叠在一起,并且重叠系数为0.9344,说明本发明的荧光探针可以用于脂滴的生物成像。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!