一种从救必应中分离罗盘草甙B的方法
一种从救必应中分离罗盘草甙b的方法
技术领域
1.本发明属于中草药分离提取技术领域,具体涉及一种从救必应中分离罗盘草甙b的方法。
背景技术:
2.救必应是冬青科植物铁冬青ilex rotunda thunb的干燥树皮,主产于两广地区,是在夏、秋两季时从铁冬青树干上剥取,经除杂、洗净、润透、切片、晒干后得到的。其性寒味苦,归肺、胃、大肠、肝脏经。具有清热解毒、利湿、止痛的功效,主治感冒发热、扁桃体炎、咽喉肿痛、急慢性咽炎、胃及十二指肠溃疡、风湿关节痛、跌打损伤、水火烫伤。
3.随着近年来对中药救必应研究的不断深入,其化学成分也在不断被分离出来,大体可以分为三萜类、酚苷类、黄酮类、芳香族类、甾类、醛类等。
4.从救必应药材中分离得到三萜类化合物主要有:齐墩果酸(oleanolic acid)、3-乙酰齐墩果酸(3-o-acetyloleanolic acid)、19α-dihydroxyurs-12-en-3-one-28-oic acid,3β,19α-dihydroxyurs-12-en-24,28-dioic acid、木栓酮(friedelin)、28-羟基一木栓酮(canophyllol)、3-羟基齐墩果烷(3β-oh-oleanane)、铁冬青酸(rotundic acid)、铁冬青酸异丙叉酮缩醇(rotundic acid isopropylidene)、长埂冬青苷(pedunculoside)、3-o-α-l-rhamanopyranose-(1
→
2)-β-d-glucopy-ranosy1-(1
→
2)-β-d-arabinopyranosyl ilexgenin b28-o-β-d-glucopyranosy1ester、3-o-[α-l-rhamnopyranosy1-(1
→
2)-β-d-glucopy-ranosy1(1
→
2)-β-d-arabinopyranosy1]-3β,19α-dihydroxyurs-12-en-28-oic-o-β-d-gluco-pyranosy1 ester。
[0005]
从救必应中分离出的芳香族类化合物以二十世纪五十年代,从救必应中分离出糖配体的救必应苷甲,也即是后来被发现的紫丁香苷(syringin)最具有代表性,九十年代从救必应干燥粗粉乙醇浸膏的丙酮提取物中分离得到芥子醛葡萄糖甙(sinapaldehyde glucoside),此后又从救必应药材中分离出酚苷类化合物两个,分别为救必应醇(rotundaol)和新化合物二丁香苷醚(disyringin ether)。其他的从救必应中发现的芳香族类化合物还有芥子醛(sinapaldehyde)、丁香醛(syringaldehyde)、咖啡酸4-o-β-d-吡喃葡萄糖苷、香草酸4-o-β-d-吡喃葡萄糖苷、邻苯二甲酸二异丁酯(di-isobutyl phthalate)、间苯三酚、顺式甲基异丁香烯(cis-methyl.isoeugenol)等。
[0006]
研究表明,从救必应药材中已分离出丁香脂素4'-o-β-d-吡喃葡萄糖苷和丁香树脂醇4',4
”‑
o-β-d-吡喃葡萄糖苷这两种木质素类化合物。
[0007]
除上述类型化合物外,救必应中还含有甾体类化合物:β-谷甾醇(β-sitosterol)、β-胡萝卜苷(β-daucosterol)和脂肪酸类化合物:硬脂酸(stearic acid)、十九烷酸(nonadecylic acid)等,葡萄糖(glucose)、肌醇(inositol)、蜂蜜曲菌素(mellein)、棕榈酸(hexadecanoic acid)、9,12-十八碳二烯酸甲酯(9,12-octadecadienoic acid methyl ester)等。
[0008]
目前,研究发现救必应乙醇提取物和水提物对金黄色葡萄球菌、乙型溶血性链球
菌有较强的抑制作用;救必应乙醇提取部位能有效抑制二甲苯诱导的小鼠耳肿胀,说明其具有显著的抗炎作用。60%乙醇溶液浸泡提取的救必应总黄酮对大肠杆菌(mic=80mg/ml)、链球菌(mic=80mg/ml)、铜绿假单胞菌(mic=80mg/ml)、粪肠球菌(mic=40mg/ml)、普通变形杆菌(mic=40mg/ml)、金黄色葡萄球菌(mic=20mg/ml)、鲍曼不动杆菌(mic=10mg/ml)均有抑菌作用。有研究表明,将救必应干品和湿品分别浸泡提取后,将提取液分别作用于大肠杆菌、伤寒杆菌、金黄色葡萄球菌,结果发现新鲜品提取液的抑菌效果优于干品提取液。在救必应抑菌机理研究方面,分别发现救必应总黄酮、救必应水提液可使产esbls大肠杆菌的细胞壁细胞膜通透性增加、dna合成量降低、凋亡比例增加、总蛋白合成减少,这些研究均初步揭示了救必应提取物的抑菌机理。关于抗炎机制研究方面,以最优工艺提取纯化的救必应提取物能显著抑制小鼠血清中谷草转氨酶(ast)和谷丙转氨酶(alt)的活性,并能明显抑制丙二醛(mda)的生成,同时还可减少炎性介质关键酶环氧化酶-2的表达量,从而使得炎性介质的合成量减少来发挥抗炎的作用。另有研究发现救必应中的成分rotendarpene可以抑制akt and nf-κb通路中tlr-2的活性来减少角质细胞中的炎性介质即活性氧的产生,从而发挥抗炎作用。
[0009]
由于救必应的化学成分十分复杂,各化合物的分离方法也比较复杂,至今仍有较多未分离鉴定的化合物成分,救必应的抑菌机理和抑菌成分未完全被披露,也未见有从救必应中分离出罗盘草甙b的相关报道。
技术实现要素:
[0010]
针对上述问题,本发明提供一种从救必应中分离罗盘草甙b的方法,能够从救必应中分离出罗盘草甙b,为救必应的物质基础研究、抑菌部位的抑菌机制及临床应用研究提供参考依据。
[0011]
本发明的技术方案如下:
[0012]
一种从救必应中分离罗盘草甙b的方法,包括以下步骤:
[0013]
s1:将救必应浸泡于75~85%乙醇溶液中,常温提取2~4天,过滤得滤渣,再用45~55%乙醇溶液浸泡,常温提取2~4天,再次过滤得滤渣,用纯净水浸泡,常温提取2~4天,合并三次滤液,浓缩得浸膏;
[0014]
s2:将浸膏依次用石油醚、乙酸乙酯、正丁醇、水进行萃取,各萃取层浓缩干燥;
[0015]
s3:将水萃取剂层的萃取物溶解于水中,然后上样于大孔吸附树脂,进行梯度洗脱,得到四个流份;
[0016]
s4:将上述四个流份中的目标流份溶解于水中,然后上样于色谱柱ⅰ中进行层析分离,将所得样品点于薄层板上,收集流份ⅰ;
[0017]
s5:将流份ⅰ进行溶解,然后上样于色谱柱ⅱ中,进行梯度洗脱,所得样品点于薄层板上,收集流份ⅱ;将流份ⅱ上样于色谱柱ⅲ,进行梯度洗脱,所得样品点于薄层板上,收集流份ⅲ,即得罗盘草甙b。
[0018]
进一步,所述的步骤s3中,大孔吸附树脂采用0~90%甲醇溶液为洗脱液,30%为一个梯度。
[0019]
进一步,所述的步骤s4中,目标流份为60%甲醇溶液洗脱得到的流份。
[0020]
进一步,所述的步骤s4中,色谱柱ⅰ为mci色谱柱,采用纯水为洗脱液。
[0021]
进一步,所述的流份ⅰ为20%甲醇溶液洗脱液中比移值为0.26~0.70的流份。
[0022]
进一步,所述的步骤s5中,色谱柱ⅱ为mci色谱柱,采用0~100%甲醇溶液为洗脱液,10%为一个梯度。
[0023]
进一步,所述的流份ⅱ为40~60%甲醇溶液洗脱液中比移值在0.17~0.30之间的流份。
[0024]
进一步,所述的步骤s5中,色谱柱ⅲ为hw-40f色谱柱,采用30~90%甲醇溶液为洗脱液,10%为一个梯度。
[0025]
进一步,所述的流份ⅲ为30%甲醇溶液洗脱液中比移值为0.44的流份。
[0026]
本文所述的比移值的概念为:化合物斑点中心至原点的距离与溶剂前沿至原点的距离的比值就是该化合物的比移值。展开分离后,化合物在薄层板上的位置用比移值(rf值)来表示。
[0027]
本文所述的溶液的百分比含量均为体积百分比。
[0028]
本发明的有益效果为:
[0029]
1.本发明能够对救必应抑菌部位进行确认,在采用石油醚、乙酸乙酯、正丁醇、水依次对救必应不同极性部位进行萃取,取水萃取层通过大孔吸附树脂进行层析分离,再通过选择合适的色谱柱进行多次色谱分析和点板操作相结合,能够从水萃取层中分离出罗盘草甙b,为救必应的物质基础研究、抑菌部位的抑菌机制及临床应用研究提供了参考依据,并为罗盘草甙b的制备来源开辟了一条新路径。
[0030]
2.本发明对分离的罗盘草甙b进行了鉴定,如实施例4所示,明确了其结构,证实其确实为罗盘草甙b;还对救必应不同极性部位萃取物进行了抑菌试验,如实施例5所示,能够确认抑菌成分位于水萃取层中,并且罗盘草甙b位于水萃取层的60%甲醇洗脱液中,该洗脱液也具有抑菌活性,可见罗盘草甙b位于抑菌成分中。
[0031]
3.本发明操作简单,有较好的连续性、稳定性和普适性,能够适用于多种化合物的分离提取,分离效果好,条件温和,成本低。
具体实施方式
[0032]
下面通过具体实施例对本发明进行详细说明。
[0033]
实施例1
[0034]
一种从救必应中分离罗盘草甙b的方法,包括以下步骤:
[0035]
s1:将救必应浸泡于75%乙醇溶液中,常温提取2天,过滤得滤渣,再用45%乙醇溶液浸泡,常温提取2天,再次过滤得滤渣,用纯净水浸泡,常温提取2天,合并三次滤液,浓缩得浸膏;
[0036]
s2:将浸膏依次用石油醚、乙酸乙酯、正丁醇、水萃取,各萃取层浓缩干燥;
[0037]
s3:将水萃取层的萃取物溶解于水中,然后上样于大孔吸附树脂,用0~90%甲醇溶液进行梯度洗脱,30%为一个梯度,得到四个流份;
[0038]
s4:将上述梯度洗脱中60%甲醇溶液洗脱得到的流份溶解于水中,然后上样于mci色谱柱中,采用10%~100%的甲醇溶液进行梯度洗脱,10%为一个梯度,将20%甲醇溶液洗脱所得样品点于薄层板上,收集比移值为0.26~0.70的流份ⅰ;
[0039]
s5:将流份ⅰ进行溶解,然后上样于mci色谱柱中,采用0~100%甲醇溶液进行梯度
洗脱,10%为一个梯度,将40~60%甲醇溶液洗脱所得样品点于薄层板上,收集比移值在0.17~0.30之间的流份ⅱ;将流份ⅱ上样于hw-40f色谱柱中,采用30~90%甲醇溶液进行梯度洗脱,10%为一个梯度,将30%甲醇溶液洗脱所得样品点于薄层板上,收集比移值为0.44的流份ⅲ,即为罗盘草甙b。
[0040]
实施例2
[0041]
一种从救必应中分离罗盘草甙b的方法,包括以下步骤:
[0042]
s1:将救必应浸泡于80%乙醇溶液中,常温提取3天,过滤得滤渣,再用50%乙醇溶液浸泡,常温提取3天,再次过滤得滤渣,用纯净水浸泡,常温提取3天,合并三次滤液,浓缩得浸膏;
[0043]
s2~s5与实施例1相同。
[0044]
实施例3
[0045]
一种从救必应中分离罗盘草甙b的方法,包括以下步骤:
[0046]
s1:将救必应浸泡于85%乙醇溶液中,常温提取4天,过滤得滤渣,再用55%乙醇溶液浸泡,常温提取4天,再次过滤得滤渣,用纯净水浸泡,常温提取4天,合并三次滤液,浓缩得浸膏;
[0047]
s2~s5与实施例1相同。
[0048]
实施例4鉴定实验
[0049]
通过理化性质和波谱学特征确定实施例1~3分离的罗盘草甙b的结构。
[0050]
经鉴定,实施例1~3分离的罗盘草甙b均为淡黄色粉末,δh 0.60~1.50之间有簇峰,且含7个甲基质子信号,从低场到高场分别为1.26,1.09,0.92,0.90,0.88,0.87,0.82,提示该化合物可能为甾醇类或萜类化合物。氢谱数据δ:5.42(1h,s,h-1
′
),6.33(1h,d,j=8.0hz,h-1
′
),碳谱数据δ:106.2(c-1
′
),77.3(c-2
′
),78.2(c-3
′
),72.0(c-4
′
),78.5(c-5
′
),63.0(c-6
′
),96.1(c-1
″
),74.4(c-2
″
),79.1(c-3
″
),71.4(c-4
″
),79.6(c-5
″
),62.5(c-6
″
)提示结构中含有两组糖片段,另外碳谱数据显示有1个羧基碳信号δ176.7,1对碳碳双键信号δ123.2和δ144.4。1h nmr(500mhz,pyr)δ:5.70(1h,s,h-12),6.33(1h,d,j=8.0hz,h-1
′
,c-28),5.42(1h,s,h-1
′
,c-3),1.26(3h,s),1.09(3h,s),0.92(3h,s),0.90(3h,s),0.88(3h,s),0.87(3h,s),0.82(3h,s)。13c nmr(125mhz,pyr)δ:37.2(c-1),26.8(c-2),89.6(c-3),40.2(c-4),56.1(c-5),19.8(c-6),34.3(c-7),39.8(c-8),48.2(c-9),36.0(c-10),24.0(c-11),123.2(c-12),144.4(c-13),42.4(c-14),28.5(c-15),23.7(c-16),47.3(c-17),42.0(c-18),46.5(c-19),31.0(c-20),33.4(c-21),32.8(c-22),28.4(c-23),17.0(c-24),15.8(c-25),17.7(c-26),26.4(c-27),176.7(c-28),33.4(c-29),23.9(c-30),glc at c-3:106.2(c-1
′
),77.3(c-2
′
),78.2(c-3
′
),72.0(c-4
′
),78.5(c-5
′
),63.0(c-6
′
),glc at c-28:96.1(c-1
″
),74.4(c-2
″
),79.1(c-3
″
),71.4(c-4
″
),79.6(c-5
″
),62.5(c-6
″
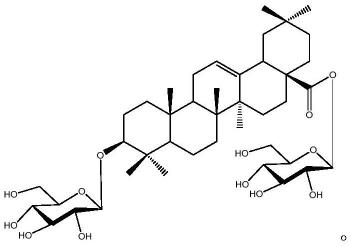
)。以上数据与文献“zhang y,peng y,li l,et al.studies on cytotoxic triterpene saponins from the leaves of aralia elata[j].food chem,2013,138(1):208-213.”一致,故鉴定为罗盘草甙b,该化合物为首次从该植物中分离得到,结构为
[0051][0052]
实施例5救必应抑菌部位抑菌活性测定实验
[0053]
1.实验方法
[0054]
以多重耐药大肠杆菌为受试菌,对流份进行抑菌活性测定,以二倍微量稀释法进行试验,操作方法和结果判定参照clsi的说明。
[0055]
2.样品的制备
[0056]
实验组1:在无菌条件下,将实施例2中步骤s2各萃取层均用5%的dmso和灭菌水溶解,分别配制成浓度为1g/ml的母液;
[0057]
实验组2:在无菌条件下,将实施例2中步骤s3大孔吸附树脂洗脱的四个流份均用5%dmso和灭菌水溶解,分别配制成浓度为80mg/ml的母液;
[0058]
空白对照:含5%dmso的灭菌水。
[0059]
3.大肠杆菌悬液的制备
[0060]
无菌条件下,用接种环挑取麦康凯琼脂培养基上的大肠杆菌菌落转接于nb肉汤中,37℃,220rpm,培养2-6h,然后用无菌nb肉汤将菌液调整至0.5麦氏浊度,再将菌液按1:1000稀释,此时菌浓度约为105cfu/ml,稀释后的菌液立即使用。
[0061]
4.实验结果
[0062]
(1)实施例2中步骤s2救必应不同极性部位抑菌性测定结果见表1。
[0063]
表1.救必应不同极性部位的最小抑菌浓度
[0064]
不同极性部位空白石油醚层乙酸乙酯层正丁醇层水层mic++++0.5(g/ml)
[0065]
注:“+”表示无抑菌作用。
[0066]
从表1可知,只有水层对多重耐药性大肠杆菌具有抑制作用,石油醚层、乙酸乙酯层、正丁醇层对多重耐药性大肠杆菌均无抑制作用。
[0067]
(2)本发明实施例2中救必应水萃取层各流份抑菌性测定结果见表2。
[0068]
表2.救必应水萃取层各流份的最小抑菌浓度
[0069]
流份空白0%甲醇洗脱液30%甲醇洗脱液60%甲醇洗脱液90%甲醇洗脱液mic+++40(mg/ml)+
[0070]
注:“+”表示无抑菌作用
[0071]
从表1可知,60%甲醇溶液洗脱得到的流份均对多重耐药性大肠杆菌具有抑制作用,其他流份对该多重耐药性大肠杆菌均无抑制作用。
[0072]
可见,本发明分离提取的罗盘草甙b存在于救必应具有抑菌活性的水萃取层及水萃取层的60%甲醇洗脱液中,该洗脱液也具有抑菌活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1