病毒样本直接扩增型保存液及应用方法与流程
1.本发明涉生物样本保存领域。尤其涉及一种病毒样本直接扩增型样本保存液及应用方法。
背景技术:
2.本发明对于背景技术的描述属于与本发明相关的相关技术,仅仅是用于说明和便于理解本发明的
技术实现要素:
,不应理解为申请人明确认为或推定申请人认为是本发明在首次提出申请的申请日的现有技术。
3.病毒是一种没有细胞结构的特殊生物,由蛋白质外壳和内部的遗传物质组成。病毒个体微小,结构简单,只含一种遗传物质(dna或rna)。病毒性感染的危害极大,例如sars或sars
‑
cov
‑
2,感染者初始症状多为发热、乏力和干咳,后续逐渐出现呼吸困难,严重者可出现急性呼吸窘迫综合征或脓毒症休克,甚至死亡。
4.病毒核酸的检测适用于疾病的早期诊断,因此,保存完整的病毒核酸对下游的基因分析具有重要的意义。病毒的核酸容易降解的,尤其是rna病毒,非常容易被广泛存在的内源性或者外源性rna酶降解。现有的常规的病毒核酸的保存方法为(1)以hank’s平衡盐、pbs等缓冲液为主体的通用型转运介质(utm)或病毒转运介质(vtm)常规病毒保存液;(2)以胍盐为主体的灭活型保存液,可以在室温下短期保存。
5.现有技术中的utm或者vtm需要在常规
‑
80℃超低温保存,需求冷链等设备,操作不便;而以胍盐为主体的灭活型保存液,已经在市场上出现,其可以灭活病毒保护检验人员的安全。如中国专利cn111718908a中公布了一种病毒样本保存液及其制备方法和应用,其公开的效果较好的实施例1中的主要组成为:50mmol/l的tris
‑
hcl、质量体积百分比为5%的异硫氰酸胍、体积百分比为5%的聚乙二醇对异辛基苯基醚、体积百分比为5%的月桂酰基肌氨酸钠和终浓度为0.1mmol/l的edta
‑
2na。又如中国专利cn111172239a公开了一种病毒样本保存液包含以下组分:硫氰酸胍、吐温
‑
20、聚多卡醇、乙醇,柠檬酸三钠、柠檬酸和二硫苏糖醇。上述的两个专利中公开试剂都可以灭活病毒,短期保存病毒中的rna稳定,并通过常规的核酸提取步骤之后,再进行rna定性和定量的rt
‑
pcr检测。
6.综上所述,虽然以胍盐为主的灭活保存液可以解决病毒灭活的技术问题,同时可以实现在短期室温保存和运输病毒中rna,但其组分中含有常含有异硫氰酸胍、螯合剂、乙醇或高浓度的表面活性剂这些常见的rt
‑
pcr抑制剂,所以依然不能避免后续要进行rna的提取步骤。而当前sars
‑
cov
‑
2检测需求一种更为快速的检验流程和方案,来提高现有rt
‑
pcr检测或临床诊断的便利性。
发明内容
7.本发明实施例的目的是提供一种病毒样本直接扩增型保存液及其应用方法。本发明所提供的保存液可以快速灭活病毒,实现直接上样扩增检测,避免步骤繁琐的核酸提取过程。
8.本发明实施例的目的是通过如下技术方案实现的:
9.本发明第一方面的实施例提供了一种病毒样本直接扩增型保存液,包括表面活性剂、缓冲剂、盐离子、还原剂、醇和核酸酶抑制剂;其中,表面活性剂的质量体积百分比为0.01
‑
5%;缓冲剂的终浓度为2
‑
250mm;盐离子的浓度为10
‑
500mm;还原剂的浓度0.5
‑
50mm;醇的质量体积百分比为0.1
‑
15%;核酸酶抑制剂的质量体积百分比为0.01
‑
1%;所述保存液ph为5.5
‑
9.5。
10.进一步的,所述保存液还可以包括基因释放剂所述基因释放剂为牛血清白蛋白(bsa)、1,2
‑
二油酰基卵磷脂、1,2
‑
二油酰基卵磷脂衍生物和/或其组合。
11.1,2
‑
二油酰基卵磷脂的结构式如下:
[0012][0013]
进一步的,所述基因释放剂为质量体积百分比为0.05
‑
0.5%的牛血清白蛋白、质量体积百分比为0.01
‑
0.5%的1,2
‑
二油酰基卵磷脂、质量体积百分比为0.01
‑
0.35%的1,2
‑
二油酰基卵磷脂衍生物和/或其组合。
[0014]
进一步的,所述表面活性剂为十二烷基硫酸三乙醇胺、十二烷基三乙醇胺、十二烷基苯三乙醇胺、brij 35、brij 56、brij 58、十二烷基硫酸钠、np40、聚乙二醇辛基苯基醚、span
‑
80、span
‑
20、十二烷基硫酸锂、十二烷基苯磺酸钠、十二烷基磺酸钠、十二烷基肌氨酸钠、十八烷基胺聚氧乙烯醚双季铵盐、十六醇聚氧乙烯醚二甲基辛烷基氯化铵、辛烷基聚氧乙烯基十四烷基氯化铵、辛烷基聚氧乙烯基十二烷基氯化铵和/或其组合。
[0015]
进一步的,所述缓冲剂为三羟基氨基甲烷、4
‑
羟乙基哌嗪乙磺酸、乙磺酸钠、乙酸钠、邻苯二甲酸氢钾、硼酸、磷酸二氢钾、二乙醇胺、三乙醇胺、丙磺酸、磷酸二氢钠、乙酸铵、硫酸铵、氯化铵、n,n
‑
二羟乙基甘氨酸、3
‑
(环己胺)
‑1‑
丙磺酸、3
‑
吗啉丙磺酸和/或其组合。
[0016]
进一步的,所述盐离子为氯化钠、氯化铵、硫酸钠、硫酸铵、氯化钾、氯化锂、乙酸钠和/或其组合。
[0017]
进一步的,所述还原剂为dtt(二硫苏糖醇)、tcep(三(2
‑
羧乙基)膦)、tcep
‑
hcl(三(2
‑
羧乙基)膦盐酸盐)、尿酸、巯基乙醇、半胱氨酸、维生素c、连二亚硫酸盐、巯基乙酸和/或
其组合。
[0018]
进一步的,所述醇为甲醇、乙醇、异丙醇、乙二醇、1
‑
丙醇、丙三醇、2
‑
丁醇、聚乙二醇200、聚乙二醇400、聚乙二醇600、聚乙二醇800、聚乙二醇1000、聚乙二醇2000、聚乙二醇6000、聚乙二醇8000和/或其组合。
[0019]
进一步的,所述核酸酶抑制剂为焦磷酸二乙酯(depc)、异硫氰酸胍、氧钒核糖核苷复合物、rna酶的蛋白质抑制剂(rnasin)、尿素、尿素、茶黄素、花青素、花白素、类黄酮,木酚素、n
‑
乙酰氨基己糖、己糖醛酸和/或其组合。
[0020]
本发明第二方面的实施例提供了一种病毒样本直接扩增型保存液的应用方法,包括如下步骤:
[0021]
获取可能含有病毒的样本;
[0022]
将可能含有的病毒样本加入含有保存液的管中;
[0023]
上下颠倒混匀后在室温静置1
‑
30min即可在环境温度下储存和运输;
[0024]
直接取样加入相应的rt
‑
pcr扩增试剂盒中进行检测;取样体积占整个扩增体系的比例为2.5
‑
50%(v/v)。
[0025]
本发明实施例具有如下有益效果:
[0026]
可实现病毒rna在环境稳定下运输和保存;
[0027]
快速灭活病原体微生物,抑制各种病毒或细菌生长,杜绝二次传染,实现传染性样本的安全运输。
[0028]
利用本发明保存液可以实现将“采样
‑
灭活
‑
提取
‑
扩增检测”流程修改为“采样
‑
扩增检测”缩短了整个流程时间。
附图说明
[0029]
图1是本发明实施例12中不同滴度假病毒加入保存液v5后进行直接扩增的rt
‑
pcr曲线扩增图。从左到右分别是10
*5
、10
*4
和10
*3
假病毒加入到保存液中直接扩增的曲线。
具体实施方式
[0030]
下面结合实施例对本申请进行进一步的介绍。
[0031]
为了更清楚地说明本发明实施例或现有技术中的技术方案,在下述说明中,不同的“一实施例”或“实施例”指的不一定是同一实施例。不同实施例之间可以替换或者合并组合,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些实施例获得其他的实施方式。
[0032]
定义
[0033]
在详细描述本教导之前,应理解本公开不限于具体的组合物或工艺步骤,因为这些可以变化。应当注意,如本说明书和所附权利要求中所使用的,单数形式“一”、“一个”和“该”包括复数指代,除非上下文另有明确说明。
[0034]
本文使用的术语“样本”或“样品”将被理解意为任何这样的样品:可能包含目标核酸物质的样品,术语“样本”或“样品”或可包括溶液,如水溶液、细胞、组织、活检、粉末、或其中一种或多种的组合。样本可以是生物学样本,如唾液、痰、口腔拭子样品、血清、血浆、血液、血沉棕黄层、咽部、鼻部/鼻咽部或鼻窦拭子或分泌物、喉部拭子或刮出物、尿液、粘液、
粪便排泄物、直肠拭子、呕吐物、胃液、胃肠道液、精液、精子、尿道拭子和分泌物、脑脊液、哺乳期或经期产物、卵黄、羊水、房水、玻璃体液、宫颈分泌物、阴道液、分泌物、拭子或刮出物、骨髓样本和抽取物、胸膜液和渗出液、汗液、脓、眼泪、淋巴液、支气管或肺灌洗液或抽取物、细胞培养物和细胞悬浮液、结缔组织、上皮、上皮拭子和涂片、粘膜、肌肉组织、胎盘组织、活检、渗出物、器官组织、神经组织、毛发、皮肤、或指甲,其中前述的样本可得自例如脊椎动物,包括哺乳动物。
[0035]
应当理解,在本公开中讨论的温度、质量、重量、体积比、浓度、时间等之前存在暗示的“约”,使得轻微和非实质性的偏差在本文的教导的范围内。通常,术语“约”表示组合物的组分量的非实质性变化,其对组合物的效果或稳定性没有任何显著影响。而且,“包含”、“含有”、和“包括”的使用不旨在是限制性的。应理解,前面的一般性描述和详细描述都仅是示例性和解释性的,并不是对本教导的限制。就通过引用并入的任何材料与本公开的表述内容不一致的程度,则以表述内容为准。
[0036]
除非特别指出,否则描述为“包含”各种组分的说明书中的实施方式也被认为是“由所述组分组成”或“基本上由所述组分组成”;描述为“由各种组分组成”的说明书中的实施方式也被认为是“包含”或“基本上由所述组分组成”。
[0037]“核酸”是指包含两个或更多个共价键合的核苷或具有含氮杂环碱基或碱基类似物的核苷类似物的多聚化合物,其中核苷通过磷酸二酯键或其他键连接在一起,以形成多核苷酸。核酸包括rna、dna或嵌合dna
‑
rna聚合物或寡核苷酸及其类似物。核酸“骨架”可以由多种连接组成,包括糖
‑
磷酸二酯键、肽
‑
核酸键中的一种或多种。核酸可以包括修饰的碱基以改变核酸的功能或行为,例如添加3'
‑
末端双脱氧核苷酸以阻止另外的核苷酸被添加到核酸中。用于体外制备核酸的合成方法在本领域中是公知的,尽管可以使用常规技术从天然来源纯化核酸。
[0038]
在本申请中,“提取”、“分离”或“纯化”是指样品的一个或多个组分被除去或与其它样品组分分离。样品组分包含常处于通常水性溶液相中的目标核酸,其也可以包含细胞片段、蛋白质、碳水化合物、脂质、盐离子、金属离子和其它核酸。“提取”、“分离”或“纯化”并不意味着任何程度的纯化。通常,分离或纯化从其它样品组分中去除至少70%或至少80%或至少90%的目标核酸。
[0039]
快速灭活病毒,实现直接上样扩增检测,避免步骤繁琐的核酸提取过程。
[0040]
一种病毒样本直接扩增型保存液,包括表面活性剂、缓冲剂、盐离子、还原剂、醇和核酸酶抑制剂。
[0041]
进一步的,所述保存液还可以包括基因释放剂。
[0042]
在本发明的另一些实施例中,所述基因释放剂可以是牛血清白蛋白(bsa)、1,2
‑
二油酰基卵磷脂(简称dopc)、1,2
‑
二油酰基卵磷脂衍生物(简称dopc
‑
r)和/或其组合。
[0043]
1,2
‑
二油酰基卵磷脂的结构式如下:
[0044][0045]
1,2
‑
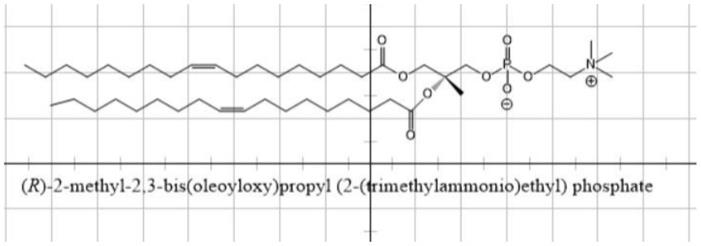
二油酰基卵磷脂衍生物结构如下:
[0046][0047]
dopc的衍生物化学名称为(r)
‑2‑
甲基
‑
2,3
‑
二(油酰)丙基(2
‑
(三甲基氨基)乙基)磷酸酯,简称dopc
‑
r。
[0048]
在本发明的另一些实施例中,所述基因释放剂可以是质量体积百分比为0.05
‑
0.5%的牛血清白蛋白、0.01
‑
0.5%的dopc、0.01
‑
0.35%的dopc
‑
r和/或其组合。
[0049]
进一步,所述保存液包括以下组成:质量体积百分比为0.01
‑
5%的表面活性剂、终浓度为2
‑
250mm的缓冲剂、10
‑
500mm的盐离子、0.5
‑
50mm的还原剂、质量体积百分比为0.1
‑
15%的醇、质量体积百分比为0.01
‑
1%的核酸酶抑制剂。
[0050]
在本发明的一些实施例中,所述保存液ph为5.5
‑
9.5。
[0051]
在本发明的另一些实施例中,所述保存液ph为6.5
‑
8.5。
[0052]
在本发明的一些实施例中,所述表面活性剂为非离子表面活性剂、阴离子表面活性剂、阳离子表面活性剂或两性表面活性剂和/或其组合。
[0053]
在本发明的另一些实施例中,所述表面活性剂为十二烷基硫酸三乙醇胺、十二烷基三乙醇胺、十二烷基苯三乙醇胺、brij 35、brij 56、brij 58、十二烷基硫酸钠、np40、聚乙二醇辛基苯基醚、span
‑
80、span
‑
20、十二烷基硫酸锂、十二烷基苯磺酸钠、十二烷基磺酸钠、十二烷基肌氨酸钠、十八烷基胺聚氧乙烯醚双季铵盐、十六醇聚氧乙烯醚二甲基辛烷基氯化铵、辛烷基聚氧乙烯基十四烷基氯化铵、辛烷基聚氧乙烯基十二烷基氯化铵和/或其组合。
[0054]
在本发明的另一些实施例中,所述表面活性剂为十二烷基硫酸三乙醇胺、十二烷基三乙醇胺、十二烷基苯三乙醇胺、brij 35、brij 56、brij 58、十二烷基硫酸钠、np40、聚乙二醇辛基苯基醚、十二烷基硫酸锂、十六醇聚氧乙烯醚二甲基辛烷基氯化铵、辛烷基聚氧乙烯基十四烷基氯化铵、辛烷基聚氧乙烯基十二烷基氯化铵和/或其组合。
[0055]
在本发明的另一些实施例中,所述表面活性剂为十二烷基三乙醇胺、十二烷基苯三乙醇胺、brij 56、brij 58、十二烷基硫酸钠、np40、聚乙二醇辛基苯基醚、十二烷基硫酸锂、辛烷基聚氧乙烯基十四烷基氯化铵和/或其组合。
[0056]
在本发明的另一些实施例中,所述表面活性剂为质量体积百分比为0.02
‑
0.1%的十二烷基三乙醇胺、0.02
‑
0.2%的十二烷基苯三乙醇胺、0.5
‑
2%的brij 56、0.5
‑
2%的brij 58、0.01
‑
0.2%的十二烷基硫酸钠、0.2
‑
2%的np40、0.2
‑
5%的聚乙二醇辛基苯基醚、0.02
‑
0.4%的十二烷基硫酸锂、0.1
‑
2%的辛烷基聚氧乙烯基十四烷基氯化铵和/或其组合。
[0057]
在本发明的一些实施例中,所述缓冲剂为三羟基氨基甲烷、4
‑
羟乙基哌嗪乙磺酸、乙磺酸钠、乙酸钠、邻苯二甲酸氢钾、硼酸、磷酸二氢钾、二乙醇胺、三乙醇胺、丙磺酸、磷酸二氢钠、乙酸铵、硫酸铵、氯化铵、n,n
‑
二羟乙基甘氨酸、3
‑
(环己胺)
‑1‑
丙磺酸、3
‑
吗啉丙磺酸和/或其组合。
[0058]
在本发明的另一些实施例中,所述缓冲液为三羟基氨基甲烷、硼酸、二乙醇胺、硫酸铵、氯化铵、n,n
‑
二羟乙基甘氨酸、3
‑
(环己胺)
‑1‑
丙磺酸和/或其组合。
[0059]
在本发明的另一些实施例中,所述缓冲剂为5
‑
50mm的三羟基氨基甲烷、2
‑
50mm的硫酸铵、2
‑
40mm的氯化铵、2
‑
100mm的n,n
‑
二羟乙基甘氨酸、5
‑
250mm的3
‑
(环己胺)
‑1‑
丙磺酸和/或其组合。
[0060]
在本发明的一些实施例中,所述盐离子为氯化钠、氯化铵、硫酸钠、硫酸铵、氯化钾、氯化锂、乙酸钠和/或其组合。
[0061]
在本发明的另一些实施例中,所述盐离子为氯化钠、氯化铵、硫酸铵、氯化钾和/或其组合。
[0062]
在本发明的另一些实施例中,所述盐离子为20
‑
200mm的氯化钠、10
‑
200mm氯化铵、20
‑
300mm硫酸铵、30
‑
500mm的氯化钾和/或其组合。
[0063]
在本发明的一些实施例中,所述还原剂为dtt(二硫苏糖醇)、tcep(三(2
‑
羧乙基)膦)、tcep
‑
hcl(三(2
‑
羧乙基)膦盐酸盐)、尿酸、巯基乙醇、半胱氨酸、维生素c、连二亚硫酸盐、巯基乙酸和/或其组合。
[0064]
在本发明的另一些实施例中,所述还原剂为dtt、tcep、维生素c和/或其组合。
[0065]
在本发明的另一些实施例中,所述还原剂为0.5
‑
25mm的dtt、0.5
‑
10mm的tcep、2
‑
50mm的维生素c和/或其组合。
[0066]
在本发明的一些实施例中,所述醇为甲醇、乙醇、异丙醇、乙二醇、1
‑
丙醇、丙三醇、2
‑
丁醇、聚乙二醇200、聚乙二醇400、聚乙二醇600、聚乙二醇800、聚乙二醇1000、聚乙二醇2000、聚乙二醇6000、聚乙二醇8000和/或其组合。
[0067]
在本发明的另一些实施例中,所述醇为乙醇、异丙醇、乙二醇、丙三醇、聚乙二醇200、聚乙二醇400、聚乙二醇600、聚乙二醇2000和/或其组合。
[0068]
在本发明的另一些实施例中,所述醇为质量体积百分比为0.1
‑
2%的乙醇、0.2
‑
2.5%的异丙醇、0.5
‑
5%乙二醇、1
‑
10%的丙三醇、1
‑
15%的聚乙二醇200、1
‑
10%的聚乙二醇600、2
‑
10%的聚乙二醇2000和/或其组合。
[0069]
在本发明的一些实施例中,所述核酸酶抑制剂为焦磷酸二乙酯(depc)、异硫氰酸胍、氧钒核糖核苷复合物、rna酶的蛋白质抑制剂(rnasin)、尿素、尿素、茶黄素、花青素、花白素、类黄酮,木酚素、n
‑
乙酰氨基己糖、己糖醛酸和/或其组合。
[0070]
在本发明的另一些实施例中,所述核酸酶抑制剂为茶黄素、花青素、木酚素、n
‑
乙酰氨基己糖和/或其组合。
[0071]
在本发明的另一些实施例中,所述核酸酶抑制剂为质量体积百分比为0.01
‑
0.5%的茶黄素、0.01
‑
1%的花青素、0.01
‑
0.25%的木酚素和/或其组合。
[0072]
在本发明的另一些实施例中,所述的核酸酶抑制剂为质量体积百分比为0.01
‑
0.2%的茶黄素、0.01
‑
0.5%的花青素、0.01
‑
0.1%的木酚素和/或其组合。
[0073]
在一个实施方式中,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,ph7.4。
[0074]
在另一个实施方式中,所述保存液包括以下组成:质量体积百分比为0.1%的十二烷基苯三乙醇胺、0.5%的brij 56、0.1%的辛烷基聚氧乙烯基十四烷基氯化铵、20mm的硫酸铵、10mm的维生素c、质量体积百分比为5%的聚乙二醇600、质量体积百分比为0.05%的花青素,ph8.0。
[0075]
在另一个实施方式中,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.1%的bsa,ph7.4。
[0076]
在另一个实施方式中,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.1%的dopc,ph7.4。
[0077]
在另一个实施方式中,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.05%的dopc
‑
r,ph7.4。
[0078]
依据本发明的第一方面,所述保存液可以保存病毒rna在环境稳定下至少2天。
[0079]
在本发明的另一些实施例中,所述保存液可以保存病毒rna在环境温度下至少稳定3天,或更多至4天,或更多至5天,或更多至7天,或至多至14天。
[0080]
所述“保存病毒rna”指的是通过rt
‑
pcr检测,ct与初始保存点相比,不超过2个。
[0081]
本发明的第二方面提供了病毒样本直接扩增型保存液的应用方法,包括如下步骤:a)获取可能含有病毒的样本;b)将可能含有的病毒样本加入含有保存液的管中;c)上下颠倒混匀后在室温静置一段时间即可在环境温度下储存和运输;d)直接取样加入相应的rt
‑
pcr扩增试剂盒中进行检测。
[0082]
在本发明的一些实施例中,所述a)“获取可能含有病毒的样本”指可以通过鼻拭子、咽拭子等取样工具进行获取可能含有病毒的样本;
[0083]
在本发明的一些实施例中,所述b)“加入含有保存液的管子”管子可以是1ml、1.5ml、2ml、3ml、5ml、10ml、12ml和15ml。保存液加入的体积可以是0.5ml、1ml、1.5ml、2ml、3ml、40ml、5ml和6ml。
[0084]
在本发明的一些实施例中,所述c)“室温静置一段时间”的时间为1
‑
30min。
[0085]
在本发明的另一些实施例中,所述c)“室温静置一段时间”的时间为5
‑
15min。
[0086]
在本发明的一些实施例中,所述d)“直接取样加入相应的rt
‑
pcr扩增试剂盒”取样
体积占整个扩增体系的比例为2.5
‑
50%(v/v)。
[0087]
在本发明的另一些实施例中,所述取样体积占整个扩增体系的比例可以是2
‑
40%(v/v)。
[0088]
在本发明的另一些实施例中,所述取样体积占整个扩增体系的比例可以是7.5
‑
30%(v/v)。
[0089]
在本发明的另一些实施例中,所述取样体积占整个扩增体系的比例可以是10
‑
25%(v/v)。
[0090]
实施例
[0091]
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。下述实施例中所述实验方法,如无特殊说明,均为常规方法;所述材料,如无特殊说明,均可从商业途径获得。
[0092]
实施例1:保存液v1
[0093]
本实施例提供一种保存液,包括质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,ph7.4。
[0094]
对比例1:保存液w1
[0095]
本实施例提供一种保存液,包括质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇,ph7.4。
[0096]
对比例2:保存液w2
[0097]
本实施例提供一种保存液,包括质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、质量体积百分比为0.5%的乙醇,ph7.4。
[0098]
对比例3:保存液w3
[0099]
实施例提供一种保存液,包括20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,ph7.4。
[0100]
实施例5使用实施例1制备的保存液v1和对比例的保存液w1
‑
w3、utm保存液、去离子水、生理盐水进行保存和直接扩增检测
[0101]
参考本发明的第二方面提供了病毒样本直接扩增型保存液的应用方法,在1ml不同的保存液中加入10
*5
假病毒(covid
‑
19
‑
pseudovirus),上下颠倒10次至混匀,室温下静置10min后使用neb公司luna universal probe one step rt
‑
qpcrkit(cat#e3006s),使用方法参考试剂盒说明书,取2μl含有假病毒的保存液样本加入到20μl体系中,检测假病毒ofr1ab基因片段,引物探针序列来源于中国cdc,通过abi荧光定量pcr仪7500fast进行检测分析rna病毒的直接扩增效果和病毒rna在保存液中的保存性能。检测假病毒样本在不同保存液中在室温下(25℃)保存第0、3和5天的ct值。从表1中可以看到,花青素的加入使保存液v的保存性能得以维持,而w1中没有添加花青素则不能在室温下保存病毒rna。保存液v1和w2对比初始的ct值我们发现还原剂对于病毒样本的裂解和rna的释放也起到了明显的作用。保存液v1与w3对比可以发现,如果不加入表面活性剂则病毒样本不能释放其中的核酸
物质,难以进行检测,而对照的utm保存液、去离子水和生理盐水也并不能释放核酸。
[0102]
qpcr仪器条件如下
[0103][0104]
表1:不同样本保存液在室温下保存病毒rna及直接扩增检测
[0105]
样本保存液day0(ct)day2(ct)day5(ct)
△
ct*v122.122.422.60.5w122.525.627.75.2w224.426.728.94.5w334.435.4nt/utmnt*ntnt/去离子水ntntnt/生理盐水nt37.638.6/
[0106]
*
△
ct=第0天ct
‑
第5天ct
[0107]
*nt为未检测
[0108]
实施例6:不同含量的花青素对于保存病毒rna的验证
[0109]
在实施例1制备的保存液v1的配方中,我们制备了含有一系列不同浓度的花青素的保存液,将参考实施例5的方案中进行实验。在1ml不同的保存液中加入10
*5
假病毒(covid
‑
19
‑
pseudovirus),上下颠倒10次至混匀,室温下静置10min后使用neb公司luna universalprobe one step rt
‑
qpcr kit(cat#e3006s),使用方法参考试剂盒说明书,取2μl含有假病毒的保存液样本加入到20μl体系中,通过检测假病毒ofr1ab基因片段,分析假病毒样本在不同保存液中在室温下(25℃)保存第0、3、5和7天的ct值。令人意外的,我们发现加入过量的花青素导致ct值的延迟甚至没有检测信号,这说明过量的花青素会抑制rt
‑
pcr的反应,而过少的花青素(如0.01%)不能很好起到保存rna的作用。因此在以下实施例中保存液的配方中,我们使用0.05%的花青素作为添加剂。
[0110]
表2:不同样本保存液在室温下保存病毒rna及直接扩增检测
[0111]
[0112][0113]
实施例7:保存液v2
[0114]
本发明提供一种保存液,所述保存液包括以下组成:质量体积百分比为0.1%的十二烷基苯三乙醇胺、0.5%的brij 56、0.1%的辛烷基聚氧乙烯基十四烷基氯化铵、20mm的硫酸铵、10mm的维生素c、质量体积百分比为5%的聚乙二醇600、质量体积百分比为0.05%的花青素,ph8.0。
[0115]
实施例8:保存液v3
[0116]
本发明提供一种保存液,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.1%的bsa,ph7.4。
[0117]
实施例9:保存液v4
[0118]
本发明提供一种保存液,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.1%的dopc,ph7.4。
[0119]
实施例10:保存液v5
[0120]
本发明提供一种保存液,所述保存液包括以下组成:质量体积百分比为0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷、150mm的氯化钾、1mm的tcep、质量体积百分比为0.5%的乙醇、质量体积百分比为0.05%的花青素,质量体积百分比为0.05%的dopc
‑
r,ph7.4。
[0121]
对比例4保存液b1
[0122]
20mm的三羟基氨基甲烷、150mm的氯化钾、0.1%bsa,ph7.4。
[0123]
对比例5保存液b2
[0124]
20mm的三羟基氨基甲烷、150mm的氯化钾、0.75%的brij 58、0.05%的十二烷基硫酸锂、20mm的三羟基氨基甲烷,ph7.4。
[0125]
实施例11:使用实施例7
‑
10,以及对比例4和5制备的保存液和去离子水进行保存和直接扩增检测
[0126]
参考本发明的第二方面提供了病毒样本直接扩增型保存液的应用方法,在1ml不同的保存液中加入10
*5
假病毒(covid
‑
19
‑
pseudovirus),上下颠倒10次至混匀,室温下静置10min后使用neb公司luna universal probe one step rt
‑
qpcrkit(cat#e3006s),使用方法参考试剂盒说明书,取2μl含有假病毒的保存液样本加入到20μl体系中,通过检测假病毒
ofr1ab基因片段,分析假病毒样本在不同保存液中在室温下(25℃)保存第0、3和5天的ct值。从表3的数据可以分析得到,添加了不同的基因释放剂后,我们发现初始的ct值更低了,这表明基因释放剂的添加更有利于核酸从病毒样本中释放出来。令人意外的,bsa作为utm和vtm保存液保存病毒和细胞完整性的配方组分,起到了保护细胞的作用,但在我们的配方测试中发现单独的保存液b2中也能起到释放病毒中核酸的方法。此外,dopc
‑
r和dopc作为基因释放剂相比bsa具有更为优异的基因释放效果。
[0127]
表3:不同样本保存液在室温下保存病毒rna及直接扩增检测
[0128][0129][0130]
实施例12:使用保存液v5测试不同浓度病毒的直接扩增
[0131]
在1ml实施例10制备的保存液v5中加入10
*5
、10
*4
、10
*3
和假病毒(covid
‑
19
‑
pseudovirus),上下颠倒10次至混匀,室温下静置10min后使用neb公司luna universal probe one step rt
‑
qpcr kit(cat#e3006s),取2μl含有假病毒的保存液样本加入到20μl体系中,通过检测假病毒ofr1ab基因片段,分析不同滴度假病毒样本在保存液中的检测结果,结果如图1所示,样本保存液v5对不同滴度的假病毒中的病毒rna都具有很好的释放效果。
[0132]
以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
[0133]
应当说明的是,上述实施例均可根据需要自由组合。以上介绍仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1