一种稳定不析出的胆硫乳琼脂平板的制作方法
1.本发明涉及一种微生物鉴定用平板,特别涉及一种稳定不析出的胆硫乳琼脂平板。
背景技术:
2.沙门氏菌是一类广泛存在于肉制品、蛋类,水产品,奶制品等常见食物中的革兰氏阴性杆菌,主要通过食物和饮水经口感染,引起急性胃肠炎、剧烈头痛、呕吐、腹泻等临床症状。志贺氏菌是一类革兰氏阴性杆菌,是人类细菌性痢疾最为常见的病原菌。在我国每年由沙门氏菌、志贺氏菌感染引起的食物中毒占细菌性食物中毒的首位,因此在日常食物以及进出口食物中,沙门氏菌、志贺氏菌的检测是非常重要的检测项目。
3.我国微生物检验标准gb/t4789.4
‑
2003、sn/t2206.3
‑
2009等均推荐胆硫乳琼脂作为分离沙门氏菌、志贺氏菌的选择性培养基。sn/t2206.3
‑
2009使用的胆硫乳琼脂(dhl)组成为:蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、牛胆盐1.0g、硫代硫酸钠2.2g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g或5g/l水溶液6ml、琼脂18.0g~20.0g、蒸馏水1000ml,ph7.3。gb/t4789.28
‑
2003规定的dhl琼脂成分为蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、去氧胆酸钠1.0g、硫代硫酸钠2.3g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g、琼脂18.0g~20.0g、蒸馏水1000ml,ph7.3。
4.即用型琼脂平板是一种预制的琼脂平板,不需要经过配制过程、直接现取现用,方便、快捷、节省人力物力财力等各种优势,是微生物检验产品发展的趋势。胆硫乳琼脂中含有蛋白胨、牛肉浸粉、乳糖、蔗糖、胆盐、硫代硫酸钠、柠檬酸钠、柠檬酸铁铵、中性红、琼脂等多种成分。由于该配方中糖、胆盐、硫代硫酸钠等种类较多,配制的平板在储存过程中容易在平板表面析出盐晶,影响平板的外观及使用。目前国内生产的胆硫乳琼脂平板均只有3个月保质期,且在保质期内平板表面出现盐晶,无法满足长期储存的需求。
技术实现要素:
5.本发明的目的在于克服现有技术的至少一个不足,提供一种稳定的胆硫乳琼脂平板。
6.本发明所采取的技术方案是:
7.本发明的第一个方面,提供:
8.组合物在制备胆硫乳琼脂平板稳定剂中的应用,所述组合物选自乳酸钠、十二烷基苯磺酸钠、甘氨酸和聚乙烯吡咯烷酮中的至少2种。
9.在一些实例中,所述组合物为乳酸钠和十二烷基苯磺酸钠。
10.在一些实例中,乳酸钠和十二烷基苯磺酸钠的质量比为(10~30):(2~6)。
11.在一些实例中,乳酸钠和十二烷基苯磺酸钠的质量比为20:5。
12.在一些实例中,所述组合物为甘氨酸和十二烷基苯磺酸钠。
13.在一些实例中,甘氨酸和十二烷基苯磺酸钠的质量比为(15~30):(1~3)。
14.在一些实例中,甘氨酸和十二烷基苯磺酸钠的质量比为20:1。
15.本发明的第二个方面,提供:
16.一种稳定的胆硫乳琼脂平板,其添加有本发明第一个方面所述的组合物。
17.在一些实例中,每1000ml培养基中添加有乳酸钠0.1~0.3g,十二烷基苯磺酸钠0.02~0.06g。
18.在一些实例中,每1000ml培养基中添加有乳酸钠0.2g,十二烷基苯磺酸钠0.05g。
19.在一些实例中,每1000ml培养基中添加有甘氨酸0.75~1.5g,十二烷基苯磺酸钠0.02~0.06g。
20.在一些实例中,每1000ml培养基中添加有甘氨酸1g,十二烷基苯磺酸钠0.05g。
21.在一些实例中,每1000ml培养基中含有蛋白胨10.0g、牛肉膏粉3g、酵母粉3g、氯化钠5g、乳糖10.0g、蔗糖10.0g、胆盐3.0g、硫代硫酸钠2.0g、柠檬酸钠2g、柠檬酸铁铵1g、中性红0.03g、琼脂14g。
22.在一些实例中,每1000ml培养基中含有蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、牛胆盐1.0g、硫代硫酸钠2.2g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g,琼脂18.0g~20.0g,余量为水。
23.在一些实例中,每1000ml培养基中含有蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、去氧胆酸钠1.0g、硫代硫酸钠2.3g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g、琼脂18.0g~20.0g,余量为水。
24.本发明的有益效果是:
25.本发明的一些实例,配置出的平板,在储存期内不会出现点状或针状盐晶,且平板的保水性能好,储存6个月后,生物学性能依旧可以达标。解决了胆硫乳琼脂平板储存过程中容易析出盐晶,影响平板的外观及使用的问题。
26.本发明的一些实例,通过对胆硫乳琼脂平板的配方进行优化,可以得到稳定性更好的胆硫乳琼脂平板。
具体实施方式
27.下面结合实例,进一步说明本发明的技术方案。
28.对比例1:
29.sn/t2206.3
‑
2009使用的胆硫乳琼脂(dhl),组成为:蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、牛胆盐1.0g、硫代硫酸钠2.2g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g,琼脂18.0gg、蒸馏水1000ml,ph7.3。
30.对比例2:
31.gb/t4789.28
‑
2003规定的dhl琼脂,成分为:蛋白胨20.0g、牛肉膏粉3.0g、乳糖10.0g、蔗糖10.0g、去氧胆酸钠1.0g、硫代硫酸钠2.3g、柠檬酸钠1.0g、柠檬酸铁铵1.0g、中性红0.03g、琼脂18.0g、蒸馏水1000ml,ph7.3。
32.对比例3:
33.一种稳定不析出的胆硫乳琼脂平板,每1000ml培养基中含有蛋白胨10.0g、牛肉膏粉3g、酵母粉3g,氯化钠5g,乳糖10.0g、蔗糖10.0g、胆盐3.0g、硫代硫酸钠2.0g,柠檬酸钠2g,柠檬酸铁铵1g,中性红0.03g,琼脂14g,ph7.3。
34.对比例4
35.同对比例3,不同之处在于还添加了稳定剂,稳定剂为聚乙烯吡咯烷酮和聚乙二醇,1000ml培养基的添加量为聚乙烯吡咯烷酮0.5g,聚乙二醇0.01g,余量为水。
36.对比例5
37.同对比例3,不同之处在于还添加了稳定剂,稳定剂为聚乙二醇和甘氨酸,1000ml培养基的添加量为聚乙二醇0.02g,甘氨酸0.5g。
38.实施例1
39.同对比例3,不同之处在于还添加了稳定剂,稳定剂为乳酸钠和十二烷基苯磺酸钠,1000ml培养基的添加量为乳酸钠0.2g,十二烷基苯磺酸钠0.05g。
40.实施例2
41.同对比例3,不同之处在于还添加了稳定剂,稳定剂为甘氨酸和十二烷基苯磺酸钠,1000ml培养基的添加量为甘氨酸1g,十二烷基苯磺酸钠0.05g。
42.实施例3
43.同对比例3,不同之处在于还添加了稳定剂,稳定剂为聚乙烯吡咯烷酮和甘氨酸,1000ml培养基的添加量为聚乙烯吡咯烷酮0.5g,甘氨酸0.5g。
44.实施例4
45.同实施例1,不同之处在于乳酸钠和十二烷基苯磺酸钠的添加量分别为0.1g和0.06g。
46.实施例5
47.同实施例1,不同之处在于乳酸钠和十二烷基苯磺酸钠的添加量分别为0.15g和0.04g。
48.实施例6
49.同实施例1,不同之处在于乳酸钠和十二烷基苯磺酸钠的添加量分别为0.3g和0.02g。
50.实施例7
51.同对比例1,不同之处在于还添加了稳定剂,稳定剂为乳酸钠和十二烷基苯磺酸钠,其添加量(每1000ml培养基)为乳酸钠0.3g、十二烷基苯磺酸钠0.03g。
52.实施例8
53.同对比例2,不同之处在于还添加了稳定剂,稳定剂为乳酸钠和十二烷基苯磺酸钠,其添加量为乳酸钠0.1g、十二烷基苯磺酸钠0.04g。
54.下面结合实验,进一步说明本发明一些实例的胆硫乳琼脂平板性能。
55.平板性能测试:
56.1材料
57.1.1菌株
58.鼠伤寒沙门氏菌(salmonella typhimurium)atcc14028,福氏志贺氏菌(shigella falfella)cmcc(b)51572,粪肠球菌(enterococcus faecalis)atcc29212,由本实验室保存的商品化菌株。这些菌株可以使用其他公知的菌株替换。
59.1.2培养基及试剂
60.胰酪胨大豆琼脂培养基平板(简称tsa平板)由广东环凯微生物科技有限公司提
供。
61.2方法
62.2.1平板外观性能评价
63.2.1.1胆硫乳琼脂平板制备:按实施例中配方以及标准配方按比例进行称量,调整ph值,煮沸溶解,冷却至50℃倾注平板,备用。
64.2.1.2将制备好的胆硫乳琼脂平板进行包装,各平板均置于同一冷库,2~8℃中储存,分别在0d、15d、30d、60d、120d、180d取样,观察平板表面析出情况。
65.2.2培养基生物学性能评价
66.生长率试验:
67.采用定量方法进行。将鼠伤寒沙门氏菌、志贺氏菌2株菌的新鲜斜面培养物制成约103cfu/ml的菌悬液。分别取上述各菌液0.1ml用全自动螺旋接种仪分别接种于待测平板,鼠伤寒沙门氏菌、志贺氏菌的菌液同时接种参比培养基tsa平板,37
±
1℃培养18
‑
24小时。每种平板进行3个重复。观察各株菌在培养基上的生长情况,并对其进行菌落计数。按下列公式计算生长率p
r
。
68.p
r
=n
s
/n0,
69.n
s
:待测培养基平板上得到的平均菌落数;n0:参比培养基平板上获得的平均菌落数。
70.选择性测试:
71.将粪肠球菌制成108cfu/ml~109cfu/ml浓度菌悬液,用1μl接种环取菌悬液1环,在待测平板及参照培养基平板表面划六条平行直线,37
±
1℃培养18
‑
24小时;培养后按以下方法对培养基计算生长指数g。
72.1)每条有比较稠密菌落生长的划线则g为1,每个培养皿上最多为6分;
73.2)如果仅一半的线有菌落生长,则g为0.5;
74.3)如果划线上没有菌落生长或生长量少于划线的一半,则g为0。
75.记录每个平板的得分总和便得到g值。
76.3结果
77.3.1平板外观性能评价
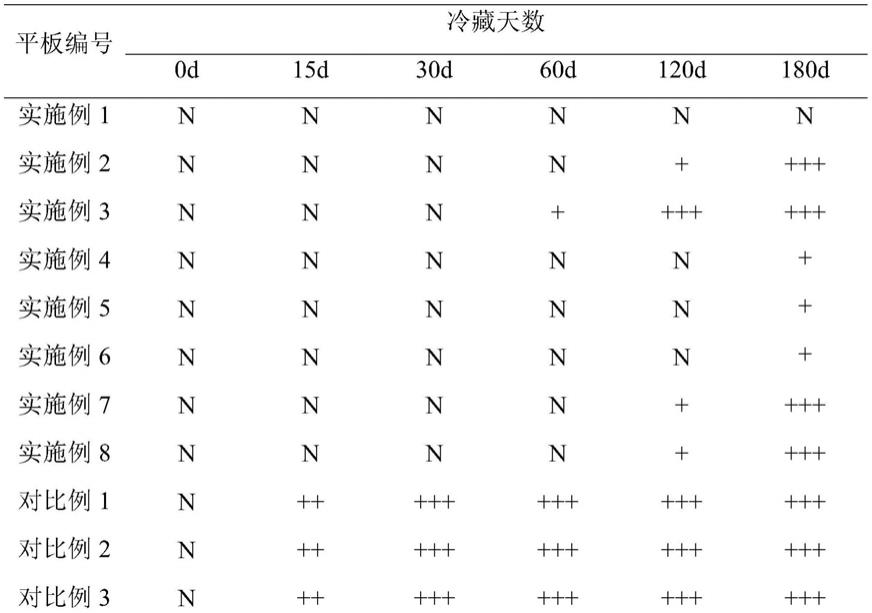
78.测试方法,目测,少量盐晶指平板表面≤10%的面积有肉眼可见的盐晶;大量盐晶指平板表面≥80%面积有肉眼可见的盐晶;介于二者之间的,计为部分盐晶。实验结果见下表。
[0079][0080][0081]
注:“n”表示无析出;“+”表示析出少量盐晶;“++”表示析出部分盐晶;“+++”表示析出大量盐晶。
[0082]
结果表明:
[0083]
1)乳酸钠、十二烷基苯磺酸钠、甘氨酸、聚乙烯吡咯烷酮中的两种,特别是乳酸钠和十二烷基苯磺酸钠组合、甘氨酸和十二烷基苯磺酸钠组合、甘氨酸和聚乙烯吡咯烷酮组合使用,均有提高胆硫乳琼脂平板作用,其中乳酸钠和十二烷基苯磺酸钠组合的效果最佳,甘氨酸和十二烷基苯磺酸钠组合次之,甘氨酸和聚乙烯吡咯烷酮组合的效果较弱;
[0084]
2)聚乙烯吡咯烷酮和聚乙二醇组合、聚乙二醇和甘氨酸组合,未显示出提高胆硫乳琼脂稳定性的效果;
[0085]
3)乳酸钠和十二烷基苯磺酸钠作为稳定剂添加在胆硫乳琼脂平板内,可以显著提高现有胆硫乳琼脂平板的稳定性;
[0086]
4)通过对胆硫乳琼脂平板的配方进行进一步优化,可以获得稳定性更佳的胆硫乳琼脂平板。
[0087]
3.2生物学
[0088]
将实施例1所述平板,与新配制的胆硫乳琼脂平板(对比例3)进行比较,结果如下:
[0089][0090]
综上所述:仅有实施案例1所述的胆硫乳琼脂平板的保质期最长,6个月后其外观未发生变化,平板表面未见杂质或盐晶,且6个月后生物学效果与新配制的平板相当,培养基的性能良好,为延长即用型成品培养基的保质期提供了新途径。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1