杂环单酰基甘油脂肪酶(MAGL)抑制剂的制作方法
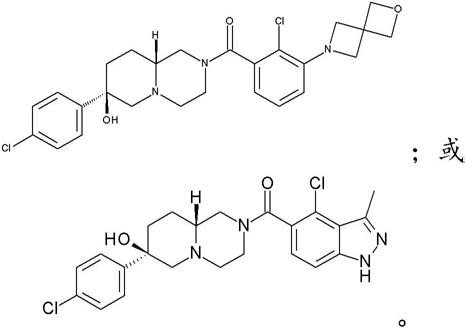
杂环单酰基甘油脂肪酶(magl)抑制剂
技术领域
1.本发明涉及可用于哺乳动物的治疗或预防的有机化合物,并且具体地涉及用于治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症、精神障碍、多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑症、偏头痛和/或抑郁症的单酰基甘油脂肪酶(magl)抑制剂。
背景技术:
2.内源性大麻素(ec)是通过与大麻素受体(cbr)、cb1和cb2相互作用而发挥其生物作用的脂质信号。它们调控多种生理过程,包括神经炎症、神经退行性疾病和组织再生(iannotti,f.a.等人,progress in lipid research 2016,63,107-28.)。在大脑中,主要的内源性大麻索2-花生四烯酰甘油(2-ag)由双酰基甘油脂肪酶(dagl)产生,并由单酰基甘油脂肪酶(magl)水解。magl可水解85%的2-ag;剩余15%被abhd6和abdh12水解(nomura,d.k.等人,science 2011,334,809)。magl在整个大脑和大多数脑细胞类型(包括神经元、星形胶质细胞、少突胶质细胞和小神经胶质细胞)中表达(chanda,p.k.等人,molecular pharmacology 2010,78,996;viader,a.等人,cell reports 2015,12,798.)。2-ag水解形成花生四烯酸(aa),即前列腺素(pg)和白三烯(lt)的前体。炎症组织中的aa氧化代谢增加。炎症过程涉及花生四烯酸氧化的两个主要酶反应途径,即产生pg的环氧化酶和产生lt的5-脂氧合酶。在炎症过程中形成的各种环氧化酶产物中,pge2是最重要的产物之一。已在炎症部位(例如在神经退行性疾病患者的脑脊液中)检测到这些产物,并且认为其助长了炎症反应和疾病进展。缺乏magl(mgll-/-)的小鼠的神经系统中的2-ag水解酶活性显著降低,而2-ag水平升高,而其他含花生四烯酸的磷酸脂和中性脂类(包括花生四烯酸乙醇胺(anandamide,aea)以及其他游离脂肪酸)保持不变。相反,衍生自aa和aa衍生的前列腺素和其他类花生酸(包括前列腺素e2(pge2)、d2(pgd2)、f2(pgf2)和血栓素b2(txb2))的水平则大大降低。磷脂酶a2(pla2)已被视为aa的主要来源,但cpla2缺陷型小鼠的大脑中aa水平不变,从而增强了大脑中的magl对aa产生和脑炎症过程的调控的关键作用。
3.神经炎症是脑部疾病的常见病理变化特征,这些疾病包括但不限于神经退行性疾病(例如,多发性硬化、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫和精神障碍诸如焦虑和偏头痛)。在大脑中,类花生酸和前列腺素的产生控制神经炎症过程。促炎剂脂多糖(lps)导致脑部类花生酸产生稳定的时间依赖性升高,该现象在mgll-/-小鼠中明显减弱。lps治疗还引起促炎性细胞因子(包括白细胞介素-1-a(il-1-a)、il-1b、il-6)和肿瘤坏死因子-a(tnf-a)(在mgll-/-小鼠中被抑制)普遍升高。
4.神经炎症的特征在于中枢神经系统的先天免疫细胞、小胶质细胞以及星形胶质细胞的活化。据报道,抗炎药在临床前模型中可抑制神经胶质细胞的活化以及疾病(包括阿尔茨海默氏病和多发性硬化症)的进展(lleo a.,cell mol life sci.2007,64,1403.)。重要的是,magl活性的遗传和/或药理破坏也阻断lps诱导的大脑中小胶质细胞的活化(nomura,
d.k.等人,science 2011,334,809.)。
5.此外,在多种神经退行性疾病(包括但不限于阿尔茨海默氏病、帕金森氏病和多发性硬化)的动物模型中,证明magl活性的遗传和/或药理破坏具有保护作用。例如,不可逆的magl抑制剂已广泛应用于神经炎症和神经退行性疾病的临床前模型中(long,j.z.等人,nature chemical biology 2009,5,37.)。全身注射此类抑制剂可重现大脑中的mgll-/-小鼠表型,包括2-ag水平升高、aa水平下降及相关的类花生酸生成,并且防止lps诱导神经炎症后发生细胞因子生成和小胶质细胞活化(nomura,d.k.等人,science 2011,334,809.),完全确认magl是一种药物靶点。
6.随着magl活性发生遗传和/或药理破坏,大脑中magl天然底物2-ag的内源性水平升高。据报道,2-ag对疼痛表现出有益的作用,例如对小鼠具有镇痛作用(ignatowska-jankowska b.等人,j.pharmacol.exp.ther.2015,353,424),并且对精神障碍(例如慢性应激模型中的抑郁症)也具有有益的作用(zhong p.等人,neuropsychopharmacology 2014,39,1763.)。
7.此外,少突胶质细胞(ol)、中枢神经系统的髓鞘细胞及其前体(opc)在其膜上表达大麻素受体2(cb2)。2-ag是cb1和cb2受体的内源性配体。据报道,大麻素和magl的药理抑制作用均减弱了ol和opc的兴奋性中毒发作弱点,因此可能具有神经保护作用(bernal-chico,a.等人,glia 2015,63,163.)。此外,magl的药理抑制提高了小鼠脑部髓鞘ol的数量,表明magl抑制作用可促进体内髓鞘ol中opc的分化(alpar,a.等人,nature communications 2014,5,4421.)。在进行性多发性硬化症的小鼠模型中,magl的抑制作用还可促进髓鞘再生和机能恢复(feliu a.等人,journal of neuroscience 2017,37(35),8385.)。
8.最后,近年来,代谢尤其是脂质代谢在癌症研究中受到高度重视。研究人员认为,从头合成脂肪酸在肿瘤发展中具有重要作用。许多研究表明,内源性大麻素具有抗肿瘤作用,包括抗增殖、诱导细胞凋亡和抗转移作用。magl作为脂质代谢和内源性大麻索系统中重要的分解酶,并且作为基因表达特征的组成部分,影响肿瘤发生的不同方面(qin,h.等人,cell biochem.biophys.2014,70,33;nomura dk等人,cell 2009,140(1),49-61;nomura dk等人,chem.biol.2011,18(7),846-856.)。
9.总之,抑制magl的作用和/或活化是治疗或预防神经炎症、神经退行性疾病、疼痛、癌症和精神障碍的有前景的全新治疗策略。此外,抑制magl的作用和/或活化是提供神经保护和髓鞘再生的有前景的全新治疗策略。因此,对新型magl抑制剂存在未得到满足的迫切的医疗需求。
技术实现要素:
10.在第一方面,本发明提供了式(i)化合物或其药用盐,
[0011][0012]
其中r1至r3如本文所定义。
[0013]
在另一方面,本发明提供了一种生产如本文所述的式(i)化合物的方法,该方法包括:
[0014]
(a)使胺12或14,其中r2如本文定义且r3为羟基(12)或氢(14)
[0015][0016]
与羧酸15,其中r1如本文定义
[0017][0018]
在偶联试剂(例如hatu、dcc、edci、hobt、tbtu或t3p)和碱(例如huenig碱、三乙胺或dmap)的存在下反应以提供其中r3是羟基或氢的所述式(i)化合物;并且任选地,前提是r3是羟基;
[0019]
(b)通过用合适的碱如nah、kh、nahmds、lihmds或lda,优选用nah处理,然后添加亲电子试剂,例如,烷基-或环烷基卤化物,例如mei、eti、ipri或cypri,将醇r3烷基化,以产生其中r3是烷氧基或环烷氧基的相应的式(l)化合物;或者
[0020]
(c)通过使其中r3是羟基的式(i)化合物与(i)酸(例如hcl、hbr、hi)、pocl3、socl2或pbr3)反应;或(ii)与合适的氨基硫试剂(例如dast)反应;或(iii)与磺酰化试剂(例如甲磺酰氯)反应,然后使中间体磺酸酯与卤化物(例如naf)反应,从而将醇r3转化为卤素以产生其中r3是卤素的相应的式(i)化合物。
[0021]
在另一方面,本发明提供了根据本文所述的方法制造的如本文所述的式(i)的化合物。
[0022]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐,其用作治疗活性物质。
[0023]
在另一方面,本发明提供了一种药物组合物,其包含如本文所述的式(i)化合物或其药用盐,以及治疗惰性载体。
[0024]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于抑制哺乳动物的单酰基甘油脂肪酶(magl)的用途。
[0025]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的用途。
[0026]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的用途。
[0027]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐,用于在抑制哺乳动物的单酰基甘油脂肪酶的方法中使用。
[0028]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐,用于在治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍中使用。
[0029]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐,用于在治疗或
预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癞痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛中使用。
[0030]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于抑制哺乳动物的单酰基甘油脂肪酶的药物中的用途。
[0031]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的药物中的用途。
[0032]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的药物中的用途。
[0033]
在另一方面,本发明提供了一种抑制哺乳动物的单酰基甘油脂肪酶的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0034]
在另一方面,本发明提供了一种治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0035]
在另一方面,本发明提供了一种治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
具体实施方式
[0036]
定义
[0037]
结合本发明的特定方面、实施例或实例描述的特征、整数、特性、化合物、化学部分或基团应理解为适用于本文所述的任何其他方面、实施例或实例,除非与其不相容。本说明书(包括任何所附权利要求、摘要和附图)中所公开的所有特征和/或由此公开的任何方法或过程的所有步骤可以任何组合进行组合,除了这些特征和/或步骤中的至少一些互相排斥的组合之外。本发明不限于任何前述实施例的细节。本发明扩展到本说明书(包括任何所附权利要求、摘要和附图)中所公开的特征的任何新颖特征或任何新颖组合,或者扩展到由此公开的任何方法或过程的步骤的任何新颖步骤或任何新颖组合。
[0038]
术语“烷基”是指1至6个碳原子(“c
1-c
6-烷基”)(例如,1、2、3、4、5或6个碳原子)的单价或多价(例如,单价或二价)直链或支链饱和烃基团。在一些实施例中,烷基基团含有1至3个碳原子,例如1、2或3个碳原子。烷基的一些非限制性实例包括甲基、乙基、丙基、2-丙基(异丙基)、正丁基、异丁基、仲丁基、叔丁基和2,2-二甲基丙基。烷基的特别优选但非限制性实例是甲基。
[0039]
术语“烷氧基”是指经由氧原子附接到母体分子部分上的如前所定义的烷基基团。
基)、三唑基(例如,1h-1,2,4-三唑-3-基、1h-三唑-4-基、2h-三唑-4-基)和四唑基(例如,2h-四唑-5-基)。
[0045]
术语“环烷氧基”是指通过氧原子连接至母体分子部分的如前文所定义的环烷基基团。
[0046]
术语“羟基”是指-oh基团。
[0047]
术语“氨基”是指-nh2基团。
[0048]
术语“氧代”是指双键氧(=o)。
[0049]
术语“烷氧基羰基”是指基团烷基-o-c(o)-(通常称为“羧酸酯”),其中烷基如本文所定义。
[0050]
术语“羧基”是指基团-c(o)oh(通常称为“羧酸”)。
[0051]
术语“烯基”表示包含至少一个c-c双键(例如,1个或2个c-c双键)的2至6个碳原子的单价或二价直链或支链烃基(“c
2-c
6-烯基”)。在特定实施例中,烯基具有2至4个碳原子和至少一个c-c双键(例如1个或2个c-c双键)。烯基的实例包括乙烯基、丙烯基、丙-2-烯基、异丙烯基、正丁烯基(例如,(z)-丁-1-烯基)、异丁烯基、烯丙基、2-甲基烯丙基、2-甲基丙-1-烯基和丙-1,2-二烯基。
[0052]
术语“羟基环烷基”是指如本文所定义的环烷基基团,其中至少一个氢原子已被羟基基团代替的环烷基基团。优选地,“羟基环烷基”是指其中烷基基团的1、2或3个氢原子(最优选1个氢原子)已被羟基基团代替的环烷基基团。羟基环烷基基团的优选的、但非限制性实例是羟基环丙基(例如,1-羟基环丙基)。
[0053]
术语“药用盐”是指保留游离碱或游离酸的生物效果和性质的那些盐,这些盐在生物学或其他方面不是不合需要的。这些盐用无机酸诸如盐酸、氢溴酸、硫酸、硝酸、磷酸等(特别是盐酸)和有机酸诸如乙酸、丙酸、乙醇酸、丙酮酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、苯甲酸、肉桂酸、扁桃酸、甲基磺酸、乙基磺酸、对甲苯磺酸、水杨酸、n-乙酰基半胱氨酸等形成。此外,这些盐可通过将无机碱或有机碱加入游离酸中来制备。衍生自无机碱的盐包括但不限于钠、钾、锂、铵、钙、镁盐等。衍生自有机碱的盐包括但不限于以下各项的盐:伯胺、仲胺和叔胺、取代胺(包括天然存在的取代胺)、环胺和碱性离子交换树脂(诸如异丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、赖氨酸、精氨酸、n-乙基哌啶、哌啶、聚亚胺树脂等)。式(i)化合物的特定药用盐为盐酸盐。
[0054]
如本文所用,术语“保护基”(pg)表示选择性封闭多功能化合物中的反应位点以便在合成化学中通常与之相关的另一未保护的反应位点上选择性发生化学反应的基团。保护基可在适当的点被去除。示例性保护基为氨基保护基、羧基保护基或羟基保护基。特定保护基为叔丁氧基羰基(boc)、苄氧基羰基(cbz)、芴基甲氧基羰基(fmoc)和苄基(bn)。另一些特定保护基为叔丁氧基羰基(boc)和芴基甲氧基羰基(fmoc)。更特定的保护基为叔丁氧基羰基(boc)。示例性保护基及其在有机合成中的应用描述于例如:t.w.greene和p.g.m.wutts,protective groups in organic chemistry,第5版,2014,john wiley&sons,n.y.。
[0055]
式(i)的化合物可以含有若干不对称中心,并且可以以光学纯对映体、对映体的混合物(例如外消旋体)、光学纯非对映体、非对映体的混合物、非对映外消旋体或非对映外消旋体的混合物存在。
[0056]
根据cahn-ingold-prelog惯例,非对称碳原子可以是“r”或“s”构型。
[0057]
缩写“magl”是指单酰基甘油脂肪酶。术语“magl”和“单酰基甘油脂肪酶”在本文中可互换使用。
[0058]
如本文所用的术语“治疗”包括:(1)抑制疾病的至少一种临床或亚临床症状的状态、病症或病情(例如,在维持治疗的情况下,阻止、减轻或延迟疾病的发展或其复发);和/或(2)缓解病情(即,使疾病的状态、病症或病情或者至少一种临床或亚临床症状消退)。对待治疗患者的益处在统计学上是显著的或者至少是患者或医生可察觉的。然而,应当理解,当向患者施用药物以治疗疾病时,结果可能并不总是有效的治疗。
[0059]
如本文所用的术语“防治”包括:预防或延迟状态、病症或病情的临床症状的出现,该状态、病症或病情在可能患有或易患该状态、病症或病情但尚未经历或显示该状态、病症或病情的临床或亚临床症状的哺乳动物中、尤其是在人类中发展。
[0060]
如本文所用,术语“神经炎症”涉及神经组织的急性和慢性炎症,该神经组织为神经系统的两个部分的主要组织成分;中枢神经系统(cns)的脑和脊髓以及周围神经系统(pns)的分支周围神经。慢性神经炎症与神经退行性疾病诸如阿尔茨海默氏病、帕金森氏病和多发性硬化症相关联。急性神经炎症通常在中枢神经系统受伤后立即发生,例如,由创伤性脑损伤(tbi)引起。
[0061]
如本文所用,术语“创伤性脑损伤”(“tbi”,也称为“颅内损伤”)涉及因外部机械力诸如快速加速或减速、冲击、冲击波或弹丸穿透而造成的脑损伤。
[0062]
如本文所用,术语“神经退行性疾病”涉及与神经元的结构或功能的进行性丧失(包括神经元死亡)相关的疾病。神经退行性疾病的实例包括但不限于多发性硬化、阿尔茨海默氏病、帕金森氏病和肌萎缩性脊髓侧索硬化症。
[0063]
如本文所用,术语“精神障碍”(也称为精神病或精神疾病)涉及可能引起痛苦或生活能力差的行为或精神模式。此类特征可能是持续的、复发的或缓和的,也可能是单个事件。精神障碍的实例包括但不限于焦虑和抑郁症。
[0064]
如本文所用,术语“疼痛”是指与实际或潜在的组织损伤相关联的不愉快的感觉和情感体验。疼痛的实例包括但不限于伤害性疼痛、慢性疼痛(包括特发性疼痛)、神经性疼痛(包括化疗诱导的神经病)、幻痛和精神性疼痛。疼痛的一个特定实例是神经性疼痛,其由影响到涉及身体感觉的神经系统(即躯体感觉系统)的任何部分的损伤或疾病引起。在一个实施例中,“疼痛”是由于截肢或开胸手术引起的神经性疼痛。在一个实施例中,“疼痛”是化疗引起的神经病。
[0065]
如本文所用,术语“神经毒性”是指神经系统的毒性。这种情况发生于暴露于天然或人造有毒物质(神经毒素)时,这些物质改变神经系统的正常活动,从而对神经组织造成损伤。神经毒性的实例包括但不限于因暴露于化疗、放射治疗、药物疗法、药物滥用和器官移植中所用的物质以及暴露于重金属、某些食品和食品添加剂、农药、工业和/或清洁溶剂、化妆品和一些天然物质而引起的神经毒性。
[0066]
如本文所用,术语“癌症”是指特征在于因异常失控的细胞(此类细胞为“癌细胞”)的生长而导致赘生物或肿瘤存在的疾病。如本文所用,术语癌症明确地包括但不限于肝细胞癌、结肠癌和卵巢癌。
[0067]
如本文所用的术语“哺乳动物”包括人类和非人类,并且包括但不限于人类、非人类灵长类动物、犬、猫、鼠、牛、马和猪。在特别优选的实施例中,术语“哺乳动物”是指人类。
[0068]
本发明的化合物
[0069]
在第一方面(a1),本发明提供式(i)化合物
[0070][0071]
或其药用盐,其中:
[0072]
r1选自由以下各项组成的组:
[0073]
(i)任选地被1-2个独立地选自由以下各项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0074]
(ii)任选地被1-2个独立地选自由以下各项组成的组的取代基取代的5元至6元杂芳基:卤素、羟基、c
1-6-烷氧基、-b(oh)2、5元至6元杂芳基、c
1-6-烷基和氨基;和
[0075]
(iii)任选地被1-3个独立地选自由以下各项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代;
[0076]
r2选自由以下各项组成的组:
[0077]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0078]
(ii)c
3-14-环烷基;
[0079]
(iii)任选地被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;
[0080]
(iv)任选地被1-3个独立地选自以下的取代基取代的5元至14元杂芳基:卤素、c
1-6-烷基、卤代-c
1-6-烷基和氧代;和
[0081]
(v)任选地被1-3个独立地选自以下的取代基取代的5元至14元杂芳氧基:卤素、c
1-6-烷基、卤代-c
1-6-烷基和氧代;和
[0082]
(vi)任选地被1-3个独立地选自以下的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基、卤代-c
1-6-烷基和氧代;
[0083]
r3选自由以下各项组成的组:氢、卤素、c
1-6-烷氧基、c
3-14-环烷氧基和羟基;
[0084]
r4选自由以下各项组成的组:氢、卤素、c
1-6-烷基、羟基-c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基、氨基、羧基、c
1-6-烷基-c(o)-nh-、c
2-6-烯基-c(o)-nh-、羧基-nh-、氧代、c
3-14-环烷基和羟基-c
3-14-环烷基;
[0085]
l选自由以下各项组成的组:共价键和-ch=ch-;
[0086]
a选自由以下各项组成的组:c
6-c
14-芳基、5元至14元杂芳基和5元至14元杂环基;且
[0087]
n为1、2、3或4。
[0088]
本发明进一步提供了以下根据第一方面a1列举的实施例(e):
[0089]
e1根据a1所述的式(i)化合物或其药用盐,其中:
[0090]
r1选自由以下各项组成的组:
[0091]
(i)任选地被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:
(2-氯-6-氟苯基)甲酮;
[0115]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-氯苯基)甲酮;
[0116]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-6-甲基吡啶-3-基)甲酮;
[0117]
[(7r,9ar)-7-苯基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-丙-2-基氧基苯基)甲酮盐酸盐;
[0118]
[(7r,9ar)-7-苯基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-1-甲基吡咯并[2,3-b]吡啶-5-基)甲酮;
[0119]
[(7r,9ar)-7-苯基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-1-丙-2-基吡咯并[2,3-b]吡啶-5-基)甲酮;
[0120]
[(7s,9as)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-溴-3-甲氧基苯基)甲酮;
[0121]
[(7r,9ar)-7-苯基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(3-氯-2-甲氧基吡啶-4-基)甲酮;
[0122]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-1-甲基吡咯并[2,3-b]吡啶-5-基)甲酮;
[0123]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-1-甲基吡唑并[3,4-b]吡啶-5-基)甲酮;
[0124]
[(7r,9ar)-7-(3,4-二氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-溴-3-甲氧基苯基)甲酮;
[0125]
[(7s,9as)-7-(3,4-二氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-溴-3-甲氧基苯基)甲酮;
[0126]
[(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0127]
[(7s,9as)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0128]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-5-甲氧基吡啶-3-基)甲酮;
[0129]
(4-氯-3-甲基-[1,2]噁唑并[5,4-b]吡啶-5-基)-[外消旋-(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0130]
[(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-3-甲基-[1,2]噁唑并[5,4-b]吡啶-5-基)甲酮;
[0131]
[(7s,9as)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(4-氯-3-甲基-[1,2]噁唑并[5,4-b]吡啶-5-基)甲酮;
[0132]
(4-氯-3-甲基-1h-吲唑-5-基)-[外消旋-(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0133]
(4-氯-[1,2]噻唑[5,4-b]吡啶-5-基)-[外消旋-(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0134]
(4-氯-3-甲基-1h-吲唑-5-基)-[外消旋-(7r,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0135]
(4-氯-3-甲基-1h-吲唑-5-基)-[外消旋-(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0136]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(4-氯-3-甲基-1h-吲唑-5-基)甲酮;
[0137]
[(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(4-氯-3-甲基-1h-吲唑-5-基)甲酮;
[0138]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0139]
[(7s,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0140]
[(7r,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0141]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0142]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0143]
[(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0144]
[2-氯-3-(2-氧杂-6-氮杂螺[3.3]庚烷-6-基)苯基]-[外消旋-(7r,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0145]
[2-氯-3-(2-氧杂-6-氮杂螺[3.3]庚烷-6-基)苯基]-[外消旋-(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0146]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-(4-氯苯基)-7-氟-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0147]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-(4-氯苯基)-7-氟-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0148]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-(4-氯苯基)-7-甲氧基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0149]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-(4-氯苯基)-7-甲氧基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0150]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-甲基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0151]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-甲基-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0152]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-(6-甲氧基吡啶-2-基)甲酮;和
[0153]
(6-氨基-4-氯吡啶-3-基)-[外消旋-(7r,9ar)-7-(3-氯-4-氟苯基)-1,3,4,6,7,
8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]甲酮。
[0154]
e4根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1选自由以下项组成的组
[0155]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0156]
(ii)任选地被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、羟基、c
1-6-烷氧基、-b(oh)2、5元至6元杂芳基、c
1-6-烷基和氨基;和
[0157]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代。
[0158]
e5根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1选自由以下项组成的组
[0159]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0160]
(ii)被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、c
1-6-烷氧基、c
1-6-烷基和氨基;和
[0161]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代。
[0162]
e6根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1是被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0163]
e7根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1是被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0164]
e8根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1是被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0165]
e9根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中r1是被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0166]
e10根据a1和e1至e9中任一项所述的式(i)化合物或其药用盐,其中r2选自由以下项组成的组
[0167]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0168]
(ii)c
3-14-环烷基;
[0169]
(iii)被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;
[0170]
(iv)被卤代-c
1-6-烷基取代的5元至14元杂芳基;和
[0171]
(v)被卤素取代的5元至14元杂芳氧基。
[0172]
e11根据a1和e1至e9中任一项所述的式(i)化合物或其药用盐,其中r2选自由以下项组成的组
[0173]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0174]
(ii)c
3-14-环烷基;
[0175]
(iii)被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;和
[0176]
(iv)被卤代-c
1-6-烷基取代的5元至14元杂芳基。
[0177]
e12根据a1和e1至e9中任一项所述的式(i)化合物或其药用盐,其中r2选自由以下项组成的组
[0178]
(i)卤代-c
6-c
14-芳基;和
[0179]
(ii)被卤代-c
1-6-烷基取代的5元至14元杂芳基。
[0180]
e13根据a1和e1至e9中任一项所述的式(i)化合物或其药用盐,其中r2选自由以下项组成的组
[0181]
(i)氯苯基;
[0182]
(ii)3-氯-4-氟-苯基;和
[0183]
(iii)被cf3取代的吡啶基。
[0184]
e14根据a1和e1至e9中任一项所述的式(i)化合物或其药用盐,其中r2选自由以下项组成的组
[0185]
(iv)氯苯基;和
[0186]
(v)被cf3取代的吡啶基。
[0187]
e15根据a1和e1至e14中任一项所述的式(i)化合物或其药用盐,其中r3为氢或羟基。
[0188]
e16根据a1和e1至e14中任一项所述的式(i)化合物或其药用盐,其中r3是羟基。
[0189]
e17根据a1和e1至e16中任一项所述的式(i)化合物或其药用盐,其中r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、羟基-c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代。
[0190]
e18根据a1和e1至e16中任一项所述的式(i)化合物或其药用盐,其中r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代。
[0191]
e19根据a1和e1至e16中任一项所述的式(i)化合物或其药用盐,其中r4选自由以下项组成的组:氢、卤素和羟基。
[0192]
e20根据a1和e1至e16中任一项所述的式(i)化合物或其药用盐,其中r4选自由以下项组成的组:氢、氟和羟基。
[0193]
e21根据a1和e1至e20中任一项所述的式(i)化合物或其药用盐,其中l是共价键。
[0194]
e22根据a1和e1至e21中任一项所述的式(i)化合物或其药用盐,其中a选自由以下项组成的组:5元至14元杂芳基和5元至14元杂环基。
[0195]
e23根据a1和e1至e21中任一项所述的式(i)化合物或其药用盐,其中a选自由以下
项组成的组:吡唑基和氮杂环丁烷基。
[0196]
e24根据a1和e1至e3中任一项所述的式(i)化合物或其药用盐,其中
[0197]
r1选自由以下项组成的组:
[0198]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0199]
(ii)被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、c
1-6-烷氧基、c
1-6-烷基和氨基;和
[0200]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代;
[0201]
r2选自由以下项组成的组:
[0202]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0203]
(ii)c
3-14-环烷基;
[0204]
(iii)被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;和
[0205]
(iv)被卤代-c
1-6-烷基取代的5元至14元杂芳基;
[0206]
r3为氢或羟基;
[0207]
r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代;
[0208]
l选自由以下项组成的组:共价键和-ch=ch-;并且
[0209]
a选自由以下项组成的组:c
6-c
14-芳基、5元至14元杂芳基和5元至14元杂环基。
[0210]
e25根据a1、e1和e3所述的式(i)化合物或其药用盐,其中:
[0211]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0212]
r2选自由以下项组成的组:
[0213]
(i)卤代-c
6-c
14-芳基;和
[0214]
(ii)被卤代-c
1-6-烷基取代的5元至14元杂芳基;
[0215]
r3为羟基;
[0216]
r4选自由以下项组成的组:氢、卤素和羟基;
[0217]
l为共价键;并且
[0218]
a选自由以下项组成的组:5元至14元杂芳基和5元至14元杂环基。
[0219]
e26根据a1、e1和e3所述的式(i)化合物或其药用盐,其中:
[0220]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0221]
r2选自由以下项组成的组:
[0222]
(i)氯苯基;和
[0223]
(ii)被cf3取代的吡啶基;
[0224]
r3为羟基;
[0225]
r4选自由以下项组成的组:氢、氟和羟基;
[0226]
l为共价键;并且
[0227]
a选自由以下项组成的组:吡唑基和氮杂环丁烷基。
[0228]
e27根据a1、e1和e3所述的式(i)化合物或其药用盐,其中:
[0229]
r1选自由以下项组成的组:
[0230]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0231]
(ii)被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、c
1-6-烷氧基、c
1-6-烷基和氨基;和
[0232]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代;
[0233]
r2选自由以下项组成的组:
[0234]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0235]
(ii)c
3-14-环烷基;
[0236]
(iii)被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;和
[0237]
(iv)被卤代-c
1-6-烷基取代的5元至14元杂芳基;
[0238]
r3为氢或羟基;
[0239]
r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代;
[0240]
l选自由以下项组成的组:共价键和-ch=ch-;
[0241]
a选自由以下项组成的组:c
6-c
14-芳基、5元至14元杂芳基和5元至14元杂环基;且
[0242]
n为1或2。
[0243]
e28根据a1、e1和e3所述的式(i)化合物或其药用盐,其中:
[0244]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0245]
r2选自由以下项组成的组:
[0246]
(i)卤代-c
6-c
14-芳基;和
[0247]
(ii)被卤代-c
1-6-烷基取代的5元至14元杂芳基;
[0248]
r3为羟基;
[0249]
r4选自由以下项组成的组:氢、卤素和羟基;
[0250]
l为共价键;
[0251]
a选自由以下项组成的组:5元至14元杂芳基和5元至14元杂环基;且
[0252]
n为1或2。
[0253]
e29根据a1、e1和e3所述的式(i)化合物或其药用盐,其中:
[0254]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0255]
r2选自由以下项组成的组:
[0256]
(i)氯苯基;
[0257]
(ii)3-氯-4-氟-苯基;和
[0258]
(iii)被cf3取代的吡啶基;
[0259]
r3为羟基;
[0260]
r4选自由以下项组成的组:氢、氟和羟基;
[0261]
l为共价键;
[0262]
a选自由以下项组成的组:吡唑基和氮杂环丁烷基;并且
[0263]
n为1或2。
[0264]
e30根据a1所述的式(i)化合物或其药用盐,其中所述式(i)化合物选自由以下项组成的组:
[0265]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0266]
[(7r,9as)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0267]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-5-基)苯基]甲酮;
[0268]
[(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-5-基)苯基]甲酮;
[0269]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-氟-1h-吡唑-4-基)苯基]甲酮;
[0270]
[(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-氟-1h-吡唑-4-基)苯基]甲酮;
[0271]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-6-甲氧基吡啶-3-基)甲酮;
[0272]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(6-氨基-2-甲基吡啶-3-基)甲酮;
[0273]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0274]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0275]
5-[(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-6-氯-1-甲基吡啶-2-酮;
[0276]
5-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-6-氯-1-甲基吡啶-2-酮;
[0277]
3-[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氯苯基]-1,3-噁唑烷-2-酮;
[0278]
1-[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氯苯基]咪唑烷-2-酮;
[0279]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(4-甲基-1h-吡唑-3-基)苯基]甲酮;
[0280]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(4-甲基-1h-吡唑-5-基)苯基]甲酮;
[0281]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[3-(4-甲基-1h-吡唑-3-基)苯基]甲酮;
[0282]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0283]
[(7s,9as)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0284]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-5-基)苯基]甲酮;
[0285]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氟-3-吗啉-4-基苯基)甲酮;
[0286]
4-[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氟苯基]哌嗪-1-甲酸叔丁酯;
[0287]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氟-3-哌嗪-1-基苯基)甲酮;
[0288]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-羟基-7-(2-甲基丙基)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0289]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-环戊基-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0290]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-羟基-7-(三氟甲基)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0291]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-[2-溴-3-[(z)-2-苯基乙烯基]苯基]甲酮;
[0292]
[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-[2-溴-3-[(e)-2-苯基乙烯基]苯基]甲酮;
[0293]
n-[4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴苯基]乙烯基]苯基]氨基甲酸叔丁酯;
[0294]
n-[4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴苯基]乙烯基]苯基]丙-2-烯酰胺;
[0295]
4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴-苯基]乙烯基]-n-甲基-苯甲酰胺;
[0296]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶
并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0297]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-羟基苯基)甲酮;
[0298]
4-(3-((7s,9ar)-7-(4-氯苯基)-7-羟基八氢-2h-吡啶并[1,2-a]吡嗪-2-羰基)-2-氟苯基)哌嗪-2-酮;
[0299]
4-[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氯苯基]哌嗪-2-酮;
[0300]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(6-氧杂-1-氮杂螺[3.3]庚烷-1-基)苯基]甲酮;
[0301]
[(7s,9as)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(二氟甲氧基)苯基]甲酮;
[0302]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(二氟甲氧基)苯基]甲酮;
[0303]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0304]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0305]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-氟苯基)甲酮;
[0306]
[(7s,9as)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-氟苯基)甲酮;
[0307]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3s)-3-羟基吡咯烷-1-基]苯基]甲酮;
[0308]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3r)-3-羟基吡咯烷-1-基]苯基]甲酮;
[0309]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3r)-3-羟基吡咯烷-1-基]苯基]甲酮;
[0310]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基-3-甲基氮杂环丁烷-1-基)苯基]甲酮;
[0311]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3s)-3-羟基哌啶-1-基]苯基]甲酮;
[0312]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3r)-3-羟基哌啶-1-基]苯基]甲酮;
[0313]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(4-羟基哌啶-1-基)苯基]甲酮;
[0314]
[2-氯-3-(3-羟基-3-甲基吡咯烷-1-基)苯基]-[外消旋-(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;
[0315]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3s,4s)-3,4-二羟基吡咯烷-1-基]苯基]甲酮;
基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮;和
[0336]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-羟基-7-[6-(三氟甲基)吡啶-3-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮。
[0337]
e31根据a1所述的式(i)化合物或其药用盐,其中所述式(i)化合物选自由以下项组成的组:
[0338]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0339]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-5-基)苯基]甲酮;
[0340]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-氟-1h-吡唑-4-基)苯基]甲酮;
[0341]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0342]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0343]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0344]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-5-基)苯基]甲酮;
[0345]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(3-羟基氮杂环丁烷-1-基)苯基]甲酮;
[0346]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3r)-3-羟基吡咯烷-1-基]苯基]甲酮;
[0347]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-[(3s,4s)-3,4-二羟基吡咯烷-1-基]苯基]甲酮;
[0348]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1h-吡唑-3-基)苯基]甲酮;
[0349]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(1h-吡唑-3-基)苯基]甲酮;
[0350]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(4-氟-1h-吡唑-5-基)苯基]甲酮;
[0351]
[(7s,9ar)-7-(3,4-二氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮;
[0352]
[(7s,9ar)-7-(3,4-二氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氟-3-(1h-吡唑-5-基)苯基]甲酮;和
[0353]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(4-氟-1h-吡唑-5-基)苯基]甲酮。
[0354]
在进一步的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0355]
r1选自由以下项组成的组:
[0356]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0357]
(ii)被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、c
1-6-烷氧基、c
1-6-烷基和氨基;和
[0358]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代;
[0359]
r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代;
[0360]
l选自由以下项组成的组:共价键和-ch=ch-;
[0361]
a选自由以下项组成的组:c
6-c
14-芳基、5元至14元杂芳基和5元至14元杂环基;且
[0362]
n为1或2。
[0363]
在进一步的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0364]
r1选自由以下项组成的组:
[0365]
(i)被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0366]
(ii)被1-2个独立地选自由以下项组成的组的取代基取代的5元至6元杂芳基:卤素、c
1-6-烷氧基、c
1-6-烷基和氨基;和
[0367]
(iii)任选地被1-3个独立地选自由以下项组成的组的取代基取代的5元至14元杂环基:卤素、c
1-6-烷基和氧代;
[0368]
r4选自由以下项组成的组:氢、卤素、c
1-6-烷基、c
1-6-烷氧基羰基、c
1-6-烷氧基羰基-nh-、羟基和氧代;
[0369]
l选自由以下项组成的组:共价键和-ch=ch-;并且
[0370]
a选自由以下项组成的组:c
6-c
14-芳基、5元至14元杂芳基和5元至14元杂环基。
[0371]
在优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0372]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0373]
r4选自由以下项组成的组:氢、卤素和羟基;
[0374]
l为共价键;
[0375]
a选自由以下项组成的组:5元至14元杂芳基和5元至14元杂环基;且
[0376]
n为1或2。
[0377]
在优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其
中
[0378]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的c
6-c
14-芳基:c
1-6-烷氧基、卤素和基团
[0379]
r4选自由以下项组成的组:氢、卤素和羟基;
[0380]
l为共价键;并且
[0381]
a选自由以下项组成的组:5元至14元杂芳基和5元至14元杂环基。
[0382]
在特别优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0383]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0384]
r4选自由以下项组成的组:氢、氟和羟基;
[0385]
l为共价键;
[0386]
a选自由以下项组成的组:吡唑基和氮杂环丁烷基;并且
[0387]
n为1或2。
[0388]
在特别优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0389]
r1为被1-2个独立地选自由以下项组成的组的取代基取代的苯基:氯、氟、甲氧基和基团
[0390]
r4选自由以下项组成的组:氢、氟和羟基;
[0391]
l为共价键;并且
[0392]
a选自由以下项组成的组:吡唑基和氮杂环丁烷基。
[0393]
在一个实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0394]
r2选自由以下项组成的组:
[0395]
(i)任选地被1-3个独立地选自卤素的取代基取代的c
1-6-烷基;
[0396]
(ii)c
3-14-环烷基;
[0397]
(iii)被1-2个独立地选自卤素的取代基取代的c
6-c
14-芳基;和
[0398]
(iv)被卤代-c
1-6-烷基取代的5元至14元杂芳基;和
[0399]
r3为氢或羟基。
[0400]
在优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0401]
r2选自由以下项组成的组:
[0402]
(i)卤代-c
6-c
14-芳基;和
[0403]
(ii)被卤代-c
1-6-烷基取代的5元至14元杂芳基;和
[0404]
r3是羟基。
[0405]
在特别优选的实施例中,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其中
[0406]
r2选自由以下项组成的组:
[0407]
(i)氯苯基;和
[0408]
(ii)被cf3取代的吡啶基;且
[0409]
r3是羟基。
[0410]
在一个实施例中,提供了如本文所述的式(i)化合物,其中式(i)化合物为式(ii)化合物:
[0411][0412]
或其药用盐,其中:
[0413]
(a)b是苯基;
[0414]
r2是被一个或多个卤素原子取代的苯基;
[0415]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;
[0416]r3a
为氢或卤素;
[0417]r4a
选自由以下项组成的组:
[0418]
(i)任选地被选自由以下项组成的组的取代基取代的杂环基:羟基、氧代、烷氧基羰基和羟基环烷基;和
[0419]
(ii)杂芳基;并且
[0420]r5a
为氢;或
[0421]
(b)b是苯基;
[0422]
r2选自由以下项组成的组:
[0423]
(i)任选地被1-3个选自由以下项组成的组的取代基取代的杂环基:卤素、烷基和卤代烷基;
[0424]
(ii)任选地被1-3个选自由以下项组成的组的取代基取代的杂芳基:卤素、烷基和卤代烷基;和
[0425]
(iii)任选地被1-3个选自由以下项组成的组的取代基取代的环烷基:卤素、烷基和卤代烷基;
[0426]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;并且
[0427]r3a
、r
4a
和r
5a
独立地选自氢、卤素、烷氧基和杂芳基;或
[0428]
(c)b是苯基;
[0429]
r2是其中x1和x2各自独立地是卤素;
[0430]
r3是羟基;并且
[0431]r3a
、r
4a
、r
5a
独立地选自氢、卤素、氨基、烷基和烷氧基;
[0432]
(d) b是杂芳基或杂环基;
[0433]
r2是被一个或多个卤素原子取代的苯基;
[0434]
r3是羟基;并且
[0435]r3a
、r
4a
和r
5a
独立地选自氢、卤素、烷基、烷氧基、氨基和氧代;或者
[0436]
(e)b是苯基;
[0437]
r2是烷基或卤代烷基;
[0438]
r3是羟基;并且
[0439]r3a
、r
4a
和r
5a
独立地选自氢、卤素和烷氧基;
[0440]
其条件为所述式(i)化合物不是:
[0441][0442]
在一个实施例中,提供了如本文所述的式(i)化合物,其中式(i)化合物为式(ii)化合物:
[0443][0444]
或其药用盐,其中:
[0445]
(a) b是苯基;
[0446]
r2是被一个或多个卤素原子取代的苯基;
[0447]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;
[0448]r3a
为氢或卤素;
[0449]r4a
选自由以下项组成的组:
[0450]
(i)任选地被选自由以下项组成的组的取代基取代的杂环基:羟基、氧代、烷氧基羰基和羟基环烷基;和
[0451]
(ii)杂芳基;并且
[0452]r5a
为氢;或
[0453]
(b)b是苯基;
[0454]
r2选自由以下项组成的组:
[0455]
(i)任选地被1-3个选自由以下项组成的组的取代基取代的杂环基:卤素、烷基和卤代烷基;
[0456]
(ii)任选地被1-3个选自由以下项组成的组的取代基取代的杂芳基:卤素、烷基和卤代烷基;和
[0457]
(iii)任选地被1-3个选自由以下项组成的组的取代基取代的环烷基:卤素、烷基和卤代烷基;
[0458]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;并且
[0459]r3a
、r
4a
和r
5a
独立地选自氢、卤素、烷氧基和杂芳基;或
[0460]
(c)b是苯基;
[0461]
r2是其中x1和x2各自独立地是卤素;
[0462]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;并且
[0463]r3a
、r
4a
、r
5a
独立地选自氢、卤素、氨基、烷基和烷氧基;
[0464]
(d)b是杂芳基或杂环基;
[0465]
r2是被一个或多个卤素原子取代的苯基;
[0466]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;并且
[0467]r3a
、r
4a
和r
5a
独立地选自氢、卤素、烷基、烷氧基、氨基和氧代;或者
[0468]
(e)b是苯基;
[0469]
r2是烷基或卤代烷基;
[0470]
r3选自由以下项组成的组:氢、卤素、烷氧基、环烷基氧基和羟基;并且
[0471]r3a
、r
4a
和r
5a
独立地选自氢、卤素和烷氧基;
[0472]
其条件为所述式(i)化合物不是:
[0473]
[0474]
[0475][0476]
在优选的实施例中,本发明提供了如本文所述的式(i)化合物,其中所述式(i)化合物具有式(ia)和(ib)
[0477][0478]
在一个实施例中,本发明提供了如本文所述的式(i)化合物,其中所述式(i)化合物具有式(ic)和(id)
[0479][0480]
在一个特定实施例中,本发明提供了如本文所述的式(i)化合物的药用盐,尤其是盐酸盐。在另一个特定实施例中,本发明提供了如本文所述的式(i)化合物。
[0481]
在一些实施例中,式(i)的化合物通过其中一个或多个原子被具有不同原子质量或质量数的原子代替而被同位素标记。此类同位素标记(即,放射性标记)的式(i)的化合物被认为在本公开的范围内。可以掺入式(i)的化合物中的同位素的实例分别包括氢、碳、氮、氧、磷、硫、氟、氯和碘的同位素,诸如但不限于2h、3h、
11
c、
13
c、
14
c、
13
n、
15
n、
15
o、
17
o、
18
o、
31
p、
32
p、
35
s、
18
f、
36
cl、
123
i和
125
i。某些同位素标记的式(i)的化合物(例如,包含放射性同位素的那些)可用于药物和/或基体组织分布研究。放射性同位素氚(即3h)和碳-14(即
14
c)对此特别有用,因为它们容易掺入并且检测手段是现成的。例如,式(i)的化合物可以富含1、2、5、10、25、50、75、90、95或99%的给定同位素。
[0482]
用较重的同位素诸如氘(即,2h)取代可以提供由于代谢稳定性更高(例如,体内半衰期增加或剂量减少要求)而带来的某些治疗优势。
[0483]
用正电子发射同位素(诸如
11
c、
18
f、
15
o和
13
n)取代可以用于检查底物受体占用的正电子发射断层扫描(pet)研究。同位素标记的式(i)的化合物通常可以通过本领域技术人员已知的常规技术或通过类似于如下所陈述的实施例中描述的那些过程使用适当的同位素标记的试剂代替之前使用的非标记的试剂来制备。
[0484]
制造过程
[0485]
本发明的式(i)化合物的制备可按照顺序或并发合成路线进行。本发明的合成如以下总体方案所示。执行反应和纯化所得产物所需的技能对于本领域的技术人员是已知的。除非指明是相反情况,否则以下方法说明中所用的取代基和指数具有本文所提供的含
义。
[0486]
如果起始物质、中间体或式(i)化合物之一含有一种或多种在一个或多个反应步骤的反应条件下不稳定或具有反应性的官能团,则可以在关键步骤之前应用本领域中众所周知的方法引入适当的保护基(如以下文献所述:t.w.greene和p.g.m.wutts,“protective groups in organic chemistry”,第5版,2014年,john wiley&sons,n.y.)。此类保护基可在合成的后期使用文献中所述的标准方法去除。
[0487]
如果起始物质或中间体含有立体异构中心,则可能获得呈非对映异构体或对映异构体的混合物形式的式(i)的化合物,其可以通过本领域中众所周知的方法(例如,手性hplc、手性sfc或手性结晶)进行分离。外消旋化合物可例如通过非对映体盐分离为相应的对应体,其通过用光学纯的酸进行结晶,或通过使用手性吸附剂或手性洗脱剂的特定色谱法分离对映体。同样可分离含有立体异构中心的起始物质和中间体,以提供非对映异构体/对映异构体富集的起始物质和中间体。在式(i)的化合物的合成中使用此类非对映异构体/对映异构体富集的起始物质和中间体通常导致相应的非对映异构体/对映异构体富集的式(i)的化合物。
[0488]
本领域的技术人员将认识到,在式(i)化合物的合成中(如果不希望如此)将应用“正交保护基策略”,其允许每次裂解多个保护基而不影响分子中的其他保护基。正交保护的原理是本领域中众所周知的,并且也已经见诸文献报道(例如,barany和r.b.merrifield,j.am.chem.soc.1977,99,7363;h.waldmann等人,angew.chem.int.ed.engl.1996,35,2056)。
[0489]
本领域的技术人员将认识到,反应顺序可根据中间体的反应性和性质而变化。
[0490]
更详细地讲,式(i)的化合物可通过下文所述的方法、实例中所述的方法或类似的方法进行生产。各个反应步骤的适当反应条件是本领域技术人员已知的。同样,有关文献中报道的影响所述反应的反应条件,参见例如:comprehensive organic transformations:a guide to functionalgroup preparations,第2版,richard c.larock,john wiley&sons,new york,ny,1999。在存在或不存在溶剂的情况下进行反应都很方便。对所用溶剂的性质没有特别的限制,只要它对反应或所涉及的试剂没有不利影响并且至少在一定程度上可以溶解试剂即可。所描述的反应可以在很宽的温度范围内发生,并且精确的反应温度对于本发明不是关键的。可以方便地在-78℃至回流的温度范围内执行上述反应。反应所需的时间还可在很大范围内变化,这取决于许多因素,特别是反应温度和试剂的性质。但是,通常需要0.5小时至几天的时间以得到所述的中间体和化合物。反应顺序不限于方案中显示的顺序,但是,根据起始物质及其相应的反应性不同,可自由改变反应步骤的顺序。
[0491]
如果起始原料或中间体无法商购获得,或者其合成未见诸文献报道,则可以采用类似于接近的类似物的现有制备方法或按照实验部分的概述进行制备。
[0492]
式(i)化合物(其中r1、r2和r3如本文所定义,具体地其中r3是羟基、烷氧基或卤素,更具体地是羟基、甲氧基或f)可以根据方案1所概述的一般程序合成。
[0493][0494]
方案1
[0495]
因此,用合适的羧酸15使用偶联试剂(例如dcc、hatu、edci、hobt或tbtu,优选t3p)和碱(如huenig碱、三乙胺或dmap)在合适的溶剂(例如n,n-二甲基甲酰胺、dma、dcm或二噁烷),优选地在0℃和50℃之间酰化pmb保护的仲胺6(可通过例如方案3所概述的一般程序获得的)以提供相应的中间体8(方案1,步骤a)。使用酸性条件,例如用纯acoh、tfoh、msoh、tsoh、或优选tfa处理,在溶剂(如甲苯或dcm)中,任选地在苯甲醚或1,3二甲氧基苯存在下,优选在dcm中且在室温至反应混合物的沸点的温度范围内(优选在室温下)去除pmb保护基团给出酮化合物9(参见例如中间体i-5,步骤b)。用苯基或烷基grignard试剂或用三甲基(三氟甲基)硅烷和tbaf试剂在溶剂(如二乙醚或thf,优选thf)中最终在lewis酸(例如licl、mgcl2、alcl3,优选cecl3)存在下且在-78℃至25℃的温度范围内(优选在0℃下)处理酮中间体9提供相应的式(i)化合物(其中r1和r2如本文所定义,且其中r3是羟基)(步骤c)。可替代地,用n-buli的己烷溶液在溶剂(如二乙醚、thf、甲苯或其混合物,优选甲苯)中且在-78℃至25℃的温度范围内(优选在-78℃下)在酮中间体9存在下处理合适的杂芳基溴化物试剂(例如2-溴-5-(三氟甲基)吡啶)提供相应的式(i)化合物(其中r1和r2如本文所定义且其中r3是羟基)(步骤c)。(i)的叔醇部分可以使用本领域已知的条件(例如在第一阶段通过使(i)与hcl、hbr、hi、pocl3、socl2或pbr3反应或与合适的氨基硫化物试剂例如dast反应或通过首先将(i)的醇转化至磺酸酯(例如甲磺酸酯),随后使所述磺酸酯与例如naf反应)进一步转化为卤素,优选转化为f,以产生式(i)化合物(其中r1和r2如本文所定义且其中r3是卤素)(方案1,步骤d)。另外,式(i)化合物(其中r3是一种卤素)可以通过本领域已知的方法转化为式(i)化合物(其中r3是另一种卤素)。(i)的叔醇部分可以通过用适合的碱(例如nah、kh、nahmds、lihmds或lda,优选用nah)在溶剂(如dmf、thf、二噁烷、或其混合物,优选dmf)中,且在-78℃至室温的温度范围内(优选在0℃下)处理,随后添加亲电子试剂(例如烷基或环烷基卤化物(例如mei、eti、ipri或cypri)进一步转化为烷氧基(优选转化为甲氧基)以给出相应式(i)化合物(其中r1和r2如本文所定义且其中r3是甲氧基)(方案1,步骤e)。
[0496]
可替代地,式(i)化合物(其中r1、r2和r3如本文所定义,具体地其中r3是羟基、卤素
或烷氧基,更具体地是羟基、f或甲氧基)可以根据方案2a所概述的一般程序合成。
[0497][0498]
方案2a
[0499]
因此,用苯基或烷基grignard试剂或用三甲基(三氟甲基)硅烷和tbaf试剂在溶剂(如二乙醚或thf,优选thf)中最终在lewis酸(例如licl、mgcl2、alcl3,优选cecl3)存在下且在-78℃至25℃的温度范围内(优选在0℃下)处理受保护酮中间体10(可通过例如方案3所概述的一般程序获得的)(其中pg是保护基团(例如boc(参见例如中间体i-1)))提供相应的中间体11(其中r1和r2如本文所定义且其中r3是羟基)(方案2a,步骤a)。可替代地,用n-buli的己烷溶液在溶剂(如二乙醚、thf、甲苯或其混合物,优选甲苯)中且在-78℃至25℃的温度范围内(优选在-78℃下)在受保护酮中间体10存在下处理合适的杂芳基溴化物试剂(例如2-溴-5-(三氟甲基)吡啶(参见例如中间体i-4a)或5-溴-2-(三氟甲基)吡啶)提供相应的中间体11(其中r1和r2如本文所定义且其中r3是羟基)(方案2a,步骤a)。在合适的条件下(例如使用酸性条件,例如用hcl处理)在溶剂(如etoac或meoh)中或用tfa的dcm溶液处理,优选在室温左右去除boc保护基团提供胺中间体12(步骤b,参见例如中间体i-2a)。随后,用羧酸化合物15(其中r1如本文所定义)通过施用偶联试剂(例如dcc、edci、hobt、tbtu、t3p,优选hatu)和碱(例如huenig碱、三乙胺或dmap)在合适的溶剂(如n,n-二甲基甲酰胺、dma、dcm或二噁烷)中,优选在0℃至室温之间完成酰胺偶联反应给出式(i)化合物(方案2a,步骤c)。(i)的叔醇部分可以使用本领域已知的条件(例如在第一阶段通过使(i)与hcl、hbr、hi、pocl3、socl2或pbr3反应或与合适的氨基硫化物试剂例如dast反应或通过首先将(i)的醇转化至磺酸酯(例如甲磺酸酯),随后使所述磺酸酯与例如naf反应)进一步转化为卤素,优选转化为f,以产生式(i)化合物(其中r1和r2如本文所定义且其中r3是卤素)(方案2a,步骤d)。另外,式(i)化合物(其中r3是一种卤素)可以通过本领域已知的方法转化为式(i)化合物(其中r3是另一种卤素)。(i)的叔醇部分可以通过用适合的碱(例如nah、kh、nahmds、lihmds
或lda,优选用nah)在溶剂(如dmf、thf、二噁烷、或其混合物,优选dmf)中,且在-78℃至室温的温度范围内(优选在0℃下)处理,随后添加亲电子试剂(例如烷基或环烷基卤化物(例如mei)进一步转化为烷氧基(优选转化为甲氧基)以给出相应式(i)化合物(其中r1和r2如本文所定义且其中r3是甲氧基)(方案2a,步骤e)。
[0500]
可替代地,式(i)化合物(其中r1、r2和r3如本文所定义,具体地其中r3是氢)可以根据方案2b所概述的一般程序合成。
[0501][0502]
方案2b
[0503]
用苯基或烷基grignard试剂在溶剂(如二乙醚或thf,优选thf)中最终在lewis酸(例如licl、mgcl2、alcl3,优选cecl3)存在下且在-78℃至25℃的温度范围内(优选在0℃下)处理保护的酮中间体10(可通过例如方案3所概述的一般程序获得的)(其中pg是保护基团(例如boc(参见例如中间体i-1)))提供相应的中间体11(其中r1和r2如本文所定义且其中r3是羟基)(方案2b,步骤a)。可替代地,用n-buli的己烷溶液在溶剂(如二乙醚、thf、甲苯或其混合物,优选甲苯)中且在-78℃至25℃的温度范围内(优选在-78℃下)在保护酮中间体10存在下处理合适的杂芳基溴化物试剂(例如2-溴-5-(三氟甲基)吡啶(参见例如中间体i-4a))提供相应的中间体11(其中r1和r2如本文所定义且其中r3是羟基)(方案2b,步骤a)。
[0504]
在酸(例如hcl、tsoh或msoh,优选msoh存在下)在溶剂(如dcm、meoh、etoh、甲苯或其混合物,优选在dcm中)且在0℃至溶剂的沸点的温度范围内(优选在室温下),伴随保护基团pg的裂解随后羟基中间体的脱水反应给出烯胺中间体13(方案2b,步骤b)。随后,使用过渡金属催化剂(例如pto2或pd/c)在mgo(优选pto2)存在下在溶剂(如thf、meoh、etoh、etoac,优选thf)中在acoh存在下在室温左右且在4bar压力的氢下进行烯烃的异种催化氢化作用给出胺中间体14(方案2b,步骤c,参见例如中间体i-6)。最后,用羧酸化合物15(其中r1如本文所定义)通过施用偶联试剂(例如dcc、edci、hobt、tbtu、t3p,优选hatu)和碱(例如huenig碱、三乙胺或dmap)在合适的溶剂(如n,n-二甲基甲酰胺、dma、dcm或二噁烷)中,优选在0℃至室温之间完成酰胺偶联反应给出式(i)化合物(步骤d)。
[0505]
中间体6和10可以通过多种条件(这可以通过方案3中所概述的一般程序所示例的)合成。
[0506][0507]
方案3
[0508]
开始于可商购的3-溴-6-吡啶甲腈(1),可以使用4-甲氧基苄醇在合适的碱(例如naoh、koh、kh,优选用nah)存在下在溶剂(如dmf、thf、二噁烷、或其混合物)中,优选在dmf和thf的混合物中且在0℃至室温的温度范围内进行亲核芳香族的取代反应以给出相应的pmb保护的化合物2(方案3,步骤a)。使用合适的还原剂(例如硼烷、氢化硼锂或氢化铝锂)在溶剂(如乙醚、dme、thf或其混合物)中且在0℃至溶剂的沸点的温度范围内,或优选使用催化氢化条件(例如raney镍)在溶剂(如meoh)中在氢氧化铵存在下在50℃左右且在3.5bar的氢气氛下完成腈基的还原以给出相应的胺3(方案3,步骤b)。随后,用溴乙酸使用合适的偶联剂(例如dcc、dci或优选edci)在溶剂(如dcm、thf、dmf、dce或ch3cn,优选dcm)中且在0℃至溶剂的沸点的温度范围内(优选在室温下)的酰胺偶联反应给出酰胺化合物4a(方案3,步骤c)。随后在溶剂(如etoh、meoh,优选ch3cn)中且优选50℃左右加热中间体4a给出吡啶中间体4b(方案3,步骤d)。随后用合适的还原剂(例如硼氢化钠)在溶剂(如meoh)下,优选在约室温下处理给出内酰胺化合物5(方案3,步骤d’)。使用合适的还原剂(例如硼烷、氢化硼锂或优选氢化铝锂)在溶剂(如乙醚、dme或其混合物,优选thf)中且在0℃至反应混合物的沸点的温度范围内(优选在回流下)进行酰胺的还原给出相应的胺化合物6(方案3,步骤e)。随后使用酸性条件,例如用纯acoh、tfoh、msoh、tsoh、或优选tfa处理,在溶剂(如甲苯或dcm)中,任选地在苯甲醚或1,3二甲氧基苯存在下,优选在dcm中且在室温至反应混合物的沸点的温度范围内(优选在室温下)去除pmb保护基团给出酮化合物7(方案3,步骤f)。最后,用合适的保护基团(方案3,步骤g)保护7中的仲胺以提供中间体10。因此,例如,任选地在碱存在下(例如dmap、tea、nahco3或优选na2co3)在合适的溶剂中(如ch3cn、dcm、二噁烷或thf,优选在ch3cn中)且在0℃至室温的温度范围内(优选在室温下)用二碳酸二叔丁酯处理产生boc保护的酮中间体i-1。
[0509]
在一个实施例中,羧酸化合物15是a、b或c型的中间体。a、b和c型的中间体可以如例如在方案4中所概述的合成程序所示例的制备。
[0510][0511]
方案4
[0512]
酯化合物40(其中b是芳基,具体地是苯基,x是卤素,优选溴或三氟甲磺酸酯,且ry是卤素或烷氧基)通过应用交叉偶联反应(例如buchwald-hartwig交叉偶联反应)可以转化为中间体41(其中r
x
是n-结合的杂环)。用合适的胺(例如氮杂环丁烷-3-醇或吗啉),使用合适的催化体系(例如pd2(dba)3或pd(oac)2和xantphos、davephos或binap)在碱(例如cs2co3或k3po4)存在下在适合的溶剂(例如二噁烷或甲苯)中在室温至溶剂的沸点的温度范围内,任选地应用微波加热,处理中间体40产生酯化合物41(方案4,步骤a)。
[0513]
可替代地,酯化合物40(其中x、b和ry如上文所定义)通过应用suzuki偶联反应可以转化为中间体51(其中r
x
是c-结合的杂环)。用合适的硼酸或酯(例如杂环基硼酸或酯,例如3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯或4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯),使用合适的催化剂(例如双(三苯基膦)氯化钯(ii)、二氯[1,1`-双(二苯基膦基)-二茂铁]钯(ii)二氯甲烷加合物、四(三苯基膦)钯(0)或乙酸钯(ii)与三苯基膦)在适合的溶剂(例如二噁烷、dme、水、甲苯、dmf或其混合物)和合适的碱(例如na2co3、nahco3、kf、k2co3或net3)中在室温至反应混合物的沸点的温度下处理中间体40产生酯化合物51(方案4,步骤a)。
[0514]
酯化合物50(其中b是芳基,具体地是苯基,x是硼酸或硼酸酯且ry是烷氧基或卤素)通过应用suzuki偶联反应可以转化为中间体51(其中r
x
是c-结合的杂环)。用合适的有机卤化物或三氟甲磺酸酯(例如用溴取代的杂芳基,例如4-溴-3-氟-1h-吡唑)使用合适的催化剂(例如双(二-叔丁基(4-二甲基氨基苯基)膦)二氯钯(ii)、双(三苯基膦)氯化钯(ii)、二氯[1,1`-双(二苯基膦基)-二茂铁]钯(ii)二氯甲烷加合物、四(三苯基膦)钯(0)或乙酸钯(ii)与三苯基膦)在适合的溶剂(例如二噁烷、dme、水、甲苯、dmf或其混合物)和合适的碱(例如na2co3、nahco3、kf、k2co3或net3)在室温至反应混合物的沸点的温度下任选地应用微波加热处理中间体50产生酯化合物51(方案4,步骤a)。
[0515]
酯化合物60(其中b是芳基,具体为苯基,x是选自碘、溴和氯的卤素,优选碘且ry是c
1-6-烷氧基或卤素)通过应用交叉偶联反应(例如ullmann交叉偶联)可以转化为中间体61(其中r
x
是酰胺结合杂环)。用带有酰胺基序的合适的结构单元(例如环脲或氨基甲酸酯(例如咪唑烷-2-酮或噁唑烷-2-酮))使用合适的催化体系(例如碘化铜(i)和n,n
′‑
二甲基乙烷-1,2-二胺)在碱存在下(例如cs2co3或k2co3)在适合的溶剂(例如二噁烷或乙腈)在室温至溶剂的沸点的温度范围内处理中间体60产生酯化合物61(方案4,步骤a)。
[0516]
最后,用合适的碱(例如水性氢氧化锂、氢氧化钠或氢氧化钾,优选氢氧化锂),在溶剂(如meoh、etoh、thf或其混合物)中且在0℃至反应混合物的沸点的温度范围内(优选在室温左右)进行中间体41,51或61的酯部分的碱水解给出a、b或c型的中间体(方案4,步骤b)。
[0517]
在一个方面,本发明提供了一种生产如本文所述的方案中任一者所述的式(i)化合物的方法。
[0518]
在另一方面,本发明提供了一种生产如本文所述的式(i)化合物的方法,该方法包括:
[0519]
(a)使化合物9(其中r1如所本文定义)
[0520][0521]
与有机锂试剂r2li或有机镁试剂r2mgx(其中x是卤素)反应以形成式(i)的叔醇(其中r2如本文所定义且r3是羟基);且任选地
[0522]
(b)通过用合适的碱如nah、kh、nahmds、lihmds或lda,优选用nah处理,然后添加亲电子试剂,例如,烷基-或环烷基卤化物,例如mei、eti、ipri或cypri,将醇r3烷基化,以产生其中r3是烷氧基或环烷氧基的相应的式(i)化合物;或者
[0523]
(c)通过使其中r3是羟基的式(i)化合物与(i)酸(例如hcl、hbr、hi)、pocl3、socl2或pbr3)反应;或(ii)与合适的氨基硫试剂(例如dast)反应;或(iii)与磺酰化试剂(例如甲磺酰氯)反应,然后使中间体磺酸酯与卤化物(例如naf)反应,从而将醇r3转化为卤素以产生其中r3是卤素的相应的式(i)化合物。
[0524]
在另一方面,本发明提供了一种生产如本文所述的式(i)化合物的方法,该方法包括:
[0525]
(a)使胺12或14,其中r2如本文定义且r3为羟基(12)或氢(14)
[0526][0527]
与羧酸15,其中r1如本文定义
[0528][0529]
在偶联试剂(例如hatu、dcc、edci、hobt、tbtu或t3p)和碱(例如huenig碱、三乙胺或dmap)的存在下反应以提供其中r3是羟基或氢的所述式(i)化合物;并且任选地,前提是r3是羟基;
[0530]
(b)通过用合适的碱如nah、kh、nahmds、lihmds或lda,优选用nah处理,然后添加亲电子试剂,例如,烷基-或环烷基卤化物,例如mei、eti、ipti或cypri,将醇r3烷基化,以产生其中r3是烷氧基或环烷氧基的相应的式(i)化合物;或者
[0531]
(c)通过使其中r3是羟基的式(i)化合物与(i)酸(例如hcl、hbr、hi)、pocl3、socl2或pbr3)反应;或(ii)与合适的氨基硫试剂(例如dast)反应;或(iii)与磺酰化试剂(例如甲磺酰氯)反应,然后使中间体磺酸酯与卤化物(例如naf)反应,从而将醇r3转化为卤素以产生其中r3是卤素的相应的式(i)化合物。
[0532]
在又进一步的方面,本发明提供了一种如本文所述的式(i)化合物,该化合物根据本文所述的方法中的任一方法进行生产。
[0533]
magl抑制活性
[0534]
本发明的化合物为magl抑制剂。因此,在一个方面,本发明提供了如本文所述的式(i)化合物用于抑制哺乳动物的magl的用途。
[0535]
在另一方面,本发明提供了如本文所述的式(i)化合物用于抑制哺乳动物的magl
的方法。
[0536]
在另一方面,本发明提供了如本文所述的式(i)化合物在制备用于抑制哺乳动物的magl药物中的用途。
[0537]
在另一方面,本发明提供了抑制哺乳动物的magl的方法,该方法包括向哺乳动物施用治疗有效量的如本文所述的式(i)化合物。
[0538]
通过在天然底物2-花生四烯酰甘油(2-ag)水解得到花生四烯酸后测定酶促活性,分析化合物对magl的抑制活性,然后可进行质谱分析。该测定在在后文缩写为“2-ag测定”。
[0539]
2-ag测定在384孔测定板(pp,greiner目录号784201)中进行,总体积为20μl。在聚丙烯板中,利用3倍稀释步骤在100%dmso(vwr chemicals 23500.297)中制备化合物稀释液,以使测定的最终浓度范围为12.5μm至0.8pm。将0.25μl化合物稀释液(100%dmso)加入9μl magl的测定缓冲液(50mm tris(gibco,15567-027)、1mm edta(fluka,03690-100ml)和0.01%(v/v)tween)中。振摇后,将板在室温下孵育15min。加入10μl 2-花生四烯酰甘油的测定缓冲液溶液,以开始反应。该测定中的最终浓度为50pm magl和8μm 2-花生四烯酰甘油。振摇并在rt孵育30min后,加入40μl含4μm d8-花生四烯酸的acn淬灭反应。利用在线spe系统(agilent rapidfire)与三重四极杆质谱仪(agilent 6460)联用系统跟踪花生四烯酸的含量。在acn/水液体设置中,使用c18 spe小柱(g9205a)。质谱仪在负电喷雾模式下操作,花生四烯酸的质量离子对为303.1
→
259.1,d8-花生四烯酸的质量离子对为311.1
→
267.0。基于[花生四烯酸/d8-花生四烯酸]的强度比计算化合物的活性。
[0540]
表1
[0541]
[0542]
[0543]
[0544]
[0545]
[0546]
[0547]
[0548]
[0549]
[0550]
[0551]
[0552]
[0553][0554]
在一个方面,本发明提供了如本文所述的式(i)化合物及其药用盐或酯,其中所述式(i)化合物及其药用盐或酯具有低于25μm、优选低于10μm、更优选地低于5μm的magl抑制ic
50
,该ic
50
值在本文所述的magl测定中测得。
[0555]
在一个实施例中,如本文所述的式(i)化合物及其药用盐或酯的ic
50
(magl抑制)值介于0.000001μm和25μm之间,特定化合物具有介于0.000005μm和10μm之间的ic
50
值,更特定的化合物具有介于0.00005μm和5μm之间的ic50值,该ic
50
值在本文所述的magl测定中测得。
[0556]
使用本发明的化合物
[0557]
在一个方面,本发明提供了一种如本文所述的式(i)化合物或其药用盐,其用作治疗活性物质。
[0558]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的用途。
[0559]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的神经炎症和/或神经退行性疾病的用途。
[0560]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的神经退行性疾病的用途。
[0561]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的癌症的用途。
[0562]
在一方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的用途。
[0563]
在优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病和/或帕金森氏病的用途。
[0564]
在特别优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐用于治疗或预防哺乳动物的多发性硬化症的用途。
[0565]
在一方面,本发明提供了用于治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的如本文所述的式(i)化合物或其药用盐。
[0566]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的神经炎症和/或神经退行性疾病。
[0567]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的癌症。
[0568]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐,用于治疗或预防哺乳动物的神经退行性疾病。
[0569]
在一方面,本发明提供了用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的如本文所述的式(i)化合物或其药用盐。
[0570]
在优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐用于在治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病和/或帕金森氏病中使用。
[0571]
在特别优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐用于在治疗或预防哺乳动物的多发性硬化症中使用。
[0572]
在一个方面,本发明提供了如本文所述的式(i)化合物或其药用盐用于制备治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的药物的用途。
[0573]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐在制备治疗或预防哺乳动物的神经炎症和/或神经退行性疾病的药物中的用途。
[0574]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的神经退行性疾病的药物中的用途。
[0575]
在一个实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的癌症的药物中的用途。
[0576]
在另一方面,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症、肝细胞癌、结肠癌、卵巢癌、神经性疼痛、化疗诱导的神经病变、急性疼痛、慢性疼痛和/或与疼痛相关的痉挛的药物中的用途。
[0577]
在优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病和/或帕金森氏病的药物中的用途。
[0578]
在特别优选的实施例中,本发明提供了如本文所述的式(i)化合物或其药用盐在制备用于治疗或预防哺乳动物的多发性硬化症的药物中的用途。
[0579]
在一个方面,本发明提供了一种治疗或预防哺乳动物的神经炎症、神经退行性疾病、疼痛、癌症和/或精神障碍的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0580]
在一个实施例中,本发明提供了一种用于治疗或预防哺乳动物的神经炎症和/或神经退行性疾病的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0581]
在一个实施例中,本发明提供了一种用于治疗或预防哺乳动物的神经退行性疾病的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0582]
在一个方面,本发明提供了一种用于治疗或预防哺乳动物的多发性硬化症、阿尔
茨海默氏病、帕金森氏病、肌萎缩性脊髓侧索硬化症、创伤性脑损伤、神经毒性、中风、癫痫、焦虑、偏头痛、抑郁症和/或疼痛的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0583]
在优选的实施例中,本发明提供了一种用于治疗或预防哺乳动物的多发性硬化症、阿尔茨海默氏病和/或帕金森氏病的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0584]
在特别优选的实施例中,本发明提供了一种用于治疗或预防哺乳动物的多发性硬化症的方法,该方法包括向哺乳动物施用有效量的如本文所述的式(i)化合物或其药用盐。
[0585]
药物组合物和施用
[0586]
在一个方面,本发明提供了一种药物组合物,该药物组合物包含如本文所述的式(i)化合物和治疗惰性载体。
[0587]
式(i)化合物及其药用盐和酯可用作药物(例如,呈药物制剂的形式)。药物制剂可以内部施用,诸如口服(例如,以片剂、包衣片剂、糖锭剂、硬明胶胶囊和软明胶胶囊、溶液、乳液或混悬剂的形式)、鼻内(例如,以鼻用喷雾的形式)或直肠内(例如,以栓剂的形式)。但是,也可通过肠胃外诸如肌内或静脉内(例如以注射液的形式)给药。
[0588]
式(i)化合物及其药用盐和酯可与药学上惰性、无机或有机助剂一起加工制成片剂、包衣片剂、糖衣丸和硬明胶胶囊。例如,可使用乳糖、玉米淀粉或其衍生物(滑石粉、硬脂酸或其盐等)作为片剂、糖衣丸和硬明胶胶囊的此类助剂。
[0589]
用于软明胶胶囊的合适的助剂为例如植物油、蜡、脂肪、半固体物质和液体多元醇等。
[0590]
用于制备溶液和糖浆的合适的助剂为例如水、多元醇、蔗糖、转化糖、葡萄糖等。
[0591]
用于注射液的合适的助剂为例如水、醇、多元醇、甘油、植物油等。
[0592]
用于栓剂的合适的助剂为例如天然或硬化油、蜡、脂肪、半固体或液体多元醇等。
[0593]
此外,药物制剂可以含有防腐剂、增溶剂、增粘物质、稳定剂、润湿剂、乳化剂、甜味剂、着色剂、香料、用于改变渗透压的盐、缓冲剂掩模剂或抗氧化剂。它们还可以含有其他有治疗价值的物质。
[0594]
剂量可以在宽范围内变化,当然将适合每种特定情况下的各种要求。一般来讲,在口服施用的情况下,日剂量为每kg体重约0.1mg至20mg、优选每kg体重约0.5mg至4mg(例如,每人约300mg)(分成优选1-3个单独剂量,这些单独剂量可以例如由相同量组成)应该是合适的。但是,显而易见的是,当显示为标明时,可超过本文中给出的上限。
[0595]
实例
[0596]
通过参考以下实施例将更全面地理解本发明。然而,权利要求不应被解释为限于实施例的范围。
[0597]
在作为对映体的混合物获得制备实施例的情况下,可以通过本文所述的方法或通过本领域技术人员已知的方法(诸如手性色谱(例如,手性sfc)或结晶)分离纯对映体。
[0598]
如果没有另行说明,则在氩气氛下制备所有反应实施例和中间体。
[0599]
缩写
[0600]
acoh=乙酸,aq.=水性,boc=叔丁基氧基羰基,binap=2,2
′‑
双(二苯基膦基)-1,1
′‑
联萘,bnbr=苄基溴,n-buli=正丁基锂,n-buoh=丁醇,cas rn=化学文摘登记号,
1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(0.8g,2.18mmol)的二噁烷(5ml)溶液添加4m hcl的二噁烷(5.45ml,21.8mmol)溶液并将反应混合物在室温下搅拌15小时。将所得的悬浮液用etoac稀释,缓慢倒入冷的饱和na2co3水溶液并用etoac萃取。将合并的有机层用盐水洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物进行手性sfc分离以分别给出(7s,9ar)-7-(4-氯苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-2a,0.195g,32%)和(7r,9as)-7-(4-氯苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-2b,0.190g,31%),它们为橘色半固体;ms(esi):m/z=267.2[m+h]
+
。
[0621]
中间体i-3a和i-3b
[0622]
(7s,9ar)-7-(3-氯-4-氟-苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇和(7r,9as)-7-(3-氯-4-氟-苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0623]
中间体i-3a和i-3b的制备类似于中间体i-2a和i-2b,但在步骤[a]中使用0.5m的3-氯-4-氟苯基溴化镁的thf(cas rn 413589-34-1)溶液以分别给出标题化合物,其为黄色油状物;ms(esi):m/z=285.1[m+h]
+
。
[0624]
中间体i-4a
[0625]
(7r,9ar)-7-[5-(三氟甲基)-2-吡啶基]-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0626]
步骤[a]外消旋-(7r,9ar)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯
[0627]
向冷却至-78℃的2-溴-5-(三氟甲基)吡啶(cas rn 50488-42-1,1g,4.42mmol)的甲苯(14.3ml)溶液中添加1.6m nbuli的己烷(3.04ml,4.87mmol)溶液并将混合物在该温度下搅拌5分钟。然后逐滴添加冷却的7-氧代-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(中间体i-1,1.24g,4.87mmol)的甲苯(14ml)溶液,期间保持-78℃的温度,并将反应混合物搅拌1.5小时。将反应用饱和nh4cl水溶液猝灭并将混合物用etoac萃取。将合并的有机物用水、盐水洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用20%至80%etoac-庚烷梯度洗脱)以给出标题化合物(0.817g,46%),其为浅黄色粘稠油状物;ms(esi):m/z=402.3[m+h]
+
。
[0628]
步骤[b](7s,9as)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯和(7r,9ar)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯
[0629]
将外消旋-(7r,9ar)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯进行手性sfc分离以分别给出(7s,9as)-7-(4-氯苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(0.326g,37%)和(7r,9ar)-7-(4-氯苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(0.252g,31%),其为浅棕色固体;ms(esi):m/z=402.3[m+h]
+
。
[0630]
步骤[c](7r,9ar)-7-[5-(三氟甲基)-2-吡啶基]-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0631]
向在0℃下冷却的(7r,9ar)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(0.25g,0.623mmol)在二噁烷(1.5ml)中的溶液添加4m hcl的二噁烷(1.56ml,6.23mmol)溶液并将反应混合物在室温下搅拌15小时。
将混合物蒸发至干燥以给出粗标题化合物(中间体i-4a,0.23g),其为浅棕色固体,其为盐酸盐;ms(esi):m/z=470.2[m+h]
+
。
[0632]
中间体i-4b
[0633]
(7s,9as)-7-[5-(三氟甲基)-2-吡啶基]-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0634]
的制备类似于中间体i-4a,但在步骤[c]中使用(7s,9as)-7-羟基-7-[5-(三氟甲基)-2-吡啶基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯以给出粗标题化合物,其为浅棕色固体,其为盐酸盐;ms(esi):m/z=470.2[m+h]
+
。
[0635]
中间体i-5
[0636]
2-(2-氯-3-甲氧基苯甲酰)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-7-酮
[0637]
步骤[a](2-氯-3-甲氧基苯基)-[7-[(4-甲氧基苯基)甲氧基]-1,3,4,6,9,9a-六氢吡啶并[1,2-a]吡嗪-2-基]甲酮
[0638]
向在0℃下冷却的2-氯-3-甲氧基苯甲酸(2.94g,15.75mmol)和7-[(4-甲氧基苯基)甲氧基]-2,3,4,6,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪(中间体i-1[e],3.6g,13.12mmol)的dmf(50ml)溶液添加tea(5.6ml,39.36mmol)随后添加t3p(9.06g,19.68mmol),然后将反应混合物加热至50℃持续12小时。将反应物用水(100ml)稀释并用etoac(2x80ml)萃取。将合并的有机层用水(2x50ml)和盐水(50ml)洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用50%至100%etoac-庚烷梯度洗脱)以给出标题化合物(3.9g,67.1%),其为黄色固体;ms(esi):m/z=443.2[m+h]
+
。
[0639]
步骤[b]2-(2-氯-3-甲氧基苯甲酰)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-7-酮
[0640]
向冷却至0℃的(2-氯-3-甲氧基-苯基)-[7-[(4-甲氧基苯基)甲氧基]-1,3,4,6,9,9a-六氢吡啶并[1,2-a]吡嗪-2-基]甲酮(3.9g,8.8mmol)的dcm(50ml)溶液中添加tfa(3.39ml,44mmol),然后将反应混合物在室温下搅拌1小时。将混合物在真空中浓缩,并将残余物溶于etoac,倒入饱和nahco3水溶液(100ml),并将水层用etoac(2x50ml)萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并蒸发。将残余物通过硅胶快速色谱法纯化(用50%至100%etoac-庚烷梯度洗脱)以给出标题化合物(2.1g,73.9%),其为浅黄色泡沫状物。ms(esi):m/z=341.2[m+h2o+h]
+
。
[0641]
中间体i-6
[0642]
(7r,9ar)-7-(4-氯苯基)八氢-1h-吡啶并[1,2-a]吡嗪
[0643]
步骤[a]7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯
[0644]
向在0℃下冷却的7-氧代-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(中间体i-1,1.0g,3.93 mmol)的thf(30ml)溶液中添加4-氯苯基溴化镁(1m在thf中的溶液,7.08ml,7.08mmol)并将反应混合物在室温下搅拌2小时。将混合物倒入饱和的nh4cl水溶液(100ml)中并用etoac(3x 50ml)萃取。将合并的有机相用盐水洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用5%至25%etoac-pe梯度洗脱)以给出标题化合物(0.820g,56.8%),其为浅黄色油状物;ms(esi):m/z=367.1[m+h]
+
。
[0645]
步骤[b]7-(4-氯苯基)-2,3,4,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪
[0646]
向7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(0.820g,2.24mmol)的dcm(25ml)的溶液中添加甲磺酸(5.0ml,164mmol)并将反应混合物在20℃下搅拌18小时。将混合物倒入饱和nahco3水溶液(100ml)并用dcm(3x50ml)萃取。合并的有机相用盐水洗涤,经na2so4干燥,过滤并浓缩在真空中以给出粗标题化合物(0.560g,),其为浅黄色油状物;ms(esi):m/z=249.1[m+h]
+
。
[0647]
步骤[c]外消旋-(7r,9as)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪、(7r,9ar)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪和(7s,9as)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪
[0648]
向7-(4-氯苯基)-2,3,4,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪(0.130g,0.523mmol)的thf(2.5ml)和acoh(0.250ml)溶液中添加pto2(0.025 g,0.523mmol)并将混合物在室温下在4bar的h2压力下搅拌2小时。将混合物过滤,并且将滤液在真空中浓缩。将残余物通过sfc纯化以分别给出外消旋-(7r,9as)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪(峰a,0.020g,14%)、(7r,9ar)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪(峰b,0.018g,11%)和(7s,9as)-7-(4-氯苯基)-2,3,4,6,7,8,9,9a-八氢-1h-吡啶并[1,2-a]吡嗪(峰c,0.015g,9%),它们为灰白色泡沫状物;ms(esi):m/z=251.2[m+h]
+
。
[0649]
中间体i-7
[0650]
[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氯-苯基]硼酸
[0651]
向用冰浴冷却至0℃的(7s,9ar)-7-(4-氯苯基)八氢-2h-吡啶并[1,2-a]吡嗪-7-醇(中间体i-2a,0.05g,0.187mmol)和2-氯-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯甲酸(cas rn 1046153-00-7,0.053g,0.187mmol)的dmf(1.5ml)的溶液中添加h
ü
nig碱(0.082ml,0.469mmol)随后添加hatu(0.086g,0.225mmol)并将反应混合物在室温下搅拌3小时。将混合物浓缩在真空中并将残余物通过反相hplc纯化以给出标题化合物(0.065g,73%),其为无色冻干粉末;ms(esi):m/z=449.3[m+h]+。
[0652]
中间体i-8
[0653]
(2-氯-3-((7r,9ar)-7-羟基-7-(5-(三氟甲基)吡啶-2-基)八氢-2h-吡啶并[1,2-a]吡嗪-2-羰基)苯基)硼酸
[0654]
的制备类似于中间体i-7,但使用(7r,9ar)-7-[5-(三氟甲基)-2-吡啶基]-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-4a)以给出粗标题化合物,其为浅黄色固体;ms(esi):m/z=484.3[m+h]
+
。
[0655]
中间体i-9
[0656]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(5-溴-4-氯吡啶-3-基)甲酮
[0657]
的制备类似于中间体i-7,但使用5-溴-4-氯烟酸(cas rn 1256790-85-8)以给出粗标题化合物,其为浅黄色固体;ms(esi):m/z=486.2[m+h]
+
。
[0658]
中间体i-10a和i-10b
[0659]
(7s,9ar)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇和(7r,9as)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0660]
步骤[a]外消旋-(7r,9as)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯
[0661]
向在-20℃下冷却的7-氧代八氢-2h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(中间体i-1,1.5g,5.9mmol)的me-thf(5ml)溶液逐滴添加0.5m的(3,4-二氟苯基)溴化镁(cas rn 90897-92-0,13ml,6.49mmol)的me-thf溶液,期间保持-20℃的温度。将反应混合物在室温下搅拌4小时。将混合物用etoac稀释,倒入饱和nh4cl(25ml)并用etoac(2
×
50ml)萃取。将有机层合并,用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将残余物通过硅胶快速色谱纯化(用10%至40%etoac的庚烷溶液梯度洗脱)以给出标题化合物(0.833g,38%,1∶3顺式∶反式),其为无色泡沫状物;ms(esi):m/z=385.2[m+h]
+
。
[0662]
步骤[b](7s,9ar)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇和(7r,9as)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇
[0663]
向用冰浴冷却至0℃的7-(3,4-二氟苯基)-7-羟基八氢-2h-吡啶并[1,2-a]吡嗪-2-甲酸叔丁酯(0.83g,2.25mmol)的dcm(2.5ml)溶液中添加tfa(1.04ml,13.5mmol)并将反应混合物在室温下搅拌过夜。将冷却的混合物通过逐滴添加2m naoh水溶液(7.88ml,15.8mmol)碱化并将所得的水相用dcm萃取。将合并的有机相经na2so4干燥,过滤并蒸发至干燥。将该粗物质通过纯化sfc以分别给出顺式产物(峰a)、顺式和反式产物的混合物(0.236g,峰b)和(7r,9as)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-10b,0.160g,峰c)之一。通过sfc二次纯化峰b以给出(7s,9ar)-7-(3,4-二氟苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-10a,0.160g,26%),其为橘色油状物;ms(esi):m/z=285.1[m+h]
+
。
[0664]
中间体i-11
[0665]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(5-溴-4-甲基吡啶-3-基)甲酮
[0666]
的制备类似于中间体i-7,但使用5-溴-4-甲基烟酸(cas rn 677702-58-8)以给出粗标题化合物,其为无色固体;ms(esi):m/z=464.2[m+h]
+
。
[0667]
中间体a-1
[0668]
2-氯-3-(3-羟基氮杂环丁烷-1-基)苯甲酸锂
[0669]
步骤[a]2-氯-3-(3-羟基氮杂环丁烷-1-基)苯甲酸甲酯
[0670]
在密封管中,将3-溴-2-氯苯甲酸甲酯(cas rn 871224-19-0,0.1g,0.401mmol)、碳酸铯(0.261g,0.802mmol)、pd2(dba)3(0.037g,0.040mmol)和xantphos(23.2mg,40.1μmol,eq∶0.1)混合在二噁烷(1ml)中。将混合物用氩气脱气,然后添加氮杂环丁烷-3-醇(cas rn 45347-82-8,0.059g,0.802mmol)并将反应混合物加热至100℃持续16小时。将混合物用etoac稀释并用水和盐水洗涤。将有机相经na2so4干燥,过滤并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用0至50%etoac-庚烷梯度洗脱)以给出标题化合物(0.034g,35%),其为橘色粘稠油状物;ms(esi):m/z=242.1[m+h]+。
[0671]
步骤[b]2-氯-3-(3-羟基氮杂环丁烷-1-基)苯甲酸锂
[0672]
向2-氯-3-(3-羟基氮杂环丁烷-1-基)苯甲酸甲酯(0.035g,0.145mmol)的thf(0.350ml)溶液中添加1m lioh水溶液(0.29ml,290mmol)并将反应混合物在室温下搅拌5小
时。将混合物在真空中浓缩并将残余物在二异丙醚中研磨,滤出并进一步在高真空中干燥以给出粗标题化合物(0.032g,82%),其为浅棕色固体,其为锂盐;ms(esi):m/z=228.1[m+h]
+
。
[0673]
中间体a-2
[0674]
2-氟-3-(3-羟基氮杂环丁烷-1-基)苯甲酸锂
[0675]
的制备类似于中间体a-1,但在步骤[a]中使用3-溴-2-氟苯甲酸甲酯(cas rn 206551-41-9)以给出粗标题化合物,其为黄色固体,其为锂盐;ms(esi):m/z=212.0[m+h]
+
。
[0676]
中间体a-3
[0677]
2-氯-3-(1h-吡唑-5-基)苯甲酸
[0678]
步骤[a]2-氯-3-(1h-吡唑-5-基)苯甲酸甲酯
[0679]
在密封管中,将3-溴-2-氯苯甲酸甲酯(cas rn 871224-19-0,0.6g,2.4mmol)、3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯(cas rn 1256359-17-7,0.778g,2.65mmol)和双(三苯基膦)氯化钯(ii)(0.169g,0.240mmol)混合在dmf(6ml)中。将反应混合物用氩气吹扫。然后添加1m na2co3(7.21ml,7.21mmol)水溶液并将反应混合物加热至100℃持续4小时。将混合物用etoac稀释,倒入水中并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并在真空下浓缩。将残余物通过硅胶快速色谱法纯化(用50%至100%etoac-庚烷梯度洗脱)以给出标题化合物(0.195g,34%),其为黄色固体;ms(esi):m/z=237.1[m+h]+。
[0680]
步骤[b]2-氯-3-(1h-吡唑-5-基)苯甲酸
[0681]
向2-氯-3-(1h-吡唑-3-基)苯甲酸甲酯(0.195g,0.824mmol)的thf(2ml)溶液中添加1m lioh(1.65ml,1.65mmol)水溶液并将反应混合物在室温下搅拌3小时。将反应混合物通过添加2m hcl水溶液(0.8ml)酸化至ph=4并将水层用me-thf(2x 10ml)萃取。将合并的有机物经na2so4干燥,过滤并蒸发至干燥以给出粗标题化合物(0.144g,82%),其为黄色固体;ms(esi):m/z=223.0[m+h]+。
[0682]
中间体a-4
[0683]
2-氯-3-(4-甲基-1h-吡唑-3-基)苯甲酸
[0684]
的制备类似于中间体a-3,但在步骤[a]中使用4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯(cas rn 1402174-62-2)以给出粗标题化合物,其为白色固体;ms(esi):m/z=237.1[m+h]
+
。
[0685]
中间体a-5
[0686]
2-氟-3-(4-甲基-1h-吡唑-3-基)苯甲酸
[0687]
的制备类似于中间体a-4,但在步骤[a]中使用3-溴-2-氟苯甲酸甲酯(cas rn 206551-41-9)以给出粗标题化合物,其为白色固体;ms(esi):m/z=221.1[m+h]
+
。
[0688]
中间体a-6
[0689]
3-(4-甲基-1h-吡唑-3-基)苯甲酸
[0690]
的制备类似于中间体a-4,但在步骤[a]使用3-溴苯甲酸乙酯(cas rn 24398-88-7)以给出粗标题化合物,其为无色油状物;ms(esi):m/z=203.0[m+h]
+
。
[0691]
中间体a-7
rn 1046153-00-7)以给出粗标题化合物,其为浅黄色固体,其为锂盐;ms(esi):m/z=254.2[m+h]
+
。
[0715]
中间体a-12
[0716]
2-氯-3-[(3s)-3-羟基吡咯烷-1-基]苯甲酸
[0717]
的制备类似于中间体a-9,但在步骤[a]中使用(s)-吡咯烷-3-醇(cas rn 100243-39-8)以给出粗标题化合物,其为浅棕色泡沫状物;ms(esi):m/z=256.1[m+h]
+
。
[0718]
中间体a-13
[0719]
2-氯-3-[(3r)-3-羟基吡咯烷-1-基]苯甲酸
[0720]
的制备类似于中间体a-9,但在步骤[a]中使用(r)-吡咯烷-3-醇(cas rn 2799-21-5)以给出粗标题化合物,其为棕色泡沫状物;ms(esi):m/z=242.1[m+h]
+
。
[0721]
中间体a-14
[0722]
2-氯-3-(3-羟基-3-甲基氮杂环丁烷-1-基)苯甲酸锂
[0723]
的制备类似于中间体a-1,但在步骤[a]中使用3-甲基氮杂环丁烷-3-醇三氟乙酸(cas rn 1104083-24-0)以给出粗标题化合物,其为浅棕色油状物,其为锂盐;ms(esi):m/z=240.2[m+h]
+
。
[0724]
中间体a-15
[0725]
2-氯-3-[(3s)-3-羟基哌啶-1-基]苯甲酸锂
[0726]
步骤[a]2-氯-3-[(3s)-3-羟基-1-哌啶基]苯甲酸甲酯
[0727]
的制备类似于中间体a-8,但使用(s)-哌啶-3-醇(cas rn 24211-55-0)以给出标题化合物,其为黄色油状物;ms(esi):m/z=270.1[m+h]
+
。
[0728]
步骤[b]2-氟-3-(3-氧代哌嗪-1-基)苯甲酸
[0729]
的制备类似于中间体a-1[b]以给出粗标题化合物,其为白色固体,其为锂盐;ms(esi):m/z=256.1[m+h]
+
。
[0730]
中间体a-16
[0731]
2-氯-3-[(3r)-3-羟基哌啶-1-基]苯甲酸锂
[0732]
的制备类似于中间体a-15,但在步骤[a]中使用(r)-哌啶-3-醇(cas rn 62414-68-0)以给出粗标题化合物,其为白色固体;ms(esi):m/z=256.1[m+h]
+
。
[0733]
中间体a-17
[0734]
2-氯-3-(4-羟基哌啶-1-基)苯甲酸锂
[0735]
的制备类似于中间体a-15,但在步骤[a]中使用哌啶-4-醇(cas rn 5382-16-1)以给出粗标题化合物,其为灰白色粉末,其为锂盐;ms(esi):m/z=256.2[m+h]
+
。
[0736]
中间体a-18
[0737]
2-氯-3-(3-羟基-3-甲基-吡咯烷-1-基)苯甲酸锂
[0738]
的制备类似于中间体a-1,但在步骤[a]中使用3-甲基吡咯烷-3-醇(cas rn 125032-87-3)以给出粗标题化合物,其为浅棕色泡沫状物;ms(esi):m/z=256.1[m+h]
+
。
[0739]
中间体a-19
[0740]
2-氯-3-((3s,4s)-3,4-二羟基吡咯烷-1-基)苯甲酸锂
[0741]
的制备类似于中间体a-1,但在步骤[a]中使用(3s,4s)-吡咯烷-3,4-二醇(cas rn 90481-32-6)以给出粗标题化合物,其为橘色无定形固体;ms(esi):m/z=258.1[m+h]
+
。
[0742]
中间体a-20
[0743]
2-氯-3-(3-氟-3-(羟基甲基)氮杂环丁烷-1-基)苯甲酸锂
[0744]
的制备类似于中间体a-1,但在步骤[a]中使用3-氟氮杂环丁烷-3-基)甲醇(cas rn 1268520-93-9)以给出粗标题化合物,其为浅黄色固体;ms(esi):m/z=260.1[m+h]
+
。
[0745]
中间体a-21
[0746]
2-氯-3-(3-(羟基甲基)氮杂环丁烷-1-基)苯甲酸锂
[0747]
的制备类似于中间体a-1,但在步骤[a]中使用氮杂环丁烷-3-基甲醇(cas rn 95849-02-8)以给出粗标题化合物,其为浅黄色固体;ms(esi):m/z=242.1[m+h]
+
。
[0748]
中间体a-22
[0749]
2-氟-3-(1h-吡唑-3-基)苯甲酸
[0750]
在密封管中,将3-溴-2-氟苯甲酸甲酯(cas rn 206551-41-9,0.155g,0.665mmol)和3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯(cas rn 1256359-17-7,0.215g,0.732mmol)溶解于dmf(2ml)中。将混合物用氩气脱气5分钟。然后,添加双(三苯基膦)氯化钯(ii)(0.047mg,0.066mmol)随后添加1m na2co3(2ml,2mmol)水溶液并将反应混合物在100℃下搅拌过夜。将混合物用etoac稀释并用h2o洗涤。分离各层,并将水相用hcl(25%)酸化至ph=1并用etoac再次萃取。将合并的有机物经na2so4干燥,过滤并在真空中浓缩。将残余物通过反相hplc纯化以给出一些产物(0.005g)。将水层蒸发至干燥以给出更多产物(0.025g)。将两种物质合并以给出标题化合物(0.030g,21.9%),其为无色固体;ms(esi):m/z=207.1[m+h]+。
[0751]
中间体b-1
[0752]
2-氯-3-(3-氟-1h-吡唑-4-基)苯甲酸
[0753]
步骤[a]2-氯-3-(3-氟-1h-吡唑-4-基)苯甲酸甲酯
[0754]
在微波小瓶中,将2-氯-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯甲酸甲酯(cas rn 2201133-24-4,0.162g,0.546mmol)、4-溴-3-氟-1h-吡唑(cas rn 1346555-56-3,0.060g,0.364mmol)和k2co3(0.151g,1.09mmol)混合在二噁烷(7.8ml)/水(2.6ml)中。将反应混合物用氩气脱气。然后将双(二-叔丁基(4-二甲基氨基苯基)膦)二氯钯(ii)(cas rn 887919-35-9,0.025g,0.036mmol)添加至混合物,将其在微波中加热至115℃持续30分钟。将混合物用etoac稀释,倒入饱和nahco3水溶液并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并在真空下浓缩。将残余物通过硅胶快速色谱法纯化(用0至50%etoac-庚烷梯度洗脱)以给出标题化合物(0.045g,49%),其为浅黄色固体;ms(esi):m/z=255.2[m+h]+。
[0755]
步骤[b]3-(3-氟-1h-吡唑-4-基)苯甲酸
[0756]
的制备类似于中间体a-3[b]以给出标题化合物,其为黄色固体。ms(esi):m/z=241.1[m+h]
+
。
[0757]
中间体b-2
[0758]
2-氟-3-异噻唑-3-基-苯甲酸
[0759]
的制备类似于中间体b-1,但在步骤[a]中使用2-氟-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯甲酸甲酯(cas rn 1638847-77-4)和3-溴异噻唑(cas rn 55512-82-8)以给出粗标题化合物,其为棕色油状物;ms(esi):m/z=224.1[m+h]
+
。
[0760]
中间体b-3
[0761]
2-氯-3-(4-氟-1h-吡唑-5-基)苯甲酸
[0762]
的制备类似于中间体b-1,但在步骤[a]中使用3-溴-4-氟-1h-吡唑(cas rn 1621526-49-5)以给出粗标题化合物,其为黄色油状物;ms(esi):m/z=255.1[m+h]
+
。
[0763]
中间体b-4
[0764]
2-氟-3-(1h-吡唑-5-基)苯甲酸锂
[0765]
步骤[a]2-氟-3-(1h-吡唑-5-基)苯甲酸甲酯
[0766]
在密封管中,将k2co3(0.412g,2.98mmol)、2-氟-3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)苯甲酸甲酯(cas rn 1638847-77-4,0.334g,1.19mmol)、3-溴-1h-吡唑(cas rn 14521-80-3,0.146g,0.993mmol)和双(二-叔丁基(4-二甲基氨基苯基)膦)二氯钯(ii)(cas rn 887919-35-9,0.070g,0.099mmol)混合于二噁烷(5.5ml)和水(1.8ml)中。将混合物用氩气脱气5分钟。将反应混合物加热至60℃持续30分钟然后加热至110℃再持续3小时。将混合物用etoac稀释,倒入饱和nahco3水溶液并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并蒸发。将残余物通过硅胶快速色谱法纯化(用0至60%etoac-庚烷梯度洗脱)以给出标题化合物(0.59g,27%),其为浅黄色固体;ms(esi):m/z=221.1[m+h]+。
[0767]
步骤[b]2-氟-3-(1h-吡唑-5-基)苯甲酸锂
[0768]
的制备类似于中间体a-1[b]以给出标题化合物,其为无色固体。ms(esi):m/z=207.0[m+h]
+
。
[0769]
中间体b-5
[0770]
2-氟-3-(4-氟-1h-吡唑-5-基)苯甲酸
[0771]
的制备类似于中间体b-4,但在步骤[a]中使用3-溴-4-氟-1h-吡唑(cas rn 1621526-49-5)以给出粗标题化合物,其为无色固体;ms(esi):m/z=225.1[m+h]
+
。
[0772]
中间体b-6
[0773]
2-氯-3-(1,2,4-噻二唑-3-基)苯甲酸锂
[0774]
的制备类似于中间体b-1,但在步骤[a]中使3-溴-1,2,4-噻二唑(cas rn 1621526-49-5)以给出粗标题化合物,其为无色固体;ms(esi):m/z=241.1[m+h]
+
。
[0775]
中间体c-1
[0776]
2-氯-3-(2-氧代噁唑烷-3-基)苯甲酸
[0777]
步骤[a]2-氯-3-(2-氧代噁唑烷-3-基)苯甲酸甲酯
[0778]
在密封管中,将2-氯-3-碘苯甲酸甲酯(cas rn 620621-51-4,0.2g,0.675mmol)、噁唑烷-2-酮(0.117g,1.35mmol)和k2co3(0.233g,1.69mmol)混合在乙腈(2ml)中。将反应混合物用氩气吹扫。然后添加n,n
′‑
二甲基乙烷-1,2-二胺(0.012g,0.135mmol)和碘化亚铜(i)(0.026g,0.135mmol)并将反应混合物加热至80℃持续15小时。将混合物用etoac稀释,倒入水中并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并在真空下浓缩。将残余物通过反相hplc纯化以给出标题化合物(0.036g,20%),其为浅棕色油状物;ms(esi):m/z=256.1[m+h]+。
[0779]
步骤[b]2-氯-3-(2-氧代噁唑烷-3-基)苯甲酸
[0780]
的制备类似于中间体a-1[b]以给出标题化合物,其为灰白色固体。ms(esi):m/z=
242.0[m+h]
+
。
[0781]
中间体c-2
[0782]
2-氯-3-(2-氧代咪唑烷-1-基)苯甲酸锂
[0783]
的制备类似于中间体c-1,但在步骤[a]中使用1,3-二甲基脲以给出粗标题化合物,其为白色固体,其为锂盐;ms(esi):m/z=241.1[m+h]
+
。
[0784]
中间体d-1a和d1-b
[0785]
2-溴-3-[(z)-苯乙烯基]苯甲酸和2-溴-3-[(e)-苯乙烯基]苯甲酸
[0786]
步骤[a](2-溴-3-甲氧基羰基-苯基)甲基-三苯基-溴化鏻
[0787]
向三苯基膦(0.439g,1.67mmol)的甲苯(5ml)溶液中添加2-溴-3-(溴甲基)苯甲酸甲酯(cas rn 750585-90-1,0.515g,1.67mmol)并将反应混合物加热至110℃持续15小时。将固体沉淀物滤出,用二乙醚洗涤3次,然后进一步干燥以给出粗标题化合物(0.918g),其为白色固体,其为氢溴酸盐;ms(esi):m/z=491.1[m+h]
+
。
[0788]
步骤[b]2-溴-3-[(z)-苯乙烯基]苯甲酸甲酯和2-溴-3-[(e)-苯乙烯基]苯甲酸甲酯
[0789]
向冷却至0℃的(2-溴-3-甲氧基羰基-苯基)甲基-三苯基-溴化鏻(0.102g,0.207mmol)的thf悬浮液(10ml)中添加叔丁醇钾(0.025g,0.226mmol)并将混合物搅拌30分钟。然后逐滴添加苯甲醛(0.019ml,0.188mmol)的thf (5ml)溶液并允许反应混合物在室温下搅拌4小时。将混合物用饱和nh4cl水溶液猝灭并用etoac萃取。将合并的有机层用盐水洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物通过纯硅胶柱色谱法化(用0至40%etoac-庚烷梯度洗脱)以分别给出2-溴-3-[(z)-苯乙烯基]苯甲酸甲酯(0.013g,17%)和2-溴-3-[(e)-苯乙烯基]苯甲酸甲酯(0.023g,38%),它们是黄色油状物;ms(esi):m/z=317.0[m+h]+。
[0790]
步骤[c]2-溴-3-[(z)-苯乙烯基]苯甲酸
[0791]
向(z)-2-溴-3-苯乙烯基苯甲酸甲酯(0.113g,0.357mmol)的thf(1ml)溶液中添加1m lioh水溶液(0.219ml,0.219mmol)并将反应混合物加热至40℃持续6小时。将反应用2m hcl水溶液中和并用etoac萃取。将有机层用na2so4干燥,过滤并在真空中浓缩以给出粗标题化合物(d1a,0.095g,87%),其为白色固体;ms(esi):m/z=303.1[m+h]
+
。
[0792]
步骤[d]2-溴-3-[(e)-苯乙烯基]苯甲酸
[0793]
的制备类似于步骤[c],但使用(e)-2-溴-3-苯乙烯基苯甲酸甲酯以给出粗标题化合物(d1b,85%),其为白色固体;ms(esi):m/z=303.1[m+h]
+
。
[0794]
中间体d-2
[0795]
2-溴-3-[(e)-2-[4-(叔丁氧基羰基氨基)苯基]乙烯基]苯甲酸
[0796]
的制备类似于中间体d-1b,但在步骤[b]中使用(4-甲酰基苯基)氨基甲酸叔丁酯(cas rn 144072-30-0)以给出粗标题化合物,其为无色油状物;ms(esi):m/z=418.2[m+h]
+
。
[0797]
中间体d-3
[0798]
2-溴-3-[(e)-2-(4-羧苯基)乙烯基]苯甲酸
[0799]
的制备类似于中间体d-1b,但在步骤[b]中使用4-甲酰基苯甲酸甲酯(cas rn 1571-08-0)以给出粗标题化合物,其为无色无定形固体;ms(esi):m/z=346.9[m+h]
+
。
[0800]
实例1
[0801]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氯-3-甲氧基苯基)甲酮
[0802]
在烧瓶中,将(7s,9ar)-7-(4-氯苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-3a,0.015g,0.053mmol)和2-氯-3-甲氧基苯甲酸(cas rn 33234-36-5,0.010g,0.055mmol)混合在dmf(0.5ml)中。然后添加h
ü
nig碱(0.023ml,0.132mmol)随后添加hatu(0.021g,0.055mmol)并将反应混合物在室温下搅拌2小时。将粗混合物通过反相hplc纯化以给出标题化合物(0.012g,50%),其为无色无定形固体;ms(esi):m/z=453.2[m+h]
+
。
[0803]
表2中列出的以下实例通过类似于针对实例1的制备所述的步骤制得,使用所示的中间体和/或可商购获得的化合物并且使用上述纯化方法诸如反相hplc(gemini nx柱)或硅胶快速层析法。
[0804]
表2
[0805]
[0806]
[0807]
[0808]
[0809]
[0810]
[0811]
[0812]
[0813]
[0814]
[0815]
[0816]
[0817]
[0818]
[0819]
[0820]
[0821]
[0822]
[0823][0824]
买例23
[0825]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2-氟-3-哌嗪-1-基苯基)甲酮
[0826]
向4-[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氟苯基]哌嗪-1-甲酸叔丁酯(实例22,0.023g,0.040mmol)的dcm
(0.5ml)溶液中添加tfa(0.047ml,0.607mmol)并将反应混合物在室温下搅拌6小时。将混合物在真空中浓缩,并将残余物溶于etoac,倒入饱和nahco3水溶液,并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并蒸发至干燥以给出粗标题化合物(0.017g,82%),其为黄色固体;ms(esi):m/z=473.3[m+h]
+
。
[0827]
实例24
[0828]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-羟基-7-(2-甲基丙基)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮
[0829]
将氯化饰(iii)(0.092g,0.372mmol)的thf(1ml)悬浮液在室温下搅拌1.5小时。将混合物用冰浴冷却至0℃,逐滴添加2m异丁基溴化镁的thf(0.155ml,0.310mmol)溶液并继续在该温度下搅拌1小时。然后添加2-(2-氯-3-甲氧基苯甲酰)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-7-酮(中间体i-5,0.100g,0.310mmol)的thf(0.3ml)溶液并将反应混合物在0℃下搅拌30分钟。将混合物用水淬灭,经dicalite过滤并用etoac洗涤。将所得的溶液经na2so4干燥,过滤并在真空中浓缩。将残余物通过反相hplc纯化以给出标题化合物(0.014,12%),其为无定形无色固体;ms(esi):m/z=381.3[m+h]
+
。
[0830]
实例25
[0831]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-环戊基-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮
[0832]
的制备类似于实例24,但使用1m环戊基溴化镁的thf溶液以给出标题化合物,其为浅黄色无定形固体;ms(esi):m/z=393.3[m+h]
+
。
[0833]
买例26
[0834]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-羟基-7-(三氟甲基)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮
[0835]
在3颈圆底烧瓶中,将2-(2-氯-3-甲氧基苯甲酰)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-7-酮(中间体i-5,0.1g,0.310mmol)的thf(1.7ml)溶液用冰盐浴冷却至-5℃。添加三甲基(三氟甲基)硅烷(0.055ml,0.372mmol),然后10分钟后将1m tbaf(0.310ml,0.310mmol)的thf溶液添加至混合物,期间保持低于2℃的温度。将反应混合物在0℃下再搅拌10分钟,然后允许升温至室温并继续搅拌2小时。将混合物用饱和nh4cl水溶液猝灭并将混合物用etoac稀释。将有机层用水、盐水洗涤,经na2so4干燥并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用50%至100%etoac-庚烷梯度洗脱)以给出标题化合物(0.022g,18%),其为无色固体;ms(esi):m/z=393.2[m+h]
+
。
[0836]
实例30
[0837]
n-[4-[(e)-2-[3-[(7r,9ar)-7-(4-氟苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴苯基]乙烯基]苯基]丙-2-烯酰胺
[0838]
步骤[a][(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-[3-[(e)-2-(4-氨基苯基)乙烯基]-2-溴-苯基]甲酮
[0839]
向n-[4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴苯基]乙烯基]苯基]氨基甲酸叔丁酯(实例29,0.007g,0.011mmol)的dcm(0.5ml)溶液添加tfa(0.017ml,0.222mmol)并将反应混合物在室温下搅拌18小时。将混合物在真空中浓缩,并将残余物溶于etoac并用饱和nahco3水溶液洗涤。将
有机层用盐水洗涤,经na2so4干燥,过滤并蒸发至干燥以给出粗标题化合物(0.008g),其为黄色固体;ms(esi):m/z=550.1[m+h]
+
。
[0840]
步骤[b]n-[4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴苯基]乙烯基]苯基]丙-2-烯酰胺
[0841]
向[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-基]-[3-[(e)-2-(4-氨基苯基)乙烯基]-2-溴-苯基]甲酮(0.008g,0.015mmol)和丙烯酸(0.001g,0.015mmol)的dmf(0.2ml)溶液添加h
ü
nig碱(0.008ml,0.046mmol)随后添加hatu(0.006g,0.017mmol)并将反应混合物在室温下搅拌15小时。将混合物用etoac稀释,用水、盐水洗涤,经na2so4干燥,过滤并在真空中浓缩。将残余物通过反相hplc纯化以给出标题化合物(0.005g,5%),其为无色无定形物;ms(esi):m/z=604.7[m+h]
+
。
[0842]
实例31
[0843]
4-[(e)-2-[3-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]-2-溴-苯基]乙烯基]-n-甲基-苯甲酰胺和3-[(e)-2-[4-[(7r,9ar)-7-(4-氯苯基)-1,3,4,6,7,8,9,9a-八氢吡啶并[1,2-a]吡嗪-2-羰基]苯基]乙烯基]-2-溴-n-甲基-苯甲酰胺
[0844]
向2-溴-3-[(e)-2-(4-羧苯基)乙烯基]苯甲酸(中间体d-3,0.04g,0.115mmol)的dmf(0.5ml)溶液中添加h
ü
nig碱(0.05ml,0.288mmol)并将混合物在室温下搅拌1小时。然后逐滴添加甲胺盐酸盐(0.008g,0.115mmol)和(7r,9ar)-7-(4-氯苯基)八氢-1h-吡啶并[1,2-a]吡嗪(中间体i-6,0.029g,0.115μmol)在dmf(0.5ml)/h
ü
nig碱(0.05ml)中的混合物并将反应混合物在室温下搅拌18小时。将水添加至混合物,将其然后在超声浴中搅拌。所得的沉淀物滤出,收集,倒入1m na2co3水溶液并将水层用dcm萃取。将有机层合并,经na2so4干燥,过滤并在真空中浓缩。将残余物通过硅胶快速色谱法纯化(用0至5%meoh-dcm梯度洗脱)以给出标题化合物(0.032g,44%),其为异构体的1∶1混合物,其为灰白色固体;ms(esi):m/z=592.2[m+h]
+
。
[0845]
实例65
[0846]
[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2,3-二氢-1h-吲哚-4-基)甲酮
[0847]
步骤[a]4-[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2,3-二氢吲哚-1-甲酸叔丁酯
[0848]
的制备类似于实例1,但使用(7s,9ar)-7-(3-氯-4-氟-苯基)-1,2,3,4,6,8,9,9a-八氢吡啶并[1,2-a]吡嗪-7-醇(中间体i-3a)和1-叔丁氧基羰基吲哚啉-4-甲酸(cas rn 208774-11-2)以给出标题化合物,其为无色泡沫状物;ms(esi):m/z=530.4[m+h]
+
。
[0849]
步骤[b][(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(2,3-二氢-1h-吲哚-4-基)甲酮
[0850]
向4-[(7s,9ar)-7-(3-氯-4-氟苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2,3-二氢吲哚-1-甲酸叔丁酯(0.03g,0.057mmol)的dcm(0.5ml)溶液添加tfa(0.087ml,1.13mmol)并将反应混合物在室温下搅拌2小时。将混合物逐滴添加至饱和nahco3(5ml)水溶液并将水相用dcm萃取。将合并的有机相经na2so4干燥,过滤并蒸发至干燥以给出标题化合物(0.007g,29%),其为无色泡沫状物;ms(esi):m/z=430.3[m+h]
+
。
[0851]
实例66
[0852]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[4-氯-5-(1h-吡唑-3-基)吡啶-3-基]甲酮
[0853]
在密封管中,将[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(5-溴-4-氯吡啶-3-基)甲酮(中间体i-9,0.023g,0.048mmol)、3-(4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷-2-基)-1h-吡唑-1-甲酸叔丁酯(cas rn 1256359-17-7,0.017g,0.058mmol)和双(三苯基膦)氯化钯(ii)(0.004g,0.005mmol)溶解于dmf(0.25ml)中。将反应混合物用氩气吹扫。然后添加1m na2co3(0.145ml,0.145mmol)水溶液并将反应混合物加热至90℃过夜。将混合物用etoac稀释,倒入水中并将水层用etoac萃取。将合并的有机物用盐水洗涤,经na2so4干燥,过滤并在真空下浓缩。将残余物通过反相hplc纯化以给出标题化合物(0.003g,12%),其为无色固体;ms(esi):m/z=472.4[m+h]
+
。
[0854]
实例67
[0855]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1,2-噻唑-3-基)苯基]甲酮
[0856]
在微波小瓶中,将[3-[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-羰基]-2-氯-苯基]硼酸(中间体i-7,0.03g,0.067mmol)、3-溴异噻唑(cas rn 55512-82-8,0.01g,0.061mmol)、双(二-叔丁基(4-二甲基氨基苯基)膦)二氯钯(ii)(cas rn 887919-35-9,0.004g,0.006mmol)和k2co3(0.025g,0.183mmol)混合在二噁烷(1.72ml)和水(0.440ml)中。将混合物用氩气脱气并在微波中加热至90℃持续15分钟。将混合物用etoac稀释,用水和盐水洗涤。将有机层经na2so4干燥,过滤并在真空中浓缩。将残余物通过反相hplc纯化以给出标题化合物(0.005g,16%),其为无色无定形固体;ms(esi):m/z=488.3[m+h]
+
。
[0857]
实例68
[0858]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1,2-噻唑-4-基)苯基]甲酮
[0859]
的制备类似于实例67,但使用4-溴异噻唑(cas rn 24340-77-0)以给出标题化合物,其为无色无定形固体;ms(esi):m/z=488.3[m+h]
+
。
[0860]
实例69
[0861]
[(7r,9ar)-7-羟基-7-[5-(三氟甲基)吡啶-2-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[2-氯-3-(1,2-噻唑-3-基)苯基]甲酮
[0862]
的制备类似于实例67,但使用2-氯-3-((7r,9ar)-7-羟基-7-(5-(三氟甲基)吡啶-2-基)八氢-2h-吡啶并[1,2-a]吡嗪-2-羰基)苯基)硼酸(中间体1-8)和溴异噻唑(cas rn 55512-82-8)以给出标题化合物,其为无色无定形固体;ms(esi):m/z=523.3[m+h]
+
。
[0863]
实例70
[0864]
[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-[4-甲基-5-(1h-吡唑-3-基)吡啶-3-基]甲酮
[0865]
的制备类似于实例66,但使用[(7s,9ar)-7-(4-氯苯基)-7-羟基-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]-(5-溴-4-甲基吡啶-3-基)甲酮(中间体i-11)以给出标题化合物,其为无色泡沫状物;ms(esi):m/z=452.3[m+h]
+
。
[0866]
实例71和72
[0867]
(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-羟基-7-[6-(三氟甲基)吡啶-3-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮和(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-羟基-7-[6-(三氟甲基)吡啶-3-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮
[0868]
向冷却至-78℃的5-溴-2-(三氟甲基)吡啶(cas rn 436799-32-5,0.12g,0.531mmol)的甲苯(4.2ml)悬浮液中添加1.6m n-buli的己烷(0.398ml,0.637mmol)溶液并将混合物在该温度下搅拌5分钟。然后在-78℃下逐滴添加2-(2-氯-3-甲氧基苯甲酰)-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-7-酮(中间体i-5,0.189g,0.584mmol)的溶液并将反应混合物在该温度下搅拌3小时。将混合物在-78℃下通过添加饱和nh4cl水溶液猝灭并用etoac萃取。将合并的有机物用h2o、盐水洗涤,经na2so4干燥,过滤并蒸发。将该粗物质通过硅胶快速色谱法纯化(用20%至60%etoac的庚烷溶液梯度洗脱)以分别给出(2-氯-3-甲氧基苯基)-[外消旋-(7r,9ar)-7-羟基-7-[6-(三氟甲基)吡啶-3-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮(实例71,0.006g,2.4%)和65mg含有反式化合物的纯度较低的物质。将该残余物通过反相hplc纯化以给出(2-氯-3-甲氧基苯基)-[外消旋-(7r,9as)-7-羟基-7-[6-(三氟甲基)吡啶-3-基]-3,4,6,8,9,9a-六氢-1h-吡啶并[1,2-a]吡嗪-2-基]甲酮(实例72,0.004g,1.8%),其为无色无定形固体;ms(esi):m/z=470.3[m+h]
+
。
[0869]
实例73
[0870]
式(i)的化合物可以以本身已知的方式用作产生以下组成的片剂的活性成分:
[0871][0872]
实例74
[0873]
式(i)的化合物可以以本身已知的方式用作产生以下组成的胶囊的活性成分:
[0874]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1