用于将细胞重新程序化成浆细胞样树突细胞或I型干扰素产生细胞的组合物、方法及其用途与流程
用于将细胞重新程序化成浆细胞样树突细胞或i型干扰素产生细胞的组合物、方法及其用途
技术领域
1.本公开内容涉及用于将细胞重新程序化成浆细胞样树突细胞或i型干扰素产生细胞的组合物、方法及其用途。
2.本公开内容涉及用于通过引入和表达分离的/合成的转录因子来从分化的、多潜能或多能干细胞制备浆细胞样树突细胞或i型干扰素产生细胞(其促进免疫抗病毒和抗肿瘤应答)的方法的开发。更具体地,本公开内容提供了通过用特定转录因子的组合的惊人有益应用进行直接细胞重新程序化而获得浆细胞样树突细胞或i型干扰素产生细胞的方法。
3.背景
4.细胞重新程序化依赖于将一种细胞状态的表观遗传和转录网络重新连接到不同细胞类型的表观遗传和转录网络。转录因子(tf)-转导实验已强调了成体体细胞或分化的细胞的可塑性,从而提供了生成任何期望细胞类型的新技术。通过tf的强制表达,可能将体细胞或分化的细胞重新程序化为与胚胎干细胞非常相似的诱导型多能干细胞(ipsc)(takahashi等人,2006;takahashi等人,2007)。可替换地,还可以将体细胞转化为另一种特化细胞类型(pereira等人,2012)。使用规定靶细胞身份的tf,已证明直接谱系转化成功地将小鼠和人成纤维细胞重新程序化为几种细胞类型,诸如神经元、心肌细胞和肝细胞(xu等人,2015)。还在造血系统中证实了谱系转化,其中tf的强制表达诱导了b细胞和成纤维细胞中的巨噬细胞命运(xie等人,2004),并且用转录因子gata2、gfi1b、cfos和etv6实现了将小鼠成纤维细胞直接重新程序化为克隆原性的造血祖细胞(pereira等人,2013)。这四种tf诱导动态的多阶段造血过程,其通过内皮样中间体进展,在体外重演发育血细胞生成(pereira等人,2016)。
5.重新程序化的细胞对于再生医学而言是非常有前途的治疗工具,并且已在临床研究中测试了通过ipsc的分化获得的细胞。
6.细胞重新程序化策略已经强调了细胞命运的灵活性,可能使用细胞类型特异性的tf将体细胞转化为多能性。一种分化的细胞类型向另一种的直接谱系转化也已被证明和探索,以阐明细胞生物学机制和用于再生医学目的。近年来,我们已经证实,抗原呈递树突细胞(dc)可以通过tf的小组合从不相关的细胞类型重新程序化(rosa等人,2018)。经典地,有人认为,骨髓dc定向祖细胞产生在功能上不同的dc子集:常规dc(cdc)和浆细胞样dc(pdc)。cdc是驱动抗原特异性免疫应答的专业抗原呈递细胞(apc),而pdc是在病毒感染期间i型干扰素的专业生产者。它们表现出先天性和适应性免疫功能,并可以作为直接影响t细胞应答的apc起作用。在dc发育期间调节不同子集的分歧的时机和确切机制仍有待确定。
7.文件ep 3 385 373涉及用于细胞诱导或将细胞重新程序化为常规树突细胞状态或抗原呈递细胞状态的组合物、核酸构建体、方法及其试剂盒,其部分基于在该文件中描述的惊人效果:允许将分化的或未分化的细胞诱导或重新程序化为dc或apc的转录因子组合的新型用途。
8.在文件ep 3 385 373中描述的转录因子的组合诱导具有dc的cdc1子集特有的表
面表型、转录标记和功能特性的dc。以前没有描述过分泌i型干扰素例如干扰素α(ifn-α)和β(ifn-β)的能力。
9.本文描述的诱导的pdc或i型干扰素产生细胞概括了检测核酸和通过分泌i型干扰素作出应答的典型pdc功能特性(reizis 2019)。
10.公开这些事实是为了说明本公开内容所解决的技术问题。
技术实现要素:
11.本发明主题鉴定了几种分离的转录因子,它们令人惊讶地在体外、离体或在体内将分化的细胞、多潜能或多能干细胞重新程序化或诱导成pdc或i型干扰素产生细胞。
12.令人惊讶的是,通过如本公开内容中所述的重新程序化产生的诱导的pdc或i型干扰素产生细胞固有地能够分泌诱导抗病毒或抗肿瘤应答所需的i型干扰素。
13.令人惊讶的是,通过如本公开内容中所述的重新程序化产生的诱导的pdc或i型干扰素产生细胞固有地能够通过分泌增加的量的诱导抗病毒应答所需的i型干扰素(例如干扰素α(ifn-α)和β(ifn-β))而对toll-样受体7(tlr7)和tlr9配体做出应答。
14.dc是遍布全身的专业apc,其在先天性和适应性免疫系统的界面处发挥功能。dc通过其捕获、处理在主要组织相容性复合物(mhc)i类和mhc ii类分子上负载的抗原并将其呈递给t细胞从而将它们靶向至不同类型的免疫应答的能力,能够提供外部环境和适应性免疫系统之间的关键联系。首先,dc必须捕获抗原并通过主要组织相容性复合物(mhc)i类和mhc ii类处理它们。在其活化后,dc能够向局部引流淋巴结迁移,从而引发多种b细胞和t细胞应答,这是适应性免疫的一个关键特征。早期保护效力主要是通过诱导b淋巴细胞产生的抗原特异性抗体来赋予。针对特定抗原的长期保护需要特异性抗体的持久性和免疫记忆的产生,所述免疫记忆可以在随后的抗原暴露以后提供快速且有效的应答。dc作为专业的apc具有交叉呈递抗原的能力,这意味着,除了其经典的在mhc ii类上呈递外源性抗原和在mhc i类上呈递内源性抗原的能力外,它们还能够在mhc i类上呈递外源性抗原,这是产生细胞毒性t淋巴细胞应答(ctl)的关键步骤。
15.个体发育和/或dc所在的微环境可能导致dc对表面受体的独特组合的表达。例如,表型标准允许将小鼠dc分类为不同的亚群。其中,淋巴组织中的cdc传统上被细分为cdc1和cdc2亚群。有人认为,不同的dc子集可能参与某些病原体的特异性识别和/或调节不同的免疫应答,例如th1或th2(免疫)或调节性t细胞(耐受性)。但是,dc的表型和功能行为也受到外部活化刺激的显著调理,表明显著的可塑性。cdc1和cdc2子集在体内不同地引发th1和th2应答。癌症的免疫疗法依赖于使用dc以引发th1或细胞毒性t淋巴细胞应答以促进肿瘤清除。与cdc一起,pdc作为一个独特的dc子集出现,在病毒感染或通过tlr7和tlr9识别自身核酸后专门生产i型干扰素(ifn)。除了有助于抗病毒免疫外,pdc还可以参与免疫原性的和致耐受性的适应性免疫应答的引发,这与自身免疫性疾病和癌症的病理学有关。
16.pdc具有响应于病毒和/或病毒衍生的核酸产生比任何其它细胞类型更多的i型干扰素的独特特征。tlr7和9在pdc中、在细胞内的胞内体隔室中高度表达。tlr7识别病毒单链rna,且tlr9检测富含未甲基化的cpg寡核苷酸的病毒双链dna。在被病毒核酸活化后,它们诱导衔接蛋白myd88和两种主要的tlr7/9细胞内信号传导途径的刺激和募集。第一个途径导致i型干扰素产生,这需要irf7易位至细胞核,从而促进ifn-α和ifn-β转录和分泌。i型干
扰素(由pdc在被核酸活化后分泌)能够连接先天性和适应性免疫系统,从而促进长期t-细胞存活和记忆,th1极化、cd8 t-细胞细胞裂解活性、nk细胞介导的细胞毒性和b-细胞生长和分化。可替换地,第二途径的活化导致促炎细胞因子tnf-α和il-6、以及趋化因子例如cxcl9(mig)、cxcl10(ip-10)、ccl3(mip-1a)、ccl4(mip-1b)和ccl5(rantes)的表达的nf-kb依赖性诱导。这些进而能够将活化的cd4和cd8 t细胞吸引到炎症部位。
17.目前,基于dc的免疫疗法依赖于自体dc前体:与效率较低的dc的产生相关的单核细胞,或以非常低的数目分离的造血祖细胞。此外,这些前体细胞通常在患有癌症的患者中受到损害,从而导致功能失调的dc和异质dc的混合物的产生。相反,非造血细胞类型诸如成纤维细胞通常不受影响。人真皮成纤维细胞(hdf)还表现出其它竞争优势;它们容易从小皮肤穿刺活检样品中获得,容易在体外扩增几代(4周后1500-2000万个细胞),并且可以冷冻保存并按需使用。鉴于dc在先天性和适应性免疫系统的界面上发挥作用的基本作用,临床仍需要寻找替代策略来产生功能性pdc的同质群体以引发抗原特异性应答。
18.近年来,pdc由于能够产生大量ifn和启动t细胞而引起了特别兴趣。由于cd4+和cd8+t细胞应答受损,pdc-缺陷型小鼠被显示不能高效地清除淋巴细胞性脉络丛脑膜炎病毒(cervantes-barragan等人,2012)。类似地,据报告,患者中irf7的无效突变负面地影响pdc对i型和iii型ifn的产生,这导致严重的流感感染(ciancanelli等人,2015)。这些发现指示,pdc对抵抗病毒感染是重要的,尤其是在早期阶段(swiecki和colonna,2015),此时ifn产生可以限制病毒复制。此外,几个临床试验已经探索了pdc诱导抗肿瘤免疫应答的潜力(tel等人,2013)。但是,pdc的治疗用途似乎受限于在血液中循环的这些细胞的低数目。因此,需要dc、特别是pdc的替代来源来满足治疗需求。
19.在一些实施方案中,与具有多肽序列(seq.id.49-seq.id.96)的参考多肽或由序列seq.id.1-seq.id.48编码的多肽具有相同或类似活性的多肽变体或家族成员可以用在本文所述的组合物、方法和试剂盒中。通常,用于本文所述的组合物、载体、构建体、方法和试剂盒中的编码pdc诱导因子的特定多肽的变体将与该特定参考多核苷酸或多肽具有至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或更多序列同一性,如通过本文描述的和本领域技术人员已知的序列比对程序和参数所确定。
20.用于比较的序列比对方法是本领域众所周知的,这样的方法包括gap、bestfit、blast、fasta和tfasta。gap使用needleman和wunsch的算法((1970)j mol biol 48:443-453)以寻找两个序列的总体(在整个序列中)比对,其使匹配数最大化并使缺口数最小化。blast算法(altschul等人(1990)j mol biol 215:403-10)计算序列同一性百分比并执行两个序列之间的相似性的统计学分析。用于执行blast分析的软件可以通过国立生物技术信息中心(national centre for biotechnology information,ncbi)公开获得。使用matgat软件包中可得到的方法之一,也可以确定相似性和同一性的总体百分比(campanella等人,bmc bioinformatics.2003年7月10日;4:29.matgat:an application that generates similarity/identity matrices using protein or dna sequences)。如本领域技术人员显而易见的,可以进行少量手动编辑以优化保守基序之间的比对。使用blast和默认参数在整个氨基酸或核苷酸序列上确定在本发明主题中作为百分比指示的序列同一性值。
21.在一个实施方案中,为了更好的结果,所述转录因子可以由选自以下的多核苷酸编码:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、hdac5(seq.id.15,seq.id.16)、hhex(seq.id.17,seq.id.18)、hoxa5(seq.id.19,seq.id.20)、id3(seq.id.21,seq.id.22)、ikzf1(seq.id.23,seq.id.24)、ikzf2(seq.id.25,seq.id.26)、ikzf3(seq.id.27,seq.id.28)、ikzf5(seq.id.29,seq.id.30)、irf7(seq.id.31,seq.id.32)、mef2c(seq.id.33,seq.id.34)、myb(seq.id.35,seq.id.36)、runx2(seq.id.37,seq.id.38)、stat3(seq.id.39,seq.id.40)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、stat1(seq.id.45,seq.id.46)和tsc22d1(seq.id.47,seq.id.48)。
22.在本公开内容的一个实施方案中,所述转录因子可以选自:irf8(seq.id.49,seq.id.50)、spib(seq.id.51,seq.id.52)、arid5a(seq.id.53,seq.id.54)、bcl11a(seq.id.55,seq.id.56)、cbfa2t3(seq.id.57,seq.id.58)、creb3l2(seq.id.59,seq.id.60)、ets1(seq.id.61,seq.id.62)、hdac5(seq.id.63,seq.id.64)、hhex(seq.id.65,seq.id.66)、hoxa5(seq.id.67,seq.id.68)、id3(seq.id.69,seq.id.70)、ikzf1(seq.id.71,seq.id.72)、ikzf2(seq.id.73,seq.id.74)、ikzf3(seq.id.75,seq.id.76)、ikzf5(seq.id.77,seq.id.78)、irf7(seq.id.79,seq.id.80)、mef2c(seq.id.81,seq.id.82)、myb(seq.id.83,seq.id.84)、runx2(seq.id.85,seq.id.86)、stat3(seq.id.87,seq.id.88)、tcf4(seq.id.89,seq.id.90)、tcf12(seq.id.91,seq.id.92)、stat1(seq.id.93,seq.id.94)和tsc22d1(seq.id.95,seq.id.96)。
23.在一个实施方案中,本公开内容的转录因子可以用在兽医或人医学中,特别是在感染性疾病或病毒性疾病或病毒诱导的疾病中,或在癌症或自身免疫性疾病或神经变性疾病中。
24.在一个实施方案中,为了更好的结果,所述细胞可以选自:多能干细胞、多潜能干细胞、造血干细胞、分化的细胞、肿瘤细胞、癌细胞、细胞系,特别是中胚层衍生的细胞系,诸如单核细胞细胞系,及其混合物。特别是哺乳动物细胞,更特别是小鼠或人细胞。
25.在一个实施方案中,为了更好的结果,本公开内容的转录因子可以用作选自多能干细胞或多潜能干细胞或分化的细胞、及其混合物的细胞向树突细胞或i型干扰素产生细胞或抗原呈递细胞、优选树突细胞或i型干扰素产生细胞的重新程序化或诱导因子。
26.在一个实施方案中,为了更好的结果,本公开内容的转录因子可以用作选自多能干细胞、多潜能干细胞或分化的细胞、及其混合物的细胞向树突细胞或i型干扰素产生细胞的重新程序化或诱导因子。
27.在一个实施方案中,为了更好的结果,本公开内容的转录因子可以用作选自肿瘤细胞、癌细胞、及其混合物的细胞向抗原呈递细胞的重新程序化或诱导因子。
28.在一个实施方案中,本公开内容的结果显示,在clec9a报告小鼠中,将pdc用tdtomato荧光蛋白标记,使得该模型适合于筛选pdc诱导因子。irf8已被描述为对cdc1和pdc规范发挥关键作用,并在两个dc子集上高度表达。因此,本发明将irf8与单独的24种候选者中的每一种组合,并在clec9a报告小鼠胚胎成纤维细胞(mef)中进行渐进加性筛选。
29.在一个实施方案中,令人惊讶的是,与spib组合的irf8足以诱导报告物活化。此外,当将irf8和spib与bcl11a、cbfa2t3、creb3l2、ets1、stat1、tcf4、tcf12或tsc22d1组合时,报告物活化的效率令人惊讶地增加。对dc功能而言重要的主要组织相容性复合物(mhc)ii类分子的表达也由基于irf8和irf8+spib的pdc诱导tf的组合诱导。
30.在一个实施方案中,irf8和spib的表达足以诱导造血标志物cd45的表面表达。值得注意的是,当将irf8和spib与ikzf1或ikzf2组合时,cd45的表面表达令人惊讶地增加。
31.在一个实施方案中,在用tlr7和tlr9配体刺激后,irf8和spib能够诱导分泌i型干扰素(即ifn-α和ifn-β)的能力,而不诱导分泌抗炎性il-10的能力,这是pdc特有的表型特性。当将irf8和spib与bcl11a、cbfa2t3、creb3l2、ets1、stat1、tcf4、tcf12或tsc22d1组合时,干扰素分泌进一步增加。用pu.1、irf8和batf3 tf生成的诱导的dc没有显示分泌i型干扰素的能力。
32.在一个实施方案中,在用tlr7和tlr9配体刺激后,irf8和spib能够诱导分泌促炎细胞因子、特别是il-6和tnf-α的能力,这是pdc特有的表型特性。当将irf8和spib与ets1、stat1、tcf12或tsc22d1组合时,细胞因子分泌会进一步增加。
33.在一个实施方案中,在用tlr7和tlr9配体刺激后,irf8和spib能够诱导分泌趋化因子即ccl5和cxcl10的能力,这是pdc特有的表型特性。当将irf8和spib与hoxa5、stat1、tcf12或tsc22d1组合时,趋化因子分泌进一步增加。
34.本发明主题的一个方面涉及一种组合物,其包含至少两种转录因子的组合,所述转录因子由分离的或合成的序列编码,所述序列与来自由转录因子组成的列表的序列具有至少90%同一性,所述转录因子选自由以下成员组成的列表:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、ikzf1(seq.id.23,seq.id.24)、stat1(seq.id.45,seq.id.46)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、tsc22d1(seq.id.47,seq.id.48)、及其混合物;
35.所述组合物用于在受试者中将干细胞或分化的细胞或其混合物重新程序化成浆细胞样树突细胞或干扰素产生细胞或抗原呈递细胞,优选浆细胞样树突细胞或i型干扰素产生细胞。
36.本发明主题的一个方面涉及包含至少两种转录因子irf8和spib的组合物,所述组合物用于在受试者中将干细胞或分化的细胞或其混合物重新程序化成浆细胞样树突细胞或i型干扰素产生细胞。
37.在一个实施方案中,本公开内容的组合物包含如本文所述的至少两种转录因子,前提条件是,至少两种转录因子(其可以是分离的或合成的转录因子)的组合不是tcf4(seq.id.41,seq.id.42)和irf8(seq.id.1,seq.id.2)。
38.在一个实施方案中,本公开内容的组合物进一步包含一种或多种选自以下的转录因子:arid5a、bcl11a、cbfa2t3、creb3l2、ets1、ikzf1、stat1、tcf4、tcf12和tsc22d1,优选bcl11a、cbfa2t3、creb3l2、ets1、ikzf1、tcf4、tcf12和tsc22d1。
39.在一个实施方案中,本公开内容的组合物可以包含至少两种转录因子的组合,所述转录因子由分离的或合成的序列编码,所述序列与来自选定的tf的序列具有至少95%同
一性,优选96%、97%、98%、99%或同一性,所述选定的tf选自:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、ikzf1(seq.id.23,seq.id.24)、stat1(seq.id.45,seq.id.46)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、tsc22d1(seq.id.47,seq.id.48)、及其混合物。
40.在本公开内容的一个实施方案中,所述转录因子与选自以下的序列具有至少90%同一性,优选91%、92%、93%、94%、95%、96%、97%、98%、99%或同一性:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、ikzf1(seq.id.23,seq.id.24)、stat1(seq.id.45,seq.id.46)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.x,seq.id.x)、tsc22d1(seq.id.47,seq.id.48)、及其混合物。
41.在一个实施方案中,本公开内容的组合物可以包含选自以下组合的转录因子的组合:
42.irf8(seq.id.1,seq.id.2)和spib(seq.id.3,seq.id.4);
43.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和arid5a(seq.id.5,seq.id.6);
44.irf8(seq.id.1,seq.id.2)、spib(seq.id.5,seq.id.6)和bcl11a(seq.id.7,seq.id.8);
45.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和cbfa2t3(seq.id.9,seq.id.10);
46.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和creb3l2(seq.id.11,seq.id.12);
47.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和ets1(seq.id.13,seq.id.14);
48.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和ikzf1(seq.id.23,seq.id.24);
49.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和stat1(seq.id.45,seq.id.46);
50.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tcf4(seq.id.41,seq.id.42);
51.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tcf12(seq.id.43,seq.id.44);
52.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tsc22d1(seq.id.47,seq.id.48),及其混合物。
53.在一个实施方案中,本公开内容的组合物可以包含选自以下组合的转录因子的组合:
54.irf8和spib;
55.irf8、spib和arid5a;
56.irf8、spib和bcl11a;
57.irf8、spib和cbfa2t3;
58.irf8、spib和creb3l2;
59.irf8、spib和ets1;
60.irf8、spib和ikzf1;
61.irf8、spib和stat1;
62.irf8、spib和tcf4;
63.irf8、spib和tcf12;
64.irf8、spib和tsc22d1;及其混合物。
65.在一个实施方案中,本公开内容的组合物可以包含转录因子的组合,其中所述组合是irf8(seq.id.1,seq.id.2)和spib(seq.id.3,seq.id.4),或irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tcf12(seq.id.43,seq.id.44)。
66.在一个实施方案中,本公开内容的组合物可以包含转录因子的组合,其中所述组合是irf8、spib和tcf12。
67.在一个实施方案中,本公开内容的组合物可以包含转录因子的组合,其中所述组合是irf8、spib和tsc22d1。
68.在一个实施方案中,本公开内容的组合物可以包含多能干细胞或多潜能干细胞、分化的细胞、及其混合物。
69.在一个实施方案中,本公开内容的组合物可以用作选自肿瘤细胞、癌细胞、及其混合物的细胞向i型干扰素产生细胞的重新程序化或诱导因子。
70.在一个实施方案中,本公开内容的组合物可以用作pdc的重新程序化或诱导因子,其中所述抗原是:癌症抗原、自体抗原、变应原、来自病原性和/或感染性生物体的抗原。
71.在一个实施方案中,通过使用本公开内容的转录因子的组合所得到的细胞具有对tlr7和tlr9刺激做出应答的能力,和/或所述细胞具有分泌i型干扰素细胞因子即ifn-α和ifn-β的能力。
72.本公开内容的另一个方面涉及本公开内容的组合物在兽医或人医学中的用途,特别是在免疫疗法中的用途,或在神经变性或老化疾病中的用途,或在癌症中的用途,或在感染性疾病中的用途,或作为药物筛选的用途。
73.本公开内容的另一个方面涉及本公开内容的组合物在癌症的诊断、疗法或治疗、抗病毒免疫应答和免疫病理学中的用途,特别是在自身免疫性疾病和免疫缺陷病况中的用途。
74.在一个实施方案中,所述多能干细胞、多潜能干细胞或分化的细胞是哺乳动物多能干细胞、多潜能干细胞或分化的细胞,特别是小鼠或人细胞。
75.在一个实施方案中,本公开内容的组合物可以用在感染性疾病、病毒性疾病或病毒诱导的疾病的治疗、疗法或诊断中。
76.在一个实施方案中,本公开内容的组合物可以用作抗病毒剂或免疫原性组合物。
77.本公开内容的另一个方面涉及一种构建体或载体,其编码在本公开内容中描述的至少两种分离的转录因子的组合,优选编码三种转录因子的组合,更优选四种转录因子的
组合。
78.在一个实施方案中,至少两种分离的转录因子的组合从5’至3’具有以下序列顺序:
79.spib(seq.id.3,seq.id.4)和irf8(seq.id.1,seq.id.2);
80.irf8(seq.id.1,seq.id.2)和spib(seq.id.3,seq.id.4);
81.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和arid5a(seq.id.5,seq.id.6);
82.spib(seq.id.5,seq.id.6)、irf8(seq.id.1,seq.id.2)和bcl11a(seq.id.7,seq.id.8);
83.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和cbfa2t3(seq.id.9,seq.id.10);
84.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和creb3l2(seq.id.11,seq.id.12);
85.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和ets1(seq.id.13,seq.id.14);
86.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和ikzf1(seq.id.23,seq.id.24);
87.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和stat1(seq.id.45,seq.id.46);
88.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tcf4(seq.id.41,seq.id.42);
89.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tcf12(seq.id.43,seq.id.44);
90.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tsc22d1(seq.id.47,seq.id.48)。
91.本公开内容的另一个方面涉及一种构建体或载体,其编码在本公开内容中描述的至少两种分离的转录因子的组合,优选编码三种转录因子的组合,其中所述至少两种分离的转录因子的组合从5’至3’具有以下序列顺序:
92.spib(seq.id.3,seq.id.4)和irf8(seq.id.1,seq.id.2);
93.irf8(seq.id.1,seq.id.2)和spib(seq.id.3,seq.id.4);
94.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和arid5a(seq.id.5,seq.id.6);
95.spib(seq.id.5,seq.id.6)、irf8(seq.id.1,seq.id.2)和bcl11a(seq.id.7,seq.id.8);
96.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和cbfa2t3(seq.id.9,seq.id.10);
97.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和creb3l2(seq.id.11,seq.id.12);
98.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和ets1(seq.id.13,
seq.id.14);
99.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和ikzf1(sed.id.23,seq.id.24);
100.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和stat1(seq.id.45,seq.id.46);
101.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tcf4(seq.id.41,seq.id.42);
102.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tcf12(seq.id.43,seq.id.44);
103.spib(seq.id.3,seq.id.4)、irf8(seq.id.1,seq.id.2)和tsc22d1(seq.id.47,seq.id.48)。
104.在一个实施方案中,所述载体是病毒载体;特别是逆转录病毒、腺病毒、慢病毒、疱疹病毒、痘病毒、副粘病毒、棒状病毒、甲病毒、黄病毒或腺相关病毒载体。
105.在一个实施方案中,所述载体或构建体是合成的mrna、裸甲病毒rna复制子或裸黄病毒rna复制子。
106.在本公开内容的一个方面,一种或多种载体包含编码至少两种转录因子irf和spib的至少两种多核苷酸序列,其用于在受试者中将干细胞或分化的细胞或其混合物重新程序化成浆细胞样树突细胞或i型干扰素产生细胞。
107.在本公开内容的一个实施方案中,所述一种或多种载体进一步编码一种或多种选自以下的转录因子:arid5a、bcl11a、cbfa2t3、creb3l2、ets1、ikzf1、stat1、tcf4、tcf12和tsc22d1,优选bcl11a、cbfa2t3、creb3l2、ets1、ikzf1、tcf4、tcf12和tsc22d1。
108.在本公开内容的一个实施方案中,一种或多种载体的转录因子各自与选自以下的序列具有至少90%同一性:irf8(seq.id.49,seq.id.50)、spib(seq.id.51,seq.id.52)、arid5a(seq.id.53,seq.id.54)、bcl11a(seq.id.55,seq.id.56)、cbfa2t3(seq.id.57,seq.id.58)、creb3l2(seq.id.59,seq.id.60)、ets1(seq.id.61,seq.id.62)、ikzf1(seq.id.71,seq.id.72)、tcf4(seq.id.89,seq.id.90)、tcf12(seq.id.91,seq.id.92)、stat1(seq.id.93,seq.id.94)和tsc22d1(seq.id.95,seq.id.96)。
109.在本公开内容的一个实施方案中,所述一种或多种载体的转录因子的组合选自以下组合:
110.irf8和spib;
111.irf8、spib和arid5a;
112.irf8、spib和bcl11a;
113.irf8、spib和cbfa2t3;
114.irf8、spib和creb3l2;
115.irf8、spib和ets1;
116.irf8、spib和ikzf1;
117.irf8、spib和stat1;
118.irf8、spib和tcf4;
119.irf8、spib和tcf12;和
120.irf8、spib和tsc22d1。
121.在本公开内容的一个实施方案中,所述一种或多种载体的转录因子的组合是irf8、spib和tcf12的组合。
122.在本公开内容的一个实施方案中,所述一种或多种载体的转录因子的组合是irf8、spib和tsc22d1的组合。
123.在本公开内容的一个实施方案中,用于使用一种或多种载体进行重新程序化的细胞选自:多能干细胞、多潜能干细胞、分化的细胞、肿瘤细胞、癌症细胞及其混合物。
124.在本公开内容的一个实施方案中,所述一种或多种载体用在兽医或人医学中,特别是在抗病毒免疫应答和免疫病理学的诊断、疗法或治疗中,尤其是自身免疫性疾病和免疫缺陷病况、瘤形成、特别是癌症(即实体或血液学肿瘤)、良性肿瘤、恶性肿瘤、早期癌症、基底细胞癌、宫颈发育不良、软组织肉瘤、生殖细胞肿瘤、视网膜母细胞瘤、年龄相关性黄斑变性、霍奇金淋巴瘤、血癌、前列腺癌、卵巢癌、子宫颈癌、子宫癌、阴道癌、乳腺癌、鼻咽癌、气管癌、喉癌、支气管癌、细支气管癌、肺癌、中空器官癌、食管癌、胃癌、胆管癌、肠癌、结肠癌、结肠直肠癌、直肠癌、膀胱癌、输尿管癌、肾癌、肝癌、胆囊癌、脾癌、脑癌、淋巴系统癌症、骨癌、胰腺癌、白血病、皮肤癌或骨髓瘤、感染性疾病、病毒性疾病或病毒诱导的疾病、中枢和周围神经系统病症、真菌性、病毒性、衣原体性、细菌性、纳米细菌性或寄生性感染性疾病或病毒性疾病或病毒诱导的疾病的诊断、疗法或治疗中,用作抗病毒剂或用作免疫原性组合物,免疫疗法,或在神经变性疾病的治疗或疗法中,在癌症的治疗或疗法中,或在感染性疾病的治疗或疗法中,真皮内和透皮疗法中,hiv、sars冠状病毒感染、亚洲流感病毒、单纯疱疹、流感病毒、带状疱疹、肝炎、人乳头瘤病毒、爱泼斯坦-巴尔病毒、人嗜t淋巴细胞病毒或病毒性肝炎、淀粉样蛋白疾病、尤其是淀粉样蛋白a淀粉样变性、阿尔茨海默氏病、轻链(al)淀粉样变性、2型糖尿病、甲状腺管道样癌、帕金森病、多神经病或海绵状脑病-creutzfeldt jakob疾病的治疗或疗法中,或用于药物筛选。
125.本公开内容的另一个方面涉及一种用于将细胞重新程序化或诱导成浆细胞样树突细胞或i型干扰素产生细胞的方法,所述方法包括下述步骤:
126.用一种或多种载体转导选自干细胞或分化的细胞、及其混合物的细胞,所述载体包含至少两种核酸序列,所述核酸序列编码与选自以下的序列具有至少90%同一性、优选至少95%同一性的序列:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、ikzf1(seq.id.23,seq.id.24)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、stat1(seq.id.45,seq.id.46)、tsc22d1(seq.id.47,seq.id.48)、及其混合物;
127.在细胞培养基中培养转导的细胞,所述细胞培养基支持浆细胞样树突细胞或i型干扰素产生细胞的生长。
128.本公开内容的另一个方面涉及用于将细胞重新程序化或诱导成浆细胞样树突细胞或i型干扰素产生细胞的体外方法,所述方法包括下述步骤:
129.用一种或多种载体转导选自干细胞或分化的细胞、及其混合物的细胞,所述载体包含至少两种转录因子irf8和spib,
130.在细胞培养基中培养转导的细胞,所述细胞培养基支持浆细胞样树突细胞或i型
干扰素产生细胞的生长。
131.在一个实施方案中,所述序列选自以下组合
132.irf8(seq.id.1,seq.id.2)和spib(seq.id.3,seq.id.4);
133.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和arid5a(seq.id.5,seq.id.6);
134.irf8(seq.id.1,seq.id.2)、spib(seq.id.5,seq.id.6)和bcl11a(seq.id.7,seq.id.8);
135.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和cbfa2t3(seq.id.9,seq.id.10);
136.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和creb3l2(seq.id.11,seq.id.12);
137.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和ets1(seq.id.13,seq.id.14);
138.irf8(seq.id.1,seq.id.2,spib(seq.id.3,seq.id.4)和ikzf1(seq.id.23,seq.id.24);
139.irf8(seq.id.1,seq.id.2,spib(seq.id.3,seq.id.4)和stat1(seq.id.45,seq.id.46);
140.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tcf4(seq.id.41,seq.id.42);
141.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tcf12(seq.id.43,seq.id.44);
142.irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)和tsc22d1(seq.id.47,seq.id.48),及其混合物。
143.在一个实施方案中,所述序列选自以下组合:
144.irf8和spib;
145.irf8、spib和arid5a;
146.irf8、spib和bcl11a;
147.irf8、spib和cbfa2t3;
148.irf8、spib和creb3l2;
149.irf8、spib和ets1;
150.irf8、spib和ikzf1;
151.irf8、spib和stat1;
152.irf8、spib和tcf4;
153.irf8、spib和tcf12;
154.irf8、spib和tsc22d1,及其混合物。
155.在一个实施方案中,所述方法可以包括将转导的细胞培养至少2天、优选至少5天、更优选至少8天、甚至更优选至少9天的步骤。
156.在一个实施方案中,所述转导步骤进一步包含至少一种载体,其选自:编码il-12的核酸序列;编码il-4的核酸序列;编码ifn-α的核酸序列;编码ifn-β的核酸序列;编码
ifn-γ的核酸序列;编码tnf的核酸序列;编码gm-csf的核酸序列;编码靶向il-10rna的sirna的核酸序列,及其混合物。
157.在一个实施方案中,所述转导步骤进一步包含至少一种载体,所述载体包含编码免疫刺激性细胞因子的核酸。
158.在一个实施方案中,所述细胞选自:多能干细胞、多潜能干细胞或分化的细胞、及其混合物;特别是哺乳动物细胞。
159.在一个实施方案中,所述多能干细胞、多潜能干细胞或分化的细胞选自:内胚层衍生的细胞、中胚层衍生的细胞、外胚层衍生的细胞、多潜能干细胞,包括间质干细胞、造血干细胞、肠干细胞、多能干细胞和细胞系。
160.在一个实施方案中,所述细胞是人的或非人的。在另一个实施方案中,所述细胞是小鼠细胞。
161.本公开内容的另一个方面涉及通过在本公开内容中描述的体外方法得到的诱导的浆细胞样树突细胞或i型干扰素产生细胞或抗原呈递细胞,优选诱导的浆细胞样树突细胞或i型干扰素产生细胞。
162.本公开内容的另一个方面涉及一种组合物,其包含治疗有效量的在本公开内容中描述的浆细胞样树突细胞或i型干扰素产生细胞或抗原呈递细胞,优选诱导的浆细胞样树突细胞或i型干扰素产生细胞,和药学上可接受的赋形剂。
163.在一个实施方案中,所述组合物可以用在兽医或人医学中。
164.在一个实施方案中,所述组合物可以用在免疫疗法中,或在神经变性疾病的治疗或疗法中,或在癌症的治疗或疗法中,或在感染性疾病的治疗或疗法中。
165.在一个实施方案中,所述组合物可以进一步包含镇痛剂、抗炎剂、化疗剂、放疗剂、抗生素、利尿剂或其混合物。
166.在一个实施方案中,所述组合物可以进一步包含填充剂、粘合剂、崩解剂或润滑剂或其混合物。
167.在一个实施方案中,所述组合物可以用在真皮内和透皮疗法中。
168.在一个实施方案中,所述组合物可以用在可注射制剂、优选原位注射剂中。
169.在一个实施方案中,所述组合物可以用在兽医或人医学中,或在药物筛选中。
170.在一个实施方案中,所述组合物可以用在中枢和周围神经系统病症的治疗、疗法或诊断中。
171.在一个实施方案中,所述组合物可以用在瘤形成、特别是癌症诸如实体或血液学肿瘤的治疗、疗法或诊断中。
172.在一个实施方案中,所述组合物、载体或构建体可以用在良性肿瘤、恶性肿瘤、早期癌症、基底细胞癌、宫颈发育不良、软组织肉瘤、生殖细胞肿瘤、视网膜母细胞瘤、年龄相关性黄斑变性、霍奇金淋巴瘤、血癌、前列腺癌、卵巢癌、子宫颈癌、子宫癌、阴道癌、乳腺癌、鼻咽癌、气管癌、喉癌、支气管癌、细支气管癌、肺癌、中空器官癌、食管癌、胃癌、胆管癌、肠癌、结肠癌、结肠直肠癌、直肠癌、膀胱癌、输尿管癌、肾癌、肝癌、胆囊癌、脾癌、脑癌、淋巴系统癌症、骨癌、胰腺癌、白血病、皮肤癌或骨髓瘤的治疗、诊断或疗法中。
173.在一个实施方案中,所述组合物、载体或构建体可以用在真菌性、病毒性、衣原体性、细菌性、纳米细菌性或寄生性感染性疾病或病毒性疾病或病毒诱导的疾病的治疗、疗法
或诊断中。
174.在一个实施方案中,所述组合物、载体或构建体可以用在hiv、sars冠状病毒感染、亚洲流感病毒、单纯疱疹、流感病毒、带状疱疹、肝炎、人乳头瘤病毒、爱泼斯坦-巴尔病毒、人嗜t淋巴细胞病毒或病毒性肝炎的治疗、疗法或诊断中。
175.在一个实施方案中,所述组合物、载体或构建体可以用在淀粉样蛋白疾病、尤其是淀粉样蛋白a淀粉样变性、阿尔茨海默氏病、轻链(al)淀粉样变性、2型糖尿病、甲状腺管道样癌、帕金森病、多神经病或海绵状脑病诸如creutzfeldt jakob疾病的治疗、疗法或诊断中。
176.本公开内容的另一个方面涉及疫苗或可注射制剂,其包含在本公开内容中描述的组合物、载体或构建体,和/或在本公开内容中描述的诱导的浆细胞样树突细胞或i型干扰素产生细胞,或所描述的抗原呈递细胞,或其混合物。
177.本公开内容的另一个方面涉及一种试剂盒,其包含下述组分中的至少一种:
178.本公开内容的诱导的浆细胞样树突细胞或i型干扰素产生细胞或抗原呈递细胞;
179.在本公开内容中描述的组合物;
180.在本公开内容中描述的一种或多种载体或构建体;或其混合物。
181.本公开内容的另一个方面涉及一种试剂盒,其包含下述组分中的至少一种:
182.本公开内容的诱导的浆细胞样树突细胞或i型干扰素产生细胞;
183.在本公开内容中描述的组合物;
184.在本公开内容中描述的一种或多种载体或构建体;或其混合物。
185.在一个实施方案中,本公开内容提供了当与spib组合时irf8在成纤维细胞中启动pdc程序的证据。这些发现为pdc规范提供了有价值的见解。未来,通过直接重新程序化来产生pdc开辟了用自体工程改造的细胞诱导抗病毒免疫应答的途径。
186.附图描述
187.以下附图提供了用于说明本公开内容的优选实施方案并且不应被视为限制本发明的范围。
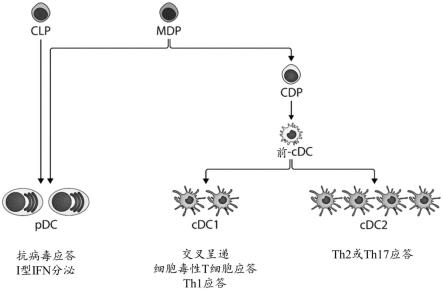
188.图1.树突细胞的主要子集的个体发育。虽然常规树突细胞1型(cdc1)和2型(cdc2)来自于源自常见树突细胞祖细胞(cdp)的前-dc群体,但浆细胞样树突细胞(pdc)可以源自常见淋巴细胞祖细胞(clp)或cdp。pdc作为独特的dc子集出现,该子集在病毒感染后专门产生i型干扰素(ifn)。cdc1在执行交叉呈递、诱导细胞毒性t细胞应答和优先极化t辅助细胞1应答的能力方面表现出色。cdc2在将抗原呈递给t辅助细胞、从而极化t辅助细胞2或17应答方面表现出色。
189.图2.通过直接细胞重新程序化产生pdc或i型干扰素(ifn)产生细胞。观察本发明主题中公开的转录因子(tf)组合对从多能干细胞、多潜能干细胞和体细胞(诸如成纤维细胞)诱导pdc的效果。pdc专门生产i型ifn,并因此将应用于个性化免疫疗法的背景下。诱导的pdc或诱导pdc的tf组合将用于在不同的患病背景(包括病毒感染和癌症)下诱导免疫。
190.图3.clec9a、irf8、tlr7和tlr9的表达限于pdc。显示clec9a、irf8、tlr7和tlr9在pdc和个体发育接近的其它免疫细胞(特别是cdc1和cdc2、巨噬细胞和单核细胞)中的表达水平的热图。从免疫基因组计划(immunological genome project)(www.immgen.com)中可用的数据获得表达概况。
191.图4.诱导pdc的tf候选物。与cdc1和cdc2相比,22种候选tf在pdc中高度富集。显示从免疫基因组计划中可用数据中提取的基因表达概况的热图。
192.图5.clec9a在pdc中表达。tdtomato在92%的从双转基因clec9a-cre x rosa26-停止-tdtomato的脾中分离的pdc(门控为cd11c
低
bst2
+
b220
+
siglec-h
+
细胞)上的表达。
193.图6.与spib组合的irf8诱导clec9a报告物活化。将从双转基因clec9a-tdtomato小鼠分离的小鼠胚胎成纤维细胞(mef)用诱导型慢病毒载体的合并物转导,所述慢病毒载体编码单独的irf8或与另外pdc诱导tf组合的irf8,并在添加dox后5天通过流式细胞计量术进行分析。用单独的irf8或与单一pdc诱导候选tf组合的irf8转导后tdtomato+细胞的定量。包括m2rtta转导的细胞作为对照。
194.图7.诱导的pdc在细胞表面表达抗原呈递分子。在第8天在irf8和spib过表达后产生的tdtomato+细胞的主要组织相容性复合物ii类(mhc-ii)表达的流式细胞计量术分析。
195.图8.另外pdc诱导tf与irf8和spib的组合增加了clec9a报告物活化的效率。用单独的irf8和spib或与各个pdc诱导因子组合的irf8和spib转导双转基因clec9a-tdtomato mef后tdtomato+细胞的定量。在第8天进行流式细胞计量术分析。包括m2rtta转导的细胞作为对照。
196.图9.另外pdc诱导tf与irf8和spib的组合增加了mhc-ii在细胞表面的表达。在第8天,用m2rtta、单独的irf8+spib或与各个pdc诱导因子组合的irf8+spib转导的mef的mhc-ii表达的流式细胞计量术分析。对于tdtomato阴性(tdt-)和阳性(tdt+)群体,显示了mhc-ii水平的定量。
197.图10.诱导的pdc在tlr7和tlr9刺激后分泌i型干扰素。用m2rtta、pib(pu.1、irf8和batf3)、单独的irf8+spib或者与arid5a、bcl11a、cbfa2t3、ets1、hoxa5、tcf4和tcf12组合的irf8+spib转导mef,并在添加多西环素后第9天分选tdtomato+细胞。将纯化的tdtomato+细胞与tlr7(r848)和tlr9(cpg odn 1668)一起温育过夜,并使用细胞计量术珠子阵列对上清液定量ifn-α(a)、ifn-β(b)和il-10(c)细胞因子分泌。
198.图11.诱导pdc的另外tf候选物。当与cdc1和cdc2相比时,stat1(a)和tsc22d1(b)在pdc中富集。从免疫基因组计划中可用的数据中提取的基因表达概况。
199.图12.另外pdc诱导tf与irf8和spib的组合增加了clec9a报告物活化和mhc-ii表面表达的效率。用m2rtta(m2)、单独的irf8+spib或者与stat1或tsc22d1组合的irf8+spib转导的mef的(a)clec9a报告物活化和(b)mhc-ii表达的流式细胞计量术分析。在第5天进行流式细胞计量术分析。包括m2rtta转导的细胞作为对照。
200.图13.诱导的pdc在tlr7和tlr9刺激后分泌i型干扰素。将mef用m2rtta、单独的irf8+spib或者与stat1和tsc22d1组合的irf8+spib转导,并在添加多西环素后第9天分选tdtomato+细胞。将纯化的tdtomato+细胞与tlr7(r848)和tlr9(cpg odn 1668)的触发剂一起温育过夜,并使用细胞计量术珠子阵列对上清液定量ifn-α(a)、ifn-β(b)和il-10(c)细胞因子分泌。
201.图14.诱导的pdc在细胞表面表达cd45。在第5天,用m2rtta、pib(pu.1、irf8和batf3)、单独的irf8+spib或与单独pdc诱导tf组合的irf8+spib转导的mef的cd45表达的流式细胞计量术分析。包括m2rtta(m2)转导的细胞作为对照。
202.图15.诱导的pdc在tlr7和tlr9刺激后分泌促炎细胞因子和趋化因子。将mef用
m2rtta、单独的irf8+spib或与arid4a、bcl11a、cbfa2t3、ets1、hoxa5、stat1、tcf4、tcf12和tsc22d1组合的irf8+spib转导,并在添加多西环素后第9天分选tdtomato+细胞。将纯化的tdtomato+细胞与tlr7(r848)和tlr9(cpg odn 1668)一起温育过夜,并使用细胞计量术珠子阵列对上清液定量il-6(a)、tnf-α(b)、ccl5(c)和cxcl10(d)细胞因子分泌。
203.详细描述
204.本公开内容涉及用于将细胞重新程序化成pdc或i型干扰素产生细胞的组合物、核酸构建体、载体、方法及其试剂盒。目的是通过引入和表达分离的/合成的转录因子,从分化的、多潜能或多能干细胞产生具有诱导抗病毒和抗肿瘤应答能力的pdc和i型干扰素产生细胞。更具体地,本公开内容提供了用于通过用特定转录因子的组合的惊人使用进行直接细胞重新程序化而得到pdc或i型干扰素产生细胞的方法。
205.天然dc是接种在所有组织中的骨髓衍生的细胞。dc准备好对环境进行采样并将收集到的信息传输给适应性免疫系统的细胞(t细胞和b细胞)。在抗原吞噬后,dc通过将处理过的抗原(以肽-主要组织相容性复合物(mhc)分子复合物的形式)呈递给淋巴组织中的原初(也就是说,未经历过抗原的)t细胞来启动免疫应答。dc可以分为2个主要子集:浆细胞样dc(pdc),以及可以进一步细分为cdc 1型(cdc1)和2型(cdc2)的常规或经典dc(cdc)(图1)。pdc的典型特征是圆形形态和低水平mhc-ii的表达,所述mhc-ii在活化后上调。在活化后,pdc通常过表达共刺激分子和mhc分子,此外还会分泌负责启动和/或增强许多t和b淋巴细胞应答的各种细胞因子和趋化因子,即肿瘤坏死因子(tnf)-α、ifn-α、ifn-β、il-12、il-6和趋化因子诸如ccl5和cxcl10。pdc表达高水平的核酸感知toll-样受体(tlr)tlr7和tlr9。tlr7或tlr9刺激允许pdc对病原体衍生的核酸的检测和大量i型干扰素(即ifn-α和ifn-β)的产生。尽管活化的pdc可以活跃地产生细胞因子并执行抗原呈递和交叉呈递,但仍不清楚这些功能特征是由相同的细胞执行还是由不同的功能特化pdc子集执行。通常通过其对主要组织相容性复合物ii类分子(mhc-ii)、共刺激分子(诸如cd80/86和cd40)和整联蛋白cd11c的高表达以及它们从非淋巴样器官迁移到淋巴样器官并刺激原初t细胞的优异能力来鉴定cdc。dngr-1(也被称作clec9a)是坏死细胞的受体,其有利于小鼠中对死细胞相关抗原的细胞毒性t淋巴细胞应答(ctl)的交叉引发。dngr-1由小鼠cdc1、cdc2和pdc选择性地高水平表达,负责识别细胞死亡后暴露的细胞内配体。近年来,显示clec9a的表达允许鉴定定型为常规或浆细胞样dc谱系及其在淋巴组织中的后代的dc前体(cdp)(schraml等人,2015)。
206.如本文所述,能够将分化的细胞重新程序化为诱导的pdc的pdc诱导因子的成功鉴定可以以多种方式促进我们对pdc生物学的基本理解。这项工作将提供对pdc最小转录网络的深入洞察。此外,pdc诱导因子的鉴定为理解pdc状态如何建立以及关键调节机制如何实施提供了前所未有的机会。
207.转录因子(tf)在发育期间所有细胞类型的规范中都发挥着关键作用。使用tf介导的重新程序化的直接重新程序化策略的成功表明,使用这样的因子将多能es/ips细胞或多潜能干细胞的分化引导至特定命运是同样似乎合理的。因此,使用本文鉴定的pdc诱导因子,可以实现通过dc富集的tf的表达将es/ips细胞定向分化为确定的dc命运。此外,使用本文鉴定的pdc诱导因子,可以实现通过dc富集的tf的表达将多潜能造血干细胞和祖细胞定向分化为确定的dc命运。
208.通常,使用病毒载体或不使用病毒载体,通过一次或重复的转导或转染,将编码pdc诱导因子的核酸(例如,dna或rna或其构建体)引入细胞中,并且基因产物的表达和/或rna分子的翻译产生在形态学上、在生物化学上和在功能上与pdc相似的细胞,如本文中所述。在用适当的抗原引发后,这些诱导的pdc能够将它们捕获、处理并呈递给免疫系统的效应细胞(巨噬细胞、t-细胞、b-细胞、nk细胞)并分泌i型ifn,从而引发针对病毒感染和癌症的抗原特异性免疫应答(图2)。
209.本公开内容的一个方面是在癌细胞(原位或离体)中使用tf或使用tf的组合以迫使它们分泌i型ifn、将它们自己的抗原呈递给免疫细胞并分泌在肿瘤微环境内的其它促炎细胞因子和化学引诱物。这种方法代表了一种可行的策略以增加抗癌免疫疗法的临床结果,因为它绕过了癌症逃避机制并增加了肿瘤免疫原性。
210.当与cdc1和cdc2以及其它相关的单核细胞相比时,浆细胞样dc特异性地表达tlr7和tlr9(图3)。tlr7和trl9受体允许pdc感知病毒dna并通过分泌i型ifn做出应答。浆细胞样dc、以及cdc1表达clec9a和irf8。
211.在一个实施方案中,选择了22种候选tf,这是由于当与cdc1和cdc2相比时它们在浆细胞样dc中的特异性富集基因表达(图4)。将22种候选tf单独克隆到重新程序化验证的多西环素(dox)诱导型慢病毒载体中。
212.在一个实施方案中,为了通过细胞重新程序化筛选pdc诱导tf和pdc诱导tf组合的效果,使用携带dc-特异性报告物(clec9a-cre x r26-停止-tdtomato)的小鼠胚胎成纤维细胞(mef)来筛选pdc诱导tf的活化dc-特异性的clec9a-tomato报告物的能力(图4)。在clec9a-tomato报告小鼠中,tdtomato荧光蛋白仅由cdp、前-dc、cdc和pdc表达(schraml等人,2015)。在培养中的巨噬细胞、其它免疫谱系或单核细胞衍生的dc不表达clec9a,且因此不会活化报告物或tdtomato蛋白的表达(图3)。分析了从clec9a报告物小鼠分离的脾细胞,证实92.4%的pdc细胞(在cd11c
低
bst2
+
b220
+
siglech
+
细胞中门控)表达tdtomato荧光蛋白(图5)。
213.从e13.5胚胎分离出双转基因clec9a-tdtomato报告物mef,并将其通过荧光活化的细胞分选(facs)排除可能已经定型为造血谱系的任何污染性tdtomato+或cd45+细胞。
214.在一个实施方案中,spib和irf8足以活化clec9a。
215.在一个实施方案中,将clec9a报告物mef用单独的irf8或2种与irf8加上其它21种候选tf之一的组合进行转导,并评价tdtomato表达。在单独使用2种候选tf或irf8的21种组合转导后,在添加dox后5天观察到tdtomato+细胞的出现(图6)。irf8和spib的组合产生了5%的tdtomato+细胞,从而提示,irf8和spib是诱导报告物活化所需的最小因子组合。在用对照m2rtta载体转导后,没有检测到tdtomato+细胞,用单独的irf8也没有检测到。
216.在一个实施方案中,抗原呈递细胞标志物mhc-ii在大约60%的用irf8和spib转导的mef中表达(图7)。
217.在一个实施方案中,评价了与irf8和spib一起表达剩余20种候选tf的影响(图8)。从测试的20种tf观察到,hhex、id3、mef2c和runx2对生成的tdtomato+细胞的数目产生负面影响。arid5a、hdac5、hoxa5、ikzf1、ikzf2、ikzf3、ikzf5、irf7、myb和stat3的添加没有影响生成的tdtomato+细胞的数目。bcl11a、cbfa2t3、creb3l2、ets1、tcf12和tcf4的添加对产生的tdtomato+细胞的数目产生积极影响,从而提高了报告物活化效率。
218.在一个实施方案中,评价了clec9a-tdtomato报告物的活化是否反映在mhc-ii(抗原呈递机制的一种关键组分)的表面表达中。值得注意的是,观察到在第8天tdtomato+细胞在表面表达mhc-ii(图9)。
219.在一个实施方案中,除了mhc-ii表面分子之外,pdc还分泌具有促炎功能的细胞因子,其对于t-细胞应答的发展而言是重要的。这些应答可以通过触发至少11种不同的toll-样受体(tlr)来启动,从而允许特异性识别不同的保守微生物或病毒结构。在dc隔室内,pdc特异性地对tlr7和tlr9触发做出响应(图3)。研究了当用tlr7(使用瑞喹莫德或r848)和tlr9(使用odn 1668)刺激攻击时,诱导的pdc是否向培养基分泌细胞因子(图10)。在诱导的pdc的tlr攻击后,当将每种tf组合产生的经刺激的细胞与非刺激细胞进行对比时,观察到用以下tf重新程序化的tdtomato+细胞对ifn-α的分泌的增加:irf8和spib(16.6倍);irf8、spib和arid5a(3.9倍);irf8、spib和bcl11a(14.8倍);irf8、spib和cbfa2t3(3.5倍);irf8、spib和ets1(3.7倍);irf8、spib和tcf4(3.6倍);irf8、spib和tcf12(8.3倍);和irf8、spib和hoxa5(7.7倍)。诱导的pdc的tlr攻击也增加了用以下tf重新程序化的tdtomato+细胞对ifn-β的分泌:irf8和spib(1.5倍);irf8、spib和arid5a(2.3倍);irf8、spib和bcl11a(2.3倍);irf8、spib和cbfa2t3(1.9倍);irf8、spib和ets1(1.6倍);irf8、spib和tcf4(1.3倍);irf8、spib和tcf12(1.9倍);和irf8、spib和hoxa5(2.6倍)。在诱导的pdc的tlr刺激后,没有观察到抗炎细胞因子il-10的分泌增加。重要的是,用tf的pu.1、irf8和batf3(pib)组合转导后获得的tdtomato+细胞对tlr7和tlr9没有应答,并且不分泌ifn-α和ifn-β。总之,这些数据表明,通过将clec9a报告物活化与干扰素分泌能力相组合,我们成功地鉴定了能够通过直接细胞重新程序化诱导pdc或i型干扰素分泌细胞的tf组合。
220.在一个实施方案中,由于与cdc1和cdc2相比它们在浆细胞样dc中特异性富集基因表达,因此选择了两种另外候选tf:stat1和tsc22d1(图11)。这两种tf分别克隆在相同的重新程序化证明的多西环素(dox)诱导型慢病毒载体中,并与irf8和spib联合测试以了解它们诱导clec9a-tdtomato报告物活化的能力(图12)。令人感兴趣的是,与单独的irf8和spib相比,stat1或tsc22d1向irf8和spib组合的添加增加了clec9a报告物活化(图12a)。由irf8、spib和stat1以及irf8、spib和tsc22d1产生的诱导的pdc也在细胞表面表达mhc-ii分子(图12b),从而支持pdc命运的获得。
221.在一个实施方案中,将诱导的pdc用tlr7/9攻击,此时观察到与由irf8和spib产生的诱导的pdc相比,用irf8、spib和stat1(1.3倍)以及irf8、spib和tsc22d1(4.8倍)重新程序化的tdtomato+细胞对ifn-α的分泌增加(图13a)。与irf8和spib诱导的细胞相比,stat1或tsc22d1的添加也增加了用irf8、spib和stat1(1.3倍)以及irf8、spib和tsc22d1(4.1倍)重新程序化的tdtomato+细胞对ifn-β的分泌(图13b)。由irf8、spib和stat1、以及irf8、spib和tsc22d1产生的诱导的pdc不能分泌抗炎细胞因子il-10。这些数据支持irf8、spib和stat1、以及irf8、spib和tsc22d1能够诱导朝向诱导的pdc命运的重新程序化和分泌i型干扰素的能力。
222.在一个实施方案中,造血标志物cd45的表面表达也是pdc的一个显著特征。研究了pdc诱导因子的组合是否能够诱导cd45的表面表达。cd45在1.79
±
0.33%的用irf8和spib产生的诱导pdc中表达。令人惊讶的是,如果将ikzf1与irf8和spib组合,cd45+群体增加直到10.16
±
0.91%(5.6倍增加)。
223.在一个实施方案中,在pdc中tlr7和tlr9对病毒或自身核酸的识别诱导了两种旁路途径,这取决于tlr7和tlr9遇到它们的配体时所在的隔室的类型。myd88-irf7途径导致i型干扰素分泌,而myd88-nf-κb途径导致促炎细胞因子和趋化因子的产生。然后研究了在tlr7/9刺激后,诱导的pdc是否分泌另外的细胞因子(图15)。事实上,经纯化的由irf8和spib的过表达产生的tdtomato+细胞分泌促炎细胞因子il-6和tnf-α和趋化因子ccl5和cxcl10。重要的是,stat1、tcf12或tsc22d1向irf8和spib组合的添加以tlr依赖性的方式增加了il-6、tnf-α、ccl5和cxcl10的分泌。诱导的pdc的tlr攻击增加了用irf8、spib和stat1(5.6倍)、irf8、spib和tcf12(7.5倍)以及irf8、spib和tsc22d1(3.5倍)重新程序化的tdtomato+细胞对il-6的分泌,而对于tnf-α观察到类似的增加(分别为1.8、3.1、1.3倍)。用irf8、spib和stat1(2.5倍)、irf8、spib和tcf12(3.1倍)以及irf8、spib和tsc22d1(2.4倍)重新程序化的tdtomato+细胞对趋化因子ccl5的分泌在tlr攻击后增加。至于cxcl10,由irf8、spib和tcf12、以及irf8、spib和tsc22d1的过表达产生的诱导的pdc在tlr刺激后也将它们的分泌分别增加了2.8和1.7倍。总之,该数据支持我们成功地鉴定足以在不相关细胞类型中诱导pdc的tf组合,它们能够通过两种细胞内途径对tlr7和9刺激作出应答,从而导致i型干扰素分泌和促炎细胞因子和趋化因子。
224.在一个实施方案中,将每种候选tf的编码区单独克隆到诱导型慢病毒pfuw-teto载体中,其中tf的表达是在四环素操纵子和最小cmv启动子的控制下。组合使用先前描述的含有在组成活性的人泛素c启动子的控制下的反向四环素反式激活因子m2rtta的慢病毒载体(fuw-m2rtta)。用编码tf的质粒、包装构建体和vsv-g包膜蛋白的混合物转染人胚胎肾(hek)293t细胞。在36、48和60小时后收获病毒上清液,过滤(0.45μm,corning)并新鲜使用或用amicon超离心过滤器(millipore)浓缩40倍。
225.在一些实施方案中,与由序列表中提供的序列所编码的参考多肽具有相同或类似活性的多肽变体或家族成员可以用在本文所述的组合物、方法和试剂盒中。通常,用于本文所述的组合物、方法和试剂盒中的编码pdc诱导因子的特定多肽的变体将与该特定参考多核苷酸或多肽具有至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或更多序列同一性,如通过本文描述的和本领域技术人员已知的序列比对程序和参数所确定的。
226.在一个实施方案中,智人干扰素调节因子8(irf8)、mrna(seq.id.1)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
227.在一个实施方案中,智人spi-b(spib)、mrna(seq.id.3)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
228.在一个实施方案中,智人at富集相互作用结构域5a(arid5a)、mrna(seq.id.5)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
229.在一个实施方案中,智人baf染色质重塑复合物亚基(bcl11a)、mrna(seq.id.7)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
230.在一个实施方案中,智人cbfa2/runx1配偶体转录辅阻遏物3(cbfa2t3)、mrna(seq.id.9)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
231.在一个实施方案中,智人camp应答元件结合蛋白3样2(creb3l2)、mrna(seq.id.11)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
232.在一个实施方案中,智人ets原癌基因1(ets1)、mrna(seq.id.13)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
233.在一个实施方案中,智人同源框a5(hoxa5)、mrna(seq.id.19)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
234.在一个实施方案中,智人ikaros家族锌指1(ikzf1)、mrna(seq.id.23)和优化的密码子,或编码相同氨基酸的不同密码子,自然考虑被对本文所述的核酸的提及涵盖。
235.在一个实施方案中,智人信号转导蛋白和转录活化剂1(stat1)、mrna(seq.id.45)和优化的密码子,或编码相同氨基酸的不同密码子,自然考虑被对本文所述的核酸的提及涵盖。
236.在一个实施方案中,智人转录因子4(tcf4)、mrna(seq.id.41)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
237.在一个实施方案中,智人转录因子12(tcf12)、mrna(seq.id.43)和优化的密码子,或编码相同氨基酸的不同密码子,自然也考虑被对本文所述的核酸的提及涵盖。
238.在一个实施方案中,智人tsc22结构域家族蛋白1(tsc22d1)、mrna(seq.id.47)和优化的密码子,或编码相同氨基酸的不同密码子,自然考虑被对本文所述的核酸的提及涵盖。
239.在本文提供的组合物、载体、构建体、方法和试剂盒的一些实施方案中,被使用或被选择从起始体细胞(诸如成纤维细胞或造血谱系细胞、多潜能干细胞、诱导的多能干细胞、癌症或肿瘤细胞)产生pdc的pdc诱导因子的数目是至少两种。在一些实施方案中,被使用或被选择的pdc诱导因子的数目是至少3种、至少4种、至少5种、至少6种、至少7种、至少8种、至少9种、至少10种、至少11种、至少12种、至少13种、至少14种、至少15种、至少16种、至少17种、至少18种、至少19种、至少20种、至少30种、至少33种、至少35种、至少40种或更多种。
240.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,将编码pdc诱导因子诸如irf8、spib、arid5a、bcl11a、cbfa2t3、creb3l2、ets1、hoxa5、izkf1、tcf4、tcf12和tsc22d1的核酸序列或构建体插入或可操作地连接到合适的表达载体中,用于使用标准的分子生物学技术转染细胞。本文中使用的“载体”表示核酸分子,诸如为插入的核苷酸序列提供有用的生物学或生化特性的dsdna分子,诸如本文所述的核酸构建体或替换盒。例子包括质粒、噬菌体、自主复制序列(ars)、着丝粒和能够在体外或在宿主细胞中复制或被复制、或者将期望的核酸区段运送到宿主细胞内期望位置的其它序列。载体可以具有一个或多个限制性内切核酸酶识别位点(无论是i、ii、iis、iii和iv型),在所述位点处可以以可确定的方式切割序列,而不丧失载体的基本生物学功能,并且可以向其中剪接或插入核酸片段以实现其复制和克隆。载体还可以包含一个或多个重组位点,其允许两个核酸分子之间的核酸序列的交换。载体可以进一步提供引物位点(例如用于pcr)、转录和/或翻译起始和/或调节位点、重组信号、复制子、另外的选择标志物等。载体可以进一步包含一种或多种选择标志物,其适用于鉴定用该载体转化的细胞。
241.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述表达载体是病毒载体。一些病毒介导的表达方法采用逆转录病毒、腺病毒、慢病毒、副粘病毒、棒状病毒、甲病毒、黄病毒、疱疹病毒、痘病毒和腺相关病毒(aav)载体,且这样的表达方法已用于基因递送并且是本领域众所周知的。
242.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述病毒载体是逆转录病毒。逆转录病毒为基因递送提供了方便平台。使用本领域已知的技术,可以将选择的基因插入载体中并包装在逆转录病毒颗粒中。然后可以将重组病毒分离并在体内或离体递送给受试者的靶细胞。已经描述了许多逆转录病毒系统。参见,例如,美国专利号5,219,740;miller和rosman(1989)biotechniques 7:980-90;miller,a.d.(1990)human gene therapy 1:5-14;scarpa等人(1991)virology 180:849-52;burns等人(1993)proc.natl.acad.sci.usa 90:8033-37;boris-lawrie和temin(1993)curr.opin.genet.develop.3:102-09。在本文所述的组合物、载体、方法和试剂盒的一些实施方案中,所述逆转录病毒是复制缺陷的。逆转录病毒载体系统利用以下事实:含有5
′
和3
′
ltr和包装信号的最小载体足以允许载体包装、感染和整合到靶细胞中,前提条件是,病毒结构蛋白在包装细胞系中以反式供给。用于基因转移的逆转录病毒载体的基本优势包括在大多数细胞类型中的有效感染和基因表达、精确的单个拷贝载体向靶细胞染色体dna中的整合以及逆转录病毒基因组的易于操作。
243.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述病毒载体是基于腺病毒的表达载体。与整合到宿主基因组中的逆转录病毒不同,腺病毒在染色体外持续存在,因此将与插入诱变相关的风险降至最低(haj-ahmad和graham(1986)j.virol.57:267-74;bett等人(1993)j.virol.67:5911-21;mittereder等人(1994)human gene therapy 5:717-29;seth等人(1994)j.virol.68:933-40;barr等人(1994)gene therapy 1:51-58;berkner,k.l.(1988)biotechniques 6:616-29;和rich等人(1993)human gene therapy4:461-76)。腺病毒载体感染多种细胞,具有广宿主范围,表现出高感染效率,指导异源基因的高水平表达,并实现那些基因在体内的长期表达。该病毒作为无细胞病毒粒子具有完全感染性,因此不必需注射生产细胞系。就安全性而言,腺病毒与严重的人病理学无关,并且源自该病毒的重组载体可以通过病毒基因组的早期区域1(“e1”)中的缺失而使得复制缺陷。也可以相对容易地大量生产腺病毒。用于本文所述的组合物、载体、方法和试剂盒中的腺病毒载体可以衍生自各种腺病毒血清型中的任一种,包括、但不限于腺病毒的超过40种血清型毒株(诸如血清型2、5、12、40和41)中的任一种。本文使用的腺病毒载体优选地是复制缺陷的并且含有可操作地连接至合适启动子的感兴趣的pdc诱导因子。
244.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,使用一种或多种诱导型慢病毒载体引入或递送编码pdc诱导因子诸如irf8、spib、arid5a、bcl11a、cbfa2t3、ets1、hoxa5、ikzf1、stat1、tcf4、tcf12和tsc22d1的核酸序列。在一些实施方案中,通过使细胞(所述细胞在处于诱导型启动子的控制下或可操作地连接至诱导型启动子的表达载体中具有至少一种pdc诱导因子)与调节剂(例如,多西环素)或其它诱导剂接触,可以实现使用一种或多种诱导型慢病毒载体递送的pdc诱导因子的表达的控制。当使用一些类型的诱导型慢病毒载体时,使这样的细胞与诱导剂接触诱导pdc诱导因子的表达,而调
节剂的撤去抑制表达。当使用其它类型的诱导型慢病毒载体时,调节剂的存在抑制表达,而调节剂的除去允许表达。本文中使用的术语“表达的诱导”表示,在例如诱导剂存在的情况下,或在一种或多种造成基因在细胞中的内源性表达的试剂或因子存在的情况下,基因的表达,诸如由诱导型病毒载体编码的pdc诱导因子的表达。
245.在本文描述的方面的一些实施方案中,使用多西环素(dox)诱导型慢病毒系统。与逆转录病毒不同,慢病毒能够转导静止细胞,使其适合转导更广泛种类的造血细胞类型。例如,pfuw-teto慢病毒系统已被显示以高效转导原代造血祖细胞。
246.在本文所述的方法的一些实施方案中,使用非整合载体(例如,腺病毒)引入或递送编码pdc诱导因子、诸如irf8(seq.id.1、seq.id.2)、spib(seq.id.3、seq.id.4)、arid5a(seq.id.5、seq.id.6)、bcl11a(seq.id.7、seq.id.8)、cbfa2t3(seq.id.9、seq.id.10)、creb3l2(seq.id.11、seq.id.12)、ets1(seq.id.13、seq.id.14)、hdac5(seq.id.15、seq.id.16)、hhex(seq.id.17、seq.id.18)、hoxa5(seq.id.19、seq.id.20)、id3(seq.id.21、seq.id.22)、ikzf1(seq.id.23、seq.id.24)、ikzf2(seq.id.25、seq.id.26)、ikzf3(seq.id.27、seq.id.28)、ikzf5(seq.id.29、seq.id.30)、irf7(seq.id.31、seq.id.32)、mef2c(seq.id.33、seq.id.34)、myb(seq.id.35、seq.id.36)、runx2(seq.id.37、seq.id.38)、stat3(seq.id.39、seq.id.40)、tcf4(seq.id.41、seq.id.42)、tcf12(seq.id.43、seq.id.44)、stat1(seq.id.45、seq.id.46)和tsc22d1(seq.id.47、seq.id.48)的核酸序列。虽然整合载体(诸如逆转录病毒载体)整合到宿主细胞基因组中并可能破坏正常基因功能,但是非整合载体通过染色体外转录控制基因产物的表达。由于非整合载体不会成为宿主基因组的一部分,因此非整合载体倾向于在细胞群中瞬时表达核酸。这部分地由于非整合载体经常使得复制缺陷的事实。因此,非整合载体具有胜过逆转录病毒载体的几个优点,包括、但不限于:(1)不会破坏宿主基因组,和(2)瞬时表达,以及(3)没有剩余的病毒整合产物。用于与本文所述方法一起使用的非整合载体的一些非限制性例子包括腺病毒、杆状病毒、甲病毒、小rna病毒和痘苗病毒。在本文所述的方法的一些实施方案中,所述非整合病毒载体是腺病毒。非整合病毒载体的其它优点包括以高滴度生产它们的能力、它们在体内的稳定性以及它们对宿主细胞的有效感染。
247.在一些实施方案中,用于在本文所述的组合物、载体、构建体、方法和试剂盒中产生诱导的pdc的核酸构建体和载体可以进一步包含一种或多种编码用于细胞的阳性和阴性选择的选择标志物的序列。这样的选择标志物序列通常可以提供对抗生素的抗性或敏感性特性,所述特性在没有引入核酸构建体的情况下通常不会在细胞中发现。选择标志物可以与选择剂诸如抗生素结合使用,以在培养物中选择表达插入的核酸构建体的细胞。编码阳性选择标志物的序列通常提供抗生素抗性,即,当阳性选择标志物序列存在于细胞的基因组中时,所述细胞对抗生素或试剂是敏感的。编码阴性选择标志物的序列通常提供对抗生素或试剂的敏感性,即,当阴性选择标志物存在于细胞的基因组中时,细胞对抗生素或试剂是敏感的。
248.在一些实施方案中,用于制备在本文所述的组合物、载体、构建体、方法及其试剂盒中的诱导的pdc的核酸构建体和载体可以进一步包含用于构建体或其它载体遗传元件的调节、表达、稳定化的其它核酸元件,例如,本领域普通技术人员已知的启动子、增强子、tata盒、核糖体结合位点、ires、2a-样自切割序列。
249.用于制备在本文所述的组合物、载体、构建体、方法和试剂盒中的诱导的pdc的核酸构建体和载体可以进一步包含2a-样自切割序列。自切割的18-22个氨基酸长的2a肽介导脯氨酸和甘氨酸残基之间的“核糖体跳跃”并抑制肽键形成,而不影响下游翻译。这些肽允许将多种蛋白编码为多蛋白,所述多蛋白在翻译后解离成组分蛋白。可以根据本发明使用的2a-样自切割序列的例子包括、但不限于来自细小rna病毒科的那些,包括口蹄疫病毒属诸如口蹄疫病毒(fmdv)、马甲型鼻炎病毒(erav)、thosea asigna病毒(tav)和猪捷申病毒-1(ptv-1)和心病毒属诸如theilovirus(例如,theiler氏鼠脑脊髓炎)和脑心肌炎病毒。
250.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述pdc诱导因子诸如irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、hoxa5(seq.id.19,seq.id.20)、ikzf1(seq.id.23,seq.id.24)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、stat1(seq.id.45,seq.id.46)和tsc22d1(seq.id.47,seq.id.48)作为合成的、修饰的rna提供,或者作为合成的、修饰的rna引入或递送到细胞中,如美国专利公开2012-0046346-a1中所述,其内容通过引用整体并入本文。在其中根据本文所述的方法使用合成的、修饰的rna将细胞重新程序化为诱导的pdc的那些实施方案中,所述方法可以涉及细胞的重复接触或涉及编码pdc诱导因子的合成的、修饰的rna的重复转染,诸如例如,至少2次、至少3次、至少4次、至少5次、至少6次、至少7次、至少8次、至少9次、至少10次、至少11次、至少12次、至少13次、至少14次、至少15次、至少16次、至少17次、至少18次、至少19次、至少20次、至少25次、至少30次或更多次转染。
251.除了一种或多种修饰的核苷之外,用于本文所述的组合物、载体、构建体、方法和试剂盒中的修饰的mrna还可以包含本领域技术人员已知的和如在美国专利公开2012-0046346-a1和20120251618a1以及pct公开wo2012/019168中描述的任何另外修饰。这样其它组分包括,例如,5'帽(例如,抗反向帽类似物(arca)帽,其含有5
′‑5′‑
三磷酸鸟嘌呤-鸟嘌呤键,其中一个鸟嘌呤含有n7甲基基团以及3
′‑
o-甲基基团;使用重组痘苗病毒加帽酶和重组2
′‑
o-甲基转移酶产生的帽,其可以在mrna的最5
′
侧核苷酸和鸟嘌呤核苷酸之间产生规范的5
′‑5′‑
三磷酸键,其中鸟嘌呤含有n7甲基化,且最终的5
′‑
核苷酸含有2
′‑
o-甲基,从而产生cap1结构);聚腺苷酸尾巴(例如,大于30个核苷酸长度、大于35个核苷酸长度、至少40个核苷酸、至少45个核苷酸、至少55个核苷酸、至少60个核苷酸、至少70个核苷酸、至少80个核苷酸、至少90个核苷酸、至少100个核苷酸、至少200个核苷酸、至少300个核苷酸、至少400个核苷酸、至少500个核苷酸、至少600个核苷酸、至少700个核苷酸、至少800个核苷酸、至少900个核苷酸、至少1000个核苷酸或更长的聚-a尾巴);kozak序列;3
′
非翻译区(3
′
utr);5
′
非翻译区(5
′
utr);一种或多种能够从核酸中切除的内含子核苷酸序列,或它们的任意组合。
252.用于本文所述的组合物、载体、构建体、方法和试剂盒中的修饰的mrna可以进一步包含内部核糖体进入位点(ires)。ires可以充当唯一的核糖体结合位点,或可以充当mrna的多个核糖体结合位点之一。含有多于一个功能性核糖体结合位点的mrna可以编码几种肽或多肽,诸如本文所述的pdc诱导因子,它们由核糖体(“多顺反子mrna”)独立翻译。当给核酸提供ires时,进一步任选地提供第二可翻译区。可以根据本发明使用的ires序列的例子
包括、但不限于来自小rna病毒(例如fmdv)、害虫病毒(cffv)、脊髓灰质炎病毒(pv)、脑心肌炎病毒(ecmv)、口蹄疫病毒(fmdv)、丙型肝炎病毒(hcv)、经典猪瘟病毒(csfv)、鼠白血病病毒(mlv)、猿猴免疫缺陷病毒(sw)或蟋蟀麻痹病毒(crpv)的那些。
253.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述合成的、修饰的rna分子包含至少一种修饰的核苷。在本文所述的组合物、载体、方法和试剂盒的一些实施方案中,所述合成的、修饰的rna分子包含至少两种修饰的核苷。
254.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,所述修饰的核苷选自:5-甲基胞嘧啶(5mc)、n6-甲基腺苷(m6a)、3,2
′‑
o-二甲基尿苷(m4u)、2-硫代尿苷(s2u)、2
′
氟代尿苷、假尿苷、2
′‑
o-甲基尿苷(um)、2
′
脱氧尿苷(2
′
du)、4-硫代尿苷(s4u)、5-甲基尿苷(m5u)、2
′‑
o-甲基腺苷(m6a)、n6,2
′‑
o-二甲基腺苷(m6am)、n6,n6,2
′‑
o-三甲基腺苷(m62am)、2
′‑
o-甲基胞苷(cm)、7-甲基鸟苷(m7g)、2
′‑
o-甲基鸟苷(gm)、n2,7-二甲基鸟苷(m2,7g)、n2,n2,7-三甲基鸟苷(m2,2,7g)和肌苷(i)。在一些实施方案中,所述修饰的核苷是5-甲基胞嘧啶(5mc)、假尿嘧啶或它们的组合。
255.修饰的mrna不需要沿分子的整个长度进行均匀修饰。不同的核苷酸修饰和/或主链结构可以存在于核酸中的不同位置。本领域普通技术人员将理解,核苷酸类似物或其它修饰可以位于核酸的任何位置,使得核酸的功能不会显著降低。修饰也可以是5'或3'末端修饰。核酸可以含有最少一个且最多100%的修饰的核苷酸,或任何中间百分比,诸如至少50%修饰的核苷酸、至少80%修饰的核苷酸或至少90%修饰的核苷酸。
256.在本公开内容的一些实施方案中,所述载体或构建体是复制病毒载体或颗粒,诸如副粘病毒载体、棒状病毒载体、甲病毒和/或黄病毒颗粒,或非病毒载体或颗粒,诸如裸甲病毒或黄病毒rna复制子。
257.在一些实施方案中,优选但并非绝对必要的是,给定的核苷在分子中的每次出现都被修饰(例如,每个胞嘧啶是修饰的胞嘧啶,例如5-甲基胞嘧啶,每个尿嘧啶是修饰的尿嘧啶,例如,假尿嘧啶,等)。例如,修饰的mrna可以包含修饰的嘧啶诸如尿嘧啶或胞嘧啶。在一些实施方案中,核酸中至少25%、至少50%、至少80%、至少90%或100%的尿嘧啶被修饰的尿嘧啶替代。还考虑到相同核苷的不同出现可以在给定的合成的、修饰的rna分子中以不同的方式修饰。修饰的尿嘧啶可以被具有单一独特结构的化合物替代,或者可以被具有不同结构(例如,2、3、4种或更多种独特结构)的多种化合物替代。在一些实施方案中,核酸中至少25%、至少50%、至少80%、至少90%或100%的胞嘧啶可以被修饰的胞嘧啶替代。修饰的胞嘧啶可以被具有单一独特结构的化合物替代,或者可以被具有不同结构(例如,2、3、4种或更多种独特结构)的多种化合物替代(例如,一些胞嘧啶修饰为5mc,其它修饰为2
′‑
o-甲基胞嘧啶或其它胞嘧啶类似物)。这样的多修饰的合成rna分子可以通过使用包含所有期望的修饰核苷的核糖核苷共混物或混合物来产生,使得当合成rna分子时,仅期望的修饰核苷被掺入所得编码pdc诱导因子的rna分子中。
258.在某些实施方案中,期望的是,在细胞内降解引入细胞中的修饰核酸,例如如果期望精确的蛋白产生时机。因此,在本文所述的组合物、载体、方法和试剂盒的一些实施方案中,本文提供了修饰的核酸,其包含能够在细胞内以定向方式被起作用的降解结构域。
259.虽然应理解诱导的pdc可以通过以核酸(dna或rna)或氨基酸序列的形式递送pdc诱导因子来产生,但是在本文所述的组合物、载体、方法和试剂盒的一些实施方案中,诱导
的pdc可以使用其它方法来诱导,例如,通过用试剂(诸如小分子或小分子混合物,其诱导一种或多种pdc诱导因子的表达)处理细胞。
260.使用本文所述的组合物、载体、方法和试剂盒检测引入细胞中或在细胞群中诱导的pdc诱导因子的表达,可以通过本领域技术人员已知的几种技术中的任一种来实现,所述技术包括、例如western印迹分析、免疫细胞化学和荧光介导的检测。
261.为了区分pdc诱导因子的给定组合是否已产生诱导的pdc,可以测量一种或多种dc活性或参数,诸如,在一些实施方案中,表面抗原的差异表达。使用本文所述的组合物、载体、方法和试剂盒产生诱导的dc,例如优选造成内源性pdc特有的细胞表面表型(诸如cd45和mhc-ii)的出现。
262.dc通过其功能行为最可靠地与其它免疫细胞区分开。dc表型或dc活性的功能方面,诸如诱导的pdc分泌细胞因子的能力,可以由本领域技术人员使用本领域已知的常规方法容易地确定。在本文描述的方面的一些实施方案中,可以使用鉴定重新程序化因子的功能测定。例如,在一些实施方案中,细胞因子分泌可以用于证实使用本文所述的组合物、载体、方法和试剂盒产生的诱导pdc的免疫调节特性。特别是,通过tlr7和tlr9途径对细胞内dna做出响应和分泌i型干扰素的能力与表征pdc功能特别相关。
263.本文中使用的“细胞参数”、“dc参数”或“细胞因子分泌”表示内源或天然dc的可测量组分或质量,特别是可以准确测量的组分。细胞参数可以是与细胞的表型、功能或行为相关的任何可测量参数。这样的细胞参数包括dc或dc群体的特征和标志物的变化,包括、但不限于活力、细胞生长、一种或多种标志物或标志物组合的表达的变化,所述标志物诸如细胞表面决定簇诸如受体、蛋白(包括其构象或翻译后修饰)、脂质、碳水化合物、有机或无机分子、核酸(例如mrna、dna)、总基因表达模式等。使用本领域技术人员已知的多种测定中的任一种,可以测量这样的细胞参数。例如,通过测定诸如锥虫蓝排除、cfse稀释和3h-胸苷掺入,可以测量活力和细胞生长。例如,使用流式细胞计数测定、western印迹技术或显微术方法,可以测量蛋白或多肽标志物的表达。例如,使用rna-测序方法和定量或半定量实时pcr测定,可以测定基因表达概况。细胞参数还可以表示功能参数或功能活性。虽然大多数细胞参数将提供定量读出值,但在一些情况下,半定量或定性结果可以是可接受的。读出值可以包括单个确定值,或可以包括平均值、中位值或方差等。特有地,可以从多个相同测定中为每种参数获得一系列参数读出值。预见到变异性,并且将使用标准统计方法和用于提供单个值的通用统计方法来获得每组测试参数的一系列值。
264.在本文所述的组合物、载体、方法和试剂盒的一些实施方案中,可以使用另外的因子和试剂来增强诱导的pdc重新程序化。例如,修饰表观遗传途径的因子和试剂可以用于促进重新程序化为诱导的pdc。
265.根据本文描述的组合物、载体、方法和试剂盒,基本上任何原代体细胞类型都可以用于产生诱导的pdc或将体细胞重新程序化为诱导的pdc。这样的原代体细胞类型还包括其它干细胞类型,包括多能干细胞,诸如诱导的多能干细胞(ips细胞);其它多潜能干细胞;寡能干细胞;和单能干细胞。可用于本文所述方法的各个方面和实施方案中的原代体细胞的一些非限制性例子包括、但不限于成纤维细胞、上皮细胞、内皮细胞、神经元细胞、脂肪细胞、心脏细胞、骨骼肌细胞、造血细胞或免疫细胞、肝细胞、脾细胞、肺细胞、循环血细胞、胃肠细胞、肾细胞、骨髓细胞和胰腺细胞,以及衍生出那些细胞的干细胞。所述细胞可以是从
任何体组织分离的原代细胞,所述体组织包括、但不限于脾、骨髓、血液、脑、肝、肺、肠道、胃、肠、脂肪、肌肉、子宫、皮肤、脾、内分泌器官、骨骼等。在一些实施方案中,术语“体细胞”进一步涵盖在培养物中生长的原代细胞,前提条件是,体细胞不是永生化的。当将细胞维持在体外条件下时,可以使用常规的组织培养条件和方法,并且它们是本领域技术人员已知的。各种原代体细胞的分离和培养方法完全是在本领域技术人员的能力范围内。
266.在本文描述的这些方面和所有这样的方面的一些实施方案中,所述体细胞是成纤维细胞。
267.在本文描述的这些方面和所有这样的方面的一些实施方案中,所述体细胞可以是造血谱系细胞。
268.在本文描述的这些方面和所有这样的方面的一些实施方案中,所述体细胞可以是癌细胞或肿瘤细胞。
269.在本文所述的组合物、载体、构建体、方法和试剂盒的一些实施方案中,待重新程序化或制成诱导的pdc细胞的体细胞是造血来源的细胞。本文中使用的术语“造血衍生的细胞”、“造血的衍生的分化细胞”、“造血谱系细胞”和“造血来源的细胞”表示衍生自或分化自多潜能造血干细胞(hsc)的细胞。因此,用于与本文所述的组合物、载体、构建体、方法和试剂盒一起使用的造血谱系细胞包括多潜能、寡能和谱系限制的造血祖细胞、粒细胞(例如,早幼粒细胞、嗜中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞)、红细胞(例如,网织红细胞、红细胞)、凝血细胞(例如,幼巨核细胞、产生血小板的巨核细胞、血小板)、单核细胞(例如,单核细胞、巨噬细胞)、树突细胞和淋巴细胞(例如,t-淋巴细胞(其携带t-细胞受体(tcr))、b-淋巴细胞或b细胞(其表达免疫球蛋白并产生抗体)、nk细胞、nkt细胞和先天性淋巴细胞)。本文中使用的术语“造血祖细胞”表示能够分化为造血系统的两种或更多种细胞类型的多潜能、寡能和谱系限制的造血细胞,包括、但不限于,粒细胞、单核细胞、红细胞、巨核细胞和淋巴细胞b-细胞和t-细胞。造血祖细胞涵盖多能祖细胞(mpp)、共同髓样祖细胞(cmp)、共同淋巴样祖细胞(clp)、粒细胞-单核细胞祖细胞(gmp)和前巨核细胞-红细胞祖细胞。谱系限制的造血祖细胞包括巨核细胞-红细胞祖细胞(mep)、原b细胞、前b细胞、前原b细胞、原t细胞、双阴性t细胞、原-nk细胞、前粒细胞/巨噬细胞、粒细胞/巨噬细胞祖(gmp)细胞和原-肥大细胞(promc)。
270.用于本文所述的组合物、载体、方法和试剂盒中的造血来源的细胞可以获得自已知包含这些细胞的任何来源,诸如胎儿组织、脐带血、骨髓、外周血、动员的外周血、脾、肝、胸腺、淋巴液等。从这些来源获得的细胞可以使用本领域技术人员可接受的任何方法离体扩增,然后与本文描述的用于制备诱导的pdc的组合物、载体、构建体、方法和试剂盒一起使用。例如,使用本领域技术人员可接受的任何程序,可以对细胞进行分选、分级分离、处理以除去特定细胞类型,或以其它方式操作以获得用于本文所述的方法中的细胞群体。可以收集单核淋巴细胞,例如,通过如美国专利号4,690,915中所述使用连续流动室分离器的重复淋巴细胞除去法,或使用clp方法的亲和纯化步骤分离,诸如使用细胞计数器的流式细胞计量术、磁性分离、使用抗体或蛋白包被的珠子、亲和色谱法或固体支持亲和分离(其中根据细胞对特定蛋白或蛋白类型的表达或表达缺乏将细胞保留在基质上)、或批式纯化(使用一种或多种针对目标细胞类型特异性表达的一种或多种表面抗原的抗体)。造血来源的细胞也可以从外周血获得。在从外周血收获细胞之前,可以用细胞因子诸如例如粒细胞-集落刺
激因子治疗受试者,以促进细胞从骨髓向血液隔室的迁移和/或促进目标群体的活化和/或增殖。例如,可以采用适用于鉴定表面蛋白的任何方法从异质群体分离造血来源的细胞。在一些实施方案中,获得造血来源的细胞(诸如淋巴细胞)的克隆群体。在一些实施方案中,造血来源的细胞不是克隆群体。
271.此外,关于本文所述的组合物、载体、构建体、方法和试剂盒的各个方面和实施方案,可以从任何哺乳动物物种获得体细胞,非限制性例子包括鼠、牛、猿猴、猪、马、羊或人细胞。在一些实施方案中,所述体细胞是人细胞。在一些实施方案中,所述细胞来自非人生物体,诸如非人哺乳动物。
272.一般而言,本文所述的制备诱导的pdc的方法涉及在本领域普通技术人员可获得和众所周知的任何培养基中培养或扩增体细胞,诸如造血来源的细胞。这样的培养基包括、但不限于dulbecco氏改良的但不限于dulbecco氏改良的(dmem)、dmem(dmem)、dmemiscove氏改良的rpmi-1640以及用于培养和扩增dc的无血清培养基。许多培养基也可作为含钠或不含钠的低葡萄糖制剂获得。在一些实施方案中,可以给与本文所述的方法一起使用的培养基补充一种或多种免疫刺激性细胞因子。常用生长因子包括、但不限于g-csf、gm-csf、tnf-α、il-4、il-3、flt-3配体和kit配体。另外,在优选的实施方案中,所述免疫刺激性细胞因子选自白介素(例如,il-1α、il-1β、il-2、il-3、il-4、il-6、il-8、il-9、il-10、il-12、il-18、il-19、il-20)、干扰素(例如,ifn-α、ifn-β、ifn-γ)、肿瘤坏死因子(tnf)、转化生长因子-β(tgf-β)、粒细胞集落刺激因子(g-csf)、巨噬细胞集落刺激因子(m-csf)、粒细胞-巨噬细胞集落刺激因子(gm-csf)、flt-3配体和kit配体。
273.例如,可以将培养中的细胞维持在悬浮液中或附着至固体支持物(诸如细胞外基质组分),或铺板在饲养细胞上。在本文所述的方法中使用的细胞可以需要促进它们附着到固体支持物的额外因子,在一些实施方案中,诸如i型和ii型胶原、硫酸软骨素、纤连蛋白、“超纤连蛋白”和纤连蛋白样聚合物、明胶、聚-d和聚-l-赖氨酸、凝血酶敏感蛋白和玻璃体结合蛋白。在一些实施方案中,细胞适合在悬浮培养物中生长。适合悬浮的宿主细胞通常是单分散的或以松散聚集体形式生长而没有大量聚集。适合悬浮的宿主细胞包括适用于悬浮培养而无需适应或操作的细胞(例如,造血来源的细胞,诸如淋巴样细胞)和通过附着依赖性细胞(例如,上皮细胞、成纤维细胞)的改变或适应而成为适合悬浮的细胞。
274.在本文描述的这些方面和所有这样的方面的一些实施方案中,所述分离的诱导的pdc进一步包含药学上可接受的载体以施用给有需要的受试者。
275.在一些方面,本文还提供了使用pdc诱导组合物和载体治疗需要治疗的受试者以诱导抗原特异性免疫应答以消除癌细胞或传染原的方法,以及制备本文所述的诱导的pdc的方法,或使用用pdc诱导因子、pdc诱导组合物和载体的任何组合或本文描述的制备诱导的pdc的方法产生的分离的诱导的pdc及其细胞克隆。在这样的治疗方法中,可以首先从受试者中分离体细胞,诸如成纤维细胞或造血谱系细胞,并且如本文所述用分别包含表达载体或合成mrna的pdc诱导组合物转导或转染分离的细胞。然后可以将使用pdc诱导因子、pdc诱导组合物和载体的任何组合或本文描述的制备诱导的pdc的方法产生的分离的诱导的pdc施用给受试者,诸如通过将诱导的pdc全身注射给受试者。
276.在一些方面,本文还提供了使用本文描述的pdc诱导组合物和载体以及pdc诱导因子的任何组合治疗需要治疗的受试者以诱导抗原特异性免疫应答以消除癌细胞或传染原的方法。在这样的治疗方法中,如本文所述,用包含表达载体的pdc诱导组合物转导癌细胞。可以首先将癌细胞从受试者中分离,用包含表达载体的pdc诱导组合物转导,并且然后施用给受试者,诸如通过全身注射。可替换地,可以用包含病毒表达载体的pdc诱导组合物原位或在体内转导癌细胞。
277.在本文所述的治疗方法的一些实施方案中,可以将使用本文所述的组合物、载体、构建体、方法和试剂盒产生的重新程序化的诱导的pdc直接使用或施用给需要免疫疗法的受试者。因此,本文所述方法的各个实施方案涉及将有效量的使用本文所述的组合物、载体、方法和试剂盒中的任一种产生的诱导的pdc或诱导的pdc群体施用给需要细胞疗法的个体或受试者。被施用的细胞或细胞群体可以是自体群体,或衍生自一种或多种异源来源。此外,可以以允许它们迁移到淋巴结并活化效应t细胞的方式施用这样的诱导的pdc。
278.本领域技术人员已知多种将细胞施用给受试者的方法。这样的方法可以包括全身注射,例如,静脉内注射,或者将细胞植入进受试者的靶部位。可以将细胞插入递送装置中,该递送装置有助于通过注射或植入进受试者而引入。这样的递送装置可以包括用于将细胞和流体注射到接受受试者的身体中的管子,例如导管。在一个优选的实施方案中,所述管子还另外具有针头,例如,通过该针头可以将细胞在期望的位置处引入受试者中。细胞可以以多种不同的形式制备用于递送。例如,当被包含在这样的递送装置中时,可以将细胞悬浮在溶液或凝胶中或嵌入支持基质中。可以将细胞与细胞在其中保持活力的药学上可接受的载体或稀释剂混合。
279.因此,通过本文所述的方法产生的细胞可以用于制备细胞以治疗或减轻几种癌症和肿瘤,包括、但不限于乳腺癌、前列腺癌、淋巴瘤、皮肤癌、胰腺癌、结肠癌、黑素瘤、恶性黑素瘤、卵巢癌、脑癌、原发性脑癌、头颈癌、神经胶质瘤、胶质母细胞瘤、肝癌、膀胱癌、非小细胞肺癌、头或颈癌、乳腺癌、卵巢癌、肺癌、小细胞肺癌、威尔曼瘤、宫颈癌、睾丸癌、膀胱癌、胰腺癌、胃癌、结肠癌、前列腺癌、生殖泌尿癌、甲状腺癌、食管癌、骨髓瘤、多发性骨髓瘤、肾上腺癌、肾细胞癌、子宫内膜癌、肾上腺皮质癌、恶性胰腺胰岛素瘤、恶性类癌、绒毛膜癌、蕈样肉芽肿病、恶性高钙血症、宫颈增生、白血病、急性淋巴细胞白血病、慢性淋巴细胞白血病、急性髓性白血病、慢性髓性白血病、慢性粒细胞白血病、急性粒细胞白血病、毛细胞白血病、神经母细胞瘤、横纹肌肉瘤、卡波西氏肉瘤、真性红细胞增多症、原发性血小板增多症、霍奇金病、非霍奇金淋巴瘤、软组织肉瘤、成骨性肉瘤、原发性巨球蛋白血症和视网膜母细胞瘤等。
280.除了上述之外,本发明的方法可以用于预防或消除已知会诱发某些癌症的病原体的感染。用于本文提供的癌症疫苗中的特别感兴趣的病原体包括乙型肝炎病毒(肝细胞癌)、丙型肝炎病毒(肝细胞瘤)、爱泼斯坦-巴尔病毒(ebv)(伯基特淋巴瘤、鼻咽癌、免疫抑制个体中的ptld)、htlvl(成体t细胞白血病)、致癌人乳头瘤病毒16、18、33、45型(成人宫颈癌)和细菌幽门螺杆菌(helicobacter pylori)(b细胞胃淋巴瘤)。在文献中广泛描述了可以在哺乳动物和更特别是人类中充当抗原的其它医学相关微生物,例如,c.g.a thomas,medical microbiology,bailliere tindall,(1983)。
281.除了上述之外,本发明的方法可以用于病毒感染。示例性的病毒病原体包括、但不
限于感染哺乳动物和更特别是人类的感染性病毒。感染性病毒的例子包括、但不限于:逆转录病毒科(例如,人免疫缺陷病毒,诸如hiv-i(也被称作htlv-iii,lav或htlv-iii/lav,或hiv-iii;和其它分离株,诸如hiv-lp);细小rna病毒科(例如脊髓灰质炎病毒、甲型肝炎病毒;肠道病毒、人柯萨奇病毒、鼻病毒、埃可病毒);杯状病毒科(例如引起胃肠炎的毒株);披膜病毒科(例如马脑炎病毒、风疹病毒);黄病毒科(例如登革热病毒、脑炎病毒、黄热病病毒);冠状病毒科(例如冠状病毒诸如sars冠状病毒);弹状病毒科(例如水疱性口炎病毒、狂犬病病毒);纤丝病毒科(例如埃博拉病毒);副粘病毒(例如副流感病毒、腮腺炎病毒、麻疹病毒、呼吸道合胞体病毒);正粘病毒科(例如流感病毒);布尼亚病毒科(例如汉坦病毒、bunga病毒、白蛉病毒和nairo病毒);沙粒病毒科(出血热病毒);呼肠孤病毒科(例如里奥病毒、环状病毒和轮状病毒);双rna病毒科;嗜肝病毒科(乙型肝炎病毒);细小病毒科(细小病毒);乳多空病毒科(乳头状瘤病毒、多瘤病毒);腺病毒科(大多数腺病毒);疱疹病毒科单纯疱疹病毒(hsv)1和2、水痘带状疱疹病毒、巨细胞病毒(cmv)、疱疹病毒;痘病毒科(天花病毒、痘苗病毒、痘病毒);和虹彩病毒科(例如非洲猪瘟病毒);和未分类的病毒(例如海绵状脑病的病原体、丁型肝炎的病原体(被认为是乙型肝炎病毒的缺陷卫星)、非甲非乙型肝炎的病原体(1类=血液(interaally)传播;2类=胃肠外传播(即丙型肝炎);诺瓦克病毒(norwalk)和有关的病毒和星状病毒)。
282.除了上述之外,本发明的方法可以用于靶向脊椎动物中的革兰氏阴性和革兰氏阳性细菌。这样的革兰氏阳性细菌包括、但不限于巴斯德氏菌属种(pasteurella sp.)、葡萄球菌属种(staphylococci sp.)和链球菌属种(streptococcus sp.)。革兰氏阴性细菌包括、但不限于大肠杆菌(escherichia coli)、假单胞菌属种(pseudomonas sp.)和沙门氏菌属种(salmonella sp.)。感染性细菌的具体例子包括、但不限于:幽门螺杆菌(helicobacter pyloris)、伯氏疏螺旋体(borella burgdorferi)、嗜肺军团菌(legionella pneumophilia)、分枝杆菌属种(例如结核分枝杆菌(m.tuberculosis)、鸟分枝杆菌(m.avium)、胞内分枝杆菌(m.intracellulare)、堪萨斯分枝杆菌(m.kansaii)、戈登分枝杆菌(m.gordonae))、金黄色葡萄球菌(staphylococcus aureus)、淋病奈瑟球菌(neisseria gonorrhoeae)、脑膜炎奈瑟球菌(neisseria meningitidis)、单核细胞增生李斯特菌(listeria monocytogenes)、酿脓链球菌(streptococcus pyogenes)(a群链球菌)、无乳链球菌(streptococcus agalactiae)(b群链球菌)、链球菌属(viridans group)、粪链球菌(streptococcus faecalis)、牛链球菌(streptococcus bovis)、链球菌属(厌氧消化种)、肺炎链球菌(streptococcus pneumoniae)、病原性弯曲杆菌属种(campylobacter sp.)、肠球菌属种(enterococcus sp.)、流感嗜血杆菌(haemophilus infuenzae)、炭疽芽孢杆菌(bacillus antracis)、白喉棒杆菌(corynebacterium diphtheriae)、棒杆菌属种(corynebacterium sp.)、猪红斑丹毒丝菌(erysipelothrix rhusiopathiae)、产气英膜梭菌(clostridium perfringers)、破伤风梭菌(clostridium tetani)、产气肠杆菌(enterobacter aerogenes)、肺炎克雷伯氏菌(klebsiella pneumoniae)、多杀巴斯德氏菌(pasturella multocida)、拟杆菌属种(bacteroides sp.)、具核梭杆菌(fusobacterium nucleatum)、念珠状链杆菌(streptobacillus moniliformis)、苍白密螺旋体(treponema pallidium)、极细密螺旋体(treponema pertenue)、钩端螺旋体属(leptospira)、立克次氏体属(rickettsia)和以色列放线菌(actinomyces israelii)。
283.除了上述之外,本发明的方法可以用于靶向病原体,所述病原体包括、但不限于感染哺乳动物和更特别是人类的感染性真菌和寄生虫。感染性真菌的例子包括、但不限于:新型隐球菌(cryptococcus neoformans)、荚膜组织胞浆菌(histoplasma capsulatum)、粗球孢子菌(coccidioides immitis)、皮炎芽生菌(blastomyces dermatitidis)、砂眼衣原体(chlamydia trachomatis)和白色假丝酵母(candida albicans)
284.除了上述之外,本发明的方法可以用于靶向寄生虫,诸如细胞内寄生虫和专性细胞内寄生虫。寄生虫的例子包括、但不限于恶性疟原虫(plasmodium falciparum)、卵形疟原虫(plasmodium ovale)、三日疟原虫(plasmodiummalariae)、间日疟原虫(plasmdodium vivax)、诺氏疟原虫(plasmodium knowlesi)、果氏巴贝虫(babesia microti)、分歧巴贝虫(babesia divergens)、克氏锥虫(trypanosoma cruzi)、刚地弓形虫(toxoplasma gondii)、旋毛形线虫(trichinella spiralis)、硕大利什曼原虫(leishmania major)、杜氏利什曼原虫(leishmania donovani)、巴西利什曼原虫(leishmania braziliensis)、热带利什曼原虫(leishmania tropica)、冈比亚锥虫(trypanosoma gambiense)、罗德西亚锥虫(trypanosoma rhodesiense)、班氏吴策线虫(wuchereria bancrofti)、马来布鲁线虫(brugia malayi)、帝汶布鲁线虫(brugia timori)、人蛔虫(ascaris lumbricoides)、旋盘尾丝虫(onchocerca volvulus)和曼森血吸虫(schistosoma mansoni)。
285.如果经修饰,诱导的pdc可以用于诱导对一种或多种靶抗原的致耐受性应答,包括未来或现有的免疫应答的抑制。因此,诱导的pdc可用于治疗或预防不期望的免疫应答,包括例如移植排斥、移植物抗宿主病、变态反应、寄生虫疾病、炎性疾病和自身免疫性疾病。可以根据本发明治疗或预防的移植排斥的例子包括与骨髓和器官(诸如心脏、肝、胰腺、肾、肺、眼、皮肤等)的移植相关的排斥。变态反应的例子包括季节性呼吸变态反应;对气源性变应原的变态反应诸如花粉热;通过减少血清ige可治疗的变态反应和嗜酸性粒细胞增多症;哮喘;湿疹;动物变态反应、食物变态反应;胶乳变态反应;皮炎;或通过变应性脱敏可治疗的变态反应。可以通过本发明治疗或预防的自身免疫性疾病包括例如银屑病、系统性红斑狼疮、重症肌无力、僵人综合征、甲状腺炎、西德纳姆舞蹈病、类风湿性关节炎、糖尿病和多发性硬化。炎性疾病的例子包括克罗恩氏病、慢性炎性眼疾病、慢性炎性肺疾病和慢性炎性肝疾病、自身免疫性溶血性贫血、特发性白细胞减少症、溃疡性结肠炎、皮肌炎、硬皮病、混合性结缔组织病、肠易激综合征、系统性红斑狼疮(sle)、多发性硬化、重症肌无力、guillan-barre综合征(抗磷脂综合征)、原发性粘液性水肿、甲状腺毒症、恶性贫血、自身免疫性萎缩性胃炎、阿狄森氏病、胰岛素依赖型糖尿病(iddm)、古德帕斯彻氏综合征、贝赫切特综合征、舍格伦综合征、类风湿性关节炎、交感性眼炎、桥本氏病/甲状腺功能减退症、乳糜泻/疱疹样皮炎和脱髓鞘病、原发性胆汁性肝硬化、混合性结缔组织病、慢性活动性肝炎、格雷夫斯病/甲状腺机能亢进、硬皮病、慢性特发性血小板减少性紫癜、糖尿病性神经病和脓毒性休克。
286.药学上可接受的载体和稀释剂包括盐水、缓冲水溶液、溶剂和/或分散介质。这样的载体和稀释剂的应用是本领域众所周知的。溶液优选地是无菌的和流体。优选地,在引入细胞之前,溶液在制造和储存条件下是稳定的,并且通过使用例如对羟基苯甲酸酯、三氯叔丁醇、苯酚、抗坏血酸、硫柳汞等针对微生物诸如细菌和真菌的污染作用进行防腐。
287.优选的是,细胞施用模式是相对非侵袭性的,例如通过静脉内注射、通过吸入的肺
部递送、局部或鼻内施用。但是,细胞施用途径将取决于待治疗的组织,并且可能包括植入。用于细胞递送的方法是本领域技术人员已知的,并且可以由医学领域的技术人员外推以与本文所述的方法和组合物一起使用。
288.在一些方面,本文还提供了用于制备诱导的pdc的试剂盒,所述试剂盒包含本文描述的含有一种或多种表达载体组分的任何pdc诱导组合物。
289.在一些方面,本文还提供了包含本文所述的一种或多种pdc诱导因子作为组分的试剂盒,其用于本文描述的制造诱导的pdc的方法。
290.因此,在一些方面,本文提供了用于制备诱导的树突细胞的试剂盒,其包含以下组分:(a)一种或多种表达载体,其编码至少1、2、3、4、5、6、7、8种或更多种选自以下的pdc诱导因子:irf8(seq.id.1,seq.id.2)、spib(seq.id.3,seq.id.4)、arid5a(seq.id.5,seq.id.6)、bcl11a(seq.id.7,seq.id.8)、cbfa2t3(seq.id.9,seq.id.10)、creb3l2(seq.id.11,seq.id.12)、ets1(seq.id.13,seq.id.14)、hdac5(seq.id.15,seq.id.16)、hhex(seq.id.17,seq.id.18)、hoxa5(seq.id.19,seq.id.20)、id3(seq.id.21,seq.id.22)、ikzf1(seq.id.23,seq.id.24)、ikzf2(seq.id.25,seq.id.26)、ikzf3(seq.id.27,seq.id.28)、ikzf5(seq.id.29,seq.id.30)、irf7(seq.id.31,seq.id.32)、mef2c(seq.id.33,seq.id.34)、myb(seq.id.35,seq.id.36)、runx2(seq.id.37,seq.id.38)、stat3(seq.id.39,seq.id.40)、tcf4(seq.id.41,seq.id.42)、tcf12(seq.id.43,seq.id.44)、stat1(seq.id.45,seq.id.46)、tsc22d1(seq.id.47,seq.id.48),和(b)其包装和说明书。
291.在一些实施方案中,本文所述的试剂盒可以进一步提供合成的mrna或一种或多种编码pdc诱导因子的表达载体,其呈混合物或作为单独等分试样。
292.在一些实施方案中,所述试剂盒可以进一步包含增强重新程序化效率的试剂。在一些实施方案中,所述试剂盒可以进一步包含一种或多种抗体或引物试剂以检测细胞类型特异性标志物以鉴定被诱导到pdc状态的细胞。
293.在一些实施方案中,所述试剂盒可以进一步包含缓冲液。在一些这样的实施方案中,所述缓冲液是ph 7.0的无rna酶的te缓冲液。在一些实施方案中,所述试剂盒进一步包含含有细胞培养基的容器。
294.本文描述的所有试剂盒可以进一步包含缓冲液、细胞培养基、转导或转染培养基和/或培养基补充剂。在优选的实施方案中,所述缓冲液、细胞培养基、转染培养基和/或培养基补充剂不含dna酶和rna酶。在一些实施方案中,在所述试剂盒中提供的合成的、修饰的rna可以呈特定量或质量(例如,20μg)的非溶液形式,诸如低压冻干的粉末形式,使得最终用户添加合适量的缓冲液或培养基以使组分达到期望的浓度,例如,100ng/μl。
295.本文描述的所有试剂盒可以进一步包含装置以促进使用本文描述的试剂盒组分生成的细胞的单次施用或重复或频繁输注,诸如不可植入的递送装置,例如,针头、注射器、笔式装置,或可植入递送装置,例如,泵、半永久性支架(例如,静脉内、腹膜内、脑池内或囊内)或蓄池。在一些这样的实施方案中,所述递送装置可以包括机构以分配单位剂量的包含诱导的pdc的药物组合物。在一些实施方案中,所述装置连续地释放组合物,例如,通过扩散。在一些实施方案中,所述装置可以包括监测受试者体内的参数的传感器。例如,所述装置可以包括例如泵和任选的相关电子元件。
296.在一个实施方案中,通过例如修饰体细胞、多能细胞、祖细胞或干细胞的至少一种本文所公开因子的基因表达,或通过使这些细胞类型中的任一种暴露于至少一种蛋白或产生至少一种如本文所公开蛋白的rna,人工制造诱导的pdc。可以进一步通过使其暴露于开启至少一种本文所公开因子的小分子来制造所述细胞。在一些方面,使用至少2、3、4、5、6、7或8种因子来制造诱导的pdc。
297.在一个实施方案中,clec9a、tlr7、tlr9和候选tf在dc子集和其它髓样细胞(单核细胞、巨噬细胞和小胶质细胞)中的表达数据获得自immgen数据库(www.immgen.org)。通过cluster 3.0(对数转换数据;居中基因;居中、聚集和标准化细胞类型)分析表达数据,并通过treeview显示。可替换地,使用graphpad prism展现表达值。
298.在一个实施方案中,以如下方式分离并纯化小鼠胚胎成纤维细胞(mef):使clec9acre/cre动物(10)与rosa26-stopflox-tdtomato报告物小鼠(the jackson laboratory)杂交以生成双重纯合的clec9acre/cre rosatdtomato/tdtomato(clec9a-tdtomato)小鼠。将所有动物圈养在受控温度(23
±
2℃)下,经历固定的12-h光照/黑暗周期,自由获得食物和水。
299.在一个实施方案中,从clec9a-tdtomato或c57bl/6小鼠的e13.5胚胎分离mef的原代培养物(6,10)。移除头、胎儿肝脏和所有内部器官,并将剩余组织机械解离。将解剖的组织使用0.12%胰蛋白酶/0.1mm乙二胺四乙酸(edta)溶液(3ml/胚胎)进行酶消化,并在37℃温育15min。每个胚胎另外添加3ml相同溶液,随后是另外15min温育时段。获得单细胞悬浮液并铺板于0.1%明胶包被的10-cm组织培养皿中的生长培养基中。使细胞生长2-3天直到汇合为止,用tryple express解离并在胎牛血清(fbs)+10%二甲亚砜(dmso)中冷冻。在铺板用于慢病毒转导之前,分选mef以移除残留的cd45+和tdtomato+细胞,其可以代表具有造血潜力的细胞。
300.在一个实施方案中,将hek293t细胞和mef维持在生长培养基[补充有10%(v/v)fbs、2mm l-谷氨酰胺和抗生素(10μg/ml青霉素和链霉素)的dulbecco氏改良的伊格尔培养基(dmem)]中。将所有细胞维持在37℃和5%(v/v)co2下。除非另有说明,否则所有组织培养试剂均来自thermo fisher scientific。
[0301]
在一个实施方案中,以如下方式进行病毒转导和重新程序化实验:将clec9a-tdtomato mef以40,000个细胞/孔的密度接种于0.1%明胶包被的6-孔平板上。将细胞以1:1fuw-teto-tf和fuw-m2rtta慢病毒颗粒的比率在补充有8μg/ml聚凝胺的生长培养基中温育过夜。在测试tf的组合时,应用相等moi的每种单独病毒颗粒。将细胞在连续几天中转导两次,并且在过夜温育后,用新鲜的生长培养基更换培养基。在第二次转导后,向生长培养基中补充多西环素(1μg/ml)-第0天。每2-3天更换培养基,持续培养的持续时间。在转导后5-8天分析新出现的tdtomato+细胞。
[0302]
在一个实施方案中,以如下方式进行流式细胞计量术分析:将转导的clec9a-tdtomato mef用tryple express解离,重新悬浮于200μl pbs 5%fbs中并保持在4℃,然后在bd facs lsr ii(bd biosciences)中进行分析。为了分析mhc-ii细胞表面标志物表达,将解离的细胞与在pbs 5%fbs中稀释的apc-缀合的大鼠抗-小鼠i-a/i-e抗体(biolegend)或apc-cy7-缀合的抗-cd45抗体(biolegend)一起在阻断非特异性结合的大鼠血清(1/100,genetex)存在的情况下在4℃温育30分钟。将细胞用pbs 5%fbs洗涤,重新悬浮于pbs 5%
fbs中并在bd facs lsr ii中进行分析。使用flowjo软件(flowjo,llc,版本7.6)分析流式细胞计量术数据。
[0303]
在一个实施方案中,以如下方式进行荧光激活细胞分选术(facs):为了纯化clec9a-tdtomato mef,将细胞与在pbs 5%fbs中稀释的apc-cy7-缀合的抗-cd45抗体(biolegend)一起在4℃温育30分钟。随后,将mef用pbs 5%fbs洗涤,重新悬浮在pbs 5%fbs中,并将tdtomato-cd45-mef在bd facsaria iii中纯化。当描述时,使用bd facsaria iii纯化tdtomato+细胞。在flowjo软件中处理facs数据。
[0304]
在一个实施方案中,使用2个无菌载玻片的磨砂末端对来自clec9a-tdtomato小鼠的新鲜分离的脾进行匀浆化。将细胞收获在补充有5%fbs的pbs中,并通过70μm细胞过滤网(bd biosciences)过滤。将红血细胞在室温下用bd pharm lyse(bd biosciences)裂解8分钟。通过添加≥5个体积的pbs 5%fbs来停止裂解。将脾细胞洗涤一次以获得单细胞悬浮液,将其与在pbs 5%fbs中稀释的fitc-缀合的抗-cd11c抗体(biolegend)、apc-缀合的抗-bst2抗体(biolegend)、apc-cy7-缀合的抗-b220抗体(biolegend)和bv605-缀合的抗-siglec-h抗体(biolegend)的混合物一起在大鼠血清存在的情况下在4℃温育30分钟。包括单染色和荧光减一对照以进行适当的补偿和门控。在4℃保持30分钟后,将细胞洗涤并用pbs 3%fbs重新悬浮,并在bd facsaria iii(bdiosciences)中进行分析。使用flowjo软件处理由此分析产生的数据。脾pdc被鉴定为活单细胞cd11c
低
bst2
+
b220
+
siglec-h
+
。
[0305]
在一个实施方案中,以如下方式进行炎性细胞因子测定:将tdtomato+细胞在第9天进行facs分选,并与1μg/ml r848(invivogen)和0.5μm cpg odn 1668(invivogen)一起培养以分别进行tlr 7和tlr9过夜刺激。在第10天评估细胞因子干扰素-α(ifn-α)、干扰素-β(ifn-β)、白介素-10(il-10)、白介素-6(il-6)、肿瘤坏死因子-α(tnf-α)、c-c基序趋化因子配体5(ccl5)和c-x-c基序趋化因子配体10(cxcl10)的水平。收集50μl来自96孔板孔的培养物上清液,并根据生产商的说明书通过带有v板的legendplextmmouse anti-virus response panel(13-plex)(biolegend)进行分析。使用bd facs lsr ii进行采集,并使用legendplextmdata analysis 8.0版(biolegend)分析数据。
[0306]
本领域技术人员将认识到或仅仅使用例行实验就能够确定许多与本文所述的本发明的具体实施方案等效的方案。本发明的范围无意限于上面的描述,而是如所附权利要求所述。
[0307]
如果没有特别排除,当在权利要求的说明书中使用单数形式的要素或特征时,也包括复数形式,反之亦然。例如,术语“一种转录因子”或“所述转录因子”还包括复数形式的“多种转录因子”或“所述转录因子”,反之亦然。在权利要求中,冠词诸如“一个/种(a)”、“一个/种(an)”和“所述”可以是指一个/种或超过一个/种,除非指示相反情形或以其它方式从上下文显而易见。如果组成员中的一个、超过一个或所有成员存在于给定的产品或过程中、在给定的产品或过程中使用、或以其它方式与给定的产品或过程相关,则认为满足了在一组的一个或多个成员之间包括“或”的权利要求或描述,除非指示相反情形或以其它方式从上下文显而易见。本发明包括这样的实施方案,其中所述组的刚好一个成员存在于给定产品或方法中、用于给定产品或方法中或者以其它方式与给定产品或方法相关。本发明还包括这样的实施方案,其中所述组成员中的超过一个或全部都存在于给定产品或方法中、用于给定产品或方法中或者以其它方式与给定产品或方法相关。
[0308]
此外,应当理解,本发明涵盖所有变体、组合和排列,其中将来自一项或多项权利要求或来自说明书的相关部分的一个或多个限制、要素、条款、描述性术语等引入另一项权利要求中。例如,从属于另一项权利要求的任何权利要求可以修改为包括在从属于同一基本权利要求的任何其它权利要求中发现的一个或多个限制。
[0309]
此外,当权利要求叙述一种组合物时,应当理解,包括为了本文中公开的任何目的而使用所述组合物的方法,并且包括根据本文中公开的任意制备方法来制备所述组合物的方法或本领域已知的其它方法,除非另外指出或除非本领域的普通技术人员明白会出现矛盾或不一致。
[0310]
在给出范围的情况下,包括端点。此外,应当理解,除非另外指出或以其它方式从上下文和/或本领域普通技术人员的理解显而易见,否则被表达为范围的值可以采用在本发明的不同实施方案中的所述范围内的任何具体值,其精确至该范围的下限单位的十分之一,除非上下文另外清楚地指明。还应当理解,除非另外指出或以其它方式从上下文和/或本领域普通技术人员的理解显而易见,否则被表达为范围的值可以采用在给定范围内的任何子范围,其中将所述子范围的端点表达至与所述范围的下限单位的1/10相同的精确度。
[0311]
本公开内容不应以任何方式被视为限于所描述的实施方案,并且本领域普通技术人员将预见到对其修改的许多可能性。
[0312]
上述实施方案是可组合的。
[0313]
下表提供了在本公开内容中包括的序列的概述。
[0314]
表1.在本公开内容中包括的seq.id.
[0315]
[0316]
[0317][0318]
以下权利要求进一步阐述了本公开内容的特定实施方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1