生长因子恢复的制作方法
生长因子恢复
1.序列表
2.本技术包含已经以ascii格式电子提交并且在此通过引用整体并入的序列表。在2020年11月19日创建的所述ascii拷贝被命名为“51518-003wo2_sequence_listing_11_19_20_st25”并且大小为13,487字节。
3.相关申请
4.本技术要求于2019年11月21日提交的美国临时申请no.62/938,879的申请日的权益,其在此通过引用整体并入。
技术领域
5.本发明涉及患者、例如人患者中组织病症并且特别是软骨病症的治疗性治疗的领域。
背景技术:
6.生长因子(例如,成纤维细胞生长因子18)是调节细胞增殖、迁移、存活、分化、组织沉积、转换和维持以及许多其他生物学功能的蛋白质。一般来说,组织中的生长因子水平随着年龄而下降。这种下降部分地是由于由许多遗传沉默机制之一介导的基因表达降低、细胞密度普遍降低(假设为其中生长因子水平下降的正反馈回路)、翻译效率和有效性降低、以及衰老细胞的比例增加。组织中的细胞密度与组织组成和物理化学特性有关。至少生长因子浓度的一些下降与疾病、组织萎缩和组织退化相关。虽然生长因子补充、替换或替代有缺陷或缺失的生长因子是广泛使用的恢复因骨关节炎而退化的软骨的方法,但仍然需要改进的治疗方法。
技术实现要素:
7.本发明涉及用于促进负责组织产生和维持的细胞的增殖的表达载体及其使用方法,所述细胞例如软骨细胞、心肌细胞和滑膜细胞。本文中提供的组合物和方法可用于治疗或预防与疾病、组织萎缩和组织退化相关的软骨病症。在一些实施方案中,软骨病症是骨关节炎。
8.在第一方面中,本发明的特征在于重组表达载体,所述重组表达载体包含编码自杀基因、和成纤维细胞生长因子18(fibroblast growth factor 18,fgf-18)多肽或其功能片段的核酸。
9.在第一方面的一些实施方案中,所述表达载体是病毒载体。
10.在第一方面的一些实施方案中,所述表达载体包含非病毒颗粒以及编码(1)自杀基因和(2)fgf-18多肽或其功能片段的核酸。
11.在第一方面的一些实施方案中,所述表达载体包含杂合病毒-非病毒颗粒以及编码(1)自杀基因和(2)fgf-18多肽或其功能片段的核酸。
12.在一些实施方案中,所述病毒载体选自腺相关病毒(adeno-associated virus,
aav)、腺病毒、细小病毒、冠状病毒、弹状病毒、副黏病毒、小核糖核酸病毒、甲病毒、疱疹病毒、痘病毒、慢病毒和逆转录病毒科病毒。
13.在前述方面中任一项的一些实施方案中,所述病毒载体是aav。
14.在前述方面中任一项的一些实施方案中,所述aav还包含衣壳。
15.在前述方面中任一项的一些实施方案中,所述衣壳包括天然存在的衣壳或经改造的衣壳(例如,包含经修饰序列的衣壳)。
16.在前述方面中任一项的一些实施方案中,所述经改造的衣壳与配体缀合(例如,用于细胞类型特异性或调节免疫原性)。
17.在前述方面中任一项的一些实施方案中,所述天然存在的衣壳是aav1、aav2、aav2quad(y-f)、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、rh10、rh39、rh43、rh74、anc80、anc80l65、dj/8、dj/9、7m8、php.b、php.eb或php.s衣壳。
18.在前述方面中任一项的一些实施方案中,所述aav是aav2或aav5。
19.在前述方面中任一项的一些实施方案中,所述自杀基因包括单纯疱疹病毒-1胸苷激酶(herpes simplex virus-1 thymidine kinase,hsv-tk)基因、胱天蛋白酶9(casp9)基因、胞嘧啶脱氨酶基因、rqr85多肽或截短的人egfr多肽。
20.在前述方面中任一项的一些实施方案中,所述自杀基因是hsv-tk基因。
21.在前述方面中任一项的一些实施方案中,所述自杀基因是casp9基因。
22.在前述方面中任一项的一些实施方案中,所述自杀基因编码与seq id no:1的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%或至少99%同一性)的氨基酸序列。
23.在前述方面中任一项的一些实施方案中,所述自杀基因是指使表达所述表达载体的细胞发生程序性细胞死亡的基因。
24.在前述方面中任一项的一些实施方案中,所述自杀基因是指使表达所述表达载体的细胞终止该表达载体的转录或翻译的基因。
25.在前述方面中任一项的一些实施方案中,所述自杀基因是指使所述表达载体在表达该表达载体的细胞中的表达水平降低的基因。
26.在前述方面中任一项的一些实施方案中,所述自杀基因是诱导型自杀基因。
27.在前述方面中任一项的一些实施方案中,所述诱导型自杀基因是雷帕霉素激活的casp9。
28.在前述方面中任一项的一些实施方案中,所述自杀基因编码与seq id no:2的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%或至少99%同一性)的氨基酸序列。
29.在前述方面中任一项的一些实施方案中,所述fgf-18多肽编码与seq id no:3的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%或至少99%同一性)的氨基酸序列。
30.在前述方面中任一项的一些实施方案中,所述表达载体还包含与编码fgf-18或其
功能片段的核酸可操作地连接的转录调节子。
31.在前述方面中任一项的一些实施方案中,所述表达载体还包含非病毒颗粒。
32.在前述方面中任一项的一些实施方案中,所述转录调节子包含tata盒、b识别元件识别元件、转录因子ii b识别元件和下游启动子元件中的任意一种或更多种。
33.在前述方面中任一项的一些实施方案中,所述非病毒颗粒包含以下中的任意一种或更多种:脂质包膜、磷脂双层、脂质体、noisome、富勒烯、基于蛋白质的纳米粒、纳米晶体、树枝状聚合物、有机/无机胶体、聚乙二醇化脂质体、聚合物胶束、反胶束、混合胶束、敏感性胶束、多组分胶束、或者多分子或单分子树枝状胶束。
34.在另一个方面中,本发明的特征在于药物组合物,其包含前述方面中任一项所述的表达载体。
35.在前述方面中任一项的一些实施方案中,所述药物组合物还包含可药用载体、稀释剂或赋形剂。
36.在另一个方面中,本发明提供了治疗软骨病症的方法,所述方法包括向对象施用前述方面中任一项所述的药物组合物。
37.在另一个方面中,本发明提供了前述方面中任一项所述的药物组合物,其用于治疗软骨病症。
38.在另一个方面中,本发明提供了前述方面中任一项所述的药物组合物用于治疗软骨病症的用途。
39.在另一个方面中,本发明提供了前述方面中任一项所述的药物组合物在制备用于治疗软骨病症的药物中的用途。在前述方面中任一项的一些实施方案中,所述软骨病症是骨关节炎。
40.在前述方面中任一项的一些实施方案中,所述药物组合物为静脉内、关节内、软骨下、滑膜内或软骨内施用。
41.在前述方面中任一项的一些实施方案中,所述药物组合物被施用于滑膜关节。
42.在另一个方面中,本发明提供了促进软骨细胞或软骨细胞前体细胞增殖的方法(例如,通过提高软骨细胞或软骨细胞前体细胞的存活,或者通过提高软骨细胞前体细胞的分化),所述方法包括使细胞与前述方面中任一项所述的表达载体或药物组合物接触。
43.在另一个方面中,本发明提供了用于促进软骨细胞或软骨细胞前体细胞的增殖(例如,通过提高软骨细胞或软骨细胞前体细胞的存活,或者通过提高软骨细胞前体细胞的分化)的前述方面中任一项所述的表达载体或药物组合物。
44.在另一个方面中,本发明提供了前述方面中任一项所述的表达载体或药物组合物用于促进软骨细胞增殖(例如,通过提高软骨细胞或软骨细胞前体细胞的存活,或者通过提高软骨细胞前体细胞的分化)的用途。在另一个方面中,本发明提供了前述方面中任一项所述的表达载体或药物组合物在制备用于促进软骨细胞或软骨细胞前体细胞增殖(例如,通过提高软骨细胞或软骨细胞前体细胞的存活,或者通过提高软骨细胞前体细胞的分化)的药物中的用途。
45.在另一个方面中,本发明提供了促进胞外基质分泌以替代软骨的方法(例如,通过促进软骨细胞或软骨细胞前体细胞的增殖、通过提高软骨细胞或软骨细胞前体细胞的存活、或通过提高软骨细胞前体细胞的分化),所述方法包括使细胞与前述方面中任一项所述
的表达载体或药物组合物接触。
46.在另一个方面中,本发明提供了用于促进胞外基质分泌以替代软骨(例如,通过促进软骨细胞或软骨细胞前体细胞的增殖、通过提高软骨细胞或软骨细胞前体细胞的存活、或通过提高软骨细胞前体细胞的分化)的前述方面中任一项所述的表达载体或药物组合物。
47.在另一个方面中,本发明提供了前述方面中任一项所述的表达载体或药物组合物用于促进胞外基质分泌以替代软骨(例如,通过促进软骨细胞或软骨细胞前体细胞的增殖、通过提高软骨细胞或软骨细胞前体细胞的存活、或通过提高软骨细胞前体细胞的分化)的用途。
48.在另一个方面中,本发明提供了前述方面中任一项所述的表达载体或药物组合物在制备用于促进胞外基质分泌以替代软骨的药物中的用途。
49.在前述方面中任一项的一些实施方案中,细胞被离体转染或转导以表达所述表达载体。在另一个方面中,本发明的特征在于药盒,其包含前述方面中任一项所述的表达载体或药物组合物、以及药品说明书,其中所述药品说明书指导所述药盒的使用者进行前述方面中任一项所述的方法。在另一个方面中,本发明的特征在于前述方面所述的药盒,其中所述药盒还包含盒(carton)、显窃启密封件(tamper evident seal)、针、注射器或预填充注射器中的一种或更多种。
附图说明
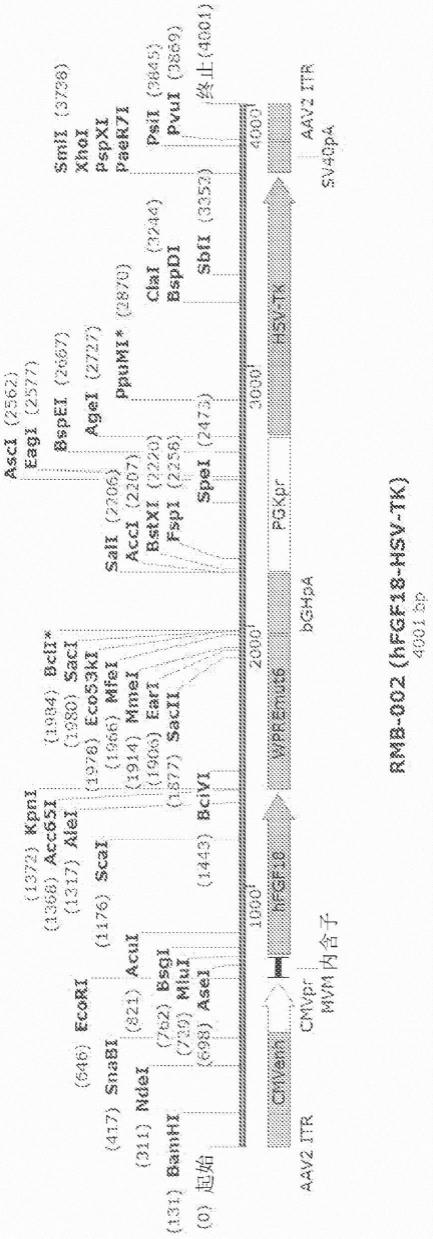
50.图1是用于持续表达如由单纯疱疹病毒-1胸苷激酶(hsv-tk)自杀基因介导的本质上安全的成纤维细胞生长因子18(fgf18)多肽的示例性腺相关病毒2(aav2)病毒载体的示意图。深色阴影框表示编码与人fgf18(hfgf18)多肽有效连接的巨细胞病毒(cytomegalovirus,cmv)增强子(cmvenh)、土拨鼠肝炎病毒转录后调节元件突变体6(wpremut6;已知显著提高表达水平但无启动子活性的dna元件)、牛生长激素多腺苷酸化信号(bovine growth hormone polyadenylation signal,bghpa)、hsv-tk自杀基因、突变的sv40早期多腺苷酸化信号(sv40pa)和侧翼aav2反向末端重复序列(inverted terminal repeat sequence,itr)的核酸序列。白色框分别表示cmv启动子和磷酸甘油酸激酶(phosphoglycerate kinase,pgk)启动子(cmvpr和pgkpr)。连接白色框和深色阴影框的粗线表示用于优化cmv启动子的功能的小鼠微小病毒(minute virus of mice,mvm)内含子。
51.图2是用于持续表达如由基于雷帕霉素激活的胱天蛋白酶9(rapacas9)的自杀基因介导的本质上安全的fgf-18多肽的示例性aav2病毒载体的示意图。深色阴影框表示编码与hfgf18多肽有效连接的cmvenh、wpremut6、bghpa、rapacas9自杀基因、sv40pa和侧翼aav2itr的核酸序列。白色框分别表示cmvpr和pgkpr。连接白色框和深色阴影框的粗线表示mvm内含子。
52.定义
53.本文中使用的“活性”是指保留天然的或天然存在的多肽的生物活性的多肽的形式,其中“生物”活性是指由天然的或天然存在的多肽引起的生物功能(例如,生长因子功能)。
54.本文中使用的“施用”是指通过任何有效途径向对象提供或给予治疗剂(例如,表
达载体)。示例性施用途径是在本文和下文中所描述的(例如,静脉内、关节内、软骨下、滑膜内或软骨内注射)。
55.本文中使用的术语“等位基因变体”是指占据生物体或生物体群体的染色体上给定基因座的基因的数种可能的天然存在的替代形式之一。
56.本文中使用的“心肌细胞”是指构成心肌的肌肉细胞(肌细胞)。本文中使用的“软骨病症”是指在患者中表现为以下的病症:软骨退化;关节间隙变窄;软骨下骨增厚;骨赘或骨刺的形成;伴有肿胀和疼痛的关节炎症;一种或更多种软骨组织组分、关节组织组分(包括细胞、蛋白质、蛋白聚糖和多糖)的密度降低;以及其他症状。除了机械损伤之外,软骨病症还与促炎细胞因子(例如肿瘤坏死因子α、白介素6(il-6)和白介素1(il-1)β)水平的增加相关。这些细胞因子可扩散到软骨中并引起蛋白酶活性的上调,导致软骨胞外基质的多种大分子被基质金属蛋白酶、聚蛋白多糖酶(aggrecanase)、透明质酸酶和其他组织消化酶降解。
57.本文中使用的术语“细胞类型”是指共用基于基因表达数据而在统计学上可分离的表型的细胞组。例如,共同细胞类型(例如,软骨细胞或滑膜细胞)的细胞可共用类似的结构和/或功能特征,例如类似的基因激活模式和抗原呈递谱。共同细胞类型的细胞可包括从共同组织(例如,关节组织)中分离的细胞和/或从生物体中的共同器官、组织系统、血管或其他结构和/或区域分离的细胞。
58.本文中使用的术语“软骨细胞”是指构成健康软骨中发现的原代细胞的细胞群。在功能上,软骨细胞产生和维持主要由胶原蛋白和蛋白聚糖组成的软骨基质。
59.本文中使用的术语“封闭末端dna(closed-end dna)”是指具有共价封闭的末端的线性双链体dna。
60.本文中使用的“密码子优化”是指根据编码dna中同义密码子(例如,编码相同氨基酸的密码子)的出现频率在不同物种中有偏差的原理修饰核酸序列的过程。这样的密码子简并性允许相同的多肽由多种核苷酸序列编码。以这种方式修饰的序列在本文中称为“经密码子优化的”。可对本说明书中描述的任何序列进行该过程以增强表达或稳定性。密码子优化可以以例如以下中所述的方式进行:例如美国专利no.7,561,972、7,561,973和7,888,112,这些专利各自通过引用整体并入本文。可根据已知方法将围绕翻译起始位点的序列转化为共有kozak序列。参见,例如,kozak et al,nucleic acids res.15:8125-8148(1989),其通过引用整体并入本文。可并入多种终止密码子。
61.本文中使用的“组合治疗”意指将两种(或更多种)不同的药剂或治疗作为针对特定疾病或病症的限定治疗方案的一部分施用于对象。治疗方案限定了每种药剂的施用剂量和周期,使得不同药剂对对象的影响重叠。在一些实施方案中,两种或更多种药剂的递送是同步或同时的,并且药剂可共配制。在另一些实施方案中,两种或更多种药剂不是共配制的并且作为处方方案的一部分以顺序方式施用。在一些实施方案中,组合施用两种或更多种药剂或治疗以使得症状或与病症相关的其他参数的降低大于在单独递送一种药剂或治疗的情况下或在不存在另一种的情况下所观察到的降低。两种治疗的作用可以是部分累加的、完全累加的或大于累加的(例如,协同的)。每种治疗剂的顺序施用或基本同时施用可通过任何合适的途径实现,所述途径包括但不限于经口途径、静脉内途径、肌内途径和通过黏膜组织直接吸收。治疗剂可通过相同途径或通过不同途径施用。例如,组合中的第一治疗剂
可通过静脉内注射施用,而组合中的第二治疗剂可经口施用。
62.本文中使用的术语“狗骨头dna(doggybone dna)”是指闭合的线性双链dna,其通过酶促消化多联体dna而产生。
63.本文中使用的术语“表达”是指以下事件中的一个或更多个:(1)从dna序列产生rna模板(例如,通过转录);(2)rna转录物的加工(例如,通过剪接、编辑、5’帽形成和/或3’末端加工);(3)将rna翻译成多肽或蛋白质;以及(4)多肽或蛋白质的翻译后修饰。目的基因在对象中的表达可例如通过检测以下来表现:编码对应蛋白质的mrna的量或浓度的提高(如例如,使用本领域已知的rna检测程序,例如定量聚合酶链反应和rna测序技术来评估的),和/或对应蛋白质的量或浓度的提高(如例如,使用本领域已知描述的蛋白质检测方法,例如western印迹来评估的)。
64.本文中使用的术语“表达载体”是指核酸载体,例如dna载体例如质粒、rna载体、病毒或其他合适的复制子(例如病毒载体)。已经开发了多种载体以用于将编码外源蛋白质的多核苷酸递送到原核或真核细胞中。这样的表达载体的一些实例在例如wo 1994/011026中公开;其通过引用并入本文,因为其涉及适合于表达目的基因的载体。适用于本文中所述的组合物和方法的表达载体包含多核苷酸序列以及例如用于表达蛋白质和/或将这些多核苷酸序列整合到哺乳动物细胞基因组中的另外的序列元件。可用于表达如本文中所述的表达载体的某些载体包括包含指导基因转录的调节序列(例如启动子和增强子区域)的质粒。用于表达表达载体的另一些可用的载体包含增强这些基因的翻译速率或改善由基因转录产生的mrna的稳定性或核输出的多核苷酸序列。这些序列元件包括例如5’和3’非翻译区、ires和多腺苷酸化信号位点,以指导表达载体上携带的基因的有效转录。适用于本文中所述的组合物和方法的表达载体还可包含编码标志物的多核苷酸,以用于选择包含这样的载体的细胞。合适的标志物的一些实例是编码针对抗生素(例如氨苄青霉素、氯霉素、卡那霉素、诺尔丝菌素(nourseothricin)或吉欧霉素(zeocin))的抗性的基因。
65.本文中使用的术语“成纤维细胞生长因子18”、“fgf-18”和“fgf18”是指维持人fgf-18蛋白的至少一种生物活性的蛋白质。本文中使用的fgf-18是指其天然形式、其成熟形式、重组形式、以及天然存在的fgf-18变体的任何其他形式(例如,剪接变体、等位基因变体、或由翻译后修饰或二级结构产生的变体)的fgf-18。本文中使用的fgf-18还指包括融合蛋白的fgf-18蛋白,其中杂合蛋白维持人fgf-18蛋白的至少一种生物活性。本文中使用的fgf-18还指经修饰的fgf-18蛋白,其中该修饰例如提高针对降解的抗性或者调节其与一种或更多种其受体结合的亲和力。人fgf-18蛋白的生物活性尤其包括提高软骨细胞或成骨细胞增殖(参见wo98/16644)或软骨形成(参见wo2008/023063)。天然人fgf-18是由关节软骨的软骨细胞表达的蛋白质。人fgf-18最初被命名为zfgf-5,并在wo98/16644中充分描述。人fgf-18具有ncbi基因id no 8817。一个示例性野生型人fgf-18核酸序列在ncbi refseq acc.no.nm_003862.3(seq id no:3)中提供,并且一个示例性野生型fgf-18氨基酸序列在ncbi refseq acc.no.np_003853.1(seq id no:4)中提供。
66.本文中使用的术语“其功能片段”是指fgf-18多肽,其可以是其天然形式、其成熟形式、重组形式、比完全的天然存在fgf-18变体更短的形式,或可以是天然存在的fgf-18变体的任何其他形式(例如,剪接变体或等位基因变体),并维持人fgf-18蛋白的至少一种生物活性。
67.本文中使用的术语“ires”是指内部核糖体进入位点。一般而言,ires序列是允许真核细胞核糖体结合mrna转录物并开始翻译而不与5’加帽末端结合的特征。包含ires序列的mrna产生两种翻译产物,一种从mrna的5’末端起始,并且另一种来自由ires介导的内部翻译机制。
[0068]“水平”意指与参照相比的蛋白质或核酸的水平。如本文中所限定的,参照可以是任何可用的参照。蛋白质或核酸的“降低的水平”或“提高的水平”意指与参照相比蛋白质或核酸水平的降低或提高(例如,降低或提高约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%、约100%、约150%、约200%、约300%、约400%、约500%或更多;与参照相比降低或提高多于约10%、约15%、约20%、约50%、约75%、约100%或约200%;降低或提高少于约0.01倍、约0.02倍、约0.1倍、约0.3倍、约0.5倍、约0.8倍或更少;或者提高多于约1.2倍、约1.4倍、约1.5倍、约1.8倍、约2.0倍、约3.0倍、约3.5倍、约4.5倍、约5.0倍、约10倍、约15倍、约20倍、约30倍、约40倍、约50倍、约100倍、约1000倍或更多)。蛋白质的水平可以以质量/体积(例如,g/dl、mg/ml、μg/ml、ng/ml)或相对于样品中总蛋白质或核酸的百分比来表示。
[0069]
本文中使用的术语“成熟形式”是指缺乏前导序列的fgf-18多肽,并且还可包含多肽的其他修饰,例如氨基末端(有或没有前导序列)和/或羧基末端的蛋白水解加工、从较大的前体中切割出较小的多肽、n-连接和/或o-连接的糖基化、以及本领域技术人员理解的其他翻译后修饰。
[0070]
本文中使用的术语“微环”是指作为没有任何细菌质粒dna骨架的环状表达盒产生的附加体dna载体。
[0071]
本文中使用的术语“ministring dna”是指线性的共价闭合dna载体,其仅包含目的基因和必需的真核表达元件。其没有免疫原性细菌序列。
[0072]
本文中使用的术语“纳米质粒
tm”是指具有小于500bp的骨架、无抗生素标志物、和具有r6k复制起点的dna载体。其可从nature technology corporation获得。
[0073]
本文中使用的术语“天然的”或“天然存在的”,当与生物物质例如核酸分子、多肽、宿主细胞等一起使用时,是指在自然界中发现的而不是由人操纵的生物物质。
[0074]
本文中使用的“骨关节炎”是指当骨末端处的柔性组织磨损时发生的表现为关节疼痛和僵硬、关节肿胀、活动范围减小、臂和腿无力或麻木以及其他症状的一种类型的软骨病症。
[0075]
相对于参照多核苷酸或多肽序列的“百分比(%)序列同一性”被定义为在比对序列并且引入空位(如果需要的话)以实现最大百分比序列同一性之后,候选序列中与参照多核苷酸或多肽序列中的核酸或氨基酸相同的核酸或氨基酸的百分比。出于确定核酸或氨基酸序列同一性百分比的目的的比对可以以本领域技术人员能力范围内的多种方式来实现,例如,使用可公开获得的计算机软件例如blast、blast-2或megalign软件来实现。本领域技术人员可确定用于比对序列的合适参数,包括在所比较的序列的全长上实现最大比对所需的任何算法。例如,可使用序列比较计算机程序blast产生序列同一性百分比的值。作为举例说明,给定核酸或氨基酸序列a相对于、与或针对给定核酸或氨基酸序列b的序列同一性百分比(可替代地表述为给定核酸或氨基酸序列a相对于、与或针对给定核酸或氨基酸序列
b具有一定的序列同一性百分比)如下计算:
[0076]
100乘以(分数x/y)
[0077]
其中x是在a和b的程序比对中通过序列比对程序(例如blast)评分为相同匹配的核苷酸或氨基酸的数目,并且其中y是b中核酸的总数目。将理解当核酸或氨基酸序列a的长度不等于核酸或氨基酸序列b的长度时,a相对于b的序列同一性百分比将不等于b相对于a的序列同一性百分比。
[0078]
本文中使用的术语“药物组合物”是指包含本文中所述的核酸的组合物,其用可药用赋形剂配制并经政府监管机构批准作为用于在对象中治疗疾病的治疗方案的一部分来制备或销售。
[0079]
本文中使用的术语“可药用”是指适合于与对象(例如哺乳动物(例如,人))的组织接触而无过度毒性、刺激、变应性反应和其他问题并发症,与合理的收益/风险比相称的那些化合物、物质、组合物和/或剂型。
[0080]
本文中使用的术语“质粒”是指可连接另外的dna区段的染色体外环状双链dna分子。质粒是一种类型的载体,其是能够运输与其连接的另外核酸的核酸分子。某些质粒能够在其被引入的宿主细胞中自主复制(例如,具有细菌复制起点的细菌质粒,和附加体哺乳动物质粒)。其他载体(例如,非附加体哺乳动物载体)可在被引入到宿主细胞中之后整合到宿主细胞的基因组中,并且从而与宿主基因组一起复制。某些质粒能够指导与其可操作地连接的基因的表达。
[0081]
本文中使用的术语“程序性细胞死亡”是指由于细胞内事件(例如凋亡或自噬)而导致的细胞死亡。
[0082]
本文中使用的术语“启动子”是指dna上被rna聚合酶结合的识别位点。聚合酶驱动转基因的转录。一些示例性启动子是适用于本文中所述的组合物和方法的启动子。另外,术语“启动子”可以指合成启动子,其为在生物系统中不天然存在的调节性dna序列。合成启动子包含与自然界中不存在的多核苷酸序列组合的天然存在启动子的部分,并且可被优化以使用多种转基因、载体和靶细胞类型表达重组dna。
[0083]
本文中使用的术语“剪接变体”是指核酸分子,通常是rna,其通过rna转录物中内含子序列的选择性加工来产生。
[0084]
本文中使用的术语“对象”是指例如出于实验、诊断、预防和/或治疗目的可施用根据本发明的组合物的任何生物体。典型的对象包括任何动物(例如,哺乳动物例如小鼠、大鼠、兔、非人灵长类和人)。对象可寻求或需要治疗、要求治疗、正在接受治疗、将在未来接受治疗,或者是由于特定疾病或病症而被训练的专业人员护理的人或动物。在一些实施方案中,对象是人。
[0085]
本文中使用的术语“自杀基因”是指引起细胞经历程序性细胞死亡的基因、终止表达载体自身的转录或翻译的基因、通过rna干扰降低表达载体的表达水平的基因、或者编码表面蛋白(例如如rqr85和截短的人表皮生长因子受体多肽)的基因。
[0086]
本文中使用的术语“滑膜细胞”是指成纤维细胞样滑膜细胞,其是位于滑膜中关节内的产生关节润滑所必需的滑液糖蛋白的特化细胞类型。
[0087]
本文中使用的术语“转录调节子”是指可响应于以下而调节蛋白质(例如fgf-18)的表达的诱导型元件:刺激(例如,炎症、细胞因子、低水平的胞外生长因子、感染、缺氧、低
或高水平的铁、低或高水平的铁蛋白、低或高水平的氨苄青霉素、低或高水平的异丙基β-d-1-硫代半乳糖吡喃糖苷、多西环素、一氧化氮、一氧化氮合酶(nos);旁分泌、内分泌或自分泌信号传导;或者引起组织退化或感染的外部刺激,其引起携带表达载体的细胞附近的结构变化)。
[0088]
本文中使用的术语“转导”和其变化形式是指将表达载体例如病毒载体构建体或其一部分引入到细胞中并随后在细胞中表达由该表达载体构建体或其一部分编码的转基因的方法。
[0089]
本文中使用的术语“转染”是指通常用于将外源dna引入到原核或真核宿主细胞中的广泛多种技术中的任一种,例如电穿孔、脂质体转染、磷酸钙沉淀、二乙基氨基乙基(deae)-右旋糖酐转染、nucleofection
tm
、挤压穿孔(squeeze-poration)、声穿孔、光学转染、magnetofection
tm
、穿刺转染(impalefection)、金颗粒轰击等。
[0090]
本文中使用的术语“治疗”或其变化形式意指治疗性治疗和防止性或预防性措施二者,其中目的是预防或减缓(减轻)不期望的生理病症、障碍或疾病,或获得有益的或期望的临床结果。有益的或期望的临床结果包括但不限于:缓解症状;减轻病症、障碍或疾病的程度;稳定(即不恶化)病症、障碍或疾病的状态;延迟病症、障碍或疾病的发作或减缓其进展;改善病症、障碍或疾病状态或者缓解(无论部分或完全),无论是可检出的或不可检出的;改善患者不一定能辨别的至少一种可测量的身体参数;或者增强或改善病症、障碍或疾病。治疗包括引起临床上显著的应答而没有过度水平的副作用。治疗还包括与如果不接受治疗的预期存活相比延长存活。
[0091]
本文中使用的术语“富含u的基序”是指连续核酸的链,其中至少80%的连续核酸是尿嘧啶(u)。
[0092]
有益效果
[0093]
本文中例示的表达载体及其使用方法提供了优于常规治疗的数种优势,所述常规治疗典型地包括重复关节内注射fgf-18多肽以用于促进软骨细胞和相应软骨的增殖。必须不断重复这些治疗方案以维持软骨增益,因为在中断注射后会恢复快速的软骨损失。首先,这些组合物和方法允许在关节内持续治疗性表达fgf-18而无需多次治疗。其次,本文中所述的表达载体编码这样的自杀基因,其用作“安全开关”机制以防止过度产生fgf-18表达或允许有条件地降低fgf-18表达水平。因此,本文中例示的表达载体及其使用方法通过用如由诱导型自杀基因介导的本质上安全的并且能够实现由fgf-18表达介导的持续治疗性再生特性的fgf-18多肽的遗传序列转导滑膜关节的细胞(例如,滑膜细胞和/或软骨细胞)克服了传统fgf-18补充的限制。
具体实施方式
[0094]
本文中所述的组合物和方法涉及用于治疗软骨病症的表达载体(例如,由腺相关病毒(aav)递送的编码自杀基因和成纤维细胞生长因子18(fgf-18)多肽或其功能片段的核酸)。在一些实施方案中,软骨病症是骨关节炎。fgf-18使软骨在退化(例如,骨关节炎中的软骨退化)之后恢复。
[0095]
自杀基因
[0096]
本发明的表达载体的特征在于编码自杀基因(例如,能够引起携带编码自杀基因
gregory rd evans.“suicide gene therapy by herpes simplex virus-1 thymidine kinase(hsv-tk).”targets in gene therapy(2011):65.)。
[0104]
在一些实施方案中,诱导型自杀基因编码与seq id no:1的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%或至少99%同一性)的氨基酸序列。
[0105]
在一些实施方案中,诱导型自杀基因是雷帕霉素激活的casp9(例如,参见stavrou,maria,et al.“a rapamycin-activated caspase 9-based suicide gene.”molecular therapy 26.5(2018):1266-1276.)。
[0106]
在一些实施方案中,诱导型自杀基因编码与seq id no:2的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%或至少99%同一性)的氨基酸序列。
[0107]
在一些实施方案中,本发明的特征在于诱导型自杀基因系统,其包含胸苷激酶自杀基因、胞嘧啶脱氨酶/5氟胞嘧啶响应元件、单纯疱疹病毒/更昔洛韦(ganciclovir)(hsv-tk/gcv)响应元件、羧基酯酶/伊立替康(irinotecan)、水痘带状疱疹病毒胸苷激酶/6-甲氧基嘌呤阿拉伯核苷、硝基还原酶nfsb/5-(氮丙啶-1-基)-24-二硝基苯甲酰胺、羧肽酶g2/4-[(2-氯乙基)(2-甲磺氧基乙基)氨基]苯甲酰基-l-谷氨酸和细胞色素p450-异环磷酰胺或细胞色素p450-环磷酰胺。
[0108]
ii.核酸酶介导的表达载体破坏
[0109]
在一些实施方案中,自杀基因可以是核酸酶或grna。可使用任何合适的核酸酶。在一些实施方案中,自杀基因是核酸酶介导的基因编辑系统的组分。例如,自杀基因在能够使表达载体转录或翻译的基因中引入改变(例如,插入、缺失(例如,敲除)、易位、倒位、单点突变或其他突变)。一些示例性基因编辑系统包括crispr系统、大范围核酸酶、zfn和talen。基于crispr的方法、zfn和talen例如在gaj et al.trends biotechnol.31.7(2013):397-405中描述。
[0110]
例如,用于破坏靶基因和/或将靶基因整合到细胞基因组中的可用的工具是crispr/cas系统,该系统最初作为细菌和古细菌中针对病毒感染的适应性防御机制演变而来。crispr/cas系统包含在质粒dna中的回文重复序列和cas蛋白(例如cas9或cas12a)。dna和蛋白质的这种集合通过首先将外来dna并入到crispr基因座中来指导靶序列的位点特异性dna切割。包含这些外来序列和crispr基因座的重复间隔元件的多核苷酸继而在宿主细胞中转录以产生grna,该grna随后可退火至靶序列并将cas核酸酶定位到该位点。以这种方式,可在外来多核苷酸中引起高度位点特异性cas介导的dna切割,因为使cas与靶dna分子靠近的相互作用受rna:dna杂交的控制。因此,可设计crispr/cas系统来切割目的靶dna分子(例如,能够使表达载体转录或翻译的基因)。该技术已被利用以编辑真核基因组(hwang et al.nature biotechnology 31:227(2013),其公开内容通过引用并入本文),并且可被用作位点特异性编辑细胞基因组的有效手段以在并入编码靶基因的基因之前切割dna。crispr/cas调节基因表达的用途已在例如us 8,697,359中描述,其公开内容通过引用并入本文。
[0111]
crispr系统已被修饰以用于真核生物中的基因编辑(例如,改变、沉默和/或增强某些基因)。参见,例如,wiedenheft et al.,nature 482:331,2012。例如,系统的这样的修饰包括将包含特别设计的crispr的质粒和一种或更多种合适的cas蛋白引入到真核细胞中。crispr基因座被转录成rna,并由cas蛋白(例如cas9)加工成包含侧翼有间隔物的重复序列的小rna。rna用作指导cas蛋白使特定dna/rna序列沉默的指导物,这取决于间隔序列。参见,例如,horvath et al.,science 327:167,2010;makarova et al.,biology direct 1:7,2006;pennisi,science 341:833,2013。在一些实例中,crispr系统包含cas9蛋白,其为切割dna两条链的核酸酶。
[0112]
在一些实施方案中,在用于本文中所述的用途的crispr系统中,例如根据本文中所述的一种或更多种方法,crispr的间隔物来源于靶基因序列,例如来源于能够使表达载体转录或翻译的基因的序列。
[0113]
在一些实施方案中,自杀基因包含用于在crispr系统中用于基因编辑的grna。在一些实施方案中,自杀基因包含大范围核酸酶或编码大范围核酸酶的mrna,其靶向(例如,切割)能够使表达载体转录或翻译的基因的核酸序列(例如,dna序列)。在一些实施方案中,自杀基因包含zfn或编码zfn的mrna,其靶向(例如,切割)能够使表达载体转录或翻译的基因的核酸序列(例如,dna序列)。在一些实施方案中,自杀基因包含talen或编码talen的mrna,其靶向(例如,切割)能够使表达载体转录或翻译的基因的核酸序列(例如,dna序列)。在一些实施方案中,自杀基因包含cas(例如,cas9)或编码cas(例如,cas9)的mrna,其靶向(例如,切割)能够使表达载体转录或翻译的基因的核酸序列(例如,dna序列)。
[0114]
在某些实施方案中,crispr系统用于编辑(例如,添加或缺失碱基对)靶基因,例如,能够使表达载体转录或翻译的基因。在另一些实施方案中,crispr系统用于引入提前终止密码子,例如,从而降低靶基因的表达。在又一些实施方案中,crispr系统用于以可逆方式(例如,类似于rna干扰)关闭靶基因。在一些实施方案中,crispr系统用于将cas(例如,cas9)引导至靶基因(例如,能够使表达载体转录或翻译的基因)的启动子,从而在空间上阻断rna聚合酶。
[0115]
在一些实施方案中,可使用例如美国公开no.20140068797;cong,science 339:819,2013;tsai,nature biotechnol.,32:569,2014;以及美国专利no.:8,871,445、8,865,406、8,795,965、8,771,945和8,697,359中描述的技术来产生crispr系统以编辑能够使表达载体转录或翻译的基因。
[0116]
在一些实施方案中,crispr干扰(crispri)技术可用于特定基因的转录阻遏,例如能够使表达载体转录或翻译的基因的转录阻遏。在crispri中,经改造的cas9蛋白(例如,无核酸酶dcas9或dcas9融合蛋白,例如dcas9-krab或dcas9-sid4x融合蛋白)可与序列特异性指导rna(specific guide rna,sgrna)配对。cas9-5grna复合物可阻断rna聚合酶,从而干扰转录延伸。该复合物还可通过干扰转录因子结合来阻断转录起始。crispri方法特别地具有最小的脱靶效应并且是可复用的,例如,可同时抑制多于一个的基因(例如,使用多个grna)。此外,crispri方法允许可逆的基因阻遏。
[0117]
在一些实施方案中,crispr介导的基因激活(crispra)可用于例如本文中所述的一种或更多种基因(例如抑制能够使表达载体转录或翻译的基因的基因)的转录激活。在crispra技术中,dcas9融合蛋白募集转录激活因子。例如,dcas9可用于募集多肽(例如,激
活结构域)例如vp64或p65激活结构域(p65d),并与sgrna(例如,单个sgrna或多个sgrna)一起使用,以激活一个或更多个基因例如内源基因。可通过使用多个sgrna来募集多个激活因子,这可提高激活效率。可使用多种激活结构域和单个或多个激活结构域。除了改造dcas9来募集激活因子之外,还可改造sgrna来募集激活因子。例如,可将rna适配体并入到sgrna中以募集蛋白质(例如,激活结构域)例如vp64。在一些实例中,协同激活介质(synergistic activation mediator,sam)系统可用于转录激活。在sam中,ms2适配体被添加至sgrna。ms2募集与p65ad和热休克因子1(heat shock factor 1,hsf1)融合的ms2外壳蛋白(ms2 coat protein,mcp)。crispri和crispra技术例如在dominguez et al.,nat.rev.mol.cell biol.17:5,2016中更详细地描述,其通过引用并入本文。
[0118]
在一些实施方案中,grna或cas(例如,cas9)可在crispr系统中用于改造基因(例如能够使表达载体转录或翻译的基因)中的改变。在另一些实例中,大范围核酸酶、zfn和/或talen可用于改造基因(例如能够使表达载体转录或翻译的基因)中的改变。一些示例性改变包括插入、缺失(例如,敲除)、易位、倒位、单点突变或其他突变。可将改变引入例如体外、离体或体内细胞中的基因中。在一些实施方案中,改变降低了能够使表达载体转录或翻译的基因的水平和/或活性(例如,敲低或敲除),例如,改变是功能的负调节子。在又一个实例中,改变在能够使表达载体转录或翻译的基因中引起缺陷(例如,引起缺陷的突变)。
[0119]
用于在将目的基因并入细胞之前通过位点特异性切割基因组dna来破坏靶dna的替代方法包括使用大范围核酸酶、zfn和talen。与crispr/cas系统不同,这些酶不包含用于定位到特定靶序列的指导多核苷酸。相反,靶标特异性由这些酶内的dna结合结构域控制。大范围核酸酶、zfn和talen在基因组编辑应用中的用途例如在umov et al.nature reviews genetics 11:636(2010);以及joung et al.nature reviews molecular cell biology 14:49(2013)中描述,两者的公开内容通过引用并入本文。在一些实施方案中,可使用本文中所述的这些基因编辑技术在包含表达载体的细胞中破坏能够使表达载体转录或翻译的基因。
[0120]
iii.通过编码干扰rna分子降低表过载体的表达水平的自杀基因
[0121]
在一些实施方案中,自杀基因是抑制性rna分子,例如,其通过rna干扰(rnai)途径发挥作用。抑制性rna分子可降低能够使表达载体转录或翻译的基因的表达水平(例如,蛋白质水平或mrna水平)。例如,抑制性rna分子包括靶向能够使表达载体转录或翻译的基因的sirna、shrna和/或mirna。sirna是通常长度为约19至25个碱基对的双链rna分子。shrna是包含发夹转角的rna分子,其通过rnai降低靶基因的表达。shrna可通过转染、电穿孔或转导以质粒(例如,病毒或细菌载体)的形式递送至细胞。微rna是通常长度为约22个核苷酸的非编码rna分子。mirna与mrna分子上的靶位点结合并例如通过引起mrna的切割、mrna的不稳定或mrna翻译的抑制使该mrna沉默。在一些实施方案中,抑制性rna分子降低能够使表达载体功能转录或翻译的基因的功能的水平和/或活性。在另一些实施方案中,抑制性rna分子降低功能正调节因子的抑制剂的水平和/或活性。
[0122]
可修饰抑制性rna分子,例如以包含经修饰的核苷酸,例如2
’‑
氟、2
’‑
o-甲基、2
’‑
脱氧、解锁核酸、2
’‑
羟基、硫代磷酸酯、2
’‑
硫尿苷、4
’‑
硫尿苷或2
’‑
脱氧尿苷。不受理论束缚,认为某些修饰可提高核酸酶抗性和/或血清稳定性或者降低免疫原性。
[0123]
在一些实施方案中,抑制性rna分子降低能够使表达载体转录或翻译的基因的水
平和/或活性或功能。在一些实施方案中,抑制性rna分子抑制能够使表达载体转录或翻译的基因的表达。在另一些实施方案中,抑制性rna分子提高能够使表达载体转录或翻译的基因的降解。抑制性rna分子可在体外化学合成或转录。基于非编码rna例如核酶、rna酶p、sirna和mirna的抑制性治疗剂的制备和使用也是本领域已知的,例如,如sioud,rna therapeutics:function,design,and delivery(methods in molecular biology).humana press 2010中描述的。
[0124]
安全元件
[0125]
在一些实施方案中,本发明的特征在于编码安全元件(例如,能够引起表达抑制、转录抑制、翻译抑制、效力减弱、携带构建体的细胞的衰老,或携带表达载体的细胞的凋亡的基因)的核酸。
[0126]
在一些实施方案中,本发明的特征在于可转录以下的安全元件:干扰rna分子例如短干扰rna、微rna或短发夹rna;或者设计为通过rna诱导的沉默复合物、drosha介导或dicer介导的途径或者仅通过fgf-18mrna的隔离或去稳定化来干扰fgf-18mrna的长非编码rna;或者用于fgf-18降解的核酶介导的系统。
[0127]
在一些实施方案中,本发明的特征在于可编码对编码fgf-18或其功能片段的核酸具有特异性的阻遏蛋白的安全元件。
[0128]
在一些实施方案中,本发明的特征在于可编码一般阻遏蛋白以促进细胞衰老的安全元件。
[0129]
在一些实施方案中,本发明的特征在于是选自以下的一种或更多种一般阻遏物的安全开关:编码一种或更多种多梳蛋白的基因、编码一种或更多种pre tf结合元件的基因、编码nrr(ear-r)的基因、编码aterf4的基因、编码had-19的基因、或者编码组蛋白脱乙酰酶家族的蛋白质中的一种或更多种的基因。
[0130]
成纤维细胞生长因子18多肽或其功能片段
[0131]
本发明的表达载体的特征在于编码成纤维细胞生长因子18(fgf-18)多肽或其功能片段的核酸。
[0132]
在一些实施方案中,表达载体编码fgf-18多肽或其功能片段,其中fgf-18多肽与seq id no:3的氨基酸序列具有至少85%序列同一性(例如,至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94、至少95%、至少96%、至少97%、至少98%、或至少99%同一性)。
[0133]
在一些实施方案中,表达载体编码fgf-18多肽,其可以是其天然形式、其成熟形式、重组形式或任何天然存在的fgf-18变体(例如,剪接变体或等位基因变体)。
[0134]
在一些实施方案中,表达载体编码fgf-18多肽或其翻译后修饰的变体,其中fgf-18多肽包含在fgf-18翻译后修饰变体中存在的一种或更多种天然存在的翻译后修饰。
[0135]
转录调节子
[0136]
在一些实施方案中,本发明的表达载体的特征在于响应于以下而发挥功能的与编码fgf-18或其功能片段的核酸序列可操作地连接的转录调节子:刺激(例如,内部刺激、炎症、细胞因子、低水平的胞外生长因子、感染、缺氧、低或高水平的铁、低或高水平的铁蛋白、低或高水平的氨苄青霉素、低或高水平的异丙基β-d-1-硫代半乳糖吡喃糖苷、多西环素、一氧化氮、一氧化氮合酶(nos);旁分泌、内分泌或自分泌信号传导;外部刺激,或者引起组织
退化或感染的外部刺激,其引起携带表达载体的细胞附近的结构变化)。
[0137]
在一些实施方案中,转录调节子是选自包括以下的列表的一种或更多种元件:启动子、阻遏物、tata盒、b识别元件识别元件、转录因子ii b识别元件和下游启动子元件。
[0138]
在一些实施方案中,本发明的特征在于转录调节子,其是选自包括以下的列表的一种或更多种启动子:lacuv5启动子、fgf基因家族启动子、转化生长因子基因家族启动子、透明质酸合酶基因家族启动子、对炎症有响应的启动子、可被细胞因子诱导的启动子、tac启动子、trc启动子、肠沙门氏菌(salmonella enterica)prpbcde(prpb)启动子、异柠檬酸裂解酶(acea)/苹果酸合酶(aceb)启动子、葡萄糖酸通透酶(gntp)/葡糖酸激酶(gntk)启动子、cj10x2启动子、tac-m启动子、麦芽糖abc转运蛋白周质蛋白(male1)启动子、arf gtp酶激活蛋白git1(git1)启动子、bcl-2相关细胞死亡激动剂(bad)启动子、squamosa启动子结合蛋白样转录因子(spl)、4-n14启动子、杂交白介素1增强子/白介素6启动子、前列腺素-内过氧化物合酶2(cox-2)启动子、诱导型细胞因子启动子、c-x-c基序趋化因子配体10(cxcl 10)启动子、lac/lacuv5启动子、t7启动子、nos启动子、泛素1启动子、核酮糖-1,5-二磷酸羧化酶/加氧酶(rbcs)启动子、阿拉伯糖诱导型arabad启动子(arapbad)、大肠杆菌(escherichia coli)鼠李糖bad启动子(rhapbad)、噬菌体λpl/pr启动子、大肠杆菌冷休克蛋白a(cspa)启动子、花椰菜花叶病毒启动子、花椰菜花叶病毒35s启动子、rna小调节rna抗毒素sokc(sokc)启动子、未表征的脂蛋白yaff(yaft)启动子、推定的整合酶(pintf)启动子、脱水胞壁肽通透酶(anhydromuropeptide permease)(ampg)启动子、酸性(多)磷酸酶(appy)启动子、脂肪酶a、溶酶体酸型(lipa)启动子、巨细胞病毒(cmv)早期启动子、延伸因子-1(ef1)α启动子、ef1启动子、cag启动子、单纯疱疹病毒-1胸苷激酶启动子、人β-肌动蛋白启动子、猿猴空泡病毒40(sv40)启动子、鼠干细胞病毒启动子、磷酸甘油酸激酶(pgk)启动子、泛素c(ubc)启动子或任何其他已知的组成型或诱导型启动子。
[0139]
在一些实施方案中,启动子是pgk启动子。
[0140]
在一些实施方案中,启动子是cmv启动子。
[0141]
另外的组分或修饰
[0142]
应当理解,基因可与或不与内含子(例如,天然存在的内含子、小鼠微小病毒内含子或合成内含子)一起使用,或/或仅与内含子(例如,天然存在的内含子、小鼠微小病毒内含子或合成内含子)的子集一起使用,和/或与表达载体中核酸序列的密码子优化一起使用。
[0143]
在一些实施方案中,编码fgf-18多肽或其功能片段的核酸可另外包含一种或更多种分泌序列以确保将多肽靶向至适当的细胞区室或胞外空间。
[0144]
在一些实施方案中,分泌序列是选自包括以下的列表的氨基酸序列中的一种或更多种:
[0145]
氨基酸序列seq id no:swshpqfek5gckpcictvpevssvfifppkpkdv6ictvpevssvfifppkpkdv7kpcictvpevssvfifppkpkdv8svfifppkpkdv9
ppkpkdv10pcictvpevssvfiefppkpkdv11mwwrlwwllllllllwpmvwa12metdtlllwvlllwpgstg13mdmrvpaqllgllllwlrgarc14mplllllpllwagala15mdamkrglccvlllcgavfvsps16mllllllllllalala17mlllllllglrlqlslg18mgvkvlfaliciavaea19mkwvtfisllflfssays20maflwllscwallgttfg21mqllscialilalv22mnllliltfvaaava23malwmrllpllallalwgpdpaaaf24mysapsactclclhflllcfqvqvlva25
[0146]
在一些实施方案中,表达载体还可包含增强子。
[0147]
在一些实施方案中,表达载体还可包含启动子。
[0148]
在一些实施方案中,启动子是组成型启动子。
[0149]
在一些实施方案中,启动子是诱导型启动子。
[0150]
在一些实施方案中,诱导型启动子是选自包括以下的列表的一种或更多种诱导型启动子:lacuv5、tac、trc、prpb、acea/aceb、gntp/gntk、cj10x2、tac-m、male1、git1、bad、spl、4-n14、cxcl10、lac/lacuv5、t7、arapbad、rhapbad、pl/pr、cspa、cox-2、杂交il-1增强子/ii-6启动子、casi启动子(例如,包含cmv和ubc增强子元件以及鸡b-肌动蛋白启动子的合成启动子)、ii型胶原蛋白启动子或细胞因子诱导型启动子。
[0151]
在一些实施方案中,启动子对刺激有响应,其与转录调节子正交、半正交和/或相反。
[0152]
在一些实施方案中,表达载体还可包含对刺激有响应的一种或更多种沉默子,其与自杀基因正交、半正交和/或相反。
[0153]
在一些实施方案中,沉默子可以是选自包括以下的基因列表的一种或更多种沉默子:cbx、bcl6、e2f6、pdgfa 5’shs、t39、jarid2、rest、yy1、pre-2-s5、gal4-cbx4、myh6pnr、zebb、gfi1/1b、elk-3、etv6/7、stat5、gata3、runx1、sp1/klf、xist、coolair或hotair、meg3、或fendrr。
[0154]
在一些实施方案中,表达载体还可包含多腺苷酸化信号(例如,天然存在的多腺苷酸化信号、牛生长激素多腺苷酸化信号或合成的多腺苷酸化信号)。
[0155]
在一些实施方案中,多腺苷酸化信号是一般哺乳动物多腺苷酸化共有序列或其变体,其包含富含u的区段(stretch),随后是约0至20个核苷酸(例如,1至19个核苷酸、2至18个核苷酸、3至17个核苷酸、4至16个核苷酸、5至15个核苷酸、6至14个核苷酸、7至13个核苷酸、8至12个核苷酸、9至11个核苷酸或约10个核苷酸),随后是ataaa的半保守共有序列,随
后是约15至30个(例如,16至29个核苷酸、17至28个核苷酸、18至27个核苷酸、19至26个核苷酸、20至25个核苷酸、21至24个核苷酸或22至23个核苷酸)核苷酸,随后是胞嘧啶(c)a,随后是0至20个核苷酸(例如,1至19个核苷酸、2至18个核苷酸、3至17个核苷酸、4至16个核苷酸、5至15个核苷酸、6至14个核苷酸、7至13个核苷酸、8至12个核苷酸、9至11个核苷酸或约10个核苷酸),随后是分化特异性元件、g或u、或富含u的区段。
[0156]
在一些实施方案中,表达载体还可包含终止区。
[0157]
在一些实施方案中,终止序列可以是选自包含以下的编码终止密码子或终止子的核酸的列表的终止密码子或终止序列中的一种或更多种:tag、taa、tga或tttatt。
[0158]
在一些实施方案中,表达载体还可包含一种或更多种选择性剪接外显子和/内含子、近端控制元件和/或下游序列。
[0159]
在一些实施方案中,表达载体还可包含一种或更多种顺式调节模块。
[0160]
在一些实施方案中,表达载体还可包含土拨鼠肝炎病毒(woodchuck hepatitis virus,whp)转录后调节元件(wpre)。
[0161]
递送
[0162]
任何合适的表达载体均可与本发明的组合物和方法结合使用,以设计和组装编码自杀基因和fgf-18多肽或其功能片段的核酸的组分。在一个实施方案中,表达载体是携带编码自杀基因、和fgf-18多肽或其功能片段的核酸的病毒载体。组装重组载体的方法是本领域已知的。参见,例如,griffiths,a.j.,et al.
″
making recombinant dna.
″
an introduction to genetic analysis.第7版.new york:wh freeman。可获自:http://www.ncbi.nlm.nih.gov/books/nbk21881(2000)。
[0163]
i.用于表达治疗性核酸的病毒载体
[0164]
病毒基因组提供了可用于将外源基因有效递送至哺乳动物细胞(例如,软骨细胞、软骨祖细胞和滑膜细胞)的载体的丰富来源。病毒基因组是用于基因递送的特别可用的载体,因为包含在这样的基因组中的多核苷酸通常通过一般化或专门化的转导并入到哺乳动物细胞的核基因组中。这些过程作为天然病毒复制周期的一部分发生,并且不需要添加蛋白质或试剂来诱导基因整合。病毒载体的一些实例是逆转录病毒(例如,逆转录病毒科病毒载体)、腺病毒(例如,ad5、ad26、ad34、ad35和ad48)、细小病毒(例如,腺相关病毒)、冠状病毒、负链rna病毒例如正黏病毒(例如流感病毒)、弹状病毒(例如狂犬病病毒和水疱性口炎病毒)、副黏病毒(例如麻疹病毒和仙台病毒)、正链rna病毒例如小核糖核酸病毒和甲病毒、以及双链dna病毒,其包括腺病毒、疱疹病毒(例如、1型和2型单纯疱疹病毒、eb病毒(epstein-barr virus)、巨细胞病毒)和痘病毒(例如牛痘、安卡拉改良牛痘(modified vaccinia ankara,mva)、鸡痘和金丝雀痘)。其他病毒包括例如诺沃克病毒(norwalk virus)、披膜病毒(togavirus)、黄病毒、呼肠孤病毒、乳多空病毒(papovavirus)、嗜肝dna病毒(hepadnavirus)、人乳头瘤病毒、人泡沫病毒和肝炎病毒。逆转录病毒的一些实例是:禽白血病肉瘤、禽c型病毒、哺乳动物c型、b型病毒、d型病毒、癌逆转录病毒(oncoretrovirus)、htlv-blv组、慢病毒、α逆转录病毒、γ逆转录病毒、泡沫病毒(spumavirus)(coffin,j.m.,retroviridae:the viruses and their replication,virology,第3版(lippincott-raven,philadelphia,(1996))。另一些实例是鼠白血病病毒、鼠肉瘤病毒、小鼠乳腺肿瘤病毒、牛白血病病毒、猫白血病病毒、猫肉瘤病毒、禽白血病
病毒、人t细胞白血病病毒、狒狒内源性病毒、长臂猿白血病病毒、mason pfizer猴病毒、猿猴免疫缺陷病毒、猿猴肉瘤病毒、劳斯肉瘤病毒(rous sarcoma virus)和慢病毒。载体的另一些实例例如在mcvey et al.,(us 5,801,030)中描述,其教导通过引用并入本文。
[0165]
ia.病毒衣壳蛋白
[0166]
可将本文中所述的核酸和载体并入到重组病毒体中以促进将核酸或载体引入到细胞中。在一些实施方案中,病毒衣壳蛋白是天然存在的衣壳或经改造的衣壳蛋白(例如,包含经修饰序列的衣壳)。
[0167]
病毒载体的衣壳蛋白构成病毒体的外部非核酸部分并由核酸编码。在一个实施方案中,病毒衣壳蛋白可在结构上由以下列表中的一种或更多种构成:包含天然和/或合成血清型的aav衣壳蛋白、一种或更多种血清型的慢病毒衣壳蛋白、一种或更多种血清型的逆转录病毒衣壳蛋白、一种或更多种血清型的疱疹病毒科衣壳蛋白、具有一种或更多种血清型的腺病毒科衣壳蛋白、具有一种或更多种血清型的细小病毒科衣壳蛋白、具有一种或更多种血清型的弹状病毒科衣壳蛋白、具有一种或更多种血清型的呼肠孤病毒科衣壳蛋白、具有一种或更多种血清型的正黏病毒科衣壳蛋白、具有一种或更多种血清型的布尼亚病毒科(bunyaviridae)衣壳蛋白、具有一种或更多种血清型的黄病毒科衣壳蛋白、具有一种或更多种血清型的逆转录病毒科衣壳蛋白、具有一种或更多种血清型的副黏病毒科衣壳蛋白、具有一种或更多种血清型的马铃薯y病毒科衣壳蛋白、具有一种或更多种血清型的冠状病毒科衣壳蛋白、具有一种或更多种血清型的杯状病毒科衣壳蛋白、具有一种或更多种血清型的乳头瘤病毒科衣壳蛋白、具有一种或更多种血清型的痘病毒科衣壳蛋白、具有一种或更多种血清型的多瘤病毒科(polymaviridae)衣壳蛋白、或者具有一种或更多种血清型的任何其他已知病毒或类病毒衣壳蛋白。
[0168]
在一些实施方案中,天然存在的病毒衣壳蛋白是经修饰的(例如,通过缀合进行修饰以用于在天然存在的病毒衣壳蛋白的表面上表达非病毒肽以用于细胞类型特异性靶向,或者通过缀合进行修饰以用于在病毒衣壳蛋白、真核蛋白或蛋白质片段之间表达融合蛋白以用于缩小向性(tropism))。
[0169]
在一些实施方案中,经改造的病毒衣壳蛋白与配体缀合(例如,用于细胞类型特异性或调节免疫原性)。
[0170]
ib.逆转录病毒载体
[0171]
本文中所述的方法和组合物中使用的递送载体可以是逆转录病毒载体。可在本文中所述的方法和组合物中使用的一种类型的逆转录病毒载体是慢病毒载体。慢病毒载体(lentiviral vector,lv)是逆转录病毒的子集,其高效地转导广泛范围的分裂和非分裂细胞类型,以实现转基因的稳定、长期表达。用于包装和转导lv的优化策略的概述在delenda,the journal of gene medicine 6:s125(2004)中提供,其公开内容通过引用并入本文。
[0172]
基于慢病毒的基因转移技术的使用依赖于体外产生重组慢病毒颗粒,所述重组慢病毒颗粒携带高度缺失的其中容纳了目的转基因的病毒基因组。特别地,重组慢病毒通过以下在允许细胞系中的反式共表达来恢复:
[0173]
(1)包装构建体,即表达gag-pol前体和rev(或者反式表达)的载体;
[0174]
(2)表达包膜受体的载体,其通常具有异源性质;以及(3)转移载体,其由缺少所有开放阅读框的病毒互补dna(cdna)组成,但维持复制、衣壳化和表达所需的序列,其中插入
了待表达的序列。
[0175]
在本文中所述的方法和组合物中使用的lv可包含5
’‑
长末端重复(long terminal repeat,ltr)、hiv信号序列、hiv psi信号5
’‑
剪接位点(sd)、δ-gag元件、rev响应元件(rev responsive element,rre)、3
’‑
剪接位点(sa)、延伸因子(elongation factor,ef)1-α启动子和3
’‑
自失活ltr(sin-ltr)中的一种或更多种。慢病毒载体任选地包含中央多嘌呤束(central polypurine tract,cppt)和土拨鼠肝炎病毒转录后调节元件(wpre),如us 6,136,597中所述,其公开内容通过引用并入本文,因为其涉及wpre。慢病毒载体还可包含phr’骨架,其可包含例如如下所提供的。
[0176]
在lu et al.,journal of gene medicine 6:963(2004)中描述的lentigen lv可用于表达dna分子和/或转导细胞。在本文中所述的方法和组合物中使用的lv可以是5
’‑
长末端重复(ltr)、hiv信号序列、hiv psi信号5
’‑
剪接位点(sd)、δ-gag元件、rev响应元件(rre)、3
’‑
剪接位点(sa)、延伸因子(ef)1-α启动子和3
’‑
自失活ltr(sin-ltr)。对于本领域的技术人员来说显而易见的是,这些区域中的一个或更多个任选地被执行类似功能的另一个区域替换。
[0177]
增强子元件可用于提高经修饰的dna分子的表达或提高慢病毒整合效率。在本文中所述的方法和组合物中使用的lv可包含nef序列。在本文中所述的方法和组合物中使用的lv可包含增强载体整合的cppt序列。cppt充当(+)-链dna合成的第二起点,并且在其天然hiv基因组的中间引入部分链重叠。在转移载体骨架中引入cppt序列极大提高了核转运以及整合到靶细胞dna中的基因组的总量。在本文中所述的方法和组合物中使用的lv可包含土拨鼠转录后调节元件(wpre)。wpre通过促进转录物的核输出和/或通过提高新生转录物的多腺苷酸化效率而在转录水平发挥作用,从而提高细胞中mrna的总量。将wpre添加至lv导致显著改善体外和体内二者中来自数种不同启动子的转基因表达的水平。在本文中所述的方法和组合物中使用的lv可包含cppt序列和wpre序列二者。该载体还可包含允许从单个启动子表达多个多肽的ires序列。
[0178]
除了ires序列之外,允许表达多种多肽的其他元件是可用的。在本文中所述的方法和组合物中使用的载体可包含允许表达多于一种多肽的多个启动子。在本文中所述的方法和组合物中使用的载体可包含允许表达多于一种多肽的蛋白质切割位点。允许表达多于一种多肽的蛋白质切割位点的一些实例在klump et al.,gene ther.8:811(2001)、osborn et al.,molecular therapy 12:569(2005)、szymczak and vignali,expert opin biol ther.5:627(2005)和szymczak et al.,nat biotechnol.22:589(2004)中描述,其公开内容通过引用并入本文,因为其涉及允许表达多于一种多肽的蛋白质切割位点。对本领域技术人员来说显而易见是,允许表达未来鉴定的多种多肽的其他元件是可用的并且可在适合于与本文中所述的组合物和方法一起使用的载体中使用。
[0179]
在本文中所述的方法和组合物中使用的载体可以是临床级载体。
[0180]
ic.腺相关病毒载体
[0181]
可将本文中所述的组合物和方法的核酸并入到重组腺相关病毒(raav)载体和/或病毒体中,以促进将它们引入到细胞(例如,软骨细胞、软骨细胞前体和滑膜细胞)中。可用于中枢神经系统的aav载体、以及适当的启动子和血清型在pignataro et al.,j neural transm.,125:575(2018)中讨论,其公开内容通过引用并入本文,因为其涉及可用于cns基
stemmer,nat.biotechnol.19:423(2001)。
[0189]
用于组装到表达载体中的可期望的aav片段包括:包括vp1、vp2、vp3和高变区的cap蛋白、包括rep 78、rep 68、rep 52和rep 40的rep蛋白、以及编码这些蛋白质的序列。这些片段可容易地用于多种载体系统和宿主细胞。这样的片段可单独使用,与其他aav血清型序列或片段组合使用,或者与来自其他aav或非aav病毒序列的元件组合使用。本文中使用的人工aav血清型包括但不限于具有非天然存在的衣壳蛋白的aav。这样的人工衣壳可通过任何合适的技术,使用所选择的aav序列(例如,vp1衣壳蛋白的片段)与可从不同的所选择的aav血清型、相同aav血清型的非连续部分、从非aav病毒来源、或者从非病毒来源获得的异源序列组合来产生。人工aav血清型可以是但不限于假型aav、嵌合aav衣壳、重组aav衣壳或“人源化”aav衣壳。假型载体在本发明中是可用的,其中一种aav的衣壳与来自具有不同衣壳蛋白的aav的itr一起使用。
[0190]
在一些实施方案中,病毒衣壳蛋白包括连接的衍生物(例如,合成的、生物的或半合成的衍生物)。
[0191]
ii.用于将外源核酸递送至靶细胞的方法
[0192]
可用于将多核苷酸(例如dna或rna,包括经密码子优化的dna或rna)引入到哺乳动物细胞(例如,软骨细胞、软骨细胞前体和滑膜细胞)的技术在本领域中是公知的。例如,可使用电穿孔通过对目的细胞施加静电势来使哺乳动物细胞(例如人靶细胞)透化。以这种方式经历外部电场的哺乳动物细胞例如人细胞随后易于摄取外源核酸(例如,能够在例如软骨细胞、软骨细胞前体和滑膜细胞中表达的核酸)。哺乳动物细胞的电穿孔例如在chu et al.,nucleic acids research 15:1311(1987)中详细描述,其公开内容通过引用并入本文。类似的技术nucleofection
tm
利用施加的电场来刺激将外源多核苷酸摄取到真核细胞的核中。nucleofection
tm
和可用于进行该技术的方案例如在distler et al.,experimental dermatology 14:315(2005)以及在us 2010/0317114中详细描述,其各自的公开内容通过引用并入本文。
[0193]
可用于转染靶细胞的另外的技术是挤压穿孔法。该技术诱导细胞的快速机械变形,以刺激通过响应于施加的压力而形成的膜孔来摄取外源dna。该技术的优势为不需要用于将核酸递送到细胞例如人靶细胞中的载体。挤压穿孔例如在sharei et al.,journal of visualized experiments 81:e50980(2013)中详细描述,其公开内容通过引用并入本文。
[0194]
脂质体转染表示另一种可用于转染靶细胞的技术。该方法涉及将核酸加载到脂质体中,其通常向脂质体外部呈递阳离子官能团,例如季铵或质子化胺。这由于细胞膜的阴离子性质而促进了脂质体与细胞之间的静电相互作用,这最终导致例如通过脂质体与细胞膜的直接融合或通过复合物的内吞作用摄取外源核酸。脂质体转染例如在us 7,442,386中详细描述,其公开内容通过引用并入本文。利用与细胞膜的离子相互作用来引发外来核酸的摄取的类似技术是使细胞与阳离子聚合物-核酸复合物接触。与多核苷酸缔合使得赋予有利于与细胞膜相互作用的正电荷的一些示例性阳离子分子是经活化的树枝状聚合物(例如在dennig,topics in current chemistry 228:227(2003)中描述的,其公开内容通过引用并入本文)、聚乙烯亚胺和deae-右旋糖酐,其作为转染剂的用途例如在gulick et al.,current protocols in molecular biology 40:1:9.2:9.2.1(1997)中详细描述,其公开内容通过引用并入本文。
[0195]
用于诱导靶细胞摄取外源核酸的另一种可用的工具是激光转染(laserfection),也称为光学转染,该技术涉及将细胞暴露于特定波长的电磁辐射以温和地透化细胞并允许多核苷酸穿透细胞膜。该技术的生物活性类似于电穿孔,并且发现在一些情况下优于电穿孔。
[0196]
穿刺转染是可用于将遗传物质递送至靶细胞的另一种技术。它依赖于使用纳米材料,例如碳纳米纤维、碳纳米管和纳米线。针样纳米结构垂直于基底表面合成。旨在用于胞内递送的包含基因的dna附着至纳米结构表面。随后将具有这些针的阵列的芯片压在细胞或组织上。被纳米结构穿刺的细胞可表达所递送的基因。该技术的一个实例在shalek et al.,pnas 107:25 1870(2010)中描述,其公开内容通过引用并入本文。
[0197]
magnetofection
tm
还可用于将核酸递送至靶细胞。magnetofection
tm
的原理是将核酸与阳离子磁性纳米粒缔合。磁性纳米粒由完全生物可降解的氧化铁制成,并用根据应用而异的特定阳离子专有分子包被。它们与基因载体(dna、sirna、病毒载体等)的缔合是通过盐诱导的胶体聚集和静电相互作用来实现的。随后通过由磁体产生的外部磁场的影响将磁性颗粒集中在靶细胞上。该技术在scherer et al.,gene therapy 9:102(2002)中详细描述,其公开内容通过引用并入本文。磁珠是可用于以温和且有效的方式转染靶细胞的另一种工具,因为该方法利用施加的磁场以引导核酸的摄取。该技术例如在us2010/0227406中详细描述,其公开内容通过引用并入本文。
[0198]
用于诱导靶细胞摄取外源核酸的另一种可用的工具是声穿孔,该技术涉及使用声音(通常是超声频率)用于改变细胞质膜的渗透性使细胞透化并允许多核苷酸穿透细胞膜。该技术例如在rhodes et al.,methods in cell biology 82:309(2007)中详细描述,其公开内容通过引用并入本文。
[0199]
微泡表示可用于根据本文中所述的方法修饰靶细胞的基因组的另一种潜在的载体。例如,通过糖蛋白vsv-g与例如基因组修饰蛋白质(例如核酸酶)的共过表达诱导的微泡可用于有效地将蛋白质递送到细胞中,该细胞随后催化内源性多核苷酸序列的位点特异性切割,以制备细胞基因组以用于共价并入目的多核苷酸,例如基因或调节序列。这样的囊泡(也称为gesicle)用于真核细胞的遗传修饰的用途例如在quinn et al.,genetic modification of target cells by direct delivery of active protein[摘要]、在methylation changes in early embryonic genes in cancer[摘要]、在proceedings of the 18th annual meeting of the american society of gene and cell therapy;2015 may 13,abstract no.122中详细描述。
[0200]
外泌体、胞外囊泡、微环dna、纳米质粒
tm
、ministring dna、狗骨头dna和封闭末端dna代表可用于根据本文中所述方法修饰靶细胞基因组的其他潜在载剂。
[0201]
在一些实施方案中,表达载体包含含有经修饰的核靶向序列的核酸序列。
[0202]
在一些实施方案中,表达载体包含环化(例如,用于有效表达)的核酸序列。
[0203]
iia.非病毒颗粒
[0204]
在一些实施方案中,本发明的特征在于包含非病毒颗粒的表达载体。在一些实施方案中,非病毒颗粒是选自包括以下的组中的任意一种或更多种:脂质纳米粒、脂质包膜、磷脂双层、脂质体、noisome、富勒烯、基于蛋白质的纳米粒、纳米晶体、树枝状聚合物、有机/无机胶体、聚乙二醇化脂质体、聚合物胶束、反胶束、混合胶束、敏感性胶束、多组分胶束、或
者多分子或单分子树枝状胶束。
[0205]
在一些实施方案中,本发明的特征在于包含非病毒颗粒的表达载体,所述非病毒颗粒与用于细胞类型特异性靶向或者细胞或组织向性优化的一种或更多种化学部分连接。
[0206]
iib.病毒衣壳蛋白
[0207]
在一些实施方案中,本发明的特征在于包含病毒衣壳蛋白的表达载体,以促进将核酸或载体引入到细胞中。在一些实施方案中,病毒衣壳蛋白是天然存在的衣壳或经改造的衣壳蛋白(例如,包含经修饰序列的衣壳)。
[0208]
病毒载体的衣壳蛋白构成病毒体的外部非核酸部分并由核酸编码。在一个实施方案中,病毒衣壳蛋白可在结构上由以下列表中的一种或更多种构成:包含天然和/或合成血清型的aav衣壳蛋白、一种或更多种血清型的慢病毒衣壳蛋白、一种或更多种血清型的逆转录病毒衣壳蛋白、一种或更多种血清型的疱疹病毒科衣壳蛋白、具有一种或更多种血清型的腺病毒科衣壳蛋白、具有一种或更多种血清型的细小病毒科衣壳蛋白、具有一种或更多种血清型的弹状病毒科衣壳蛋白、具有一种或更多种血清型的呼肠孤病毒科衣壳蛋白、具有一种或更多种血清型的正黏病毒科衣壳蛋白、具有一种或更多种血清型的布尼亚病毒科衣壳蛋白、具有一种或更多种血清型的黄病毒科衣壳蛋白、具有一种或更多种血清型的逆转录病毒科衣壳蛋白、具有一种或更多种血清型的副黏病毒科衣壳蛋白、具有一种或更多种血清型的马铃薯y病毒科衣壳蛋白、具有一种或更多种血清型的冠状病毒科衣壳蛋白、具有一种或更多种血清型的杯状病毒科衣壳蛋白、具有一种或更多种血清型的乳头瘤病毒科衣壳蛋白、具有一种或更多种血清型的痘病毒科衣壳蛋白、具有一种或更多种血清型的多瘤病毒科衣壳蛋白、或者具有一种或更多种血清型的任何其他已知病毒或类病毒衣壳蛋白。
[0209]
在一些实施方案中,天然存在的病毒衣壳蛋白是经修饰的(例如,通过缀合进行修饰以用于在天然存在的病毒衣壳蛋白的表面上表达非病毒肽以用于细胞类型特异性靶向,或者通过缀合进行修饰以用于在病毒衣壳蛋白、真核蛋白或蛋白质片段之间表达融合蛋白以用于缩小向性)。
[0210]
在一些实施方案中,经改造的病毒衣壳蛋白与配体缀合(例如,用于细胞类型特异性或调节免疫原性)。
[0211]
iii.用于表达治疗性核酸的示例性表达载体
[0212]
在一些实施方案中,表达载体是包含编码自杀基因、和fgf-18多肽或其功能片段的核酸的病毒载体(例如,aav2)。例如,病毒载体可包含与人fgf18(hfgf18)多肽有效连接的巨细胞病毒(cmv)增强子(cmvenh)、土拨鼠肝炎病毒转录后调节元件突变体6(wpremut6;已知显著提高表达水平但无启动子活性的dna元件)、牛生长激素多腺苷酸化信号(bghpa)、hsv-tk自杀基因、突变的sv40早期多腺苷酸化信号(sv40pa)和侧翼aav2反向末端重复序列(itr)的核酸序列(图1)。或者,例如,病毒载体可包含与hfgf18多肽有效连接的cmvenh、wpremut6、bghpa、rapacas9自杀基因、sv40pa和侧翼aav2itr的核酸序列(图2)。
[0213]
在一些实施方案中,表达载体是经修饰的(例如,以除去itr并将表达载体置于微环或可最佳靶向至核的任何其他构型以用于在有和没有整合的情况下进行有效表达)。
[0214]
iv.用于递送治疗性核酸的递送装置
[0215]
本发明可通过药物递送装置(例如基因枪、预填充注射器、自动注射器、气溶胶喷
雾剂、喷雾罐或贴片注射器)递送而无限制,或者可储存在安瓿、筒、胶囊、小瓶、成型-填充-密封(form-fill-seal)或吹-填充-密封(blow-fill-seal)容器中用于随后通过第二合适的方式施用。
[0216]
可对靶组织、外周(periphery)或远端组织或器官进行递送。因此,在自分泌的情况下,构建体可在为表达的蛋白质或酶的靶标的细胞中表达。或者,构建体可由在为表达的蛋白质的最终靶标的细胞和组织的外周、周围、邻近或与其混合的细胞表达。最后,构建体可由在靶组织或器官之外的细胞表达,并且以内分泌方式作用于一种或更多种靶组织、器官或细胞。特别地,在不限制本发明的范围的情况下,该构建体可被递送至滑膜关节,并且可靶向软骨细胞以用于表达fgf-18并将fgf-18递送至邻近的软骨细胞,或者该构建体可被递送至衬于关节囊的细胞以用于表达fgf-18并将fgf-18递送至近端软骨细胞。
[0217]
药物组合物的配制和给药
[0218]
本文中所述的表达载体(例如,核酸)可被配制成药物组合物,其用于以适合于体内施用的生物相容形式施用于表现出软骨病症或处于发生软骨病症的风险中的患者例如人患者。包含例如本文中所述的表达载体(例如包含编码自杀基因和fgf-18多肽或其功能片段的核酸的aav2或aav5)的药物组合物通常包含可药用稀释剂或载体。药物组合物可包含例如无菌盐水溶液和核酸(例如,由例如无菌盐水溶液和核酸组成)。无菌盐水通常是药用级盐水。药物组合物可包含例如无菌水和核酸(例如,由例如无菌水和核酸组成)。无菌水通常是药用级水。药物组合物可包含以下(例如,由以下组成):例如,缓冲剂(例如,磷酸缓冲盐水(phosphate-buffered saline,pbs)、2-(n-吗啉代)乙磺酸(mes)、2,2-双(羟甲基)-2,2’,2
”‑
次氮基三乙醇(bis-tris)、二甘氨酸(gly-gly)、盐水、2-氨基-2-甲基-1-丙醇(amp)或n-(2-羟基-1,1-双(羟甲基)乙基)甘氨酸(tricine))和核酸。缓冲剂通常是药用级缓冲剂。
[0219]
在某些实施方案中,药物组合物包含一种或更多种表达载体和一种或更多种赋形剂。在某些实施方案中,赋形剂选自水、盐溶液、醇、聚乙二醇、明胶、乳糖、淀粉酶、硬脂酸镁、滑石、硅酸、黏性石蜡、羟甲基纤维素和聚乙烯吡咯烷酮。
[0220]
在某些实施方案中,表达载体可与可药用活性和/或惰性物质混合用于制备药物组合物或制剂。用于配制药物组合物的组合物和方法取决于许多标准,其包括但不限于施用途径、疾病程度或待施用的剂量。
[0221]
在某些实施方案中,包含表达载体的药物组合物涵盖抑制剂的任何可药用盐、抑制剂的酯或这样的酯的盐。在某些实施方案中,包含表达载体的药物组合物在施用于对象(例如,人)之后,能够(直接或间接)提供生物活性代谢物或其残基。因此,例如,本公开内容还涉及抑制剂的可药用盐、前药、这样的前药的可药用盐和其他生物等同物。合适的可药用盐包括但不限于钠盐和钾盐。在某些实施方案中,前药包含与表达载体连接的一种或更多种缀合物基团,其中该缀合物基团被体内的内源性核酸酶切割。
[0222]
脂质部分已以多种方法用于核酸治疗。在某些这样的方法中,将核酸引入到预形成的脂质体或脂质复合物中,其由阳离子脂质和中性脂质的混合物制成。在某些方法中,在不存在中性脂质的情况下形成具有单阳离子脂质或多阳离子脂质的dna复合物。在某些实施方案中,选择脂质部分以提高药剂向特定细胞或组织的分布。在某些实施方案中,选择脂质部分以提高药剂向脂肪组织的分布。在某些实施方案中,选择脂质部分以提高药剂向肌
肉组织的分布。
[0223]
在某些实施方案中,药物组合物包含递送系统。递送系统的一些实例包括但不限于脂质体和乳剂。某些递送系统可用于制备某些药物组合物,包括包含疏水性化合物的药物组合物。在某些实施方案中,使用某些有机溶剂例如二甲亚砜。
[0224]
在某些实施方案中,药物组合物包含一种或更多种组织特异性递送分子,其被设计用于将本发明的一种或更多种药剂递送至特定组织或细胞类型。例如,在某些实施方案中,药物组合物包含用组织特异性抗体包被的脂质体。
[0225]
在某些实施方案中,药物组合物包含共溶剂系统。某些这样的共溶剂系统包含例如苯甲醇、非极性表面活性剂、水混溶性有机聚合物和水相。在某些实施方案中,这样的共溶剂系统用于疏水化合物。这样的共溶剂系统的一个非限制性实例是vpd共溶剂系统,其为包含3%w/v苯甲醇、8%w/v非极性表面活性剂聚山梨醇酯80
tm
((x)-山梨糖醇单-9-十八碳烯酸聚(氧基-1,2-乙烷二基))和65%w/v聚乙二醇300的无水乙醇溶液。这样的共溶剂系统的比例可在不显著改变其溶解度和毒性特征的情况下发生显著变化。此外,共溶剂组分的身份可变化:例如,可使用其他表面活性剂代替聚山梨醇酯80
tm
((x)-山梨糖醇单-9-十八碳烯酸聚(氧基-1,2-乙烷二基));聚乙二醇的级分尺寸可变化;其他生物相容性聚合物可替代聚乙二醇,例如聚乙烯吡咯烷酮;以及其他糖或多糖可替换右旋糖。
[0226]
在某些实施方案中,制备用于通过注射(例如,静脉内、关节内、软骨下、滑膜内或软骨内)施用的药物组合物。在某些这样的实施方案中,药物组合物包含载体并且被配制在水溶液中,例如水或生理相容性缓冲剂,例如hanks溶液、林格氏(ringer’s)溶液或生理盐水缓冲剂。在某些实施方案中,包含其他成分(例如,有助于溶解或用作防腐剂的成分)。在某些实施方案中,使用合适的液体载体、助悬剂等制备可注射混悬剂。某些注射用药物组合物以单位剂量形式例如在安瓿中或在多剂量容器中存在。某些注射用药物组合物是油性或水性载剂中的混悬剂、溶液剂或乳剂,并且可包含配制剂,例如助悬剂、稳定剂和/或分散剂。适用于注射用药物组合物中的某些溶剂包括但不限于亲脂性溶剂和脂肪油(例如芝麻油)、合成脂肪酸酯(例如油酸乙酯或甘油三酯)、以及脂质体。
[0227]
如本文中所述,施用于对象用于治疗软骨病症(例如,骨关节炎)的药物组合物的剂量可取决于例如透明软骨的形态和或表达谱、对象、药物配制方法、施用方法(例如施用时间)、对象的年龄、体重、性别、正在治疗的软骨病症的严重程度、以及对象是否已经用组合治疗进行治疗。施用的药物组合物的剂量可以为例如0.1mg至1.0mg(例如0.2至0.9mg、0.3至0.8mg、0.4至0.6mg、或约0.5mg)。药物组合物可以以任何合适的剂量施用。剂量的一些非限制性实例为约0.3mg药物组合物至约0.7mg药物组合物(例如,约0.31mg药物组合物至约0.69mg药物组合物、约0.33mg药物组合物至约0.67mg药物组合物、约0.38mg药物组合物至约0.62mg药物组合物、约0.48mg药物组合物至约0.58mg药物组合物、或约0.53mg药物组合物)。另外的示例性剂量为约0.1mg药物组合物至约3.0mg药物组合物(例如,约0.2mg药物组合物至约2.9mg药物组合物、约0.4mg药物组合物至约2.7mg药物组合物、约0.9mg药物组合物至约2.2mg药物组合物、约1.4mg药物组合物至约1.7mg的药物组合物、或约1.55mg药物组合物)。
[0228]
可以以任何合适的剂量施用药物组合物,使得递送的病毒颗粒的数目为约1.0
×
109vg/ml至约4.5
×
10
11
vg/ml(例如,约1.1
×
109vg/ml至约4.4
×
10
11
vg/ml、约1.5
×
109vg/
ml至约4.0
×
10
11
vg/ml、约2.5
×
109vg/ml至约3.0
×
10
11
vg/ml、或约9.1
×
10
10
vg/ml)。
[0229]
本文中所述的组合物可以以足以改善软骨病症(例如骨关节炎)的一种或更多种病理特征的量施用。施用本文中所述的组合物可分别改善软骨细胞形态和/或表达谱,以更接近地与与透明软骨相关的胞外基质的形态和/或表达谱类似;分别改善滑膜细胞形态和/或表达谱,以更接近地与与透明软骨相关的胞外基质的形态和/或表达谱类似;提高软骨细胞增殖、提高软骨细胞前体增殖、提高软骨厚度、或提高总股胫关节软骨厚度。可使用标准技术(例如酶联免疫测定、western印迹分析、免疫组织化学分析或定量逆转录聚合酶链反应)评估fgf-18的水平,以比较组织样品中治疗之前和之后对象中fgf-18基因和/或蛋白质的水平。根据评价的结局,对象可接受另外的治疗。
[0230]
药盒
[0231]
本文中所述的组合物可在用于治疗软骨病症的药盒中提供。药盒可包含一种或更多种如本文中所述的表达载体或药物组合物。药盒可包含指导药盒使用者(例如医师)进行任何一种本文中所述的方法的药品说明书。药盒可任选地包含注射器或其他用于施用组合物的装置。药盒可任选地包含盒、显窃启密封件、针或预填充注射器。在一些实施方案中,药盒可包含一种或更多种另外的治疗剂。
[0232]
组合治疗
[0233]
本文中所述的表达载体可与用于治疗软骨病症的一种或更多种另外的治疗剂组合施用。一种或更多种另外的治疗剂可包含非甾体抗炎剂(例如吡罗昔康(piroxicam)、布洛芬(ibuprofen)、塞来昔布(celecoxib)、阿司匹林(aspirin)、依托度酸(etodolac)、美洛昔康(meloxicam)、双氯芬酸(diclofenac)、吲哚美辛(indomethacin)和萘普生(naproxen))、镇痛剂(例如辣椒素和对乙酰氨基酚)、膳食补充剂(例如,s-腺苷甲硫氨酸和透明质酸)、或麻醉剂(例如曲马多(tramadol)),或其组合。
[0234]
实施例
[0235]
旨在举例说明而非限制本公开内容的以下实施例旨在向本领域普通技术人员提供关于可如何使用、制备和评价本文中所述的组合物和方法的说明。这些实施例旨在仅是对本公开内容的示例,而非旨在限制发明人视为其发明的范围。
[0236]
实施例1:使用病毒载体在人对象中治疗软骨病症
[0237]
根据本文中公开的方法,可向对象例如人对象施用药物组合物(例如,包含编码自杀基因和fgf-18多肽或其功能片段的核酸的aav2或aav5病毒载体以及可药用载体、稀释剂或赋形剂;图1和2)以在对象中治疗软骨病症。为此,向患者施用药物组合物(例如,包含编码自杀基因和fgf-18多肽或其功能片段的核酸的aav2或aav5病毒载体以及可药用载体、稀释剂或赋形剂)。将其药物组合物静脉内、关节内、软骨下、滑膜内或软骨内施用于对象。可将其药物组合物静脉内、关节内、软骨下、滑膜内、或软骨内和双侧施用于滑膜关节。药物组合物可以以任何合适的剂量施用。剂量的一些非限制性实例为约0.1mg至0.5mg,例如0.1mg、0.2mg、0.3mg、0.4mg和0.5mg的药物组合物。对象可接受约0.5mg至约1.0mg剂量的药物组合物,例如对象可接受约1.0mg剂量的药物组合物。
[0238]
实施例2:使用慢病毒载体在人对象中治疗软骨病症
[0239]
根据本文中公开的方法,可向对象例如人对象施用药物组合物(例如,包含编码自杀基因和fgf-18多肽或其功能片段的核酸的慢病毒病毒载体以及可药用载体、稀释剂或赋
形剂)以在对象中治疗软骨病症。为此,向患者施用药物组合物(例如,包含编码自杀基因和fgf-18多肽或其功能片段的核酸的慢病毒病毒载体以及可药用载体、稀释剂或赋形剂)。将其药物组合物静脉内、关节内、软骨下、滑膜内或软骨内施用于对象。可将其药物组合物静脉内、关节内、软骨下、滑膜内、或软骨内和双侧施用于滑膜关节。药物组合物可以以任何合适的剂量施用。剂量的一些非限制性实例为约0.1mg至0.5mg,例如0.1mg、0.2mg、0.3mg、0.4mg和0.5mg的药物组合物。对象可接受约0.5mg至约1.0mg剂量的药物组合物,例如对象可接受约1.0mg剂量的药物组合物。
[0240]
实施例3:使用非病毒颗粒在人对象中治疗软骨病症
[0241]
根据本文中公开的方法,可向对象例如人对象施用药物组合物(例如,包含dna微环和含有编码自杀基因和fgf-18多肽或其功能片段的核酸的非病毒颗粒(例如,脂质纳米粒)的表达载体以及可药用载体、稀释剂或赋形剂)以在对象中治疗软骨病症。为此,向患者施用药物组合物(例如,包含dna微环和含有编码自杀基因和fgf-18多肽或其功能片段的核酸的非病毒颗粒(例如,脂质纳米粒)的表达载体以及可药用载体、稀释剂或赋形剂)。将其药物组合物静脉内、关节内、软骨下、滑膜内或软骨内施用于对象。可将其药物组合物静脉内、关节内、软骨下、滑膜内、或软骨内和双侧施用于滑膜关节。药物组合物可以以任何合适的剂量施用。剂量的一些非限制性实例为约0.001mg/kg至1.0mg/kg,例如0.001mg/kg、0.002mg/kg、0.003mg/kg、0.004mg/kg、0.005mg/kg、0.015mg/kg、0.055mg/kg、0.155mg/kg、0.500mg/kg和1.0mg/kg的药物组合物。对象可接受约0.001/kg mg至约1.0mg/kg剂量的药物组合物,例如对象可接受约1mg/kg剂量的药物组合物。
[0242]
其他实施方案
[0243]
本说明书中提及的所有出版物、专利和专利申请均通过引用并入本文,程度如同每个独立出版物或专利申请被具体地和单独地指明通过引用并入一样。
[0244]
虽然本发明已结合其具体实施方案进行了描述,但应理解其能够进行进一步修改,并且本技术旨在涵盖通常遵循本发明的原则并且包括了对本发明的这样的偏离的对本发明的任何更改、使用或改编,所述偏离在本发明所属领域中已知的或惯例实践之内,以及可适用于上文所述和在权利要求书给出的范围内的基本特征。
[0245]
另一些实施方案在权利要求书之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1