在免疫球蛋白重链编码序列中具有DH-DH重排能力的非人动物的制作方法
在免疫球蛋白重链编码序列中具有dh
‑
dh重排能力的非人动物
1.本技术是申请号为201980039940.2、申请日为2019年6月14日、发明名称为“在免疫球蛋白重链编码序列中具有dh
‑
dh重排能力的非人动物”的中国发明专利申请的分案申请,原申请为国际申请号为pct/us2019/037285的国家阶段申请,该国际申请要求2018年6月14日提交的美国临时专利申请第62/685,203号、2018年7月23日提交的美国临时专利申请第62/702,206号以及2019年3月1日提交的美国临时专利申请第62/812,580号的优先权。
2.序列表
3.序列表的正式副本以ascii格式的序列表通过efs
‑
web以电子方式提交,文件名为“10347_st25.txt”,该文件创建于2019年6月13日,大小为约50千字节,与本说明书同时提交。该ascii格式的文档中含有的序列表是说明书的一部分,并且以引用的方式整体并入本文。
背景技术:
4.单克隆抗体产品彻底改变了生物制药行业,并在几种疾病的治疗方面取得了重大进展。这些单克隆抗体产品中的许多产品都利用了抗体分子(即传统的免疫球蛋白基因区段)的天然特征,并且在一些情况下并入了其他特征,诸如标记(例如聚乙二醇化、放射性标记)或与其他药物缀合。按照目前的批准速率,到2020年,预计将有大约70种单克隆抗体产品投放市场。尽管取得了这些进展并且通过将单克隆抗体用于治疗用途而获得了知识,但是与单克隆抗体难以结合和/或接近的靶标相关联的疾病仍然持续存在,这突出了对开发不同的有效治疗方法的需求。
技术实现要素:
5.本发明包括认识到,需要对非人动物(例如,啮齿动物(例如大鼠,例如小鼠)进行工程化,以建立额外的体内系统来鉴定和开发可以用于治疗多种疾病的新的基于抗体的治疗剂和在一些实施方案中抗体药剂(例如,单克隆抗体和/或其片段)。此外,本发明还包括在包含一个或多个d
h
区段(其被工程化以有效地连接至允许d
h
与d
h
重排的重组信号序列,所述重排导致含有以与野生型(或参考)cdr3相比氨基酸长度更长并且在一些实施方案中指导与特定抗原的结合的多样性为特征的互补决定区三(cdr3)的抗体表达增加)的免疫球蛋白重链可变区(例如异源免疫球蛋白重链可变区,例如人免疫球蛋白重链可变区)内具有工程化重链多样性(d
h
)簇(或工程化d
h
区域)的非人动物的需要。在一些实施方案中,本文所述的非人动物提供了用于开发施用至人类的抗体和/或基于抗体的治疗剂的体内系统。
6.本文描述的是核苷酸分子,其包含有效地连接至23聚体重组信号序列(rss)的至少一个免疫球蛋白重链多样性(d
h
)基因区段,任选地其中所述d
h
基因区段可以位于例如免疫球蛋白重链可变区(例如人或人源化免疫球蛋白重链可变区)的工程化d
h
区内。这样,在一些实施方案中,本文所述的核苷酸分子包含含有与23聚体(rss)有效地连接的至少一个d
h
基因区段的工程化免疫球蛋白重链多样性(d
h
)区。在一些实施方案中,工程化d
h
区包含
(i)有效地连接至23聚体rss的至少一个d
h
基因区段和(ii)在一侧侧接有12聚体rss并且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段,其中(i)有效地连接至23聚体rss的至少一个d
h
基因区段和(ii)在一侧侧接有12聚体rss并且在另一侧侧接有另一个12聚体rss的种系d
h
基因区段被有效地连接,使得(i)和(ii)能够连接成根据12/23规则的d
h
‑
d
h
重组事件。还提供了靶向载体、包含本文所述核苷酸分子的非人动物(例如,啮齿动物(例如,大鼠或小鼠))和非人动物细胞(例如,啮齿动物细胞(例如,大鼠细胞或小鼠细胞)、使用本文所述的核苷酸分子的方法等。
7.在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段包含有效地连接至23聚体rss的人d
h
基因区段。在一些实施方案中,人d
h
基因区段包含至少19个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,人d
h
基因区段包含至少20个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,人d
h
基因区段包含至少23个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,人d
h
基因区段包含至少28个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,人d
h
基因区段包含至少31个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,人d
h
基因区段包含至少37个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含有效地连接至23聚体rss的人d
h
2基因区段。在一些实施方案中,d
h
2基因区段包含至少30个核苷酸和/或编码两个半胱氨酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含选自由以下组成的组的d
h
基因区段:人d
h3‑
3基因区段、d
h3‑
9基因区段、d
h3‑
10基因区段、d
h3‑
16基因区段、d
h3‑
22基因区段、人d
h2‑
2基因区段、人d
h2‑
8基因区段、或人d
h2‑
15基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含选自由以下组成的组的人d
h
基因区段:人d
h3‑
3基因区段、人d
h2‑
2基因区段、人d
h2‑
8基因区段、和人d
h2‑
15基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含选自由以下组成的组的人d
h
基因区段:人d
h3‑
3基因区段、人d
h2‑
2基因区段、人d
h2‑
8基因区段、和人d
h2‑
15基因区段。在一些实施方案中,人d
h
基因区段包含人d
h3‑
3基因区段。在一些实施方案中,人d
h
基因区段包含人d
h2‑
2基因区段。在一些实施方案中,人d
h
基因区段包含人d
h2‑
8基因区段。在一些实施方案中,人d
h
基因区段包含人d
h2‑
15基因区段。
8.在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段包含:(a)有效地连接至23聚体rss的人d
h3‑
3基因区段,任选地其中所述23聚体rss与人d
h3‑
3基因区段的5'端相邻,(b)有效地连接至23聚体rss的人d
h2‑
2基因区段,任选地其中所述23聚体rss与人d
h2‑
2基因区段的3'端相邻,(c)有效地连接至23聚体rss的人d
h2‑
8基因区段,任选地其中所述23聚体rss与人d
h2‑
8基因区段的3'端相邻,(d)有效地连接至23聚体rss的人2
‑
15基因区段,任选地其中所述23聚体rss与人d
h2‑
15基因区段的3'端相邻,或(e)(a)
‑
(d)的任何组合。
9.在一些实施方案中,本文所述的核苷酸分子(例如,有效地连接至23聚体rss的d
h
基因区段,工程化d
h
区、免疫球蛋白重链可变区等)包含含有seq id no:52所示序列的核苷酸序列。
10.在一些实施方案中,本文所述的核苷酸分子(例如,有效地连接至23聚体rss的d
h
基因区段,工程化d
h
区、免疫球蛋白重链可变区等)包含含有seq id no:61所示序列的核苷酸序列。
11.在一些实施方案中,本文所述的核苷酸分子(例如,有效地连接至23聚体rss的d
h
基因区段,工程化d
h
区、免疫球蛋白重链可变区等)包含含有seq id no:70所示序列的核苷酸序列。
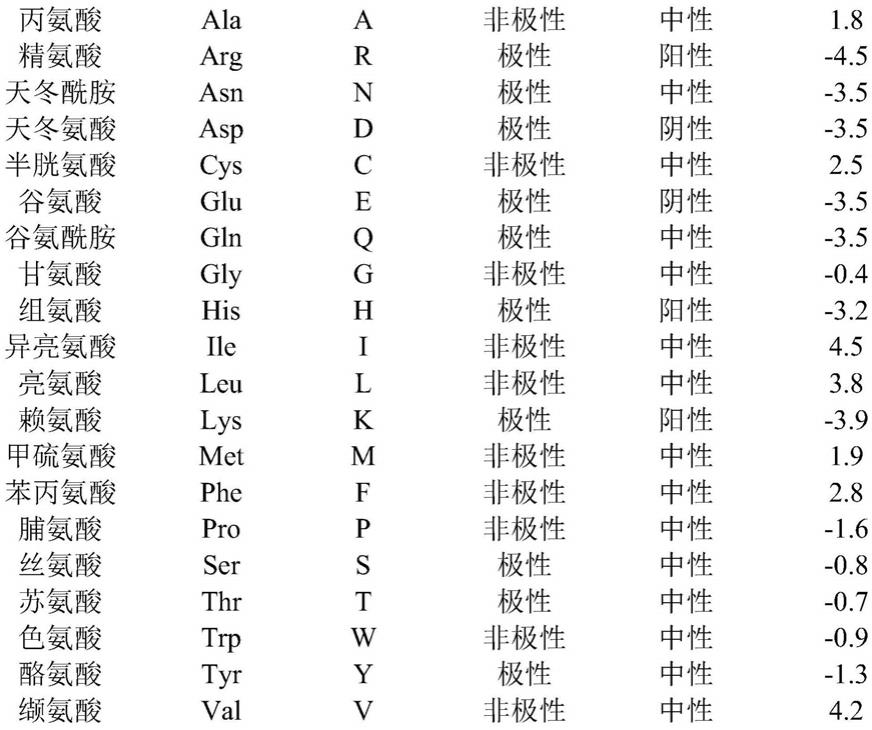
12.在一些实施方案中,本文所述的核苷酸分子(例如,有效地连接至23聚体rss的d
h
基因区段,工程化d
h
区、免疫球蛋白重链可变区等)包含含有seq id no:71所示序列的核苷酸序列。
13.在一些实施方案中,本文所述的核苷酸分子(例如,有效地连接至23聚体rss的d
h
基因区段,工程化d
h
区、免疫球蛋白重链可变区等)包含含有seq id no:72所示序列的核苷酸序列。
14.在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段从5’至3’包含23聚体rss和d
h
基因区段,例如从5’至3’包含23聚体rss、(人)d
h
基因区段和12聚体rss,例如所述23聚体rss与d
h
基因区段的5'端相邻,例如所述d
h
基因区段有效地连接至5'端23聚体rss。在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段包含有效地连接至5'端23聚体rss的人d
h3‑
3基因区段,例如核苷酸分子从5’至3’包含23聚体rss、人d
h3‑
3基因区段和12聚体rss。
15.包含至少一个d
h
基因区段与5'端23聚体rss的工程化d
h
区可以还包含在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段(例如,在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段包含种系d
h
基因区段,例如在其种系构型中的d
h
基因区段等),其中所述未重排的d
h
基因区段位于有效地连接至5'端23聚体的至少一个d
h
基因区段的上游并与之有效地连接。在一些实施方案中,在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段包含在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的人d
h
基因区段。
16.在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段从5’至3’包含d
h
基因区段和23聚体rss,例如从5’至3’包含12聚体rss、(人)d
h
基因区段和23聚体rss,例如所述23聚体rss与d
h
基因区段的3'端相邻,例如所述d
h
基因区段有效地连接至3'端23聚体等。在一些实施方案中,有效地连接至3'端23聚体rss的d
h
基因区段包含有效地连接至3'端23聚体rss的人d
h
2基因区段,其中d
h
2基因区段选自由以下组成的组:人d
h2‑
2基因区段、人d
h2‑
8基因区段和人d
h2‑
15基因区段。在一些实施方案中,有效地连接至23聚体rss的d
h
基因区段从5’至3’包含:有效地连接至3'端23聚体rss的人d
h2‑
2基因区段、有效地连接至3'端23聚体rss的人d
h2‑
8基因区段、和有效地连接至3'端23聚体rss的人d
h2‑
15基因区段。在一些实施方案中,有效地连接至3'端23聚体rss的d
h
基因区段从5’至3’包含:含有12聚体rss、人d
h2‑
2基因区段和23聚体rss的第一连续核苷酸序列,含有12聚体rss、人d
h2‑
8基因区段和23聚体rss的第二连续核苷酸序列,以及含有12聚体rss、人d
h2‑
15基因区段和23聚体rss的第三连续核苷酸序列。
17.包含有效地连接至3'端23聚体rss的至少一个d
h
基因区段的工程化d
h
区可以还包含在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段(例如,在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段可以包含种系d
h
基因区段,例如在其种系构型中的d
h
基因区段等),其中所述在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段位于有效地连接至3'端23聚体rss的至少一个d
h
基因区段的下游并与之有效地连接。在一些实施方案中,在一侧
侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段包含在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的人d
h
基因区段。
18.在一些实施方案中,如本文所述的工程化d
h
区包含(i)一个或多个未重排的人d
h
基因区段,其中所述一个或多个人d
h
基因区段中的每一个在其5'端和3'端侧接有12聚体rss,和(ii)包含人d
h
基因区段(例如人d
h3‑
3基因区段)的、有效地连接至23聚体rss的至少一个d
h
基因区段在其5'端有效地连接至23聚体rss。在一些实施方案中,如本文所述的工程化dh区从5'至3'包含(i)有效地连接至23聚体rss的至少一个d
h
基因区段,例如至少一个人d
h
2基因区段在其3'端有效地连接至23聚体rss,任选地其中在其3'端有效地连接至23聚体rss的至少一个人d
h
2基因区段包含在其3'端有效地连接至23聚体rss的人d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段、或其任何组合,以及(ii)一个或多个人d
h
基因区段,其中所述一个或多个人d
h
基因区段中的每一个在其5'端和3'端侧接有12聚体rss。
19.在一些实施方案中,如本文所述的工程化d
h
区仅包含人d
h
基因区段。
20.在一些实施方案中,本文所述的核苷酸分子(例如,工程化d
h
区、免疫球蛋白重链可变区等)包含有效地连接至23聚体rss的d
h
基因区段和在一侧侧接有12聚体rss并且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段,其中所述有效地连接至23聚体rss的d
h
基因区段和所述在一侧侧接有12聚体rss并且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段尚未经历与(i)另一个d
h
基因区段、(ii)v
h
基因区段、(iii)j
h
基因区段、或(iv)其任何组合的重组。在一些实施方案中,本文所述的核苷酸分子包括包含工程化d
h
区(其包含已经与(i)另一个d
h
基因区段、(ii)v
h
基因区段、(iii)j
h
基因区段、或其任何组合重组的一个或多个d
h
基因区段)的分子,例如包含编码免疫球蛋白重链可变区的重排vdj或vddj编码序列的核苷酸分子。
21.因此,在一些实施方案中,本文所述的包含如本文所述的工程化d
h
区的核苷酸分子在有效连接中还包含:(a)位于工程化d
h
区的上游并与之有效地连接的至少一个未重排的免疫球蛋白重链可变(v
h
)基因区段(例如,未重排的人v
h6‑
1基因区段),(b)位于工程化d
h
区的下游并与之有效地连接的至少一个未重排的免疫球蛋白重链连接(j
h
)基因区段(例如,未重排的人j
h
6基因区段),或者(a)和(b)的组合。
22.在一些实施方案中,所述至少一个未重排的v
h
基因区段包含功能性未重排的人v
h
基因区段的全部库,其跨越并包括在未重排的人v
h3‑
74和未重排的人v
h1‑
6基因区段。在一些实施方案中,所述至少一个未重排的v
h
基因区段包含处于种系构型中的功能性未重排的人v
h
基因区段的全部库,其跨越并包括未重排的人v
h3‑
74和未重排的人v
h1‑
6基因区段。在一些实施方案中,所述至少一个未重排的j
h
基因区段包含未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。在一些实施方案中,所述至少一个未重排的j
h
基因区段包含未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、和未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。在一些实施方案中,所述至少一个未重排的j
h
基因区段包含处于种系构型中的未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、和未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。
23.在一些实施方案中,本文所述的核苷酸分子包含含有如本文所述的工程化d
h
区的
免疫球蛋白重链可变(v
h
)区,例如,在可操作的连接中从5’至3’包含:
24.(a)至少一个未重排的免疫球蛋白重链可变(v
h
)基因区段,
25.(b)包含有效地连接至23聚体rss的至少一个d
h
基因区段的工程化d
h
区,和
26.(c)至少一个未重排的免疫球蛋白重链连接(j
h
)基因区段。
27.在一些实施方案中,
28.(a)所述至少一个未重排的v
h
基因区段包含
29.(i)未重排的人v
h6‑
1基因区段,
30.(ii)未重排的人v
h2‑
1基因区段和未重排的人v
h6‑
1基因区段,和/或
31.(iii)所有功能性未重排的人v
h
基因区段,其跨越并包括未重排的人v
h3‑
74至未重排的人v
h6‑
1基因区段,例如,处于种系构型中的所有功能性未重排的人v
h
基因区段,任选地其中啮齿动物adam6基因替换在未重排的人v
h2‑
1与v
h6‑
1基因区段之间的假基因;
32.(b)工程化d
h
区从5’至3’包含:
33.(i)一个或多个(例如多个)未重排的人d
h
基因区段,其中所述多个未重排的人d
h
基因区段中的每一个在其5'端和3'端侧接有12聚体rss;以及在其5'端有效地连接至23聚体rss的人d
h
基因区段,任选地其中所述多个未重排的人d
h
基因区段包含跨越并包括未重排的人d
h1‑
1基因区段和未重排的人d
h1‑
26基因区段的未重排的人d
h
基因区段,和/或其中在其5'端有效连接至23聚体rss的人基因区段是人d
h3‑
3基因区段,例如,其中所述工程化d
h
包含处于种系构型中的未重排的人d
h
基因区段的全部库,例外是未重排的人d
h7‑
27基因区段(其被有效地连接至5'端23聚体rss的d
h3‑
3基因区段替换);
34.(ii)在其3'端与23聚体rss有效地连接的至少一个人d
h
基因区段以及一个或多个(例如多个)人d
h
基因区段,其中所述一个或多个人d
h
基因区段中的每一个在其5'端和3'端侧接有12聚体rss,任选地其中在其3'端与23聚体rss有效地连接的所述至少一个人d
h
基因区段包含在其3'端有效地连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段,和/或其中所述一个或多个人d
h
基因区段包含跨越并包括未重排的人d
h1‑
1基因区段和未重排的人d
h7‑
27基因区段的d
h
基因区段,任选地其中所述工程化d
h
包含处于种系构型中的未重排的人d
h
基因区段的全部库,例外是未重排的人d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段分别被在其3'端有效地连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、和在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段替换;
35.(iii)或者(b)(i)和(b)(ii)的组合;和
36.(c)至少一个未重排的j
h
基因区段包含
37.(i)未重排的人j
h
6基因区段,
38.(ii)未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段,和/或
39.(iii)未重排的人j
h
基因区段的全部库,例如,未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段,任选地其中所述未重排的人j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中。在一些实施方案中,免疫球蛋白v
h
区(包含至少一个功能性v
h
基因区段、工程化d
h
区和至少一个功能性j
h
基因区段)是人免疫球蛋白v
h
区,例如,每个基因区段
(例如在其中的每个v
h
、d
h
和j
h
基因区段)(包括有效地连接至23聚体rss的d
h
基因区段)是人(v
h
、d
h
或j
h
)基因区段。
40.在一些实施方案中,包含如本文所述的免疫球蛋白v
h
区的核苷酸分子在有效连接中从5’至3’包含
41.(a)至少一个未重排的人v
h6‑
1基因区段,例如,跨越并包括未重排的人v
h3‑
74至未重排的人v
h6‑
1基因区段的所有功能性未重排的人v
h
基因区段的全部或部分,例如功能性未重排的人v
h
基因区段的全部库,任选地包括在两个未重排的人v
h
基因区段之间的啮齿动物adam6基因,例如(例如其中所述啮齿动物adam6基因位于人v
h1‑
2基因区段与人v
h6‑
1基因区段之间);
42.(b)人工程化d
h
区,其从5’至3’包含跨越并包括在未重排的人d
h1‑
1基因区段和未重排的人d
h1‑
26基因区段的处于种系构型中的未重排的人d
h
基因区段,以及有效地连接至5'端23聚体rss的未重排的人d
h3‑
3基因区段,例如,处于种系构型中的未重排的人d
h
基因区段的全部库,例外是被有效地连接至5'端23聚体rss的未重排的人d
h3‑
3基因区段替换的未重排的人d
h7‑
27基因区段,以及
43.(c)至少一个未重排的人j
h
6基因区段。
44.在一些实施方案中,包含如本文所述的免疫球蛋白v
h
区的核苷酸分子在有效连接中从5’至3’包含
45.(a)至少一个未重排的人v
h6‑
1基因区段,例如,跨越并包括未重排的人v
h3‑
74至未重排的人v
h6‑
1基因区段的所有功能性未重排的人v
h
基因区段的全部或部分,例如功能性未重排的人v
h
基因区段的全部库,任选地包括在两个未重排的人v
h
基因区段之间的啮齿动物adam6基因,例如(例如其中所述啮齿动物adam6基因位于人v
h1‑
2基因区段与人v
h6‑
1基因区段之间);
46.(b)人工程化d
h
区,其从5’至3’包含跨越并包括在未重排的人d
h1‑
1基因区段和未重排的人d
h1‑
26基因区段之间的处于种系构型中的未重排的人d
h
基因区段,以及有效地连接至5'端23聚体rss的未重排的人d
h3‑
3基因区段,例如,处于种系构型中的未重排的人d
h
基因区段的全部库,例外是被有效地连接至5'端23聚体rss的未重排的人d
h3‑
3基因区段替换的未重排的人d
h7‑
27基因区段,以及
47.(c)未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。
48.在一些实施方案中,包含如本文所述的免疫球蛋白v
h
区的核苷酸分子在有效连接中从5’至3’包含
49.(a)至少一个未重排的人v
h6‑
1基因区段,例如,跨越并包括未重排的人v
h3‑
74至未重排的人v
h6‑
1基因区段的所有功能性未重排的人v
h
基因区段的全部或部分,例如功能性未重排的人v
h
基因区段的全部库,任选地包括在两个未重排的人v
h
基因区段之间的啮齿动物adam6基因,例如(例如其中所述啮齿动物adam6基因位于人v
h1‑
2基因区段与人v
h6‑
1基因区段之间);
50.(b)人工程化d
h
区,其从5’至3’包含未重排的人d
h1‑
1基因区段、在其3'端有效地连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段、以及跨越并包括未重排的人d
h3‑
16基因区段和未重排的人d
h7‑
27基因区段的未重排的人d
h
基因区段,任选地其中所述工程化d
h
包含处于种系构型中的未重排的人d
h
基因区段的全部库,例外是未重排的人d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段分别被在其3'端有效地连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、和在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段替换,和
51.(c)未重排的人j
h
基因区段的全部库,例如,未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段,任选地其中所述未重排的人j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中。
52.在一些实施方案中,如本文所述的核苷酸分子从5’至3’包含(a)含有至少一个(人)v
h
基因区段、如本文所述的(人)工程化d
h
区和至少一个(人)j
h
基因区段的(人)免疫球蛋白重链可变(v
h
)区,其有效地连接至(b)重链免疫球蛋白恒定区(c
h
)或其一部分,任选地其中所述c
h
是包含啮齿动物内含子增强子区域、啮齿动物igm基因、啮齿动物igd基因、啮齿动物igg基因、啮齿动物iga基因、啮齿动物ige基因或其任何组合的啮齿动物c
h
。在一些实施方案中,如本文所述的核苷酸分子从5’至3’包含(a)含有至少一个人v
h
基因区段、如本文所述的人工程化d
h
区和至少一个人j
h
基因区段的人免疫球蛋白重链v
h
区,其有效地连接至(b)包含至少一个啮齿动物内含子增强子区域和任选地啮齿动物igm基因的啮齿动物c
h
区。在一些实施方案中,本文所述的核苷酸分子从5’至3’包含(a)含有至少一个人v
h
基因区段、如本文所述的人工程化d
h
区和至少一个人j
h
基因区段的人v
h
区,其有效地连接至(b)包含至少一个啮齿动物内含子增强子区域和啮齿动物igm基因的啮齿动物c
h
区。在一些实施方案中,本文所述的核苷酸分子从5’至3’包含(a)含有至少一个人v
h
基因区段、如本文所述的人工程化d
h
区和至少一个人j
h
基因区段的人v
h
区,其有效地连接至(b)例如在内源性啮齿动物免疫球蛋白重链基因座处的内源性啮齿动物c
h
区。在一些实施方案中,啮齿动物可以是大鼠。在一些实施方案中,啮齿动物可以是小鼠。
53.在一些实施方案中,如本文所述的核苷酸分子还包含啮齿动物adam6基因。在一些实施方案中,啮齿动物adam6基因位于人v
h2‑
1与v
h6‑
1基因区段之间,例如,替换位于处于种系构型中的人v
h2‑
1与v
h6‑
1基因区段之间的人adam6基因。在一些实施方案中,啮齿动物可以是大鼠。在一些实施方案中,啮齿动物可以是小鼠。
54.在一些实施方案中,如本文所述的核苷酸分子包含一个或多个药物选择盒,例如侧翼为一个或多个位点特异性重组位点的药物抗性基因,例如侧翼为loxp位点特异性重组识别位点的新霉素药物抗性基因,其中所述一个或多个药物抗性盒中的至少一个任选地紧邻有效地连接至23聚体rss的至少一个d
h
基因区段的上游。在一些实施方案中,核苷酸分子包含图2所示的序列。
55.本文还描述了靶向载体,例如用于修饰非人动物(例如,啮齿动物,诸如大鼠或小鼠)的基因组(例如,种系基因组)以包含如本文所述的工程化d
h
区。通常,如本文所述的靶向载体包含本文所述的任何核苷酸分子,并且任选地包含用于免疫球蛋白重链可变区内的同源重组的5'
‑
和3'
‑
同源臂,任选地其中所述免疫球蛋白重链可变区是人或人源化免疫球蛋白重链可变区。在一些实施方案中,如本文所述的靶向载体包含含有未重排的人基因区段(例如v
h6‑
1基因区段)的5’同源臂、和/或含有啮齿动物(例如小鼠)c
h
区或其一部分(例如啮齿动物(小鼠)c
h
内含子增强子区域和/或啮齿动物(小鼠)igm基因)的3’同源臂。
56.在一些实施方案中,靶向载体包含如本文所述的核苷酸分子、以及被配置为允许与免疫球蛋白重链序列进行同源重组的5'
‑
和3'
‑
同源臂,所述免疫球蛋白重链序列可以任选地位于内源性啮齿动物免疫球蛋白重链基因座处和/或包含人或人源化免疫球蛋白重链可变区。在一些实施方案中,包含含有未重排的人基因区段(例如,v
h6‑
1基因区段)、人工程化d
h
区、至少一个未重排的人j
h
基因区段的5’同源臂以及含有啮齿动物(小鼠)c
h
内含子增强子区域的3’同源臂的如本文所述的靶向载体、和/或啮齿动物(小鼠)可以被用于在包含人源化免疫球蛋白重链基因座的啮齿动物(例如包含用人免疫球蛋白可变序列对小鼠免疫球蛋白可变序列的替换的小鼠,例如小鼠)中对d
h
区进行工程化,所述包含人源化免疫球蛋白重链基因座的啮齿动物可以任选地包含恢复其生育力的功能性adam6基因、经修饰的内源性重链恒定区基因序列(其包含完整的内源性igm基因和另一个经修饰的内源性恒定区基因(例如igg)用于产生缺乏功能性ch1结构域的反向嵌合非igm抗体)、编码反向嵌合人源化共同轻链的序列、编码反向嵌合人源化κ轻链的序列、编码反向嵌合人源化λ轻链的序列、编码杂合κ/λ或κ/λ轻链的序列、未重排的种系人重链基因区段和/或经组氨酸密码子修饰用于表达具有组氨酸氨基酸并可能表现出ph敏感性抗原结合的可变结构域的(未)重排的种系轻链基因区段、和/或用于增加抗原受体多样性的末端脱氧核苷酸转移酶(tdt)。参见例如,美国专利号9,035,128;9,066,502;9,163,092;9,150,662;9,334,333;9,850,462;9,844,212;9,029,628;9,006,511;9,394,373;9,206,261;9,206,262;9,206,263;9,226,484;9,399,683;9,540,452;9,012,717;9,796,788、8,697,940;8,754,287;9,334,334;9,801,362;9,332,742;9,969,814;美国专利公开2011/0195454、2012/0021409、2012/0192300、2013/0185821、2013/0302836、2013/0045492、和2018/0125043;pct公开号wo2017210586和wo2019/113065,每个专利以全文引用的方式并入本文。
57.这样,本文描述了例如在啮齿动物中工程化用于进行d
h
‑
d
h
重组的d
h
区的方法。在一些实施方案中,所述方法包括修饰包含一个或多个未重排的d
h
基因区段的d
h
区,以包含有效地连接至23聚体rss的至少一个d
h
基因区段。在一些实施方案中,修饰免疫球蛋白重链可变区以工程化d
h
‑
d
h
重组的方法包括获得包含含有一个或多个未重排的d
h
基因区段的d
h
区的免疫球蛋白重链可变区,所述未重排的d
h
基因区段中的每一个在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss,并且修饰所述d
h
区以还包含有效地连接至23聚体rss的至少一个d
h
基因区段。在一些实施方案中,d
h
区是包含一个或多个未重排的人d
h
基因区段的人d
h
区,例如其中所述多个未重排的人d
h
基因区段任选地包含例如处于种系构型中的所有功能性未重排的人d
h
基因区段,其跨越并包括d
h1‑
1基因区段和d
h7‑
27基因区段。在一些实施方案中,修饰包括替换所述在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的一个或多个未重排的d
h
基因区段中的一个或多个,例如功能性未重排的人d
h
基因区段,其中所述至少一个d
h
基因区段有效地连接至23聚体rss。在一些实施方案中,用有效地连接至23聚体rss的
d
h基因区段替换在所述d
h
区中的在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的3’最末端的未重排的d
h
基因区段,其中所述有效地连接至23聚体rss的d
h
基因区段从5’至3’包含23聚体rss、d
h
基因区段和12聚体rss。在一些实施方案中,用被工程化以有效地连接至23聚体rss的对应d
h
基因区段替换在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段。在一些实施方案中,其中所述d
h
区
包含未重排的人d
h7‑
27基因区段(例如,种系d
h7‑
27基因区段),所述未重排的人d
h7‑
27基因区段被有效地连接至5'端23聚体rss的人d
h
基因区段(例如,未重排的人d
h3‑
3基因区段)替换。在一些实施方案中,其中所述d
h
区包含未重排的d
h2‑
2基因区段、未重排的d
h2‑
8基因区段和/或未重排的d
h2‑
15基因区段(例如其中所述工程化d
h
包含处于种系构型中的未重排的人d
h
基因区段的全部库)、未重排d
h2‑
2基因区段、未重排d
h2‑
8基因区段和/或未重排的d
h2‑
15基因区段分别被在其3'端有效连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、和/或在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段替换。在一些实施方案中,修饰包括用23聚体rss替换侧翼为未重排的d
h
基因区段(例如人种系d
h
基因区段)的两个12聚体rss中的一个。在一些实施方案中,待修饰的免疫球蛋白重链可变区除包含d
h
区外,还包含有效地连接至所述d
h
区的j
h
区(任选地包含人种系
j
h基因区段的全部库,其包含人种系j
h
1基因区段、人种系j
h
2基因区段、人种系j
h
3基因区段、人种系j
h
4基因区段、人种系j
h
5基因区段和人种系j
h
6基因区段,任选地其中所述人种系j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中),并且替换在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的的未重排的d
h
基因区段包括缺失在所述j
h
区中包含的至少一个未重排的j
h
基因区段,例如导致与所述d
h
区邻接的未重排的人j
h
1、j
h
2、j
h
3、j
h
4和/或j
h
5基因区段的缺失。在一些实施方案中,缺失在j
h
区中包含的至少一个种系j
h
基因区段包括缺失未重排的人j
h
1、j
h
2和j
h
3基因区段,和任选地进一步缺失j
h
4和j
h
5基因区段。在一些实施方案中,替换所有功能性d
h
基因区段中的一个或多个,例如用有效地连接至5'端23聚体rss的d
h
基因区段(例如有效地连接至5'端23聚体rss的d
h3‑
3基因区段)替换d
h7‑
27基因区段导致与所述d
h
区相邻的未重排的人j
h
1、j
h
2和j
h
3基因区段的缺失。在一些实施方案中,替换所有功能性d
h
基因区段中的一个或多个,例如用有效地连接至5'端23聚体rss的d
h
基因区段(例如有效地连接至5'端23聚体rss的d
h3‑
3基因区段)替换d
h7‑
27基因区段导致与所述d
h
区相邻的未重排的人j
h
1、j
h
2、j
h
3、j
h
4和j
h
5基因区段的缺失。在一些实施方案中,修饰
d
h区以包含有效地连接至23聚体rss的至少一个d
h
基因区段,其中所述有效地连接至23聚体rss的至少一个d
h
基因区段包含(a)有效地连接至23聚体rss的人d
h3‑
3基因区段,任选地其中所述23聚体rss与所述d
h3‑
3基因区段的5'端相邻,(b)有效地连接至23聚体rss的人d
h2‑
2基因区段,任选地其中所述23聚体rss与所述d
h2‑
2基因区段的3'端相邻,(c)有效地连接至23聚体rss的人d
h2‑
8基因区段,任选地其中所述23聚体rss与所述d
h2‑
8基因区段的3'端相邻,(d)有效地连接至23聚体rss的人d
h2‑
15基因区段,任选地其中所述23聚体rss与所述d
h2‑
15基因区段的3'端相邻,或(e)(a)
‑
(d)的任何组合。
58.此类方法可以产生包含工程化d
h
区的免疫球蛋白重链可变区,例如包含如本文所述的(人)免疫球蛋白重链可变区的核苷酸分子,其中所述(未)重排的(人)免疫球蛋白重链区可以任选地连接至非人免疫球蛋白重链恒定区或其一部分,例如,包含至少一个啮齿动物c
h
内含子增强子区和/或啮齿动物igm基因的啮齿动物免疫球蛋白重链恒定区(例如任选地在内源性非人免疫球蛋白重链基因座处)。在一些实施方案中,重组后,这样的免疫球蛋白重链基因座(例如内源性免疫球蛋白重链基因座)包含重排的免疫球蛋白重链可变区编码序列,其编码免疫球蛋白重链可变结构域,例如具有互补决定区3(cdr3)的、氨基酸长度为超过20个氨基酸的免疫球蛋白重链可变结构域,该长度可能是v
h
(d
h
a
‑
d
h
b)j
h
、v
h
d
h
j
h
6、或v
h
(d
h
a
‑
d
h
b)j
h
6重组的结果。因此,本文提供了包含编码包含cdr3的免疫球蛋白重链可变结
构域的重排的免疫球蛋白重链v
h
(d
h
a
‑
d
h
b)j
h
、v
h
(d
h
)j
h
6、或v
h
(d
h
a
‑
d
h
b)j
h
6序列的啮齿动物、啮齿动物细胞、基因座和/或核苷酸分子,其中所述cdr3的长度为至少20个氨基酸。
59.本文还描述了例如在其基因组(例如种系基因组)中包含本发明的工程化d
h
区(例如,如本文所述的核酸、靶向载体和/或免疫球蛋白重链基因座)的非人动物(例如啮齿动物)。本文还描述了此类非人动物基因组,例如啮齿动物基因组。在一些实施方案中,本文描述了啮齿动物,其种系基因组包含(或啮齿动物种系基因组包含)如所描述的免疫球蛋白重链可变区,其中所述免疫球蛋白重链可变区包含:(i)至少一个未重排的重链可变(v
h
)基因区段,(ii)工程化重链可变区多样性(d
h
)区,其中所述工程化d
h
区包含各自在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的一个或多个未重排的d
h
基因区段、和各自有效地连接至23聚体重组信号序列(rss)的一个或多个d
h
基因区段,以及(iii)至少一个未重排的重链连接(j
h
)基因区段,其中(i)
‑
(iii)在有效连接中使得在重组后所述免疫球蛋白重链可变区包含编码免疫球蛋白重链可变结构域的重排的重链可变区序列,任选地其中在v
h
(d
h
‑
d
h
)j
h
重组事件之后形成重排的重链可变区序列,任选地其中各自有效地连接至23聚体重组信号序列(rss)的所述一个或多个d
h
基因区段中的至少一个在所述v
h
(d
h
‑
d
h
)重组事件期间连接各自在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的所述一个或多个未重排的d
h
基因区段中的一个。在一些实施方案中,有效地连接至23聚体rss的一个或多个d
h
区段包含有效地连接至3’端23聚体rss的d
h
基因区段。在一些实施方案中,有效地连接至23聚体rss的一个或多个d
h
区段包含有效地连接至5’端23聚体rss的d
h
基因区段。在一些实施方案中,免疫球蛋白重链可变区是仅包含人v
h
、d
h
和j
h
基因区段的人免疫球蛋白重链可变区。在一些实施方案中,人免疫球蛋白重链可变区有效地连接至免疫球蛋白重链恒定区。在一些实施方案中,免疫球蛋白重链恒定区是非人动物或非人动物基因组例如在内源性免疫球蛋白重链基因座处的内源性免疫球蛋白重链恒定区。在一些实施方案中,免疫球蛋白重链可变区包含处于种系构型中的跨越在v
h3‑
74至v
h6‑
1之间的人v
h
基因区段。在一些实施方案中,免疫球蛋白重链可变区包含人j
h
6基因区段。在一些实施方案中,免疫球蛋白重链可变区包含编码一个或多个啮齿动物adam6多肽的一个或多个核苷酸分子(例如,啮齿动物adam6基因),其可以任选地被插入在两个人v
h
基因区段之间(例如,被插入在人v
h1‑
2基因区段与人v
h6‑
1基因区段之间)和/或被插入人adam6假基因的位置中。在一些实施方案中,非人动物是啮齿动物。在一些实施方案中,啮齿动物基因组对于工程化d
h
区而言是杂合的。在一些实施方案中,啮齿动物基因组对于工程化d
h
区而言是纯合的。在一些实施方案中,啮齿动物可以是大鼠。在一些实施方案中,啮齿动物可以是小鼠。在一些实施方案中,啮齿动物、啮齿动物基因组或啮齿动物细胞是大鼠、小鼠、大鼠基因组、小鼠基因组、大鼠细胞或小鼠细胞(例如啮齿动物(大鼠或小鼠)胚胎干细胞)。
60.在一些实施方案中,本文所述的啮齿动物、啮齿动物基因组或啮齿动物细胞还包含重排的重链vdj和/或编码免疫球蛋白重链可变结构域的v
h
(d
h
a
‑
d
h
b)j
h
编码序列。在一些实施方案中,本文描述了非人动物(例如啮齿动物,例如大鼠或小鼠),其包含(1)在其种系基因组中(例如在生殖细胞中)的含有有效地连接至23聚体rss的d
h
基因区段的工程化d
h
区的免疫球蛋白重链基因座,以及(2)在其体细胞基因组中(例如在b细胞中)的重排的重链可变区v
h
(d
h
a
‑
d
h
b)j
h
编码序列,其中所述第一或第二d
h
基因区段(分别为d
h
a或d
h
b)源自于有效地连接至23聚体rss的d
h
基因区段或其一部分(例如,包含与有效地连接至23聚体rss的d
h
基因区段的至少一部分的序列相同的序列、其体细胞高突变变体和/或其简并变体)。在一些实施方案中,其中所述b细胞是原代b细胞和/或重排的重链可变区编码序列与igm恒定区序列有效地连接,d
h
a和d
h
b基因区段中的至少一个包含与由有效地连接至23聚体rss的d
h
基因区段编码的核苷酸分子对齐的至少9个连续核苷酸,并且d
h
a和d
h
b基因区段中的每一个包含与种系d
h
基因区段的核苷酸分子对齐的至少5个连续核苷酸。在一些实施方案中,其中所述b细胞是浆细胞或记忆b细胞和/或重排的重链可变区编码序列是体细胞高突变的和/或与非igm恒定区序列(例如,igg、iga、ige等)有效地连接,d
h
a和d
h
b中的每一个分别与第一和第二种系d
h
基因区段显示出40%同一性,具有最多1个核苷酸突变。在一些实施方案中,啮齿动物中所有重排的重链vdj和/或v
h
(d
h
a
‑
d
h
b)j
h
编码序列中的至少95%的cdr3长度为至少10个氨基酸,任选地其中啮齿动物中所有重排的重链vdj和/或v
h
(d
h
a
‑
d
h
b)j
h
编码序列中的至少70%的cdr3长度为至少11个氨基酸,任选地啮齿动物中所有重排的重链vdj和/或v
h
(d
h
a
‑
d
h
b)j
h
编码序列中的至少15%的cdr3长度为至少14个氨基酸。在一些实施方案中,啮齿动物中的vdj和/或v
h
(d
h
a
‑
d
h
b)j
h
编码序列的群体具有至少15个氨基酸(任选地至少16个氨基酸、任选地至少17个氨基酸、和任选地至少18个氨基酸)的cdr3长度。在一些实施方案中,本文描述了表达核酸或免疫球蛋白基因座的啮齿动物或啮齿动物细胞、或所述核酸或免疫球蛋白基因座,所述核酸或免疫球蛋白基因座包含重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,其中第二种系d
h
基因区段是d
h3‑
3,任选地其中所述重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列编码长度为20个以上氨基酸的cdr3。在一些实施方案中,本文描述了表达核酸或免疫球蛋白基因座的啮齿动物或啮齿动物细胞、或所述核酸或免疫球蛋白基因座,所述核酸或免疫球蛋白基因座包含重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,其中第一种系d
h
基因区段是d
h2‑
2、d
h2‑
8或d
h2‑
15,任选地其中所述重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列编码长度为20个以上氨基酸的cdr3。在一些实施方案中,本文描述了表达编码长度为20个以上氨基酸的cdr3的重排的重链v
h
(d
h
a
‑
d
h
b)j
h
6编码序列的啮齿动物或啮齿动物细胞。
61.在一些实施方案中,提供了包含与啮齿动物免疫球蛋白重链恒定区序列有效地连接的重排的人免疫球蛋白重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列的啮齿动物基因组、核酸或免疫球蛋白基因座。在一些实施方案中,d
h
b基因区段源自于人种系d
h3‑
3基因区段。在一些实施方案中,d
h
a基因区段源自于人种系d
h2‑
2、d
h2‑
8或d
h2‑
15基因区段。在一些实施方案中,由于d
h
a和d
h
b中的每一个分别与第一和第二种系d
h
基因区段显示出40%同一性(具有最多1个核苷酸突变),所以重排的重链被确定为是v
h
(d
h
a
‑
d
h
b)j
h
编码序列。在一些实施方案中,重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列编码长度为20个以上氨基酸的cdr3。在一些实施方案中,j
h
基因区段源自于人种系j
h
6基因区段。在一些实施方案中,提供了包含v
h
(d
h
a
‑
d
h
b)j
h
编码序列的啮齿动物或啮齿动物细胞。在一些实施方案中,啮齿动物是大鼠或小鼠,或者啮齿动物细胞是大鼠细胞或小鼠细胞。在一些实施方案中,啮齿动物细胞是啮齿动物b细胞。在一些实施方案中,提供了包含与骨髓瘤细胞融合的啮齿动物b细胞的杂交瘤,所述啮齿动物b细胞表达重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列。在一些实施方案中,当序列被鉴定为各自分别与第一和第二种系d
h
基因区段显示出40%同一性(具有最多1个核苷酸突变)的d
h
a和d
h
b时,确认v
h
(d
h
a
‑
d
h
b)j
h
序列是d
h
‑
d
h
重组事件的结果。
62.在一些实施方案中,提供了非人动物或细胞,其基因组包含免疫球蛋白重链可变区,所述免疫球蛋白重链可变区包括工程化d
h
区,其中所述工程化d
h
区包含与第一和第二重
组信号序列(rss)有效地连接的至少一个d
h
区段。在一些实施方案中,所述第一rss是23聚体rss,而所述第二rss是12聚体rss。在一些实施方案中,所述第一rss是12聚体rss,而所述第二rss是23聚体rss。
63.在一些实施方案中,提供了非人动物,其基因组包含免疫球蛋白重链可变区,所述免疫球蛋白重链可变区包括工程化d
h
区,所述工程化d
h
区包含各自有效地连接至23聚体重组信号序列(rss)的一个或多个d
h
区段。
64.在一些实施方案中,提供了非人细胞或组织,其基因组包含免疫球蛋白重链可变区,所述免疫球蛋白重链可变区包括工程化d
h
区,所述工程化d
h
区包含各自有效地连接至23聚体重组信号序列(rss)的一个或多个d
h
区段。在一些实施方案中,细胞来自淋巴或骨髓谱系。在一些实施方案中,细胞为淋巴细胞。在一些实施方案中,细胞选自b细胞、树突状细胞、巨噬细胞、单核细胞和t细胞。在一些实施方案中,组织选自脂肪、膀胱、大脑、乳房、骨髓、眼、心、肠、肾、肝、肺、淋巴结、肌肉、胰腺、血浆、血清、皮肤、脾、胃、胸腺、睾丸、卵子或它们的任何组合。
65.在一些实施方案中,提供了由如本文所述的非人细胞制成的永生细胞,例如,通过将如本文所述的从非人动物中分离的b细胞与骨髓瘤细胞融合制成的杂交瘤细胞。
66.在一些实施方案中,非人类细胞是非人类胚胎干(es)细胞。在一些实施方案中,非人类胚胎干细胞是啮齿类动物胚胎干细胞。在一些实施方案中,啮齿动物胚胎干细胞是小鼠胚胎干细胞并且来自129品系、c57bl品系或其混合物。在一些实施方案中,啮齿动物胚胎干细胞是小鼠胚胎干细胞,并且是129和c57bl品系的混合物。
67.在一些实施方案中,提供了本文所述的非人类胚胎干细胞用于制备非人类动物的用途。在一些实施方案中,非人胚胎干细胞是小鼠胚胎干细胞,并且用于制备包含免疫球蛋白重链可变区的小鼠,所述免疫球蛋白重链可变区包括如本文所述的工程化d
h
区。在一些实施方案中,非人胚胎干细胞是大鼠胚胎干细胞,并且用于制备包含免疫球蛋白重链可变区的大鼠,所述免疫球蛋白重链可变区包括如本文所述的工程化d
h
区。在一些实施方案中,用于制备包含包括工程化d
h
区的免疫球蛋白重链可变区的大鼠的非限制性示例性方法可以包括在us20140309487(该专利以引用的方式整体并入本文)中公开的方法。
68.在一些实施例中,提供了包含本文所述的非人胚胎干细胞、由其制备、由其获得或由其产生的非人胚胎。在一些实施方案中,非人胚胎是啮齿动物胚胎;在一些实施方案中,是小鼠胚胎;在一些实施方案中,是大鼠胚胎。
69.在一些实施方案中,提供了本文描述的非人类胚胎用于制备非人类动物的用途。在一些实施方案中,非人胚胎是小鼠胚胎,并且用于制备包含免疫球蛋白重链可变区的小鼠,所述免疫球蛋白重链可变区包括如本文所述的工程化d
h
区。在一些实施方案中,非人胚胎是大鼠胚胎,并且用于制备包含免疫球蛋白重链可变区的大鼠,所述免疫球蛋白重链可变区包括如本文所述的工程化d
h
区。
70.本文提供了制备其基因组包含工程化d
h
区的啮齿动物的方法,所述方法包括(a)修饰啮齿动物胚胎干细胞的基因组以包含含有各自有效地连接至23聚体rss的一个或多个d
h
区段的dna片段,例如,其中所述dna片段包含本文所述的核苷酸分子、靶向载体和/或工程化d
h
区,并且(b)使用(a)的经修饰的啮齿动物胚胎干细胞产生啮齿动物。在一些实施方案中,所述方法包括修饰免疫球蛋白重链可变区的未重排的d
h
区,以包含有效地连接至23
聚体rss的至少一个d
h
区段,其中所述未重排的d
h
区还包含其每一个都在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的一个或多个未重排的d
h
基因区段,从而制成所述啮齿动物。在一些实施方案中,修饰包括用有效地连接至23聚体rss的至少一个d
h
区段替换一个或多个未重排的人d
h
基因区段并且任选地替换或缺失一个或多个j
h
基因区段。在一些实施方案中,免疫球蛋白重链可变区是人免疫球蛋白重链可变区,例如,其中所述人免疫球蛋白重链可变区包含含有至少一个v
h
基因区段的未重排的人免疫球蛋白重链v
h
基因簇、含有一个或多个未重排的人d
h
基因区段的未重排的人免疫球蛋白重链d
h
区、以及含有至少一个未重排的人j
h
基因区段的未重排的人免疫球蛋白重链j
h
基因簇,其中所述未重排的人免疫球蛋白重链d
h
区被修饰以包含有效地连接至23聚体rss的至少一个d
h
区段。在一些实施方案中,修饰步骤产生免疫球蛋白重链可变区,其包含(i)功能性人v
h
基因区段的全部库,例如跨越并包括v
h3‑
74至v
h6‑
1的所有功能性v
h
基因区段,(ii)未重排的人d
h
基因区段的全部库,但被有效地连接至23聚体rss的至少一个d
h
基因区段替换的d
h7‑
27除外,以及(iii)至少一个未重排的人j
h
6基因区段、以及任选地至少一个未重排的j
h
4基因区段、未重排的j
h
5基因区段、和未重排的j
h
6基因区段。在一些实施方案中,有效地连接至23聚体rss的至少一个d
h
基因区段包含有效地连接至5
’‑
23聚体rss的d
h3‑
3基因区段。在一些实施方案中,修饰步骤产生免疫球蛋白重链可变区,其包含(i)功能性人v
h
基因区段的全部库,例如跨越并包括v
h3‑
74至v
h6‑
1的所有功能性v
h
基因区段,(ii)未重排的人d
h
基因区段的全部库,但未重排的人d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段分别被在其3'端有效地连接至23聚体rss的d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、和在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段替换除外,以及(iii)未重排的人j
h
基因区段的全部库,例如未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。在一些实施方案中,免疫球蛋白重链可变区(a)还包含一个或多个啮齿动物adam6基因,任选地其中所述一个或多个啮齿动物adam6基因位于两个未重排的v
h
基因区段之间,例如位于未重排的人v
h1‑
2基因区段与未重排的人v
h6‑
1基因区段之间,和/或(b)被有效地连接至免疫球蛋白重链恒定区,任选地其中所述免疫球蛋白重链恒定区是内源性啮齿动物免疫球蛋白重链恒定区,例如在内源性免疫球蛋白重链基因座处的内源性啮齿动物免疫球蛋白重链恒定区。在一些实施方案中,所述啮齿动物是大鼠或小鼠。
71.在一些实施方案中,提供了试剂盒,其包含如本文所述的非人动物、如本文所述的非人细胞或组织、如本文所述的永生细胞、如本文所述的非人胚胎干细胞或如本文所述的非人胚胎。
72.在一些实施例中,提供了如本文所述的试剂盒,用于制造和/或开发用于治疗或诊断的药物(例如,抗体或其抗原结合片段)。在一些实施例中,提供了如本文所述的试剂盒,用于制备和/或开发用于治疗、预防或改善疾病、病症或状况的药物(例如,抗体或其抗原结合片段)。
73.在一些实施例中,提供了本文所述的转基因、核酸构建体、dna构建体或靶向载体。在一些实施方案中,转基因、核酸构建体、dna构建体或靶向载体包含如本文所述的工程化d
h
区。在一些实施方案中,转基因、核酸构建体、dna构建体或靶向载体包含dna片段,所述dna片段包括有效地连接至23聚体rss的一个或多个d
h
区段。在一些实施方案中,转基因、核
酸构建体、dna构建体或靶向载体还包含一个或多个选择性标记。在一些实施方案中,转基因、核酸构建体、dna构建体或靶向载体还包含一个或多个位点特异性重组位点(例如,loxp、frt或它们的组合)。在一些实施方案中,转基因、核酸构建体、dna构建体或靶向载体如图2所描绘。
74.在一些实施方案中,提供了本文所述的转基因、核酸构建体、dna构建体或靶向载体用于制备非人动物、非人细胞、非人胚胎干细胞和/或非人胚胎的用途。
75.在一些实施方案中,一个或多个d
h
区段各自有效地连接至3’23聚体rss。在一些实施方案中,一个或多个d
h
区段各自有效地连接至5’23聚体rss。
76.在一些实施方案中,工程化d
h
区包含有效地连接至5’23聚体rss的一个d
h
区段。在一些实施方案中,工程化d
h
区包含有效地连接至3’rss的一个d
h
区段。在有效地连接至5’23聚体rss的一个d
h
区段的一些实施方案中,所述一个d
h
区段是合成的d
h
区段;在一些实施方案中,合成的人d
h
区段;在一些实施方案中,具有与人d
h3‑
3区段相同或基本上相同的序列的合成的人d
h
区段。在有效地连接至3’23聚体rss的一个d
h
区段的一些实施方案中,所述一个d
h
区段是合成的d
h
区段;在一些实施方案中,合成的人d
h
区段;在一些实施方案中,具有与人d
h3‑
3区段相同或基本上相同的序列的合成的人d
h
区段。
77.在一些实施方案中,工程化d
h
区包含各自有效地连接至5’23聚体rss的三个d
h
区段。在各自有效地连接至5’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是合成的d
h
区段。在各自有效地连接至5’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是人d
h
2家族区段。在各自有效地连接至5’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段选自人d
h2‑
2、人d
h2‑
8、人d
h2‑
15、人d
h2‑
21及其组合。在各自有效地连接至5’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是人d
h2‑
2、人d
h2‑
8和人d
h2‑
15。
78.在一些实施方案中,工程化d
h
区包含各自有效地连接至3’23聚体rss的三个d
h
区段。在各自有效地连接至3’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是合成的d
h
区段。在各自有效地连接至3’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是人d
h
2家族区段。在各自有效地连接至3’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段选自人d
h2‑
2、人d
h2‑
8、人d
h2‑
15、人d
h2‑
21及其组合。在各自有效地连接至3’23聚体rss的三个d
h
区段的一些实施方案中,所述三个d
h
区段是人d
h2‑
2、人d
h2‑
8和人d
h2‑
15。
79.在一些实施方案中,如本文所述的工程化d
h
区包括多个人d
h
区段,其中所述多个人d
h
基因区段中的至少一个被有效地连接至5’或3’rss;在一些实施方案中,5’23聚体rss。在一些实施方案中,如本文所述的工程化d
h
区包括多个人d
h
区段,其中所述多个人d
h
基因区段中的至少三个各自被有效地连接至5’或3’rss;在一些实施方案中,3’23聚体rss。
80.在一些实施方案中,所提供的非人动物、非人细胞或非人组织的基因组缺乏一个或多个野生型d
h
区段。在一些实施方案中,所提供的非人动物、非人细胞或非人组织的基因组缺乏所有或基本上所有的野生型d
h
区段。在一些实施方案中,所提供的非人动物、非人细胞或非人组织的基因组仅含有人d
h
区段。
81.在一些实施例中,免疫球蛋白重链可变区是人免疫球蛋白重链可变区。在一些实施方案中,人免疫球蛋白重链可变区有效地连接至免疫球蛋白重链恒定区。在一些实施方
案中,免疫球蛋白重链恒定区是内源性(例如,非人)免疫球蛋白重链恒定区。
82.在一些实施方案中,人免疫球蛋白重链可变区包括从v
h3‑
74至v
h6‑
1的人v
h
基因区段。在一些实施方案中,人免疫球蛋白重链可变区包括至少人j
h
基因区段j
h
6。在一些实施方案中,人免疫球蛋白重链可变区包括至少人j
h
基因区段j
h
4、j
h
5和j
h
6。在一些实施方案中,人免疫球蛋白重链可变区包括人j
h
基因区段j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6。
83.在非人动物、非人细胞或非人组织的一些实施方案中,基因组缺乏内源性adam6基因。在非人动物、非人细胞或非人组织的一些实施方案中,基因组还包含编码一个或多个啮齿动物adam6多肽的一个或多个核苷酸序列的插入;在一些实施方案中,所述一个或多个核苷酸序列被插入在第一和第二人v
h
基因区段之间;在一些实施方案中,所述一个或多个核苷酸序列被插入人adam6假基因的位置中;在一些实施方案中,所述一个或多个核苷酸序列被插入在人v
h
基因区段与人d
h
基因区段之间。在一些实施方案中,第一人类v
h
基因区段为人类v
h1‑
2,并且第二人类v
h
基因区段为人类v
h6‑
1.
84.在一些实施方案中,所提供的非人动物、非人细胞或非人组织对于如本文所述的工程化d
h
区而言是纯合的、杂合的或半合的。在一些实施方案中,所提供的非人动物、非人细胞或非人组织对于如本文所述的工程化d
h
区而言是转基因的。
85.在一些实施方案中,提供了一种制备基因组包含免疫球蛋白重链可变区的非人动物的方法,所述免疫球蛋白重链可变区包括工程化d
h
区,所述方法包括(a)将dna片段插入非人胚胎干细胞中,所述dna片段包含各自有效地连接至23聚体rss的一个或多个d
h
区段;(b)获得在(a)中产生的非人胚胎干细胞;并且(c)使用(b)的非人胚胎干细胞创建非人动物。
86.在一些实施方案中,包含一个或多个d
h
区段的dna片段各自有效地连接至3’23聚体rss。在一些实施方案中,dna片段包含有效地连接至3’23聚体rss的一个d
h
区段。在一些实施方案中,dna片段包含有效地连接至3’23聚体rss的一个合成的人d
h
区段。在一些实施方案中,dna片段包含有效地连接至3’23聚体rss的一个合成的人d
h3‑
3区段。在一些实施方案中,dna片段包含各自有效地连接至3’23聚体rss的三个d
h
区段。在一些实施方案中,dna片段包含各自有效地连接至3’23聚体rss的三个人d
h
区段。在一些实施方案中,dna片段包含各自有效地连接至3’23聚体rss的三个人d
h
区段,所述人d
h
区段是人d
h2‑
2、人d
h2‑
8和人d
h2‑
15。
87.在一些实施方案中,dna片段包含其每一个都有效地连接至5’23聚体rss的一个或多个d
h
区段。在一些实施方案中,dna片段包含有效地连接至5’23聚体rss的一个d
h
区段。在一些实施方案中,dna片段包含有效地连接至5’23聚体的一个合成的人d
h
区段。在一些实施方案中,dna片段包含有效地连接至5’23聚体rss的一个合成的人d
h3‑
3区段。在一些实施方案中,dna片段包含有效地连接至5’23聚体rss的一个合成的人d
h3‑
3区段,所述合成的人d
h3‑
3区段被定位于人d
h
区中的人d
h7‑
27区段的位置中。
88.在一些实施方案中,dna片段包含一个或多个选择标记。在一些实施方案中,dna片段包含一个或多个位点特异性重组位点。
89.在一些实施方案中,提供了一种制备基因组包含免疫球蛋白重链可变区的非人动物的方法,所述免疫球蛋白重链可变区包括工程化d
h
区,所述方法包括以下步骤:修饰非人动物或非人动物细胞的基因组使得其包含免疫球蛋白重链可变区,所述免疫球蛋白重链可
变区包括工程化d
h
区,所述工程化d
h
区包含各自有效地连接至23聚体rss的一个或多个d
h
区段,从而制成所述非人动物。
90.在制备非人动物的一些实施方案中,非人动物或非人动物细胞的基因组被修饰以包括各自被有效地连接至5’23聚体rss的一个或多个d
h
区段。在制备非人动物的一些实施方案中,非人动物或非人动物细胞的基因组被修饰以包括各自被有效地连接至3’23聚体rss的一个或多个d
h
区段。
91.在一些实施方案中,提供了在非人动物中生产抗体的方法。在一些实施方案中,生产抗体或获得编码其的核酸的方法包括用抗原免疫非人动物(例如,啮齿动物(例如,大鼠或小鼠)),所述啮齿动物具有包含工程化d
h
区(其包含各自有效地连接至23聚体rss的一个或多个d
h
区段)的种系基因组,并且允许所述啮齿动物对包括抗体的抗原、或编码结合抗原的所述抗体的核酸产生免疫应答。在一些实施方案中,所述方法还包括从啮齿动物或啮齿动物细胞(例如,为b细胞或杂交瘤)中回收抗体或编码所述抗体的核酸。在一些实施方案中,所述一个或多个d
h
区段各自被有效地连接至5’23聚体rss。在一些实施方案中,一个或多个d
h
区段各自有效地连接至3’23聚体rss。
92.在一些实施方案中,所述方法包括以下步骤:(a)用抗原免疫非人动物,所述非人动物具有包含免疫球蛋白重链可变区的基因组,所述免疫球蛋白重链可变区包括工程化d
h
区,所述工程化d
h
区包含各自有效地连接至23聚体rss的一个或多个d
h
区段;(b)将啮齿动物维持在足以使非人动物对所述抗原产生免疫应答的条件下;并且(c)从与非人动物或非人动物细胞中回收结合所述抗原的抗体。在一些实施方案中,非人动物细胞是b细胞。在一些实施方案中,非人动物细胞是杂交瘤。
93.在一些实施方案中,提供了其基因组包含人免疫球蛋白重链可变区的非人动物,所述人免疫球蛋白重链可变区包含一个或多个人v
h
基因区段、包括有效地连接至23聚体rss的至少一个人d
h
区段的工程化d
h
区、和至少一个人j
h
基因区段,其中所述人免疫球蛋白重链可变区被有效地连接至一个或多个内源性免疫球蛋白恒定区基因使得所述啮齿动物的特征在于当用抗原免疫所述啮齿动物时,其产生包含人重链可变结构域的抗体,所述人重链可变结构域包括通过人d
h
‑
d
h
重组和/或增强的至j
h
6基因区段的重组产生的cdr3区,并且其中所述抗体显示出与所述抗原的特异性结合。在一些实施方案中,有效地连接至23聚体rss的至少一个人d
h
区段被定位于人d
h7‑
27区段的位置中。在一些实施方案中,人免疫球蛋白重链可变区包含少于全部六个人j
h
基因区段。在一些实施方案中,人免疫球蛋白重链可变区仅包含六个人j
h
基因区段中的一个。在一些实施方案中,人免疫球蛋白重链可变区包含人j
h
6基因区段,并且缺乏功能性j
h
1基因区段、缺乏功能性j
h
2基因区段、缺乏功能性j
h
3基因区段、缺乏功能性j
h
4基因区段且缺乏功能性j
h
5基因区段。在一些实施方案中,人免疫球蛋白重链可变区仅包含六个人j
h
基因区段中的三个。在一些实施方案中,人免疫球蛋白重链可变区仅包含人j
h
4基因区段、人j
h
5基因区段和人j
h
6基因区段,并且缺乏功能性j
h
1基因区段、缺乏功能性j
h
2基因区段且缺乏功能性j
h
3基因区段。在一些实施方案中,其中其基因组包含含有少于全部六个人j
h
基因区段的人免疫球蛋白重链可变区(例如仅包含六个人j
h
基因区段中的一个的人免疫球蛋白重链可变区(例如包含人j
h
6基因区段并且缺乏功能性j
h
1基因区段、缺乏人功能性j
h
2基因区段、缺乏功能性j
h
3基因区段、缺乏功能性j
h
4基因区段且缺乏功能性j
h
5基因区段的人免疫球蛋白重链可变区))的非人动物表现出与包含含
有全部六个人j
h
基因区段的人免疫球蛋白重链可变区的对照非人动物相比与j
h
6基因区段的重组增强,例如,所述非人动物与所述对照非人动物相比包含更大百分比的含有j
h
6基因区段序列或其部分和/或编码其至少20个氨基酸长度的cdr3的重排的免疫球蛋白重链序列。在一些实施方案中,其中其基因组包含含有少于全部六个人j
h
基因区段的人免疫球蛋白重链可变区(例如仅包含六个人j
h
基因区段中的三个的人免疫球蛋白重链可变区(例如包含含有人j
h
4基因区段、人j
h
5基因区段和人j
h
6基因区段,并且缺乏功能性j
h
1基因区段、缺乏功能性j
h
2基因区段且缺乏功能性j
h
3基因区段的人免疫球蛋白重链可变区的人免疫球蛋白重链可变区))的非人动物表现出与包含含有全部六个人j
h
基因区段的人免疫球蛋白重链可变区的对照非人动物相比与j
h
6基因区段的重组增强,例如,所述非人动物与所述对照非人动物相比包含更大百分比的含有j
h
6基因区段序列或其部分和/或编码至少20个氨基酸长度的cdr3的重排的免疫球蛋白重链序列。
94.在一些实施方案中,提供了其基因组包含人免疫球蛋白重链可变区的非人动物,所述人免疫球蛋白重链可变区包含一个或多个人v
h
基因区段、包括在3’侧接有23聚体rss的至少一个人d
h
区段的工程化d
h
区、和至少两个人j
h
基因区段,其中所述人免疫球蛋白重链可变区有效地连接至一个或多个内源性免疫球蛋白恒定区基因,使得所述啮齿动物的特征在于当用抗原对其免疫时,其产生包含人重链可变结构域的抗体,所述人重链可变结构域包括由人d
h
‑
d
h
重组产生的cdr3区,并且其中所述抗体显示出与所述抗原的特异性结合。在一些实施方案中,工程化d
h
区包括各自在3’侧接有23聚体rss的至少三个人d
h
区段。在一些实施方案中,工程化d
h
区包括各自在3’侧接有23聚体rss的三个人d
h
区段,所述三个人d
h
区段是人d
h2‑
2、人d
h2‑
8和人d
h2‑
15。在一些实施方案中,人免疫球蛋白重链可变区包括从v
h3‑
74至v
h6‑
1的人v
h
基因区段。
95.在一些实施方案中,所述抗原是病原体,例如细菌、真菌或病毒病原体。在一些实施方案中,对本文非人动物的免疫包括用病原体(例如细菌、真菌或病毒病原体)感染所述非人动物。在一些实施方案中,对本文非人动物的免疫包括向所述非人动物施用从病原体(例如细菌、真菌或病毒病原体)分离的基因组或蛋白质物质。在一些实施方案中,抗原是受体(例如,补体受体、趋化因子受体等)或其部分。在一些实施方案中,抗原是编码受体或其部分的核酸。在一些实施方案中,抗原是表达受体或其部分的细胞。在一些实施方案中,抗原是离子通道或其部分。在一些实施方案中,抗原是编码离子通道或其部分的核酸。在一些实施方案中,抗原是表达离子通道或其部分的细胞。
96.在一些实施方案中,所提供的非人动物、非人细胞或非人组织具有还包含在内源性轻链基因座中的一个或多个人v
l
基因区段和一个或多个人j
l
基因区段的插入的基因组。在一些实施方案中,人v
l
和j
l
区段是v和j基因区段,并且被插入内源性轻链基因座中。在一些实施例中,人v和j基因区段与啮齿类动物c基因(例如小鼠或大鼠c基因)有效地连接。在一些实施方案中,人v
l
和j
l
区段是v和j基因区段,并且被插入内源性轻链基因座中。在一些实施例中,人v和j基因区段与啮齿类动物c基因(例如小鼠或大鼠c基因)有效地连接。
97.在一些实施方案中,提供了将如本文所述的非人类动物、非人类细胞或非人类组织用于制造和/或开发用于医学(诸如用作药剂)的药物或疫苗的用途。在一些实施方案中,提供了如本文所述的非人动物、非人细胞或非人组织在制造和/或开发用于施用至人类的抗体中的用途。在一些实施方案中,提供了如本文所述的非人动物、非人细胞或非人组织在
制造用于治疗、预防或改善疾病、障碍或病症的药物中的用途。
98.在一些实施方案中,提供了用于制造和/或开发用于治疗或诊断的药物的如本文所述的非人类动物、非人类细胞或非人类组织。在一些实施方案中,提供了用于制造用于治疗、预防或改善疾病、病状或病症的药剂的如本文所述的非人类动物、非人类细胞或非人类组织。
99.在一些实施方案中,本文提供的非人动物是啮齿动物;在一些实施方案中,小鼠;在一些实施方案中,大鼠。在许多实施方案中,本文提供的非人动物细胞是啮齿动物细胞;在一些实施方案中,小鼠细胞;在一些实施方案中,大鼠细胞。在许多实施方案中,本文提供的非人动物组织是啮齿动物组织;在一些实施方案中,小鼠组织;在一些实施方案中,大鼠组织。
100.在一些实施方案中,23聚体rss包含含有如seq id no:151所示序列的核苷酸序列。
附图说明
101.本文中包括的由以下各图组成的附图仅用于举例说明目的而非用于限制。
102.图1示出了本发明实施方案的未按比例显示的一般性图示,其显示了在具有未经修饰的d
h
区(上图)和工程化d
h
区(下图)的免疫球蛋白重链可变区基因区段的dj重组事件中基因区段的有序组装。12聚体重组信号序列(rss)被描绘为未填充的三角形。23聚体rss被描绘为带有垂直条纹的三角形。说明性的未经修饰的v
h
基因区段(未填充的框)和d
h
基因区段(填充的框)分别被描绘为未填充的框和填充的框,并使用字母来提供通用的命名法。有效地连接至23聚体rss的d基因区段(例如d
h3‑
3)和未经修饰的j
h
基因区段分别被描绘为水平条纹填充的框和未填充的框,并提供了其适当的命名法。还显示了μ0启动子(μ0pro)。未描绘v
h
基因区段与重组dj基因区段的重组。
103.图2示出了根据实施例1制备的靶向载体的示例性实施方案的未按比例显示的图示。哈希线(hash line)代表包括在靶向载体中但未具体描绘的d
h
基因区段。
104.图3显示了通过电穿孔(ep)将23:d
h3‑
3:12/j
h
6靶向载体插入在小鼠es细胞基因组中的人源化免疫球蛋白重链可变区基因座中的非限制性示例性实施方案的未按比例显示的图示。哈希线代表包括在重链可变区基因座中但未具体描绘的v
h
基因区段或d
h
基因区段。
105.图4示出了在如实施例1和2中所述的23:d
h3‑
3:12/j
h
6靶向载体的电穿孔和整合之后在人源化免疫球蛋白重链基因座中cre介导的选择盒的缺失的非限制性示例性实施方案的未按比例显示的图示。哈希线代表包括在重链可变区基因座中但未具体描绘的v
h
基因区段或d
h
基因区段。
106.图5显示了通过电穿孔(ep)将23:d
h3‑
3:12/j
h4‑
6靶向载体插入在小鼠es细胞基因组中的人源化免疫球蛋白重链可变区基因座中的非限制性示例性实施方案的未按比例显示的图示。哈希线代表包括在重链可变区基因座中但未具体描绘的v
h
基因区段或d
h
基因区段。
107.图6示出了在如实施例1和2中所述的23:d
h3‑
3:12/j
h4‑
6靶向载体的电穿孔和整合之后在人源化免疫球蛋白重链基因座中cre介导的选择盒的缺失的非限制性示例性实施方案的未按比例显示的图示。哈希线代表包括在重链可变区基因座中但未具体描绘的v
h
基因
靶向载体修饰的小鼠的骨髓或脾脏中具有长度大于21个氨基酸的cdr3的读段的百分比。bm和脾脏细胞数量未彼此归一化。n=1。
118.图13示出了与本发明的一个实施方案有关的结果,显示了从用23:d
h3‑
3:12/j
h
6靶向载体修饰并编码具有其全部的长度为20个以上氨基酸的氨基酸(aa)长度(x轴)的重链cdr3(hcdr3)的小鼠的骨髓(bm)或脾脏中分离出的推测的重排的免疫球蛋白重链v
h
d
h
a
‑
d
h
bj
h
基因序列(根据表7中列出的严格标准)的百分比(%;y轴)。bm和脾脏细胞数量未彼此归一化。n=1。
119.定义
120.本发明的范围由本文所附权利要求书限定,并且不受本文所描述的特定实施方案的限制;本领域的技术人员在阅读本公开内容后将认识到可以等同于这些所描述的实施方案或者在权利要求书的范围内的多个修改。一般来讲,术语是根据所述术语在本领域中所理解的含义,除非另外明确指出。本文和下文提供了某些术语的明确定义;这些和其它术语在说明书自始至终在特定情况下的含义根据上下文对于本领域技术人员是明确的。下述术语和其它术语的另外定义在说明书各处阐述。本说明书中引用的参考文献或其相关部分以引用方式整体并入本文。
121.在权利要求中使用序数术语如“第一”、“第二”、“第三”等来修饰权利要求要素,其本身并不意味着一个权利要求要素相对于另一个要素的任何优先性、优先级或顺序或者其中执行方法行为的时间顺序,而是仅用作区分具有某一名称的一个权利要求要素与具有相同名称的另一个要素(但使用序数术语)的标记,以区分权利要求要素。
122.除非明确指出相反,否则说明书和权利要求中的冠词“一个”和“一种”应该理解为包括复数指代物。在组的一个或多个成员之间包括“或”的权利要求或描述应当被视为是满足以下情况,即组成员中的一个、多于一个或全部存在于、被应用于给定的产品或方法中,或以其他方式与给定的产品或方法相关,除非指出相反或根据上下文明显不同。本发明包括这样的实施方案,其中组中的一个确切成员存在于、被应用于给定的产品或方法中,或以其他方式与给定的产品或方法相关。本发明还包括这样的实施方案,其中多于一个组成员或全部组成员存在于、被应用于给定的产品或方法中,或以其他方式与给定的产品或方法相关。此外,应当理解,本发明涵盖所有的变化、组合和置换,其中来自一条或多条所列权利要求的一个或多个限制、要素、条款、描述性用语等被引入从属于同一基础权利要求的另一个权利要求(或者相关的任何其他权利要求)中,除非另外指明或除非对于本领域的普通技术人员来说明显会引起矛盾或不一致。当要素以列表的形式(例如,以马库什组或类似形式)呈现时,应当理解这些要素的每个亚组也被公开,并且任何要素可从该组中去除。应当理解,通常,在本发明或本发明的多个方面被称为包括特定要素、特征等的情况下,本发明的多个实施方案或本发明的多个方面由这些元素、特征等组成或基本上由这些元素、特征等组成。为了简洁起见,这些实施方案并不是在每种情况下都用本文的那么多词语来具体描述。还应当理解,本发明的任何实施方案或方面可明确地从权利要求排除,不管在说明书中是否描述了此类具体排除。
123.如本专利申请中所用,术语“约”和“大约”可等同使用。本技术中与或不与约/大约一起使用的任何数字意在涵盖由相关领域普通技术人员所理解的任何正常波动(例如,+/
‑
5%)。
124.施用:是指将组合物施用至受试者或系统(例如施用至细胞、器官、组织、生物体或它们的相关组分或它们的组分集)。所属领域的技术人员将了解,投药途径可以根据例如组成物正施用于的受试者或系统、组成物的性质、投药目的等而变化。
125.例如,在一些实施方案中,针对动物受试者(例如,针对人或啮齿动物)的施用可以是支气管施用(包括通过支气管滴注)、面颊施用、肠内施用、皮内施用、动脉内施用、真皮内施用、胃内施用、髓内施用、肌肉内施用、鼻内施用、腹膜内施用、鞘内施用、静脉内施用、心室内施用、粘膜施用、鼻腔施用、口服、直肠施用、皮下施用、舌下施用、局部施用、气管施用(包括通过气管滴注)、透皮施用、阴道施用和/或玻璃体施用。在一些实施方案中,施用可以涉及间歇给药。在一些实施方案中,施用可以涉及连续给药(例如,灌注)达至少一段选定的时间。在一些实施方案中,可以将由本文公开的非人动物产生的抗体施用至受试者(例如,人受试者或啮齿动物)。在一些实施方案中,药物组合物包括由本文公开的非人动物产生的抗体。在一些实施方案中,药物组合物可以包括缓冲剂、稀释剂、赋形剂或其任何组合。在一些实施方案中,包括由本文公开的非人动物产生的抗体的药物组合物可以包括在用于储存或施用的容器(例如小瓶、注射器(例如iv注射器)或袋子(例如iv袋))中。
126.生物学活性:是指在体外或在体内(例如在生物体中)在生物系统中具有活性的任何药剂的特征。例如,当存在于生物体中时,在该生物体内具有生物学效应的药剂被认为具有生物学活性。
127.在特定实施方案中,当蛋白质或多肽具有生物学活性时,给予所述蛋白质或多肽的至少一种生物学活性的所述蛋白质或多肽的部分通常称为“生物学活性”部分。
128.可比较的:是指两个或更多个药剂、实体、情况、条件集等,它们可以彼此不相同但是足够相似以允许在其之间进行比较,从而可以基于所观察到的差异或相似来合理地得出结论。所属领域的技术人员将理解,在上下文中,在任何既定情况下,两种或更多种此类药剂、实体、情形、条件集合等被视为相当需要何种程度的一致性。
129.保守的:是指保守氨基酸置换,即,氨基酸残基被具有化特性(例如电荷或疏水性)类似的侧链r基的另一个氨基酸残基置换。一般来讲,保守氨基酸置换实质上不会改变蛋白质的所关注的功能性质,例如,受体结合配体的能力。侧链具有相似化学特性的氨基酸组实例包括:脂族侧链,例如甘氨酸、丙氨酸、缬氨酸、亮氨酸和异亮氨酸;脂族羟基侧链,例如丝氨酸和苏氨酸;含酰胺侧链,例如天冬酰胺和谷氨酰氨;芳香族侧链,例如苯丙氨酸、酪氨酸和色氨酸;碱性侧链,例如赖氨酸、精氨酸和组氨酸;酸性侧链,例如天冬氨酸和谷氨酸;以及含硫侧链,例如半胱氨酸和甲硫氨酸。保守性氨基酸取代群组包括例如缬氨酸/亮氨酸/异亮氨酸、苯丙氨酸/酪氨酸、赖氨酸/精氨酸、丙氨酸/缬氨酸、谷氨酸/天冬氨酸和天冬酰胺/谷氨酰胺。
130.在一些实施例中,保守性氨基酸取代可以是蛋白质中的任何原生残基被丙氨酸取代,如例如丙氨酸扫描突变诱发中所使用。在一些实施方案中,进行保守置换,所述保守置换在gonnet,g.h.等人,1992,science 256:1443
‑
1445(据此以全文引用的方式并入)公开的pam250对数似然矩阵中具有正值。在一些实施方案中,如果置换在pam250对数似然矩阵中具有非负值,则该置换是适度保守置换。
131.对照:是指在本领域中所理解的“对照”的含义,所述对照是与结果进行比较的标准品。通常,对照通过分离变量以得出有关此类变量的结论而用于增进实验完整性。在一些
实施方案中,对照是与测试反应或测定同时进行以提供比较的反应或测定。“对照”可指“对照动物”“对照动物”可以具有如本文所述的修饰(与本文所述的修饰不同的修饰)或不具有修饰(即,野生型动物)。在一个实验中,施加“测试”(即,所测试的变量)。在第二个实验中,施加“对照”,不施加所测试的变量。对照可以是阳性对照或阴性对照。
132.在一些实施方案中,对照是历史对照(即,此前进行的测试或测定,或此前已知的量或结果)。在一些实施方案中,对照为或包括印刷或以其他方式保存的记录。
133.断裂:是指与dna分子(例如,与内源性同源序列诸如基因或基因座)同源重组事件的结果。
134.在一些实施方案中,断裂可实现或代表插入、缺失、置换、替换、错义突变或dna序列移码或它们的任何组合。插入可包括插入整个基因、基因片段例如外显子(其可具有除内源序列外的起源(例如,异源序列))、或者从特定目的基因衍生或分离的编码序列。在一些实施方案中,破坏可以增强基因或基因产物(例如由基因编码的蛋白质)的表达和/或活性。在一些实施方案中,断裂可减少基因或基因产物的表达和/或活性。在一些实施方案中,破坏可以改变基因或编码的基因产物(例如编码的蛋白质)的序列。在一些实施方案中,破坏可以改变基因组中染色体的序列或染色体位置。在一些实施方案中,破坏可以截断或分裂基因或已编码的基因产物(例如已编码的蛋白质)。在一些实施方案中,断裂可以延伸基因或所编码的基因产物。在一些此类实施例中,破坏可以实现融合蛋白的组装。在一些实施方案中,断裂可影响基因或基因产物的水平但不影响其活性。在一些实施方案中,断裂可影响基因或基因产物的活性但不影响其水平。在一些实施方案中,断裂可对基因或基因产物的水平无显著影响。在一些实施方案中,断裂可对基因或基因产物的活性无显著影响。在一些实施方案中,断裂可对基因或基因产物的水平或活性都无显著影响。在一些实施方案中,可以通过例如但不限于学生t检验来测量显著影响。
135.内源性基因座或内源性基因:是指在引入如本文所述的改变、破坏、缺失、插入、修饰、置换或替换之前在亲本或参考生物体(或细胞)中发现的遗传基因座。
136.在一些实施方案中,内源性基因座包含天然存在的序列(全部或部分)。在一些实施例中,内源基因座为野生型基因座。在一些实施方案中,参考生物体为野生型生物体。在一些实施方案中,参考生物体为经工程化的生物体。在一些实施方案中,参考生物体为实验室繁育的生物体(无论是野生型还是经工程化的)。
137.内源性启动子:是指例如在野生型生物体中与内源性基因或遗传基因座天然关联的启动子。
138.被工程化:通常是指由人工操纵的方面。如通常实践并且由本领域的技术人员所理解的,即使实际的操作是对先前的实体进行的,被工程化多核苷酸或细胞的子代通常仍然被称为“被工程化”。此外,本领域的技术人员将认识到,可以通过多种可用的方法来实现本文所述的“工程化”。
139.在一些实施方案中,当不以自然界中的顺序连接在一起的两个或更多个序列通过人工操纵而在经工程化多核苷酸中直接彼此连接时,多核苷酸可被视为“经工程化”。在一些实施方案中,经工程化多核苷酸可以包含自然界中存在的与第一编码序列有效地连接但不与第二编码序列有效地连接的调控序列,所述调控序列通过人工连接而使得其与第二编码序列有效地连接。在本文的工程化d
h
基因区段实施方案中,d
h
基因区段由人工操纵以有效
地连接至(例如,在至少一侧侧接有、与之相邻、与之邻接、与之紧邻)23聚体rss。在一些实施方案中,被工程化以有效地连接至23聚体rss的d
h
基因区段衍生自另一个d
h
基因区段,例如,有效地连接至23聚体rss的d
h
基因区段包含一个核苷酸序列,所述核苷酸序列与其他d
h
基因区段的核苷酸序列相同但由于遗传密码的简并性和/或12聚体rss被23聚体rss替换而具有差异。另一个d
h
基因区段和从其衍生的工程化d
h
基因区段(例如,有效地连接至23聚体rss的d
h
基因区段)可以被认为是对应的基因区段。例如,有效地连接至23聚体rss的人d
h3‑
3基因区段可以被认为对应于在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的d
h3‑
3基因区段,其中所述有效地连接至23聚体rss的d
h3‑
3基因区段和所述在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的d
h3‑
3基因区段,除了由于遗传密码的简并性和/或两个12聚体rss中的一个被23聚体rss替换导致的差异之外,共享相同的核苷酸序列。可替代地或另外地,在一些实施例中,各自编码在自然界中彼此不连接的多肽元件或结构域的第一核酸序列和第二核酸序列可在单个经改造的多核苷酸中彼此连接。相比之下,在一些实施方案中,如果细胞或生物体已被操纵而使得其遗传信息被改变(例如,此前不存在的新遗传物质已经被引入,或者此前存在的遗传物质已被改变或移除),则所述细胞或生物体可被视为“经工程化”。
140.在一些实施方案中,“工程化”可以涉及通过使用计算机系统进行选择或设计(例如,核酸序列、多肽序列、细胞、组织和/或生物体的选择或设计),所述计算机系统经编程以执行分析或比较,或者分析、推荐和/或选择序列、改变等)。可替代地或另外地,在一些实施方案中,“工程化”可以涉及使用体外化学合成方法学和/或重组核酸技术,例如核酸扩增(例如通过聚合酶链式反应)杂交、突变、转化、转染等,和/或多种受控交配方法中的任一种。如将由本领域的技术人员所理解,多种确立的此类技术(例如,用于重组dna、寡核苷酸合成以及组织培养和转化(例如,电穿孔、脂质转染等))是本领域熟知的并且在本说明书全文中所引用和/或讨论的多种一般和更具体的参考文献中有所描述。参见例如sambrook等人,molecular cloning:a laboratory manual(第2版,cold spring harbor laboratory press,cold spring harbor,n.y.,1989;以引用的方式整体并入本文)。
141.基因:是指编码产物(例如,rna产物和/或多肽产物)的染色体中的dna序列。为了清晰起见,术语“基因”通常是指编码多肽的核酸的一部分;该术语可以任选地涵盖调控序列,如本领域的普通技术人员将从上下文清晰地理解那样。该定义无意排除将术语“基因”应用于非蛋白质编码表达单元,而是为了阐明,在大多数情况下,本文档所用的术语是指编码多肽的核酸。
142.在一些实施方案中,基因包括编码序列(即,编码特定产物的序列)。在一些实施方案中,基因包括非编码序列。在一些实施方案中,基因可以包括编码(例如,外显子)和非编码(例如,内含子)序列二者。在一些实施方案中,基因可以包括例如可以控制或影响基因表达的一个或多个方面(例如,细胞类型特异性表达、诱导型表达等)的一个或多个调控序列(例如,启动子、增强子等)和/或内含子序列。
143.异源的:是指不同来源的药剂或实体。例如,当用于提及存在于特定细胞或生物体中的多肽、基因或基因产物时,所述术语阐明,相关的多肽或其片段、基因或其片段、或基因产物或其片段:(1)通过人工被工程化;(2)通过人工(例如,经由基因工程化)被引入细胞或生物体(或其前体);和/或(3)不是相关细胞或生物体(例如,相关细胞类型或生物体类型)
天然产生的或不存在于它们中。另一个实例包括通常存在于特定天然细胞或生物体中的多肽或其片段、基因或其片段、或基因产物或其片段,但已经在非天然关联的且在一些实施方案中非内源性的调控元件(例如,启动子)的控制下例如通过突变或替换而进行了修饰。
144.宿主细胞:是指将异源(例如,外源)核酸或蛋白质引入其中的细胞。本领域技术人员在阅读本公开后将理解,此类术语不仅指特定的主题细胞,而且还用于指该细胞的子代。因为某些修饰可因突变或环境影响而在后续世代中发生,所以这样的子代事实上可不等同于亲本细胞,但仍包括在本文中使用的术语"宿主细胞"的范围内。
145.在一些实施方案中,宿主细胞为或包括原核细胞或真核细胞。在实施方案中,宿主细胞是或包含哺乳动物细胞。一般来讲,宿主细胞是适于接受和/或产生异源核酸或蛋白质的任何细胞,而与该细胞被指定所属的生命界无关。示例性细胞包括原核生物和真核生物的那些细胞(单细胞或多细胞)、细菌细胞(例如大肠杆菌(escherichia coli)、芽孢杆菌属(bacillus spp.)、链霉菌属(streptomyces spp.)等的菌株)、分枝杆菌细胞、真菌细胞、酵母细胞(例如,酿酒酵母(saccharomyces cerevisiae)、粟酒裂殖酵母(schizosaccharomyces pombe)、巴斯德毕赤酵母(pichia pastoris)、甲醇毕赤酵母(pichia methanolica)等)、植物细胞、昆虫细胞(例如,sf
‑
9、sf
‑
21、杆状病毒感染的昆虫细胞、粉纹夜蛾(trichoplusia ni)等)、非人动物细胞,人细胞,或细胞融合物,例如杂交瘤或四重杂交瘤。
146.在一些实施例中,细胞是人类、猴、猿、仓鼠、大鼠或小鼠细胞。在一些实施例中,细胞是真核细胞且选自以下细胞:cho(例如cho k1、dxb
‑
11cho、veggie
‑
cho)、cos(例如cos
‑
7)、视网膜细胞、vero、cv1、肾脏(例如hek293、293ebna、msr 293、mdck、hak、bhk)、hela、hepg2、wi38、mrc 5、colo205、hb 8065、hl
‑
60(例如bhk21)、jurkat、daudi、a431(表皮)、cv
‑
1、u937、3t3、l细胞、c127细胞、sp2/0、ns
‑
0、mmt 060562、塞特利氏细胞(sertoli cell)、brl 3a细胞、ht1080细胞、骨髓瘤细胞、肿瘤细胞,和来源于前述细胞的细胞系。在一些实施例中,细胞包含一个或多个病毒基因,例如表达病毒基因的视网膜细胞(例如细胞)。在一些实施方案中,宿主细胞为或包括分离的细胞。在一些实施方案中,宿主细胞为组织的一部分。在一些实施方案中,宿主细胞为生物体的一部分。
147.人源化:是指非人起源的并且其一部分已以使得经修饰的(例如,人源化)分子保留其生物学功能和/或维持执行所保留的生物学功能的结构的的方式被对应人类分子的对应部分替换的分子(例如核酸、蛋白质等)。相比之下,“人”等涵盖只来源于人的分子,例如分别只包含人核苷酸和氨基酸序列的人核苷酸或蛋白质。术语“人(源化)”用于反映人(源化)分子可为(a)人分子或(b)人源化分子。
148.同一性:结合序列比较,是指由可用于测量核苷酸和/或氨基酸序列同一性的本领域已知的许多不同算法所确定的同一性。
149.在一些实施方案中,使用clustalw v.1.83(慢)比对(采用开放缺口罚分10.0、延伸缺口罚分0.1)和使用gonnet相似性矩阵(macvector
tm
10.0.2,macvector inc.,2008)来确定本文所述的同一性。
150.在体外:是指在人造环境中,例如在试管或反应容器中,在细胞培养物等中,而不是在多细胞生物体内发生的事件。
151.在体内:是指在多细胞生物体,诸如人类和/或非人类动物内发生的事件。在基于
细胞的系统的语境中,该术语可以用于指在活细胞内(与例如体外系统相对)发生的事件。
152.分离的:是指已经(1)在最初产生时(无论在自然中和/或在实验环境中)与其关联的组分中的至少一些组分分离的物质和/或实体,和/或(2)经人手设计、生产、制备和/或制造的物质和/或实体。分离的物质和/或实体可以与它们最初关联的约10种或更多种其他组分分开。在一些实施方案中,分离的药剂是至少约80%或更高百分比纯的。如果物质基本上不含其他组分,则其是“纯的”。在一些实施方案中,如将由本领域的技术人员所理解,在与某些其他组分(例如,一种或多种载剂或赋形剂(如,缓冲液、溶剂、水等))组合后,物质仍可被认为是“分离的”或甚至是“纯的”;在此类实施方案中,计算不包括此类载剂或赋形剂的物质的分离百分比或纯度。
153.仅举一个例子,在一些实施方案中,天然存在的生物聚合物诸如多肽或多核苷酸(a)在因其衍生的起源或来源而不与在其天然状态下天然伴随其的一些或全部组分关联时;(b)在其实质上不含与天然产生其的物种相同的物种的其他多肽或核酸时;(c)当由不是天然产生其的物种的细胞或其他表达系统表达或以其他方式与这些细胞或其他表达系统的组分关联时,被认为是“分离的”。因此,例如,在一些实施方案中,化学合成或在与天然产生多肽的细胞系统不同的细胞系统中合成的多肽被认为是“分离的”多肽。可替代地或另外地,在一些实施方案中,已历经一种或多种纯化技术的多肽在其已与a)在自然界中与其关联的;和/或b)当最初产生时与其关联的其他组分分离的程度上可被认为是“分离的”多肽。
154.非人动物:是指并非人类的任何脊椎动物生物体。
155.在一些实施方案中,非人动物是圆口类的鱼、硬骨鱼、软骨鱼(例如鲨鱼或鳐)、两栖动物、爬行动物、哺乳动物和鸟类。在一些实施方案中,非人哺乳动物为灵长类动物、山羊、绵羊、猪、狗、奶牛或啮齿动物。在一些实施方案中,非人动物为啮齿动物,例如大鼠或小鼠。
156.核酸:在其最广泛的意义上,是指被或可以被掺入寡核苷酸链中且通常可与核酸分子、核酸序列、核苷酸分子、核苷酸分子互换的任何化合物和/或物质,这些术语也是可彼此互换的。
157.在一些实施方案中,“核酸”是为寡核苷酸链或可以通过磷酸二酯键并入寡核苷酸链中的化合物和/或物质。从上下文可以看出,在一些实施方案中,“核酸”是指单个核酸残基(例如,核苷酸和/或核苷);在一些实施方案中,“核酸”是指包含单个核酸残基的寡核苷酸链。在一些实施方案中,“核酸”为或包含rna;在一些实施方案中,“核酸”为或包含dna。在一些实施方案中,“核酸”是一个或多个天然核酸残基,包含一个或多个天然核酸残基,或由一个或多个天然核酸残基组成。在一些实施方案中,“核酸”是一种或多种核酸类似物,包含一种或多种核酸类似物,或由一种或多种核酸类似物组成。在一些实施方案中,核酸类似物不同于“核酸”,因为核酸类似物不利用磷酸二酯主链。例如,在一些实施方案中,“核酸”是、包含、或由一个或多个“肽核酸”组成,这些肽核酸在本领域中已知并且在主链中具有肽键而不是磷酸二酯键,被视为在本发明的范围内。可替代地或另外地,在一些实施方案中,“核酸”具有一个或多个硫代磷酸酯和/或5'
‑
n
‑
亚磷酰胺键,而不是磷酸二酯键。在一些实施方案中,“核酸”为一个或多个天然核苷(例如,腺苷、胸苷、鸟苷、胞苷、尿苷、脱氧腺苷、脱氧胸苷、脱氧鸟苷和脱氧胞苷)、包含一个或多个天然核苷、或由一个或多个天然核苷组成。在一
些实施方案中,“核酸”为一个或多个核苷类似物(例如,2
‑
氨基腺苷、2
‑
硫代胸苷、肌苷、吡咯并嘧啶、3
‑
甲基腺苷、5
‑
甲基胞苷、c
‑
5丙炔基胞苷、c
‑
5丙炔基尿苷、2
‑
氨基腺苷、c5
‑
溴尿苷、c5
‑
氟尿苷、c5
‑
碘尿苷、c5
‑
丙炔基尿苷、c5
‑
丙炔基胞苷、c5
‑
甲基胞苷、2
‑
氨基腺苷、7
‑
脱氮腺苷、7
‑
脱氮鸟苷、8
‑
氧代腺苷、8
‑
氧代鸟苷、o(6)
‑
甲基鸟嘌呤、2
‑
硫代胞苷、甲基化碱基、插入型碱基以及它们的组合)、包含一个或多个核苷类似物或由一个或多个核苷类似物组成。在一些实施方案中,“核酸”包含一种或多种与天然核酸中的那些糖相比被修饰的糖(例如,2'
‑
氟核糖、核糖、2'
‑
脱氧核糖、阿拉伯糖和己糖)。在一些实施方案中,“核酸”具有编码功能性基因产物(例如rna或蛋白质)的核苷酸序列。在一些实施方案中,“核酸”具有编码多肽片段(例如,肽)的核苷酸序列。在一些实施方案中,“核酸”包括一个或多个内含子。在一些实施方案中,“核酸”包括一个或多个外显子。在一些实施方案中,“核酸”包括一个或多个编码序列。在一些实施方案中,“核酸”通过下述方式中的一种或多种来制备:从天然来源分离、通过基于互补模板的聚合(体内或体外)进行的酶学合成、在重组细胞或系统中的复制以及化学合成。在一些实施方案中,“核酸”为至少3个或更多个残基长。在一些实施方案中,“核酸”是单链的;在一些实施方案中,“核酸”是双链的。在一些实施方案中,“核酸”具有包含至少一个元件的核苷酸序列,所述至少一个元件编码多肽或其片段或者是编码多肽或其片段的序列的互补序列。在一些实施方案中,“核酸”具有酶促活性。
158.有效地连接的:是指其中所描述的组分处于允许它们以它们的预期方式发挥功能的关系中的并置。
159.在一些实施方案中,有效地连接的核苷酸序列与彼此邻接,例如,含有与rss有效地连接的免疫球蛋白基因区段的核酸序列包含与rss核苷酸序列邻接的免疫球蛋白基因区段核苷酸序列,例如免疫球蛋白基因区段以连续的方式在至少一侧上侧接有(例如,毗邻)rss核苷酸序列,使得所述免疫球蛋白基因区段紧邻所述rss核苷酸序列。
160.在其他实施方案中,有效连接不需要邻接。例如,彼此“有效地连接”的未重排的可变区基因区段能够重排以形成重排的可变区基因,所述未重排的可变区基因区段可能不一定彼此邻接。彼此有效地连接并且与连续恒定区基因有效地连接的未重排的可变区基因区段能够重排以形成重排的可变区基因,所述重排的可变区基因与恒定区基因一起表达为抗原结合蛋白的多肽链。与编码序列“有效地连接”的控制序列以这样的方式连接,使得在与所述控制序列相容的条件下实现所述编码序列的表达。"有效地连接"序列包括与所关注基因邻接的表达控制序列和按照反式或在一定距离发挥作用以控制所关注基因的表达控制序列。
161.术语“表达控制序列”是指多核苷酸序列,所述多核苷酸序列是影响它们所连接的编码序列的表达和加工所必需的。“表达控制序列”包括合适的转录起始、终止、启动子和增强子序列;有效的rna加工信号例如剪接和多聚腺苷酸化信号;使细胞质mrna稳定的序列;增强翻译效率的序列(即kozak共有序列);增强蛋白稳质定性的序列;以及当需要时,增强蛋白分质泌的序列。这种控制序列的性质根据宿主生物体而不同。例如,在原核生物中,这种控制序列一般包括启动子、核糖体结合位点和转录终止序列,而在真核生物中,通常地,这种控制序列包括启动子和转录终止序列。术语“控制序列”旨在包括这样的组分:它们的存在对于表达和加工来说是必需的,并且还可包括这样的另外组分,它们的存在是有利的,例如前导序列和融合伴侣序列。
162.通常,每个未重排的免疫球蛋白v基因区段、d基因区段或j基因区段与重组信号序列(rss)有效地连接(例如,与之关联、在一侧或两侧上侧接有它、与之邻接等),所述重组信号序列可以是12聚体rss或23聚体rss。在每一侧上均侧接有rss的任何基因区段(包括有效地连接至23聚体rss的d
h
基因区段)均未经历重组,并且因此可以被视为“未重排的”基因区段。在一些实施方案中,本文中未重排的基因区段可以包含处于其种系(例如,野生型)构型中的基因区段,例如,各自在两侧均侧接有23聚体rss的种系v
h
基因区段和种系j
h
基因区段。相比之下,种系d
h
基因区段(例如未重排的d
h
基因区段)在每一侧上都侧接有12聚体rss。有效地连接至23聚体rss的d
h
基因区段(例如工程化d
h
基因区段)也未经历过重组,并且因此包含(i)23聚体rss和(ii)12聚体rss。工程化d
h
基因区段(例如,有效地连接至23聚体rss的d
h
基因区段)能够与另一个有效地连接至12聚体rss的d
h
基因区段根据12/23重组规则进行重排。
163.生理条件:具有其在本领域理解的含义,是指细胞或生物体生存和/或繁殖的条件。在一些实施例中,该术语指对于生物或细胞系统在自然界可发生的外部或内部环境的条件。在一些实施方案中,生理条件是存在于人类或非人类动物体内的那些条件,尤其是存在于手术部位处和/或手术部位内的那些条件。生理条件通常包括例如20
‑
40℃的温度范围、大气压力1、ph 6
‑
8、1
‑
20mm的葡萄糖浓度、以大气水平的氧浓度和如它在地球上遇到的重力。在一些实施例中,实验室中的条件在生理条件下操纵和/或维持。在一些实施例中,生理条件在生物(例如,非人动物)中遇到。
164.多肽:是指氨基酸的任何聚合链。
165.在一些实施方案中,多肽具有在天然中存在的氨基酸序列。在一些实施方案中,多肽具有不在天然中存在的氨基酸序列。在一些实施方案中,多肽具有这样的氨基酸序列:其包含在自然中彼此单独存在的部分(即,来自两种或更多种不同的生物体,例如人类和非人类部分)。在一些实施方案中,多肽具有由于通过人工行为来设计和/或产生而工程化的氨基酸序列。在一些实施例中,多肽可包含多个片段或由多个片段组成,所述片段各自相对于彼此以与目的多肽中发现的那种不同的空间排列在相同亲本多肽中发现(例如在亲本中直接连接的片段可在目的多肽中在空间上分开,或反之亦然,和/或片段可在目的多肽中以与在亲本中不同的次序存在),使得目的多肽是其亲本多肽的衍生物。
166.重组:是指通过重组手段设计、工程化、制备、表达、创建或分离的多肽,诸如使用转染至宿主细胞中的重组表达载体来表达的多肽,从重组、组合人多肽文库中分离的多肽(hoogenboom h.r.,1997 tib tech.15:62
‑
70;hoogenboom h.和chames p.,2000,immunology today 21:371
‑
378;azzazy h.和highsmith w.e.,2002,clin.biochem.35:425
‑
445;gavilondo j.v.和larrick j.w.,2002,biotechniques 29:128
‑
145)、从对于人免疫球蛋白基因而言是转基因的动物(例如小鼠)中分离的抗体(参见例如,taylor,l.d.等人,1992,nucl.acids res.20:6287
‑
6295;little m.等人,2000,immunology today 21:364
‑
370;kellermann s.a.和green l.l.,2002,current opinion in biotechnology 13:593
‑
597;murphy,a.j.等人,2014,proc.natl.acad.sci.u.s.a.111(14):5153
‑
5158;每篇文献以全文引用的方式并入本文)、或者通过涉及将所选的序列元件剪接至彼此的任何其他手段制备、表达、创建或分离的多肽。
167.在一些实施方案中,此类选定的序列元件中的一个或多个是天然存在的。在一些
实施方案中,此类选定的序列元件中的一个或多个是通过计算机模拟(in silico.)来设计的。在一些实施方案中,一个或多个此类选定的序列元件由已知序列元件(例如,来自天然或合成来源)的诱变(例如,体内或体外)产生。例如,在一些实施例中,重组多肽包含在目的源生物(例如人、小鼠等)的基因组(或多肽)中发现的序列。在一些实施例中,重组多肽包含在两种不同生物(例如人和非人生物)中,在自然界中彼此分开存在的序列(即,来自两种或更多种不同生物,例如人和非人部分)。在一些实施例中,重组多肽具有来源于诱变(例如在体外或体内,例如在非人动物中)的氨基酸序列,使得重组多肽的氨基酸序列是这样的序列,其虽然源于多肽序列且与多肽序列相关,但可能并非天然存在于非人动物体内.的基因组内。
168.参考:是指与所关注的药剂、动物、队列、个体、群体、样品、序列或值相比较的标准或对照药剂、动物、队列、个体、群体、样品、序列或值。“参考”可以是指“参考动物”。“参考动物”可以具有如本文所述的修饰,与本文所述不同的修饰或不具有修饰(即,野生型动物)。典型地,如所属领域的技术人员所理解,参考药剂、动物、群组、个体、群体、样品、序列或值是在与用于测定或表征所关注的药剂、动物(例如哺乳动物)、群组、个体、群体、样品、序列或值的条件相当的条件下测定或表征。
169.在一些实施例中,参考药剂、动物、群组、个体、群体、样品、序列或值的测试和/或测定基本上与所述药剂、动物、群组、个体、群体、样品、序列或值的测试或测定同时进行。在一些实施方案中,参考药剂、动物、队列、个体、群体、样品、序列或值为历史参考,其任选地以有形介质体现。在一些实施方案中,参考可以指对照。
170.实质上:是指表现出所关注的特征或特性的全部或几乎全部程度或程度的定性状况。生物学领域的普通技术人员将理解,生物学和化学现象很少(如果有的话)进行至完成和/或进行至完全,或实现或避免绝对的结果。因此术语“实质上”用于捕获许多生物学和化学现象固有的完全性的潜在缺乏。
171.实质上同源性:是指氨基酸或核酸序列之间的比较。如将由本领域的普通技术人员所理解,如果两个序列在对应的位置上含有同源的残基,则它们通常被认为是“实质上同源的”。同源残基可以是相同的残基。或者,同源残基可以是具有适当相似的结构和/或功能特征的不相同的残基。例如,如本领域的普通技术人员所熟知,某些氨基酸通常被归类为“疏水性”或“亲水性”氨基酸,和/或被归类为具有“极性”或“非极性”侧链。一个氨基酸对另一个相同类型的氨基酸的置换可以通常被认为是“同源”置换。典型的氨基酸分类汇总如下:
[0172][0173][0174]
如本领域中所熟知,氨基酸或核酸序列可以使用多种算法中的任何算法来进行比较,所述算法包括商业计算机程序中可获得的那些算法,诸如用于核苷酸序列的blastn以及用于氨基酸序列的blastp、空位blast和psi
‑
blast。示例性的此类程序在以下文献中有所描述:altschul,s.f.等人,1990,j.mol.biol.,215(3):403
‑
410;altschul,s.f.等人,1996,methods in enzymol.266:460
‑
80;altschul,s.f.等人,1997,nucleic acids res.,25:3389
‑
402;baxevanis,a.d.和b.f.f.ouellette(编辑)bioinformatics:a practical guide to the analysis of genes and proteins,wiley,1998;以及misener等人(编辑)bioinformatics methods and protocols(methods in molecular biology,第132卷),humana press,1998。除了鉴定同源序列以外,上文提及的程序通常还提供同源性程度的指示。
[0175]
在一些实施方案中,如果两个序列的至少95%或更多的相应残基在相关的残基序列段(stretch)上是同源的,则这两个序列被认为是基本上同源的。在一些实施方案中,相关序列段为完全序列。在一些实施方案中,相关序列段为至少9个或更多个残基。在一些实施方案中,相关序列段包括沿着完全序列的邻接的残基。在一些实施方案中,相关序列段包
括沿着完全序列的非邻接的残基,例如通过多肽或其一部分的折叠构象集中在一起的非邻接的残基。在一些实施方案中,相关序列段为至少10个或更多个残基。
[0176]
实质上同一性:是指氨基酸或核酸序列之间的比较。如将由本领域的普通技术人员所理解,如果两个序列在对应的位置上含有相同残基,则这两个序列通常被认为是“实质上相同的”。如本领域中所熟知,氨基酸或核酸序列可以使用多种算法中的任何算法来进行比较,所述算法包括商业计算机程序中可获得的那些算法,诸如用于核苷酸序列的blastn以及用于氨基酸序列的blastp、空位blast和psi
‑
blast。示例性的此类程序在以下文献中有所描述:altschul,s.f.等人,1990,j.mol.biol.,215(3):403
‑
410;altschul,s.f.等人,1996,methods in enzymol.266:460
‑
80;altschul,s.f.等人,1997,nucleic acids res.,25:3389
‑
3402;baxevanis,a.d.和b.f.f.ouellette(编辑)bioinformatics:apractical guide to the analysis of genes and proteins,wiley,1998;以及misener等人(编辑)bioinformatics methods and protocols(methods in molecular biology,第132卷),humana press,1998。除了鉴定相同的序列以外,上文提及的程序通常还提供同一性程度的指示。
[0177]
在一些实施方案中,如果两个序列的至少95%或更多的相应残基在相关的残基序列段(stretch)上是相同的,则这两个序列被认为是实质上相同的。在一些实施方案中,相关序列段为完全序列。在一些实施方案中,相关序列段为至少10个或更多个残基。
[0178]
靶向载体或靶向构建体:是指包含靶向区域的多核苷酸分子。靶向区域包含这样的序列:该序列与靶细胞、组织或动物中的序列相同或实质上相同,并且提供了靶向构建体经由同源重组至所述细胞、组织或动物的基因组内的位置的整合。还包括使用位点特异性重组酶识别位点(例如,loxp或frt位点)进行靶向的靶向区域。
[0179]
在一些实施例中,如本文所述的靶向构建体还包含特定目的核酸序列或基因、可选择标记物、对照和/或调控序列、以及允许通过外源添加蛋白质介导的重组的其它核酸序列,所述蛋白质帮助或促进涉及此类序列的重组。在一些实施方案中,如本文所述的靶向构建体还包含全部或部分的所关注的基因,其中所关注的基因是编码全部或部分的多肽的异源基因,所述多肽具有与内源序列编码的蛋白质相似的功能。在一些实施方案中,如本文所述的靶向构建体还包含全部或部分的所关注的人源化基因,其中所关注的人源化基因编码全部或部分的多肽,所述多肽具有与内源序列编码的多肽相似的功能。在一些实施方案中,靶向构建体(或靶向载体)可以包含由人工操纵的核酸序列。例如,在一些实施方案中,靶向构建体(或靶向载体)可构建为包含含有两个或更多个序列的经工程化的或重组多核苷酸,所述两个或更多个序列不以自然界中的顺序连接在一起,而是由人工操纵为在经工程化的或重组多核苷酸中彼此直接连接。
[0180]
转基因或转基因构建体:是指诸如通过本文所述的方法由人工引入细胞内的核酸序列(编码例如全部或部分所关注的多肽)。转基因对于它所被引入其中的转基因动物或细胞可为部分或完全异源的,即外源的。转基因可以包括一个或多个转录调控序列和任何其他核酸,诸如内含子或启动子,它们对于选定的核酸序列的表达可为必需的。转基因可以包括允许随后选择已经摄取所述转基因的后代(例如,细胞)的一种或多种选择性标记。
[0181]
转基因动物、转基因非人动物、或tg
+
:在本文中可互换使用,并且是指任何非天然存在的非人动物,其中非人动物的一种或多种细胞含有编码全部或部分所关注多肽的异源
核酸和/或基因。
[0182]
在一些实施方案中,通过有意的遗传操纵(诸如通过显微注射或通过用重组病毒感染)直接或间接引入前体细胞内,从而将异源核酸序列和/或基因引入细胞中。术语遗传操作不包括经典育种技术,而是涉及重组dna分子的引入。该分子可以整合进染色体内,或者它可以是染色体外复制的dna。术语“tg
+”包括异源核酸和/或基因的杂合子或纯合子动物,和/或具有单拷贝或多拷贝的异源核酸和/或基因的动物。
[0183]
载体:是指能够转运与其关联的另一种核酸的核酸分子。
[0184]
在一些实施方案中,载体能够在宿主细胞(诸如真核和/或原核细胞)中进行染色体外复制和/或表达它们所连接的核酸。能够指导有效地连接的基因的表达的载体在本文中被称为“表达载体”。
[0185]
野生型:具有其本领域理解的含义,是指具有如在“正常”(相对于突变的、患病的、工程化的、改变的等)状态或环境中天然存在的结构和/或活性的实体。本领域的普通技术人员将理解,野生型基因和多肽通常以多种不同的形式(例如,等位基因)存在。
[0186]
本发明的其他特征、目的和优点在以下的一些实施方案的详细描述中是显而易见的。然而,应当理解,详细描述虽然指示本发明的一些实施方案,但其仅通过举例说明的方式给出,而不是限制性的。所属领域的技术人员从详细描述将显而易见属于本发明范围内的各种变化和修改。
具体实施方式
[0187]
本发明尤其提供了具有编码人免疫球蛋白的一个或多个部分(功能片段、结合部分等)的异源遗传物质的转基因或工程化非人动物,所述异源遗传物质被插入免疫球蛋白重链可变区基因座中,从而使所述异源遗传物质与重链恒定(c
h
)基因有效地连接。预期此类非人动物展示出产生由重排的v(dd)j序列编码的抗体的能力。还预期,如与具有由野生型免疫球蛋白重链可变区基因座(或在自然界中出现的免疫球蛋白重链可变区基因座)产生的具有免疫球蛋白重链可变cdr3多样性的抗体群体相比,此类非人动物展示出特征在于具有增加的cdr3多样性的重链可变区的抗体群体。因此,所提供的非人动物对于结合特定抗原(特别是与低和/或差的免疫原性相关的抗原或以不利于被传统(或野生型)抗体结合的一个或多个表位为特征的抗原)的基于抗体的治疗剂的开发特别有用。特别地,本发明涵盖导致在vdj重组期间d
h
与d
h
区段重排的能力的在免疫球蛋白重链可变区中与d
h
区的一个或多个d
h
区段紧邻(例如其5’或3’)的23聚体重组信号序列的引入、以及如与由涉及单个d
h
区段的vdj重组产生的抗体相比可能以更长的氨基酸长度为特征的具有重链可变区(以及尤其是cdr3区)的抗体的表达。此类转基因非人动物提供了一种体内系统,用于鉴定和开发结合超出了既有药物发现技术的靶向能力的疾病靶标的抗体和/或基于抗体的治疗剂。此外,此类转基因非人动物提供了用于开发抗体和/或基于抗体的治疗剂的有用动物模型系统,所述抗体和/或基于抗体的治疗剂集中于或设计用于破坏对于影响人的各种疾病和/或疾病病理学关键的蛋白质
‑
蛋白质相互作用。
[0188]
如图1顶图所示,免疫球蛋白基因区段之间的重组遵循通常称为12/23规则的规则,其中侧翼为重组信号序列(rss)的基因区段通过有序过程进行连接。每个rss由以下项组成:与编码序列(例如,v
h
、d
h
或j
h
区段)邻接的七个核苷酸的保守嵌段(七聚体;5
’‑
cacagtg
‑3’
;seq id no:144),随后是长度为12bp或23bp的非保守区(称为间隔子),以及九个核苷酸的第二保守嵌段(九聚体;5
’‑
acaaaaacc
‑3’
;seq id no:145)。间隔子的序列可以变化,但是其保守长度对应于dna双螺旋的一个或两个匝。这会将七聚体和九聚体序列带到dna螺旋的同一侧,在此处它们可以被催化重组的蛋白质复合物结合。具有23bp间隔子的rss是23聚体rss,并且具有12bp间隔子的rss是12聚体rss。12/23重组规则通常会促进在12聚体rss与23聚体rss之间的重组,并禁止在23聚体rss与另一个23聚体rss之间或在12聚体rss与另一个12聚体rss之间的重组,例如,禁止直接种系v
h
与种系j
h
重组(即23聚体与23聚体连接)或种系d
h
‑
种系d
h
重组(即,12聚体与12聚体连接),尽管已经报告了例外情况。
[0189]
在一些实施方案中,如本文所述的非人动物包含免疫球蛋白重链可变区,所述免疫球蛋白重链可变区含有工程化多样性簇(即工程化d
h
区),所述工程化多样性簇的特征在于其每一个都有效地连接至23聚体rss并且因此能够进行d
h
‑
d
h
重组的一个或多个d
h
区段的存在。在一些实施方案中,含有由这种重组产生的cdr3的抗体可以被表征为具有增加的多样性,这是由更长的氨基酸长度指导与特定抗原(例如,病毒、膜通道等)结合引起的。在一些实施方案中,本文所述的非人动物包含与工程化d
h
区有效地连接的人重链可变(v
h
)和连接(j
h
)基因区段,使得在所述v
h
、j
h
和超过一个d
h
区段之间发生vdj重组以产生结合所关注的抗原的重链可变区。在一些实施方案中,如本文所述的工程化d
h
区含有一个或多个(例如,1个、2个、3个、4个、5个、10个或更多个)人d
h
区段,其被工程化以允许(或促进)以与参考免疫球蛋白重链可变区基因座相比增加的频率进行d
h
与d
h
重组。在一些实施方案中,如本文所述的非人动物在非人动物基因组中的免疫球蛋白重链可变区处包含与各自有效地连接至23聚体重组信号序列(rss)的一个或多个d
h
区段有效地连接的多个v
h
和j
h
基因区段。在许多实施方案中,v
h
和j
h
区段是人v
h
和人j
h
基因区段。
[0190]
在一些实施方案中,如本文所述的非人动物还包含人或人源化免疫球蛋白轻链基因座(例如,和/或),使得所述非人动物产生包含人可变区(即,重和轻)和非人恒定区的抗体。在一些实施方案中,所述人或人源化免疫球蛋白轻链基因座包含与啮齿动物轻链恒定区(例如,啮齿动物c或c)有效地连接的人v
l
和j
l
基因区段。在一些实施方案中,本文所述的非人动物还包含如在以下文献中所描述的免疫球蛋白轻链基因座:美国专利号9,796,788;9,969,814;美国专利申请公开号2011/0195454 a1、2012/0021409 a1、2012/0192300 a1、2013/0045492 a1、2013/0185821 a1、2013/0302836 a1、2018/0125043;国际专利申请公开号wo 2011/097603、wo 2012/148873、wo 2013/134263、wo 2013/184761、wo 2014/160179、wo 2014/160202;和wo2019/113065,每个专利据此以全文引用的方式并入。
[0191]
在下面的章节中详细地描述本发明的各个方面。章节的使用并不意味着限于本文所述的实施方案。每个章节可以应用于本文所述的任何方面或实施方案。在本技术中,除非另有说明,"或"的使用意指"和/或"。
[0192]
vdj重组
[0193]
负责免疫球蛋白合成的基因存在于动物的所有细胞中,并排列在沿染色体顺序排列的基因区段中。可以继承的人基因区段的构型(例如,人基因区段的种系构型,例如人种系基因组(例如,传给下一代的基因组)中人基因区段的顺序可以在以下文献中找到:lefranc,m.
‑
p.,exp.clin.immunogenet.,18,100
‑
116(2001)(以全文引用的方式并入本文),其还显示了在人免疫球蛋白重链基因座内以种系构型存在的功能性基因区段和假基
因。涉及几种遗传组分的一系列重组事件作用于从基因区段(例如v、d和j)的有序排列装配免疫球蛋白。已知基因区段的这种装配是不精确的,并且因此,通过组合不同基因区段和经由不精确连接形成独特连接两者实现免疫球蛋白多样性。通过称为体细胞超突变的过程生成进一步的多样性,其中改变所述免疫球蛋白的可变区序列,以增加对于抗原的亲和力和特异性。免疫球蛋白分子是由两个相同的重链和两个相同的轻链(其每一个具有两个结构组分:一个可变结构域和一个恒定结构域)构成的y形多肽。它是由基因区段装配形成的重链和轻链的可变结构域,而恒定结构域通过rna剪接与可变结构域融合。尽管装配(或连接)基因区段的机制对于重链和轻链是相似的,但轻链只需要一个连接事件(即v与j),而重链需要两个连接事件(即d与j和v与dj)。
[0194]
重链和轻链可变区的基因区段的组装(分别称为vdj重组和vj重组)由位于每个基因区段侧翼的保守非编码dna序列(称为重组信号序列(rss))指导,所述保守非编码dna序列确保相对于v、d和j编码序列在精确的位置进行dna重排(参见例如,ramsden,d.a.等人,1994,nuc.acids res.22(10):1785
‑
96;以全文引用的方式并入本文)。如技术人员所理解的,涉及重链基因区段的vdj重组的序列的代表性示意图如图1中所示。每个rss均由与编码序列(例如v、d或j区段)邻接的七个核苷酸的保守嵌段(七聚体)、随后是间隔子(12bp或23bp)和九个核苷酸的第二保守嵌段(九聚体)组成。尽管个体之间在12bp或23bp间隔子中存在相当大的序列差异,但这些序列的长度通常不会改变。免疫球蛋白基因区段之间的重组遵循通常称为12/23规则的规则,其中侧翼为带有12bp间隔子(或12聚体)的rss的基因区段通常与侧翼为23bp间隔子(或23聚体;参见例如,hiom,k.和m.gellert,1998,mol.cell.1(7):1011
‑
9;以全文引用的方式并入本文)的基因区段连接。已经报道了rss的序列影响与特定基因区段的重组的效率和/或频率(参见例如,ramsden,d.a和g.e.wu,1991,proc.natl.acad.sci.u.s.a.88:10721
‑
5;boubnov,n.v.等人,1995,nuc.acids res.23:1060
‑
7;ezekiel,u.r.等人,1995,immunity 2:381
‑
9;sadofsky,m.等人,1995,genes dev.9:2193
‑
9;cuomo,c.a.等人,1996,mol.cell biol.16:5683
‑
90;ramsden,d.a.等人,1996,embo j 15:3197
‑
3206;每篇文献以全文引用的方式并入本文)。确实,许多报告指出个体之间的基因区段(特别是d
h
区段)的使用有高度偏倚和可变的使用。除非另有说明或者除非其对本领域普通技术人员而言显而易见的是将出现矛盾或不一致,否则推测不参考rss的未重排的基因区段包含两个与基因区段自然地关联(例如位于其侧翼、与其有效地连接等)的rss。在一些实施方案中,本文中未重排的基因区段可以包含处于其种系(例如,野生型)构型中的基因区段,例如,各自在两侧均侧接有23聚体rss的种系v
h
基因区段和种系j
h
基因区段。相比之下,种系d
h
基因区段(例如,未重排的d
h
基因区段)在每一侧分别侧接有12聚体rss。
[0195]
这样,未重排的基因区段也可以是指处于其种系构型中的基因区段,包括与这种种系构型关联的任何rss。此外,处于其种系构型中的多个基因区段通常不仅是指每个单独的基因区段处于其种系(例如,未重排的)构型中,而且还是指功能性基因区段的顺序和/或位置。关于人v、d和j基因区段的种系构型,参见例如,lefranc,m.
‑
p.,exp.clin.immunogenet.,18,100
‑
116(2001);以全文引用的方式并入本文。
[0196]
形成重链和轻链可变区的基因区段的组装导致免疫球蛋白的抗原结合区(或位点)的形成。这样的抗原结合区部分特征在于高变区的存在,所述高变区通常被称为互补决
定区(cdr)。对于重链和轻链两者存在三个cdr(即总共六个cdr),其中cdr1和cdr2两者完全由v基因区段编码。然而,cdr3由来源于对于轻链的v和j区段,以及对于重链的v、d和j区段连接的序列编码。因此,在重组期间采用的另外的基因区段以形成重链可变区编码序列显著增加了重链的抗原结合位点的多样性。因此,所提供的含有如本文所述的工程化d
h
区的非人动物产生以d
h
与d
h
重组为特征的cdr3多样性,并且如与由传统vdj重组产生的重链可变区的cdr3区相比具有增加的氨基酸长度。
[0197]
不受理论的束缚,认为通过增加形成重排的重链可变区基因序列的连接的数量和/或增加cdr3区的长度,有可能实现在重链cdr3库中的进一步多样性。增加连接的数量和/或增加cdr3区的长度的一种机制可以是通过甚至在随后的d
h
‑
j
h
和v
‑
d
h
j
h
重组事件之前的d
h
‑
d
h
重组事件中将第一d
h
区段(其通常可以被称为d
h“a”)与另一个d
h
区段(通常可以被称为d
h”b”)连接,从而导致v
h
(d
h
a
‑
d
h
b)j
h
基因序列。在自然界中,长期以来认为d
h
‑
d
h
重组事件被12/23规则所禁止(alt,f.w.等人,1984,embo j.3(6):1209
‑
19;以全文引用的方式并入本文)。然而,似乎在违背12/23法则的情况下d
h
‑
d
h
‑
重组事件确实以极低的频率发生在人类中(800个中有1个或约0.125%的原代b细胞;参见例如,ollier,p.j.等人1985,embo j.4(13b):3681
‑
88;milner,e.c.b.等人1986,immunol.today 7:36
‑
40;liu,z.等人,1987,nucleic acids res.15(11):4688;liu,z.等人,1987,nucleic acids res.15(15):6296;meek,k.d.等人,1989,j.exp.med.169(2):519
‑
33;meek,k.d.等人,1989,j.exp.med.170:39
‑
57;baskin,b.等人1998,clin.exp.immunol.112:44
‑
7;briney,b.s.等人,2012immunol.137:56
‑
64;每篇文献以全文引用的方式并入本文),并且被认为是产生在一些重链中观察到的异常长的cdr3的主要机制(janeway’s immunobiology.第9版kenneth murphy,casey weaver.第5章,2017;以全文引用的方式并入)。然而,一些潜在的治疗靶标(例如但不限于病毒、细胞表面受体、iv型跨膜蛋白如gpcr、离子通道)具有掩蔽或隐蔽的表位,这些表位是正常抗体无法接近的但可以被具有长的hcdr3序列的抗体识别。例如,在具有慢性病毒感染的患者中经常发现具有非常长的hcdr3的抗体,并且所述抗体在一些情况下具有广泛中和活性(例如,针对hiv
‑
1或流感的广泛中和抗体)。为了选择能够到达这些隐藏表位的抗体,增加具有非常长的hcdr3的重链的频率将是有用的。不希望受到理论的束缚,实现这一目标的一种方式是通过工程化d
h
区段以包含23聚体rss和/或增加d
h
基因区段与更长的j
h
6基因区段的重组的频率来增加重链v
h
(d
h
a
‑
d
h
b)j
h
重排的频率。在小鼠中,d
h
‑
j
h
连接被认为发生在两个有序步骤中:(1)将近端dq52区段(在人类中称为d
h7‑
27)与最近的j
h
区段(j
h
1或j
h
2)中的一个进行初次重排。然后,dq52上游的强大的μ0启动子使其余的j
h
区段(j
h
3和j
h
4)更容易被重组激活基因(rag)接近;(2)将远端d
h
区段重排与其余j
h
区段(j
h
3或j
h
4)中的一个进行二次重排。参见图1,顶图。这与在小鼠(j
h3‑
j
h
4)和人(j
h4‑
j
h
6)两者中观察到的下游j
h
区段的更频繁使用是一致的(nitschke等人2001j.immunol.166:2540
‑
52,以全文引用的方式并入本文)。不希望受理论的束缚,假设用具有5’23聚体rss和3’12聚体rss的合成的d
h
基因(例如,合成的d
h3‑
3区段)替代d
h7‑
27和j
h1‑
j
h
3(或j
h1‑
j
h
5)将导致高频率的v
h
(d
h
‑
d
h
)j
h
重组,并且可能通过三步骤机制发生:(1)23
‑
d
h
‑
12与j
h
4、j
h
5或j
h
6重排以产生23(d
h
)j
h
,(2)重排远端d
h
(d
h1‑
1至d
h1‑
26)与23(d
h
)j
h
重排以产生12(d
h
‑
d
h
)j
h
(v
h
与23(d
h
)j
h
的重排将被12/23规则所禁止),(3)v
h
与12(d
h
‑
d
h
)j
h
重排以产生编码免疫球蛋白重链可变结构域的vddj编码序列。参见例如,图1,底图。还假设分别用与5'端12聚体rss和3'端23聚
体rss有效地连接的那些基因区段替代d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段(它们是长的d
h
基因区段(包含编码可以形成被认为稳定长的hcdr3区的二硫键的两个半胱氨酸的超过31个核苷酸[参见例如wang等人2013cell 153:1379
‑
93,以全文引用的方式并入本文]))也将导致可能通过三步骤机制发生的高频率的v
h
(d
h
‑
d
h
)j
h
重组:(1)12:d
h
‑
12与j
h
4、j
h
5或j
h
6重排以产生12(d
h
)j
h
,(2)远端12:d
h2‑
2:23、12:d
h2‑
8:23、或12:d
h2‑
15
‑
23与12(d
h
)j
h
重排以产生12(d
h
‑
d
h
)j
h
,和(3)v
h
与12(d
h
‑
d
h
)j
h
重排以产生编码免疫球蛋白重链可变结构域的vddj编码序列。如本文所述,通过在与一个或多个d
h
区段紧邻的5’或3’侧翼位置处放置23聚体间隔子来构建工程化d
h
区,从而使在人源化免疫球蛋白重链可变区基因座中能够进行d
h
与d
h
的重组。
[0198]
在一些实施方案中,本文所述的非人动物包含与参考非人动物相比表现出不遵循12/23规则的vdj重组的免疫球蛋白重链可变区基因座。在一些实施方案中,本文所述的非人动物包含与野生型d
h
区段相比被修饰的在一个或多个d
h
区段附近或侧翼的一个或多个rss。在一些实施方案中,如本文所述的非人动物的免疫球蛋白重链可变区的一个或多个d
h
基因区段各自有效地连接至5’或3’23聚体rss,使得与参考非人动物相比在所述非人动物中d
h
‑
d
h
重组的频率增加。在一些实施方案中,重组效率和/或频率可以通过抗体序列群(例如,来自一个个体或一组个体;参见例如,arnaout,r.等人,2011,plos one6(8):e22365;glanville,j.等人,2011,proc.natl.acad.sci.u.s.a.108(50):20066
‑
71;每篇文献以全文引用的方式并入本文)中基因区段的使用频率来确定。因此,在一些实施方案中,本文所述的非人动物可以包含各自有效地连接至或侧翼为23聚体rss的一个或多个d
h
区段,使得与参考非人动物中的d
h
‑
d
h
重组相比d
h
‑
d
h
重组以增加的频率发生。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少3倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少4倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少5倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少10倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少20倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少30倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少40倍增加频率的d
h
‑
d
h
重组。在一些实施方案中,与在参考非人动物中的d
h
‑
d
h
重组相比,包含如本文所述的工程化d
h
区的啮齿动物表现出至少50倍增加频率的d
h
‑
d
h
重组。
[0199]
提供的体内系统
[0200]
本发明基于以下认识:特定抗原与低和/或不良的免疫原性相关,并且因此是基于抗体的治疗剂的不良靶标。实际上,许多疾病靶标(例如,病毒、通道蛋白)已被表征为难治的或不可治疗的。因此,本发明基于用于开发抗体和基于抗体的治疗剂的体内系统的创建,所述抗体和基于抗体的治疗剂克服了与已建立的药物发现技术和/或方法相关的缺陷。在一些实施方案中,本发明提供了一种体内系统,其特征在于存在免疫球蛋白基因座(特别是
人源化免疫球蛋白重链可变区基因座),所述免疫球蛋白基因座包括工程化d
h
区,其中一个或多个dh rss从12聚体
‑
d
h
‑
12聚体形式改变、修饰或工程化为12聚体
‑
d
h
‑
23聚体或23聚体
‑
d
h
‑
12聚体形式,从而使得与在参考体内系统中观察到的d
h
与d
h
重组相比能够以增加的频率进行d
h
与d
h
重组。本公开具体地证明了其基因组包含免疫球蛋白重链可变区的转基因啮齿动物的构建,所述免疫球蛋白重链可变区包括工程化d
h
区,所述工程化d
h
区包括各自与相对于一个或多个d
h
区段中的每一个而定位的23聚体rss有效地连接以允许d
h
‑
d
h
重组的频率增加的一个或多个d
h
区段。本文所述的方法可以适于实现任何数量的d
h
区段(例如,传统的或合成的),其各自有效地连接至5’或3’23聚体rss以产生如本文所述的工程化d
h
区。一旦整合到免疫球蛋白重链可变区中(即,置于与v
h
和j
h
基因区段和/或一个或多个恒定区的有效连接中),工程化d
h
区就提供了v
h
和j
h
基因区段与超过一个d
h
区段的重组,例如以产生以具有增加的多样性的重链(即长cdr3,例如其中至少95%的重链cdr3序列为至少14个氨基酸的长度)为特征的抗体以直接结合特定抗原。在一些实施方案中,此类重链可变区具有进入病毒、通道蛋白、gpcr等中的难以到达的表位的能力。
[0201]
不希望受任何特定理论的束缚,我们注意到本文提供的数据证明,在一些实施方案中,其基因组包含免疫球蛋白重链可变基因座的啮齿动物有效地产生通过v(dd)j重组产生的抗体,所述免疫球蛋白重链可变基因座包括以包含与5’23聚体rss有效地连接的d
h
区段为特征的工程化d
h
区。我们还注意到本文提供的数据证明,在一些实施方案中,其基因组包含免疫球蛋白重链可变基因座的啮齿动物有效地产生通过v(dd)j重组产生的抗体,所述免疫球蛋白重链可变基因座包括以包含各自与3’23聚体rss有效地连接的三个d
h
区段为特征的工程化d
h
区。本文还指出,j
h
6基因区段上游的一些或全部五个j
h
基因区段的缺失导致优先与j
h
6基因区段重组。值得注意的是,j
h
6基因区段包含63个核苷酸,例如比其他j
h
1、j
h
2、j
h
3、j
h
4和j
h
5基因区段(它们分别包含52个、53个、50个、40个和51个核苷酸)多了10个核苷酸。因此,本公开在至少一些实施方案中包括开发用于产生针对顽固性疾病靶标的抗体和/或基于抗体的治疗剂的体内系统,例如,通过提供产生重排的免疫球蛋白重链可变区基因序列(例如v
h
d
h
j
h
和v
h
(d
h
a
‑
d
h
b)j
h
,例如v
h
(d
h
a
‑
d
h
b)j
h
6)、编码cdr3长度为至少20个氨基酸(例如cdr3长度在20
‑
30个氨基酸长度之间)的重链可变结构域的序列的啮齿动物。在一些实施方案中,至少8
‑
10%的重排的免疫球蛋白重链可变区基因序列,例如本文所述的非人动物的v
h
d
h
j
h
和v
h
(d
h
a
‑
d
h
b)j
h
基因序列编码长度为至少21个氨基酸的cdr3区。
[0202]
在一些实施方案中,本文描述的是非人动物(例如啮齿动物,例如大鼠或小鼠),其包含(1)在其种系基因组中(例如在生殖细胞中)的包含含有与23聚体rss有效地连接的d
h
基因区段的工程化d
h
区的免疫球蛋白重链基因座,以及(2)在其体细胞基因组中(例如在b细胞中)的重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,其中第一或第二d
h
基因区段(即,分别为v
h
(d
h
a
‑
d
h
b)j
h
编码序列的d
h
a或d
h
b)包含有效地连接至23聚体rss或其一部分的d
h
基因区段,例如,其中第一或第二d
h
基因区段具有与有效地连接至23聚体rss的d
h
基因区段对齐的至少9个连续核苷酸,并且其中所述第一和第二d
h
基因区段中的每一个均包含与对应种系d
h
基因区段对齐(无论是否有重叠)的至少5个连续核苷酸。
[0203]
在一些实施方案中,所提供的非人动物包含免疫球蛋白重链基因座,其特征在于存在以种系型构排列并有效地连接至非人免疫球蛋白重链恒定区基因、增强子和调节区的多个人v
h
、d
h
和j
h
的基因区段。在一些实施方案中,所提供的非人动物包含与非人免疫球蛋
白重链恒定区有效地连接的一个或多个人v
h
基因区段、一个或多个人d
h
基因区段和一个或多个人j
h
基因区段。
[0204]
在一些实施方案中,所提供的非人动物包含至少人v
h
基因区段v
h3‑
74、v
h3‑
73、v
h3‑
72、v
h2‑
70、v
h1‑
69、v
h3‑
66、v
h3‑
64、v
h4‑
61、v
h4‑
59、v
h1‑
58、v
h3‑
53、v
h5‑
51、v
h3‑
49、v
h3‑
48、v
h1‑
46、v
h1‑
45、v
h3‑
43、v
h4‑
39、v
h4‑
34、v
h3‑
33、v
h4‑
31、v
h3‑
30、v
h4‑
28、v
h2‑
26、v
h1‑
24、v
h3‑
23、v
h3‑
21、v
h3‑
20、v
h1‑
18、v
h3‑
15、v
h3‑
13、v
h3‑
11、v
h3‑
9、v
h1‑
8、v
h3‑
7、v
h2‑
5、v
h7‑4‑
1、v
h4‑
4、v
h1‑
3、v
h1‑
2和v
h6‑
1。
[0205]
在一些实施方案中,所提供的非人动物包含人d
h
基因区段d
h1‑
1、d
h2‑
2、d
h3‑
3、d
h4‑
4、d
h5‑
5、d
h6‑
6、d
h1‑
7、d
h2‑
8、d
h3‑
9、d
h3‑
10、d
h5‑
12、d
h6‑
13、d
h2‑
15、d
h3‑
16、d
h4‑
17、d
h5‑
18、d
h6‑
19、d
h1‑
20、d
h2‑
21、d
h3‑
22、d
h6‑
25和d
h1‑
26。在一些实施方案中,所提供的非人动物还包含d
h1‑
14、d
h4‑
11、d
h4‑
23、d
h5‑
24或其组合。在一些实施方案中,所提供的非人动物还包含人d
h7‑
27。
[0206]
在一些实施方案中,本文描述的是非人动物(例如啮齿动物,例如大鼠或小鼠),其包含(1)在其种系基因组中(例如在生殖细胞中)的包含含有与23聚体rss有效地连接的d
h
基因区段的工程化d
h
区的免疫球蛋白重链基因座,以及(2)在其体细胞基因组中(例如在b细胞中)的重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,其中第一或第二d
h
基因区段(即,分别为v
h
(d
h
a
‑
d
h
b)j
h
编码序列的d
h
a或d
h
b)包含有效地连接至23聚体rss或其一部分的d
h
基因区段,例如,其中第一或第二d
h
基因区段具有与有效地连接至23聚体rss的d
h
基因区段对齐的至少9个连续核苷酸,并且其中所述第一和第二d
h
基因区段中的每一个均包含与对应种系d
h
基因区段对齐(无论是否有重叠)的至少5个连续核苷酸。在一些实施方案中,所提供的非人动物包含有效地连接至23聚体rss的人d
h
基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含两个半胱氨酸密码子。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少37个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少19个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少20个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少23个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少28个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少31个核苷酸。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含至少37个核苷酸。
[0207]
在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
1基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
2基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
3基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
4基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
5基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
6基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h
7基因区段。
[0208]
在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h1‑
1基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h2‑
2基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h3‑
3基因区段。在一些实
施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h4‑
4基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h5‑
5基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h6‑
6基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h1‑
7基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h2‑
8基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h3‑
9基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h3‑
10基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h5‑
12基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h6‑
13基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h2‑
15基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h3‑
16基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h4‑
17基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h5‑
18基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h6‑
19基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h1‑
20基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h2‑
21基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h3‑
22基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h6‑
25基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h1‑
26基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h1‑
14基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h4‑
11基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h4‑
23基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h5‑
24基因区段。在一些实施方案中,有效地连接至23聚体rss的人d
h
基因区段包含人d
h7‑
27基因区段。
[0209]
在一些实施方案中,所提供的非人动物包含通常以在未重排的人基因组可变基因座中发现的顺序排列的人d
h
基因区段的全部或基本上全部库,其中将所述全部或基本上全部库的所述人d
h
基因区段中的一个用工程化为有效地连接至23聚体rss的d
h
基因区段替换。在一些实施方案中,将所述全部或基本上全部库的所述人d
h
基因区段中的一个用工程化为有效地连接至23聚体rss的对应d
h
基因区段替换,例如将野生型d
h2‑
2基因区段用工程化为有效地连接至23聚体rss的d
h2‑
2基因区段替换。在一些实施方案中,将所述全部或基本上全部库的所述人d
h
基因区段中的一个用工程化为有效地连接至23聚体rss的另一个d
h
基因区段替换,例如将野生型d
h7‑
27基因区段用工程化为有效地连接至23聚体rss的d
h3‑
3基因区段替换。在一些实施方案中,将通常以在未重排的人基因组可变基因座中发现的顺序排列的人d
h
基因区段的全部或基本上全部库的d
h1‑
1基因区段用工程化为有效地连接至23聚体rss(例如3’23聚体rss)的对应或另一个d
h
基因区段替换。在一些实施方案中,将通常以在未重排的人基因组可变基因座中发现的顺序排列的人d
h
基因区段的全部或基本上全部库的d
h1‑
1、d
h2‑
2、d
h2‑
8、d
h2‑
15、d
h2‑
21基因区段用工程化为有效地连接至23聚体rss(例如3’23聚体rss)的对应或另一个d
h
基因区段替换。在一些实施方案中,将通常以在未重排的人基因组可变基因座中发现的顺序排列的人d
h
基因区段的全部或基本上全部库的d
h2‑
2、d
h2‑
8、和d
h2‑
15基因区段中的每一个用工程化为有效地连接至23聚体rss(例如3’23聚体
rss)的对应或另一个d
h
基因区段替换。
[0210]
在一些实施方案中,所提供的非人动物包含至少人j
h
基因区段j
h
6。在一些实施方案中,所提供的非人动物包含至少人j
h
基因区段j
h
4、j
h
5和j
h
6。在一些实施方案中,所提供的非人动物包含人j
h
基因区段j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6。
[0211]
在一些实施方案中,非人免疫球蛋白重链恒定区包括一个或多个非人免疫球蛋白重链恒定区基因,例如免疫球蛋白m(igm)、免疫球蛋白d(igd)、免疫球蛋白g(igg)、免疫球蛋白e(ige)和免疫球蛋白a(iga)。在一些实施方案中,非人免疫球蛋白重链恒定区包括啮齿动物igm、啮齿动物igd、啮齿动物igg3、啮齿动物igg1、啮齿动物igg2b、啮齿动物igg2a、啮齿动物ige和啮齿动物iga恒定区基因。在一些实施方案中,所述人v
h
、d
h
和j
h
基因区段有效地连接至一个或多个非人免疫球蛋白重链增强子(即,增强子序列或增强子区)。在一些实施方案中,所述人v
h
、d
h
和j
h
基因区段有效地连接至一个或多个非人免疫球蛋白重链调节区(或调控序列)。在一些实施方案中,所述人v
h
、d
h
和j
h
基因区段有效地连接至一个或多个非人免疫球蛋白重链增强子(或增强子序列)和一个或多个非人免疫球蛋白重链调节区(或调控序列)。
[0212]
在一些实施方案中,所提供的非人动物不含有(或缺乏)内源性adam6基因。在一些实施方案中,所提供的非人动物不含有或缺乏在相同物种的野生型非人动物的种系基因组中存在的相同种系基因组位置中的内源性adam6基因(或adam6编码序列)。在一些实施方案中,所提供的非人动物不含有或缺乏人adam6假基因。在一些实施方案中,所提供的非人动物包含编码一种或多种非人(例如,啮齿动物)adam6多肽的至少一个核苷酸序列的插入。所述插入可以在如本文所述的经工程化免疫球蛋白重链基因座的外部(例如,v
h
基因区段的5’最末端的上游)、在工程化免疫球蛋白重链基因座内或者非人动物(例如,随机引入的非人adam6编码序列)、细胞或组织的种系基因组中。在一些实施方案中,所提供的非人动物不含有或缺乏功能性内源性adam6假基因。
[0213]
在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不可检测地表达抗体分子中的全部或部分内源性非人v
h
区。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不含有编码抗体分子中的全部或部分内源性非人v
h
区(例如,v
h
、d
h
和/或j
h
)的一个或多个核苷酸序列(或缺乏它们或含有它们的缺失)。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织具有包括全部或部分内源性非人v
h
、d
h
和j
h
基因区段的缺失的种系基因组。在一些实施方案中,所提供的非人动物是可育的。
[0214]
在一些实施方案中,所提供的非人动物还包含工程化免疫球蛋白轻链基因座,所述工程化免疫球蛋白轻链基因座的特征在于存在排列成种系构型并且插入非人c基因的上游以及与之有效地连接的多个人v和j基因区段。
[0215]
在一些实施方案中,工程化免疫球蛋白轻链基因座包含出现在人免疫球蛋白轻链基因座的近端可变簇(或近端臂或近端重复)中的至少人v基因区段。在一些实施方案中,工程化免疫球蛋白轻链基因座包含至少人v基因区段v 2
‑
40、v1
‑
39、v1
‑
33、v2
‑
30、v2
‑
8、v1
‑
27、v2
‑
24、v6
‑
21、v3
‑
20、v1
‑
17、v 1
‑
16、v3
‑
15、v1
‑
12、v 3
‑
11、v1
‑
9、v1
‑
8、v1
‑
6、v1
‑
5、v5
‑
2和v4
‑
1。在一些实施方案中,工程化免疫球蛋白轻链基因座包含至少1个、2个、3个、4个、5个、10个或15个人v基因区段,所述人v基因区段选自v2
‑
40、v1
‑
39、v1
‑
33、v2
‑
30、v2
‑
8、v1
‑
27、v2
‑
24、v6
‑
21、v3
‑
20、v1
‑
17、v1
‑
16、v3
‑
15、v1
‑
12、v3
‑
11、v1
‑
9、v1
‑
8、v1
‑
6、v1
‑
5、v 5
‑
2和v 4
‑
1。在一些实施方案中,工程化免疫球蛋白轻链基因座包含人j基因区段j1、j 2、j3、j4和j5。在一些实施方案中,工程化免疫球蛋白轻链基因座包含至少1个、2个、3个、或4个人j基因区段,所述人j基因区段选自j1、j 2、j3、j 4和j 5。
[0216]
在许多实施方案中,所述人类v和j基因区段有效地连接至一个或多个非人免疫球蛋白轻链增强子(即,增强子序列或增强子区)。在一些实施方案中,所述人v和j基因区段有效地连接至鼠ig轻链内含子增强子区(ig ei或ei)。在许多实施方案中,所述人v和j基因区段有效地连接至一个或多个非人免疫球蛋白轻链调节区(或调控序列)。在一些实施方案中,所述人v和j基因区段有效地连接至鼠ig轻链3’增强子区(ig
[0217]3’
e或3’e)。在一些实施方案中,所述人v和j基因区段有效地连接至鼠ei,并且有效地连接至鼠3’e。在一些实施方案中,所述人v和j基因区段有效地连接至一个或多个非人免疫球蛋白轻链增强子(或增强子序列或增强子区)和一个或多个非人免疫球蛋白轻链调节区(或调控序列)。在一些实施方案中,工程化免疫球蛋白轻链基因座含有与野生型免疫球蛋白轻链基因座中出现的相同的非人免疫球蛋白轻链增强子区(或增强子序列)。在一些实施方案中,工程化免疫球蛋白轻链基因座含有出现在不同物种(例如,不同的啮齿动物物种)的野生型免疫球蛋白轻链基因座中的非人ig轻链增强子区(或增强子序列)。
[0218]
在一些实施方案中,如本文所述的工程化免疫球蛋白轻链基因座不含有(即,缺乏)人vpreb基因(或人vpreb基因编码序列)。
[0219]
在一些实施方案中,工程化免疫球蛋白轻链基因座的非人c基因包括啮齿动物c基因,例如小鼠c基因或大鼠c基因。在一些实施方案中,工程化免疫球蛋白轻链基因座的非人c基因是或包含来自包括129品系、balb/c品系、c57bl/6品系、混合129xc57bl/6品系或它们的组合的遗传背景的小鼠c 基因。
[0220]
在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不可检测地表达抗体分子中的全部或部分内源性非人v区。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不含有编码抗体分子中的全部或部分内源性非人v区的一个或多个核苷酸序列(或缺乏它们或含有它们的缺失)。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织具有包括全部或部分内源性非人v和j基因区段的缺失的种系基因组。
[0221]
在一些实施方案中,所提供的非人动物还包含野生型或灭活的(例如通过基因靶向)免疫球蛋白轻链基因座。
[0222]
在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不可检测地表达抗体分子中的全部或部分内源性非人v区。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织不含有编码抗体分子中的全部或部分内源性非人v区的一个或多个核苷酸序列(或缺乏它们或含有它们的缺失)。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织具有包括全部或部分内源性非人v和j基因区段的缺失的种系基因组。在一些实施方案中,如本文所述的所提供的非人动物、非人细胞或非人组织具有包括全部或部分内源性非人v、j和c基因区段的缺失的种系基因组。
[0223]
可以在美国专利号8,642,835、8,697,940、9,006,511、9,012,717、9,029,628、9,035,128、9,066,502、9,150,662和9,163,092(将其以全文引用的方式并入本文)中找到创
建具有此类工程化免疫球蛋白基因座的靶向载体、非人细胞和动物的指南。本领域的技术人员知道本领域已知的用于实现非人类(如,哺乳动物)基因组的这种基因工程和/或操纵或者用于制备、提供或制造引入非人类动物的种系基因组的此类序列的许多技术。
[0224]
dna构建体
[0225]
通常,将含有如本文所述的免疫球蛋白基因区段(特别是各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段)的多核苷酸分子插入载体(优选地dna载体)中,以便在合适的宿主细胞中复制所述多核苷酸分子。
[0226]
由于其大小,d
h
区段可以直接从获得自商业供应商处的基因组来源克隆而来,或者基于可获得自genbank的公开序列通过计算机设计而来。可替代地,细菌人工染色体(bac)文库可以提供免疫球蛋白序列。bac文库含有100
‑
150kb的平均插入片段大小,并且能够携带高达300kb的插入片段(shizuya等人,1992,proc.natl.acad.sci.,usa 89:8794
‑
8797;swiatek等人,1993,genes and development 7:2071
‑
2084;kim等人,1996,genomics 34 213
‑
218;以引用的方式并入本文)。例如,已构建人和小鼠基因组bac文库,并且这些文库可商购获得(例如,invitrogen,carlsbad calif.)。基因组bac文库也可以作为免疫球蛋白序列以及转录控制区的来源。
[0227]
可替代地,可以从酵母人工染色体(yac)分离、克隆和/或转移免疫球蛋白序列。整个免疫球蛋白基因座或其实质部分可以被克隆并包含在一个或几个yac中。如果使用多个yac并且它们含有重叠同源性区域,则它们可以在酵母宿主菌株内重组以产生代表整个基因座的单一构建体。yac臂可以用哺乳动物选择盒进一步修饰,所述修饰通过改造以帮助通过本领域已知的和/或本文所述的方法将构建体引入胚胎干细胞或胚胎中来进行。
[0228]
dna构建体可以使用本领域已知的方法制备。例如,dna构建体可以制备为较大质粒的一部分。这种制备允许以本领域已知的有效方式克隆和选择正确的构建体。含有各自有效地连接至如本文所述的5’或3’23聚体rss的一个或多个d
h
区段的dna片段可以定位于质粒上的简便限制性位点之间,使得它们可易于从其余的质粒序列分离,以掺入所需的动物。
[0229]
在一些实施方案中,用于制备质粒和转化宿主生物体的方法是本领域已知的。关于适用于原核细胞与真核细胞的其它表达系统,以及通用重组程序,参见分子克隆:a laboratory manual,第2版,sambrook,j.等人编,cold spring harbor laboratory press:1989;以全文引用的方式并入本文。
[0230]
非人类动物的产生
[0231]
提供了非人动物,所述非人动物表达具有以由于与允许非人动物基因组中免疫球蛋白重链可变区内的d
h
与d
h
重组的一个或多个d
h
区段紧邻的23聚体rss的整合而产生的长的氨基酸长度为特征的重链cdr3多样性的抗体。本文描述的合适的实例包括啮齿类动物,具体地讲,小鼠。在许多实施方案中,一个或多个d
h
区段包括异源性d
h
区段(例如人d
h
区段)。还提供了用于制备含有与野生型或参考非人动物相比能够以增加的频率进行d
h
‑
d
h
重组的所述d
h
区段的非人动物、非人胚胎以及细胞的非人动物、胚胎、细胞和靶向构建体。
[0232]
在一些实施方案中,一个或多个d
h
区段被修饰为与非人动物基因组中的免疫球蛋白重链可变区的多样性簇(即d
h
区)内的5’或3’23聚体rss邻近(或与之有效地连接)。在一些实施方案中,免疫球蛋白重链可变区的d
h
区(或其部分)没有缺失(即完整)。在一些实施
方案中,免疫球蛋白重链可变区的d
h
区(或其部分)被改变、破坏、缺失、工程化或被各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段替换。在一些实施方案中,全部或基本上全部的d
h
区被各自有效地连接至5’或3’23聚体rss的一个或多个合成的d
h
区段替换;在一些实施方案中,在免疫球蛋白重链可变区的d
h
区中一个或多个传统的d
h
基因区段未被缺失或替换。在一些实施方案中,d
h
区含有传统的d
h
区段(即各自有效地连接至5’12聚体rss和3’12聚体rss的一个或多个d
h
区段)和工程化d
h
基因区段(即各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段)。在一些实施方案中,如本文所述的d
h
区是合成的d
h
区。在一些实施方案中,d
h
区是人d
h
区。在一些实施方案中,d
h
区是鼠d
h
区。在一些实施方案中,将如本文所述的工程化d
h
区(或其部分)插入免疫球蛋白重链可变区,使得所述工程化d
h
区(或其部分)与一个或多个v
h
基因区段和/或一个或多个j
h
基因区段有效地连接。在一些实施方案中,将所述工程化d
h
区插入免疫球蛋白重链可变区的两个拷贝之一中,从而产生相对于所述工程化d
h
区杂合的非人动物。在一些实施方案中,提供了对于工程化d
h
区纯合的非人动物。在一些实施方案中,提供了对于工程化d
h
区杂合的非人动物。
[0233]
在一些实施方案中,如本文所述的非人动物在其基因组内含有随机整合的人免疫球蛋白重链可变区,所述人免疫球蛋白重链可变区包括含有各自与5’或3’23聚体rss有效地连接的一个或多个d
h
区段的d
h
区。因此,此类非人动物可以被描述为具有包含工程化d
h
区的人免疫球蛋白重链转基因。可以使用多种方法检测工程化d
h
区,所述方法包括例如pcr、western印迹、southern印迹、限制性片段长度多态性(rflp)或等位基因获得(goa)或等位基因缺失(loa)测定。在一些此类实施方案中,如本文所述的非人动物相对于如本文所述的工程化d
h
区是杂合的。在一些此类实施方案中,如本文所述的非人动物相对于如本文所述的工程化d
h
区是纯合的。在一些此类实施方案中,如本文所述的非人动物相对于如本文所述的工程化d
h
区是半合子的。在一些此类实施方案中,如本文所述的非人动物含有如本文所述的工程化d
h
区的一个或多个拷贝。
[0234]
在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括与5’23聚体rss关联(或与之有效地连接)的至少一个d
h
区段。在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括与3’23聚体rss关联(或与之有效地连接)的至少一个d
h
区段。在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括与5’23聚体rss关联(或与之有效地连接)的至少一个人d
h3‑
3区段。在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括至少一个与3’23聚体rss关联(或与之有效地连接)的人d
h
2区段,其中所述人d
h
2区段选自由以下项组成的组:人d
h2‑
2、人d
h2‑
8、人d
h2‑
15和人d
h2‑
21。
[0235]
在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括各自与5’23聚体rss关联(或与之有效地连接)的超过一个d
h
区段。在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括各自与3’23聚体rss关联(或与之有效地连接)的超过一个d
h
区段。在一些实施方案中,如本文所述的非人动物的工程化d
h
区包括各自与3’23聚体rss关联(或与之有效地连接)的人d
h2‑
2、人d
h2‑
8和人d
h2‑
15区段。
[0236]
提供了用于制备其基因组包含包括工程化d
h
区的免疫球蛋白重链可变区的非人动物的组合物和方法,其中所述工程化d
h
区包括各自与5’或3’23聚体rss关联(或与之有效地连接)的一个或多个d
h
区段,包括用于制备表达包含重链可变区的抗体的非人动物的组合物和方法,所述重链可变区包括具有由含有与一个或多个非人重链恒定区基因有效地连
接的人v
h
和j
h
基因区段的免疫球蛋白重链基因座中的超过一个d
h
区段编码的氨基酸序列的cdr3区。在一些实施方案中,还提供了用于制备在一个或多个内源性增强子和/或一个或多个内源性调控序列的控制下表达此类抗体的非人类动物的组合物和方法。在一些实施方案中,还提供了用于制备在一个或多个异源性增强子和/或一个或多个异源性调控序列的控制下表达此类抗体的非人类动物的组合物和方法。方法包括将允许与野生型d
h
区段相比以增加的频率进行d
h
‑
d
h
重组的一个或多个d
h
区段和其他序列插入非人动物基因组中,使得表达包括由v(dd)j重组产生的免疫球蛋白重链的抗体。
[0237]
在一些实施方案中,方法包括插入dna,所述dna包括具有与一个或多个j
h
基因区段有效地连接的5’23聚体rss和3’12聚体rss的d
h
基因区段。如本文所述,d
h
基因区段被定位于0启动子序列的下游。在一些实施方案中,方法包括在相对于0启动子序列的位置中插入具有5’23聚体rss和3’12聚体rss的d
h
区段,使得在重组期间rag基因(例如,rag
‑
1和/或rag
‑
2)可接近所述j
h
基因区段。可以将包括上述d
h
区段和侧翼rss的遗传物质插入非人动物的基因组中,从而创建具有包含所述d
h
区段和必要的rss以允许与紧邻的d
h
基因区段以及v
h
和j
h
基因区段进行重组的工程化d
h
区的非人动物。
[0238]
在一些实施方案中,方法包括插入dna,所述dna包括各自与有效地连接至六个j
h
基因区段的5’12聚体rss和3’23聚体rss关联的d
h
基因区段。如本文所述,d
h
基因区段被定位于各自与5’和3’12聚体rss关联的多个d
h
基因区段之中。在一些实施方案中,方法包括将各自与5’12聚体rss和3’23聚体rss关联的d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段插入具有各自与传统的或野生型rss关联的多个其他dh基因区段的多样性簇中。可以将包括上述d
h
基因区段和侧翼rss的遗传物质插入非人动物的基因组中,从而创建具有包含所述d
h
区段和必要的rss以允许与紧邻的d
h
基因区段以及v
h
和j
h
基因区段进行重组的工程化d
h
区的非人动物。
[0239]
在适当的情况下,可以修饰对应于(或编码)d
h
区段的序列以包括针对在非人动物中表达而优化的密码子(例如参见,美国专利号5,670,356和5,874,304;每个专利以全文引用的方式并入)。密码子优化的序列是合成序列,并且优选编码由非密码子优化的亲本多核苷酸编码的相同多肽(或具有与全长多肽基本上相同的活性的全长多肽的生物活性片段)。在一些实施方案中,对应于(或编码)d
h
区段的序列可以包括改变的序列以优化针对特定细胞类型(例如,啮齿动物细胞)的密码子使用。例如,可以优化与待插入非人动物(例如啮齿动物)基因组中的d
h
区段对应的序列的密码子,以在非人动物的细胞中表达。此序列可描述为密码子优化的序列。
[0240]
将与5’或3’23聚体rss有效地连接的d
h
区段插入d
h
区使得所述d
h
区段与v
h
和j
h
基因区段(例如,多个v
h
和j
h
基因区段)有效地连接采用相对最小的基因组修饰,并导致包含以具有更长的氨基酸长度的cdr3为特征的重链的抗体的表达。
[0241]
用于产生转基因非人动物的方法,包括敲除和敲入,是本领域熟知的(参见例如gene targeting:a practical approach,joyner编,oxford university press,inc.(2000);以全文引用的方式并入本文)。例如,转基因啮齿动物的产生可以任选地涉及一个或多个内源性啮齿动物基因(或基因区段)的遗传基因座的断裂以及将各自有效地连接至23聚体rss的一个或多个d
h
区段引入啮齿动物基因组中,在一些实施方案中,与内源性啮齿动物基因(或基因区段)相同的位置处。在一些实施方案中,将各自有效地连接至23聚体rss的一个或多个d
h
区段引入在啮齿动物基因组中随机插入的免疫球蛋白重链基因座的d
h
区
中。在一些实施方案中,将各自有效地连接至23聚体rss的一个或多个d
h
区段引入啮齿动物基因组中的内源性免疫球蛋白重链基因座的d
h
区中;在一些实施方案中,内源性免疫球蛋白重链基因座被改变、修饰或工程化以包含有效地连接至一个或多个恒定区基因(例如人或鼠)的人基因区段(例如v和/或j)。
[0242]
图2中提供了用于构建工程化d
h
区并整合到啮齿动物胚胎干(es)细胞中以创建其基因组包含包括工程化多样性簇(即d
h
区)的免疫球蛋白重链可变区的啮齿动物的代表性靶向载体的示意性图示(未按比例绘制),所述多样性簇包括各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段。图3
‑
8中提供了将此类载体插入啮齿动物es细胞基因组中的免疫球蛋白重链可变区中的示例性策略和方法。在图2
‑
8的每一个图中,所示的noti限制性酶识别位点是适当的,针对所显示的各种等位基因(未按比例)显示了不同引物/探针集(参见表4)的名称和大致位置(小破折号),并且除非另有说明,否则空心符号和线条代表人序列,而实心符号和深色线代表小鼠序列。每个附图均使用以下缩写:spec:壮观霉素抗性基因;neo:新霉素抗性基因;hyg:潮霉素抗性基因;lp:loxp位点特异性重组识别位点;ei:鼠重链内含子增强子;igm:鼠免疫球蛋白m恒定区基因;l:loxp位点序列;frt:翻转酶识别靶序列;0pro::0启动子序列。
[0243]
如图2所示,含有多个d
h
区段(其中一个d
h
区段有效地连接至5’23聚体rss(图2,顶图和中间图)或者三个d
h
区段各自有效地连接至3’23聚体rss(图2,底图))的dna片段使用velocigene技术(参见例如,美国专利号6,586,251和valenzuela等人,2003,nature biotech.21(6):652
‑
659;以全文引用的方式并入本文)。)和本领域已知的分子生物学技术来制备。在图2中,除非另有说明,否则空心符号和线条代表人序列,而实心符号和深色线代表小鼠序列。描绘了人v
h6‑
1、d
h2‑
2、d
h2‑
8、d
h2‑
15、d
h3‑
3、以及j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段(如果存在)的不按比例的相对位置,并且任何未命名的基因区段都是d
h
基因区段。通常,如用#号标记描绘的d
h
区包含未重排的人d
h
基因区段的全部库(参见例如www.imgt.org/imgtrepertoire/index.php?section=locusgenes&repertoire=locus&species=human&group=igh;以全文引用的方式并入本文),但以下情况除外:顶部两个靶向载体缺乏最后的d
h7‑
27基因,其被包含侧翼为5'端23聚体rss和3'端12聚体rss(描绘为空心箭头)的d
h3‑
3基因区段的序列替换;底部的靶向载体缺乏未重排的人d
h2‑
2基因区段、未重排的人d
h2‑
8基因区段和d
h2‑
15基因区段,它们分别被侧翼为5'端12聚体rss和3'端23聚体rss的d
h2‑
2基因区段、侧翼为5'端12聚体rss和3'端23聚体rss的d
h2‑
8基因区段、和侧翼为5'端12聚体rss和3'端23聚体rss的d
h2‑
15基因区段(所述工程化d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段中的每一个如空心箭头所描绘)替换。未填充的垂直矩形代表与置于12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体中以可帮助确保正确修饰靶向载体/es细胞的序列引物和探针同源的独特人工40聚体的位置。表示为“1”、“2”、“10”、“16”、“8”和“18”的独特人工40聚体的序列分别如seq id no:73、seq id no:74、seq id no:75、seq id no:76、seq id no:77和seq id no:78所示。
[0244]
dna片段用同源臂组装,以精确靶向插入人源化免疫球蛋白重链可变区基因座中(图3、5、7)。将侧翼为位点特异性重组识别位点(例如loxp)的选择盒(例如新霉素)包含在靶向载体中以帮助筛选es细胞克隆中的正确插入,并且可以通过在阳性es细胞克隆中瞬时表达重组酶(例如cre)来去除(图4、6、8)。一旦整合到免疫球蛋白重链基因座中,dna片段就
包含用于适当组装(即重组)、转录和表达重链可变区的所需序列。设计靶向载体,使得工程化d
h
区的5’侧接有人v
h
基因组dna且3’侧接有人j
h
基因组dna和非人(例如啮齿动物)基因组重链恒定区dna(例如,内含子增强子和igm恒定区基因)。用于掺入非人细胞(例如,啮齿动物胚胎干细胞)基因组中的最终靶向载体含有v
h
基因组dna(例如,含有一个或多个v
h
基因区段、工程化d
h
区、3’j
h
基因组dna和非人(例如,啮齿动物)基因组重链恒定区dna,所有这些都有效地连接以允许在v
h
基因区段、工程化d
h
区和j
h
基因区段一旦整合到非人动物的基因组中就进行重组。一旦进行组装,靶向载体就被线性化并电穿孔到啮齿动物es细胞中。
[0245]
将靶向载体引入啮齿动物(例如小鼠)胚胎干细胞中,使得靶向载体中包含的序列(即工程化d
h
区)导致非人细胞或非人动物(例如小鼠)能够表达包含具有由超过一个d
h
区段编码的氨基酸的cdr3的抗体。
[0246]
如本文所述,产生转基因啮齿动物,其中已经将工程化d
h
区引入啮齿动物基因组的免疫球蛋白重链基因座(例如,工程化为含有人可变区基因区段的免疫球蛋白重链基因座,其可以是如此工程化的内源性免疫球蛋白重链基因座)中。
[0247]
包含人可变区基因区段的免疫球蛋白基因座是本领域已知的,并且可见于例如美国专利第5,633,425号;第5,770,429号;第5,814,318号;第6,075,181号;第6,114,598号;第6,150,584号;第6,998,514号;第7,795,494号;第7,910,798号;第8,232,449号;第8,502,018号;第8,697,940号;第8,703,485号;第8,754,287号;第8,791,323号;第8,809,051号;第8,907,157号;第9,035,128号;第9,145,588;9,206,263号;第9,447,177号;第9,551,124号;第9,580,491号和第9,475,559号;其中每个专利以全文引用的方式并入本文中;以及美国专利公布第20100146647号、第20110195454号、第20130167256号、第20130219535号、第20130326647号、第20130096287号和第2015/0113668号,其中每个公开以全文引用的方式并入本文中;以及pct公开第wo2007117410号、第wo2008151081号、第wo2009157771号、第wo2010039900号、第wo2011004192号、第wo2011123708号和第wo2014093908号,其中每个公开以全文引用的方式并入本文中。
[0248]
在一些实施方案中,如本文公开的非人动物包含能够在小鼠的前体b细胞中重排的、含有工程化d
h
区的外源性完全人免疫球蛋白转基因(alt等人,1985,immunoglobulin genes in transgenic mice,trends genet 1:231
‑
236;以全文引用的方式并入本文)。在这些实施方案中,可以(随机)插入包含工程化d
h
区的完全人免疫球蛋白转基因,并且也可以敲除内源性免疫球蛋白基因(green等人,1994,antigen
‑
specific human monoclonal antibodies from mice engineered with human ig heavy and light chain yacs,nat genet 7:13
‑
21;lonberg等人,1994,antigen
‑
specific human antibodies from mice comprising four distinct genetic modifications,nature 368:856
‑
859;jakobovits等人,2007,from xenomouse technology to panitumumab,the first fully human antibody product from transgenic mice,nat biotechnol 25:1134
‑
1143;每篇文献以全文引用的方式并入),例如,其中例如,通过靶向缺失每个内源性基因座的小而关键的部分,随后引入人免疫球蛋白基因的基因座作为随机整合的大转基因或微型染色体,使内源性免疫球蛋白重链和κ轻链基因座失活(tomizuka等人,2000,double trans
‑
chromosomic mice:maintenance of two individual human chromosome fragments containing ig heavy and kappa loci and expression of fully human antibodies,pnas usa 97:
722
‑
727;以全文引用的方式并入)。
[0249]
在一些实施方案中,包含工程化d
h
区的人或人源化免疫球蛋白重链和轻链基因座分别位于内源性免疫球蛋白重链和轻链基因座处。先前已经描述了用于用人种系免疫球蛋白可变基因基因座对小鼠种系免疫球蛋白可变基因基因座进行大量原位基因替换,同时保持小鼠产生子代的能力的方法。参见例如美国专利第6,596,541号和第8,697,940号,每个专利以全文引用的方式并入。具体地讲,描述了小鼠重链和κ轻链免疫球蛋白可变基因基因座的六兆碱基用其人对应部分精确替换,同时保持小鼠恒定区完整。因此,已经建立了整个种系免疫球蛋白可变谱经同等人种系免疫球蛋白可变序列精确替换,同时维持小鼠恒定区的小鼠。人可变区连接于小鼠恒定区,形成嵌合人
‑
小鼠免疫球蛋白基因座,所述基因座重排并以生理学上适当的水平表达。所表达的抗体是“反向嵌合体”,即,它们包含人可变区序列和小鼠恒定区序列。具有表达具有人或人源化可变区和小鼠恒定区的抗体的人源化免疫球蛋白可变区的这些小鼠称为小鼠。
[0250]
人源化小鼠表现出与野生型小鼠基本上不可区分的完全功能性体液免疫系统。它们在b细胞发育的所有阶段均显示正常细胞群体。它们表现出正常的淋巴器官形态。小鼠的抗体序列表现出正常v(d)j重排和正常体细胞超突变频率。这些小鼠中的抗体群体反映由正常类别转换(例如,正常同种型顺式转换)产生的同种型分布。对小鼠进行免疫接种产生稳固的体液免疫应答,其产生具有适合用作治疗候选物的人免疫球蛋白可变结构域的大型多样化抗体谱。此平台提供了用于制造药学上可接受的抗体和其它抗原结合蛋白的天然亲和力成熟的人免疫球蛋白可变区序列的丰富来源。还已经显示用人v
h
基因区段替换甚至单个内源性v
h
基因区段也可以导致包含人源化免疫球蛋白可变结构域的免疫应答。参见例如tien等人(2016)《细胞(cell)》166:1471
‑
84;以全文引用的方式并入本文中。正是用人免疫球蛋白可变序列精确替换小鼠免疫球蛋白可变序列使得人免疫球蛋白可变序列以反向嵌合方式与内源非人恒定区基因序列有效地连接,从而允许制造小鼠。
[0251]
以反向嵌合方式进行修饰的小鼠包括经过修饰以在内源免疫球蛋白基因座处包含有效地连接于内源恒定区的人(源化)可变区(例如包含(d)、j和一个或多个人v基因区段),例如
[0252]
(a)在内源重链基因座处∶
[0253]
(i)与内源性重链恒定区有效地连接的未重排的人(源化)免疫球蛋白重链可变区,其中所述未重排的人(源化)免疫球蛋白重链可变区包含多个未重排的人重链可变区v
h
基因区段(例如,所有功能性未重排的人v
h
基因区段)、一个或多个未重排的免疫球蛋白重链d
h
基因区段和一个或多个未重排的免疫球蛋白重链j
h
基因区段,
[0254]
任选地,其中所述一个或多个未重排的免疫球蛋白重链d
h
基因区段和所述一个或多个未重排的免疫球蛋白重链j
h
基因区段是一个或多个未重排的人免疫球蛋白重链d
h
基因区段(例如,所有功能性人d
h
基因区段)和/或一个或多个未重排的人免疫球蛋白重链j
h
基因区段(例如,所有功能性人j
h
基因区段);
[0255]
(ii)与内源性重链恒定区有效地连接的限制性未重排的人(源化)重链可变区,其中所述限制性未重排的人(源化)重链可变区基本上由与一个或多个未重排的免疫球蛋白重链d
h
基因区段和一个或多个未重排的免疫球蛋白重链j
h
基因区段有效地连接的单个未重
排的人重链可变区v
h
基因区段组成,任选地,其中所述一个或多个未重排的免疫球蛋白重链d
h
基因区段和所述一个或多个未重排的免疫球蛋白重链j
h
基因区段分别是一个或多个未重排的人免疫球蛋白重链d
h
基因区段和/或一个或多个未重排的人免疫球蛋白重链j
h
基因区段;
[0256]
(iii)与内源性重链恒定区有效地连接的经组氨酸修饰的未重排的人(源化)轻链可变区,其中所述经组氨酸修饰的未重排的人(源化)重链可变区包含未重排的免疫球蛋白重链可变基因序列,所述未重排的免疫球蛋白重链可变基因序列在互补决定区3(cdr3)编码序列中包含至少一个非组氨酸密码子经组氨酸密码子的取代或至少一个组氨酸密码子的插入;或
[0257]
(iv)包含与内源性重链恒定区有效地连接的未重排的人(源化)重链可变区的仅重链免疫球蛋白编码序列,其中所述内源性重链恒定区包含(1)编码与轻链关联的igm同种型的完整的内源性igm基因和(2)缺乏编码功能性ch1结构域的序列的非igm基因(例如igg基因),其中所述非igm基因编码缺乏能够与轻链恒定结构域共价关联的ch1结构域的非igm同种型;
[0258]
和/或
[0259]
(b)在内源轻链基因座处:
[0260]
(i)与内源性轻链恒定区有效地连接的未重排的人(源化)免疫球蛋白轻链可变区,其中所述未重排的人(源化)免疫球蛋白轻链可变区包含多个未重排的人轻链可变区v
l
基因区段(例如,所有功能性未重排的人v
l
基因区段)和一个或多个未重排的免疫球蛋白轻链j
l
基因区段,
[0261]
任选地,其中所述一个或多个未重排的免疫球蛋白轻链j
l
基因区段是一个或多个未重排的人免疫球蛋白轻链j
l
基因区段(例如,所有功能性人j
h
l基因区段),
[0262]
任选地,其中所述内源性免疫球蛋白轻链基因座是内源性免疫球蛋白轻链(κ)基因座,所述未重排的人(源化)免疫球蛋白轻链可变区包含人可变κ(vκ)和连接κ(jκ)基因区段,并且其中所述内源性轻链恒定区是内源性链恒定区序列和/或其中所述内源性免疫球蛋白轻链基因座是内源性免疫球蛋白轻链兰布达(λ),未重排的人(源化)的免疫球蛋白轻链可变区包含人可变λ(vλ)和连接λ(jλ)基因区段,并且所述内源性轻链恒定区是内源性λ链恒定区序列,任选地其中所述内源性免疫球蛋白轻链λ基因座包含(a)一个或多个人vλ基因区段,(b)一个或多个人jλ基因区段,和(c)一个或多个人cλ基因区段,其中(a)和(b)有效地连接至(c)和啮齿动物免疫球蛋白轻链恒定(c基因区段,并且其中所述内源性免疫球蛋白λ轻链基因座还包含:一个或多个啮齿动物免疫球蛋白λ轻链增强子(eλ和一个或多个人免疫球蛋白λ轻链增强子(eλ),任选地包含三个人eλ;
[0263]
(ii)包含与内源性轻链恒定区有效地连接的重排的人(源化)轻链可变区序列的常见轻链编码序列,其中所述重排的人(源化)轻链可变区序列包含与免疫球蛋白轻链j
l
基因区段重排的人轻链可变区v
l
基因区段;
[0264]
(iii)与内源性轻链恒定区有效地连接的限制性未重排的人(源化)轻链可变区,其中所述限制性未重排的人(源化)轻链可变区包含不超过两个与一个或多个未重排的人免疫球蛋白轻链连接(j
l
)基因区段有效地连接的未重排的人免疫球蛋白轻链可变区(v
l
)基因区段;
[0265]
(iv)与内源轻链恒定区呈有效连接的经过组氨酸修饰的未重排的人(源化)轻链可变区,其中所述经过组氨酸修饰的未重排的人(源化)轻链可变区包含未重排的人(源化)免疫球蛋白轻链可变基因序列,所述未重排的人(源化)免疫球蛋白轻链可变基因序列在互补决定区3(cdr3)编码序列中包含至少一个非组氨酸密码子经组氨酸密码子取代或插入至少一个组氨酸密码子;或
[0266]
(v)与内源轻链恒定区呈有效连接的经过组氨酸修饰的重排的人(源化)轻链可变区,其中所述经过组氨酸修饰的重排的人(源化)轻链可变区包含重排的人(源化)免疫球蛋白轻链可变基因序列,所述重排的人(源化)免疫球蛋白轻链可变基因序列在互补决定区3(cdr3)编码序列中包含至少一个非组氨酸密码子经组氨酸密码子取代或插入至少一个组氨酸密码子,
[0267]
任选地,其中所述小鼠还包含
[0268]
(i)人(源化)免疫球蛋白重链基因座,其包含功能性adam6基因,使得小鼠展现非人动物的野生型繁殖力;和/或
[0269]
(ii)用于增加抗原受体多样性的外源末端脱氧核苷酸转移酶(tdt)基因,任选地使得重排的可变区基因的至少10%包含非模板添加,
[0270]
先前已经对所述小鼠进行了描述。参见例如,美国专利号8,697,940;8,754,287;9,204,624;9,334,334;9,801,362;9,332,742;和9,516,868;美国专利公开20110195454、20120021409、20120192300、20130045492;20150289489;20180125043;20180244804;pct公开号wo2019/113065、wo2017210586和wo2011163314;lee等人(2014)《自然生物技术(nature biotechnology)》32:356;各以全文引用的方式并入本文中。
[0271]
在一些实施方案中,本发明包括基因组、例如种系基因组包含以下的经过基因修饰的非人动物:
[0272]
包含免疫球蛋白重链可变区的内源性免疫球蛋白基因座,所述免疫球蛋白重链可变区包含人v
h
基因区段、本发明的人工程化d
h
基因区和人j
h
基因区段,其中所述免疫球蛋白重链可变区有效地连接至恒定区,和/或
[0273]
内源链基因座,其包含包括人vl基因区段和人jl基因区段的免疫球蛋白轻链可变区,其中所述免疫球蛋白轻链可变区有效地连接于恒定区。
[0274]
在一些实施方案中,非人动物(例如啮齿动物,例如大鼠或小鼠),在其基因组中包含在内源性免疫球蛋白重链基因座处的一个或多个内源性v
h
、d
h
和j
h
区段经一个或多个人v
h
、d
h
和j
h
区段的替换,其中所述一个或多个人v
h
、d
h
和j
h
区段包含与23聚体rss有效地连接的人d
h
基因区段并且有效地连接至内源性免疫球蛋白重链基因;以及任选地与例如在内源性非人轻链基因座处的非人(例如啮齿动物,例如小鼠或大鼠)或人免疫球蛋白轻链恒定(c
l
)区基因有效地连接的未重排的或重排的人v
l
和人j
l
区段。
[0275]
在某些实施方案中,经基因修饰的非人动物在其基因组、例如种系基因组中包含免疫球蛋白基因座(外源或内源),所述免疫球蛋白基因座含有包含一个或多个未重排的人免疫球蛋白可变区基因区段(包括工程化d
h
区)的免疫球蛋白可变区和包含免疫球蛋白恒定区基因的免疫球蛋白恒定区,并且其中所述一个或多个未重排的人免疫球蛋白可变区基因区段有效地连接至免疫球蛋白恒定区基因。
[0276]
一般来讲,经过基因修饰的免疫球蛋白基因座包含有效地连接于免疫球蛋白恒定
区的免疫球蛋白可变区(包含免疫球蛋白可变区基因区段)。在一些实施方案中,经基因修饰的免疫球蛋白基因座包含与重链恒定区基因有效地连接的一个或多个人未重排的免疫球蛋白重链可变区基因区段,包括工程化d
h
区。在一些实施方案中,经过基因修饰的免疫球蛋白基因座包含有效地连接于κ链恒定区基因的人未重排的免疫球蛋白可变区κ基因区段。在一些实施方案中,经过基因修饰的免疫球蛋白基因座包含有效地连接于κ链恒定区基因的人未重排的免疫球蛋白可变区λ基因区段。在一些实施方案中,经过基因修饰的免疫球蛋白基因座包含有效地连接于λ链恒定区基因的人未重排的免疫球蛋白可变区λ基因区段。
[0277]
在某些实施方案中,非人动物在内源性重链基因座处包含与内源性重链恒定区有效地连接的包含工程化d
h
区的未重排的人(源化)免疫球蛋白重链可变区,其中免疫球蛋白可变区含有一个或多个未重排的人ig重链可变区基因区段。在一些实施方案中,所述一个或多个未重排的人ig可变区基因区段包含至少一个人免疫球蛋白重链可变(v
h
)区段、一个或多个免疫球蛋白重链多样性(d
h
)区段(例如,有效地连接至23聚体rss的一个或多个未重排的人d
h
区段)、以及一个或多个免疫球蛋白重链连接(j
h
)区段(任选地一个或多个未重排的人j
h
区段)。在一些实施方案中,未重排的人ig可变区基因区段包含多个未重排的人v
h
区段、一个或多个未重排的(人)d
h
区段(例如,有效地连接至23聚体rss的一个或多个未重排的(人)d
h
区段)和一个或多个未重排的(人)j
h
区段。在一些实施方案中,未重排的人ig可变区基因区段包含至少3个v
h
基因区段、至少18个v
h
基因区段、至少20个v
h
基因区段、至少30个v
h
基因区段、至少40个v
h
基因区段、至少50个v
h
基因区段、至少60个v
h
基因区段、至少70个v
h
基因区段、或至少80个v
h
基因区段。在一些实施方案中,未重排的人ig基因区段包括所有功能性人d
h
基因区段,其中所述功能性人d
h
基因区段中的至少一个被修饰为有效地连接至23聚体rss。在一些实施方案中,未重排的人ig基因区段包括所有功能性人j
h
基因区段。例如以下中提供了包含ig重链基因区段的示例性可变区:macdonald等人,《美国国家科学院sci.)》usa 111:5147
‑
52和补充信息,其以全文引用的方式并入本文中。
[0278]
在一些实施方案中,本文提供的非人动物在内源性重链基因座处包含与包含至少一个非人igm基因的内源性重链恒定区有效地连接的限制性未重排的人(源化)重链可变区,其中所述限制性未重排的人(源化)重链可变区的特征在于单个人v
h
基因区段、多个d
h
基因区段(例如,人d
h
基因区段,包括有效地连接至23聚体rss的一个或多个未重排的(人)d
h
区段)和多个j
h
基因区段(例如人j
h
基因区段),其中所述限制性免疫球蛋白重链基因座能够重排并形成多个不同的重排,其中每个重排均源自所述单个人v
h
基因区段、所述d
h
区段中的一个和所述j
h
区段中的一个,并且其中每个重排编码不同的重链可变结构域(例如,如在美国专利公开号20130096287中所述,其据此以全文引用的方式并入)。在一些实施方案中,单个人v
h
基因区段为v
h1‑
2或v
h1‑
69.
[0279]
在某些实施方案中,非人动物在内源轻链基因座处包含与内源轻链恒定区呈有效连接的未重排的人(源化)免疫球蛋白轻链可变区。在一些实施方案中,未重排的人(源化)免疫球蛋白轻链可变区含有未重排的人igκ可变区基因区段。在一些实施方案中,未重排的人(源化)免疫球蛋白可变区包含多个未重排的人vκ区段和一个或多个未重排的人j
k
区段。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含所有人jκ区段。在一些实施方案中,免疫球蛋白可变区基因区段包含四个功能性vκ区段和所有人jκ区段。在一些实施方案中,免疫球蛋白可变区基因区段包含16个功能性vκ区段和所有人jκ区段(例如,所有
功能性人vκ区段和jκ区段)。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含所有人vκ区段和所有人jκ区段。例如以下中提供了包含igκ基因区段的示例性可变区:macdonald等人,《美国国家科学院sci.)》usa 1 11:5147
‑
52和补充信息,其以全文引用的方式并入本文中。
[0280]
在一些实施方案中,与内源性轻链恒定区有效地连接的限制性未重排的人(源化)轻链可变区的特征在于所述未重排的人(源化)轻链可变区包含不超过两个人v
l
基因区段和多个j
l
基因区段(例如,双轻链小鼠或dlc,如美国专利号9,796,788中所述,其据此以全文引用的方式并入)。在一些实施方案中,v
l
基因区段是vκ基因区段。在一些实施方案中,v
l
基因区段是vλ基因区段。在一些实施方案中,vκ基因区段是igkv3
‑
20和igkv1
‑
39。在一些实施方案中,非人动物包含与在小鼠内源性κ轻链基因座处的小鼠轻链恒定区有效地连接的恰好两个未重排的人vκ基因区段和五个未重排的人jκ基因区段,任选地其中所述恰好两个未重排的人vκ基因区段是人vκ1
‑
39基因区段和人vκ3
‑
20基因区段,其中所述五个未重排的人jκ基因区段是人jκ1基因区段、人jκ2基因区段、人jκ3基因区段、人jκ4基因区段和人jκ5基因区段,其中所述未重排的人κ轻链基因区段能够重排和编码抗体的人可变结构域,并且任选地进一步其中所述非人动物不包含能够重排以形成免疫球蛋白轻链可变区的内源性vκ基因区段。
[0281]
在某些实施方案中,与内源轻链恒定区呈有效连接的未重排的人(源化)免疫球蛋白轻链可变区含有未重排的人igλ可变区基因区段。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含多个人vλ区段和一个或多个人jλ区段。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含一个或多个人vλ区段、一个或多个人jλ区段和一个或多个人cλ恒定区序列。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含所有人vλ区段。在一些实施方案中,未重排的人免疫球蛋白可变区基因区段包含所有人jλ区段。例如以下中提供了包含igλ基因区段的示例性可变区:美国专利第9,035,128号和第6,998,514号,每个专利以全文引用的方式并入本文中。在一些实施方案中,与内源性轻链恒定区有效地连接的未重排的人(源化)免疫球蛋白轻链可变区包含(a)一个或多个人vλ基因区段,(b)一个或多个人jλ基因区段,和(c)一个或多个人cλ基因区段,其中(a)和(b)有效地连接至(c)和内源性(例如啮齿动物)cλ基因区段,并且其中所述内源性免疫球蛋白λ轻链基因座还包含:一个或多个啮齿动物免疫球蛋白λ轻链增强子(eλ)、以及一个或多个人免疫球蛋白λ轻链增强子(eλ),任选地包含三个人eλ。
[0282]
在某些实施方案中,与内源轻链恒定区呈有效连接的未重排的人(源化)免疫球蛋白轻链可变区包含有效地连接于内源(例如啮齿动物,例如大鼠或小鼠)cκ基因的未重排的人igλ可变区基因区段,使得非人动物表达包含来源于v和j基因区段的人可变结构域序列与内源κ恒定结构域融合的免疫球蛋白轻链,参见例如美国专利第9,226,484号,以全文引用的方式并入本文中。
[0283]
在一些实施方案中,包含未重排的人免疫球蛋白可变区基因区段的免疫球蛋白可变区还包括人免疫球蛋白可变区基因间序列。在一些实施方案中,免疫球蛋白可变区包括非人(例如啮齿动物、大鼠、小鼠)ig可变区基因间序列。在一些实施方案中,基因间序列是内源物种来源。
[0284]
在一些实施方案中,免疫球蛋白可变区是重排的轻链可变区(通用轻链可变区)。
在一些实施方案中,重排的ig轻链可变区基因是人重排的ig轻链可变区基因。示例性重排的ig轻链可变区在以下中提供:例如美国专利第9,969,814号、第10,130,181号和第10,143,186号和美国专利公布第20120021409号、第20120192300号、第20130045492号、第20130185821号、第20130302836号和第20150313193号,各以全文引用的方式并入本文中。在一些实施方案中,包含通用轻链可变区的非人生物体(“通用轻链”生物体)用于产生双特异性抗体。在一些实施方案中,共同轻链编码序列包含有效地连接于内源轻链恒定区的单个重排的人免疫球蛋白轻链vκ/jκ序列,其中单个重排的人免疫球蛋白轻链vκ/jκ序列为(i)包含人vκ1
‑
39基因区段与人jκ5基因区段融合的人vκ1
‑
39/jκ5序列,或(ii)包含人vκ3
‑
20基因区段与人jκ1基因区段融合的人vκ3
‑
20/jκ1序列。
[0285]
在一些实施方案中,免疫球蛋白可变区为包括插入和/或替换组氨酸密码子的轻链和/或重链免疫球蛋白可变区,所述组氨酸密码子的插入和/或替换被设计成引入ph依赖性结合特性至在此类非人生物体中产生的抗体中。在一些此类实施方案中,组氨酸密码子在编码cdr3的核酸序列中插入和/或替换。各种这样的轻链和/或重链免疫球蛋白基因座在美国专利第9,301,510号、第9,334,334号和第9,801,362号和美国专利申请公布第20140013456号中提供,各以全文引用的方式并入本文中。在一些实施方案中,与内源轻链恒定区呈有效连接的经过组氨酸修饰的重排的人(源化)轻链可变区包含包括人vκ和jκ区段序列的单个重排的人免疫球蛋白轻链可变区基因序列,任选地其中vκ区段序列来源于人vκ1
‑
39或vκ3
‑
20基因区段,并且其中单个重排的人免疫球蛋白轻链可变区基因序列包含vκ区段序列的至少一个非组氨酸密码子经组氨酸密码子取代,所述组氨酸密码子在选自由以下组成的群组的位置表达:105、106、107、108、109、111和其组合(根据imgt编号)。在一些实施方案中,与内源性重链恒定区有效地连接的经组氨酸修饰的未重排的人(源化)重链可变区包含未重排的人(源化)免疫球蛋白重链可变基因序列,其在互补决定区3(cdr3)编码序列中(例如,包含在经修饰以有效地连接至23聚体rss的(人)d
h
基因区段中)包含至少一个非组氨酸密码子经组氨酸密码子的取代或至少一个组氨酸密码子的插入。在一些实施方案中,未重排的人(源化)免疫球蛋白重链可变基因序列包含未重排的人v
h
基因区段、未重排的人d
h
基因区段或包括与23聚体rss有效地连接的d
h
基因区段的合成的d
h
基因区段、以及未重排的人j
h
基因区段,任选地其中所述未重排的人d
h
或合成的d
h
基因区段或有效地连接至23聚体rss的d
h
基因区段包含至少一个非组氨酸密码子经组氨酸密码子的取代或至少一个组氨酸密码子的插入。在一些实施方案中,与内源性重链恒定区有效地连接的经组氨酸修饰的未重排的人(源化)轻链可变区包含未重排的v
l
和未重排的j
l
基因区段。在一些实施方案中,经组氨酸修饰的未重排的人(源化)轻链可变区包含不超过两个未重排的人v
l
(例如,不超过两个vκ基因区段)和一个或多个未重排的人j
l
(例如jκ)基因区段,其中所述不超过两个人v
l
基因区段中的每一个在cdr3编码序列中包含至少一个非组氨酸密码子经组氨酸密码子的取代或至少一个组氨酸密码子的插入。在一些实施方案中,所述至多两个未重排的人vκ基因区段为各自包含非组氨酸密码子经组氨酸密码子一次或多次取代的人vκ1
‑
39和vκ3
‑
20基因区段,并且其中人vκ和jκ基因区段能够重排并且人vκ和jκ基因区段编码在选自由以下组成的群组的位置包含一个或多个组氨酸的人轻链可变结构域:105、106、107、108、109、111(根据igmt编号)和其组合,其中一个或多个组氨酸来源于一次或多次取代。
[0286]
在一些实施方案中,免疫球蛋白恒定区包含重链恒定区基因。在一些实施方案中,
重链恒定区基因是人重链恒定区基因。在一些实施方案中,重链恒定区基因是内源物种来源。在一些实施方案中,重链恒定区基因是小鼠恒定区基因或大鼠恒定区基因。在一些实施方案中,恒定区基因是人和非人序列的混合物。例如,在一些实施方案中,恒定区基因编码人ch1区和非人(例如内源物种来源、小鼠、大鼠)ch2和/或ch3区。在一些实施方案中,重链恒定区基因是cμ、cδ、cγ(cγl、cγ2、cγ3、cγ4)、cα或cε恒定区基因。在一些实施方案中,恒定区基因是内源恒定区基因。在一些实施方案中,恒定区基因编码突变的ch1区域,使得非人动物表达只有重链的抗体(参见例如美国专利第8,754,287号、美国专利申请公布第2015/0289489号,各以全文引用的方式并入本文中)。在一些实施方案中,例如,在目标是产生重链以制备双特异性抗体的情况下(例如,在通用或双轻链生物体中),重链的fc结构域包含促进重链异二聚体形成和/或抑制重链同二聚体形成的修饰。这样的修饰例如在以下中提供:美国专利第5,731,168号、第5,807,706号、第5,821,333号、第7,642,228号和第8,679,785号以及美国专利公布第2013/0195849号,各以全文引用的方式并入本文中。
[0287]
在一些实施方案中,免疫球蛋白恒定区包含轻链恒定区基因。在一些实施方案中,轻链恒定区基因是κ恒定区基因。在一些实施方案中,轻链恒定区基因是λ恒定区基因。在一些实施方案中,轻链恒定区基因是内源物种来源。在一些实施方案中,轻链恒定区基因是小鼠恒定区基因或大鼠恒定区基因。在一些实施方案中,轻链恒定区基因是人和非人序列的混合物。
[0288]
在一些实施方案中,包含人可变区基因区段的免疫球蛋白可变区和可变区基因区段有效地连接于的免疫球蛋白恒定区基因位于内源免疫球蛋白基因座处。在一些实施方案中,内源免疫球蛋白基因座是内源重链基因座。在一些实施方案中,内源免疫球蛋白基因座是内源κ基因座。在一些实施方案中,内源免疫球蛋白基因座是内源λ基因座。在一些实施方案中,人可变区基因区段有效地连接于的恒定区基因是内源恒定区基因。
[0289]
在一些实施方案中,本文提供的非人动物的基因组中的一个或多个内源免疫球蛋白基因座或一个或多个内源基因座(例如可变区和/或恒定区)的一部分失活。可使用本领域已知的任何方法使内源免疫球蛋白可变区基因基因座和其部分失活,包括但不限于基因座或其一部分从生物体的基因组缺失、用不同核酸序列替换基因座或其一部分、基因座的一部分倒置和/或基因座的一部分移到非人生物体基因组中的另一位置。在一些实施方案中,基因座的失活仅是部分失活。在一些实施方案中,基因座的可变区是失活的,但恒定区保持功能(例如,因为其有效地连接于非内源可变区基因区段)。
[0290]
在一些实施方案中,经过基因修饰的非人动物包括失活的内源免疫球蛋白重链基因座。在一些实施方案中,内源免疫球蛋白重链基因座或其一部分通过内源重链基因座的内源可变区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,缺失、替换、移位和/或倒置的内源重链基因座的可变区的至少一部分包含可变区的j区段。在一些实施方案中,内源免疫球蛋白重链基因座或其部分通过内源重链基因座的内源恒定区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,缺失、替换、移位和/或倒置的恒定区的内源重链基因座的至少一部分包含内源恒定区的ομ基因。
[0291]
在一些实施方案中,经过基因修饰的非人动物包括失活的内源免疫球蛋白κ链基因座。在一些实施方案中,内源免疫球蛋白κ链基因座或其一部分通过内源κ链基因座的内源可变区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,缺失、替
换、移位和/或倒置的内源κ链基因座的可变区的至少一部分包含可变区的j区段。在一些实施方案中,内源免疫球蛋白κ链基因座或其一部分通过内源κ链基因座的内源恒定区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,缺失、替换、移位和/或倒置的内源κ链基因座的恒定区的至少一部分包含内源恒定区的cκ基因。
[0292]
在一些实施方案中,经过基因修饰的非人动物包括失活的内源免疫球蛋白λ链基因座。在一些实施方案中,内源免疫球蛋白λ链基因座或其一部分通过内源λ链基因座的内源可变区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,内源λ链基因座中的至少一个v
‑
j
‑
c基因簇的至少一部分缺失、替换、移位和/或倒置。在一些实施方案中,内源免疫球蛋白λ基因座或其一部分通过内源λ链基因座的内源恒定区的至少一部分的缺失、替换、移位和/或倒置而失活。在一些实施方案中,缺失、替换、移位和/或倒置的内源λ链基因座的恒定区的至少一部分包含内源恒定区的c基因。
[0293]
在各种实施方案中,免疫球蛋白基因座修饰不影响非人动物的繁殖力。在一些实施方案中,重链基因座包含功能性,例如内源adam6a基因、adam6b基因或两者,并且基因修饰不影响内源adam6a基因、adam6b基因或两者的表达和/或功能。在一些实施方案中,基因修饰的非人动物的基因组还包含位于异位的功能性,例如内源adam6a基因、adam6b基因,或两者。表达外源adam6a和/或adam6b的示例性非人动物在以下中描述:美国专利第8,642,835号和第8,697,940号,各以全文引用的方式并入本文中。
[0294]
在一些实施方案中,经过基因修饰的非人动物还包含外源末端脱氧核苷酸转移酶(tdt)以增加抗原受体多样性。在pct公布wo 2017210586中描述了表达外源tdt的示例性非人动物,所述公布以全文引用的方式并入本文中。
[0295]
在一些实施方案中,所提供的非人动物基因组还包含一个或多个人免疫球蛋白重链和/或轻链基因(参见例如,美国专利号8,502,018;美国专利号8,642,835;美国专利号8,697,940;美国专利号:8,791,323;和美国专利申请公开号2013/0096287a1和2018/0125043a1;和pct公开号wo2019/113065;每个专利以全文引用的方式并入本文。)。可替代地,可以将工程化d
h
区引入不同修饰品系、例如velocimmune品系的胚胎干细胞中(参见例如,美国专利号8,502,018或美国专利号8,642,835;以全文引用的方式并入本文)。在一些实施方案中,可以通过将本文所述的靶向载体引入修饰品系的细胞中来制备本文所述的非人动物。仅举一个实例,可以将如本文所述的靶向载体引入如美国专利号8,642,835和8,697,940(以全文引用的方式并入本文)中所述的非人动物中,所述非人动物表达具有完全人可变区和小鼠恒定区的抗体。在一些实施方案中,如本文所述的非人类动物被制备为还包含人类免疫球蛋白基因(可变和/或恒定区基因)。在一些实施方案中,如本文所述的非人动物包含如本文所述的工程化d
h
区和来自异源物种(例如,人)的遗传物质,其中所述遗传物质编码一个或多个人重链和/或轻链可变区的全部或部分。
[0296]
本文所述的非人动物可以如上文所述那样或使用本领域已知的方法制备为包含另外的人或人源化基因,这通常取决于非人动物的预期用途。此类另外的人或人源化基因的遗传物质可通过进一步改变具有上述遗传修饰的细胞(例如,胚胎干细胞)的基因组,或通过本领域已知的繁育技术利用所需的其他基因修饰品系引入。
[0297]
例如,如本文所述,包含工程化d
h
区的非人动物可以还包含(例如,通过杂交或多种基因靶向策略)一种或多种修饰,如以下专利所述:美国专利申请公开号2011
‑
0195454a1、2012
‑
0021409a1、2012
‑
0192300a1、2013
‑
0045492a1、2013
‑
0185821a1、2013
‑
0198880a1、2013
‑
0302836a1、2015
‑
0059009a1;国际专利申请公开号wo 2011/097603、wo 2012/148873、wo 2013/134263、wo 2013/184761、wo 2014/160179、wo 2014/160202;将所述专利全部据此以全文引用的方式并入。
[0298]
可以基于在其基因组中工程化d
h
区的存在和/或包括含有由在非人动物的组织或细胞中的d
h
‑
d
h
重组产生的氨基酸的cdr3区的抗体的表达来鉴定转基因首建者非人动物。然后转基因首建者非人动物可以用于繁育携带工程化d
h
区的另外的非人动物,从而创建各自携带一个或多个拷贝的工程化d
h
区的非人动物系列。此外,根据需要,携带工程化d
h
区的转基因非人动物还可以与携带其他转基因(例如,人免疫球蛋白基因)的其他转基因非人动物交配。
[0299]
还可以产生含有所选系统的转基因非人类动物,所选系统能够调控或引导转基因的表达。示例性系统包括噬菌体p1的cre/loxp重组酶系统(参见例如lakso,m.等人,1992,proc.natl.acad.sci.usa 89:6232
‑
6236;所述文献以全文引用的方式并入)和酿酒酵母的flp/frt重组酶系统(o’gorman,s.等人,1991,science 251:1351
‑
1355;每篇文献以全文引用的方式并入)。此类动物可以通过构建“双”转基因动物,例如通过两个转基因动物(一个动物含有包含选定修饰(例如,工程化d
h
区)的转基因,并且另一个动物含有编码重组酶(例如,cre重组酶)的转基因)的交配来提供。
[0300]
尽管在小鼠(即具有与其全部有效地连接至一个或多个鼠重链恒定区基因的人v
h
和j
h
基因区段有效地连接的工程化d
h
区的小鼠)中采用工程化d
h
区的实施方案在本文中广泛讨论,还提供了包含工程化d
h
区的其他非人动物。在一些实施方案中,此类非人动物包含与内源性v
h
和j
h
基因区段有效地连接的工程化d
h
区。在一些实施方案中,此类非人动物包含与人源化v
h
和j
h
基因区段有效地连接的工程化d
h
区。此类非人动物包括那些可以被基因修饰以表达具有包括由与如本文所公开的野生型免疫球蛋白重链基因座相比以增加的频率进行的d
h
‑
d
h
重组而产生的氨基酸的cdr3的抗体的任何动物,包括例如,哺乳动物,例如小鼠、大鼠、兔、猪、牛(例如,奶牛、公牛、水牛)、鹿、绵羊、山羊、鸡、猫、狗、貂、灵长类动物(例如,狨猴、猕猴)等。例如,对于合适的可经遗传修饰的es细胞不容易获得的那些非人类动物,采用其他方法来制备包含遗传修饰的非人类动物。此类方法包括例如修饰非es细胞基因组(例如,成纤维细胞或诱导的多能细胞)并利用体细胞核转移(scnt)来将经遗传修饰的基因组转移至合适的细胞,例如去核卵母细胞,以及在适于形成胚胎的条件下在非人类动物中孕育经修饰的细胞(例如,经修饰的卵母细胞)。
[0301]
用于修饰非人动物(例如,猪、奶牛、啮齿动物、鸡等)基因组的方法包括例如利用锌指核酸酶(zfn)、转录活化因子样效应子核酸酶(talen)或cas蛋白(即,crispr/cas系统)将基因组修饰为包括如本文所述的工程化d
h
区。用于修饰非人动物的种系基因组的方法的指南可以在例如美国专利申请公开号2015
‑
0376628 a1、us 2016
‑
0145646 a1和us 2016
‑
0177339 a1(以全文引用的方式并入本文)中找到。
[0302]
在一些实施方案中,如本文所述的非人类动物是哺乳动物。在一些实施方案中,如本文所述的非人类动物是小型哺乳动物,例如跳鼠总科(dipodoidea)或鼠总科(muroidea)的小型哺乳动物。在一些实施方案中,如本文所述的经遗传修饰的动物是啮齿动物。在一些实施方案中,如本文所述的啮齿动物选自小鼠、大鼠和仓鼠。在一些实施方案中,如本文所
述的啮齿动物选自鼠总科。在一些实施方案中,如本文所述的经遗传修饰的动物来自选自以下的科:丽仓鼠科(calomyscidae)(例如,类小鼠的仓鼠)、仓鼠科(cricetidae)(例如,仓鼠、新世界大鼠和小鼠、田鼠)、鼠科(muridae)(真小鼠和大鼠、沙鼠、刺毛鼠、冠鼠)、马岛鼠科(nesomyidae)(攀鼠、岩鼠、白尾大鼠、马达加斯加大鼠和小鼠)、刺睡鼠科(platacanthomyidae)(例如,多刺睡鼠)和鼹形鼠科(spalacidae)(例如,鼹鼠、竹鼠和鼢鼠)。在一些实施方案中,如本文所述的经遗传修饰的啮齿动物选自真小鼠或大鼠(鼠科)、沙鼠、刺毛鼠和冠鼠。在一些实施方案中,如本文所述的经遗传修饰的小鼠来自鼠科的成员。在一些实施方案中,如本文所述的非人类动物是啮齿动物。在一些实施方案中,如本文所述的啮齿动物选自小鼠和大鼠。在一些实施方案中,如本文所述的非人类动物是小鼠。
[0303]
在一些实施方案中,如本文所述的非人类动物是啮齿动物,所述啮齿动物是选自以下的c57bl品系的小鼠:c57bl/a、c57bl/an、c57bl/grfa、c57bl/kalwn、c57bl/6、c57bl/6j、c57bl/6byj、c57bl/6nj、c57bl/10、c57bl/10scsn、c57bl/10cr和c57bl/ola。在一些实施方案中,本发明的小鼠为选自下列品系的129品系:129p1、129p2、129p3、129x1、129s1(例如129s1/sv、129s1/svim)、129s2、129s4、129s5、129s9/svevh、129/svjae、129s6(129/svevtac)、129s7、129s8、129t1、129t2(参见例如,festing等人,1999,mammalian genome 10:836;auerbach,w.等人,2000,biotechniques29(5):1024
‑
1028,1030,1032;以全文引用的方式并入本文)。在一些实施方案中,如本文所述的经遗传修饰的小鼠是前述129品系和前述c57bl/6品系的混合品系。在一些实施方案中,如本文所述的小鼠是前述129品系的混合品系,或前述bl/6品系的混合品系。在一些实施方案中,如本文所述的混合品系的129品系是129s6(129/svevtac)品系。在一些实施方案中,如本文所述的小鼠是balb品系,例如balb/c品系。在一些实施方案中,如本文所述的小鼠是balb品系和另一种前述品系的混合品系。
[0304]
在一些实施方案中,如本文所述的非人类动物是大鼠。在一些实施方案中,如本文所述的大鼠选自wistar大鼠、lea品系、sprague dawley品系、fischer品系、f344、f6和dark agouti。在一些实施方案中,如本文所述的大鼠品系是选自wistar、lea、sprague dawley、fischer、f344、f6和dark agouti的两个或更多个品系的混合品系。
[0305]
方法
[0306]
已经开发了几种体外和体内技术来生产基于抗体的治疗剂。特别地,体内技术的特征是含有人免疫球蛋白基因的转基因动物(即啮齿动物)的产生,所述人免疫球蛋白基因被随机地掺入动物基因组中(例如,参见美国专利号5,569,825,以全文引用的方式并入本文)或被精确地放置在与动物的内源性免疫球蛋白恒定区有效地连接的内源性免疫球蛋白基因座处(例如,参见美国专利号8,502,018;8,642,835;8,697,940;和8,791,323;每个专利以全文引用的方式并入)。这两种方法在生产用于人中使用的有希望的抗体治疗候选物方面均具有成效。此外,两种方法均优于体外方法,因为抗体候选物选自体内产生的抗体库,这包括对宿主免疫系统内部环境中的抗原的亲和力和特异性的选择。这样,抗体与天然存在的抗原(在相关的生物表位和表面内)结合,而不是可以伴随体外技术的人工环境或计算机预测结合。尽管从体内技术产生了强大的抗体库,但是针对复合物(例如,病毒、通道多肽)或细胞质抗原的抗体仍然存在困难。进一步地,由于免疫耐受性,生成针对在物种(例如,人和小鼠)之间共享高度序列同一性的多肽的抗体仍是挑战。
[0307]
因此,本发明基于以下认识:以由非传统基因区段重排(即d
h
与d
h
重组)产生的cdr(特别是cdr3)的多样性增加的抗体的产生为特征的体内系统构建可以使用各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段进行。与缺乏此类工程化d
h
基因区段的免疫球蛋白重链基因座相比,通过具有5’或3’23聚体rss,在d
h
区段之间的重组增加。这种增加的多样性可以指导与特定抗原(例如,病毒、通道多肽)的结合。在v
h
基因区段、至少两个d
h
基因区段和j
h
基因区段重组后,形成包含具有通过d
h
与d
h
重组产生的氨基酸序列的cdr3区的重链可变区编码序列。此外,由于氨基酸长度增加,由d
h
与d
h
重组产生的这种cdr3含有增加的多样性。此外,这样的cdr3区具有直接结合原本不能被通过传统vdj重组产生的抗体结合的特定抗原(或表位)的能力。
[0308]
所提供的非人动物可以用于制备人抗体,其中所述人抗体包含从由如本文所述的非人动物的细胞遗传物质编码的一个或多个可变区核酸序列衍生的可变结构域。例如,在足以使非人动物对所述所关注抗原产生免疫应答的条件下,用所关注抗原(例如全部或部分的病毒或通道多肽)免疫所提供的非人动物,并持续足以使非人动物对所述所关注抗原产生免疫应答的时间。从非人动物(或者一个或多个细胞,例如一个或多个b细胞)中分离抗体,并且使用各种测定进行表征,所述测定测量例如亲和力、特异性、表位作图、阻断配体
‑
受体相互作用的能力、抑制性受体活化等。在一些实施方案中,所提供的非人动物产生的抗体包含一个或多个人可变结构域,所述人可变结构域衍生自从非人动物分离的一个或多个人可变区核苷酸序列。在一些实施方案中,可以在所提供的非人动物中产生抗药物抗体(例如抗独特型抗体)。
[0309]
如本文所述的非人动物提供了用于产生可用于多种测定的人抗体的改进的体内系统和生物材料(例如,细胞)来源。在一些实施方案中,将所提供的非人动物用于开发靶向一种或多种病毒和/或调节病毒活性和/或调节病毒与其他结合伴侣(例如细胞表面受体)的相互作用的治疗剂。在一些实施方案中,将所提供的非人动物用于开发靶向一种或多种通道蛋白和/或调节通道蛋白活性和/或调节通道蛋白与其他结合伴侣的相互作用的治疗剂。在一些实施方案中,将所提供的非人动物用于鉴定、筛选和/或开发结合一种或多种病毒、通道或g蛋白偶联受体(gpcr)多肽的候选治疗剂(例如,抗体、sirna等)。在一些实施方案中,将所提供的非人动物用于筛选和开发阻断一种或多种病毒多肽、一种或多种人通道多肽或一种或多种人gpcr多肽的活性的候选治疗剂(例如,抗体、sirna等)。在一些实施方案中,将所提供的非人动物用于确定一种或多种人gpcr多肽或一种或多种人通道多肽的拮抗剂和/或激动剂的结合谱。在一些实施方案中,将所提供的非人动物用于确定结合一种或多种人gpcr多肽或结合一种或多种人通道多肽的一种或多种候选治疗性抗体的一个或多个表位。
[0310]
在一些实施方案中,将所提供的非人动物用于确定抗体的药代动力学特征。在一些实施方案中,一种或多种所提供的非人动物和一种或多种对照或参考非人动物各自以多个剂量(例如,0.1mg/kg、0.2mg/kg、0.3mg/kg、0.4mg/kg、0.5mg/kg、1mg/kg、2mg/kg、3mg/kg、4mg/kg、5mg/mg、7.5mg/kg、10mg/kg、15mg/kg、20mg/kg、25mg/kg、30mg/kg、40mg/kg或50mg/kg或更高)暴露于一种或多种候选治疗性抗体。候选治疗性抗体可以经由各种所需的施用途径(包括肠胃外和非肠胃外施用途径)来给药。肠胃外途径包括例如静脉内、动脉内、门静脉内、肌肉内、皮下、腹膜内、脊柱内、鞘内、脑室内、颅内、胸膜内或其他注射途径。非肠
胃外途径包括例如口服、鼻腔、透皮、肺部、直肠、面颊、阴道、眼部。施用也可以通过连续输注、局部施用、从植入物(凝胶、膜等)的持续释放和/或静脉内注射(例如使用静脉内流体袋)进行。在多个时间点(例如,0小时、6小时、1天、2天、3天、4天、5天、6天、7天、8天、9天、10天、11天或最多30天或更多天)从非人类动物(人源化和对照)分离血液。可以使用从如本文所述的非人类动物获得的样品来进行多种测定,以确定所施用的候选治疗性抗体的药代动力学性质,包括但不限于总igg、抗治疗性抗体应答、凝集等。
[0311]
在一些实施方案中,将所提供的非人动物用于测量阻断或调节靶抗原活性的治疗效果以及由于如本文所述非人动物的细胞的靶抗原的细胞变化或细胞表面密度(在细胞表面受体的情况下)而对基因表达的影响。在一些实施方案中,将所提供的非人动物或从其分离的细胞暴露于结合所关注的抗原的候选治疗剂,并且在随后的一段时间之后,分析对靶抗原依赖性过程(或相互作用)(例如,配体
‑
受体相互作用或抗原相关信号)的影响。
[0312]
在一些实施方案中,将所提供的非人动物用于测量阻断或调节通道活性(或通道信号传导、或通道介导的相互作用或通道动作电位)的治疗效果以及由于如本文所述非人动物的细胞的细胞变化或通道密度而对基因表达的影响。在一些实施方案中,将所提供的非人动物或从其分离的细胞暴露于结合人通道多肽(或其一部分)的候选治疗剂,并且在随后的一段时间之后分析对通道依赖性过程(或相互作用)(例如配体
‑
受体相互作用或通道动作电位)的影响。
[0313]
在一些实施方案中,所提供的非人动物表达抗体,因此可以产生细胞、细胞系和细胞培养物以用作可用于在结合和功能测定中使用的抗体来源,例如,用于测定拮抗剂或激动剂的结合或功能,特别是在拮抗剂或激动剂对人多肽序列或表位具有特异性或者可替代地对在配体
‑
受体相互作用(结合)中起作用的人多肽序列或表位具有特异性的情况下。在一些实施方案中,可以使用从所提供的非人动物中分离的细胞来确定被候选治疗性抗体或sirna结合的表位。
[0314]
在一些实施方案中,可以分离来自所提供的非人动物的细胞并随时使用,或者可以在培养中维持许多代。在一些实施方案中,来自所提供的非人动物的细胞是永生化的(例如,通过使用病毒)并且在培养中无限期维持(例如,在连续培养中)。
[0315]
在一些实施方案中,如本文所述的非人动物提供了用于产生结合人靶抗原的抗体变体的体内系统。此类变体包括对由两个或更多个人靶抗原共享的共同表位具有所需的功能性、特异性、低交叉反应性的抗体。在一些实施方案中,将所提供的非人动物用于产生抗体组以产生针对所需的或改善的功能性进行筛选的一系列抗体变体。
[0316]
在一些实施方案中,如本文所述的非人动物提供了用于产生抗体文库的体内系统。此类文库提供了重链和轻链可变区序列源,其可基于所需效应子功能移植到不同的fc区上和/或使用本领域已知的技术(例如定点诱变、易错pcr等)用作可变区序列的亲和力成熟的来源。
[0317]
在一些实施方案中,如本文所述的非人动物提供了用于分析和测试药物或疫苗的体内系统。在一些实施方案中,候选药物或疫苗可以递送至一种或多种所提供的非人动物,然后监测所述非人动物以确定对药物或疫苗的一种或多种免疫应答、药物或疫苗的安全性质,或对疾病或病症和/或疾病或病症的一个或多个症状的作用。用于确定安全性概况的示例性方法包括测量毒性、最佳剂量浓度、抗体(即抗药物)应答、药物或疫苗的功效以及可能
的危险因素。此类药物或疫苗可以在此类非人类动物中进行改进和/或开发。
[0318]
疫苗功效可以多种方式确定。简言之,使用本领域已知的方法疫苗接种本文所述的非人动物,然后用疫苗攻击或将疫苗施用于已经感染的非人动物。一种或多种非人类动物对疫苗的应答可以通过以下方法进行测量:监测一种或多种非人类动物(或从它们分离的细胞),和/或对一种或多种非人类动物(或从它们分离的细胞)进行一种或多种测定以确定疫苗的功效。然后使用本领域已知的和/或本文所述的一种或多种测量,将一种或多种非人类动物对疫苗的应答与对照动物进行比较。
[0319]
疫苗功效还可以通过病毒中和测定来确定。简而言之,对如本文所述的非人类动物进行免疫,并且在免疫后的不同天数收集血清。将连续稀释的血清与病毒一起预温育,在此期间血清中对病毒具有特异性的抗体将与其结合。然后将病毒/血清混合物加入受纳细胞,以通过噬菌斑测定或微量中和测定来确定传染性。如果血清中的抗体中和病毒,则与对照组相比,存在较少的噬菌斑或较低的相对荧光素酶单位。
[0320]
如本文所述的非人动物提供了用于开发和表征用于在癌症和/或炎性疾病中使用的基于抗体的治疗剂的改进的体内系统。炎症长期以来一直与癌症相关(例如综述于grivennikov,s.i.等人,2010,cell 140:883
‑
99;rakoff
‑
nahoum,s.,2006,yale j.biol.med.79:123
‑
30,每篇文献以全文引用的方式并入本文)。事实上,发展中的肿瘤环境的特征部分在于各种炎症介质的浸润。此外,持续的炎症可导致发展中的癌症的更高概率。因此,在一些实施方案中,如本文所述的非人动物提供了用于开发和/或鉴定抗癌和/或抗炎治疗剂的体内系统。在一些实施方案中,可以将所提供的非人动物或对照非人动物(例如,具有与本文所述不同的遗传修饰或没有遗传修饰,即野生型)植入肿瘤(或肿瘤细胞),随后施用一种或多种候选治疗剂。在一些实施例中,候选治疗剂可包括多特异性抗体(例如双特异性抗体)或抗体混合物。在一些实施例中,候选治疗剂包括组合疗法,例如,序贯或同时给药的两种或更多种单特异性抗体的施用。在一种或多种候选治疗剂施用之前,可允许肿瘤在非人动物内的一个或多个位置中建立足够的时间。可在施用候选治疗之前和之后测量肿瘤细胞增殖、生长、存活等。也可根据需要在非人动物中测量候选治疗剂的细胞毒性。
[0321]
试剂盒
[0322]
本发明还提供包装或试剂盒,其包括装有至少一种本文所述的非人动物、非人细胞、dna片段和/或靶向载体的一个或多个容器。试剂盒可以用于任何适用的方法(例如,研究方法)。任选地与一个或多个此类容器相关的可以是由政府机构规定形式的注意事项,该注意事项规定药物或生物产品的制造、使用或销售,该注意事项反映了(a)机构关于用于人类施用的制造、使用或销售的批准,(b)使用说明或它们二者,或管理两个或更多个实体之间的材料和/或生物产品(例如,本文所述的非人动物或非人细胞)的转移的合约。
[0323]
本发明的其他特征将在以下对示例性实施例的描述的过程中显而易见,这些示例性实施例是为了说明而给出的,而无意限制本发明。
[0324]
本文还包括以下实施方式:
[0325]
实施方式1:一种包含工程化重链多样性(d
h
)基因区段的核苷酸分子,所述工程化重链多样性基因区段包含有效地连接至23聚体重组信号序列(rss)的至少一个d
h
基因区段。
[0326]
实施方式2:根据实施方式1所述的核苷酸分子,其中所述核苷酸序列包含工程化
d
h
区,所述工程化d
h
区包含(i)有效地连接至23聚体rss的至少一个d
h
基因区段和(ii)在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段,并且
[0327]
其中(i)所述至少一个有效地连接至23聚体rss的d
h
基因区段和(ii)所述在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss的未重排的d
h
基因区段被有效地连接,使得(i)和(ii)能够根据12/23规则在d
h
‑
d
h
重组事件中进行连接,
[0328]
任选地其中所述工程化d
h
区仅包含人d
h
基因区段。
[0329]
实施方式3:根据实施方式2所述的核苷酸分子,其中所述核苷酸分子还包含:
[0330]
(a)至少一个未重排的免疫球蛋白重链可变(v
h
)基因区段,其位于所述工程化d
h
区的上游并与之有效地连接,
[0331]
(b)至少一个未重排的免疫球蛋白重链连接(j
h
)基因区段,其位于所述工程化d
h
区的下游并与之有效地连接,或
[0332]
(c)(a)和(b)的组合。
[0333]
实施方式4:根据实施方式3所述的核苷酸分子,其中所述至少一个v
h
基因区段包含未重排的人v
h6‑
1基因区段,所述至少一个j
h
基因区段包含未重排的人j
h
6基因区段,或其组合。
[0334]
实施方式5:根据实施方式3或4所述的核苷酸分子,其中所述至少一个未重排的j
h
基因区段包含未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。
[0335]
实施方式6:根据实施方式3
‑
5中任一项所述的核苷酸分子,其中所述至少一个未重排的j
h
基因区段包含未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段,任选地其中所述未重排的人j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中。
[0336]
实施方式7:根据实施方式3
‑
6中任一项所述的核苷酸分子,其中至少一个未重排的v
h
基因区段包含任选地处于种系构型中的、跨越并包括未重排的人v
h3‑
74和未重排的人v
h1‑
6基因区段的功能性未重排的人v
h
基因区段的全部库。
[0337]
实施方式8:根据前述实施方式中任一项所述的核苷酸分子,其还包含一个或多个功能性啮齿动物adam6基因,任选地其中所述一个或多个功能性啮齿动物adam6基因位于人v
h1‑
2基因区段与人v
h6‑
1基因区段之间和/或替换人adam6基因。
[0338]
实施方式9:根据前述实施方式中任一项所述的核苷酸分子,其中所述23聚体rss与所述至少一个d
h
基因区段的5'端邻接。
[0339]
实施方式10:根据前述实施方式中任一项所述的核苷酸分子,其中所述23聚体rss与所述至少一个d
h
基因区段的3'端邻接。
[0340]
实施方式11:根据前述实施方式中任一项所述的核苷酸分子,其中所述至少一个有效地连接至23聚体rss的d
h
基因区段包含:
[0341]
(a)有效地连接至23聚体rss的人d
h3‑
3基因区段,任选地其中所述23聚体rss与所述d
h3‑
3基因区段的5'端邻接,
[0342]
(b)有效地连接至23聚体rss的人d
h2‑
2基因区段,任选地其中所述23聚体rss与所述d
h2‑
2基因区段的3'端邻接,
[0343]
(c)有效地连接至23聚体rss的人d
h2‑
8基因区段,任选地其中所述23聚体rss与所
述d
h2‑
8基因区段的3'端邻接,
[0344]
(d)有效地连接至23聚体rss的人2
‑
15基因区段,任选地其中所述23聚体rss与所述d
h2‑
15基因区段的3'端邻接,
[0345]
(e)(a)
‑
(d)的任何组合。
[0346]
实施方式12:根据前述实施方式中任一项所述的核苷酸分子,其包含含有如seq id no:52所示序列的核苷酸序列。
[0347]
实施方式13:根据实施方式1
‑
11中任一项所述的核苷酸分子,其包含含有如seq id no:61所示序列的核苷酸序列。
[0348]
实施方式14:根据实施方式1
‑
13中任一项所述的核苷酸分子,其包含含有如seq id no:70所示核苷酸序列的核苷酸序列。
[0349]
实施方式15:根据实施方式1
‑
14中任一项所述的核苷酸分子,其包含含有如seq id no:71所示核苷酸序列的核苷酸序列。
[0350]
实施方式16:根据实施方式1
‑
15中任一项所述的核苷酸分子,其包含含有如seq id no:72所示核苷酸序列的核苷酸序列。
[0351]
实施方式17:一种核苷酸分子,其从5'至3'在有效连接中包含:
[0352]
(a)一个或多个未重排的人v
h
基因区段;
[0353]
(b)从5'至3'包含以下项的工程化d
h
区
[0354]
(i)一个或多个未重排的人d
h
基因区段,其中所述一个或多个人d
h
基因区段中的每一个在其5’和3'端侧接有12聚体rss,以及
[0355]
(ii)包含在其5'端有效地连接至23聚体rss的人d
h3‑
3基因区段的有效地连接至23聚体rss的至少一个d
h
基因区段;和
[0356]
(c)一个或多个未重排的人j
h
基因区段。
[0357]
实施方式18:一种核苷酸分子,其从5'至3'在有效连接中包含:
[0358]
(a)一个或多个未重排的人v
h
基因区段;
[0359]
(b)工程化d
h
区,其中所述工程化d
h
区从5'至3’包含
[0360]
(i)有效地连接至23聚体rss的至少一个d
h
基因区段,包括在其3'端有效地连接至23聚体rss的至少一个人d
h
2基因区段,任选地其中在其3'端有效地连接至23聚体rss的所述至少一个人d
h
2基因区段包含在其3'端有效地连接至23聚体rss的人d
h2‑
2基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
8基因区段、在其3'端有效地连接至23聚体rss的人d
h2‑
15基因区段、或其任何组合,以及
[0361]
(ii)一个或多个人d
h
基因区段,其中所述一个或多个人d
h
基因区段中的每一个在其5'端和3'端侧接有12聚体rss;和
[0362]
(c)一个或多个未重排的人j
h
基因区段。
[0363]
实施方式19:根据实施方式17或实施方式18所述的核苷酸分子,其中所述一个或多个未重排的人v
h
基因区段从5’至3’包含未重排的人v
h1‑
2基因区段和未重排的人v
h6‑
1基因区段,其中所述核苷酸在所述未重排的人v
h1‑
2基因区段与所述未重排的人v
h6‑
1基因区段之间还包含一个或多个功能性啮齿动物adam6基因,并且其中所述未重排的人v
h1‑
2基因区段、所述一个或多个啮齿动物adam6基因和所述未重排的人v
h6‑
1基因区段是邻接的。
[0364]
实施方式20:根据实施方式17
‑
19中任一项所述的核苷酸分子,其中所述一个或多
个未重排的人v
h
基因区段包含任选地处于种系构型中的、跨越并包括未重排的人v
h3‑
74和未重排的人v
h1‑
6基因区段的功能性未重排的人v
h
基因区段的全部库。
[0365]
实施方式21:根据实施方式17
‑
20中任一项所述的核苷酸分子,其中所述一个或多个未重排的人j
h
基因区段包含未重排的人j
h
6基因区段。
[0366]
实施方式22:根据实施方式21所述的核苷酸分子,其中所述一个或多个未重排的人j
h
基因区段包含未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和所述未重排的人j
h
6基因区段。
[0367]
实施方式23:根据实施方式22所述的核苷酸分子,其中所述一个或多个未重排的人j
h
基因区段包含未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、所述未重排的人j
h
4基因区段、所述未重排的人j
h
5基因区段和所述未重排的人j
h
6基因区段,任选地其中所述未重排的人j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中。
[0368]
实施方式24:根据实施方式1
‑
23中任一项所述的核苷酸分子,其还在其3'端包含重链免疫球蛋白恒定区(c
h
)或其一部分。
[0369]
实施方式25:根据实施方式24所述的核苷酸分子,其中所述c
h
是啮齿动物c
h
区或其一部分。
[0370]
实施方式26:根据实施方式25所述的核苷酸分子,其中所述啮齿动物c
h
区或其一部分包含啮齿动物内含子增强子区和啮齿动物igm基因。
[0371]
实施方式27:根据实施方式1
‑
26中任一项所述的核苷酸分子,其还包含药物选择盒,
[0372]
其中所述药物选择盒位于有效地连接至23聚体rss的所述d
h
基因区段的上游,并且
[0373]
其中所述药物选择盒任选地侧翼为一个或多个位点特异性重组位点。
[0374]
实施方式28:一种包含根据实施方式1
‑
27中任一项所述的核苷酸分子的靶向载体,其包含被配置为允许与免疫球蛋白重链序列进行同源重组的5'
‑
和3'
‑
同源臂,任选地其中所述免疫球蛋白重链序列在内源性啮齿动物免疫球蛋白重链基因座处、包含人或人源化免疫球蛋白重链可变区、或其组合。
[0375]
实施方式29:一种修饰免疫球蛋白重链可变区以工程化d
h
‑
d
h
重组的方法,所述方法包括:
[0376]
获得包含含有一个或多个未重排的d
h
基因区段的d
h
区的免疫球蛋白重链可变区,所述未重排的d
h
基因区段中的每一个在一侧侧接有12聚体rss且在另一侧侧接有另一个12聚体rss,和
[0377]
修饰所述d
h
区以还包含有效地连接至23聚体rss的至少一个d
h
基因区段。
[0378]
实施方式30:根据实施方式29所述的方法,其中所述一个或多个未重排的d
h
基因区段包含一个或多个未重排的人d
h
基因区段。
[0379]
实施方式31:根据实施方式30所述的方法,其中所述一个或多个未重排的d
h
基因区段包含任选地处于种系构型中的跨越并包括所述种系人d
h1‑
1和所述种系人d
h7‑
27基因区段的所有功能性种系人d
h
基因区段。
[0380]
实施方式32:根据实施方式29
‑
31中任一项所述的方法,其中修饰包括
[0381]
(a)用有效地连接至23聚体rss的d
h
基因区段替换所述一个或多个未重排的d
h
基因
区段中的至少一个,
[0382]
(b)用23聚体rss替换在未重排的d
h
基因区段侧翼的两个12聚体rss中的至少一个,或
[0383]
(c)(a)和(b)的组合。
[0384]
实施方式33:根据实施方式32所述的方法,其中所述免疫球蛋白重链可变区还包含含有至少一个未重排的j
h
基因区段的j
h
区,
[0385]
其中所述j
h
区有效地连接至d
h
区,并且
[0386]
其中用有效地连接至所述23聚体rss的所述d
h
基因区段替换所述一个或多个未重排的d
h
基因区段中的至少一个包括缺失包含在所述j
h
区中的至少一个未重排的j
h
基因区段。
[0387]
实施方式34:根据实施方式33所述的方法,其中所述j
h
区包含含有人种系j
h
1基因区段、人种系j
h
2基因区段、人种系j
h
3基因区段、人种系j
h
4基因区段、人种系j
h
5基因区段和人种系j
h
6基因区段的人种系j
h
基因区段的全部库,任选地其中所述人种系j
h
1、j
h
2、j
h
3、j
h
4、j
h
5和j
h
6基因区段处于种系构型中,并且
[0388]
其中缺失包含在所述j
h
区中的至少一个种系j
h
基因区段包括缺失所述未重排的人j
h
1、j
h
2和j
h
3基因区段,以及任选地进一步缺失所述j
h
4和j
h
5基因区段。
[0389]
实施方式35:根据实施方式29至34中任一项所述的方法,其中有效地连接至23聚体rss的所述至少一个d
h
基因区段包含
[0390]
(a)有效地连接至23聚体rss的人d
h3‑
3基因区段,任选地其中所述23聚体rss与所述d
h3‑
3基因区段的5'端邻接,
[0391]
(b)有效地连接至23聚体rss的人d
h2‑
2基因区段,任选地其中所述23聚体rss与所述d
h2‑
2基因区段的3'端邻接,
[0392]
(c)有效地连接至23聚体rss的人d
h2‑
8基因区段,任选地其中所述23聚体rss与所述d
h2‑
8基因区段的3'端邻接,
[0393]
(d)有效地连接至23聚体rss的人
dh2
‑
15基因区段,任选地其中所述23聚体rss与所述d
h2‑
15基因区段的3'端邻接,
[0394]
(e)(a)
‑
(d)的任何组合。
[0395]
实施方式36:根据实施方式32
‑
35中任一项所述的方法,其中被替换的所述至少一个未重排的d
h
基因区段包含所述d
h
区的3’最末端未重排的d
h
基因区段。
[0396]
实施方式37:根据实施方式32
‑
36中任一项所述的方法,其中被替换的所述至少一个未重排的d
h
基因区段包含与有效地连接至23聚体rss的所述至少一个d
h
基因区段相对应的d
h
基因区段。
[0397]
实施方式38:一种免疫球蛋白重链基因座,其包含根据实施方式1
‑
27中任一项所述的核苷酸分子、根据实施方式28所述的靶向载体或根据实施方式29
‑
37中任一项所述的方法修饰的所述免疫球蛋白重链可变区。
[0398]
实施方式39:一种啮齿动物基因组,其包含根据实施方式1
‑
27中任一项所述的核酸、根据实施方式28所述的靶向载体、根据实施方式29
‑
37中任一项所述的方法修饰的所述免疫球蛋白重链可变区、或根据实施方式38所述的免疫球蛋白重链基因座,其中所述啮齿动物基因组任选地是啮齿动物种系基因组。
[0399]
实施方式40:一种包含免疫球蛋白重链可变区的啮齿动物种系基因组,所述免疫球蛋白重链可变区包含:
[0400]
(i)未重排的重链可变(v
h
)基因区段,
[0401]
(ii)工程化重链可变区多样性(d
h
)区,其中所述工程化d
h
区包含一个或多个种系d
h
基因区段和有效地连接至23聚体重组信号序列(rss)的一个或多个d
h
基因区段,以及
[0402]
(iii)未重排的重链连接(j
h
)基因区段,
[0403]
其中(i)
‑
(iii)处于有效连接中,使得在重组后所述免疫球蛋白重链可变区包含编码免疫球蛋白重链可变结构域的重排的重链可变区序列,任选地其中所述重排的重链可变区序列在v
h
(d
h
‑
d
h
)j
h
重组事件之后形成。
[0404]
实施方式41:根据实施方式40所述的啮齿动物种系基因组,其中有效地连接至23聚体重组信号序列(rss)的所述一个或多个d
h
基因区段包含有效地连接至3’23聚体rss的d
h
区段。
[0405]
实施方式42:根据实施方式40或实施方式41所述的啮齿动物种系基因组,其中有效地连接至23聚体重组信号序列(rss)的所述一个或多个d
h
基因区段包含有效地连接至5’23聚体rss的d
h
基因区段。
[0406]
实施方式43:根据实施方式40
‑
42中任一项所述的啮齿动物种系基因组,其中所述免疫球蛋白重链可变区是仅包含人v
h
、d
h
和j
h
基因区段的人免疫球蛋白重链可变区。
[0407]
实施方式44:根据实施方式43所述的啮齿动物种系基因组,其中所述人免疫球蛋白重链可变区有效地连接至免疫球蛋白重链恒定区。
[0408]
实施方式45:根据实施方式44所述的啮齿动物种系基因组,其中所述免疫球蛋白重链恒定区是内源性啮齿动物免疫球蛋白重链恒定区,任选地在内源性啮齿动物免疫球蛋白重链基因座处。
[0409]
实施方式46:根据实施方式40
‑
45中任一项所述的啮齿动物种系基因组,其中所述未重排的v
h
基因区段包含任选地处于种系构型中的跨越并包括v
h3‑
74至v
h6‑
1的功能性种系人v
h
基因区段的全部库。
[0410]
实施方式47:根据实施方式40
‑
46中任一项所述的啮齿动物种系基因组,其中所述未重排的重链j
h
基因区段包含人j
h
6基因区段。
[0411]
实施方式48:根据实施方式40
‑
47中任一项所述的啮齿动物种系基因组,其中啮齿动物种系基因组缺乏内源性adam6基因。
[0412]
实施方式49:根据实施方式40
‑
47中任一项所述的啮齿动物种系基因组,其还包含一个或多个啮齿动物adam6基因,任选地其中所述一个或多个啮齿动物内源性adam6基因包含内源性啮齿动物adam6基因。
[0413]
实施方式50:根据实施方式49所述的啮齿动物种系基因组,其中所述一个或多个啮齿动物adam6基因被插入两个人v
h
基因区段之间。
[0414]
实施方式51:根据实施方式50所述的啮齿动物种系基因组,其中所述一个或多个啮齿动物adam6基因被插入人v
h1‑
2基因区段与人v
h6‑
1基因区段之间。
[0415]
实施方式52:根据实施方式49所述的啮齿动物种系基因组,其中所述一个或多个一个或多个啮齿动物adam6基因被插入人adam6假基因的位置。
[0416]
实施方式53:根据实施方式49所述的啮齿动物种系基因组,其中所述一个或多个
一个或多个啮齿动物adam6基因被插入人v
h
基因区段与人d
h
基因区段之间。
[0417]
实施方式54:根据实施方式39
‑
53中任一项所述的啮齿动物种系基因组,其还包含末端脱氧核苷酸转移酶基因。
[0418]
实施方式55:根据实施方式39
‑
54中任一项所述的啮齿动物种系基因组,其特征在于其对于所述工程化d
h
区是纯合的。
[0419]
实施方式56:根据实施方式39
‑
54中任一项所述的啮齿动物种系基因组,其特征在于其对于所述工程化d
h
区是杂合的。
[0420]
实施方式57:根据实施方式39
‑
56中任一项所述的啮齿动物种系基因组,其中所述啮齿动物是大鼠或小鼠。
[0421]
实施方式58:一种啮齿动物或啮齿动物细胞,所述啮齿动物或啮齿动物细胞包含根据实施方式39
‑
57中任一项所述的啮齿动物种系基因组。
[0422]
实施方式59:根据实施方式58所述的啮齿动物或啮齿动物细胞,其中所述啮齿动物或啮齿动物细胞是大鼠、小鼠、大鼠细胞或小鼠细胞。
[0423]
实施方式60:根据实施方式58或实施方式59所述的啮齿动物或啮齿动物细胞,其中所述啮齿动物细胞是啮齿动物胚胎干细胞。
[0424]
实施方式61:一种啮齿动物或啮齿动物胚胎,所述啮齿动物或啮齿动物胚胎由根据实施方式60所述的啮齿动物胚胎干细胞产生。
[0425]
实施方式62:根据实施方式58
‑
61中任一项所述的啮齿动物、啮齿动物胚胎或啮齿动物细胞,其还包含体细胞基因组,所述体细胞基因组包含重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,
[0426]
任选地其中所述重排的重链v
h
(d
h
a
‑
d
h
b)j
h
基因区段有效地连接至igm恒定区基因序列和/或其中d
h
a或d
h
b衍生自有效地连接至23聚体rss的d
h
基因区段或其一部分,并且d
h
a或d
h
b的至少9个碱基对与有效地连接至23聚体rss的d
h
基因区段或其一部分的至少9个碱基对碱基对和其每个相同。
[0427]
实施方式63:根据实施方式58
‑
62中任一项所述的啮齿动物,其中所述啮齿动物中所有重排的重链vdj编码序列的至少95%具有至少10个氨基酸的cdr3长度,任选地其中所述啮齿动物中所有重排的重链vdj基因序列的至少70%具有至少11个氨基酸的cdr3长度,任选地所述啮齿动物中所有重排的重链vdj基因序列的至少15%具有至少14个氨基酸的cdr3长度。
[0428]
实施方式64:根据实施方式58
‑
63中任一项所述的啮齿动物,其特征在于,与在参考啮齿动物中的d
h
‑
d
h
重组的频率相比,所述啮齿动物表现出至少3倍增加的d
h
‑
d
h
重组频率。
[0429]
实施方式65:一种制备基因组包含工程化d
h
区的啮齿动物的方法,所述方法包括从根据实施方式60所述的胚胎干细胞中产生啮齿动物。
[0430]
实施方式66:一种制备基因组包含工程化d
h
区的啮齿动物的方法,所述方法包括
[0431]
(a)修饰啮齿动物胚胎干细胞的基因组使其包含含有各自有效地连接至23聚体rss的一个或多个d
h
基因区段的dna片段,任选地其中所述dna片段包含根据实施方式1
‑
27中任一项所述的核苷酸分子、根据实施方式28所述的靶向载体、根据实施方式30
‑
37中任一项所述的方法修饰的免疫球蛋白重链可变区或根据实施方式38所述的免疫球蛋白重链,和
[0432]
(b)使用(a)的经修饰的啮齿动物胚胎干细胞产生啮齿动物。
[0433]
实施方式67:一种制备基因组包含工程化d
h
区的啮齿动物的方法,所述方法包括
[0434]
修饰免疫球蛋白重链可变区的未重排的d
h
区使其包含有效地连接至23聚rss的至少一个d
h
区段,其中所述未重排的d
h
区还包含一个或多个种系d
h
基因区段,
[0435]
从而制备所述啮齿动物。
[0436]
实施方式68:根据实施方式67所述的方法,其中修饰包括用有效地连接至23聚体rss的所述至少一个d
h
基因区段替换所述一个或多个未重排的人d
h
基因区段,以及任选地替换一个或多个j
h
基因区段。
[0437]
实施方式69:根据实施方式67或实施方式68所述的方法,其中所述免疫球蛋白重链可变区是人免疫球蛋白重链可变区,任选地其中所述人免疫球蛋白重链可变区包含含有至少一个v
h
基因区段的未重排的人免疫球蛋白重链v
h
基因簇、含有一个或多个未重排的人d
h
基因区段的未重排的人免疫球蛋白重链d
h
区、以及含有至少一个未重排的人j
h
基因区段的未重排的人免疫球蛋白重链j
h
基因簇,其中所述未重排的人免疫球蛋白重链d
h
区被修饰以包含有效地连接至23聚体rss的至少一个d
h
基因区段。
[0438]
实施方式70:根据实施方式69所述的方法,其中所述修饰步骤导致包含以下的免疫球蛋白重链可变区
[0439]
(i)功能性人v
h
基因区段的全部库,任选地所有所述功能性人v
h
基因区段跨越并包括v
h3‑
74至v
h6‑
1,任选地其中所有所述功能性v
h
基因区段被定位于种系构型中,
[0440]
(ii)未重排的人d
h
基因区段的全部库,但被有效地连接至23聚体rss的所述至少一个d
h
基因区段替换的d
h7‑
27除外,以及
[0441]
(iii)至少一个未重排的人j
h
6基因区段,和任选地至少一个未重排的人j
h
4基因区段、一个未重排的人j
h
5基因区段和一个未重排的人j
h
6基因区段。
[0442]
实施方式71:根据实施方式70所述的方法,其中所述有效地连接至23聚体rss的所述至少一个d
h
基因区段包含有效地连接至5
’‑
23聚体rss的d
h3‑
3基因区段。
[0443]
实施方式72:根据实施方式69所述的方法,其中所述修饰步骤导致包含以下的免疫球蛋白重链可变区
[0444]
(i)功能性人v
h
基因区段的全部库,任选地所有功能性v
h
基因区段跨越并包括v
h3‑
74至v
h6‑
1,任选地其中所有所述功能性v
h
基因区段被定位于种系构型中,
[0445]
(ii)未重排的人d
h
基因区段的全部库,但其每一个被至少一个有效地连接至23聚体rss的d
h
基因区段替换的未重排的d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段除外,和
[0446]
(iii)未重排的人j
h
基因区段的全部库,任选地未重排的人j
h
1基因区段、未重排的人j
h
2基因区段、未重排的人j
h
3基因区段、未重排的人j
h
4基因区段、未重排的人j
h
5基因区段和未重排的人j
h
6基因区段。
[0447]
实施方式73:根据实施方式72所述的方法,其中有效地连接至23聚体rss的所述至少一个d
h
基因区段包含有效地连接至3’23聚体rss的人d
h2‑
2基因区段、有效地连接至3’23聚体rss的d
h2‑
8基因区段、或有效地连接至3’23聚体rss的人d
h2‑
15基因区段,任选地其中所述未重排的d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段分别被替换为有效地连接至3'端23聚体rss的人d
h2‑
2基因区段、有效地连接至3'端23聚体rss的人d
h2‑
8基因区段、和有效地连接至3'端23聚体rss的人d
h2‑
15基因区段。
[0448]
实施方式74:根据实施方式67
‑
73中任一项所述的方法,其中所述免疫球蛋白重链可变区
[0449]
(a)还包含一个或多个啮齿动物adam6基因,任选地其中所述一个或多个啮齿动物adam6基因位于两个未重排的v
h
基因区段之间,任选地在未重排的人v
h1‑
2基因区段与未重排的人v
h6‑
1基因区段之间,和/或
[0450]
(b)有效地连接至免疫球蛋白重链恒定区,任选地其中所述免疫球蛋白重链恒定区是内源性啮齿动物免疫球蛋白重链恒定区,任选地在内源性免疫球蛋白重链基因座处的内源性啮齿动物免疫球蛋白重链恒定区。
[0451]
实施方式75:根据实施方式65
‑
74中任一项所述的方法,其中所述啮齿动物是大鼠或小鼠。
[0452]
实施方式76:一种产生抗体或获得编码所述抗体的核酸的方法,所述方法包括
[0453]
用抗原免疫啮齿动物,所述啮齿动物包含种系基因组,所述种系基因组包含含有各自有效地连接至23聚体rss的一个或多个d
h
区段的工程化d
h
区,其中所述啮齿动物是根据实施方式58
‑
64中任一项所述的啮齿动物,和
[0454]
允许所述啮齿动物对所述抗原产生免疫应答,包括结合抗原的抗体或编码所述抗体的核酸。
[0455]
实施方式77:根据实施方式76所述的方法,其还包括从所述啮齿动物或啮齿动物细胞回收所述抗体或编码所述抗体的核酸。
[0456]
实施方式78:根据实施方式76所述的方法,其中所述啮齿动物细胞是b细胞或杂交瘤。
[0457]
实施方式79:根据实施方式76
‑
78中任一项所述的方法,其中各自有效地连接至23聚体rss的一个或多个d
h
区段包含有效地连接至5’23聚体rss的d
h
基因区段。
[0458]
实施方式80:根据实施方式76
‑
79中任一项所述的方法,其中各自有效地连接至23聚体rss的所述一个或多个d
h
区段包含有效地连接至3’23聚体rss的d
h
基因区段。
[0459]
实施方式81:根据实施方式76
‑
80中任一项所述的方法,其中所述啮齿动物是大鼠或小鼠。
[0460]
实施方式82:一种啮齿动物基因组、核酸或免疫球蛋白基因座,其包含有效地连接至啮齿动物重链恒定区基因序列的重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列,任选地其中由于d
h
a和d
h
b中的每一个分别显示与第一和第二种系d
h
基因区段具有40%的同一性、最多1个核苷酸突变,所以所述重排的重链在体细胞上是超突变的和/或被确定为是v
h
(d
h
a
‑
d
h
b)j
h
编码序列。
[0461]
实施方式83:根据实施方式82所述的啮齿动物基因组、核酸或免疫球蛋白基因座,其中所述d
h
b基因区段源自人种系d
h3‑
3基因区段。
[0462]
实施方式84:根据实施方式82所述的啮齿动物基因组、核酸或免疫球蛋白基因座,其中所述d
h
a基因区段源自人种系d
h2‑
2、d
h2‑
8或d
h2‑
15基因区段。
[0463]
实施方式85:根据实施方式82
‑
84中任一项所述的啮齿动物基因组、核酸或免疫球蛋白基因座,其中所述重排的重链v
h
(d
h
a
‑
d
h
b)j
h
编码序列编码20个以上氨基酸的cdr3长度。
[0464]
实施方式86:根据实施方式82
‑
85中任一项所述的啮齿动物基因组、核酸或免疫球
蛋白基因座,其中所述j
h
基因区段源自人种系j
h
6基因区段。
[0465]
实施方式87:一种啮齿动物或啮齿动物细胞,其包含根据实施方式82
‑
86中任一项所述的基因组、核酸或免疫球蛋白基因座。
[0466]
实施方式88:根据实施方式87所述的啮齿动物或啮齿动物细胞,其中所述啮齿动物是大鼠或小鼠或者所述啮齿动物细胞是大鼠细胞或小鼠细胞。
[0467]
实施方式89:根据实施方式87或实施方式88所述的啮齿动物或啮齿动物细胞,其中所述啮齿动物细胞是啮齿动物b细胞。
[0468]
实施方式90:一种杂交瘤,其包含与骨髓瘤细胞融合的根据实施方式89所述的啮齿动物b细胞。
[0469]
实施例
[0470]
以下实施例的提供是为了向所属领域的技术人员描述如何制备和使用本发明的方法和组合物,而非希望限制本发明人视为其发明的范围。除非另外指明,否则温度用摄氏度说明,且压力是或接近大气压。
[0471]
实施例1.靶向载体设计与构建
[0472]
本实施例说明了用于插入非人动物诸如啮齿动物(例如小鼠)的基因组内的靶向载体的构建。特别地,在本实施例中所描述的方法展示了用于插入啮齿动物(例如小鼠)胚胎干(es)细胞的基因组中以产生啮齿动物的靶向载体的产生,所述啮齿动物的基因组包含免疫球蛋白重链可变区,所述免疫球蛋白重链可变区包括工程化重链多样性(d
h
)区,所述工程化d
h
区包括各自有效地连接至5’或3’23聚体rss的一个或多个d
h
区段。在本实施例中,描述了三种靶向载体:含有包括有效地连接至5’23聚体rss并有效地连接至一个人j
h
区段的近端(或3’)d
h
区段的工程化d
h
区的第一靶向载体,含有包括有效地连接至5’23聚体rss并有效地连接至三个人j
h
区段的近端(或3’)d
h
区段的工程化d
h
区的第二靶向载体,和含有包括各自与3’23聚体rss关联并有效地连接至六个人j
h
区段的三个d
h
区段的工程化d
h
区的第三靶向载体(图2)。产生这些靶向载体中的每一个并将其分别插入人源化免疫球蛋白重链可变区中(图3、5、7)。如下所述,将工程化d
h
区放置成与重链可变区(v
h
)和重链连接(j
h
)区段有效地连接,使得在vdj重组后,具有由d
h
‑
d
h
重组产生的cdr3的抗体得以表达。
[0473]
使用velocigene技术(参见例如,美国专利号6,586,251和valenzuela等人,2003,nature biotech.21(6):652
‑
659;每篇文献以全文引用的方式并入本文)和本领域已知的分子生物学技术来创建含有用于插入免疫球蛋白重链可变区中的各自与5’或3’23聚体rss关联的一个或多个人d
h
区段的靶向载体。在本实施例中所描述的方法可以根据需要用于利用任何一个d
h
区段、d
h
区段的集合或d
h
区段的组合。
[0474]
a.23:d
h3‑
3:12/j
h
6靶向载体(图2)
[0475]
简言之,使用含有多个人d
h
区段和定位于人d
h7‑
27位置的合成的人d
h3‑
3区段的基因组dna片段来构建第一靶向载体。体外cas9/ga修饰的供体通过从头合成(blue heron bio)制备并且从5’至3’包含:(a)从d
h7‑
27的5’12聚体rss的上游350bp开始的100bp同源臂,(b)用于插入新霉素抗性盒的agei和xhoi位点,(c)d
h7‑
27的5'端12rss上游的250bp区,(d)工程化为具有5'端23聚体rss(来自j
h
4)和3'端12聚体rss(来自d
h3‑
3)的合成的人d
h3‑
3区段,以及(3)从j
h
5下游3bp开始的100bp同源盒。loxp
‑
ubc
‑
em7
‑
neo
‑
loxp盒(例如侧翼为loxp位点特异性重组识别位点的新霉素抗性基因)通过连接到agei和xhoi位点中被定位于
合成的d
h
区段上游约250bp和下游,以允许在大肠杆菌和小鼠es细胞中进行选择。将包括新霉素盒的此23:d
h3‑
3:12/j
h
6供体(seq id no:61)用于通过使用两个cas9:grna复合物的体外cas9/ga修饰bac。在修饰之前,bac在序列上与小鼠的嵌合igh基因座相同(参见例如图3和图4,其显示对于包含缺乏j
h
基因区段并有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的6394等位基因和包含有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的1460等位基因为杂合的小鼠的示例性非限制性内源性免疫球蛋白重链基因座)。具体地,bac与从最近端人v
h
基因(v
h6‑
1)开始并包括所有27个人d
h
基因、所有6个人j
h
基因、小鼠igh内含子增强子(eμ)、小鼠igm开关区(sμ)和小鼠igm基因的前4个外显子的1460等位基因相同。bac还包括壮观霉素(spec)抗性盒和在v
h6‑
1基因上游的约29kb的人基因间序列。人
‑
小鼠接头是人j
h
6基因的3’222bp和小鼠eμ增强子的5’490bp。通过ga将23:d3
‑
3:12/j
h
6供体插入bac中导致包含d
h7‑
7基因区段经工程化23:d3
‑
3:12区段的替换和j
h
1、j
h
2、j
h
3、j
h
4和j
h
5基因区段的缺失的最终23:d3
‑
3:12/j
h
6靶向载体(图2)。表1提供了用于确定23:d
h3‑
3:12/j
h
6靶向载体的准确构建的grna、引物和探针的序列。
[0476]
表1:用于构建23:d
h3‑
3:12/j
h
6靶向载体的引物和grna序列
[0477][0478][0479]
将23:d3
‑
3:12/jh6靶向载体用noti线性化,并电穿孔到小鼠胚胎干细胞中,所述小鼠胚胎干细胞的基因组对于以下等位基因是杂合的:人源化免疫球蛋白重链可变区(即,第一重链等位基因(1460het),所述第一重链等位基因含有与包括啮齿动物重链增强子和调控区的啮齿动物免疫球蛋白重链恒定区有效地连接的多个人v
h
、d
h
和j
h
区段并且含有编码一个或多个鼠adam6基因的插入核苷酸序列(例如,美国专利号8,642,835和8,697,940,每个专利以全文引用的方式并入本文);和第二重链等位基因(6394het),所述第二重链等位基因含有多个人v
h
和d
h
区段、一个j
h
区缺失和包括啮齿动物重链增强子和调控区的啮齿
动物免疫球蛋白重链恒定区并且含有编码一个或多个鼠adam6基因的插入核苷酸序列(例如,美国专利号8,642,835和8,697,940,每个专利以全文引用的方式并入本文);并且所述小鼠胚胎干细胞的基因组对于以下基因是纯合的(ho):包含与内源性小鼠免疫球蛋白重链cκ区(1293)有效地连接的人免疫球蛋白轻链vκ和jκ基因区段的全部库的人源化内源性κ基因座(参见图3)。6799等位基因是通过电穿孔和将1460等位基因与包含新霉素盒的23:d3
‑
3:12/j
h
6靶向载体正确同源重组而创建的。(图3)。将对6394和679等位基因杂合的这些工程化小鼠es细胞用于促进对阳性es克隆的有效筛选(参见下文),并且随后对药物抗性盒进行cre介导的去除,之后缺失6394和6799等位基因分别被称为6643和6800(图4)。
[0480]
b.23:d
h3‑
3:12/j
h4‑
6靶向载体(图2)
[0481]
以类似的方式,使用含有多个人d
h
区段和定位于人d
h7‑
27位置的合成的人d
h3‑
3区段的相同的基因组dna片段来构建另一个靶向载体(23:d
h3‑
3:12/j
h4‑
6)。然而,此第二靶向载体包括六个人j
h
区段中的三个(即、j
h
4、j
h
5、j
h
6)。为了创建最终的23:d
h3‑
3:12/j
h4‑
6靶向载体,使用供体来修饰在序列上与小鼠的嵌合igh基因座相同的bac(参见例如图3和图4,其显示对于包含缺乏j
h
基因区段并有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的6394等位基因和包含有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的1460等位基因为杂合的小鼠的示例性非限制性内源性免疫球蛋白重链基因座)。供体从5’至3’包含:(a)从d7
‑
27的5’端12聚体rss的上游350bp开始的100bp同源盒,(b)用于插入新霉素抗性盒的agei和xhoi位点,(c)d7
‑
27的5'端12rss上游的250bp区,(d)5'侧接有23聚体rss(来自j
h
4)和3'侧接有12聚体rss(来自d
h3‑
3)的合成的人d
h3‑
3区段,以及(e)从j
h
3下游3bp开始的100bp同源盒。loxp
‑
ubc
‑
em7
‑
neo
‑
loxp盒(例如侧翼为loxp位点特异性重组识别位点的新霉素抗性基因)通过连接到agei和xhoi位点中被定位于合成的d
h
区段上游约250bp,以允许在大肠杆菌和小鼠es细胞中进行选择。将包括新霉素盒的包含如seq id no:52所示核苷酸序列的此23:d3
‑
3:12/j
h4‑
6供体用于修饰在序列上与1460等位基因相同的bac(图3和4)。具体地,bac与从最近端人v
h
基因(v
h6‑
1)开始并包括所有27个人d
h
基因、所有6个人j
h
基因、小鼠igh内含子增强子(eμ)、小鼠igm开关区(sμ)和小鼠igm基因的前4个外显子的1460等位基因相同。bac还包括壮观霉素(spec)抗性盒和在v
h6‑
1基因上游的约29kb的人基因间序列。人
‑
小鼠接头是人j
h
6基因的3’222bp和小鼠eμ增强子的5’490bp。用两种cas9:grna复合物通过体外cas9/ga将23:d3
‑
3:12/j
h4‑
6供体插入bac中导致包含d
h7‑
7基因区段经工程化23:d3
‑
3:12区段的替换和j
h
1、j
h
2、和j
h
3基因区段的缺失的最终23:d3
‑
3:12/j
h4‑
6靶向载体(图2)。表2提供了用于确定23:d
h3‑
3:12/j
h
6靶向载体的准确构建的grna、引物和探针的序列。
[0482]
表2:用于构建23:d
h3‑
3:12/jh4
‑
6靶向载体的引物和grna序列
[0483][0484][0485]
将23:d3
‑
3:12/j
h4‑
6靶向载体也用noti线性化,并电穿孔到小鼠胚胎干细胞中,所述小鼠胚胎干细胞的基因组对于以下等位基因是杂合的:人源化免疫球蛋白重链可变区(即,第一重链等位基因(1460het),所述第一重链等位基因含有与包括啮齿动物重链增强子和调控区的啮齿动物免疫球蛋白重链恒定区有效地连接的多个人v
h
、d
h
和j
h
区段)并且含有编码一个或多个鼠adam6基因的插入核苷酸序列[例如,美国专利号8,642,835和8,697,940,每个专利以全文引用的方式并入];和第二重链等位基因(6394het),所述第二重链等位基因含有多个人v
h
和d
h
区段、一个j
h
区缺失和包括啮齿动物重链增强子和调控区的啮齿动物免疫球蛋白重链恒定区并且含有编码一个或多个鼠adam6基因的插入核苷酸序列[例如,美国专利号8,642,835和8,697,940,每个专利以引用的方式并入本文];并且所述小鼠胚胎干细胞的基因组对于以下基因是纯合的(ho):包含与内源性小鼠免疫球蛋白重链cκ区(1293)有效地连接的人免疫球蛋白轻链vκ和jκ基因区段的全部库的人源化内源性κ基因座(参见图5)。6797等位基因是通过电穿孔和将1460等位基因与包含新霉素盒的23:d3
‑
3:12/j
h4‑
6靶向载体正确同源重组而创建的。(图5)。将对6394和6797等位基因杂合的这些工程化小鼠es细胞用于促进对阳性es克隆的有效筛选(参见下文),并且随后对药物抗性盒进行cre介导的去除,之后缺失6394和6797等位基因分别被称为6643和6798(图6)。
[0486]
c.12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23/j
h1‑
6靶向载体(图2)
[0487]
简言之,使用含有包括各自具有一个12聚体5’rss和一个23聚体3’rss的三个d
h
2家族基因区段(d
h2‑
2、d
h2‑
8和d
h2‑
15)的多个人d
h
区段的dna片段来构建第三靶向载体。首先,bac在序列上与小鼠的嵌合igh基因座相同(参见例如图3和图4,其显示对于包含缺乏j
h
基因区段并有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的6394等位基因和包含有效地连接至内源性小鼠免疫球蛋白重链恒定区序列的人源化可变区的1460等位基因为杂合的小鼠的示例性非限制
性内源性免疫球蛋白重链基因座)。具体地,使用细菌同源重组(bhr)修饰与从最近端人v
h
基因(v
h6‑
1)开始并包括所有27个人d
h
基因、所有6个人j
h
基因、小鼠igh内含子增强子(eμ)、小鼠igm开关区(sμ)和小鼠igm基因的前4个外显子的1460等位基因相同的bac,以在第一人d
h
区段(d
h1‑
1)上游512bp插入loxp
‑
ubc
‑
em7
‑
neo
‑
loxp盒(例如侧翼为loxp位点特异性重组识别位点的新霉素抗性基因)用于在大肠杆菌和小鼠es细胞中进行选择。随后使用体外cas9/ga用三个供体修饰了此所得的bac。
[0488]
1.用于修饰d
h2‑
2的第一供体从5’至3’含有从d
h2‑
2的5'端12rss的上游1419bp开始的50bp同源盒、多克隆位点(mrei
‑
nsii
‑
ecori
‑
kpni
‑
mrei)、经修饰的d2
‑
2基因(其中3'端12聚体rss被从人v
h1‑
69衍生的经优化的3'端23聚体rss替换(cacagtgtga aaacccacat cctgagagtg acacaaacc;t
‑
>a、g
‑
>c;seq id no:151))、和在d2
‑
2的3'端23聚体rss下游863bp终止的50bp同源盒。用于修饰d
h2‑
2的此第一供体的核苷酸序列如seq id no:70所示。由于d
h
区由约10kb的四个正向重复序列组成,因此设计用于筛选的独特引物和探针极为困难。为了克服这个问题,插入了两个独特的40bp序列:一个在5'同源框的下游74bp和一个在3'同源框的上游40bp。将这些独特的40聚体用作pcr/测序引物和taqman探针的结合位点,由图2的未填充垂直矩形“1”和“2”表示,并包含分别如seq id no:73和seq id no:74所示的核苷酸序列。
[0489]
2的hcvr氨基酸序列。用于修饰d
h2‑
8的第二供体从5’至3’含有从d
h2‑
8的5'端12rss的上游552bp开始的50bp同源盒、多克隆位点(mrei
‑
nsii
‑
ecori
‑
kpni
‑
mrei)、经修饰的d2
‑
8基因(其中3'端12聚体rss被从人vh1
‑
69衍生的经优化的3'端23聚体rss替换(cacagtgtga aaacccacat cctgagagtg acacaaacc;t
‑
>a、g
‑
>c;seq id no:151))、和在d2
‑
8的3'端23聚体rss下游867bp终止的50bp同源盒。用于修饰d
h2‑
8的此第二供体的核苷酸序列如seq id no:71所示。由于d
h
区由约10kb的四个正向重复序列组成,因此设计用于筛选的独特引物和探针极为困难。为了克服这个问题,插入了两个独特的40bp序列:一个在5'同源框的下游74bp和一个在3'同源框的上游40bp。将这些独特的40聚体用作pcr/测序引物和taqman探针的结合位点,由图2的未填充垂直矩形“10”和“16”表示,并包含分别如seq id no:75和seq id no:76所示的核苷酸序列。
[0490]
3.用于修饰d
h2‑
15的第三供体从5’至3’含有从d
h2‑
15的5'端12rss的上游391bp开始的50bp同源盒、多克隆位点(mrei
‑
nsii
‑
ecori
‑
kpni
‑
mrei)、经修饰的d2
‑
15基因(其中3'端12聚体rss被从人v
h1‑
69衍生的经优化的3'端23聚体rss替换(cacagtgtga aaacccacat cctgagagtg acacaaacc;t
‑
>a、g
‑
>c;seq id no:151))、和在d2
‑
15的3'端23聚体rss下游867bp终止的50bp同源盒。用于修饰d
h2‑
2的此第三供体的核苷酸序列如seq id no:72所示。由于d
h
区由约10kb的四个正向重复序列组成,因此设计用于筛选的独特引物和探针极为困难。为了克服这个问题,插入了两个独特的40bp序列:一个在5'同源框的下游74bp和一个在3'同源框的上游40bp。将这些独特的40聚体用作pcr/测序引物和taqman探针的结合位点,由图2的未填充垂直矩形“8”和“18”表示,并包含分别如seq id no:77和seq id no:78所示的核苷酸序列。
[0491]
在用三个供体进行体外cas9/ga修饰之后,最终的靶向载体从5’至3’包含:含有人可变区dna的49kb 5’同源臂、新霉素选择盒、包括各自5’侧接有12聚体rss且3’侧接有23聚体rss的三个人dh区段的工程化人d
h
区、六个人j
h
区段、以及含有小鼠重链内含子增强子
(ei)和小鼠igm恒定区基因的24kb3’同源臂。(图2)。表3提供了用于确定12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23/j
h1‑
6靶向载体的准确构建的grna、引物和探针的序列。
[0492]
表3:用于构建12:dh2
‑
2:23|12:dh2
‑
8:23|12:dh2
‑
15:23/jh1
‑
6的引物和grna序列
[0493]
[0494]
[0495]
[0496]
[0497][0498][0499]
dna引入小鼠胚胎干(es)细胞内,随后在选择培养基中进行培养。图3、图5和图7分别描绘了用于对每个靶向载体电穿孔的es细胞的基因组。如上文所述在电穿孔后10天挑选抗药性集落,并且使用检测工程化d
h
基因区段的正确整合的引物/探针组(表4;f:正向引物,p:探针,r:反向引物)通过taqman和核型分析筛选正确的靶向(valenzuela等人,出处同上;frendewey,d.等人,2010,methods enzymol.476:295
‑
307;所述文献以全文引用的方式并入本文)。
[0505]
使用方法(dechiara,t.m.等人,2010,methods enzymol.476:285
‑
294;dechiara,t.m.,2009,methods mol.biol.530:311
‑
324;poueymirou等人,2007,nat.biotechnol.25:91
‑
99;所述文献以全文引用的方式并入本文),其中将被靶向的es细胞注射到未压实的8细胞期swiss webster胚胎内,以产生对于工程化d
h
区而言是杂合的并表达包含包括由d
h
‑
d
h
重组产生的cdr3区的重链可变区的抗体的健康的完全es细胞来源的f0代小鼠。使f0代杂合子雄性与c57bl6/ntac雌性交配产生f1杂合子,所述f1杂合子杂交以产生f2代纯合子,并且与野生型小鼠交配。
[0506]
药物选择盒可以任选地通过随后添加重组酶(例如,通过cre处理)或通过繁殖成cre缺失子小鼠品系而去除(参见例如,国际专利申请公开号wo2009/114400,以全文引用的方式并入本文),以便除去例如在es细胞阶段或在胚胎中未被去除的、由靶向构建体引入的任何lox选择盒。任选地,选择盒保留在小鼠中。通过瞬时表达cre重组酶,在阳性es细胞中去除被工程化到本文所述靶向载体中的选择盒(分别参见图4、图6和图8)。
[0507]
表4.用于es细胞筛选的引物/探针集
[0508]
[0509][0510]
实施例3.对用23:d
h3‑
3:12/j
h
6、23:d
h3‑
3:12/j
h4‑
6、或12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23/j
h1‑
6靶向载体修饰的小鼠的表征
[0511]
免疫表型分型
[0512]
针对对于相应6800或6795修饰的等位基因杂合的小鼠进行了用23:d
h3‑
3:12/j
h
6或23:d
h3‑
3:12/j
h4‑
6靶向载体修饰的动物的免疫表型分型分析(参见图4和图6)。针对繁殖成对于20188修饰的等位基因呈纯合性的小鼠进行了用12:d
h2‑
2:23|12:d
h2‑
8:2
‑
23|12:d
h2‑
15:23/j
h1‑
6靶向载体修饰的动物的免疫表型分型分析。通过荧光激活细胞分选(facs)分析了在这些动物中的b细胞发育。简言之,脾脏和腿骨(股骨和胫骨)采集自:
[0513]
velocimmune小鼠(n=3,26%c57bl/6 23%129s6/svevtac 51%balb/canntac;参见例如,美国专利号8,502,018和8,642,835),
[0514]
用23:d
h3‑
3:12/j
h
6靶向载体修饰的6643het/6800het//1293ho小鼠(25%c57bl/
6ntac 25%129s6/svevtac 50%balb/canntac);参见图4;n=3;
[0515]
用23:d
h3‑
3:12/j
h4‑
6靶向载体修饰的6643het/6798het//1293ho小鼠(25%c57bl/6ntac 25%129s6/svevtac 50%balb/canntac);参见图6;n=3);或
[0516]
用12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h
2.1523/j
h1‑
6靶向载体修饰的20188ho/1293ho小鼠(25%c57bl/6ntac 25%129s6/svfvtac 50%balb/canntac);n=3)。
[0517]
通过离心从股骨中收集骨髓。用ack裂解缓冲液(gibco)裂解来自脾和骨髓制备物的红血细胞,随后用含2%fbs的1xpbs洗涤。将分离的细胞(1x106)与选定抗体混合物一起在+4℃下孵育30分钟:染色1:大鼠抗小鼠cd43
‑
fitc(biolegend 121206,克隆1b11),大鼠抗小鼠c
‑
kit
‑
pe(biolegend 105808,克隆2b8),大鼠抗小鼠igm
‑
pecy(ebiosciences 25
‑
5790
‑
82,克隆ii/41),大鼠抗小鼠igd
‑
percp
‑
cy5.5(biolegend 405710,克隆11
‑
26c.2a),大鼠抗小鼠cd3
‑
pb(biolegend 100214,克隆17
‑
a2),大鼠抗小鼠b220
‑
apc(ebiosciences 17
‑
0452
‑
82,克隆ra3
‑
6b2),以及大鼠抗小鼠cd19
‑
apc
‑
h7(bd 560143克隆1d3)。染色2:大鼠抗小鼠κ
‑
fitc(bd 550003,克隆187.1),大鼠抗小鼠λ
‑
pe(biolegend 407308,克隆rml
‑
42),大鼠抗小鼠igm
‑
pecy(ebiosciences 25
‑
5790
‑
82,克隆ii/41),大鼠抗小鼠igd
‑
percp
‑
cy5.5(biolegend 405710,克隆11
‑
26c.2a),大鼠抗小鼠cd3
‑
pb(biolegend100214,克隆17
‑
a2),大鼠抗小鼠b220
‑
apc(ebiosciences 17
‑
0452
‑
82,克隆ra3
‑
6b2),以及大鼠抗小鼠cd19
‑
apc
‑
h7(bd 560143克隆1d3)。在染色后,将细胞洗涤并然后在2%甲醛中固定。数据采集在bd lsrfortessa流式细胞仪(bd biosciences)上进行,并用flowjo软件(bd biosciences)进行分析。
[0518]
与对照小鼠相比,在对于6800或6798等位基因杂合的小鼠中,在脾脏和骨髓中的总b细胞数量均减少,并且在骨髓中观察到的祖b细胞有所增加(数据未显示)。总体而言,b细胞具有相似的κ和λ使用(数据未显示)。在对于20188等位基因纯合的小鼠中,看到脾脏中的λ
+
b细胞水平略高(数据未显示)。与对照小鼠相比,在表达6800、6798或20188等位基因的小鼠的b细胞群中没有观察到差异被认为影响这些动物的b细胞发育(数据未显示)。
[0519]
d
h
‑
d
h
重排的频率和特性
[0520]
通过igm库测序分析用23:d
h3‑
3:12/j
h
6靶向载体、23:d
h3‑
3:12/j
h4‑
6靶向载体、或12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体修饰的未免疫的原代小鼠中的基因重排。使用对小鼠恒定igm特异的引物(表5,“nnnnnn”代表使得能够复用测序样品的6bp索引序列),使用race(cdna末端的快速扩增)cdna扩增试剂盒(clontech)制备来自脾脏b细胞的igm库文库。然后在miseq测序仪(illumina)上对所制备的库文库进行测序。
[0521]
基于质量和与重链igm恒定区引物的完美匹配,将illumina miseq配对末端序列(2x300个循环)合并并过滤。将重排的重链序列与种系v、d和j参考数据库(imgt)进行比对。随后的分析仅包括生产性重排,其定义为在开放阅读框和框内vdj连接内的无终止密码子的序列。
[0522]
表5:用于igm库测序的文库制备中使用的引物
[0523][0524]
在用23:d
h3‑
3:12/j
h
6靶向载体或23:d
h3‑
3:12/j
h4‑
6靶向载体修饰的未免疫的动物中,没有检测到d
h7‑
27的表达,并且如预期的那样,j
h
使用分别限于j
h
6或j
h
4、j
h
5和j
h
6(数据未显示)。在用12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体修饰的未免疫的动物中,检测到与所有j
h1‑
6基因区段的重组,但是在经修饰的和对照动物中均以更高的频率(约50%)看到与j
h
4的重组(数据未显示)。在所有经修饰的动物中,使用了多个v
h
基因区段(例如但不限于v
h4‑
39、v
h3‑
23等)并且多个d
h
基因区段(例如但不限于d
h1‑
7、d
h3‑
10和d
h5‑
12)与工程化d
h
基因区段重组。有趣的是,与对照动物(2.57%、3.44%;3.58%;n=3)相比,在用12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体修饰的动物(2.41%;6.34%;6.91%;n=3)中d
h2‑
2、d
h2‑
8和d
h2‑
15基因区段的使用趋势更高。(表6)。
[0525]
使用以下标准进一步确认了在连接区内鉴定出的具有最少两个连续d
h
区段的功能序列是由d
h
‑
d
h
重组事件产生的。在从用23:d
h3‑
3:12/j
h
6靶向载体或23:d
h3‑
3:12/j
h4‑
6靶向载体修饰的小鼠分离的序列中,当(1)所鉴定的“连续”或3’d
h
区段与ighd3
‑
3 d
h
基因区段的种系序列比对上最少9个连续碱基对,和(2)所鉴定的前导5’和连续3’d
h
基因区段与种系d
h
基因区段比对上最少5个连续碱基对而不管任何重叠时,d
h
‑
d
h
重组事件得以确认。在从用12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体修饰的小鼠分离的序列中,当(1)所鉴定的“前导”或5’d
h
区段与ighd2
‑
2 d
h
基因区段、ighd2
‑
8 d
h
基因区段、或ighd2
‑
15 d
h
基因区段的种系序列比对上最少9个连续碱基对,和(2)所鉴定的前导5’和连续3’d
h
基因区段与种系d
h
基因区段比对上最少5个连续核苷酸而不管任何重叠时,d
h
‑
d
h
重组事件得以确认。
[0526]
表6提供了作为绝对量和占总读段的百分比的功能性ig读段数量,源自d
h2‑
2基因区段、d
h2‑
8基因区段或d
h2‑
15基因区段的所有功能读段的百分比、以及符合要确认为d
h
‑
d
h
重组事件的结果的标准的源自d
h2‑
2基因区段、d
h2‑
8基因区段或d
h2‑
15基因区段的所有读
段的百分比。
[0527]
表6
[0528]
小鼠d2
‑
2/d2
‑
8/d2
‑
15使用%d
h
‑
d
h
融合%对照3.440.20
*
对照3.580.10
*
对照2.570.08
*
20188s16.343.8020188s22.411.6920188s36.914.16
[0529]
*
使用针对用12:d
h2‑
2:23|12:d
h2‑
8:23|12:d
h2‑
15:23靶向载体修饰的那些动物所设定的相同标准,确认了在这些对照动物中每一只的d
h
‑
d
h
融合。
[0530]
如表6所示,与对照动物相比,所有未免疫的经修饰的动物均显示d
h
‑
d
h
‑
重组事件增加。在用工程化2
‑
2、2
‑
8和2
‑
15基因区段修饰的动物(例如对于20188等位基因为纯合子)中,在包含三个工程化2
‑
2、2
‑
8、2
‑
15d
h
基因区段之一的所有重排的1.69%至4.16%中确认了d
h
‑
d
h
重组事件。相比之下,在对照动物中,在源自2
‑
2、2
‑
8或2
‑
15基因区段的所有重排中的少于0.2%中确认了d
h
‑
d
h
重组。在一个单独的实验中,对于6800小鼠(图4)为杂合子的小鼠中涉及工程化d
h3‑
3基因区段的已确认的d
h
‑
d
h
重组事件的频率在源自d
h3‑
3基因区段的所有功能性读段的0.6%至1.2%的范围内。
[0531]
在所有经修饰的动物中,重排的v
h
(d
h
a
‑
d
h
b)j
h
重排编码更长的cdr3长度(例如但不限于约21个氨基酸的cdr3长度),并掺入更多的半胱氨酸残基。(例如,图9和图10)。
[0532]
总之,由于利用了工程化d
h
基因区段,用工程化d
h
基因区段修饰的小鼠表现出相对正常的b细胞表型、和增加的d
h
‑
d
h
重组事件的频率。另外,d
h
‑
d
h
重组序列编码长度更长并且具有更高的半胱氨酸掺入率的cdr3。
[0533]
实施例4.抗体的产生
[0534]
本实施例证明了啮齿动物中抗体的产生,所述啮齿动物的基因组包含包括如本文所述的工程化d
h
区的免疫球蛋白重链可变区。根据需要,本实施例中描述的方法和/或本领域熟知的免疫方法可以用于用多肽或其片段(例如,来源于所需表位的肽)或者多肽或其片段的组合免疫含有如本文所述的工程化d
h
区的啮齿动物。
[0535]
简言之,使用本领域已知的免疫方法用所关注的抗原免疫包括如本文所述的工程化d
h
区的小鼠的队列。通过elisa免疫测定和/或通过msd在工程化细胞上监测抗体免疫应答(即,血清滴度)。当实现所需的免疫应答时,收集脾细胞(和/或其他淋巴组织)并与小鼠骨髓瘤细胞融合,以保持其活力并形成永生化杂交瘤细胞系。对杂交瘤细胞系进行筛选(例如,通过elisa测定或msd)和选择,以鉴定产生抗原特异性抗体的杂交瘤细胞系。还可以根据需要表征杂交瘤的相对结合亲和力和同种型。使用该技术,获得了若干抗原特异性嵌合抗体(即,具有人可变结构域和啮齿动物恒定结构域的抗体)。
[0536]
编码重链和轻链可变区的dna可被分离并连接至重链和轻链的期望同种型(恒定区),用于制备全人抗体。可以在细胞(诸如cho细胞)中产生这样的抗体。然后表征完全人类抗体对所关注的抗原的相对结合亲和力和/或中和活性。
[0537]
编码抗原特异性嵌合抗体或轻链和重链的可变域的dna可以直接从抗原特异性淋
巴细胞分离。最初,分离具有人可变区和啮齿动物恒定区的高亲和力嵌合抗体,并表征和选择所需的特征,包括但不限于亲和力、选择性、表位等。用所需的人恒定区替换啮齿动物(例如但不限于大鼠、小鼠等)恒定区以产生全人抗体。虽然所选的恒定区可以根据特定用途而变化,但是高亲和力抗原结合和靶标特异性特征留在可变区中。还在不融合至骨髓瘤细胞的情况下,从抗原阳性b细胞(来自免疫的小鼠)直接分离抗原特异性抗体,如例如美国专利no.7,582,298中所述,该专利以引用的方式整体并入本文。使用这种方法,制备了几种完全人类抗原特异性抗体(即,具有人类可变域和人类恒定域的抗体)。
[0538]
在一个实验中,将对照小鼠(例如具有人源化免疫球蛋白重链和轻链可变区基因座的小鼠(n=4
‑
6;参见例如美国专利号8,697,940和8,642,835;每个专利以全文引用的方式并入本文))和测试小鼠(例如,经修饰以包含如本文所述的工程化23:d
h3‑
3:12/j
h4‑
6或23:d
h3‑
3:12/j
h
6区的小鼠(n=4
‑
6))用不同的抗原和/或编码所述抗原的核酸(g蛋白偶联受体(gpcr)、离子通道、趋化因子受体或病原体)免疫)。
[0539]
小鼠能够产生对每种测试抗原的应答,应答在从低滴度到高特异性滴度的范围内(数据未显示)。具有如本文所述的工程化23:d
h3‑
3:12/j
h
6区的小鼠表现出与具有人源化免疫球蛋白重链和轻链可变区基因座的对照小鼠相当的对表达gpcr的细胞系的滴度(图11;实心圆代表表达gpcr的工程化细胞系;非实心圆是不表达gpcr的对照细胞)。
[0540]
另外,在包含工程化d
h
区的小鼠中产生的23种对g蛋白偶联受体(gpcr)具有特异性的测试抗体中的100%具有10个或更多个氨基酸的重链cdr3长度;20%具有14个氨基酸的cdr3长度,并且有1个抗体具有18个氨基酸的cdr3长度(数据未显示)。相比之下,在具有人源化免疫球蛋白重链和轻链可变区基因座而不是工程化d
h
区的小鼠中产生的8种对gpcr具有特异性的抗体中的仅约60%具有10个或更多个氨基酸的cdr3长度,没有一个具有14个或更多个氨基酸的cdr3长度(数据未显示)。
[0541]
从具有工程化23:d
h3‑
3:12/j
h4‑
6区的小鼠中分离出多种抗病毒抗体,其中至少一种表现出优于比较分子的中和活性(数据未显示)。
[0542]
来自具有工程化23:d
h3‑
3:12/j
h
6并用离子通道免疫的小鼠的抗体包含起源于v
h
d
h
j
h
和v
h
d
h
a
‑
d
h
bj
h
重排(如通过本实施例中所述的严格标准所确定)的hcdr3长度大于21个氨基酸的抗体群,发现与脾脏相比,编码更长hcdr3长度的序列在骨髓中更多(图12)。图13中显示了由根据本实施例的严格标准确定为v
h
d
h
a
‑
d
h
bj
h
重排的结果的序列编码的cdr3长度的分析(当使用本实施例的严格标准时,所检测到的每个d
h
基因区段必须显示出与种系d基因区段最少40%的同一性,3’d
h
基因区段必须源自d
h3‑
3基因区段,并且在每个d
h
基因区段中有最多1个核苷酸突变)。下表7提供了使用本实施例中所述的严格标准或本实施例中所述的非严格标准(当使用本实施例的非严格标准时,所检测到的每个d
h
基因区段必须显示出与种系d基因区段最少5个核苷酸同一性,这3’d
h
基因区段必须源自d
h3‑
3基因区段),比较了骨髓或脾脏中v
h
d
h
a
‑
d
h
bj
h
重组的频率。
[0543]
表7:v
h
d
h
a
‑
d
h
bj
h
重组频率
[0544] 非严格标准严格标准骨髓3.541.7脾脏0.380.04
[0545]
等同物
[0546]
在如此描述本发明的至少一个实施例的若干方面后,所属领域的技术人员应了解,所属领域的技术人员将容易想到各种更改、修改和改进。这些更改、修改以及改进希望是本公开的一部分,并且希望属于本发明的精神和范围内。因此,前述描述和附图只是为了举例且本发明通过以下权利要求书详细描述。
[0547]
所属领域的技术人员将了解可归因于本文所述分析或其它过程中所得值的偏差或误差的典型标准。本文引用的描述本发明背景以及提供与其实施有关的其他细节的出版物、网站和其他参考材料均据此以引用的方式整体并入。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1