西地那非及其中间体的制备方法与流程
1.本发明属于化学合成领域,且更具体而言,涉及化学合成西地那非 (sildenafil)及中间体的方法。
背景技术:
2.枸橼酸西地那非由辉瑞(pfizer)研发,最早于1998年3月27日获美国食品药品管理局(fda)批准,之后于1998年9月14日获欧洲药物管理局 (ema)批准,后又于1999年1月25日获日本医药品医疗器械综合机构 (pmda)批准上市,由辉瑞最初在美国上市销售,商品名
3.枸橼酸西地那非是一种5型磷酸二酯酶(pde-5)抑制剂,通过抑制能促使环磷酸鸟苷(cgmp)降解的cgmp特异性磷酸二酯酶5型的活性,而对阴茎血流水平进行调控。枸橼酸西地那非用于治疗勃起功能障碍(ed)。
4.专利(us5250534a)报道了西地那非的合成方法
[0005][0006]
专利(ep812845)报道了西地那非改进的合成方法
[0007][0008]
现有的方法存在诸多问题,如制备中间体3硝化反应的安全性问题和硝化废液的处置问题;制备酰胺4中间体使用了二氯亚砜,产生大量的废酸废气。同时还存在路线长、副反应多、收率低、原子不经济等缺点。
[0009]
因此发现并开发出更安全、更环保、更简易、更高效、条件温和、成本低廉、适于工业化生产的西地那非新合成路线与工艺条件,就显得尤为重要。同时新方法也要满足esh管理体系的要求,符合安全环保绿色合成的更高追求和理念,适于开发为绿色可持续性的生产工艺。
技术实现要素:
[0010]
技术问题
[0011]
因此,为了克服已有技术的不足,本公开的发明人经过大量的反复的实验,发现了一种反应条件温和,工艺简便,且适合工业化的制备西地那非及其中间体的方法,并在此基础上完成了本公开。
[0012]
技术方案
[0013]
本公开的一个目的是提供一种式i化合物的制备方法。
[0014][0015]
本公开的另一个目的是提供一种由式v表示的化合物及其盐。
[0016][0017]
根据本公开的一个实施方式,其提供了一种制备式i化合物的方法,所述方法为:
[0018][0019]
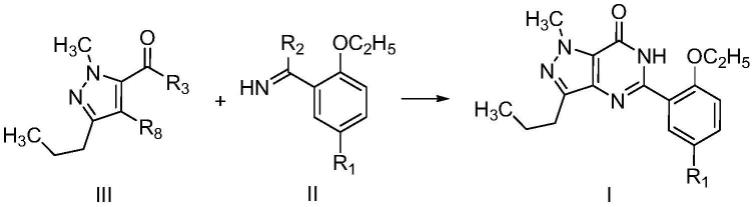
使式ii化合物或其盐化合物与式iii化合物反应生成式i化合物:
[0020][0021]
其中,r1选自h(氢)或
[0022]
r2选自or4或nh2,
[0023]
r3选自or5、nr6r7、氯、溴或碘,
[0024]
r8为h(氢)、or9或卤素,
[0025]
其中,式ii化合物的盐选自无机酸盐和有机酸盐,所述无机酸盐选自盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐;所述有机酸盐选自甲酸盐、乙酸盐、丙酸盐、羟乙酸盐、乙二酸盐、丙二酸盐、丁二酸盐、富马酸盐、马来酸盐、乳酸盐、苹果酸盐、柠檬酸盐、酒石酸盐、苦味酸盐、谷氨酸盐、甲磺酸盐和苯磺酸盐;
[0026]
化合物ii和iii包括其溶剂合物形式,如水合物、醇合物。
[0027]
其中,r4选自取代或未取代的c
1-c
20
直链或支链烷基、取代或未取代的 c
3-c
20
环状烷基、取代或未取代的c
3-c
20
烯烃基、取代或未取代的c
6-c
20
芳基、或取代或未取代的含有选自氧、氮、硫和磷中的一个或多个原子的c
2-c
20
杂芳基,其中,取代基选自以下中的一个或多个:卤素;羟基;c
1-c
20
烷基;
ꢀ‑
o-(c
1-c
20
烷基);优选地,r4选自甲基、甲氧基乙基或苯基;
[0028]
其中,r5选自氢、取代或未取代的c
1-c
20
直链或支链烷基、取代或未取代的c
3-c
20
环状烷基、取代或未取代的c
3-c
20
烯烃基、取代或未取代的c
6-c
20
芳基、或取代或未取代的含有选自氧、氮、硫和磷中的一个或多个原子的 c
2-c
20
杂芳基,其中,取代基选自以下中的一个或多个:卤素;羟基;c
1-c
20
烷基;-o-(c
1-c
20
烷基);优选地,r5选自氢、甲基、乙基或甲氧基乙基;
[0029]
其中,r6和r7各自独立地选自氢和c
1-c4烷基;c
3-c
20
烯烃基;c
6-c
20
芳基;含有选自氧、氮、硫和磷中的一个或多个原子的c
2-c
20
杂芳基;c
3-c
20
环烷基;优选地,r6和r7各自独立地为氢、甲基、乙基或羟基乙基;
[0030]
其中,r9选自全氟代烷基磺酰基(-so2rn,氟代烷基rn为c1~c
10
直链或者支链或者环状全氟取代烷基);烷基磺酰基(-so2rm,烷基rm为c1~c
10
直链或者支链或者环状烷基);芳基或取代芳基的苯磺酰基(-so2ar1,ar1为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的芳香环基);芳基甲基或取代芳基甲基磺酰基(-so2ch2ar2,ar2为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的苯基);优选地,r9选自三氟甲磺酰基(-tf,-so2cf3);甲磺酰基(-ms,
ꢀ‑
so2me)、乙磺酰基(-so2et);苯磺酰基(-so2ph)、对甲苯磺酰基(-ts,
ꢀ‑
so2c4h
6-4-me);苯甲基磺酰基(-so2ch2ph);乙烯磺酰基(-so2ch=ch2)、苯乙烯基磺酰基(-so2ch=chph);
[0031]
其中,所述反应条件为:
[0032]
(1)式ii化合物及其盐和式iii所示化合物在碱性试剂的存在下反应制备得式i所示化合物;
[0033]
在反应条件(1)中:
[0034]
所述碱性试剂为选自碳酸铵、碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢铵、碳酸氢钠、碳酸氢钾、磷酸铵、磷酸钠、磷酸钾、磷酸一氢铵、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0035]
其中,所述式ii化合物或其盐和式iii所示的化合物的投料摩尔比为 0.9:1~1:1.5,优选的1:1.1;
[0036]
其中,所述式ii化合物及其盐与碱性试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0037]
该反应在加入或不加入过渡金属配合物下进行,所用的过渡金属化合物为选自氯化亚铜、溴化亚铜、碘化亚铜、氧化亚铜、氰化亚铜、乙酸亚铜、氯化铜、溴化铜、氧化铜、乙酸铜、硫酸铜、硝酸铜中的一种或几种的混合物,所用的配体选自乙二胺、n-甲基乙二胺、n-丁基乙二胺、n,n
’‑
二甲基乙二胺、n,n-二甲基乙二胺、三甲基乙二胺、四甲基乙二胺、(顺)-1,2-环己二胺、(反)-1,2-环己二胺、1,2-环己二胺外消旋体、(反)-n,n
’‑
二甲基-1,2-环己二胺、(反)-n,n
’‑
二乙基-1,2-环己二胺、(反)-n,n
’‑
二异丙基-1,2-环己二胺、2,2
’‑
联吡啶、1,10-菲啰啉、2,9-二甲基-1,10-菲啰啉、3,4,7,8-四甲基-1,10
‑ꢀ
菲啰啉、4,7-二苯基-1,10-菲啰啉中的一种或几种的混合物;
[0038]
在加入过渡金属配合物的情况下,所述式ii化合物及其盐与过渡金属化合物的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;所述式ii与配体的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;
[0039]
反应所用的溶剂选自二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲苯、二甲苯、氯苯、乙腈、丙酮、乙醇、异丙醇、正丁醇、叔丁醇、乙二醇、吡啶、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;或者
[0040]
(2)在存在(a)钯化合物和叔膦或(b)钯卡宾络合物时碱性条件下将式ii化合物及其盐和式iii所示化合物反应制备得式i所示化合物;
[0041]
在反应条件(2)中:
[0042]
所用的碱性试剂为选自碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢钠、碳酸氢钾、磷酸钠、磷酸钾、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6
‑ꢀ
二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0043]
其中,所述式ii化合物及其盐和式iii所示的化合物的投料摩尔比为 0.9:1~1:1.5,优选的1:1.1;
[0044]
其中,所述式ii化合物及其盐与碱性试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0045]
其中(a)钯化合物选自乙酸钯、钯碳、氧化钯、氯化钯、溴化钯、碘化钯、硫酸钯或硝酸钯,优选的钯化合物选自氯化钯或醋酸钯;
[0046]
其中,所述式ii化合物及其盐与钯化合物的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;
[0047]
叔膦选自三苯基膦、三叔丁基膦、2-(二叔丁基膦基)-1,1
’‑
联苯、2-(二叔丁基膦基)-2
’‑
甲基-1,1
’‑
联苯、2-(二叔丁基膦基)-1,1
’‑
联萘、2-二环己基膦基
ꢀ‑2’
,6
’‑
二异丙氧基-1,1
’‑
联苯、2-二环己基膦基-2’,6
’‑
二甲氧基-1,1
’‑
联苯、 n-苯基-2-(二叔丁基膦基)吡咯和1-苯基-2-(二叔丁基膦基)-1h-茚组成的组中的至少一个成员;
[0048]
其中,所述式ii化合物及其盐与叔膦的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;
[0049]
其中(b)钯卡宾络合物选自三苯基膦钯、三(二亚苄基丙酮)二钯、三苯基膦醋酸钯、二(三叔丁基膦)钯、双三苯基磷二氯化钯、双(三环己基膦)二氯化钯、双(三环己基磷)钯、(1,5-环辛二烯)二氯化钯、1,4-双(二苯基膦丁烷)二氯化钯、烯丙基氯-[1,3-双(2,6-二异丙基苯基)咪唑-2-亚基]钯、烯丙基氯-[1,3
‑ꢀ
双(2,6-二异丙基苯基)-4,5-二氢咪唑-2-亚基]钯;
[0050]
其中,所述式ii化合物及其盐与钯卡宾络合物的投料摩尔比为 1:0.001~1:0.5,优选为1:0.005~1:0.01;
[0051]
特别地,反应所用的溶剂选自二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲苯、二甲苯、氯苯、乙腈、丙酮、乙醇、异丙醇、正丁醇、叔丁醇、乙二醇、吡啶、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;
[0052]
其中,所述方法的反应温度为50~200℃,优选的,反应温度为100~200℃。
[0053]
根据本公开的另一个实施方式,其提供了另一种制备式i化合物的方法,所述方法为:
[0054]
使式iv化合物或其盐与式iii化合物反应得到式v化合物,再发生关环反应生成式i化合物,
[0055][0056]
其中,在式i、iii、iv和v化合物中,
[0057]
r1选自h(氢)或
[0058]
r3选自or5、nr6r7、氯、溴或碘,
[0059]
r8为h(氢)、or9或卤素,
[0060]
其中,式iv化合物的盐选自无机酸盐和有机酸盐,所述无机酸盐选自盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐;所述有机酸盐选自甲酸盐、乙酸盐、丙酸盐、羟乙酸盐、乙二酸盐、丙二酸盐、丁二酸盐、富马酸盐、马来酸盐、乳酸盐、苹果酸盐、柠檬酸盐、酒石酸盐、苦味酸盐、谷氨酸盐、甲磺酸盐和苯磺酸盐;
[0061]
其中,r5选自氢、取代或未取代的c
1-c
20
直链或支链烷基、取代或未取代的c
3-c
20
环状烷基、取代或未取代的c
3-c
20
烯烃基、取代或未取代的c
6-c
20
芳基、或取代或未取代的含有选自氧、氮、硫和磷中的一个或多个原子的 c
2-c
20
杂芳基,其中,取代基选自以下中的一个或多个:卤素;羟基;c
1-c
20
烷基;-o-c
1-c
20
烷基;优选地,r5选自氢、ch3、c2h5或-ch2ch2och3;
[0062]
其中,r6和r7各自独立地选自氢和c
1-c4烷基;c
3-c
20
烯烃基;c
6-c
20
芳基;含有选自氧、氮、硫和磷中的一个或多个原子的c
2-c
20
杂芳基;c
3-c
20
环烷基;优选地,r6和r7各自独立地为氢、甲基、乙基或羟基乙基;
[0063]
其中,r9选自全氟代烷基磺酰基(-so2rn,氟代烷基rn为c1~c
10
直链或者支链或者环状全氟取代烷基);烷基磺酰基(-so2rm,烷基rm为c1~c
10
直链或者支链或者环状烷基);芳基或取代芳基的苯磺酰基(-so2ar1,ar1为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的芳香环基);芳基甲基或取代芳基甲基磺酰基(-so2ch2ar2,ar2为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的苯基);优选地,r9选自三氟甲磺酰基(-tf,-so2cf3);甲磺酰基(-ms,
ꢀ‑
so2me)、乙磺酰基(-so2et);苯磺酰基(-so2ph)、对甲苯磺酰基(-ts,
ꢀ‑
so2c4h
6-4-me);苯甲基磺酰基(-so2ch2ph);乙烯磺酰基(-so2ch=ch2)、苯乙烯基磺酰基(-so2ch=chph);
[0064]
其中,所述反应条件为:
[0065]
(1)步骤a式iv化合物或其盐和式iii化合物在碱性试剂的存在下缩合反应得到式v化合物,
[0066]
在反应条件(1)中:
[0067]
所述碱性试剂为选自碳酸铵、碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢铵、碳酸氢钠、碳酸氢钾、磷酸铵、磷酸钠、磷酸钾、磷酸一氢铵、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢
氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0068]
其中,所述式iv和式iii所示的化合物的投料投料摩尔比为0.9:1~1:1.5,优选的1:1.1;
[0069]
其中,所述式iv与碱性试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0070]
其中,反应所用的溶剂选自二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲苯、二甲苯、氯苯、乙腈、丙酮、乙醇、异丙醇、正丁醇、叔丁醇、乙二醇、吡啶、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;
[0071]
其中,所述方法的反应温度为50~150℃,优选的,反应温度为50~100℃;
[0072]
在步骤b中,
[0073]
反应条件包括:
[0074]
(b1)式v在碱性试剂的存在下反应制备得式i所示化合物;
[0075]
其中,所用的碱性试剂为选自碳酸铵、碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢铵、碳酸氢钠、碳酸氢钾、磷酸铵、磷酸钠、磷酸钾、磷酸一氢铵、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0076]
其中,所述式v与碱性试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0077]
特别地,该反应可以加入或不加入过渡金属配合物下进行,所用的过渡金属化合物为选自氯化亚铜、溴化亚铜、碘化亚铜、氧化亚铜、氰化亚铜、乙酸亚铜、氯化铜、溴化铜、氧化铜、乙酸铜、硫酸铜、硝酸铜中的一种或几种的混合物,所用的配体选自乙二胺、n-甲基乙二胺、n-丁基乙二胺、n,n
’‑ꢀ
二甲基乙二胺、n,n-二甲基乙二胺、三甲基乙二胺、四甲基乙二胺、(顺)-1,2
‑ꢀ
环己二胺、(反)-1,2-环己二胺、1,2-环己二胺外消旋体、(反)-n,n
’‑
二甲基
ꢀ‑
1,2-环己二胺、(反)-n,n
’‑
二乙基-1,2-环己二胺、(反)-n,n
’‑
二异丙基-1,2
‑ꢀ
环己二胺、2,2
’‑
联吡啶、1,10-菲啰啉、2,9-二甲基-1,10-菲啰啉、3,4,7,8-四甲基-1,10-菲啰啉、4,7-二苯基-1,10-菲啰啉中的一种或几种的混合物;
[0078]
在加入过渡金属配合物的情况下,所述式v与过渡金属化合物的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;所述式v与配体的投料摩尔比为1:0.001~1:0.5,优选为1:0.005~1:0.01;
[0079]
其中,反应所用的溶剂选自二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲苯、二甲苯、氯苯、乙腈、丙酮、乙醇、异丙醇、正丁醇、叔丁醇、乙二醇、吡啶、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;或者
[0080]
(b2)在存在(a)钯化合物和叔膦或(b)钯卡宾络合物时碱性条件下将式v所示化合物发生关环反应制备得式i所示化合物;
[0081]
在反应条件(b2)中,
[0082]
所用的碱性试剂为选自碳酸铵、碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢铵、碳酸氢钠、碳酸氢钾、磷酸铵、磷酸钠、磷酸钾、磷酸一氢铵、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0083]
其中,所述式v与碱性试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0084]
其中(a)钯化合物选自乙酸钯、钯碳、氧化钯、氯化钯、溴化钯、碘化钯、硫酸钯或硝酸钯,优选的钯化合物选自氯化钯或醋酸钯;
[0085]
其中,所述式v与钯化合物的投料摩尔比为1:0.001~1:0.5,优选为 1:0.005~1:0.01;
[0086]
叔膦选自三苯基膦、三叔丁基膦、2-(二叔丁基膦基)-1,1
’‑
联苯、2-(二叔丁基膦基)-2
’‑
甲基-1,1
’‑
联苯、2-(二叔丁基膦基)-1,1
’‑
联萘、2-二环己基膦基
ꢀ‑2’
,6
’‑
二异丙氧基-1,1
’‑
联苯、2-二环己基膦基-2’,6
’‑
二甲氧基-1,1
’‑
联苯、 n-苯基-2-(二叔丁基膦基)吡咯和1-苯基-2-(二叔丁基膦基)-1h-茚组成的组中的至少一种;
[0087]
其中,所述式v与叔膦的投料摩尔比为1:0.001~1:0.5,优选为 1:0.005~1:0.01;
[0088]
其中(b)钯卡宾络合物选自三苯基膦钯、三(二亚苄基丙酮)二钯、三苯基膦醋酸钯、二(三叔丁基膦)钯、双三苯基磷二氯化钯、双(三环己基膦)二氯化钯、双(三环己基磷)钯、(1,5-环辛二烯)二氯化钯、1,4-双(二苯基膦丁烷)二氯化钯、烯丙基氯-[1,3-双(2,6-二异丙基苯基)咪唑-2-亚基]钯、烯丙基氯-[1,3
‑ꢀ
双(2,6-二异丙基苯基)-4,5-二氢咪唑-2-亚基]钯;
[0089]
其中,所述式v与钯卡宾络合物的投料摩尔比为1:0.001~1:0.5,优选为 1:0.005~1:0.01;
[0090]
其中,反应所用的溶剂选自二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲苯、二甲苯、氯苯、乙腈、丙酮、乙醇、异丙醇、正丁醇、叔丁醇、乙二醇、吡啶、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;
[0091]
其中,所述方法的反应温度为100~200℃,优选的,反应温度为 100~150℃;
[0092]
根据本公开的另一个实施方式,其提供了另一种制备式i化合物的方法,所述方法为:
[0093]
式iv化合物及其盐与式iii化合物缩合反应得到式v化合物,其中,r3为羟基,
[0094][0095]
其中,在式i、iii、iv和v化合物中,
[0096]
r1选自氢或
[0097]
r8为氢、or9或卤素
[0098]
其中,式iv化合物的盐选自无机酸盐和有机酸盐,所述无机酸盐选自盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐;所述有机酸盐选自甲酸盐、乙酸盐、丙酸盐、羟乙酸盐、乙二酸盐、丙二酸盐、丁二酸盐、富马酸盐、马来酸盐、乳酸盐、苹果酸盐、柠檬酸盐、酒石酸盐、苦味酸盐、谷氨酸盐、甲磺酸盐和苯磺酸盐;
[0099]
其中,r9选自全氟代烷基磺酰基(-so2rn,氟代烷基rn为c1~c
10
直链或者支链或者环状全氟取代烷基);烷基磺酰基(-so2rm,烷基rm为c1~c
10
直链或者支链或者环状烷基);芳基或取代芳基的苯磺酰基(-so2ar1,ar1为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的芳香环基);芳基甲基或取代芳基甲基磺酰基(-so2ch2ar2,ar2为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的苯基);优选地,r9选自三氟甲磺酰基(-tf,-so2cf3);甲磺酰基(-ms,
ꢀ‑
so2me)、乙磺酰基(-so2et);苯磺酰基(-so2ph)、对甲苯磺酰基(-ts,
ꢀ‑
so2c4h
6-4-me);苯甲基磺酰基(-so2ch2ph);乙烯磺酰基(-so2ch=ch2)、苯乙烯基磺酰基(-so2ch=chph);
[0100]
其中,在所述缩合反应中,所用缩合剂为羰基二亚胺类缩合剂、鎓盐类缩合剂或有机磷类缩合剂中的一种或者两种;
[0101]
其中羰基二亚胺类缩合剂选自二环己基碳二亚胺(dcc)、二异丙基碳二亚胺(dic)、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edci)、4,5
‑ꢀ
二氰基咪唑(dci)、n,n
’‑
羰基二咪唑(cdi);
[0102]
其中,鎓盐类缩合剂选自2-(7-氮杂苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸(hatu)、苯并三氮唑-n,n,n',n'-四甲基脲六氟磷酸盐(hbtu)、6-氯苯并三氮唑-1,1,3,3-四甲基脲六氟磷酸酯(hctu)、(苯并三唑-1
‑ꢀ
基)-n,n,n',n'-二吡咯基脲六氟磷酸酯(hbpyu)、2-(1h-苯并三偶氮l-1
‑ꢀ
基)-1,1,3,3-四甲基脲四氟硼酸酯(tbtu)、2-琥珀酰亚胺基-1,1,3,3-四甲基脲四氟硼酸酯、2-(5-降冰片烯-2,3-二甲酰亚胺基)-1,1,3,3-四甲基脲四氟硼酸季铵盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐(bop)、1h-苯并三唑-1-基氧三吡咯烷基六氟磷酸盐(pybop)、六氟磷酸(7-氮杂苯并三唑
ꢀ‑
1-氧基)三吡咯烷磷(pyaop),(2-肟基-氰基乙酸乙酯)-n,n-二甲基-吗啉基脲六氟磷酸酯(comu);
[0103]
其中,有机磷缩合剂包含1-丙基磷酸酐(t3p)、二苯基次膦酰氯 (dpp-cl)、叠氮磷酸二苯酯(dppa)、双(2-氧代-3-恶唑烷基)次磷酰氯 (bop-cl);
[0104]
其中,所述式iv与缩合试剂的投料摩尔比为1:0.5~1:2,优选为1:1~1:1.1;
[0105]
该反应可以加入或不加入碱下进行,所用的碱性试剂为选自碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢钠、碳酸氢钾、磷酸钠、磷酸钾、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的
一种或几种的混合物;
[0106]
其中,步骤d与上述步骤b使用的试剂及条件相同。
[0107]
根据本公开的另一个实施方式,其提供了另一种制备式i化合物的方法,所述方法为:
[0108]
式iv化合物及其盐与式iii化合物缩合反应得到式v化合物,其中,r3为氯,
[0109][0110]
其中,在式i、iii、iv和v化合物中,
[0111]
r1选自氢或
[0112]
r8为氢、or9或卤素,
[0113]
其中,式iv化合物的盐选自无机酸盐和有机酸盐,所述无机酸盐选自盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐;所述有机酸盐选自甲酸盐、乙酸盐、丙酸盐、羟乙酸盐、乙二酸盐、丙二酸盐、丁二酸盐、富马酸盐、马来酸盐、乳酸盐、苹果酸盐、柠檬酸盐、酒石酸盐、苦味酸盐、谷氨酸盐、甲磺酸盐和苯磺酸盐;
[0114]
其中,r9选自全氟代烷基磺酰基(-so2rn,氟代烷基rn为c1~c
10
直链或者支链或者环状全氟取代烷基);烷基磺酰基(-so2rm,烷基rm为c1~c
10
直链或者支链或者环状烷基);芳基或取代芳基的苯磺酰基(-so2ar1,ar1为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的芳香环基);芳基甲基或取代芳基甲基磺酰基(-so2ch2ar2,ar2为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的苯基);优选地,r9选自三氟甲磺酰基(-tf,-so2cf3);甲磺酰基(-ms,
ꢀ‑
so2me)、乙磺酰基(-so2et);苯磺酰基(-so2ph)、对甲苯磺酰基(-ts,
ꢀ‑
so2c4h
6-4-me);苯甲基磺酰基(-so2ch2ph);乙烯磺酰基(-so2ch=ch2)、苯乙烯基磺酰基(-so2ch=chph);
[0115]
步骤e,式iii-oh所示化合物通过氯代反应制备式iii-cl所示化合物;
[0116]
步骤f,式iii-cl所示化合物与式iv所示化合物反应,获得v所示的化合物;
[0117]
其中,步骤d与上述步骤b使用的试剂及条件相同;
[0118]
在步骤e中,所述的氯代反应所用的氯代试剂为选自二氯亚砜、三氯氧磷、五氯化磷、草酰氯、光气、二(三氯甲基)碳酸酯中的一种或几种的混合物;
[0119]
在步骤e中,所述的氯代反应在溶剂中进行,所用的溶剂为选自二氯甲烷、氯仿、苯、甲苯、二甲苯、氯苯、乙腈、四氢呋喃、2-甲基四氢呋喃、二氧六环、乙二醇二甲醚、甲基叔丁基醚中的一种或几种的混合物,优选为二氯甲烷;
[0120]
在步骤f中加入或不加入碱性试剂;
[0121]
在加入碱性试剂的情况下,所述碱性试剂为选自碳酸锂、碳酸钠、碳酸钾、碳酸铯、碳酸氢钠、碳酸氢钾、磷酸钠、磷酸钾、磷酸一氢钠、磷酸一氢钾、氢氧化锂、氢氧化钠、氢氧化钾、碳酸镁、氢氧化镁、碳酸钙、氢氧化钙、氧化钙、氧化镁、甲醇锂、甲醇钠、甲醇钾、乙醇钠、乙醇钾、异丙醇锂、异丙醇钠、异丙醇钾、叔丁醇锂、叔丁醇钠、叔丁醇钾、甲醇镁、乙醇镁、叔丁醇镁、氨水、三乙胺、二异丙基胺、二异丙基乙基胺、三正丁胺、吡啶、2-甲基吡啶、2,6-二甲基吡啶、4-二甲氨基吡啶、四氢吡咯、吗啉、哌啶、2,2,6,6-四甲基哌啶中的一种或几种的混合物;
[0122]
步骤f在溶剂中进行,所用的溶剂为选自四氢呋喃、二氧六环、2-甲基四氢呋喃、乙二醇二甲醚、甲基叔丁基醚、甲苯、二甲苯、二氯甲烷、氯仿、乙腈、丙酮、吡啶、n,n-二甲基甲酰胺、n-甲基吡咯烷酮、二甲基亚砜、水中的一种或几种的混合物;
[0123]
优选地,所述步骤e和步骤f使用一锅法进行,即步骤e制备的式v-2 所示的化合物不经分离,直接进行步骤f的反应;
[0124]
根据本公开的另一个实施方式,其提供了一种由式v表示的化合物及其盐:
[0125][0126]
其中,在式v化合物中,
[0127]
r1选自h(氢)或
[0128]
r8为h(氢)、or9或卤素;
[0129]
其中,r9选自全氟代烷基磺酰基(-so2rn,氟代烷基rn为c1~c
10
直链或者支链或者环状全氟取代烷基);烷基磺酰基(-so2rm,烷基rm为c1~c
10
直链或者支链或者环状烷基);芳基或取代芳基的苯磺酰基(-so2ar1,ar1为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的芳香环基);芳基甲基或取代芳基甲基磺酰基(-so2ch2ar2,ar2为带有一个或者多个c
1-c
10
直链或者支链或者环状烷基、c
1-c
10
直链或者支链或者环状烷氧基、硝基、卤素、三氟甲基、羰基、氰基、酯基、羧基等取代基的苯基);优选地,r9选自三氟甲磺酰基(-tf,-so2cf3);甲磺酰基(-ms,
ꢀ‑
so2me)、乙磺酰基(-so2et);苯磺酰基(-so2ph)、对甲苯磺酰基(-ts,
ꢀ‑
so2c4h
6-4-me);苯甲基磺酰基(-so2ch2ph);乙烯磺酰基(-so2ch=ch2)、苯乙烯基磺酰基(-so2ch=chph);
[0130]
其中,式v化合物的盐选自无机酸盐和有机酸盐,所述无机酸盐选自盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐;所述有机酸盐选自甲酸盐、乙酸盐、丙酸盐、羟乙酸盐、乙二酸盐、丙二酸盐、丁二酸盐、富马酸盐、马来酸盐、乳酸盐、苹果酸盐、柠檬酸盐、酒石酸盐、苦味酸盐、谷氨酸盐、甲磺酸盐和苯磺酸盐。
[0131]
在本公开中,卤素为氟、氯、溴或碘。
[0132]
有益效果
[0133]
本方法制备西地那非及其中间体避免硝化反应引入胺基及其他步骤中的副反应,从源头上避免了大量酸的使用。本发明的合成方法具有简单高效、条件温、副反应少、安全环保等优点,适于开发为绿色可持续性的生产工艺。
具体实施方式
[0134]
本发明公开了用于西地那非及其类似物的制备和纯化方法。举例来说,本发明公开了用于制备西地那非及其类似物的方法。下列实施例仅用于示例性说明本发明的实施方案。应了解本发明的实施方案不受限于下列实施例中的特定细节,因为鉴于本发明的公开内容,其他变化对本领域普通技术人员是已知和显而易见的。
[0135]
上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
[0136]
实施例1:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0137][0138]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物ii-1(10g)、碳酸钾(9.25g)和iii-1(13.2g),氮气置换空气5次,加热120℃搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(15.7g),收率80%。
[0139]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值(理论值):c
17h21
n4o2,[m+h
+
]313.16645,实测值: 313.16580.
[0140]
实施例2:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0141]
[0142]
向100ml三颈瓶中加入二氧六环(20ml)、化合物ii-1(10g)、碳酸铯 (23.8g)、iii-2(15.9g)和碘化亚铜(580mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(18.7g),收率95%。1hnmr(400mhz, cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46(m 1h),7.15(m 1h),7.04 (d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j=7.6hz,2h),1.95
–
1.83(m, 2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h).hrms(esi)计算值: c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580
[0143]
实施例3:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0144][0145]
向100ml三颈瓶中加入二甲苯(20ml)、化合物ii-1(10g)、碳酸铯(23.8g) 和iii-3(19.4g),(
±
)-2,2'-双-(二苯膦基)-1,1'-联萘(380mg)和醋酸钯(136mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(19.4g),收率99%。
[0146]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2([m+h
+
]313.16645,实测值:313.16580.
[0147]
实施例4:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0148][0149]
向100ml三颈瓶中加入n-甲基吡咯烷酮(20ml)、化合物ii-2(11g)、磷酸铵(9.1g)、iii-3(19.4g)、(
±
)-2,2'-双-(二苯膦基)-1,1'-联萘(380mg)和醋酸钯(136mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(18g),收率92%。
[0150]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2([m+h
+
]313.16645,实测值:313.16580.
[0151]
实施例5:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0152][0153]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物ii-1(6.8g)、 hbtu(14.2g)和iii-4(10g)、氮气置换空气5次,0-10℃,滴入n,n-二异丙基乙胺(17.6g),25-30℃搅拌12小时,反应完全后,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到v-1(16.4g),收率90%。
[0154]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物v-1(9.8g)、碘化亚铜(850mg)和碳酸铯(14.5g)、氮气置换空气5次,90℃搅拌12小时,反应完全后,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(7g),收率98%。
[0155]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580.
[0156]
实施例6:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0157][0158]
向100ml三颈瓶中加入n,n-二甲基乙酰胺(20ml)、化合物ii-1(10g)、叔丁醇镁(12.5g)和iii-5(14.3g),氮气置换空气5次,加热120℃搅拌12 小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(16.1g),收率83%
[0159]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j=7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580.
[0160]
实施例7:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0161][0162]
向100ml三颈瓶中加入n-甲基吡咯烷酮(20ml)、化合物ii-1(10g)、叔丁醇钾(7.5g)、iii-6(20.18g)、双(三环己基膦)二氯化钯(250mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水 (20ml),大量白色固体析出,过滤,烘干得到
标题化合物(14g),收率72%。
[0163]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580.
[0164]
实施例8:西地那非的制备
[0165][0166]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物iv-1(10g)、磷酸钾(7.8g)和iii-7(9.0g),氮气置换空气5次,加热120℃搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(12.36g),收率85%。
[0167]1h nmr(400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j =8.8,2.4hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h), 3.10(br s,4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j= 7.5hz,2h),1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz, cdcl3):δ159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1, 113.0,66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m +h
+
).
[0168]
实施例9:西地那非的制备
[0169][0170]
向100ml三颈瓶中加入n,n-二甲基丙酰胺(20ml)、化合物iv-2(10g)、叔丁醇锂(3.0g)和iii-8(5.5g),氮气置换空气5次,加热120℃搅拌12 小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(9.8g),收率83%。
[0171]1h nmr(400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j =8.8,2.4hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h), 3.10(br s,4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j= 7.5hz,2h),1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz, cdcl3):δ159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1, 113.0,66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m +h
+
).
[0172]
实施例10:西地那非的制备
[0173][0174]
向100ml三颈瓶中加入n,n-二甲基乙酰胺(20ml)、化合物iv-1(10g)、磷酸钾(7.8g)和iii-9(8.8g),氮气置换空气5次,加热120℃搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(11.3g),收率78%。
[0175]1h nmr(400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j =8.8,2.4hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h), 3.10(br s,4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j= 7.5hz,2h),1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz, cdcl3):δ159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1, 113.0,66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m +h
+
).
[0176]
实施例11:西地那非的制备
[0177][0178]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物iv-1(10g)、 iii-10(11.8g)、氧化铜(10mg)和2,9-二甲基-1,10-菲啰啉(30mg)、氮气置换空气5次,90℃搅拌12小时,反应完全后,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(13g),收率89%。1h nmr(400mhz, cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j=8.8,2.4hz,1h), 7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h),3.10(br s,4h), 2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j=7.5hz,2h), 1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz,cdcl3):δ 159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1,113.0, 66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m+h
+
).
[0179]
实施例12:西地那非的制备
[0180][0181]
向100ml三颈瓶中加入n,n-二甲基甲酰胺(20ml)、化合物iv-1(10g)、 iii-11(10.3g)、钯碳(100mg)和n-苯基-2-(二叔丁基膦基)吡咯(300mg)、氮气置换空气5次,90℃搅拌12小时,反应完全后,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(13.8g),收率95%。1h nmr (400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j=8.8,2.4 hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h),3.10(br s, 4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j=7.5hz,2h), 1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz,cdcl3):δ 159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1,113.0, 66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m+h
+
).
[0182]
实施例13:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0183][0184]
向100ml三颈瓶中加入二氯甲烷(20ml)、化合物ii-1(10g)和三乙胺 (6.8g)氮气置换空气5次,-10-10℃滴入iii-12(19.1g)的二氯甲烷溶液,
ꢀ‑
10-10℃保温2-3h,反应完全后,缓慢滴入水(20ml)分液,有机相浓缩至小体积,缓慢滴入甲醇(20ml),大量白色固体析出,过滤,烘干得到化合物v-1(26.3g),收率98%。
[0185]1h nmr(400mhz,cdcl3)δ11.12(br,1h),9.07(br,1h),8.81(d,1h), 7.53(t,1h),7.12(t,1h),7.02(m,1h),4.26(q,2h),4.20(s,3h),2.62(t,2h), 1.71(m,2h),1.54(t,3h),0.99(t,3h).ms(esi)m/z:441.09(m+h
+
).
[0186]
向100ml三颈瓶中加入二氧六环(20ml)、化合物v-1(10g)、碳酸钠 (2.9g)、乙酸铜(50mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(6.8g),收率95%。
[0187]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j= 7.6hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580
[0188]
实施例14:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d] 嘧啶-7-酮的制备
[0189][0190]
向100ml三颈瓶中加入二氯甲烷(20ml)、化合物ii-1(10g)和n,n-二异丙基乙胺(9.5g)氮气置换空气5次,-10-10℃滴入iii-12(20.8g)的二氯甲烷溶液,-10-10℃保温2-3h,反应完全后,缓慢滴入水(20ml)分液,有机相浓缩至小体积,缓慢滴入甲醇(20ml),大量白色固体析出,过滤,烘干得到化合物v-1(23.0g),收率96%。
[0191]1h nmr(400mhz,cdcl3)δ11.11(br,1h),8.98(br,1h),8.78(d,1h), 7.52(t,1h),7.11(t,1h),7.01(m,1h),4.26(q,2h),4.18(s,3h),2.62(t,2h), 1.72(m,2h),1.54(t,3h),0.99(t,3h).ms(esi)m/z:393.1(m+h
+
).
[0192]
向100ml三颈瓶中加入二氧六环(20ml)、化合物v-2(10g)、碳酸氢钾 (2.9g)、乙酸铜(50mg),氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(7.2g),收率91%。
[0193]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j=7.6 hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c17h21n4o2([m-h+]313.16645,实测值:313.16580 实施例15:5-(2-乙氧基苯基)-1-甲基-3-丙基-1,6-二氢-7h-吡唑啉[4,3-d]嘧啶-7-酮的制备
[0194][0195]
向100ml三颈瓶中加入二氯甲烷(20ml)、化合物ii-1(10g)和碳酸钾 (9.2g)氮气置换空气5次,0-10℃缓慢滴入iii-5(14.3g)的二氯甲烷溶液,反应完全后,将反应液倒入入水(20ml)中,分液,有机相浓缩至小体积,缓慢滴入异丙醇(20ml),大量白色固体析出,过滤,烘干得到化合物v-3 (19.1g),收率90%。
[0196]1h nmr(400mhz,cdcl3)δ11.12(br,1h),9.06(br,1h),8.77(d,1h), 7.56(t,1h),7.16(t,1h),7.05(m,1h),4.38(q,2h),4.20(s,3h),2.65(t,2h), 1.73(m,2h),1.56(t,3h),1.00(t,3h).ms(esi)m/z:349.2(m+h
+
).
[0197]
向100ml三颈瓶中加入二氧六环(20ml)、化合物v-3(10g)、二异丙基乙基胺(380mg)、氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(7.9g),收率88%。
[0198]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j=7.6 hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2.[m+h
+
]313.16645,实测值:313.16580.
[0199]
实施例16:西地那非的制备
[0200][0201]
向100ml三颈瓶中加入乙腈(20ml)、化合物iv-2(10g)、iii-13(10.4g) 和磷酸钾(3g)氮气置换空气5次,反应升至80℃反应2h,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到化合物v-3(16g),收率95%。
[0202]1h nmr(400mhz,cdcl3)δ11.13(br,1h),9.41(s,1h),8.70(br,1h), 7.87(d,1h),7.14(d,1h),4.36(q,2h),4.21(s,3h),2.74(m,4h),2.62(m,4h), 2.60(m,2h),2.44(s,3h),1.71(m,2h),1.60(t,3h),0.98(t,3h).
[0203]
向100ml三颈瓶中加入二氧六环(20ml)、化合物v-4(10g)、氧化亚铜(30mg)n-丁基乙二胺(230mg)、氮气置换空气5次,加热回流搅拌12 小时,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(7.7g),收率97%。
[0204]1h nmr(400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j =8.8,2.4hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h), 3.10(br s,4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j= 7.5hz,2h),1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz, cdcl3):δ159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1, 113.0,66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m +h
+
).
[0205]
实施例17:西地那非的制备
[0206][0207]
向100ml三颈瓶中加入乙腈(20ml)、化合物iv-3(10g)、iii-14(7.2g) 和叔丁基氯化镁(2mol/l)(12ml)氮气置换空气5次,反应升至60℃反应 12h,反应完全后,降至室温,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到化合物v-3(9.4g),收率75%。
[0208]1h nmr(400mhz,cdcl3)δ11.09(br,1h),9.41(s,1h),8.70(br,1h), 7.87(d,1h),7.13(d,1h),4.35(q,2h),4.19(s,3h),3.10(m,4h),2.62(m,2h), 2.55(m,4h),2.32(s,3h),1.70(m,2h),1.60(t,3h),0.98(t,3h).
[0209]
向100ml三颈瓶中加入二氧六环(10ml)、化合物v-4(5g)、碘化亚铜 (30mg)2,2
’‑
联吡啶(140mg)、氮气置换空气5次,加热回流搅拌12小时,反应完全后,降至室温,缓慢滴入水(10ml),大量白色固体析出,过滤,烘干得到标题化合物(4g),收率94%。
[0210]1h nmr(400mhz,cdcl3):δ10.81(s,1h),8.83(d,j=2.4hz,1h),7.84(dd,j =8.8,2.4hz,1h),7.14(d,j=8.8hz,1h),4.37(q,j=7.0hz,2h),4.27(s,3h), 3.10(br s,4h),2.93(t,j=7.4hz,2h),2.50(br s,4h),2.27(s,3h),1.86(q,j=7.5hz,2h),1.64(t,j=6.9hz,3h),1.02(t,j=7.3hz,3h);
13
c nmr(100mhz, cdcl3):δ159.3,153.6,147.0,146.4,138.4,131.6,131.2,129.0,124.5,121.1, 113.0,66.1,54.0,45.8,45.6,38.2,27.7,22.2,14.5,14.0;ms(esi)m/z:475.2(m +h
+
).
16(8.28g)、氮气置换空气5次,0-10℃,加入nahco3(17.6g), 25-30℃搅拌12小时,反应完全后,缓慢滴入水(20ml)中,大量白色固体析出,过滤,烘干得到v-3(12.8g),收率90%。
[0224]
向100ml三颈瓶中加入二氧六环(20ml)、化合物v-3(6.9g)、氯化亚铜(394mg)和碳酸钾(14.5g)、氮气置换空气5次,90℃搅拌12小时,反应完全后,缓慢滴入水(20ml),大量白色固体析出,过滤,烘干得到标题化合物(5.98g),收率96%。
[0225]1hnmr(400mhz,cdcl3)δ11.14(s,1h),8.48(d,j=8.0hz,1h),7.46 (m 1h),7.15(m 1h),7.04(d,j=8.4hz,1h),4.35
–
4.23(m,5h),2.95(t,j=7.6 hz,2h),1.95
–
1.83(m,2h),1.61(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h). hrms(esi)计算值:c
17h21
n4o2,[m+h
+
]313.16645,实测值:313.16580。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1