引物组、包含该引物组的试剂盒以及该引物组的用途的制作方法
引物组、包含该引物组的试剂盒以及该引物组的用途
1.本技术是申请日为2020年12月7日、申请号为202011428705.5、发明名称为“引物组、包含该引物组的试剂盒以及该引物组的用途”的发明专利申请的分案申请。
技术领域
2.本发明涉及基因检测技术领域,更特别涉及引物组、包含该引物组的试剂盒以及该引物组的用途。
背景技术:
3.sma是严重困扰人类的典型性疾病,其特点是:(1)是国家第一批罕见病名录中列入的疾病;(2)早诊早筛意义重大,一旦致死,致残比例较高;(3)sma致病率为万分之0.6
‑
2;(4)致病机理和位点明确。
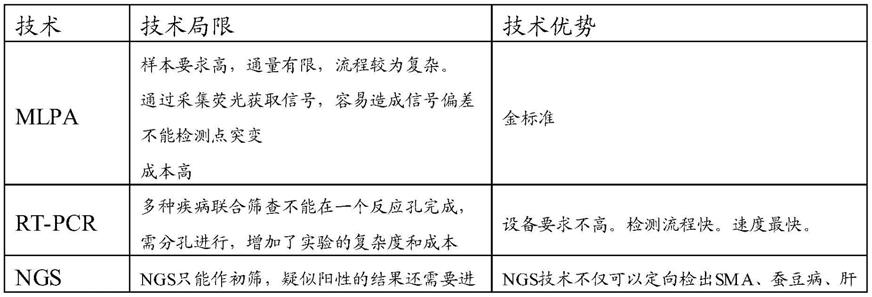
4.现有技术中,可以通过基因检测技术对这种疾病的热门点突变进行检测,来诊断是否患病。概括而言,可以具体使用的基因检测技术包括mlpa、rt
‑
pcr以及ngs。这些基因检测技术优缺点如下表所示:
[0005][0006][0007]
由上表可见,mlpa、rt
‑
pcr以及ngs均存在流程复杂且成本高的缺点。
[0008]
与此同时,massarray技术是通过单碱基延伸,利用差异碱基间分子量的差异来区分检测位点的方法,其能直接准确的检测所测检点碱基类型,特异性强;不使用荧光探针,避免了相似位点的荧光干扰,检测结果精确。该技术可以实现一个反应完成实验,不使用荧光探针,实验成本低。
[0009]
因此,需要提供一种利用massarray技术对sma进行基因检测,进而实现以下优点:一个反应即可对多个基因位点突变进行测定、排除了反应孔之间的干扰、操作简单、筛查成本低、对样本要求低,干血斑、全血标本均能很好检出且适合普筛。
技术实现要素:
[0010]
为了解决上述技术问题,本发明的第一方面提供用于检测sma中相关突变位点的
引物组,其中所述引物组包括扩增引物和延伸引物,所述扩增引物的序列如seq id nos.:7
‑
12所示,所述延伸引物的序列如seq id nos.:60
‑
62所示。
[0011]
本发明的第二方面提供一种用于检测sma中相关突变位点的试剂盒,其包括根据第一方面所述的引物组。
[0012]
在一种实施方案中,根据本发明第二方面所述的试剂盒还包括pcr扩增反应试剂、碱性磷酸酶处理试剂和单碱基延伸反应试剂。
[0013]
在一种实施方案中,根据本发明第一方面所述的引物组或根据本发明第二方面所述的试剂盒,其中所述突变位点的信息为sma1 e7:nm_000344.4:c.840c>t、sma2 e7:nm_017411.4:c.840t>c、sma1 e8:nm_000344.4:c.*239=、sma2 e8:nm_017411.4:c.*239=。
[0014]
本发明的第三方面提供根据本发明第一方面所述的引物组在制备用于筛查sma的试剂盒中的用途。
[0015]
在一种实施方案中,本发明的第三方面所述的用途中,所述筛查sma包括以下步骤:
[0016]
s1.从样本中提取dna;
[0017]
s2.利用本发明第一方面所述的所述的扩增引物和上述步骤s1中所述的dna进行多重pcr扩增反应;
[0018]
s3.对上述步骤s2的扩增产物进行去磷酸化反应;
[0019]
s4.使用本发明第二方面所述的所述的延伸引物对上述步骤s3获得的产物进行延伸反应;
[0020]
s5.对上述步骤s4获得的产物进行纯化;
[0021]
s6.通过massarray技术测量上述步骤s5获得的纯化产物中被延伸的延伸引物的分子量,并利用差异碱基间分子量的差异检测所述相关突变位点的碱基类型;
[0022]
s7.基于上述步骤s6检测到的碱基类型,判断受检者是否患有sma。
[0023]
本发明取得了如下有益技术效果:
[0024]
(1)massarray技术检测sma,判读算法准确性高,通量大,筛查成本低;且对样本要求低,干血斑、全血标本均能很好检出,适合普筛;
[0025]
(2)massarray技术检测通过单碱基延伸,利用差异碱基间分子量的差异来区分检测位点,能直接准确的检测所测检点碱基类型,特异性强;不使用荧光探针,避免了相似位点的荧光干扰,检测结果精确。一个反应完成实验,不使用荧光探针,实验成本低。
附图说明
[0026]
图1是sma检测位点质谱图。
[0027]
图2是内参基因rpp40质谱图。
具体实施方式
[0028]
参考以下本技术的优选实施方案的详述以及包括的实施例可更容易地理解本公开内容。
[0029]
除非另有限定,本文使用的所有技术以及科学术语具有与本技术所属领域普通技术人员通常理解的相同的含义。当存在矛盾时,以本说明书中的定义为准。
[0030]
如本文所用,术语“由
…
制备”与“包含”同义。本文中所用的术语“包含”、“包括”、“具有”、“含有”或其任何其它变形,意在覆盖非排它性的包括。
[0031]
连接词“由
…
组成”排除任何未指出的要素、步骤或组分。如果用于权利要求中,此短语将使权利要求为封闭式,使其不包含除那些描述的材料以外的材料,但与其相关的常规杂质除外。当短语“由
…
组成”出现在权利要求主体的子句中而不是紧接在主题之后时,其仅限定在该子句中描述的要素;其它要素并不被排除在作为整体的所述权利要求之外。
[0032]
当量、浓度、或者其它值或参数以范围、优选范围、或一系列上限优选值和下限优选值限定的范围表示时,这应当被理解为具体公开了由任何范围上限或优选值与任何范围下限或优选值的任一配对所形成的所有范围,而不论该范围是否单独公开了。例如,当公开了范围“1至5”时,所描述的范围应被解释为包括范围“1至4”、“1至3”、“1
‑
2”、“1
‑
2和4
‑
5”、“1
‑
3和5”等。当数值范围在本文中被描述时,除非另外说明,否则该范围意图包括其端值和在该范围内的所有整数和分数。
[0033]
如本文所用,术语“sma”(spinal muscular atrophy,脊肌萎缩症)是一种常染色体隐性遗传性进行性运动神经元病,以脊髓前角细胞和脑干运动性脑神经核的进行性变性为主要特征。临床主要表现为进行性、对称性肌无力和萎缩,近端重于远端,下肢重于上肢。该病患儿在新生儿中约占1/10000,而致病基因携带者约占1/50。根据发病年龄和临床表现可分为4型,即小于6个月起病的脊肌萎缩症ⅰ型(spinal muscular atrophy typeⅰ,sma1,也称作werdnig
‑
hoffmann disease)、6~18个月起病的脊肌萎缩症ⅱ型(spinal muscular atrophy typeⅱ,sma2)、儿童期或青少年起病的脊肌萎缩症ⅲ型(spinal muscular atrophy typeⅲ,sma3,也称作kugelherg
‑
welander disease)和成年起病的脊肌萎缩症ⅳ型(spinal muscular atrophy typeⅳ,sma4)。4种亚型的sma致病基因相同,为运动神经元存活基因1(survival motor neuronl,smn1)[omim600354]。smn1基因位于5号染色体,全长约20kb,含9个外显子。与其紧邻的smn2和smn1高度同源,仅有5个核昔酸的差异。smn2为调节基因,其拷贝数与sma的病情严重程度成反比。
[0034]
第一引物组、包含该第一引物组的试剂盒以及该第一引物组的用途
[0035]
本发明的第一方面提供用于检测sma中相关突变位点的引物组,其中所述引物组包括扩增引物和延伸引物,所述扩增引物的序列如seq id nos.:7
‑
12所示,所述延伸引物的序列如seq id nos.:60
‑
62所示。
[0036]
本发明的第二方面提供一种用于检测检测sma中相关突变位点的试剂盒,其包括根据第一方面所述的引物组。
[0037]
在一种实施方案中,根据本发明第二方面所述的试剂盒还包括pcr扩增反应试剂、碱性磷酸酶处理试剂和单碱基延伸反应试剂。
[0038]
在一种实施方案中,根据本发明第一方面所述的引物组或根据本发明第二方面所述的试剂盒,其中所述突变位点的信息为sma1 e7:nm_000344.4:c.840c>t、sma2 e7:nm_017411.4:c.840t>c、sma1 e8:nm_000344.4:c.*239=、sma2 e8:nm_017411.4:c.*239=。
[0039]
本发明的第三方面提供根据本发明第一方面所述的引物组在制备用于筛查sma的试剂盒中的用途。
[0040]
在一种实施方案中,本发明的第三方面所述的用途中,所述筛查sma包括以下步骤:
[0041]
s1.从样本中提取dna;
[0042]
s2.利用本发明第一方面所述的所述的扩增引物和上述步骤s1中所述的dna进行多重pcr扩增反应;
[0043]
s3.对上述步骤s2的扩增产物进行去磷酸化反应;
[0044]
s4.使用本发明第二方面所述的所述的延伸引物对上述步骤s3获得的产物进行延伸反应;
[0045]
s5.对上述步骤s4获得的产物进行纯化;
[0046]
s6.通过massaarray技术测量上述步骤s5获得的纯化产物中被延伸的延伸引物的分子量,并利用差异碱基间分子量的差异检测所述相关突变位点的碱基类型;
[0047]
s7.基于上述步骤s6检测到的碱基类型,判断受检者是否患有sma。
[0048]
在一种实施方案中,根据本发明的第三方面所述的用途中,所述样本来自人,优选来自体液、血液、血清、血浆、尿、唾液、汗液、痰、精液、粘液、泪液、淋巴液、羊水、间质液、肺灌洗液、脑脊液、粪便和组织样本,更优选为新鲜或冷冻抗凝血。
[0049]
在一种实施方案中,根据本发明的第三方面所述的用途中,所述去磷酸化反应使用碱性磷酸酶实现,优选使用sap实现。
[0050]
在一种实施方案中,根据本发明的第三方面所述的用途中,所述纯化使用树脂实现。
[0051]
在一种实施方案中,根据本发明的第三方面所述的用途中,所述利用差异碱基间分子量的差异检测所述相关突变位点的碱基类型通过使用软件typer4.0实现。
[0052]
优选实施例
[0053]
下面结合说明书附图,进一步对本发明的优选实施例进行详细描述,以下的描述为示例性的,并非对本发明的限制,任何的其他类似情形也都落入本发明的保护范围之中。
[0054]
1、反应混合液配置
[0055]
1.1 pcr引物混合液配置
[0056]
如下表格,pcr primer mix配置表:
[0057][0058][0059]
把扩增引物配成混合液pcr primer mix,pcr扩增引物在混合液中终浓度为0.5~1μm,优选在同一个反应孔中进行pcr扩增反应。;
[0060]
所述扩增引物信息如下表所示:
[0061][0062]
1.2 pcr反应混合液配置
[0063]
pcr反应混合液体系:
[0064][0065]
1.3 sap反应混合液配置
[0066]
sap反应混合液体系:
[0067][0068][0069]
1.4延伸引物混合液配置
[0070]
如下表格,iplex primer mix配置表:
[0071]
检测疾病检测基因snp id延伸引物延伸引物在混合液中的浓度内参rpp40rpp40rpp40_e5~15μmsmasmn1、smn2smn_e7smn1
‑
2_e7_e5~15μmsmasmn1、smn2smn_e8smn1
‑
2_e8_e5~15μm
[0072]
把延伸引物配成混合液iplex primer mix,延伸引物在混合液中终浓度为5~15μm,优选在同一个反应孔中进行延伸反应;
[0073]
所述延伸引物信息如下:
[0074][0075]
1.5延伸反应混合液配置
[0076]
延伸反应混合液体系
[0077][0078]
2、基因组dna获得
[0079]
新鲜或冷冻抗凝血标本用英芮城磁珠法血液基因组dna提取试剂盒提取基因组dna,
[0080]
血斑卡标本用英芮城磁珠法血斑基因组dna提取试剂盒提取基因组dna。
[0081]
gdna为阴性对照,正常人样本。promega购买的human genomic dna,货号g1471。
[0082]
3、多重扩增环节
[0083]
3.1 pcr扩增环节
[0084]
混匀1.2配置的pcr反应混合液体后,分装到384孔板对应的反应孔中,每孔分装4μl,然后加入1μl待检样本。每次检测时需含阴性对照gdna和空白对照水。贴紧贴膜,稍稍离心后放置基因扩增仪上,按以下pcr程序进行扩增:
[0085][0086]
3.2 sap纯化环节
[0087]
向3.1pcr结束的每孔pcr扩增反应产物中加入2μl sap反应混合液(1.3配置),贴紧贴膜,稍稍离心后放置基因扩增仪上,按以下sap程序进行纯化:
[0088]
37℃40min85℃5min8℃hold
[0089]
3.3延伸反应环节
[0090]
向3.2 sap结束的每孔sap纯化反应产物中加入2μl延伸反应混合液(1.5配置),贴紧贴膜,稍稍离心后放置基因扩增仪上,按以下延伸反应程序进行延伸:
[0091][0092]
4、脱盐处理、质谱仪打谱
[0093]
延伸反应程序结束后,瞬时离心。每孔加入16μl的灭菌双蒸水,6mg洁净树脂(resin,agena公司的clean resin)。颠倒混匀15min,离心力3200x g离心5min。样本点样,打谱。该质谱仪打谱使用massarray方法进行,具体针对的检测位点如下表所示:
[0094][0095]
5、数据分析和检测结果判读
[0096]
仪器配套软件typer4.0导出的原始文件.xml档,路径view
→
plate data pane;call列结果是snp检测位点基因型结果
[0097]
上述延伸引物扩增后用质谱测试的结果如下表所示:
[0098][0099]
检测结果比较
[0100]
7例样本:1例阴参、5例正常人、1例有突变患者
[0101]
massarray方法检测和金标方法检测结果比较结果如下表所示:
[0102][0103]
由上表的测试结果可以,与金标方法相比,本发明的massarray方法取得了至少相同,甚至更优的测试结果,取得了明显的有益技术效果。
[0104]
前述的示例仅是说明性的,用于解释本公开的特征的一些特征。所附的权利要求旨在要求可以设想的尽可能广的范围,且本文所呈现的实施例仅是根据所有可能的实施例的组合的选择的实施方式的说明。因此,申请人的用意是所附的权利要求并不被说明本技术的特征的示例的选择限制。如在权利要求中使用的,术语“包括”和其语意上的变体在逻辑上也包括不同和变化的用语,例如但不限于“基本组成为”或“组成为”。当需要时,提供了一些数值范围,而这些范围也包括了在其之间的子范围。这些范围中的变化也对于本领域技术人员也是自明的,且不应被认为被捐献给公众,而这些变化也应在可能的情况下被解释为被所附的权利要求覆盖。而且在科技上的进步将形成由于语言表达的不准确的原因而未被目前考虑的可能的等同物或子替换,且这些变化也应在可能的情况下被解释为被所附的权利要求覆盖。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1