噁唑酰草胺的合成方法与流程
1.本发明属于有机分子合成领域,涉及一种噁唑酰草胺的合成方法。
背景技术:
2.除草剂(herbicide)是指可使杂草彻底地或选择地发生枯死的药剂,又称除莠剂,用以消灭或抑制植物生长的一类物质。世界除草剂发展渐趋平稳,主要发展高效、低毒、广谱、低用量的品种,对环境污染小的一次性处理剂逐渐成为主流。
3.噁唑酰草胺的化学名称为:(r)
‑2‑
[4
‑
(6
‑
氯
‑
1,3
‑
苯并恶唑
‑2‑
基氧)苯氧基]
‑
n
‑
(2
‑
氟苯基)
‑
n
‑
甲基丙酰胺,英文名称:(r)
‑2‑
[4
‑
(6
‑
chlorobenzo[d]oxazol
‑2‑
yloxy)phenoxy]
‑
n
‑
(2
‑
fluorophenyl)
‑
n
‑
methylpropionamide。化学结构如式
ⅵ
所示:
[0004][0005]
噁唑酰草胺是芳氧苯氧丙酸酯类(aopp)除草剂,能抑制乙酰辅酶a羧化酶(acc酶),促进植物脂肪酸合成。噁唑酰草胺作为一种乙酰辅酶a羧化酶抑制剂,用于水稻田茎叶处理,可有效防除直播与移栽水稻田主要杂草,如稗草、马唐、千金子和牛筋草。该药经茎叶吸收,通过维管束传导至生长点,达到除草效果。推荐剂量下使用,对水稻安全制剂:10%乳油,10%可湿性粉剂。
[0006]
目前,噁唑酰草胺的合成工艺主要有:
[0007]
1.由原料(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基丙酸和酰氯化试剂经酰氯化反应得到中间体(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基丙酰氯;在缚酸剂的作用下,(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基丙酰氯与高纯度的n
‑
甲基
‑2‑
氟苯胺发生取代反应得到噁唑酰草胺。该方法需要用到酰氯化试剂,会产生大量的废气或者废水。且反应后体系是强酸性的,遇水后很容易使产品分解,纯度低,对保持条件要求苛刻。
[0008][0009]
2.由原料(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基丙酸和n
‑
甲基邻氟苯胺一步脱水生产噁唑酰草胺。该方法用到大量的三苯基膦,成本昂贵,产生含磷废水,对环境很不友好,最主要的是,反应收率太低,只有23%。
[0010][0011]
3.原料(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基
‑
n
‑
(2氟苯基)丙酰胺经nah脱氢后与碘甲烷进行亲核取代反应得到噁唑酰草胺。该方法使用的试剂nah太危险,导致工业化生产风险大,同时碘甲烷毒性大、价格昂贵,没法实现大规模工业生产。
[0012][0013]
综上,现有的噁唑酰草胺合成方法都有各自弊端,成本高,三废多,得到的产品纯度低。
技术实现要素:
[0014]
本发明的目的是通过以下技术方案实现的:
[0015]
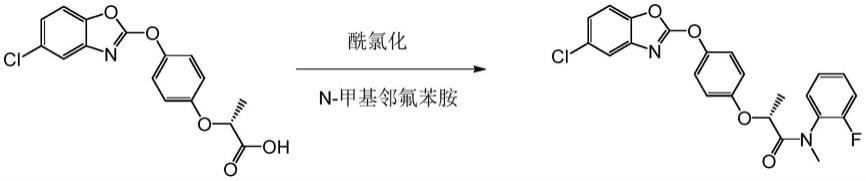
一种噁唑酰草胺的合成方法,合成路线为:
[0016][0017]
[0018]
包括以下步骤:
[0019]
步骤(1)、以水为反应溶剂,在温度40~45℃下,r
‑2‑
(4
‑
羟基苯氧基)丙酸与氢氧化钾发生中和反应生成r
‑2‑
(4
‑
羟基苯氧基)丙酸钾盐;以丙酮和水的混合溶剂为反应溶剂,在温度50~53℃下,2,6
‑
二氯苯并噁唑和r
‑2‑
(4
‑
羟基苯氧基)丙酸钾盐发生醚化反应生成2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐;
[0020]
步骤(2)、以水为反应溶剂,在温度5~10℃下,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐和盐酸发生中和反应生成2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸;
[0021]
步骤(3)、以甲苯为反应溶剂,在温度75~77℃下,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸和氯化亚砜发生酰氯化反应生成2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯;
[0022]
步骤(4)、以甲苯为溶剂,以氢氧化钠为缚酸剂,在温度0~5℃(确保酰氯在低温稳定)下,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯和n
‑
甲基
‑2‑
氟苯胺发生酰胺化反应,生成噁唑酰草胺。
[0023]
步骤(1)中,所述的r
‑2‑
(4
‑
羟基苯氧基)丙酸和氢氧化钾的摩尔比为1:1~1:6,优选为1:6。
[0024]
所述的2,6
‑
二氯苯并噁唑和r
‑2‑
(4
‑
羟基苯氧基)丙酸的摩尔比为1.1:1~1.2:1,优选为1.12:1。
[0025]
所述的丙酮和水的混合溶剂是由丙酮和水(不包括r
‑2‑
(4
‑
羟基苯氧基)丙酸与氢氧化钾反应生成的产物水)按照重量比为1:1混合而成。
[0026]
具体的,在温度30℃下,以水为反应溶剂,先投加氢氧化钾搅拌溶解,再投入r
‑2‑
(4
‑
羟基苯氧基)丙酸,升温至40~45℃,常压保温反应,r
‑2‑
(4
‑
羟基苯氧基)丙酸的转化率100%;反应液不处理,直接往反应液中滴加2,6
‑
二氯苯并噁唑和丙酮的混合液,在温度50~53℃下反应,反应结束后,脱去丙酮,抽滤,得到2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐。滤液含有氯化钾,通过蒸发结晶回收氯化钾。
[0027]
步骤(2)中,所述的盐酸为稀盐酸,优选为质量分数10%的盐酸。
[0028]
以hcl计,所述的盐酸和2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐的摩尔比为1:1。
[0029]
具体的,以水为反应溶剂,投入2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐,再滴加稀盐酸,滴加完毕后,在温度5~10℃下保温反应;反应结束后,反应液过滤,得到2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸。滤液含有氯化钾,通过蒸发结晶回收氯化钾。
[0030]
步骤(3)中,所述的2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸和氯化亚砜的摩尔比为1:1~1:1.2,优选为1:1.2。发明人通过筛选发现,若选用草酰氯为氯化试剂,由于草酰氯高毒性、腐蚀性强,并不适用于本发明工艺。
[0031]
优选的,考虑到酰氯化反应产生h2s,采用碱吸收废气。
[0032]
具体的,以甲苯为反应溶剂,投入2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸,升温至45℃,滴加氯化亚砜,滴加完毕后,升温至75~77℃,保温反应,反应结束后,降温至35~40℃,负压脱除甲苯,得到2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯。
[0033]
步骤(4)中,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯和n
‑
甲基
‑2‑
氟苯胺的摩尔比为1:1~1:1.25,优选为1:1.2。
[0034]
所述的2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯和氢氧化钠的摩尔比为1:1~1:1.1。本发明以氢氧化钠为缚酸剂,与酰胺化反应生成的氯化氢发生中和反应生成氯化钠和水,确保反应后体系不是强酸性,从而避免噁唑酰草胺遇水分解,提高了产品收率。
[0035]
具体的,以甲苯为溶剂,投入n
‑
甲基
‑2‑
氟苯胺、氢氧化钠,在温度0~5℃下,滴加2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯,滴加完毕,常压、0~5℃保温反应,反应结束后,负压脱除甲苯,过滤,得到噁唑酰草胺。
[0036]
和现有技术相比,本发明的有益效果:
[0037]
本发明以(r)
‑2‑
(4
‑
((6
‑
氯苯并噁唑)氧基)苯氧基丙酸为原料,不会由原料带入杂质,制得的噁唑酰草胺纯度高,光学纯度不随反应体系改变。
[0038]
本发明操作简单,没有危险步骤,安全可靠;本发明降低了生产成本,不会产生大量影响环保的三废,总收率在87%左右,适合工业化大生产。
具体实施方式
[0039]
下面通过具体实施方式对本发明的技术方案做进一步说明。
[0040]
实施例1
[0041]
一种噁唑酰草胺的合成方法,步骤如下:
[0042]
步骤(1)、在500ml四口瓶中,加入水57.5g、氢氧化钾76.5g,30℃搅拌溶解后,投入r
‑2‑
(4
‑
羟基苯氧基)丙酸(式ⅰ)41.5g,升温至40℃,常压保温2小时,生成r
‑2‑
(4
‑
羟基苯氧基)丙酸钾盐(式ⅱ),r
‑2‑
(4
‑
羟基苯氧基)丙酸的转化率100%;再向四口瓶内滴加2,6
‑
二氯苯并噁唑48g和丙酮57.5g的混合液,50~53℃常压反应2小时,r
‑2‑
(4
‑
羟基苯氧基)丙酸钾盐的转化率98%,负压脱去丙酮,再抽滤,得到滤饼81g,即为2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐(式ⅲ),收率96%。
[0043][0044]
步骤(2)、在500ml四口瓶中加入水52g,在温度5~10℃、常压下,投入2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐81g,再滴加质量分数10%的盐酸80g(由质量分数为30%的盐酸和水配制成10%的稀盐酸),滴加完毕后保温1小时,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸钾盐的转化率98%,过滤,滤饼即为2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸(式ⅳ)73g,纯度97.5%,收率98%。
[0045][0046]
步骤(3)、在500ml四口瓶中加入180g甲苯、73g2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸,升温至45℃,滴加氯化亚砜31.2g,滴加完毕后,升温至75~77℃,常压,保温1小时,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酸的转化率97%,反应过程中采用碱吸收废气;反应结束后,降温至35~40℃,负压脱出甲苯,得到2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯(式
ⅴ
)74.6g,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯的收率96.8%。
[0047][0048]
步骤(4)、向另一个500ml反应瓶内加入150g甲苯、32.2gn
‑
甲基
‑2‑
氟苯胺、9g氢氧化钠,降温至0~5℃,滴加步骤(3)得到的2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯74.6g,滴加完毕,常压、0~5℃保温1小时,2
‑
(4
‑
((6
‑
氯苯并[d]噁唑
‑2‑
基)氧基)苯氧基)丙酰氯的转化率96%,负压脱除甲苯,过滤,得到噁唑酰草胺(式
ⅵ
)产品92.3g,纯度97%,收率95.5%;总收率87%。
[0049][0050]
对比例1
[0051]
在500ml四口瓶中,加入水57.5g、r
‑2‑
(4
‑
羟基苯氧基)丙酸41.5g,再向四口瓶内滴加2,6
‑
二氯苯并噁唑48g和丙酮57.5g的混合液,50~53℃常压反应,监测反应,反应2h后,未检测到产物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1