一种杂环类化合物及其有机电致发光器件的制作方法
1.本发明涉及有机光电技术领域,具体涉及一种杂环类化合物及其有机电致发光器件。
背景技术:
2.随着信息时代的来临,人机界面新型显示器的研究越来越引起人们的重视,特别是各类平板显示器件技术,其中有机电致发光器件(organic light-emitting device,oled)由于其本身具有更薄更轻、主动发光、视角广、高清晰、图像稳定、色彩丰富、响应快速、低能耗、低温、抗震性能优异、柔性、制作成本低的优点,被越来越多地被应用于手机、个人电子助理(pda)、数码相机、车载显示、笔记本电脑、电视以及军事领域,成为近年来新材料及显示技术领域研究开发的热点。
3.oled的发光原理是:从阴、阳两极分别注入电子和空穴,被注入的电子和空穴在发光层复合形成激子,激子辐射跃迁回到基态,从而发光。oled器件根据出光方向可分为三种类型:底部发光器件、顶部发光器件和两侧发光器件。近年来,顶部发光器件因其具有不受像素电路的限制以及较大的发光面积等优点受到研发工作者的关注。
4.虽然顶发射器件不用考虑像素电路对于出光面积的影响,但是从该发光元件的发光层中发出的光入射到其他膜时,会在ito薄膜和玻璃衬底的界面以及玻璃衬底和空气的界面处发生全反射,致使从发光层发出的光出射到oled器件外部时,其光取出效率受到极大影响。
5.目前,提高oled光取出效率的方法基本包括以下几类:在基底出光表面形成如褶皱、光子晶体、微透镜阵列(mla)和添加表面覆盖层等。前两种方式会影响oled的辐射光谱角度分布,第三种方式制作工艺较为复杂,所以,在oled器件表面添加覆盖层是目前最有效的方式。然而现有技术中覆盖层材料存在折射率较低及薄膜稳定性较差等问题。因此,本领域亟待开发一种新型的具有如下特点的覆盖层材料:(1)高折射率,光取出效率高;(2)高玻璃化转变温度,高分解温度,材料能蒸镀但不会热分解;(3)材料所成薄膜的稳定性高、耐久性优异,寿命长。
技术实现要素:
6.为了解决上述有机电致发光器件内部由于全反射导致的光取出效率降低的问题,本发明提供了一种杂环类化合物及其有机电致发光器件,能显著提高有机电致发光器件的光取出效率,进而提高有机电致发光器件的发光效率。
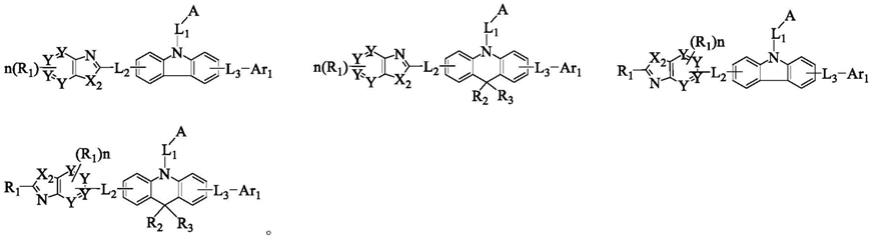
7.具体的,本发明提供了一种杂环类化合物,所述杂环化合物由式i表示:
8.9.在式i中,所述x1选自单键或cr2r3,所述r2、r3相同或不同的选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中的任一种;
10.所述x2选自o、s或nr4,所述r4选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中的任一种;
11.所述y独立的选自c原子或n原子;
12.所述r1选自氢、氘、氰基、卤素原子、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种;
13.所述n选自0、1、2、3或4,当n大于1时,两个或多个r1彼此相同或不同,或相邻的两个r1之间键合形成取代或未取代的环;
14.所述a选自下列基团:
15.其中,所述x3选自o、s或cr5r6,所述r5、r6相同或不同的选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中的任一种;
16.所述e1选自取代或未取代的苯基、取代或未取代的萘基、取代或未取代的苯并呋喃基、取代或未取代的苯并噻吩基、取代或未取代的茚基中的任一种;
17.所述“取代或未取代的苯基”、“取代或未取代的萘基”、“取代或未取代的苯并呋喃基”、“取代或未取代的苯并噻吩基”、“取代或未取代的茚基”中取代的基团选自下列基团中的任意一个或一个以上:氘、氰基、c1~c12的烷基、c3~c12的环烷基、c6~c30的芳基、c3~c30的杂芳基;当有多个取代基存在时,多个取代基彼此相同或不同;
18.所述ra选自氢、氘、氰基、卤素原子、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种;
19.所述m选自0、1、2、3或4,当m大于1时,两个或多个ra彼此相同或不同,或相邻的两个ra之间可键合形成取代或未取代的环;
20.所述l1~l3独立的选自单键、取代或未取代的c6~c30的亚芳基、取代或未取代的c3~c30的亚杂芳基中的任一种;
21.所述ar1选自氢、氘、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种。
22.本发明还提供了一种有机电致发光器件,包含阳极、有机物层以及阴极,所述有机物层位于所述阳极与阴极之间或位于所述阳极或阴极中的一个或一个以上电极的外侧,所述有机物层包含本发明所述的杂环类化合物。
23.有益效果:
24.本发明提供的杂环类化合物具有较大的刚性以及良好的平面性,使其杂环类化合物具有较高的玻璃化转变温度,薄膜状态下不易结晶,具有良好的热稳定性及成膜性;另一
方面,杂环类化合物可提高极化率,进而折射率提高,将其应用于有机电致发光器件的覆盖层时,可减少器件出光时发生的全反射现象,有效提高器件的光取出效率,进而提高有机电致发光器件的发光效率。
25.综上所述,本发明提供的杂环类化合物具有较高的折射率、较高的玻璃化转变温度、良好的成膜性和热稳定性,将其应用于有机电致发光器件的覆盖层时,能有效提高有机电致发光器件的发光效率,延长器件的使用寿命,本发明所述的杂环类化合物在有机电致发光器件中具有良好的应用前景。
具体实施方式
26.下面将结合本发明实施例的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本发明所限定的范围。
27.在本说明书中,意指与另一取代基连接的部分。
28.本发明所述的卤素原子实例可包括氟、氯、溴和碘。
29.本发明所述的烷基是指烷烃分子中去掉一个氢原子而成的烃基,可为直链烷基、支链烷基,优选具有1至12个碳原子,更优选具有1至10个碳原子,特别优选具有1至6个碳原子,实例可包括甲基、乙基、丙基、异丙基、正丁基、叔丁基、异丁基、戊基、异戊基、己基等,但不限于此。
30.本发明所述的环烷基是指烷烃分子中去掉两个氢原子而成环的烃基,优选具有3至14个碳原子,更优选具有3至12个碳原子,特别优选具有3至6个碳原子,实例可包括环戊基、环己基、金刚烷基、降冰片烷基等,但不限于此。
31.本发明所述的芳基是指芳烃分子的芳核碳上去掉一个氢原子后,剩下一价基团的总称,可为单环芳基、多环芳基或稠环芳基,优选具有6至30个碳原子,更优选具有6至22个碳原子,再优选具有6至18个碳原子,进一步优选具有6至14个碳原子,最优选具有6至12个碳原子,实例可包括苯基、联苯基、三联苯基、萘基、蒽基、芘基、菲基、三亚苯基、芴基、苯并芴基、苝基等,但不限于此。
32.本发明所述的杂芳基是指由碳和杂原子构成的芳杂环的核碳上去掉一个氢原子,剩下一价基团的总称,所述杂原子可为n、o、s中的一个或多个,可为单环杂芳基、多环杂芳基或稠环杂芳基,优选具有3至30个碳原子,更优选具有3至22个碳原子,再优选具有3至18个碳原子,进一步优选具有3至12个碳原子,最优选3至8个碳原子,实例可包括吡啶基、嘧啶基、三嗪基、噻吩基、吡咯基、呋喃基、吲哚基、喹啉基、异喹啉基、苯并噻吩基、苯并呋喃基、二苯并呋喃基、二苯并噻吩基、苯并二苯并呋喃基、苯并二苯并噻吩基、噁唑基、噻唑基、苯并噁唑基、苯并噻唑基、萘并噁唑基、萘并噻唑基、咔唑基、苯并咔唑基、吩嗪基、咪唑基、喹喔啉基、喹唑啉基、嘌呤基等,但不限于此。
33.本发明所述的亚芳基是指芳烃分子的芳核碳上去掉二个氢原子后,剩下二价基团的总称,可为单环亚芳基、多环亚芳基或稠环亚芳基,优选具有6至30个碳原子,更优选具有6至22个碳原子,再优选具有6至18个碳原子,进一步优选具有6至14个碳原子,最优选具有6至12个碳原子,实例可包括亚苯基、亚联苯基、亚三联苯基、亚萘基、亚蒽基、亚芘基、亚菲
基、亚三亚苯基、亚芴基、亚苯并芴基、亚苝基等,但不限于此。
34.本发明所述的亚杂芳基是指由碳和杂原子构成的芳杂环的核碳上去掉二个氢原子,剩下二价基团的总称,所述杂原子可为n、o、s中的一个或多个,可为单环亚杂芳基、多环亚杂芳基或稠环亚杂芳基,优选具有3至30个碳原子,更优选具有3至22个碳原子,进一步优选具有3至12个碳原子,再优选具有3至18个碳原子,最优选3至8个碳原子,实例可包括亚吡啶基、亚嘧啶基、亚三嗪基、亚噻吩基、亚吡咯基、亚呋喃基、亚吲哚基、亚喹啉基、亚异喹啉基、亚苯并噻吩基、亚苯并呋喃基、亚二苯并呋喃基、亚苯并二苯并呋喃基、亚苯并二苯并噻吩基、亚二苯并噻吩基、亚噁唑基、亚噻唑基、亚苯并噁唑基、亚苯并噻唑基、亚萘并噁唑基、亚萘并噻唑基、亚咔唑基、亚吩嗪基、亚咪唑基、亚喹喔啉基、亚喹唑啉基、亚嘌呤基等,但不限于此。
35.本发明所述的“取代”指化合物基团中的氢原子被替换成其他原子或基团,且取代的位置不受限制。
36.本发明所述的“取代或未取代的”中所述取代基可以独立的选自氘、氰基、硝基、卤素原子、取代或未取代的c1~c12的烷基、取代或未取代的c1~c12的烷氧基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c6~c30的芳氧基、取代或未取代的c3~c30的杂芳基,取代或未取代的c1~c30的硅烷基、取代或未取代的c6~c30的芳胺基中的任意一个,优选氘、卤素原子、氰基、c1~c10的烷基、c3~c12的环烷基、c6~c30的芳基、c3~c30的杂芳基,具体实例可包括氘、氰基、硝基、卤素原子、甲基、乙基、正丙基、异丙基、叔丁基、金刚烷基、降冰片烷基、甲氧基、苯基、联苯基、三联苯基、萘基、蒽基、芘基、菲基、三亚苯基、吩噻嗪基、嘧啶基、吩噁嗪基、9,9-二甲基芴基、9,9-二苯基芴基、苯氧基、呋喃基、咔唑基、噻吩基、苯并呋喃基、苯并噻吩基、二苯并呋喃基、二苯并噻吩基、吖啶基、哌啶基、吡啶基、三苯基硅基、三甲基硅基、吡嗪基、三嗪基、苯并噁唑基、苯并噻唑基等,但不限于此。
37.本发明所述的连接成环是指两个基团通过化学键彼此连接并任选地进行芳构化。如下所示例:
[0038][0039]
本发明中,连接形成的环可以为五元环或六元环或者稠合环,例如苯、萘、芴、环戊烯、环戊烷、环己烷并苯、喹啉、异喹啉、二苯并噻吩、菲或芘,但不限于此。
[0040]
本发明提供了一种杂环类化合物,具有式i表示的结构:
[0041][0042]
在式i中,所述x1选自单键或cr2r3,所述r2、r3相同或不同的选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中
的任一种;
[0043]
所述x2选自o、s或nr4,所述r4选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中的任一种;
[0044]
所述y独立的选自c原子或n原子;
[0045]
所述r1选自氢、氘、氰基、卤素原子、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种;
[0046]
所述n选自0、1、2、3或4,当n大于1时,两个或多个r1彼此相同或不同,或相邻的两个r1之间键合形成取代或未取代的环;
[0047]
所述a选自下列基团:
[0048]
其中,所述x3选自o、s或cr5r6,所述r5、r6相同或不同的选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基中的任一种;
[0049]
所述e1选自取代或未取代的苯基、取代或未取代的萘基、取代或未取代的苯并呋喃基、取代或未取代的苯并噻吩基、取代或未取代的茚基中的任一种;所述“取代或未取代的苯基”、“取代或未取代的萘基”、“取代或未取代的苯并呋喃基”、“取代或未取代的苯并噻吩基”、“取代或未取代的茚基”中取代的基团选自下列基团中的任意一个或一个以上:氘、氰基、c1~c12的烷基、c3~c12的环烷基、c6~c30的芳基、c3~c30的杂芳基;当有多个取代基存在时,多个取代基彼此相同或不同;
[0050]
所述ra选自氢、氘、氰基、卤素原子、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种;
[0051]
所述m选自0、1、2、3或4,当m大于1时,两个或多个ra彼此相同或不同,或相邻的两个ra之间键合形成取代或未取代的环;
[0052]
所述l1~l3独立的选自单键、取代或未取代的c6~c30的亚芳基、取代或未取代的c3~c30的亚杂芳基中的任一种;
[0053]
所述ar1选自氢、氘、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c3~c12的环烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任一种。
[0054]
优选的,所述式i化合物选自下列结构中的任一种:
[0055][0056][0057]
优选的,所述式i化合物选自下列结构中的任一种:
[0058][0059]
优选的,所述a选自下列基团中的任一种:
[0060][0061]
所述r7彼此相同或不同,选自氢、氘、氰基、c1~c12的烷基、c3~c12的环烷基、c6~c30的芳基、c3~c30的杂芳基中的任意一种;
[0062]
所述i1选自0、1、2或3,i2选自0、1、2、4、5或6,i3选自0、1、2、3或4,i4选自0、1、2、3、4或5,i5选自0、1、2、3、4、5、6、7或8,i6选自0、1、2、3、4、5、6或7。
[0063]
再优选的,所述a选自下列基团中的任一种:
[0064][0065][0066]
优选的,所述ar1选自氢、氘、氰基、金刚烷基、降冰片烷基、取代或未取代的苯基、
取代或未取代的萘基、取代或未取代的联苯基、取代或未取代的三联苯基、取代或未取代的蒽基、取代或未取代的菲基、取代或未取代的三亚苯基、取代或未取代的芴基、取代或未取代的二苯并呋喃基、取代或未取代的二苯并噻吩基、取代或未取代的咔唑基、取代或未取代的苯并噁唑基、取代或未取代的苯并噻唑基、取代或未取代的苯并咪唑基、取代或未取代的吡啶并噁唑基、取代或未取代的吡啶并噻唑基、取代或未取代的吡啶并咪唑基中的任一种;所述“取代或未取代的”中取代的基团选自氘、氰基、金刚烷基、降冰片烷基、c1~c6的烷基、c6~c12的芳基、c3~c12的杂芳基中的一个或一个以上,当有多个取代基存在时,多个取代基彼此相同或不同,或两个相邻的取代基之间键合成环。
[0067]
再优选的,所述ar1选自
[0068]
再优选的,所述ar1选自下列基团中的任一种:
[0069]
[0070][0071]
优选的,所述l1~l3独立的选自单键或下列基团中的任一种:
[0072][0073]
优选的,所述中,至少有一个y选自n原子,其余的选自c原子;或者至少有两个y选自n原子,其余的选自c原子;或者至少有三个y选自n原子,其余的选自c原子;至少有四个y选自n原子。
[0074]
优选的,所述选自下列基团中任一种:
[0075][0076]
最优选的,所述式i化合物选自下列结构中的任一种:
[0077]
[0078]
[0079]
[0080]
[0081]
[0082]
[0083]
[0084]
[0085]
[0086]
[0087]
[0088][0089]
以上列举了本发明所述的有机化合物的一些具体结构形式,但本发明并不局限于所列这些化学结构,凡是以化学式ⅰ所示结构为基础,取代基为如上所限定的基团都应包含在内。
[0090]
本发明还提供了一种所述式ⅰ化合物的制备方法,但本发明不限于此:
[0091]
(1)当与选自相同基团时:
[0092][0093]
(2)当与不相同时:
[0094][0095]
hal独立的选自i、br、cl中的任意一种,x1、x2、y、l1~l3、ar1、a限定与上述限定相同;上述制备路线中制备所用到的原料来源可以为市售产品,也可经本领域技术人员熟知的方法制备得到。
[0096]
本发明提供了一种有机电致发光器件,包含阳极、有机物层以及阴极,所述有机物层位于所述阳极与阴极之间或位于所述阳极或阴极中的一个或一个以上电极的外侧,所述有机物层包含本发明所述的杂环类化合物。
[0097]
优选的,本发明所述的有机电致发光器件可以包含一个或一个以上有机物层,所述有机物层可包含空穴注入层、空穴传输层、电子阻挡层、发光辅助层、发光层、空穴阻挡层、电子传输层、电子注入层、覆盖层等,具体的,所述位于阳极与阴极之间的有机物层可包含空穴注入层、空穴传输层、电子阻挡层、发光辅助层、发光层、空穴阻挡层、电子传输层、电子注入层等,所述位于阳极及阴极中的一个以上的电极的外侧的有机层可以包含覆盖层等。所述有机物层可以由单层结构形成,也可以由层叠以上有机层的多层结构形成;同时,所述的各个有机物层还可包含一层或多层结构,具体的,所述空穴传输层包含第一空穴传输层以及第二空穴传输层。但是,有机电致发光器件的结构并不仅限于此,可以包含更少或更多的有机物层。
[0098]
优选的,本发明所述的覆盖层可包含单层或多层结构,例如所述的覆盖层包含第一覆盖层以及第二覆盖层,所述覆盖层选自单一化合物构成的单层结构,两种或两种以上化合物构成的单层结构,两种或两种以上化合物构成的多层结构中的任意一种。
[0099]
优选的,所述覆盖层含有至少一种本发明所述的杂环类化合物。
[0100]
以下对用于本发明所述的有机电致发光器件各功能层的材料进行说明。
[0101]
作为本发明的基板材料,可选用典型的有机发光装置中使用的任何基板。可以是玻璃或透明塑料基板,也可以是不透明材料如硅或不锈钢的基板,还可以是柔性pi膜。不同基板具有不同的机械强度、热稳定性、透明性、表面光滑度、防水性,根据基板的性质不同,使用方向不同。
[0102]
作为本发明的阳极,可以是透射电极、反射电极或半透射电极。当阳极是透射电极时,用于形成阳极的材料可以选自氧化铟锡(ito)、氧化铟锌(izo)、氧化锡(sno2)、氧化锌(zno)或它们的任意组合;当阳极是半透射电极或反射电极时,用于形成阳极的材料可以选自镁(mg)、银(ag)、铝(al)、铝-锂(al-li)、钙(ca)、镁-铟(mg-in)、镁-银(mg-ag)或它们的任意组合。阳极可以具有单层结构或者包括两层或更多层的多层结构,例如,阳极可以具有ito/ag/ito的三层结构,但阳极的结构不限于此。
[0103]
作为本发明的阴极,可以选自透射电极、半反射电极或反射电极。当阴极为透射电
极,用于形成阴极的材料可选自透明金属氧化物(例如,ito、izo、等);当阴极为半反射电极或反射电极,用于形成阴极的材料可选自ag、mg、cu、al、pt、pd、au、ni、nd、ir、cr、li、ca、lif/ca、lif/al、mo、ti、包括它们的化合物或它们的混合物(例如,ag和mg的混合物),但不限于与此。
[0104]
作为本发明的空穴注入层材料,优选具有良好接受空穴能力的材料。具体实例可包括:吩嗪类化合物,酞菁化合物,联苯胺类化合物等材料,如n,n,n',n'-四(4-甲氧基苯基)联苯胺(meo-tpd)、n,n'-二苯基-n,n'-二-[4-(n,n-二苯基胺)苯基]联苯胺(npnpb)、酞菁铜、二喹喔啉并[2,3-a:2',3'-c]吩嗪(hatna)等,但不限于此。
[0105]
作为本发明的空穴传输层材料,优选具有优良的空穴传输性能以及与相应的阳极材料相匹配的homo能级的材料。具体实例可包括二苯胺类化合物,芴类化合物和咔唑类化合物等材料,如4-[1-[4-[二(4-甲基苯基)氨基]苯基]环己基]-n-(3-甲基苯基)-n-(4-甲基苯基)苯胺(tapc)、n,n'-二苯基-n,n'-(1-萘基)-1,1'-联苯-4,4'-二胺(npb)、n,n'-二苯基-n,n'-二(3-甲基苯基)-1,1'-联苯-4,4'-二胺(tpd)等,但不限于此。
[0106]
作为本发明的发光层材料,可以包含主体材料(也称基质材料)和掺杂材料(也称客体材料),发光层材料可包含多个主体材料和多个掺杂材料。发光层可为单一的发光层,也可为横向或纵向叠加在一起的复合发光层。对于掺杂材料的种类选择,可以为荧光材料,也可以为磷光材料。对于掺杂材料的用量选择,优选0.1~70%质量,更优选为0.1~30质量%、进一步优选为1~30质量%、更进一步优选为1~20质量%、特别优选为1~10质量%。
[0107]
可用于本发明的荧光掺杂材料可包括:稠合多环芳族衍生物、苯乙烯基胺衍生物、稠环胺衍生物、含硼化合物、吡咯衍生物、吲哚衍生物、咔唑衍生物等,但不限于此。可用于本发明的磷光掺杂材料可包括:重金属配合物、磷光发光性的稀土类金属配合物等,但不限于此。重金属配合物可举出例如铱配合物、铂配合物、锇配合物等;稀土类金属配合物可举出例如铽络合物、铕络合物等,但不限于此。
[0108]
可用于本发明的主体材料可包括:主体材料包括稠合芳族环衍生物、含杂环的化合物等。具体地,稠合芳族环衍生物包括蒽衍生物、芘衍生物、萘衍生物、并五苯衍生物、菲衍生物、荧蒽衍生物等,以及含杂环的化合物包括咔唑衍生物、二苯并呋喃衍生物、二苯并噻吩衍生物、嘧啶衍生物等,但不限于此。
[0109]
作为本发明的电子传输层材料,优选具有较强吸电子能力及较低的homo及lumo能级的材料。具体实例可包括喹啉类,咪唑类,邻二氮菲衍生物,三唑类等材料,如2,9-(二甲基)-4,7-联苯-1,10-邻二氮菲(bcp)、8-羟基喹啉-锂(liq)、1,3,5-三(1-苯基-1h-苯并咪唑-2-基)苯(tpbi)、3-(联苯-4-基)-5-(4-叔丁基苯基)-4-苯基-4h-1,2,4-三唑(taz)、4,4'-二(4,6-二苯基-1,3,5-三嗪基)联苯(btb)、1,3,5-三[(3-吡啶基)-苯基]苯(tmpypb)、2-(萘-2-基)-4,7-(二苯基)-1,10-邻二氮菲(hnbphen)等,但不限于此。
[0110]
作为本发明的电子注入层材料,优选与临近的有机传输材料或主体材料等的势垒相差较小的材料。具体实例可包括:金属氧化物如al2o3、moo3,碱金属盐如lif、csf,碱土金属盐如mgf2,但不限于此。
[0111]
本发明所述的有机电致发光器件可以通过依次层叠上述的结构而制造。制造方法可使用湿式成膜法、干式成膜法等公知方法。作为湿式成膜法的具体例,可举出旋涂法、浸渍法、流延法、喷墨法等各种涂布法,作为干式成膜法的具体例,可举出真空蒸镀法、溅射
法、等离子体法、离子电镀法等,但不限于此。
[0112]
本发明所述有机发光器件可广泛应用于面板显示、照明光源、柔性oled、电子纸、有机太阳能电池、有机感光体或有机薄膜晶体管、指示牌、信号灯等领域。
[0113]
上述有机电致发光器件的制造在以下实施例中具体地进行说明。但是,下述实施例只是用于例示本说明书,而本说明书的范围并不限定于该实施例。
[0114]
化合物的制备及表征
[0115]
原料、试剂以及表征设备的说明:
[0116]
本发明对以下实施例中所采用的原料来源没有特别的限制,可以为市售产品或采用本领域技术人员所熟知的制备方法制备得到。
[0117]
质谱使用英国沃特斯g2-si四极杆串联飞行时间高分辨质谱仪,氯仿为溶剂;
[0118]
元素分析使用德国elementar公司的vario el cube型有机元素分析仪,样品质量为5~10mg;
[0119]
合成实施例1:化合物1的合成
[0120][0121]
(1)合成中间体c-1
[0122]
在三口瓶中,通氮气保护下,加入原料a-1(23.86g,65mmol),450mldmf,原料b-1(22.24g,136.5mmol),pd(oac)2(0.34g,1.63mmol),dppf(0.13ml,0.24mmol),搅拌,然后加入k3po4水溶液(38.21g,180mmol),加热回流反应24小时,取样点板,反应完全。自然冷却,将混合物抽滤并取滤饼在真空干燥箱中干燥,使用硅胶柱层析法洗脱粗品(pe/ea,2/1,v/v),得到中间体c-1(20.75g,收率72%)。
[0123]
(2)合成化合物1
[0124]
在三口瓶中,通氮气保护下,加入中间体c-1(20.19g,46.2mmol),原料d-1(13.74g,44mmol),450ml甲苯搅拌混合,然后加入pd2(dba)3(0.20g,0.22mmol),p(t-bu)3(0.089g,0.44mmol),naot-bu(10.57g,110mmol),加热回流反应22小时,取样点板,反应完全;自然冷却至室温,过滤,滤液旋蒸至无馏分,所得残余物使用硅胶柱层析法洗脱粗品(pe/dcm,1/1,v/v),最后得到固体化合物1(19.53g,收率67%),hplc检测固体纯度≥99.7%。
[0125]
质谱m/z:659.2237(理论值:659.2209)。理论元素含量(%)c
45h29
n3o3:c,81.92;h,4.43;n,6.37。实测元素含量(%):c,81.78;h,4.61;n,6.21。
[0126]
合成实施例2:化合物33的合成
[0127]
[0128]
将合成实施例1中的a-1换成等摩尔的a-33,其他步骤相同,合成化合物33(17.79g),hplc检测固体纯度≥99.6%。
[0129]
质谱m/z:617.1751(理论值:617.1739)。理论元素含量(%)c
42h23
n3o3:c,81.67;h,3.75;n,6.80。实测元素含量(%):c,81.54;h,3.87;n,6.73。
[0130]
合成实施例3:化合物38的合成
[0131][0132]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-38,其他步骤相同,合成化合物38(19.27g),hplc检测固体纯度≥99.9%。
[0133]
质谱m/z:617.1716(理论值:617.1739)。理论元素含量(%)c
42h23
n3o3:c,81.67;h,3.75;n,6.80。实测元素含量(%):c,81.74;h,3.60;n,6.89。
[0134]
合成实施例4:化合物45的合成
[0135][0136]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-45,其他步骤相同,合成化合物45(18.28g),hplc检测固体纯度≥99.7%。
[0137]
质谱m/z:617.1758(理论值:617.1739)。理论元素含量(%)c
42h23
n3o3:c,81.67;h,3.75;n,6.80。实测元素含量(%):c,81.47;h,3.95;n,6.64。
[0138]
合成实施例5:化合物49的合成
[0139][0140]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-49,其他步骤相同,合成化合物49(18.50g),hplc检测固体纯度≥99.3%。
[0141]
质谱m/z:633.1536(理论值:633.1511)。理论元素含量(%)c
42h23
n3o2s:c,79.60;h,3.66;n,6.63。实测元素含量(%):c,79.47;h,3.85;n,6.73。
[0142]
合成实施例6:化合物57的合成
[0143][0144]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-57,其他步骤相同,合成化合物57(20.03g),hplc检测固体纯度≥99.8%。
[0145]
质谱m/z:633.1487(理论值:633.1511)。理论元素含量(%)c
42h23
n3o2s:c,79.60;h,3.66;n,6.63。实测元素含量(%):c,79.84;h,3.42;n,6.52。
[0146]
合成实施例7:化合物64的合成
[0147][0148]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-64,其他步骤相同,合成化合物64(19.31g),hplc检测固体纯度≥99.6%。
[0149]
质谱m/z:643.2241(理论值:643.2260)。理论元素含量(%)c
45h29
n3o2:c,83.96;h,4.54;n,6.53。实测元素含量(%):c,84.08;h,4.39;n,6.48。
[0150]
合成实施例8:化合物83的合成
[0151][0152]
将合成实施例1中的b-1换成等摩尔的b-83,d-1换成等摩尔的d-83,其他步骤相同,合成化合物83(24.03g),hplc检测固体纯度≥99.4%。
[0153]
质谱m/z:811.2859(理论值:811.2835)。理论元素含量(%)c
57h37
n3o3:c,84.32;h,4.59;n,5.18实测元素含量(%):c,84.11;h,4.83;n,5.06。
[0154]
合成实施例9:化合物101的合成
[0155][0156]
(1)合成中间体d
’‑
101
[0157]
在三口瓶中,通入氮气,加入原料d-1(17.83g,60mmol),450ml甲苯溶剂,原料n-101(10.16,65mmol),pd(oac)2(0.34g,1.5mmol),dppf(0.12ml,0.22mmol),搅拌,然后加入
k3po4水溶液(36.09g,170mmol),加热回流反应8小时,取样点板,反应完全。自然冷却,将混合物过滤并取滤饼在真空干燥箱中干燥,所得粗产物使用甲苯重结晶,得到中间体d
’‑
101(14.2g,收率72%)。
[0158]
(2)合成化合物101
[0159]
将合成实施例1中的a-1换成等摩尔的a-33,d-1换成等摩尔的d-101,其他步骤相同,合成化合物101(21.09g),hplc检测固体纯度≥99.7%。
[0160]
质谱m/z:693.2076(理论值:693.2052)。理论元素含量(%)c
48h27
n3o3:c,83.10;h,3.92;n,6.06。实测元素含量(%):c,83.25;h,3.78;n,5.99。
[0161]
合成实施例10:化合物102的合成
[0162][0163]
将合成实施例9中的d-1换成等摩尔的d-83,n-101换成等摩尔的n-102,其他步骤相同,得到中间体d
’‑
102(14.98g,收率75%)。
[0164]
将合成实施例9中的d
’‑
101换成等摩尔的d
’‑
102,其他步骤相同,合成化合物102(20.38g),hplc检测固体纯度≥99.6%。
[0165]
质谱m/z:697.2329(理论值:697.2303)。理论元素含量(%)c
48h23
d4n3o3:c,82.62;h,4.48;n,6.02。实测元素含量(%):c,82.81;h,4.37;n,5.94。
[0166]
合成实施例11:化合物105的合成
[0167][0168]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-83,其他步骤相同,合成化合物105(23.10g),hplc检测固体纯度≥99.5%。
[0169]
质谱m/z:769.2343(理论值:769.2365)。理论元素含量(%)c
54h31
n3o3:c,84.25;h,4.06;n,5.46。实测元素含量(%):c,84.38;h,3.98;n,5.54。
[0170]
合成实施例12:化合物106的合成
[0171][0172]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-83,d-1换成等摩尔的d-83,其他步骤相同,合成化合物106(24.02g),hplc检测固体纯度≥99.8%。
[0173]
质谱m/z:769.2387(理论值:769.2365)。理论元素含量(%)c
54h31
n3o3:c,84.25;h,4.06;n,5.46。实测元素含量(%):c,84.08;h,4.17;n,5.39。
[0174]
合成实施例13:化合物108的合成
[0175][0176]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-108,d-1换成等摩尔的d-83,其他步骤相同,合成化合物108(26.45g),hplc检测固体纯度≥99.4%。
[0177]
质谱m/z:869.2695(理论值:869.2678)。理论元素含量(%)c
62h35
n3o3:c,85.60;h,4.06;n,4.83。实测元素含量(%):c,85.76;h,3.97;n,4.75。
[0178]
合成实施例14:化合物114的合成
[0179][0180]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-114,d-1换成等摩尔的d-83,其他步骤相同,合成化合物114(22.12g),hplc检测固体纯度≥99.7%。
[0181]
质谱m/z:769.2379(理论值:769.2365)。理论元素含量(%)c
54h31
n3o3:c,84.25;h,4.06;n,5.46。实测元素含量(%):c,84.11;h,4.00;n,5.58。
[0182]
合成实施例15:化合物115的合成
[0183][0184]
(1)合成中间体d
’‑
115
[0185]
将合成实施例9中的d-1换成等摩尔的d-115,其他步骤相同,得到中间体d
’‑
115(15.19g,收率77%)。
[0186]
(2)合成化合物115
[0187]
将合成实施例9中的b-1换成等摩尔的b-115,d
’‑
101换成等摩尔的d
’‑
115,其他步骤相同,合成化合物115(24.77g),hplc检测固体纯度≥99.5%。
[0188]
质谱m/z:793.2391(理论值:793.2365)。理论元素含量(%)c
56h31
n3o3:c,84.72;h,3.94;n,5.29。实测元素含量(%):c,84.91;h,3.75;n,5.35。
[0189]
合成实施例16:化合物123的合成
[0190][0191]
(1)合成中间体b-123
[0192]
在三口瓶中,通氮气保护下,加入中间体m-123(73.81g,320.00mmol),b2pin2(121.89g,480.00mmol)和koac(94.21g,960mmol)溶于dmf(800ml)中,加入pd(dppf)cl2(4.68g,6.40mmol)加热回流反应3小时。待反应结束后,冷却至室温并加入1000ml水,用二氯甲烷萃取,有机层用无水mgso4干燥,浓缩,使用乙酸乙酯重结晶,得到中间体b-123(76.66g,收率74%)。
[0193]
(2)合成化合物123
[0194]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-123,d-1换成等摩尔的d-123,其他步骤相同,合成化合物123(24.26g),hplc检测固体纯度≥99.8%。
[0195]
质谱m/z:797.2815(理论值:797.2791)。理论元素含量(%)c
55h35
n5o2:c,82.79;h,4.42;n,8.78。实测元素含量(%)c,82.86;h,4.25;n,8.86。
[0196]
合成实施例17:化合物136的合成
[0197][0198]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-136,d-1换成等摩尔的d-38,其他步骤相同,合成化合物136(19.33g),hplc检测固体纯度≥99.7%。
[0199]
质谱m/z:619.1664(理论值:619.1644)。理论元素含量(%)c
40h21
n5o3:c,77.54;h,3.42;n,11.30。实测元素含量(%):c,77.67;h,3.25;n,11.41。
[0200]
合成实施例18:化合物137的合成
[0201][0202]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-137,d-1换成等摩尔的d-38,其他步骤相同,合成化合物137(18.34g),hplc检测固体纯度≥99.4%。
[0203]
质谱m/z:619.1621(理论值:619.1644)。理论元素含量(%)c
40h21
n5o3:c,77.54;h,3.42;n,11.30。实测元素含量(%):c,77.31;h,3.67;n,11.22。
[0204]
合成实施例19:化合物141的合成
[0205][0206]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-123,其他步骤相同,合成化合物141(23.16g),hplc检测固体纯度≥99.8%。
[0207]
质谱m/z:771.2241(理论值:771.2270)。理论元素含量(%)c
52h29
n5o3:c,80.92;h,3.79;n,9.07。实测元素含量(%):c,80.73;h,3.95;n,9.17。
[0208]
合成实施例20:化合物155的合成
[0209]
[0210]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-83,d-1换成等摩尔的d-155,其他步骤相同,合成化合物155(24.52g),hplc检测固体纯度≥99.7%。
[0211]
质谱m/z:785.2151(理论值:785.2137)。理论元素含量(%)c
54h31
n3o2s:c,82.53;h,3.98;n,5.35。实测元素含量(%):c,82.68;h,3.81;n,5.41。
[0212]
合成实施例21:化合物173的合成
[0213][0214]
将合成实施例1中的b-1换成等摩尔的b-173,d-1换成等摩尔的d-173,其他步骤相同,合成化合物173(24.78g),hplc检测固体纯度≥99.6%。
[0215]
质谱m/z:825.2901(理论值:825.2926)。理论元素含量(%)c
57h39
n5s:c,82.88;h,4.76;n,8.48。实测元素含量(%):c,82.68;h,4.89;n,8.56。
[0216]
合成实施例22:化合物188的合成
[0217][0218]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-188,其他步骤相同,合成化合物188(19.49g),hplc检测固体纯度≥99.8%。
[0219]
质谱m/z:649.1304(理论值:649.1283)。理论元素含量(%)c
42h23
n3os2:c,77.64;h,3.57;n,6.47。实测元素含量(%):c,77.79;h,3.41;n,6.56。
[0220]
合成实施例23:化合物298的合成
[0221][0222]
(1)合成中间体e-298
[0223]
在三口瓶中,通氮气保护下,加入原料a-298(29.46g,105mmol),500mldmf,原料b-1(17.96g,110.25 84mmol),pd(oac)2(0.43g,1.9mmol),dppf(0.21ml,0.39mmol),搅拌,然后加入k3po4水溶液(53.07g,250mmol),加热回流反应24小时,取样点板,反应完全。自然冷却,将混合物过滤并取滤饼在真空干燥箱中干燥,所得残余物使用硅胶柱层析法洗脱粗品(pe/ea,1/2,v/v),得到中间体e-298(23.43g,收率70%)。
[0224]
(2)合成中间体c-298
[0225]
在三口瓶中,通氮气保护下,加入中间体e-298(22.31g,70mmol),450mldmf,原料f-298(15.83g,74.67mmol),pd(oac)2(0.39g,1.75mmol),搅拌,然后加入k3po4水溶液(42.03g,198mmol),加热回流反应24小时,取样点板,反应完全。自然冷却,将混合物过滤并
取滤饼在真空干燥箱中干燥,所得残余物使用硅胶柱层析法洗脱粗品(pe/ea,2/1,v/v),得到中间体c-298(21.44g,收率68%)。
[0226]
(3)合成化合物298
[0227]
在三口瓶中,通氮气保护下,加入中间体c-298(20.34g,45.15mmol),原料d-298(12.78g,43mmol),450ml甲苯搅拌混合,然后加入pd2(dba)3(0.20g,0.22mmol),p(t-bu)3(0.087g,0.43mmol),naot-bu(10.57g,110mmol),加热回流反应22小时,取样点板,反应完全;自然冷却至室温,过滤,滤液旋蒸至无馏分,所得残余物使用硅胶柱层析法洗脱粗品(pe/dcm,1/3,v/v),最后得到固体化合物298(18.94g,收率66%),hplc检测固体纯度≥99.6%。
[0228]
质谱m/z:666.1919(理论值:666.1943)。理论元素含量(%)c
47h26
n2o3:c,84.67;h,3.93;n,4.20。实测元素含量(%):c,84.78;h,3.81;n,4.33。
[0229]
合成实施例24:化合物299的合成
[0230][0231]
将合成实施例23中的f-298换成等摩尔的b-188,d-298换成等摩尔的d-299,其他步骤相同,合成化合物299(19.27g),hplc检测固体纯度≥99.8%。
[0232]
质谱m/z:633.1537(理论值:633.1511)。理论元素含量(%)c
42h23
n3o2s:c,79.60;h,3.66;n,6.63。实测元素含量(%):c,79.48;h,3.82;n,6.56。
[0233]
合成实施例25:化合物313的合成
[0234][0235]
将合成实施例1中的a-1换成等摩尔的a-33,b-1换成等摩尔的b-313,d-1换成等摩尔的d-38,其他步骤相同,合成化合物313(24.38g),hplc检测固体纯度≥99.8%。
[0236]
质谱m/z:801.1934(理论值:801.1909)。理论元素含量(%)c
54h31
n3os2:c,80.87;h,3.90;n,5.24。实测元素含量(%):c,80.68;h,4.04;n,5.17。
[0237]
实施例26:折射率及玻璃化转变温度的测定
[0238]
折射率采用美国j.a.woollam公司的m-2000光谱型椭偏仪进行测定,首先将玻璃基板进行uv臭氧清洗20分钟,然后将玻璃基板转移至真空蒸镀装置中,将体系内真空度控制在1
×
10-3
pa,在玻璃基板上蒸镀本发明化合物1、33、38、45、49、57、64、83、101、102、105、106、108、114、115、123、136、137、141、155、173、188、298、299、313以及对比化合物1制成薄膜样品,蒸镀厚度为80nm,蒸镀速度为0.1nm/s,对于上述制备的薄膜样品分别在525nm处进行折射率n的测试,折射率测试结果如表1所示:
[0239]
玻璃化转变温度(tg)由示差扫描量热法(dsc,德国耐驰公司dsc204f1示差扫描量
热仪)进行测定,测试样品:化合物1、33、38、45、49、57、64、83、101、102、105、106、108、114、115、123、136、137、141、155、173、188、298、299、313以及对比化合物1,单独测试,每份样品质量为5mg。
[0240]
测试气氛为氮气,氮气的流速为50ml/min;升温速率为为10℃/min,温度范围为50~350℃。玻璃化温度(tg)测试结果如表1所示:
[0241]
表1:玻璃化转变温度及折射率测试结果
[0242][0243][0244]
根据表1可知,一方面,本发明提供的杂环类化合物具有高折射率,满足作为有机电致发光器件覆盖层材料的基本条件,将本发明化合物应用于有机电致发光器件的覆盖层时,能有效提高有机电致发光器件的光取出效率,另一方面,本发明提供的杂环类化合物具有高玻璃化转变温度,薄膜状态下不易结晶,具有良好的热稳定性。
[0245]
[器件实施例1]
[0246]
首先,将ito(15nm)/ag(150nm)/ito(15nm)玻璃基板,放在蒸馏水中清洗2次,超声波洗涤30分钟,再用蒸馏水反复清洗2次,超声波洗涤10分钟,蒸馏水清洗结束后,采用异丙醇、丙酮、甲醇溶剂按顺序进行超声波洗涤后,在加热到120℃的热板上进行干燥,将干燥后的基板转移到等离子体清洗机里,洗涤5分钟后将基板转移至蒸镀机中。
[0247]
利用真空蒸镀装置,蒸镀膜厚为10nm的hi-1和hi-2作为空穴注入层,hi-1和hi-2的质量比为97:3。接着蒸镀膜厚为130nm的hi-1作为空穴传输层。上述空穴传输材料蒸镀结束后,制作oled发光器件的发光层,使用rh-1作为主体材料,rd-1作为掺杂材料,rh-1和rd-1质量比为98:2,发光层膜厚为40nm。在上述发光层之后,继续真空蒸镀膜厚为35nm的et-1和liq作为电子传输层,et-1和liq质量比为1:1,接着蒸镀膜厚为1nm的lif作为电子注入层。在电子注入层上,通过真空蒸镀装置,蒸镀膜厚为13nm的mg:ag作为阴极,mg、ag质量比为1:9,在阴极上,真空蒸镀70nm的本发明化合物1作为覆盖层,从而制备有机电致发光器件。
[0248][0249]
[器件实施例2~25]
[0250]
用本发明化合物33、化合物38、化合物45、化合物49、化合物57、化合物64、化合物83、化合物101、化合物102、化合物105、化合物106、化合物108、化合物114、化合物115、化合物123、化合物136、化合物137、化合物141、化合物155、化合物173、化合物188、化合物298、化合物299、化合物313分别代替器件实施例1中的化合物1作为覆盖层,除此之外,通过与器件实施例1相同的制备方法,制备有机电致发光器件。
[0251]
[对比实施例1~2]
[0252]
用对比化合物1、对比化合物2替代器件实施例1中的化合物1作为覆盖层,除此之外,通过与器件实施例1相同的制备方法,制备有机电致发光器件。
[0253]
将测试软件、计算机、美国keithley公司生产的k2400数字源表和美国photo research公司的pr788光谱扫描亮度计组成一个联合ivl测试系统来测试有机电致发光器件的发光效率。寿命的测试采用mcscience公司的m6000 oled寿命测试系统。测试的环境为大气环境,温度为室温。本发明器件实施例中器件1~25、对比实施例1~2所得有机电致发光器件的发光特性测试结果见表2所示。
[0254]
表2:有机电致发光器件的发光特性测试数据
[0255]
[0256][0257]
表2结果表明,与对比实施例1相比,使用本发明提供的杂环类化合物作为有机电致发光器件的覆盖层时,能有效提高器件的光取出效率,进而提高有机电致发光器件的发光效率与使用寿命。
[0258]
应当指出,本发明用个别实施方案进行了特别描述,但在不脱离本发明原理的前提下,本领域普通技术人可对本发明进行各种形式或细节上的改进,这些改进也落入本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1