一种基因分型检测试剂盒及其应用
1.本发明属于试剂盒领域,具体涉及一种基因分型检测试剂盒及其应用。
背景技术:
2.肺癌是世界上最常见的癌症和导致癌症死亡的主要原因。随着外科治疗、免疫治疗、放化疗和分子靶向治疗在肺癌治疗方面取得的显著成就,肺癌的治疗虽然得到了很大进步,但我国肺癌患者5年生存率仍《20%。肺癌患者的预后受多种因素干扰,预测难度较大。因此,寻找有效的生物标志物对于预测肺癌患者预后、针对肺癌患者进行个体化治疗和提高肺癌患者5年生存率至关重要。大量研究证据表明,肺癌的发生发展受环境和个体遗传等多种因素共同影响。基因多态性是人体最常见的基因变异,已被证明可以影响基因表达并预测包括肺癌在内的多种癌症患者的预后。
技术实现要素:
3.本发明是为了解决上述问题而进行的,目的在于提供一种基因分型检测试剂盒及其应用。
4.本发明提供了一种基因分型检测试剂盒,具有这样的特征,包括:用于对癌症患者的全血基因组进行pcr的引物组,该引物组包括第一上游引物和第一下游引物,
5.其中,第一上游引物的核苷酸序列如序列表中seq no:1所示,第一下游引物的核苷酸序列如序列表中seq no:2所示。
6.在本发明提供的基因分型检测试剂盒中,还可以具有这样的特征:其中,基因分型检测为检测camkk1 rs7214723位点基因的基因型,基因分型检测的结果包括:tt基因型、tc基因型以及cc基因型。
7.在本发明提供的基因分型检测试剂盒中,还可以具有这样的特征,还包括:5’通用探针、3’通用探针、位点识别序列、qpcr通用引物、5’特异连接探针以及3’特异连接探针。
8.在本发明提供的基因分型检测试剂盒中,还可以具有这样的特征:其中,癌症为肺癌。
9.在本发明提供的基因分型检测试剂盒中,还可以具有这样的特征:其中,肺癌为非小细胞肺癌。
10.本发明提供了一种基因分型检测试剂盒在预测肺癌患者预后生存中的应用。
11.发明的作用与效果
12.根据本发明所涉及的基因分型检测试剂盒,因为该试剂盒包括引物组,该引物组包括第一上游引物和第一下游引物,通过该引物组能够对癌症患者的全血基因组进行pcr扩增,并根据扩增结果判断癌症患者的camkk1 rs7214723位点基因的基因型,根据该基因型的分型结果可以对癌患者预后生存进行预测。
附图说明
13.图1是本发明的实施例2中cck8细胞增殖实验结果图,其中,图1(a)为a549,图1(b)为nci-h358;
14.图2是本发明的实施例2中a549细胞划痕实验结果图,其中,图2(a)-(d)分别为a549野生型0h、a549野生型24h、a549 camkk1rs7214723位点突变株0h、a549 camkk1 rs7214723位点突变株24h;
15.图3是本发明的实施例2中nci-h358细胞划痕实验结果图,其中,图3(a)-(d)分别为nci-h358野生型0h、nci-h358野生型24h、nci-h358 camkk1 rs7214723位点突变株0h、nci-h358 camkk1rs7214723位点突变株24h;
16.图4是本发明的实施例2中细胞凋亡实验结果图,其中,图4(a)为a549野生型,图4(b)为a549 camkk1 rs7214723位点突变株(a549 camkk1-w),图4(c)为nci-h358野生型,图4(b)为nci-h358 camkk1 rs7214723位点突变株(nci-h358camkk1-w);以及
17.图5是本发明的实施例3中基因分型检测的过程示意图。
具体实施方式
18.为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,以下实施例结合附图对本发明基因分型检测试剂盒及其应用作具体阐述。
19.以下实施例中所使用的qiagen blood dna extraction kit(qiagen,hilden,germany)、cell counting kit-8、annexin v-fitc细胞凋亡检测试剂盒均为市售试剂盒。
20.《实施例1》
21.本实施例提供了一种基因分型检测试剂盒,该试剂盒包括:用于对癌症患者的全血基因组进行pcr的引物组、5’通用探针、3’通用探针、位点识别序列、qpcr通用引物、5’特异连接探针以及3’特异连接探针。
22.其中,引物组包括第一上游引物和第一下游引物。第一上游引物的核苷酸序列如序列表中seq no:1所示,第一下游引物的核苷酸序列如序列表中seq no:2所示。
23.第一上游引物和第一下游引物的浓度均为10mm。
[0024]5’
通用探针、3’通用探针、位点识别序列、qpcr通用引物、5’特异连接探针以及3’特异连接探针均购自上海天昊生物科技有限公司,且浓度以及使用条件均与上海天昊生物科技有限公司的2
×
48-plex snp scantm试剂盒相同。
[0025]
通过使用上述基因分型检测试剂盒对癌症患者的全血基因组进行pcr扩增可以判断癌症患者是否在camkk1 rs7214723位点存在基因突变,并基于camkk1 rs7214723位点的基因突变情况得到三种基因分型检测结果:tt基因型、tc基因型以及cc基因型(其中位点c为突变型)。
[0026]
《实施例2》
[0027]
实施例2提供了一种在细胞水平上验证camkk1 rs7214723位点发生基因突变对细胞的影响试验,该试验利用crispr-cas9基因编辑技术对camkk1 rs7214723位点进行点突变,具体过程如下:
[0028]
1.1设计用于crispr-cas9基因编辑的核苷酸序列
[0029]
1.1.1选择sgrna序列。
[0030]
sgrna序列如序列表中seq no:3所示。
[0031]
1.1.2设计含有camkk1 rs7214723突变位点的ssdna序列。
[0032]
设计的含有camkk1 rs7214723突变位点的ssdna序列如序列表中seq no:4所示。
[0033]
1.1.3设计oligo引物
[0034]
oligo引物包括第二上游引物和第二下游引物。其中,第二上游引物的序列如序列表中seq no:5所示,第二下游引物的序列如序列表中seq no:6所示。
[0035]
1.1.4利用oligo引物和含有camkk1 rs7214723突变位点的ssdna退火连接成双链dna。
[0036]
1.2表达载体构建
[0037]
使用的载体为质粒pspcas9(bb)-2a-puro(px459)v2.0,利用bbs1内切酶进行酶切,酶切后回收,并用t4 dna ligase与含有camkk1 rs7214723突变位点的双链dna进行连接,并转化提取质粒。
[0038]
1.3脂质体转染
[0039]
将构建成功的表达载体、sgrna以及含有camkk1 rs7214723突变位点的ssdna共同转进a549细胞以及nci-h358细胞,24h后用puromycin dihydrochloride(碧云天,st551)筛选,并挑选阳性克隆进行pcr,对pcr产物进行测序鉴定。
[0040]
其中,pcr鉴定所使用的引物包括第三上游引物、第三下游引物以及测序引物。第三上游引物的序列如序列表中seq no:7所示,第三下游引物的序列如序列表中seq no:8所示,测序引物的序列如序列表中seq no:9所示。
[0041]
1.4细胞扩大培养
[0042]
对鉴定正确的a549-camkk1-w、nci-h358-camkk1-w细胞进行扩大培养,并与其相对应的野生型作为对照进行后续细胞试验。
[0043]
1.5细胞试验
[0044]
1.5.1 cck8细胞增殖实验
[0045]
根据实验方法(cell counting kit-8,ck04),将细胞接种96孔板中,24h后用全波长酶标仪(biotek全波长酶标仪epoch)在450nm吸光度下检测细胞增殖,每组实验设置对照孔,重复三次。
[0046]
1.5.2细胞划痕实验
[0047]
该实验用于检测细胞迁移能力,具体包括:在6孔板中加入约5
×
105个细胞,第二天用枪头比着直尺,尽量垂至于背后的横线划痕,用pbs洗细胞3次,去处划下的细胞,加入无血清培养基,放入37℃5%co2培养箱培养。24小时取样,拍照,每组实验设置对照孔,重复三次。
[0048]
1.5.3细胞凋亡实验
[0049]
采用annexinv-fitc细胞凋亡检测试剂盒(碧云天beyotime,c1062s),在6孔板中加入约5
×
105个细胞,24小时取样,使用流式细胞仪检测凋亡率。每组实验设置对照孔,重复三次。
[0050]
1.6实验结果
[0051]
1.6.1细胞增殖
[0052]
图1是本发明的实施例2中cck8细胞增殖实验结果图,其中,图1(a)为a549,图1(b)
为nci-h358。
[0053]
如图1所示,通过cck8细胞增殖实验检测发现,a549 camkk1rs7214723位点突变株和nci-h358 camkk1 rs7214723位点突变株相对其野生型,三次生物学重复平均值结果细胞增殖分别降低了11.6%和13.3%。所以camkk1 rs7214723位点突变株对a549和nci-h358细胞株的增殖能力有所影响,均会降低两者的增殖能力。
[0054]
1.6.2细胞迁移
[0055]
图2是本发明的实施例2中a549细胞划痕实验结果图,其中,图2(a)-(d)分别为a549野生型0h、a549野生型24h、a549camkk1 rs7214723位点突变株0h、a549 camkk1 rs7214723位点突变株24h。图3是本发明的实施例2中nci-h358细胞划痕实验结果图,其中,图3(a)-(d)分别为nci-h358野生型0h、nci-h358野生型24h、nci-h358 camkk1 rs7214723位点突变株0h、nci-h358camkk1 rs7214723位点突变株24h。
[0056]
如图2和图3所示,通过细胞划痕实验发现,正常培养24h后,a549野生型和nci-h358野生型细胞迁移性强于a549camkk1rs7214723位点突变株和nci-h358 camkk1 rs7214723位点突变株。可以判断camkk1 rs7214723位点突变对a549和nci-h358细胞的迁移能力有影响。
[0057]
1.6.3细胞迁移
[0058]
图4是本发明的实施例2中细胞凋亡实验结果图,其中,图4(a)为a549野生型,图4(b)为a549 camkk1 rs7214723位点突变株(a549 camkk1-w),图4(c)为nci-h358野生型,图4(b)为nci-h358 camkk1 rs7214723位点突变株(nci-h358camkk1-w)。
[0059]
如图4所示,通过细胞凋亡实验检测发现,a549 camkk1rs7214723位点突变株(a549 camkk1-w)的凋亡率比a549野生型高5.63%。nci-h358camkk1 rs7214723位点突变(nci-h358camkk1-w)的凋亡率比nci-h358野生型高3.98%。因此,可以看出camkk1 rs7214723位点突对a549、nci-h358的凋亡有促进作用。
[0060]
实施例2的上述实验结果表明,camkk1 rs7214723位点突变对a549细胞和nci-h358细胞的增殖、迁移以及凋亡均有影响,这表明camkk1 rs7214723可以作为生物标志物对非小细胞肺癌细胞进行进一步研究。
[0061]
《实施例3》
[0062]
实施例3提供了一种实施例1中的基因分型检测试剂盒在预测肺癌患者预后生存中的应用。具体过程如下:
[0063]
2009年1至11月期间收集海军军医大学(第二军医大学)附属长海医院536例、复旦大学泰州健康科学研究院352例共888例原发性肺癌患者。纳入标准:病理组织学检查确诊的新发肺癌患者,无其他器官恶性肿瘤史,无年龄、性别限制。临床资料来源于病历,随访资料来源于电话访谈,所有患者均为中国人。本研究通过复旦大学生命科学学院伦理委员会批准,流行病学调查资料收集及血液样本采集均获得研究对象知情同意。
[0064]
2.1使用实施例1的基因分型检测试剂盒检测患者的camkk1rs7214723基因型
[0065]
2.1.1血液样本采集
[0066]
所有患者均捐献了5ml血液。
[0067]
2.1.2 dna提取
[0068]
使用qiagen blood dna extraction kit(qiagen,hilden,germany)提取血液中
的基因组dna。
[0069]
2.1.3使用实施例1的基因分型检测试剂盒对基因组dna进行检测图5是本发明的实施例3中基因分型检测的过程示意图。
[0070]
如图5所示,采用连接酶连接反应的高特异性实现对snp位点等位基因的识别,然后通过在连接探针末段引入不同长度的非特异序列以及通过连接酶加接反应获得位点对应的不同长度连接产物,利用标记荧光的通用引物对连接产物进行pcr扩增。
[0071]
pcr扩增反应体系包括:2
×
es taq mastermix(北京百奥莱博科技有限公司)、引物组(各0.5mm)、100ng人全血基因组dna。
[0072]
pcr循环条件为:每次循环94℃30s,60℃30s,72℃30s,共进行25次循环。
[0073]
通过荧光毛细管电泳对扩增产物进行电泳分离,最后通过对genemapper软件分析获取各个snp位点的基因型,判断camkk1rs7214723位点的基因突变情况,确定其属于三种基因分型(tt基因型、tc基因型以及cc基因型(其中位点c为突变型))中的哪一种。
[0074]
2.2统计患者临床资料
[0075]
收集患者基本临床资料,包括性别,年龄,吸烟史,恶性肿瘤家族史,肺癌病理类型,tnm分期。
[0076]
2.3根据数据统计结论推测肺癌患者预后生存基于肺癌患者基因分型检测结果和临床信息,根据我们的统计学分析结论预测肺癌患者预后死亡风险。
[0077]
2.4统计学分析statistical analysis
[0078]
采用rv3.6.2软件进行统计学处理。人口统计变异值、人群吸烟状况、家族癌症病史、对照组与病例组等位基因频率差异,及哈迪-温伯格平衡(hardy-weinberg equilibrium,hwe)检验采用χ2检验分析。分别采用等位基因模型、基因型模型、显性模型和隐性模型进行cox回归分析,计算风险比(hazard ratio,hr)和95%置信区间(confidence interval,ci),校正采用年龄、性别。进一步按年龄、性别、吸烟情况、家族史、肺癌组织学类型等对各种模型分别进行分析,评估基因多态性与肺癌预后之间的关系。p<0.05表示差异有统计学意义。
[0079]
2.5实验结果
[0080]
2.5.1患者的人口特征和临床特征
[0081]
随访时间从2009年1开始至2019年11月15日。由于临床资料不完整,排除49例患者后,对839例患者的数据进行分析。研究样本为汉族,668例(79.6%)死亡,103例(12.3%)存活时间超过5年,68例(8.1%)失访。其中男性610例(72.7%),年龄≥60岁524例(62.5%),吸烟史582例(69.4%),恶性肿瘤家族史302例(36%)。从肿瘤亚型看,腺癌367例(43.7%),鳞癌282例(33.6%),sclc 72例(8.6%),其他类型118例(14.1%)。包括腺鳞癌(asc)、大细胞癌(lcc)、癌肉瘤(cs)和黏液表皮样癌(mec)。154例(18.4%)患者诊断为i期和ii期疾病,625例(74.5%)患者诊断为iii期和iv期疾病(表1)。
[0082]
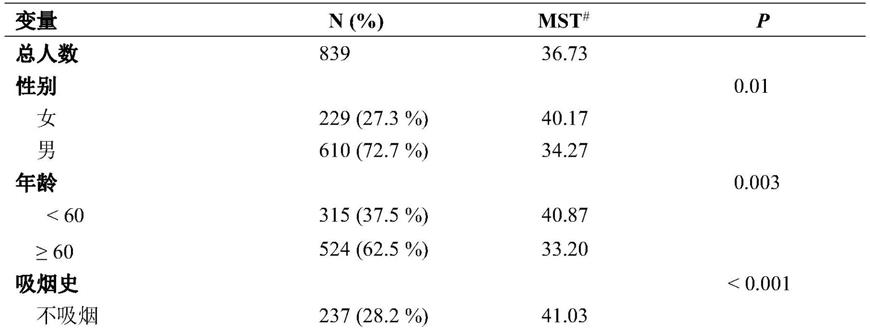
表1.中国肺癌患者特征分布及预后分析表
[0083][0084][0085]
*其它癌症包括腺鳞癌(asc)、大细胞癌(lcc)、癌肉瘤(cs)、黏液表皮样癌(mec);
#
mst,中位生存时间。
[0086]
2.5.2患者特征与肺癌预后的关系
[0087]
如表1所示,男性患者的中位生存时间明显低于女性患者(男,34.27个月;女,40.17个月;p=0.01)。年龄<60岁患者的中位生存时间明显高于年龄≥60岁患者(40.87个月、33.20个月;p=0.003)。不吸烟患者的中位生存时间明显高于吸烟患者(41.03个月、33.90个月;p《0.001))。此外,与早期肿瘤患者相比,晚期肿瘤患者的中位生存时间显著缩短(29.4个月、113.93个月;p《0)。不同医院患者特征与肺癌预后的相关性无显著统计学差异。
[0088]
表2.camkk1 rs7214723基因分型(基因多态性)与中国肺癌患者预后关系表
[0089][0090][0091]
*
ci,置信区间;hr,风险比;ref,参考.a根据年龄、性别和医院来调整.
[0092]
如表2所示,在camkk1基因rs7214723位点有341个tt、400个tc和91个cc基因型,基因型检出率为99.17%。camkk1基因rs7214723位点t/c的基因型频率与hwe一致(p=0.102),表明调查人群处于遗传平衡(即人群调查数据可信)。此外,在camkk1基因rs7214723位点检测到1082个t等位基因和582个c等位基因。在死亡患者组中,t和c等位基因的频率分别为65.16%(864/1326)和34.84%(462/1326)。与tt+tc基因型相比,隐性cc基因型个体的死亡风险较低(cc的调整hr=0.78;95%ci:0.61-1.00,p=0.049)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1