多元稠杂环类化合物及其制备方法
1.本发明涉及有机合成技术领域,尤其涉及多元稠杂环类化合物及其制备方法。
背景技术:
2.多元稠杂环化合物是一类非常重要的杂环化合物,其往往具有优异的生物活性,例如:(-)-kopsinine,perophoramidine,myrioxazine a,perinadine a。其中,单吲哚类生物碱蕊木宁为海南蕊木的化学成分,具有舒筋活络、解毒止痛、利水消肿的功效;perophoramidine也被发现具有抗肿瘤活性;myrioxazine a与perinadinea可作为抗生素的同时,perinadinea还具有抗肿瘤活性。因此,多元稠杂环的构建吸引了许多合成化学工作者和药物化学工作者的极大兴趣。然而,由于多元稠杂环往往具有非常复杂的结构,通常是含有至少两个以上的并环结构,因此,其合成路线比较复杂、繁琐,通常需要多步化学反应才能实现,且总收率较低。鉴于此,开发快速、高效的方法用于构建结构复杂的多元稠杂环骨架具有十分重要的意义。
技术实现要素:
3.本发明的目的之一,就在于提供一类结构新颖的多元稠杂环类化合物。
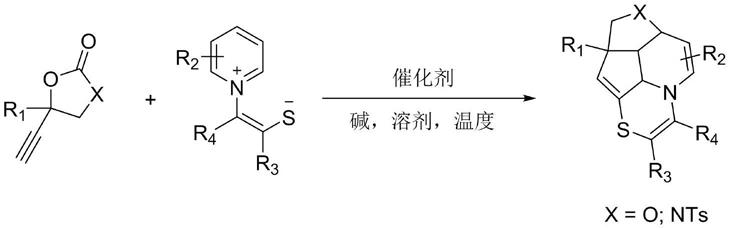
4.为了实现上述目的,本发明采用的技术方案如下:一类多元稠杂环类化合物,具有如下结构式(ⅳ)所示的结构:
[0005][0006]
上述结构式中,r1基、r3基和r4基选自单取代基或多取代基,所述取代基选自烷基,烷氧基,酯基或芳基;r2基选自烷基,烷氧基或卤素;nts即对硝基甲苯邻磺酸。
[0007]
本发明所提供的多元稠杂环类化合物是一类结构新颖的含三种杂原子的四元并环杂环结构骨架。其包含有环戊烯并四氢呋喃/吡咯环、环戊烯并吡啶环、四氢吡啶并噻嗪环,以及四氢呋喃并四氢吡啶环。这些杂环单元,广泛存在于各种天然产物及药物分子中,对于天然产物结构骨架的构建具有重要意义。同时,也为新药研发和化学药物合成提供了结构新颖、多样的先导化合物库
[0008]
本发明的化合物的应用价值在于:多元稠杂环骨架广泛存在于天然产物中,通常具有一定的生物活性。因此,本发明以一种简单高效的一锅反应合成了一种含有三种杂原子的新的稠杂环化合物,具有极大的潜在药用价值,可以充实先导化合物库,为药物候选分子的发现提供充足的化合物源。
[0009]
本发明的目的之二,在于提供上述化合物的制备方法,采用的技术方案为,
[0010]
包括如下步骤:
[0011]
在惰性气体保护下,将环状乙炔基碳酸酯(ⅰ)或氨基甲酸内酯(ⅱ)和碱加入到吡啶1,4-两性离子硫醇盐(ⅲ)与金属铜盐的有机溶剂中,在35℃下搅拌反应3.0-10.0小时,待反应完毕,直接分离纯化,得到多元稠杂环类产物(ⅳ);
[0012]
其中,所述环状乙炔基碳酸酯(ⅰ)具有如下结构:
[0013][0014]
所述氨基甲酸内酯(ⅱ)具有如下结构:
[0015][0016]
所述吡啶1,4-两性离子硫醇盐(ⅲ)具有如下结构:
[0017][0018]
合成路线为:
[0019][0020]
本发明采用上述的合成方法,通过一步反应即合成了一系列新型的多元稠杂环类化合物。
[0021]
作为优选的技术方案:所述有机溶剂选自乙腈、甲醇、二氯甲烷、甲苯、四氢呋喃、三氟乙醇、乙酸乙酯、1,4-二氧六环、六氟异丙醇中的至少一种。
[0022]
作为优选的技术方案:所述金属铜盐选自三氟甲磺酸铜、一水合醋酸铜、碘化亚铜、四氟硼酸四乙腈铜、甲苯络合的三氟甲磺酸亚铜、六氟磷酸四乙腈铜、氯化亚铜、溴化亚铜、碘化亚铜、双乙酰丙酮铜中的至少一种。
[0023]
作为优选的技术方案:所述的碱选自n,n-二异丙基乙二胺、n,n-二环己基甲胺、三乙胺、碳酸钾、磷酸钾中的至少一种。
[0024]
作为优选的技术方案:所述铜盐用量最低为10mol%。
[0025]
作为优选的技术方案:所述有机碱用量最低为1.0当量。
[0026]
作为优选的技术方案:所述分离纯化方法为柱层析。
[0027]
本发明的优点在于:本发明采用铜盐催化4-乙炔基碳酸酯/4-氨基甲酸内酯与1,4-两性离子硫醇盐发生多步串联环加成反应,简捷高效的合成了一系列多元稠杂环类化合物;本方法制得的化合物丰富了稠杂环化合物库,为先导化合物和药物候选分子的筛选提供充足的化合物源。本方法具有反应速度快,反应条件温和,简单易操作,原料易制得,使用的金属催化剂和碱都是商业易得的等优点。
附图说明
[0028]
图1为实施例1制得的
ⅳ‑
a的氢谱图;
[0029]
图2为实施例1制得的
ⅳ‑
a的碳谱图;
[0030]
图3为实施例1制得的
ⅳ‑
a的单晶图。
具体实施方式
[0031]
下面将结合附图对本发明作进一步说明。
[0032]
本发明所用的原料、溶剂、催化剂、分子筛等等,均为市购。
[0033]
实施例1:合成化合物(
ⅳ‑
a)
[0034][0035]
化合物
ⅳ‑
a的合成:
[0036]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-a(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5:1)得化合物
ⅳ‑
a,不同的反应条件如表1所示,具体反应情况如下:
[0037][0038]
表1不同的反应条件
[0039][0040][0041]
从表1中可见,不同种类的铜盐对反应的活性的影响都略有差异;通过单因素试验比较,铜盐选择甲苯络合的三氟甲烷磺酸亚铜((cuotf)2·
toluene)时,反应效果最好。碱对反应活性也有较大的影响,没有碱时,反应收率只有48%;通过比较,碱选用三乙胺(net3)时反应效果最佳。此外,溶剂对反应有很大的影响,溶剂选择三氟乙醇时,反应的收率最好,为80%。最终,采用甲苯络合的三氟甲烷磺酸亚铜为催化剂、以三乙胺为碱、三氟乙醇为溶剂、反应温度35℃时反应为优选的方案。
[0042]
在最优方案下,得到的iv-a情况如下:
[0043]
黄色固体,95mg,收率80%;m.p.150.1℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.34(d,j=3.1hz,4h),7.25(dd,j=5.7,2.9hz,1h),6.43(d,j=8.5hz,1h),6.23(s,1h),5.15(dd,j=7.9,6.2hz,1h),4.45(t,j=6.5hz,1h),4.40(d,j=9.2hz,1h),4.08(d,j=9.0hz,1h),3.83(s,3h),3.70(s,3h),3.65(d,j=9.1hz,1h),δ3.32(dd,j=9.1,7.2hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.9,163.4,143.3,139.9,130.9,129.6,129.0,128.6,126.7,126.6,101.8,100.5,74.5,70.4,69.5,60.5,53.4,52.7,49.2;hrms(esi)calcd.for c21h19no5s[m+h]
+
:398.1057;found:398.1062.
[0044]
iv-a的氢谱、碳谱和单晶图谱分别如图1-3所示。
[0045]
实施例2:合成化合物(iv-b)
[0046][0047]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-b(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余
物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
b。黄色固体;109.4mg,收率80.4%;m.p.68.8℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.36(d,j=8.5hz,2h),7.25(d,j=8.4hz,2h),6.43(d,j=7.4hz,1h),6.21(s,1h),5.15(dd,j=8.1,6.0hz,1h),4.43(t,j=6.5hz,1h),4.39(d,j=9.3hz,1h),4.05(d,j=9.0hz,1h),3.83(s,3h),3.71(s,3h),3.64(d,j=9.1hz,1h),3.30(dd,j=9.2,7.2hz,1h),1.26(s,9h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.9,163.4,149.1,140.2,139.8,131.0,129.5,128.8,126.2,125.4,101.8,100.4,74.4,70.4,69.1,60.5,53.4,52.7,49.1,34.1,31.1;hrms(esi)calcd.for c25h27no5s[m+h]
+
:454.1683;found:454.1690。
[0048]
实施例3:合成化合物(iv-c)
[0049][0050]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-c(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
c。黄色固体;84.3mg,收率68.3%;m.p.79.5℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.22(d,j=8.1hz,2h),7.15(d,j=8.0hz,2h),6.43(d,j=8.2hz,1h),6.21(s,1h),5.15(dd,j=8.1,6.0hz,1h),4.43(d,j=6.4hz,1h),4.38(d,j=9.8hz,1h),4.04(d,j=9.0hz,1h),3.83(s,3h),3.70(s,3h),3.62(d,j=9.1hz,1h),3.31
–
3.26(m,1h),2.27(s,3h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.9,163.4,140.3,139.8,135.9,131.0,129.5,129.1,128.8,126.4,101.8,100.5,74.5,70.4,69.2,60.5,53.4,52.7,49.2,20.5;hrms(esi)calcd.for c22h21no5s[m+h]
+
:412.1213;found:412.1223。
[0051]
实施例4:合成化合物(iv-d)
[0052][0053]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-d(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
d。黄色固体;86.2mg,收率61.6%;m.p.75.9℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.42
–
7.40(m,1h),
7.40
–
7.36(m,1h),7.35
–
7.30(m,2h),6.43(d,j=8.1hz,1h),6.25(s,1h),5.14(dd,j=8.2,5.9hz,1h),4.47(t,j=6.4hz,1h),4.42(d,j=9.3hz,1h),4.07(d,j=9.1hz,1h),3.83(s,3h),3.70(s,3h),3.62(d,j=9.1hz,1h),3.34(dd,j=9.5,7.2hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.83,163.39,145.73,139.84,133.40,130.47,130.10,129.79,129.57,126.78,126.51,125.40,101.84,100.35,74.27,70.38,69.37,60.35,53.44,52.73,49.03;hrms(esi)calcd.for c21h19clno5s[m+h]
+
:432.0667;found:432.0671。
[0054]
实施例5:合成化合物(iv-e)
[0055][0056]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-e(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
e。白色固体;66.9mg,收率51.6%;m.p.127.4℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.38(q,j=8.7hz,4h),6.43(d,j=8.1hz,1h),6.23(s,1h),5.14(dd,j=8.2,5.9hz,1h),4.46(t,j=6.5hz,1h),4.40(d,j=9.2hz,1h),4.06(d,j=9.1hz,1h),3.83(s,3h),3.70(s,3h),3.62(d,j=9.1hz,1h),3.30(dd,j=9.3,7.0hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.8,163.4,142.3,139.8,131.5,130.28,129.6,129.6,128.6,128.5,101.8,100.4,74.3,70.4,69.1,60.4,53.4,52.7,49.3;hrms(esi)calcd.for c21h19clno5s[m+h]
+
:432.0667;found:432.0669。
[0057]
实施例6:合成化合物(iv-f)
[0058][0059]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-f(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
f。黄色固体;86.2mg,收率61.6%;m.p.66.9℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.63-7.58(m,2h),7.36(dd,j=8.4,2.2hz,1h),6.42(d,j=8.2hz,1h),6.25(d,j=1.2hz,1h),5.14(dd,j=
8.2,5.9hz,1h),4.48(t,j=6.5hz,1h),4.42(d,j=9.3hz,1h),4.06(d,j=9.1hz,1h),3.82(s,3h),3.70(s,3h),3.60(d,j=9.2hz,1h),3.33(dd,j=9.3,7.0hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.9,163.4,144.4,139.9,131.4,130.7,130.2,129.7,129.7,129.6,128.8,127.2,101.9,100.4,74.2,70.4,69.1,60.3,53.5,52.8,49.1;hrms(esi)calcd.for c21h17cl2no5s[m+h]
+
:466.0227;found:466.0278。
[0060]
实施例7:合成化合物(iv-f)
[0061][0062]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-f(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
f。淡黄色固体;72.5mg,收率58.2%;m.p.165.1℃;
[0063]1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.43
–
7.32(m,2h),7.25
–
7.15(m,2h),6.44(d,j=8.1hz,1h),6.23(s,1h),5.16(dd,j=8.1,6.1hz,1h),4.42(t,j=6.4hz,1h),4.35(d,j=9.2hz,1h),4.07(dd,j=9.0,3.4hz,1h),3.83(s,3h),3.70(s,3h),3.66(d,j=9.0hz,1h),3.47(dd,j=8.9,7.2hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.8,163.4,159.3,139.9,130.1,129.6,129.0,124.7,124.7,116.3,116.2,101.6,100.4,73.2,69.9,66.7,60.5,53.5,52.8,47.6;hrms(esi)calcd.for c21h18fno5s[m+h]
+
:416.0962;found:416.0965。
[0064]
实施例8:合成化合物(iv-g)
[0065][0066]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-f(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
f。淡黄色固体;72.5mg,收率58.2%;m.p.129.1℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.19
–
7.13(m,2h),6.42(d,j=8.2hz,1h),6.22(s,1h),5.15(dd,j=8.1,6.0hz,1h),4.45(t,j=6.5hz,1h),
4.40(d,j=9.2hz,1h),4.06(d,j=9.1hz,1h),3.83(s,3h),3.70(s,3h),3.62(d,j=9.1hz,1h),3.29(dd,j=9.2,7.1hz,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)163.9,163.5,139.9,130.7,129.6,129.3,128.6,128.6,115.4,115.3,101.9,100.5,74.5,70.4,69.0,60.5,53.5,52.8,49.4.;hrms(esi)calcd.for c21h18fno5s[m+h]
+
:416.0962;found:416.0966。
[0067]
实施例9:合成化合物(iv-h)
[0068][0069]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-h(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
f。黄色固体;93.9mg,收率65.7%;m.p.70.1℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.54
–
7.51(m,1h),7.45(d,j=7.9hz,1h),7.38(d,j=7.9hz,1h),7.34
–
7.28(m,1h),6.43(d,j=8.2hz,1h),6.25(s,1h),5.14(dd,j=8.1,6.0hz,1h),4.47(t,j=6.5hz,1h),4.42(d,j=9.3hz,1h),4.07(d,j=9.1hz,1h),3.83(s,3h),3.70(s,3h),3.61(d,j=9.1hz,1h),3.34
–
3.31(m,1h);
13
c nmr(151mhz,dmso-d6)δ(major diastereomer)164.3,163.9,146.5,140.31,131.2,130.6,130.3,130.2,130.0,129.8,126.3,122.6,100.8,74.8,70.8,69.8,60.8,53.9,53.2,49.5;hrms(esi)calcd.for c21h18brno5s[m+h]
+
:476.0162;found:476.0177。
[0070]
实施例10:合成化合物(iv-i)
[0071][0072]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-i(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
g。黄色固体;80.1mg,收率62.5%;m.p.94.3℃;1h nmr(600mhz,dmso-d6)δ(major diastereomer)7.29
–
7.23(m,1h),6.91(d,j=8.3hz,1h),6.86(t,j=2.0hz,1h),6.82(dd,j=8.2,2.2hz,1h),6.43(d,j=8.2hz,1h),6.22(d,j=1.0hz,1h),5.15(dd,j=8.1,5.9hz,1h),4.46
–
4.42(m,1h),4.40(d,j=10.0hz,1h),4.06(d,j=9.0hz,1h),3.83(s,3h),3.75(s,3h),3.70(s,3h),3.63(d,
j=9.1hz,1h),3.34(dd,j=9.3,7.1hz,1h);
13
c nmr(151mhz,dmso-d6)δ163.9,163.5,159.5,144.8,139.9,130.8,129.7,129.6,129.0,118.7,112.6,101.8,100.5,74.4,70.4,69.6,55.1,53.4,52.7;hrms(esi)calcd.for c22h21no6s[m+h]+:428.1162;found:428.1167。
[0073]
实施例11:合成化合物(iv-j)
[0074][0075]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-j(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
j。黄色固体;46.6mg,收率51%;m.p.86.2℃;1h nmr(600mhz,dmso-d6)δ7.24(d,j=8.7hz,2h),6.90(d,j=8.8hz,2h),6.42(d,j=8.1hz,1h),6.20(d,j=1.2hz,1h),5.14(dd,j=8.1,6.0hz,1h),4.43(t,j=6.4hz,1h),4.38(d,j=9.3hz,1h),4.05
–
4.01(m,1h),3.83(s,3h),3.73(s,3h),3.70(s,3h),3.61(d,j=9.1hz,1h),3.25(dd,j=9.3,7.0hz,1h);
13
c nmr(151mhz,dmso-d6)δ163.9,163.5,158.1,139.8,135.2,131.1,129.5,128.7,127.6,114.0,101.8,100.5,74.6,70.4,68.9,60.5,55.1,53.4,52.7,49.3;hrms(esi)calcd.for c22h21no6s[m+h]
+
:428.1162;found:428.1167。
[0076]
实施例12:合成化合物(iv-k)
[0077][0078]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-k(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
k。黄色固体;25.5mg,收率20%;m.p.92.1℃;1h nmr(600mhz,dmso-d6)δ7.29
–
7.23(m,1h),7.22(dd,j=7.7,1.6hz,1h),7.04(d,j=8.2hz,1h),6.94
–
6.89(m,1h),6.41(d,j=8.1hz,1h),6.18(s,1h),5.15(dd,j=8.1,6.0hz,1h),4.42(t,j=6.5hz,1h),4.27(dd,j=9.3,1.2hz,1h),3.98(d,j=8.8hz,1h),3.83(s,3h),3.81(s,3h),3.70(d,j=1.8hz,3h),3.68(s,1h),3.45(dd,j=9.3,6.9hz,1h);
13
c nmr(151mhz,dmso-d6)δ163.5,156.9,139.9,130.0,129.8,129.5,
129.1,128.5,127.5,120.5,112.0,101.3,100.8,73.1,70.0,67.6,60.8,55.5,53.4,52.7,47.0;hrms(esi)calcd.for c22h21no6s[m+h]
+
:428.1162;found:428.1166。
[0079]
实施例13:合成化合物(iv-l)
[0080][0081]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-l(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
l。黄色固体;41.7mg,收率34.5%;m.p.137.7℃;1h nmr(600mhz,dmso-d6)δ7.44(dd,j=5.0,1.2hz,1h),7.04(dd,j=3.6,1.2hz,1h),7.01(dd,j=5.1,3.5hz,1h),6.43(d,j=8.1hz,1h),6.21(s,1h),5.14(dd,j=8.1,5.9hz,1h),4.46(t,j=6.5hz,1h),4.36(d,j=9.5hz,1h),4.01(d,j=9.2hz,1h),3.83(s,3h),3.71(s,3h),3.69(d,j=9.1hz,1h),3.23(dd,j=9.3,7.1hz,1h);
13
c nmr(151mhz,dmso-d6)δ163.8,163.3,146.9,139.9,130.3,129.8127.3,124.7,123.8,101.6,100.4,74.8,70.1,66.3,60.1,53.5,52.8,51.2;hrms(esi)calcd.for c19h18no5s2[m+h]
+
:404.0621;found:404.0626。
[0082]
实施例14:合成化合物(iv-m)
[0083][0084]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯i-m(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=5;1)得化合物
ⅳ‑
m。黄色固体;103.6mg,收率77.2%;m.p.113.5℃;1h nmr(600mhz,dmso-d6)δ7.90(dd,j=13.3,8.7hz,3h),7.86
–
7.84(m,1h),7.53
–
7.47(m,3h),6.46(d,j=8.2hz,1h),6.33(d,j=1.0hz,1h),5.18(dd,j=8.1,5.9hz,1h),4.54
–
4.50(m,1h),4.47(d,j=9.3hz,1h),4.15(d,j=9.1hz,1h),3.84(s,3h),3.78(d,j=9.1hz,1h),3.71(s,3h),3.43(dd,j=9.3,7.1hz,1h);
13
c nmr(151mhz,dmso-d6)δ163.4,140.6,139.9,132.9,131.8,130.7,129.6,128.3,127.8,127.4,126.4,126.0,125.5,124.6,101.9,100.5,74.3,70.5,69.7,60.5,53.5,52.8,49.3;hrms(esi)calcd.for c19h18no5s2[m+h]
+
:448.1216;found:448.1213。
[0085]
实施例15:合成化合物(iv-n)
[0086][0087]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),氨基酸内酯
ⅱ‑
a(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=3:1)得化合物
ⅳ‑
n。黄色固体;143.2mg,收率84.5%;m.p.106.5℃;1h nmr(600mhz,dmso-d6)δ8.07
–
8.03(m,1h),7.68(d,j=8.2hz,2h),7.37(d,j=8.1hz,2h),7.18
–
7.13(m,4h),6.07(d,j=7.7hz,1h),5.96(dd,j=9.5,5.9hz,1h),5.77(dd,j=9.9,4.0hz,1h),4.97(t,j=7.1hz,1h),4.64(dd,j=4.0,1.4hz,1h),3.79(d,j=6.3hz,2h),3.77(s,3h),3.72(s,3h),2.37(s,3h),2.18(s,3h),1.10(s,1h);
13
c nmr(151mhz,dmso-d6)δ163.6,163.1,142.7,138.9,138.0,135.9,130.5,129.7,127.9,127.6,127.3,126.4,126.0,121.6,118.2,112.8,105.4,101.0,96.8,57.7,53.3,52.8,45.1,26.8,21.0,20.3;hrms(esi)calcd.for c22h22no5s[m+h]
+
:565.1462;found:565.1462。
[0088]
实施例16:合成化合物(iv-o)
[0089][0090]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
a(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),氨基酸内酯
ⅱ‑
b(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=3:1)得化合物
ⅳ‑
o。黄色固体;102.1mg,收率60.3%;m.p.109.4℃;1h nmr(400mhz,dmso-d6)δ7.68(d,j=8.2hz,2h),7.46(d,j=8.0hz,2h),7.08(s,4h),6.43(d,j=8.2hz,1h),6.18(d,j=1.1hz,1h),5.23(dd,j=8.2,6.0hz,1h),4.43(d,j=9.0hz,1h),3.88(d,j=9.2hz,1h),3.86(s,3h),3.71(s,3h),3.43(dd,j=7.8,6.1hz,1h),2.71(d,j=9.8hz,1h),2.39(s,3h),2.22(s,3h);
13
c nmr(101mhz,dmso-d6)δ163.7,163.3,144.1,140.2,139.9,136.1,130.6,130.4,130.0,129.2,128.7,128.1,127.8,126.1,100.8,100.6,60.5,58.4,53.5,52.9,52.7,48.4,21.1,20.5;hrms(esi)calcd.for c22h22no5s[m+h]+:565.1462;found:565.1462。
[0091]
实施例17:合成化合物(iv-p)
[0092][0093]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
b(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯
ⅱ‑
a(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=3:1)得化合物
ⅳ‑
p。黄色固体;18.3mg,收率12.8%;m.p.87.6℃;1h nmr(600mhz,dmso-d6)δ7.35
–
7.33(m,4h),7.26(dd,j=4.9,3.6hz,1h),6.73(s,1h),6.25(d,j=1.1hz,1h),4.61(d,j=7.5hz,1h),4.43(d,j=9.1hz,1h),4.13(d,j=9.2hz,1h),3.83(s,3h),3.72(s,3h),3.70(d,j=9.2hz,1h),3.51(dd,j=9.0,7.7hz,1h);
13
c nmr(151mhz,dmso-d6)δ164.0,162.8,142.6,137.6,130.9,129.2,128.9,128.7,126.9,126.6,107.8,94.9,76.4,73.9,69.4,59.4,53.6,53.0,49.7;hrms(esi)calcd.for c21h19brno5s[m+h]
+
:476.0162;found:476.0166。
[0094]
实施例18:合成化合物(iv-q)
[0095][0096]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
c(0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯
ⅱ‑
a(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=3:1)得化合物
ⅳ‑
q。黄色固体;15.5mg,收率12.6%;m.p.73.4℃;1h nmr(600mhz,dmso-d6)δ7.35(d,j=4.3hz,4h),7.27
–
7.23(m,1h),6.20(d,1h),6.15(d,1h),4.30(dd,j=8.4,3.9hz,2h),4.07(d,j=9.1hz,1h),3.84(s,3h),3.69(s,3h),3.66(d,j=9.1hz,1h),3.43(dd,j=12,6hz,1h),1.79(s,3h);
13
c nmr(151mhz,dmso-d6)δ164.0,163.6,143.4,140.3,130.1,129.3,128.6,126.7,126.6,123.6,109.3,99.8,74.9,74.8,69.3,60.0,53.4,52.6,49.5,19.0;hrms(esi)calcd.for c22h22no5s[m+h]
+
:412.1213;found:412.1217。
[0097][0098]
实施例19:合成化合物(iv-r)
[0099][0100]
在一根干燥的反应试管中,将铜盐(0.03mmol),吡啶1,4-两性离子硫醇盐
ⅲ‑
d 0.45mmol)溶解在3ml溶剂中,然后在氩气保护下,依次加入有机碱(0.3mmol),4-乙炔基碳酸酯
ⅱ‑
a(0.3mmol),反应混合液在35℃搅拌反应;反应完全后,减压蒸除溶剂,粗产品残余物经柱色谱分离纯化(石油醚:乙酸乙酯=3:1)得化合物
ⅳ‑
r。黄色固体;47.3mg,收率38.3%;m.p.130.6℃;1h nmr(600mhz,dmso-d6)δ7.37
–
7.34(m,4h),7.27
–
7.23(m,1h),6.27(d,j=8.3hz,1h),6.12(s,1h),4.90(d,j=8.3hz,1h),4.39(d,j=10.3hz,1h),3.97(s,2h),3.83(s,3h),3.70(s,3h),3.32(d,j=9.5hz,1h),1.30(s,3h);
13
c nmr(151mhz,dmso-d6)δ163.8,163.5,144.1,140.0,131.6,128.7,128.1,126.7,126.6,126.2,106.9,102.0,75.2,72.2,69.7,60.1,54.2,53.4,52.7,26.1;hrms(esi)calcd.for c22h22no5s[m+h]
+
:412.1213;found:412.1218。
[0101]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1