一种可裂解的DdeBiotin-PEG4-DBCO类化合物、制备方法及其应用与流程
一种可裂解的ddebiotin-peg4-dbco类化合物、制备方法及其应用
技术领域
1.本发明属于化学技术领域,尤其涉及可裂解的ddebiotin-peg4-dbco(化合物4,美国化学文摘号[1951424-94-4])为代表的一类化合物的制备方法及其应用。
背景技术:
[0002]
目前,二苯并氮杂环辛烷(dbco或adibo)是一种应变环辛烷,在常用的应变环辛烷中具有最高的二阶速率常数(~0.35m-1
s-1
)。环辛炔醇、bcn、dbco-cooh和dbco-nhs(wo20180893730)等试剂的成本仍超过1000美元/g,这对于聚合物或材料化学来说是不可接受的高成本。虽然已经开展了工作,以开发有效的可扩展的方法,较少反应性的应变环辛烷,如(2-环辛烷-1-乙氧基)乙酸等。biotin-peg4-dbco[1255942-07-4]是常用于点击化学的生物探针。dbco中的炔键部分可与叠氮化合物在无需铜离子的催化下形成结构稳定的三氮唑[angew,chem.,int.ed.2008,47,2253;bioconjugatechem.2010,21,2076,]。是研究活体细胞表面糖类与类脂的首选试剂。缺点是发生捕获后不能释放。为了弥补现有技术的不足,亟需开发一种新的、可裂解的并含有应变环辛烷生物素探针及其合成方法。
[0003]
可裂解的ddebiotin-peg4-dbco则是一种可用于以上叠氮反应(点击化学)的生物素探针,它可使捕获的生物分子从链霉菌素中有效释放出来。其包含一个生物素分子,通过一个可被肼裂解的dde连接体通过聚乙二醇(peg)与dbco基团相连。其优点在于,捕获的生物大分子可以被2%肼水溶液有效释放(tetrahedronlett.,1996,37,2625)。可裂解的ddebiotin-peg4-dbco是截至目前还没有公开文献报道过的、可切割的生物素试剂之一(chem.commun.,2013,49,5366)。
[0004]
通过上述分析,现有技术存在的问题及缺陷为:现有应变环辛烷的合成方法均需要经过色谱纯化,成本较高。
[0005]
解决上述技术问题后带来的意义为:
[0006]
聚乙二醇链接剂的导入后的水溶性增强、dde连接体裂解条件的简易性与缓和性、dbco点击化学的高效性为一体。并可作为官能团化的聚乙二醇链接剂修饰蛋白质,做诊断试剂,adc挂载,脂质体的表面靶向分子挂载等多种用途。
技术实现要素:
[0007]
针对现有技术存在的问题,本发明提供了可裂解的ddebiotin-peg4-dbco类化合物、制备方法及其应用。首次公开了以可裂解的ddebiotin-peg4-dbco(化合物4,美国化学文摘号[1951424-94-4])为代表的一类化合物、及其制备方法与应用。
[0008]
本发明是这样实现的,可裂解的ddebiotin-peg4-dbco类化合物的制备方法,所述可裂解的ddebiotin-peg4-dbco类化合物的制备方法包括以下步骤:
[0009]
步骤一,生物素(biotin,化合物1)首先与五氟苯酚在edci作用下偶联成酯后,直接加入15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯进行氨解得到化合物2的叔丁酯;然后
直接酸性水解得到化合物2;
[0010]
步骤二,化合物2与5,5-二甲基-1,3-环己二酮在edci作用下发生酰化反应得到化合物3;
[0011]
步骤三,将化合物3加到化合物5的甲醇溶液中反应后得到化合物4。
[0012]
进一步,所述步骤一五氟苯酚采用可氨解醇或酚代替;所述化合物1为消旋体,对应异构体或它们的侧链长短不同的同系物;所述edci为偶联试剂,包括dcc,rococl,r为烷基;所述乙腈为溶液,为任何其它可使用的溶剂;
[0013]
所述15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯为含有不同聚乙二醇链接体;所述盐酸为三氟乙酸或其它的酸以及不同浓度的混合物。
[0014]
进一步,所述步骤一化合物2的核磁数据包括:
[0015]1hnmr(400mhz,d2o)δ4.39(dd,j=7.9,4.8hz,1h),4.20(dd,j=7.9,4.5hz,1h),3.72
–
3.29(m,16h),3.23
–
3.04(m,3h),2.77(dd,j=13.1,4.9hz,1h),2.56(d,j=13.0hz,1h),2.45(t,j=6.0hz,2h),2.06(t,j=7.2hz,2h),1.58
–
1.11(m,6h)。
[0016]
进一步,所述步骤二5,5-二甲基-1,3-环己二酮或为其它衍生物5,5-二烷基-1,3-环己二酮或1,3-环己二酮;所述dmf溶剂包括有机、无机溶剂;
[0017]
所述dmap为有机碱、无机碱或碱金属碱土金属的弱酸盐中的一种,所述有机碱包括吡啶,三乙胺;无机碱包括naoh;所述碱金属碱土金属的弱酸盐包括碳酸钠,碳酸钾。
[0018]
进一步,所述步骤三化合物5为
[0019][0020]
进一步,所述步骤三甲醇或用其他有机、无机溶剂代替;
[0021]
所述化合物4核磁数据包括:
[0022]1hnmr(400mhz,cdcl3)δ13.48(s,1h),7.69(d,j=7.4hz,1h),7.54
–
7.08(m,7h),6.75(t,j=5.4hz,1h),5.97(s,1h),5.19(dd,j=13.9,1.9hz,1h),5.07(s,1h),4.58
–
4.38(m,1h),4.37
–
4.21(m,1h),3.76
–
3.33(m,17h),3.15(dd,j=9.9,5.6hz,3h),2.90(dd,j=12.8,4.9hz,1h),2.78
–
2.56(m,2h),2.39
–
2.06(m,7h),1.86
–
1.58(m,8h),1.53
–
1.33(m,2h),1.01(s,6h)。
[0023]
进一步,所述的可裂解的ddebiotin-peg4-dbco类化合物的制备方法的反应通式如下:
[0024][0025]
本发明的目的在于提供一种上述制备方法制备得到的可裂解的ddebiotin-peg4-dbco类化合物,所述可裂解的ddebiotin-peg4-dbco类化合物的结构通式如下:
[0026][0027]
本发明的目的在于提供一种上述的通式化合物在生物化学,分子生物学,药物化学,医疗诊断领域的应用。
[0028]
本发明的目的在于提供一种上述的通式化合物作为官能团化的聚乙二醇链接剂修饰蛋白质,在制备诊断试剂,adc挂载,脂质体的表面靶向分子挂载上的用途。
[0029]
结合上述的所有技术方案,本发明所具备的优点及积极效果为:设计并合成了全
新结构的dde biotin-peg4-dbco可切割的生物素试剂。主要优点体现在,聚乙二醇链接剂的导入后的水溶性增强、dde连接体裂解条件的简易性与缓和性、dbco点击化学的高效性为一体。
[0030]
制备方法简单,原料易得,步骤短,成本低廉,应用前景广泛。并可作为官能团化的聚乙二醇链接剂修饰蛋白质,做诊断试剂,adc挂载,脂质体的表面靶向分子挂载等多种用途。
附图说明
[0031]
为了更清楚地说明本发明实施例的技术方案,下面将对本发明实施例中所需要使用的附图做简单的介绍,显而易见地,下面所描述的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下还可以根据这些附图获得其他的附图。
[0032]
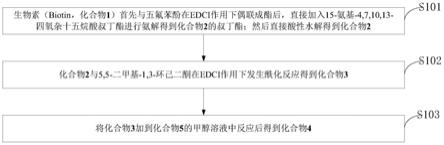
图1是本发明实施例提供的可裂解的ddebiotin-peg4-dbco类化合物的制备方法流程图。
具体实施方式
[0033]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0034]
本发明实施例提供了可裂解的ddebiotin-peg4-dbco类化合物的制备方法包括以下步骤:
[0035]
步骤一,生物素(biotin,化合物1)首先与五氟苯酚在edci作用下偶联成酯后,直接加入15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯进行氨解得到化合物2的叔丁酯;然后直接酸性水解得到化合物2;
[0036]
步骤二,化合物2与5,5-二甲基-1,3-环己二酮在edci作用下发生酰化反应得到化合物3;
[0037]
步骤三,将化合物3加到化合物5的甲醇溶液中反应后得到化合物4。
[0038]
所述化合物4(其示例中各个反应底物的用量和比例以及溶剂的选择在不影响反应效果的情况下可以合理改变)的制备方法的反应通式如下:
[0039][0040]
本发明的另一目的在于提供一类应用所述的生物探针化合物的制备方法,制备得到的化合物4,所述化合物4的结构及其结构通式如下:
[0041][0042]
进一步,所述化合物2的合成,还包括:
[0043]1hnmr(400mhz,d2o)δ4.39(dd,j=7.9,4.8hz,1h),4.20(dd,j=7.9,4.5hz,1h),3.72
–
3.29(m,16h),3.23
–
3.04(m,3h),2.77(dd,j=13.1,4.9hz,1h),2.56(d,j=13.0hz,1h),2.45(t,j=6.0hz,2h),2.06(t,j=7.2hz,2h),1.58
–
1.11(m,6h)。
[0044]
所述化合物4的合成,还包括:
[0045]1hnmr(400mhz,cdcl3)δ13.48(s,1h),7.69(d,j=7.4hz,1h),7.54
–
7.08(m,7h),6.75(t,j=5.4hz,1h),5.97(s,1h),5.19(dd,j=13.9,1.9hz,1h),5.07(s,1h),4.58
–
4.38(m,1h),4.37
–
4.21(m,1h),3.76
–
3.33(m,17h),3.15(dd,j=9.9,5.6hz,3h),2.90(dd,j=12.8,4.9hz,1h),2.78
–
2.56(m,2h),2.39
–
2.06(m,7h),1.86
–
1.58(m,8h),1.53
–
1.33(m,2h),1.01(s,6h)
[0046]
本发明的另一目的在于提供一种所描述的通式化合物在生物化学,分子生物学,药物化学,医疗诊断领域的应用。
[0047]
本发明的另一目的在于提供所描述的通式化合物作为官能团化的聚乙二醇链接剂修饰蛋白质,在制备诊断试剂,adc挂载,脂质体的表面靶向分子挂载上的用途。
[0048]
针对现有技术存在的问题,本发明提供了一种ddebiotin-peg4-dbco类化合物的制备方法,下面结合附图对本发明作详细的描述。
[0049]
如图1所示,本发明实施例提供的可裂解的ddebiotin-peg4-dbco类化合物的制备方法包括以下步骤:
[0050]
s101,生物素(biotin,化合物1)首先与五氟苯酚在edci作用下偶联成酯后,直接加入15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯进行氨解得到化合物2的叔丁酯;然后直接酸性水解得到化合物2;
[0051]
s102,化合物2与5,5-二甲基-1,3-环己二酮在edci作用下发生酰化反应得到化合物3;
[0052]
s103,将化合物3加到化合物5的甲醇溶液中反应后得到化合物4。
[0053]
所述步骤s101五氟苯酚采用可氨解醇或酚代替;所述化合物1为消旋体,对应异构体或它们的侧链长短不同的同系物;所述edci为偶联试剂,包括dcc,rococl,r为烷基;所述乙腈为溶液,为任何其它可使用的溶剂;
[0054]
所述15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯为含有不同聚乙二醇链接体;所述盐酸为三氟乙酸或其它的酸以及不同浓度的混合物。
[0055]
所述步骤s101化合物2的核磁数据包括:
[0056]1hnmr(400mhz,d2o)δ4.39(dd,j=7.9,4.8hz,1h),4.20(dd,j=7.9,4.5hz,1h),3.72
–
3.29(m,16h),3.23
–
3.04(m,3h),2.77(dd,j=13.1,4.9hz,1h),2.56(d,j=13.0hz,1h),2.45(t,j=6.0hz,2h),2.06(t,j=7.2hz,2h),1.58
–
1.11(m,6h)。
[0057]
所述步骤s102 5,5-二甲基-1,3-环己二酮或为其它衍生物5,5-二烷基-1,3-环己二酮或1,3-环己二酮;所述dmf溶剂包括有机、无机溶剂;
[0058]
所述dmap为有机碱、无机碱或碱金属碱土金属的弱酸盐中的一种,所述有机碱包括吡啶,三乙胺;无机碱包括naoh;所述碱金属碱土金属的弱酸盐包括碳酸钠,碳酸钾。
[0059]
所述步骤s103化合物5为
[0060][0061]
所述步骤s103甲醇或用其他有机、无机溶剂代替;
[0062]
在本发明一实施例中,所述的可裂解的ddebiotin-peg4-dbco类化合物的制备方法的反应通式如下:
[0063][0064]
本发明还提供可裂解的ddebiotin-peg4-dbco类化合物的结构通式如下:
[0065][0066]
下面结合具体实施例对本发明的技术方案作进一步描述。
[0067]
1.化合物2的合成
[0068]
室温下,将五氟苯酚(14.17g,77.01mmol)缓慢加到化合物1(此化合物是从武汉博仁凯润药业有限公司购买,具体信息请参照www.borenpharm.com)(17.10g,70mmol)和edci(16.10g,84mmol)的乙腈(150ml)溶液中去,室温1h后加入15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯(24.75g,77mmol),室温3h后反应已完全。反应液拉干后加入200ml水,二氯甲烷萃取,水洗3次,拉干过柱子得到32.58g白色固体。将该白色固体溶于6n盐酸(150ml),室温4h后,反应已完全,水相直接用二氯甲烷多次萃取,拉干得到27.53g白色固体,收率80%。
[0069]1hnmr(400mhz,d2o)δ4.39(dd,j=7.9,4.8hz,1h),4.20(dd,j=7.9,4.5hz,1h),3.72
–
3.29(m,16h),3.23
–
3.04(m,3h),2.77(dd,j=13.1,4.9hz,1h),2.56(d,j=13.0hz,1h),2.45(t,j=6.0hz,2h),2.06(t,j=7.2hz,2h),1.58
–
1.11(m,6h).
[0070]
2.化合物3的合成
[0071]
室温下,将5,5-二甲基-1,3-环己二酮(1.06g,7.57mmol)缓慢加到化合物2(3.72g,7.57mmol)和edci(1.14g,5.96mmol)的dmf(30ml)溶液中去,加入dmap(93mg,0.76mmol),室温过夜,tlc显示反应已完全。反应液旋干dmf,加入20ml饱和食盐水,盐酸调至酸性,二氯甲烷萃取,水洗3次,拉干过柱子得到2.23g白色固体,收率48%。
[0072]
3.化合物4的合成
[0073]
室温下,将化合物3(2g,3.26mmol)加到化合物5(1.08g,3.91mmol)的甲醇(30ml)溶液中去,室温过夜,tlc显示反应已完全。反应液拉干过柱子得到1.90g白色固体,收率67%。
[0074]1hnmr(400mhz,cdcl3)δ13.48(s,1h),7.69(d,j=7.4hz,1h),7.54
–
7.08(m,7h),6.75(t,j=5.4hz,1h),5.97(s,1h),5.19(dd,j=13.9,1.9hz,1h),5.07(s,1h),4.58
–
4.38(m,1h),4.37
–
4.21(m,1h),3.76
–
3.33(m,17h),3.15(dd,j=9.9,5.6hz,3h),2.90(dd,j=12.8,4.9hz,1h),2.78
–
2.56(m,2h),2.39
–
2.06(m,7h),1.86
–
1.58(m,8h),1.53
–
1.33(m,2h),1.01(s,6h).
[0075]
在本发明的描述中,除非另有说明,“多个”的含义是两个或两个以上;术语“上”、“下”、“左”、“右”、“内”、“外”、“前端”、“后端”、“头部”、“尾部”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,术语“第一”、“第二”、“第三”等仅用于描述目的,而不能理解为指示或暗示相对重要性。
[0076]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1