一种病毒的检测方法及其检测系统与流程
1.本发明涉及检验检疫的技术领域,特别涉及一种病毒的检测方法及其检测系统。
背景技术:
2.当前,国内外有thermo fisher、hamilton、perkin elmer和agilent等多家公司在生产与销售病毒检测类的工作站,其中,在深圳科技园具有分公司凯杰深圳生物工程有限公司的qiagen(总部位于德国杜塞尔多夫),在全自动生物样本处理工作站方面在生物样品自动化核酸提取和纯化的基础上,整合了自动化核酸提取与pcr体系配制和自动化加样三个步骤,其在售的产品qiasymphony sp在国内已获得医疗器械注册证,但是,该类产品占用的空间大。
3.早期快速诊断新冠病毒是防止病毒扩散的关键,目前应用最广的方法是逆转录rna,再作定量pcr扩增定性(rt-qpcr)分析病毒核酸,根据新型冠状病毒感染的肺炎诊疗快速指南(第一版),在符合疑似病例标准的基础上,需要对咽拭子等标本行实时荧光rt-pcr检测covid-19核酸阳性;rt-pcr技术具有高特异性和高灵敏度特性,能够对超低量的病毒核酸进行精确诊断,已经广泛应用于临床实验室。目前rt-qpcr通常特异检测新型冠状病毒(covid-19)n基因,e基因、s基因和orf1ab基因区域,rt-pcr检测n基因用于covid-19病毒筛查,而orf1ab检测为进一步证实covid-19病毒感染;病毒检测是防止病毒扩散的非常重要的环节,covid-19早期诊断的主要挑战是检测时间太长,通常需要几个小时或一天才能出检测结果,检测的时间很长,检测的速度和效率有待进一步提高。
技术实现要素:
4.本发明为了提高病毒检测的速度和效率,提供了一种病毒的检测方法及其检测系统,可以对病毒进行快速的检测。
5.本发明的病毒检测方法通过以下述技术方案实现:一种病毒的检测方法,包括以下步骤:
6.通过控制装置预设快速荧光pcr仪的运行参数,所述控制装置可以为电脑或手机等用户可以操作并进行控制的控制终端,所述控制装置通过通信单元控制快速荧光pcr仪,所述通信单元可以为蓝牙模块或usb接口等用于通信的单元,所述控制装置可以通过有线或无线对快速荧光pcr仪进行控制;
7.所述控制装置根据所述运行参数,通过控制快速荧光pcr仪的升降机构带动光学模块上升和下降以及控制快速荧光pcr仪的转盘正传和反转,以升高或降低试剂的温度,并通过光学模块获取荧光强度数据;
8.所述控制装置分析所述荧光强度数据,从而判定试剂中是否存在病毒。
9.在上述技术方案中,通过光学模块的升降可以和转盘的正反转同步进行,提升了检测速度和检测效率。
10.本技术方案可以进一步设置为:所述通过控制装置预设快速荧光pcr仪的运行参
数的步骤包括:预设第一时间,预设第二时间,预设第三时间,预设第四时间,预设转盘上第一恒温区域的温度,预设转盘上第二恒温区域的温度,预设转盘上第三恒温区域的温度和预设转盘上第四恒温区域的温度。
11.在上述技术方案中,通过光学模块与不同的恒温模块接触预设的时间,可以实现试剂的快速升温和快速降温。
12.本技术方案可以进一步设置为:所述控制装置根据所述运行参数,通过控制快速荧光pcr仪的升降机构,带动光学模块上升和下降以及快速荧光pcr仪的转盘正传和反转,以升高或降低试剂的温度,并通过光学模块获取荧光强度数据的步骤包括以下步骤:
13.所述控制装置控制电机,所述电机带动转盘转动,当所述第一恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第一恒温区域与光学模块接触,使试剂进行第一次升温,当试剂升温至第一温度时,所述光学模块在第一恒温区域停留第一时间;
14.所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第二恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第二恒温区域与光学模块接触,使试剂进行第二次升温,当试剂升温至第二温度时,所述光学模块在第二恒温区域停留第二时间;
15.所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第二恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第二恒温区域与光学模块接触,当试剂升温至第二温度时,所述光学模块在第二恒温区域停留第三时间;
16.所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第三恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第三恒温区域与光学模块接触,使试剂进行降温;
17.当试剂降温至第四恒温区域的温度时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第四恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第四恒温区域与光学模块接触,保持试剂的温度与第四恒温区域的温度相同,并且,所述光学模块在第四恒温区域停留第四时间,同时,所述光学模块获取荧光强度数据。
18.在上述技术方案中,通过光学模块上升和下降以及快速荧光pcr仪的转盘正传和反转,可以快速升高或降低试剂的温度,便于光学模块获取荧光强度数据。
19.本技术方案可以进一步设置为:所述第一温度为50℃,所述第二温度为95℃,所述第三温度为20℃,所述第四温度为60℃,所述第一时间为5分钟,所述第二时间和第三时间均为10秒,所述第四时间为30秒,并在所述第四时间里获取荧光强度数据。
20.还包括依次循环以下步骤n次,所述n为正整数,所述n次可以为四十次:
21.所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第二恒温区域转至光学模块的正下方时,所
述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第二恒温区域与光学模块接触,当试剂升温至第二温度时,所述光学模块在第二恒温区域停留第三时间的步骤;
22.所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第三恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第三恒温区域与光学模块接触,使试剂进行降温的步骤;
23.以及
24.当试剂降温至第四恒温区域的温度时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块上升,所述控制装置控制电机,所述电机带动转盘转动,当所述第四恒温区域转至光学模块的正下方时,所述控制装置通过控制快速荧光pcr仪的升降机构带动光学模块下降,使所述第四恒温区域与光学模块接触,保持试剂的温度与第四恒温区域的温度相同,并且,所述光学模块在第四恒温区域停留第四时间,同时,所述光学模块获取荧光强度数据的步骤。
25.通过采用上述技术方案,可以使光学模块不断在95℃与60℃的加热程序间循环40次,并记录40个荧光的荧光强度数据。
26.本技术方案可以进一步设置为:所述控制装置分析所述荧光强度数据,从而判定试剂中是否存在病毒的步骤包括以下步骤:
27.在具有x轴和y轴的二维坐标系中设置阈值线,所述阈值线为y轴荧光强度与x轴平行的线;
28.根据所述荧光强度数据,在二维坐标系中画出扩增曲线;
29.当所述扩增曲线与所述阈值线出现交点时,记录所述交点在二维坐标系中的坐标值,并设置所述交点坐标值的x轴坐标值为ct值;
30.若所述ct值落入预设的范围时,则判定试剂中存在病毒。
31.通过荧光强度数据画出扩增曲线,把二维坐标系中扩增曲线与所述阈值线的交点x轴坐标值置为ct值,根据ct值判定试剂中是否存在病毒的方法,非常直观,并且判定速度非常快,效率非常高。
32.本发明的病毒检测方法通过以下述技术方案实现:一种实现所述病毒的检测方法的检测系统,包括:控制装置和由所述控制装置控制的快速荧光pcr仪,所述快速荧光pcr仪包括壳体、电机、转盘、光学模块、升降机构、温度传感器和试管拆装结构,所述光学模块通过升降机构与壳体连接,所述升降机构带动光学模块上升和下降,所述升降机构与壳体固定连接,所述温度传感器和试管拆装结构均安装于光学模块上,所述转盘通过电机与壳体连接,所述电机与壳体固定连接,所述电机带动转盘转动,所述温度传感器用于检测试管拆装结构所固定的试管中的试剂温度,所述转盘具有第一恒温区域、第二恒温区域、第三恒温区域和第四恒温区域。
33.上述技术方案中,转盘在光学模块的下方正传和反转,光学模块可以同时上升和下降,可以加快病毒的检测速度,并且,在检测相同试剂数量的情况下,缩小了检测系统的体积,使检测仪器便于携带,方便在口岸检疫实验室、机场检疫实验室、检验检疫局实验室和码头检疫实验室等应用场景中的使用。
34.本技术方案可以进一步设置为:所述控制装置包括:
35.电机转动模块,用于控制电机的正传和反转;
36.荧光强度获取模块,用于控制光学模块获取荧光强度数据;
37.升降控制模块,用于控制升降机构带动光学模块的上升和下降;
38.温度检测模块,用于实时监控温度传感器检测出的试剂温度,所述控制装置实时采集试剂的温度值;
39.病毒判定模块,用于分析荧光强度数据,以判定试剂中是否存在病毒。
40.上述技术方案中,控制装置集中控制快速荧光pcr仪进行核实检测,使所述检测系统操作简单,使用方便。
41.本技术方案可以进一步设置为:第一恒温区域为温度范围50℃~70℃的恒温单元,第二恒温区域为温度范围80℃~100℃的恒温单元,第三恒温区域为温度范围0℃~20℃的恒温单元,第四恒温区域为温度范围40℃~60℃的恒温单元。
42.在上述技术方案中,预先设置相应的恒温区域,可以实现对试剂进行快速的升温和降温,以便对试剂进行病毒检测操作。
43.本发明相对于现有技术具有如下的优点及效果:
44.1、本发明中待检测的样品试剂温度变化快,可缩短病毒检测的整体运行时间,并且,通过转盘转动的同时上升下降光学模块的设计,进一步缩短了病毒的检测时间,有效提高了检测的速度和检测的效率。
45.2、本发明的圆形转盘设计以及在转盘的上方设置光学模块,充分运用了仪器设备内部的空间,缩小了检测仪器所占用的空间,使检测仪器体积小巧,方便携带,便于在口岸检疫实验室、机场检疫实验室、检验检疫局实验室和码头检疫实验室等应用场景中的使用。
46.3、本发明的检测方法一次性最多可以检测192个样本,在提高检测速度和检测效率的同时,还提高了一次性检测试剂样本的数量。
附图说明
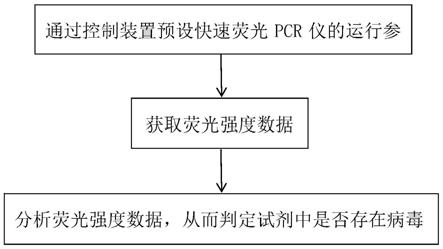
47.图1是本发明的检测方法的整体流程图。
48.图2是本发明的检测系统的整体框图。
49.图3是本发明的检测系统中控制装置的框图。
50.图4是本发明的检测系统中转盘的恒温区域和光学模块位置的平面布局图;
51.图5是本发明的试剂中存在病毒的扩增曲线图。
52.图6为本发明的检测方法的温度和时间参数图。
53.图7为本发明的快速荧光pcr仪的结构示意图。
54.其中,1为第一恒温区域,2为第二恒温区域,3为第三恒温区域,4为第四恒温区域,5为光学模块,6为电机,7为转盘,8为壳体,9为温度传感器,10为升降机构,11为试管拆装结构,12为通信单元。
具体实施方式
55.下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
56.实施例
57.如图1所示,一种病毒的检测方法,包括以下步骤:
58.通过控制装置预设快速荧光pcr仪的运行参数;
59.所述控制装置根据所述运行参数,通过控制快速荧光pcr仪的升降机构带动光学模块上升和下降以及控制快速荧光pcr仪的转盘正传和反转,以升高或降低试剂的温度,并通过光学模块获取荧光强度数据;
60.所述控制装置分析所述荧光强度数据,从而判定试剂中是否存在病毒。
61.预设所述快速荧光pcr仪的运行参数具体如表1所示:
[0062][0063]
表1
[0064]
所述所述控制装置根据所述运行参数,通过控制快速荧光pcr仪的升降机构带动光学模块上升和下降以及控制快速荧光pcr仪的转盘正传和反转,以升高或降低试剂的温度,并通过光学模块获取荧光强度数据的步骤具体如图6所示:
[0065]
①
把装有检测样品试剂的试管通过试管拆装结构安装于光学模块上,并使第二恒温区域的温度升高至95℃并保持恒定,第三恒温区域的温度降低至20℃并保持恒定,第四恒温区域的温度升高至60℃并保持恒定,第一恒温区域的温度升高至50℃并保持恒定。
[0066]
②
转动转盘,让温度升高至50℃的第一恒温区域转至光学模块正下方,下降光学模块与第一恒温区域接触,当安装有温度传感器的光学模块的温度升至50℃,开始保持5分钟;本步骤的作用:针对rna病毒,50℃保持5分钟,将rna核酸逆转录为dna核酸。
[0067]
③
升高光学模块,让温度升高至95℃的第二恒温区域转至光学模块正下方,下降光学模块与第二恒温区域接触,当光学模块温度升至95℃,开始保持10秒;本步骤的作用:95℃保持10秒,可以使dna核酸的双螺旋的双链结构因高温变成单链结构。
[0068]
④
升高光学模块,让温度升高至95℃的第二恒温区域转至光学模块正下方,下降光学模块与第二恒温区域接触,当光学模块温度升至95℃,开始保持10秒;本步骤的作用:95℃保持10秒,开始退火延申。
[0069]
⑤
升高光学模块,让温度降低至20℃的第三恒温区域转至光学模块正下方,下降光学模块与第三恒温区域接触,让光学模块温度降至60℃。本步骤的作用:试剂从95℃降温至60℃,试剂中的引物探针结合到单链结构中,在60℃时,试剂中的taq酶对单链核酸进行复制。
[0070]
⑥
升高光学模块,让温度升高至60℃的第四恒温区域转至光学模块正下方,下降光学模块与第四恒温区域接触,保持30秒,并采集荧光信号,并且,所述控制装置通过光学模块获取荧光强度数据。保持60℃的温度30秒后,试剂中的taq酶可以完成对单链核酸的复制,复制完成后,单链结构再变回双螺旋的双链结构,所述光学模块发出激发光照射试剂,试剂中的探针荧光基团吸收了激发光后,发出特定波长的荧光,光学模块记录该波长的荧光的荧光强度数据。
[0071]
⑦
循环步骤
④
、步骤
⑤
和步骤
⑥
共40次,可以使所述光学模块不断在95℃与60℃的加热程序间循环40次,并记录40个荧光的荧光强度数据。
[0072]
检测的试剂中含有足够多的与病毒核酸匹配的荧光探针,当检测样本中有病毒核酸时,探针会在延申过程中与病毒核酸匹配并被taq酶水解,水解后荧光探针发出荧光,设备就能收集到荧光信号;如果样本中没有病毒核酸,则探针无法被水解,就不会发出荧光;所以,每循环一次,就会多一倍的荧光探针被水解发出荧光,循环次数越往后,荧光强度就会越高,如果以循环次数为x轴,荧光强度为y轴,就能绘制出一个荧光曲线,有病毒核酸的样本就会出现一条荧光曲线,无病毒核酸的样本就没有荧光曲线。
[0073]
如图5所示的,以循环次数为x轴,光强度为y轴,绘制出原始的荧光曲线图,随着循环次数的增加,核酸被复制的越多,光的强度就越高。在前20次循环,由于荧光强度低于背景强度,荧光强度数据显示为0,当循环次数超过20次以后,荧光强度数据从0开始增大。
[0074]
所述控制装置分析所述荧光强度数据,从而判定试剂中是否存在病毒的步骤具体如下:
[0075]
设置阈值线,所述阈值线为y轴荧光强度与x轴平行的线,并根据所述荧光强度数据,在二维坐标系中画出扩增曲线,所述阈值线与扩增曲线在二维坐标系中出现交点,所述交点的坐标值为(28.38,0.1178),将所述坐标值的x轴值置为ct值,即:ct值为28.38。
[0076]
预设ct值≤37时,判定检测的试剂中存在病毒,而图6中的ct值为28.38,则判定检测的所述试剂中存在病毒。
[0077]
如图2所示,一种实现病毒检测方法的检测系统,包括:控制装置和由所述控制装置控制的快速荧光pcr仪,所述快速荧光pcr仪的结构示意图如图7所示,所述快速荧光pcr仪包括壳体8、电机6、转盘7、光学模块5、升降机构10、温度传感器9、试管拆装结构11和通信单元12,所述通信单元12安装于壳体8上,本实施例中的所述控制装置采用电脑,所述通信单元12采用usb接口,所述电脑通过usb接口控制快速荧光pcr仪,所述光学模块5通过升降机构10与壳体8连接,所述升降机构10带动光学模块5的上升和下降,所述升降机构10与壳体8固定连接,所述温度传感器9和试管拆装结构11均安装于光学模块5上,所述转盘7通过电机6与壳体8连接,所述电机6与壳体8固定连接,所述电机6带动转盘7转动,所述温度传感器9用于检测试管拆装结构11所固定的试管中的试剂温度,所述转盘7具有两个第一恒温区域1、两个第二恒温区域2、两个第三恒温区域3和两个第四恒温区域4,所述快速荧光pcr仪具有两个光学模块5,如图4所示,所述转盘7的两个第一恒温区域1、两个第二恒温区域2、两个第三恒温区域3和两个第四恒温区域4与两个光学模块5位置的平面布局图,所述转盘7可以在光学模块5的下方正传和反转。
[0078]
如图3所示,所述控制装置包括:
[0079]
电机转动模块,用于控制电机的正传和反转;
[0080]
荧光强度获取模块,用于控制光学模块获取荧光强度数据;
[0081]
升降控制模块,用于控制升降机构带动光学模块的上升和下降;
[0082]
温度检测模块,用于实时监控温度传感器检测出的试剂温度;
[0083]
病毒判定模块,用于分析荧光强度数据,以判定试剂中是否存在病毒。
[0084]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,
均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1