针对ALPPL2和/或ALPP的抗原结合分子及其用途的制作方法
针对alppl2和/或alpp的抗原结合分子及其用途
技术领域
1.本发明总体上涉及肿瘤学领域。具体而言,本发明涉及特异性结合alppl2和/或alpp但不结合alpl或alpi的抗原结合分子。
背景技术:
2.抗体是有吸引力的治疗剂,因为它们能够结合细胞表面抗原并清除癌细胞。临床上获批的抗体治疗剂包括赫赛汀(herceptin)和美罗华(rituxan),它们是治疗包括血液癌和实体癌在内的各种癌症的非常成功的药物。抗体疗法通过例如募集效应细胞(诸如自然杀伤细胞或t细胞)或通过调节癌细胞的信号传导通路而发挥作用。抗体也可以与毒素或放射性同位素缀合,以帮助清除癌细胞。成功抗体疗法的开发需要靶向优先在癌细胞上表达的细胞表面抗原。这是因为相同的表面抗原在正常健康细胞上表达可能会导致不期望的副作用。
3.一般而言,缺乏合适的肿瘤相关抗原来进行针对癌症的靶向抗体疗法。此外,开发针对此类抗原的有效疗法来治疗癌症是一项重大挑战。
4.相应地,通常希望克服或改善一个或多个上述难题。
技术实现要素:
5.本文公开了特异性结合alppl2和/或alpp但不结合alpl或alpi的抗原结合分子,其包含:
6.(a)重链可变区(vh),其包含vhcdr1、vhcdr2和vhcdr3氨基酸序
7.列;以及
8.(b)轻链可变区(v
l
),其包含vlcdr1、vlcdr2和vlcdr3氨基酸序列;其中vhcdr1、vhcdr2、vhcdr3、vlcdr1、vlcdr2和vlcdr3氨基酸序列的组合显示在表1中的任一行中。
9.本文公开了包含如本文定义的抗原结合分子和异源部分的嵌合分子。
10.本文公开了一种分离的多核苷酸,其包含编码如本文定义的抗原结合分子或嵌合分子的核酸序列。
11.本文公开了一种构建体,其包含编码如本文定义的抗原结合分子或嵌合分子的核酸序列,该核酸序列与一个或多个调控序列可操作地连接。
12.本文公开了一种宿主细胞,其包含如本文定义的构建体。
13.本文公开了一种药物组合物,其包含如本文定义的抗原结合分子或嵌合分子以及药学上可接受的载剂。
14.本文公开了一种用于降低癌细胞中alppl2的表达或活性的方法,该方法包括使癌细胞与如本文定义的抗原结合分子或嵌合分子接触。
15.本文公开了一种用于减少或抑制受试者中肿瘤的增殖、存活和活力的方法,该方法包括向受试者施用如本文定义的抗原结合分子或嵌合分子。
16.本文公开了一种治疗受试者中癌症的方法,其中该方法包括向受试者施用如本文
定义的抗原结合分子或嵌合分子。
17.本文公开了如本文所定义的抗原结合分子或嵌合分子用于治疗癌症。
18.本文公开了如本文定义的抗原结合分子或嵌合分子在制备用于治疗癌症的药物中的用途。
19.本文公开了治疗受试者中与不期望的alppl2表达相关的疾病或病况的方法,其中该方法包括向受试者施用如本文定义的抗原结合分子或嵌合分子。
20.本文公开了一种用于检测癌症的试剂盒,该试剂盒包含如本文定义的抗原结合分子或嵌合分子。
21.本文公开了一种确定受试者患癌症可能性的方法,其中该方法包括检测获自受试者的样品中的alppl2,其中与参照相比所述样品中alppl2水平的增加指示受试者患癌症的可能性。
22.本文公开了一种治疗受试者中癌症的方法,其中该方法包括a)检测获自受试者的样品中的alppl2,其中与参照相比所述样品中alppl2水平的增加指示受试者患癌症的可能性上升;并b)治疗发现患癌症可能性上升的受试者。
23.本文公开了一种鉴定可能对抗alppl2抗体治疗作出响应的受试者的方法,该方法包括检测获自受试者的样品中的alppl2,其中alppl2水平的增加指示该受试者可能对alppl2抗体的治疗有响应。
24.本文公开了一种鉴定和治疗可能对抗alppl2抗体治疗作出响应的受试者的方法,该方法包括a)检测获自受试者的样品中的alppl2,其中alppl2水平的增加指示该受试者可能对alppl2抗体的治疗有响应;并b)治疗发现可能对alppl2抗体的治疗有响应的受试者。
25.本文公开了一种制备特异性结合alppl2但不结合alpl或alpi的抗原结合分子的方法,该方法包括:
26.a)用alppl2免疫动物,优选兔,
27.b)从所述动物中分离出特异性结合alppl2但不结合alpl或alpi的b细胞,和
28.c)确定由所述b细胞表达的抗体的氨基酸序列。
附图说明
29.下文参照附图,仅以非限制性示例的方式来描述本发明的实施方案,在附图中:
30.图1示出了设定一系列标准来选择编码细胞膜蛋白的候选基因。胎盘样碱性磷酸酶alppl2成为后续靶标验证的最佳候选物之一。
31.图2示出了胃癌细胞系(顶部)和胃肿瘤微阵列(底部)的免疫组织化学染色。
32.图3示出了通过elisa和facs鉴定由兔b细胞上清液中产生的alppl2/alpp特异性克隆(顶部),并通过生物膜干涉技术在单一浓度下对所选克隆的亲和力测量(底部)。
33.图4示出了如通过elisa(顶部)和表面等离子共振(底部)测量的,对我们的人源化抗体和现有技术中公开的相当的人源化抗体的alppl2反应性和alpi反应性之间的比较。
34.图5示出了c36、c45和c130对不同胃癌细胞系的福尔马林固定、石蜡包埋(ffpe)切片的ihc染色(a)。通过c36对ffpe-人胃癌、卵巢癌、结直肠癌、胰腺癌、睾丸癌、间皮瘤和子宫内膜肿瘤微阵列的ihc染色,具有不同的h评分为ihc 1+、ihc 2+和ihc 3+(b)。通过c36对ffpe-正常组织的ihc染色。除了胎盘组织显示阳性ihc 2+染色外,所有正常组织均未显示
c36染色(阴性)(c)。
35.图6示出了通过facs筛选来鉴定由兔b细胞上清液中产生的所选克隆与恒河猴直系同源物的交叉反应性(a)。通过facs分析,重组人源化c4和c36克隆与过表达恒河猴直系同源物的cho细胞结合,但不与wt cho结合(b)。
36.图7示出了如通过表面等离子体共振(spr)测量的,所选克隆人源化后保留了高alpp/alppl2亲和力。
37.图8示出了人源化克隆对adcc的诱导。在高表达胃癌细胞系mkn1与jurkats cd16a报告细胞(顶行,左侧)的共培养物中,以及在低表达胃癌细胞系mkn74与jurkats cd16a报告细胞(顶行,右侧)的共培养物中测量的adcc诱导。通过对与原代nk细胞共培养的胃癌细胞系(中行,左侧),以及卵巢癌和胰腺癌细胞系与jurkats cd16a报告细胞的共培养物(中行,右侧)进行celltiter-glo测定测量的c4对adcc的增强作用。如通过在mkn74与jurkats cd16a报告细胞的共培养物中测量的,人源化c4的fc工程化对adcc的增强作用(底行)。
38.图9示出了通过celltiter-glo测定法测量adc对胃癌细胞系的杀伤作用。经由与二级抗体缀合的vc-mmaf的人源化克隆对高表达胃癌细胞系的杀伤作用(顶行)。与vc-mmae缀合的人源化c4(中行,左侧)和c12(中行,右侧)对胃癌细胞系的杀伤作用。经由与二级抗体缀合的vc-mmaf的人源化c4(底行,左侧)和c12(底行,右侧)对胃癌细胞系的杀伤作用。
39.图10示出了通过对与扩增的人t细胞共培养的癌细胞进行xcelligence实时细胞分析来测定,来源自人源化克隆的t细胞衔接体(t-cell engager)对不同癌细胞系的强效杀伤作用。无论靶标表达水平如何,c4始终表现出对胃癌、卵巢癌和胰腺癌细胞系的pm级杀伤作用。
40.图11示出了具有不同形式的不同抗cd3变体的t细胞衔接体对不同癌细胞系的强效杀伤作用。通过不同的抗cd3配对并以不同的形式,人源化fab片段适于产生强效t细胞衔接体。
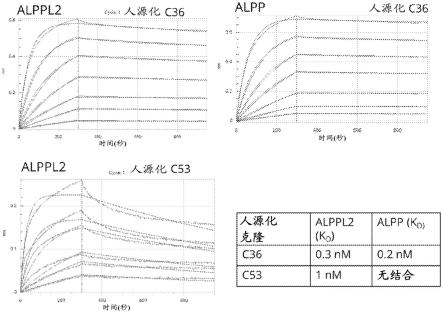
41.图12示出了所选克隆对alppl2而非alpp的反应性,以及这些克隆在人源化后对癌细胞的杀伤效力。facs显示嵌合性c53和c78结合alppl2但不结合alpp,而兔c4结合二者(a)。elisa显示嵌合性c53和c78结合alppl2,但不结合alpp(b)。显示了通过mkn74与jurkats cd16a报告细胞共培养所测量的嵌合性克隆对adcc的诱导(c)。elisa显示了嵌合性c53和c78与通过facs鉴定的过表达恒河猴直系同源物的cho细胞发生交叉反应(d)。人源化c53通过elisa显示出alppl2特异性(e),并且n87与jurkats cd16a报告细胞的共培养显示出人源化后保持了adcc诱导活性(f)。通过生物膜干涉技术测定,人源化c53表现出对alppl的nm级结合亲和力,但对alpp不是这样,而人源化c36对alppl2和alpp表现出相似的结合亲和力(g)。通过对与扩增的人t细胞共培养的n87胃癌细胞进行xcelligence实时细胞分析来测量的,人源化c53显示出t细胞衔接体对n87细胞的强效杀伤作用(h)。人源化c53 t细胞衔接体表现出与c36 t细胞衔接体相似的pm级杀伤作用。
42.图13示出了人源化c4、c36和c53与人碱性磷酸酶家族的不同同等型、癌细胞系和正常免疫细胞的结合概况。通过facs分析,人源化c4和c36显示出与人alppl2和alpp结合,但不与人alpi和alpl结合,而人源化c53与人alppl2特异性结合,但不与在293t细胞中瞬时表达的人alpp、alpi和alpl结合(a)。不同剂量的人源化c36、c4和c53显示出与alppl2/alpp阳性细胞系(nci-n87)结合,但不与阴性细胞系(miapaca-2)结合。人源化c53具有与市售抗
体(产品货号:ebioscience#14-9870-82)类似的结合亲和力,但与人源化c4和c36相比,结合亲和力更弱(b)。人源化c36、c4和c53显示出与幼稚和cd3/cd28微珠+il-2活化的人pbmc(cd4+/cd8+t细胞、b细胞、cd11b+髓系细胞)无结合(c)。人源化c36、c4和c53显示出与t细胞、b细胞和髓系细胞无结合(d)。
43.发明详述
44.本公开教导了特异性结合alppl2和/或alpp,而非alpl或alpi的抗原结合分子。所述抗原结合分子可以以约14pm至约10nm的亲和力结合alppl2和/或alpp或者表达alppl2和/或alpp的细胞。
45.本文公开了特异性结合alppl2和/或alpp但不结合alpl或alpi的抗原结合分子,其包含:(a)重链可变区(vh),其包含vhcdr1、vhcdr2和vhcdr3氨基酸序列;以及(b)轻链可变区(v
l
),其包含vlcdr1、vlcdr2和vlcdr3氨基酸序列;其中vhcdr1、vhcdr2、vhcdr3、vlcdr1、vlcdr2和vlcdr3氨基酸序列的组合显示在表1中的任一行中。
46.碱性磷酸酶胎盘样蛋白2(alppl2)是碱性磷酸酶(ap)家族的一员,由在胎盘滋养层中表达的两种密切相关的同等型(alppl2和alpp)以及两个广泛表达的成员alpl(组织非特异性,肝脏/骨骼/肾脏)和alpi(肠)组成。在一个实施方案中,抗原结合分子特异性结合alppl2和/或alpp。在一个实施方案中,抗原结合分子特异性结合人alppl2和/或人alpp。在一个实施方案中,由于对alppl2和/或alpp的高亲和力,抗原结合分子具有增强的功效。
47.在一个实施方案中,抗原结合分子不具有任何可检测到的与alpl或alpi的结合。在一个实施方案中,抗原结合分子不具有任何可检测到的与人alpl或人alpi的结合。这也可称为具有大于10nm、大于100nm、大于1μm、大于10μm、大于100μm或大于1mm的可检测到的与人alpl或人alpi结合的解离常数(kd)。在一个实施方案中,由于缺乏与alpl或alpi的结合,抗原结合分子具有期望的治疗窗口。在一个实施方案中,抗原结合分子不诱导(或诱导极小的)对正常细胞的t细胞杀伤作用。
48.不受理论束缚地,本发明人已经分离出针对肿瘤相关抗原,即人胎盘样碱性磷酸酶(alppl2)的单克隆抗体,其具有高亲和力(亚nm级kd)和特异性(对密切相关的alpl或alpi无反应性)、免疫组织化学活性(可用于开发配套诊断)、与非人灵长类动物直系同源物的交叉反应性(可用于毒理学研究)。本发明人已经通过将互补决定区(cdr)移植到人igg1骨架上,对一些克隆进行了人源化,并显示这些人源化抗体保留了对alppl2的高亲和力。本发明人还证明了,在jurkats报告细胞和原代自然杀伤(nk)细胞与胃癌细胞系的共培养测定中,这些裸人源化抗体诱导了强力的抗体依赖性细胞毒性(adcc)。在卵巢癌和胰腺癌细胞系中也观察到adcc诱导。通过初级缀合物(primary conjugate)在次级测定(secondary assay)中对癌细胞的杀伤作用,本发明人已经证明了使用这些人源化抗体作为抗体-药物缀合物的适用性。本发明人还通过这些人源化抗体与抗cd3抗体的异二聚化产生了双特异性抗体。这些双特异性抗体作为强效的t细胞衔接体(tce)发挥作用,并实现了对胃癌、卵巢癌和胰腺癌细胞系的皮摩尔(pm)级杀伤。因此,这些抗体可以用作针对在细胞表面上表达alppl2的肿瘤的靶向疗法。
49.表1示出了抗原结合分子上可以存在的cdr的可能组合。
50.51.52.[0053][0054]
表2示出了来源于36种抗体克隆的抗原结合分子中vh和v
l
序列(cdr1、2和3带下划线)的组合。
[0055]
[0056]
[0057]
[0058]
[0059][0060]
表3提供了人源化克隆的vh、v
l
序列的一些示例
[0061]
[0062][0063]
本发明的抗原结合分子可以是分离的、纯化的、合成的或重组的形式。合适的抗原结合分子可以选自抗体及其抗原结合片段,包括单克隆抗体(mab)、嵌合抗体、人源化抗体、人抗体、和此类抗体的抗原结合片段。抗原结合分子可以是多价的(例如,二价的)或单价的。在一些实施方案中,抗原结合分子包含fc结构域。在其它实施方案中,抗原结合分子缺少fc结构域。在一些实施方案中,抗原结合分子是单价抗原结合分子(例如,fab、scfab、fab'、scfv、单臂抗体等)。
[0064]
所谓“抗原结合分子”意指对靶抗原具有结合亲和力的分子。应当理解的是,该术语扩展到了免疫球蛋白、免疫球蛋白片段和表现出抗原结合活性的非免疫球蛋白衍生的蛋白质骨架。可用于实施本发明的代表性抗原结合分子包括抗体及其抗原结合片段。术语“抗原结合分子”包括抗体和抗体的抗原结合片段。
[0065]
如本文所定义的抗原结合分子可以是裸露的或者与其他分子或部分(例如毒素、放射性同位素、小分子药物、多肽等)缀合。
[0066]
如本文所用的术语“抗体”,意指任何抗原结合分子或分子复合物,其包含至少一个与特定抗原特异性结合或相互作用的互补决定区(cdr)。术语“抗体”包括全长免疫球蛋白分子及其多聚体(例如,igm),所述免疫球蛋白分子包含四条多肽链,即通过二硫键相互连接的两条重(h)链和两条轻(l)链。每条重链包含重链可变区(其可以缩写为hcvr或vh)和重链恒定区。重链恒定区包含3个结构域,即ch1、ch2和ch3。每条轻链包含轻链可变区(其可
以缩写为lcvr或v
l
)和轻链恒定区。轻链恒定区包含1个结构域(c
l
1)。vh和v
l
区域可以进一步细分为高变区,称为互补决定区(cdr),其间穿插着更保守的区域,称为框架区(fr)。每个vh和v
l
由3个cdr和4个fr组成,按以下顺序从氨基末端到羧基末端排列:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。在本发明的不同实施方案中,本发明抗体的fr(或其抗原结合部分)可以与人类种系序列相同,或者可以是天然的或人工修饰的。基于对两个或更多个cdr的并排分析,可以定义氨基酸共有序列。
[0067]
抗体包括任何类别的抗体,例如igg、iga或igm(或其亚类),并且抗体不必属于任何特定类别。根据抗体重链恒定区的抗体氨基酸序列,可以将免疫球蛋白分为不同的类别。免疫球蛋白主要有五类:iga、igd、ige、igg和igm,而且其中几种还可以进一步分为亚类(同种型),例如igg1、igg2、igg3、igg4、iga1和iga2。与不同类别的免疫球蛋白相对应的重链恒定区分别被称为α、δ、ε、γ和μ。不同类别免疫球蛋白的亚基结构和三维构型是众所周知的。
[0068]
如本文所用的,术语“互补决定区”(cdr;即cdr1、cdr2和cdr3)指的是抗体可变结构域的氨基酸残基,其存在是抗原结合所必需的。每个可变结构域通常具有标识为cdr1、cdr2和cdr3的三个cdr区域。每个互补决定区可以包含来自例如由kabat定义的“互补决定区”的氨基酸残基(即,轻链可变结构域中约第24-34(l1)、50-56(l2)和89-97位残基(l3)以及重链可变结构域中约第31-35(h1)、50-65(h2)和95-102位残基(h3);kabat等人,sequences of proteins of immunological interest,第5版public health service,national institutes of health,bethesda,md.(1991))和/或来自“高变环”的那些残基(即,轻链可变结构域中约第26-32(l1)、50-52(l2)和91-96位残基(l3)以及重链可变结构域中约第26-32(h1)、53-55(h2)和96-101位残基(h3);chothia和lesk j.mol.biol.196:901-917(1987))。在某些情况下,互补决定区可以包括来自根据kabat定义的cdr区域和高变环两者的氨基酸。
[0069]“人源化”抗体指的是包含来自非人cdr的氨基酸残基和来自人fr的氨基酸残基的抗体。在某些实施方案中,人源化抗体将基本上包含全部的至少一个(通常是两个)可变结构域,其中全部或基本上全部的cdr对应于非人抗体的cdr,并且全部或基本上全部的fr对应于人抗体的fr。人源化抗体任选地可以包含来源于人抗体的抗体恒定区的至少一部分。
[0070]
如本文所用的,“嵌合”分子是指包含一种或多种不相关类型的组分或者含有两种或更多种化学上不同区域的分子,这些组分或区域可以彼此缀合、融合、连接、翻译、通过接头附接、化学合成、由核酸序列表达等。例如,肽和核酸序列、肽和可检测标记物、不相关的肽序列等。在嵌合分子包含不同来源的氨基酸序列的实施方案中,嵌合分子包括(1)在自然界中未发现在一起的多肽序列(即,氨基酸序列的至少一种相对于其他氨基酸序列的至少一种是异源的),或者(2)非天然邻接的氨基酸序列。例如,如本文所用的“嵌合抗体”,指的是一种抗体,其中重链和/或轻链的一部分源自特定来源或物种,而重链和/或轻链的其余部分源自不同来源或物种。
[0071]
如本文所用的,术语“抗原”及其语法上的等同表述(例如,“抗原的”)指的是可被特定的体液或细胞免疫产物(例如,抗体分子或t细胞受体)特异性结合的化合物、组合物或物质。抗原可以是任何类型的分子,包括例如半抗原、简单中间代谢物、糖类(例如,寡糖)、脂类和激素,以及大分子,例如复合碳水化合物(例如,多糖)、磷脂和蛋白质。常见的抗原类别包括但不限于病毒抗原、细菌抗原、真菌抗原、原生动物和其它寄生生物抗原、肿瘤抗原、
参与自身免疫性疾病、过敏反应和移植排斥的抗原、毒素和其它混杂抗原。
[0072]“抗原结合位点”指的是抗原结合分子中提供与抗原相互作用的位点,即一个或多个氨基酸残基。例如,抗体的抗原结合位点包含来自互补决定区(cdr)的氨基酸残基。天然免疫球蛋白分子通常具有两个抗原结合位点,fab分子通常具有单个抗原结合位点。本文所述的抗原结合分子的抗原结合位点通常特异性结合抗原,更具体而言,结合该抗原的表位。
[0073]
术语“抗原结合片段”、“抗原结合部分”、“抗原结合结构域”和“抗原结合位点”在本文中可互换使用,指的是参与抗原结合的抗原结合分子的一部分。这些术语包括特异性结合抗原以形成复合物的任何天然存在的、酶促可获得的、合成的或基因工程改造的多肽或糖蛋白。
[0074]
抗体的抗原结合片段可以使用任何合适的标准技术,诸如蛋白水解消化或重组基因工程技术,包括操控和表达编码抗体可变结构域和任选地恒定结构域的dna,从例如完整抗体分子中获得。这种dna是已知的和/或可从例如商业来源、dna文库(包括,例如噬菌体-抗体文库)中轻易获得,或者可以合成。可以通过化学方式或利用分子生物学技术对dna进行测序和操控,从而例如,将一个或多个可变和/或恒定结构域排列成合适的构型,或者引入密码子、创建半胱氨酸残基、修饰、添加或删除氨基酸等。
[0075]
抗原结合片段的非限制性示例包括:(i)fab片段;(ii)f(ab')2片段;(iii)fd片段;(iv)fv片段;(v)单链fv(scfv)分子;(vi)dab片段;以及(vii)由模拟抗体高变区的氨基酸残基组成的最小识别单元(例如,分离的互补决定区(cdr),如cdr3肽),或受限的fr3-cdr3-fr4肽。其它工程化分子,例如结构域特异性抗体、单结构域抗体、结构域缺失抗体、嵌合抗体、cdr移植抗体、单臂抗体、双抗体、三抗体、四抗体、微抗体、纳米抗体(如,单价纳米抗体、双价纳米抗体等)、小型模块化免疫药物(smip)和鲨鱼的可变ignar结构域,也包含在如本文所用的表述“抗原结合片段”中。
[0076]
抗体的抗原结合片段通常将包含至少一个可变结构域。可变结构域可以是任何大小或氨基酸组成,并且一般将包含至少一个cdr,该cdr与一个或多个框架序列相邻或符合读框。在具有与v
l
结构域关联的vh结构域的抗原结合片段中,vh和v
l
结构域可以按照任何合适的排列彼此相对地配置。例如,可变区可以是二聚化的,并且含有v
h-vh、v
h-v
l
或v
l-v
l
二聚体。备选地,抗体的抗原结合片段可以含有单体vh或v
l
结构域。
[0077]
在某些实施方案中,抗体的抗原结合片段可以含有至少一个可变结构域,该可变结构域与至少一个恒定结构域共价连接。可以存在于本发明抗体的抗原结合片段中的可变和恒定结构域的非限制性示例性构型包括:(i)v
h-ch1;(ii)v
h-ch2;(iii)v
h-ch3;(iv)v
h-ch1-ch2;(v)v
h-ch1-ch2-ch3;(vi)v
h-ch2-ch3;(vii)v
h-c
l
;(viii)v
l-ch1;(ix)v
l-ch2;(x)v
l-ch3;(xi)v
l-ch1-ch2;(xii)v
l-ch1-ch2-ch3;(xiii)v
l-ch2-ch3;和(xiv)v
l-c
l
。在可变和恒定结构域的任何构型包括上文列出的任何示例性构型中,可变和恒定结构域可以直接相互连接,也可以通过全部或部分铰链区或接头区连接。铰链区可以至少由2个(例如,5、10、15、20、40、60或更多个)氨基酸组成,这引起单个多肽分子中相邻的可变和/或恒定结构域之间形成柔性或半柔性的连接。此外,本公开的抗体的抗原结合片段可以包含上文列出的任何可变和恒定结构域构型的同型二聚体或异型二聚体(或其它多聚体),它们彼此之间和/或与一个或多个单体vh或v
l
结构域以非共价方式缔合(例如,通过二硫键)。多特异性抗原结合分子通常将包含至少两种不同的可变结构域,其中每种可变结构域能够特异性结合分别的
抗原或同一抗原上的不同表位。使用本领域现有的常规技术,任何多特异性抗原结合分子形式,包括双特异性抗原结合分子形式,都可适应于在本公开抗体的抗原结合片段的情况中使用。
[0078]
术语“可变区”或“可变结构域”指的是参与抗原结合分子与抗原结合的抗体重链或轻链的结构域。天然抗体的重链和轻链的可变结构域(分别是vh和v
l
)通常具有相似的结构,每个结构域包含四个保守框架区(fr)和三个高变区(hvr)。参见,例如kindt等人,kuby immunology,第6版,w.h.freeman and co.,第91页(2007)。单个vh或v
l
结构域可能足以赋予抗原结合特异性。
[0079]
如本文所用的术语“恒定结构域”或“恒定区”,表示除可变区以外的抗体结构域的总和。恒定区不直接参与抗原的结合,但表现出多种免疫效应功能。
[0080]
术语“双特异性抗原结合分子”指的是一种多特异性抗原结合分子,其具有结合同一抗原或两种不同抗原上两种不同表位的能力。双特异性抗原结合分子可以是二价的、三价的或四价的。如本文所用的,“价”、“效价”、“结合价”或其其他语法变体意指抗原结合分子中抗原结合位点的数量。这些抗原识别位点可以识别相同的表位或不同的表位。二价和双特异性分子描述于例如,kostelny等人,1992.j immunol 148:1547;pack和pl
ü
ckthun,1992.biochemistry 31:1579;gruber等人,1994.j lmmunol 5368;zhu等人,1997.protein sci 6:781;hu等人,1996.cancer res.56:3055;adams等人,1993.cancer res.53:4026;和mccartney等人,1995.protein eng.8:301。三价双特异性抗原结合分子和四价双特异性抗原结合分子也是本领域已知的。参见,例如kontermann re(编著),springer heidelberg dordrecht london new york,第199-216页(2011)。双特异性抗原结合分子还可以具有高于4价,并且也在本发明的范围内。这种抗原结合分子可以通过例如对接和锁定(dock and lock)缀合方法来产生。(chang,c.-h.等人,在bispecific antibodies中.kontermann re(2011),见上文)。
[0081]
短语“特异性结合”或“特异性的结合”指的是在生理条件下,两个分子之间的结合反应至少是背景的两倍,更为典型的是,超过背景分子缔合的10至100倍。当使用的一种或多种可检测结合剂是蛋白质时,在蛋白质和其他生物制品的异质性群体中,特异性结合确定了蛋白质的存在。因此,在指定的免疫测定条件下,规定的抗原结合分子结合特定的抗原决定簇,从而鉴定其存在。在这种条件下,与抗原决定簇的特异性结合需要根据其对该决定簇的特异性来选择抗原结合分子。这种选择可以通过排除与其他分子发生交叉反应的抗原结合分子来实现。可以使用多种免疫测定形式来选择抗原结合分子(例如,免疫球蛋白),以使它们与特定抗原发生特异性免疫反应。例如,固相elisa免疫测定法通常用于选择与蛋白质发生特异性免疫反应的抗体(参见,例如harlow和lane,antibodies,a laboratory manual(1988),以了解可用于确定特异性免疫反应性的免疫测定形式和条件的描述)。确定结合亲和力和特异性的方法也是本领域众所周知的(参见,例如harlow和lane,见上文);friefelder,“physical biochemistry:applications to biochemistry and molecular biology”(w.h.freeman and co.1976))。
[0082]
在一个实施方案中,抗原结合分子与表达alppl2的细胞特异性结合,其亲和力为约14pm至约10nm。
[0083]“亲和力”或“结合亲和力”指的是分子(例如,抗原结合分子)的单个结合位点与其
结合伴侣(例如,抗原)之间非共价相互作用总和的强度。除非另有说明,如本文所用的“结合亲和力”指的是反映结合对成员(例如,抗原结合分子)之间1:1相互作用的内在结合亲和力。分子x对其伴侣y的亲和力通常可以用解离常数(kd)来表示,解离常数是解离和结合速率常数(分别为k
off
和k
on
)的比值。因此,只要速率常数的比值保持不变,等效亲和力可以包括不同的速率常数。可以通过本领域已知的常用方法来测量亲和力,包括本文所述的方法。测量亲和力的一种特定方法是表面等离子体共振(spr)。
[0084]
术语“多肽”、“肽”或“蛋白质”在本文中可互换使用,用于表示通过相邻残基的α-氨基和羧基之间的肽键彼此连接的氨基酸残基的线性系列。氨基酸残基通常是天然的“l”异构形式。然而,“d”异构形式的残基可以置换任何l-氨基酸残基,只要多肽保留了所需的功能特性。
[0085]
如本文所用的,术语“经修饰抗体”包括合成形式的抗体,其经过改变以使它们不再是天然存在的,例如,包含至少两个重链部分但不包含两个完整重链的抗体(如结构域缺失抗体或微抗体);多特异性形式的抗体(例如,双特异性、三特异性等),其经过改变以结合两种或更多种不同的抗原或者结合单一抗原上的不同表位;与scfv分子连接的重链分子等。scfv分子在本领域中是已知的并且描述于例如第5,892,019号美国专利中。另外,术语“经修饰抗体”包括多价形式的抗体(例如,与同一抗原的三个或更多个拷贝结合的三价、四价等抗体)。
[0086]
在一个实施方案中,抗原结合分子特异性结合恒河猴alppl2。恒河猴alppl2可具有如genbank id xp_011726419.1中所示的序列。
[0087]
在一个实施方案中,抗原结合分子包括:(a)vh氨基酸序列,其与表2或表3中任一行所示的vh氨基酸序列具有至少90%(包括至少91%至100%以及其间的所有整数百分比)序列同一性,和(b)v
l
氨基酸序列,其与表2或表3中和该vh氨基酸序列在同一行所示的v
l
氨基酸序列具有至少90%(包括至少91%至100%以及其间的所有整数百分比)序列同一性。
[0088]
在一个实施方案中,抗原结合分子特异性结合alppl2和alpp,但不特异性结合alpl或alpi。
[0089]
例如,所述抗原结合分子可以包括:
[0090]
a)与seq id no:281具有至少90%序列同一性的vh氨基酸序列和与seq id no:282具有至少90%序列同一性的vl氨基酸序列,
[0091]
b)与seq id no:283具有至少90%序列同一性的vh氨基酸序列和与seq id no:284具有至少90%序列同一性的v
l
氨基酸序列,
[0092]
c)与seq id no:285具有至少90%序列同一性的vh氨基酸序列和与seq id no:286具有至少90%序列同一性的v
l
氨基酸序列,
[0093]
d)与seq id no:287具有至少90%序列同一性的vh氨基酸序列和与seq id no:288具有至少90%序列同一性的v
l
氨基酸序列,
[0094]
e)与seq id no:289具有至少90%序列同一性的vh氨基酸序列和与seq id no:290具有至少90%序列同一性的v
l
氨基酸序列,
[0095]
f)与seq id no:291具有至少90%序列同一性的vh氨基酸序列和与seq id no:292具有至少90%序列同一性的v
l
氨基酸序列,或
[0096]
g)与seq id no:293具有至少90%序列同一性的vh氨基酸序列和与seq id no:
294具有至少90%序列同一性的v
l
氨基酸序列。
[0097]
本说明书中提及的短语“至少90%序列同一性”可以包括至少91%至100%以及其间的所有整数百分比。
[0098]
在一个实施方案中,抗原结合分子不与alpp结合。抗原结合分子可结合alppl2,但不结合alpp。在一个实施方案中,抗原结合分子与alppl2结合,但不与alpp、alpl或alpi结合。所述抗原结合分子可以包括:
[0099]
a)包含seq id no:31、seq id no:32和seq id no:33的氨基酸序列的重链可变区(vh),以及包含seq id no:34、seq id no:35和seq id no:36的氨基酸序列的轻链可变区(v
l
),
[0100]
b)包含seq id no:67、seq id no:68和seq id no:69的氨基酸序列的重链可变区(vh),以及包含seq id no:70、seq id no:71和seq id no:72的氨基酸序列的轻链可变区(v
l
),
[0101]
c)包含seq id no:85、seq id no:86和seq id no:87的氨基酸序列的重链可变区(vh),以及包含seq id no:88、seq id no:89和seq id no:90的氨基酸序列的轻链可变区(v
l
),
[0102]
d)包含seq id no:127、seq id no:128和seq id no:129的氨基酸序列的重链可变区(vh),以及包含seq id no:130、seq id no:131和seq id no:132的氨基酸序列的轻链可变区(v
l
),
[0103]
e)包含seq id no:133、seq id no:134和seq id no:135的氨基酸序列的重链可变区(vh),以及包含seq id no:136、seq id no:137和seq id no:138的氨基酸序列的轻链可变区(v
l
),
[0104]
f)包含seq id no:169、seq id no:170和seq id no:171的氨基酸序列的重链可变区(vh),以及包含seq id no:172、seq id no:173和seq id no:174的氨基酸序列的轻链可变区(v
l
);或
[0105]
g)包含seq id no:205、seq id no:206和seq id no:207的氨基酸序列的重链可变区(vh),以及包含seq id no:208、seq id no:209和seq id no:210的氨基酸序列的轻链可变区(v
l
)。
[0106]
在一个实施方案中,抗体包括:
[0107]
a)与seq id no:221具有至少90%序列同一性的vh氨基酸序列和与seq id no:222具有至少90%序列同一性的v
l
氨基酸序列,
[0108]
b)与seq id no:223具有至少90%序列同一性的vh氨基酸序列和与seq id no:224具有至少90%序列同一性的v
l
氨基酸序列,
[0109]
c)与seq id no:239具有至少90%序列同一性的vh氨基酸序列和与seq id no:240具有至少90%序列同一性的v
l
氨基酸序列,
[0110]
d)与seq id no:253具有至少90%序列同一性的vh氨基酸序列和与seq id no:254具有至少90%序列同一性的v
l
氨基酸序列,
[0111]
e)与seq id no:255具有至少90%序列同一性的vh氨基酸序列和与seq id no:256具有至少90%序列同一性的v
l
氨基酸序列,
[0112]
f)与seq id no:267具有至少90%序列同一性的vh氨基酸序列和与seq id no:
268具有至少90%序列同一性的v
l
氨基酸序列,或
[0113]
g)与seq id no:279具有至少90%序列同一性的vh氨基酸序列和与seq id no:280具有至少90%序列同一性的v
l
氨基酸序列。
[0114]
在一个实施方案中,抗原结合分子是抗体或其抗原结合片段或者嵌合抗原受体(car)。
[0115]
在一个实施方案中,抗体或其抗原结合片段是人源化的或嵌合的。
[0116]
在一个实施方案中,抗体或其抗原结合片段是人源化抗体,包括:
[0117]
a)重链可变区,其包含:
[0118]
i)vhfr1,其与evqlvesggglvqpggslrlscaasg(seq id no:295)具有至少90%序列同一性,
[0119]
ii)vhfr2,其与wvrqapgkgle(seq id no:296)具有至少90%序列同一性,
[0120]
iii)vhfr3,其与下列序列具有至少90%序列同一性:
[0121]
aswakgrftisrdnskntlylqmnslraedtavyyca(seq id no:297),
[0122]
iv)vhfr4,其与wgqgtlvtvss(seq id no:298)具有至少90%序列同一性,和
[0123]
b)轻链可变区,其包含:
[0124]
i)v
l
fr1,其与下列序列具有至少90%序列同一性:diqmtqspsslsasvgdrvtitcqag(seq id no:299),
[0125]
ii)vhfr2,其与wyqqkpgkvpk(seq id no:300)具有至少90%序列同一性,
[0126]
iii)vhfr3,其与gvpsrfsgsgsgtdftltisslqpedvatyyc(seq id no:301)具有至少90%序列同一性,
[0127]
i)vhfr4,其与fgqgtkveik(seq id no:302)具有至少90%序列同一性。
[0128]
在一个实施方案中,抗体或其抗原结合片段包含与下列序列具有至少90%(包括至少91%至100%以及其间的所有整数百分比)序列同一性的ch1氨基酸序列:
[0129]
astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkk(seq id no:319)。
[0130]
在一个实施方案中,抗体或其抗原结合片段包含与下列序列具有至少90%(包括至少91%至100%以及其间的所有整数百分比)序列同一性的c
l
氨基酸序列:
[0131]
rtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:320)。
[0132]
本公开涵盖的代表性抗原结合分子包括全长免疫球蛋白和抗原结合片段,包括重组抗原结合分子,其可以是单价或多价的、单特异性或多特异性的。
[0133]
在一个实施方案中,抗体或其抗原结合片段是全长抗体、基本上完整的抗体、fab片段、scfab、fab'、单链可变片段(scfv)或单臂抗体。
[0134]
在一个实施方案中,抗体具有选自由igg1、igg2、igg3和igg4组成的组中的同种型。在一个实施方案中,抗体是igg1抗体。该抗体可具有抗体依赖性细胞介导的细胞毒性(adcc)活性,并可诱导nk细胞杀伤作用。重链恒定区可以是野生型人fc区,或者是包含一个或多个氨基酸取代的人fc区。抗体可以具有稳定免疫球蛋白两条重链之间二硫键的突变,例如igg4铰链区中的突变,正如在现有技术中所公开的那样(例如,angal等人,1993.mol.immunol.,30:105-08)。另见,例如u.s.2005/0037000。重链恒定区还可以具有改
变抗原结合分子特性(例如,降低下列中一项或多项:fc受体结合、抗原结合分子糖基化、脱酰胺、与补体结合或甲硫氨酸氧化)的取代。在某些情况下,抗原结合分子可以具有突变,例如在第5,624,821号和第5,648,260号美国专利中描述的那些突变。在一些实施方案中,对抗原结合分子进行修饰,以降低或消除效应功能。
[0135]
在一个实施方案中,本发明的抗原结合分子是单价抗原结合分子。非限制性单价抗原结合分子包括:由v
l
、vh、c
l
和ch1结构域组成的fab片段;由v
l
、vh、c
l
和ch1结构域以及ch2结构域的一部分组成的fab'片段;由vh和ch1结构域组成的fd片段;由抗体单臂的v
l
和vh结构域组成的fv片段;单链抗体分子(例如,scfab和scfv);单域抗体(dab)片段(ward等人,1989nature341:544-546),其由vh结构域组成;以及单臂抗体(例如描述于us20080063641(genentech)中)或其它单价抗体(例如描述于wo2007048037(amgen)中)。
[0136]
在一个实施方案中,单价抗原结合分子包含fv片段。fv片段是具有抗原结合活性功能的免疫球蛋白分子的最小单元。scfv(单链可变片段)形式的抗原结合分子由重(vh)链和轻(v
l
)链的可变区组成,这些可变区通过柔性肽接头连接在一起,其可以在表达宿主如大肠杆菌和哺乳动物细胞中以功能形式轻松表达,允许蛋白质工程对scfv特性的改进,例如增加亲和力和改变特异性(ahmed等人,2012.clin dev immunol.2012:980250)。接头序列的代表性示例在下文第4.5节中描述。在scfv构建中,结构域的顺序可以是v
h-接头-v
l
或v
l-接头-vh,并且两个方向都可以适用。
[0137]
在一些实施方案中,scfv中使用的接头序列是五肽ggggs[seq id no:66](或者g4s或gly4ser)的多聚体。这些接头包括15聚体(g4s)3(huston等人,1988.proc natl acad sci usa.85(16),5879
–
83)、18聚体ggssrssssggggsgggg[seq id no:67](andris-widhopf等人,“generation of human scfv antibody libraries:pcr amplification and assembly of light-and heavy-chain coding sequences.”cold spring harbor protocols,2011(9))和20聚体(g4s)4(schaefer等人,“construction of scfv fragments from hybridoma or spleen cells by pcr assembly.”在antibody engineering中,r.kontermann和s.d
ü
bel,springer verlag,heidelberg,germany(2010)第21-44页)。已经提出了许多其他序列(经常在特定抗体序列的背景下),包括具有附加功能性的序列,例如表位标签或含有cre-lox重组位点的编码序列或改善scfv特性的序列。
[0138]
如所述的(schaefer等人,2010,见上文),scfv的克隆通常通过两步法重叠pcr(也称为重叠延伸剪接术或soe-pcr)来完成。首先对vh和v
l
结构域进行扩增和凝胶纯化,然后在组装pcr的单一步骤中进行二次组装。通过两个内引物的重叠或者通过添加其序列覆盖整个接头或更多的接头引物(三片段组装pcr)来产生接头。
[0139]
在带有适当翻译、转录起始位点和信号肽序列(在哺乳动物表达的情况下)的适当表达载体的背景下,克隆scfv的蛋白质编码序列后,可以在例如大肠杆菌、昆虫细胞或哺乳动物宿主细胞中重组产生单链fv(scfv)抗原结合分子。
[0140]
在一个实施方案中,单价抗原结合分子包含fab片段。在这种类型的说明性实例中,单价抗原结合分子是由或基本上由单一抗原结合片段(fab)和fc区组成的单臂抗体,其中该fc区包含第一和第二fc多肽,并且其中该第一和第二fc多肽存在于复合物中。
[0141]
含fc的单价抗原结合分子的重组表达通常可能导致不受欢迎的二价同型二聚体的污染。抑制同型二聚体形成的策略是已知的,包括将突变引入免疫球蛋白恒定区以产生
结构改变的方法,该结构改变支持多肽链之间产生不利的相互作用并抑制不想要的fc同型二聚体形成。这种促进异二聚化的策略的非限制性实例包括在两个多肽中引入把手入孔(knob-into-hole)(kih)结构,以及利用c
l
和ch1结构域的天然存在的异二聚化(参见,kontermann,见上文,第1-28页(2011)ridgway等人,1996.protein eng.9(7):617-21;atwell等人,1997.j mol biol.270(1):26-35;如wo 2005/063816中所述)。这些kih突变促进了含有把手的fc和含有孔的重链的异二聚化,从而改善了单价抗体的组装并降低了不需要的二价抗体的水平。
[0142]
还可能需要对抗原结合分子的fc结构域进行修饰以减少fc受体结合,并因此降低fcγriia介导的血小板活化的可能性。例如,已知人igg(包括igg1)中所谓的“lala”双突变(leu234ala和leu235ala一起)会显著损害fc受体结合和效应功能(lund等人,1991,j.immunol.147,2657
–
2662;lund等人,1992,mol.immunol.29:53
–
59)。对于人igg4,先前已经证明工程化突变s228p/l235e变体(sple)具有最小的fcγr结合(newman等人,2001,clin.immunol.98,164
–
174)。可以组合igg1或igg4 fc结构域中的突变,例如将人igg1中的lala突变与p329g处的突变组合,或将人igg4中的sple突变与p329g处的突变组合,完全消除了fcγr和c1q相互作用(schlothauer等人,2016,protein eng des.sel.29,457-466)。
[0143]
在一个实施方案中,抗原结合分子(例如,mab或其抗原结合片段)中抗体的每条igg1 fc链都携带p329g、l235a、l234a(p329g lala)突变或每条igg4 fc链都携带p329g、s228p、l235e突变,以减少或消除抗原结合分子的任何不期望的交联、血小板活化或免疫效应功能(例如,抗体依赖性细胞介导的细胞毒性(adcc)、抗体依赖性细胞介导的吞噬作用(adcp)和补体依赖性细胞毒性(cdc))。
[0144]
在一个实施方案中,抗原结合分子(或抗体)的每条igg1 fc链都携带突变,包括a)s239d、a330l和i332e,或b)f243l、r292p、y300l、v305i和p396l,其增强了抗原结合分子的免疫效应功能(例如,adcc)。
[0145]
在一个实施方案中,抗原结合分子(或抗体)包含与seq id no:321、seq id no:322或seq id no:323的氨基酸序列具有至少70%序列同一性的ch
2-ch3序列。
[0146]
抗原结合分子可以包含重链序列。重链序列可以例如包含或组成为表3中列出的vh序列,该vh序列与ch1序列(例如,seq id no:319)和ch2-ch3序列(例如,seq id no:321、seq id no:322或seq id no:33)融合。例如,重链序列可以包含与seq id no:326、seq id no:327、seq id no:329、seq id no:330、seq id no:332或seq id no:333具有至少70%序列同一性的氨基酸序列。
[0147]
抗原结合分子可以包含轻链序列。轻链序列可以例如包含或组成为表3中列出的v
l
序列,该v
l
序列与cl序列(例如,seq id no:320)直接融合。例如,轻链序列可以包含与seq id no:328、seq id no:331或seq id no:334具有至少70%序列同一性的氨基酸序列。
[0148]
在一个实施方案中,本发明涵盖通过共表达轻链、重链和截短型fc结构域产生的单价抗原结合分子。适当地,重链包含孔突变和p329g lala突变,而截短型fc结构域包含把手突变和p329g lala突变。
[0149]
在带有适当翻译、转录起始位点和信号肽序列(在适当情况下)的适当表达载体的背景下,克隆构建体的蛋白质编码序列后,可以在例如细菌(如大肠杆菌)、酵母、昆虫或哺乳动物宿主细胞中实现本文公开的抗原结合分子的表达。
[0150]
在一个实施方案中,抗原结合分子是多价抗原结合分子,其非限制性实例包括:免疫球蛋白、f(ab')2、串接scfv(tafv或scfv2)、scfv-fc、双抗体、dab2/vhh2、微抗体、zip微小抗体、barnase-barstar二聚体、把手入孔衍生物、seed-igg、异型fc-scfv、fab-scfv、(fab)2/sc(fab)2、scfv-(tnfα)3、scfv-jun/fos、fab
′‑
jun/fos、三抗体(tribody)、三聚体(trimerbody)、tribi微抗体(tribi-minibody)、barnase-barstar三聚体、collabody、dnl-f(ab)3、scfv
3-ch1/c
l
、fab-scfv2、igg-scfab、igg-scfv、scfv-igg、scfv
2-fc、f(ab
′
)
2-scfv2、scdb-fc、scdb-ch3、db-fc、scfv
2-h/l、dvd-ig、tandab、scfv-dhlx-scfv、dab
2-igg、dab-igg、dab-fc-dab、四抗体(tetrabody)、streptabody(scfv-链霉亲和素)4、(scfv-p53)4、[sc(fv)2]2、串接双抗体(tandab)及其组合。
[0151]
在一个实施方案中,多价抗原结合分子选自下列分子,即igg样抗体(例如,triomab/四源杂交瘤,trion pharma/fresenius biotech;把手入孔,genentech;crossmabs,roche;静电配对抗体,amgen;luz-y,genentech;链交换工程化结构域(seed)体,emd serono;biolonic,merus;和fab交换抗体,genmab)、对称性igg样抗体(例如,双靶向(dt)-ig,gsk/domantis;二合一抗体,genentech;交联型mab,karmanos癌症中心;mab2,f-star;和coy x体,coy x/pfizer)、igg融合体(例如,双可变结构域(dvd)-ig,abbott;igg样双特异性抗体,eli lilly;ts2ab,medimmune/az;bsab,zymogenetics;hercules,biogen idec;tvab,roche)、fc融合体(例如,scfv/fc融合体,academic institution;scorpion,emergent biosolutions/trubion,zymogenetics/bms;双亲和重靶向技术(fc-dart),macrogenics;双(scfv)
2-fab,national research center for antibody medicine)、fab融合体(例如,f(ab)2,medarex/amgen;双作用或bis-fab,genentech;对接和锁定(dnl),immunomedics;二价双特异性,biotechnol;和fab-fv,ucb-celltech)、基于scfv和双抗体的抗体(例如,双特异性t细胞衔接体(bites),micromet;串接双抗体(tandab),affimed;darts,macrogenics;单链双抗体,academic;tcr样抗体,ait,receptor logics;人血清白蛋白scfv融合体,merrimack;和combodies,epigen biotech)、igg/非igg融合体(例如,免疫细胞因子,emdserono,philogen,immungene,immunomedics;超抗原融合蛋白,active biotech;和免疫动员抗癌mtcr,immtac)和寡克隆抗体(例如,symphogen和merus)。
[0152]
在一个实施方案中,抗体是双特异性或三特异性抗体。在一个实施方案中,抗体是双特异性抗体。双特异性抗体可以是包含特异性结合alppl2的第一抗原结合位点和特异性结合cd3的第二抗原结合位点的抗体。在一个实施方案中,双特异性抗体能够与癌细胞结合并募集免疫效应细胞(例如,t细胞)以杀伤癌细胞。特异性结合cd3的抗原结合多肽是本领域熟知的。第二抗原结合位点可以例如包含来自莫罗单抗(muromonab)(orthoclone okt3)、福拉鲁单抗(foralumab)、特普利珠单抗(teplizumab)、博纳吐单抗(blinatumomab)或维西珠单抗(visilizumab)的cd3特异性cdr序列或vh/vl序列。双特异性抗体可以例如包含seq id no:335-337的vh cdr序列和seq id no:338-340的vl cdr序列。备选地,该抗体可以包含seq id no:341-343的vh cdr序列和seq id no:344-346的vl cdr序列。
[0153]
在一个实施方案中,本发明的双特异性抗体是使用“凸起入内腔”策略形成的,该策略也称为“把手入孔”,其作用是在第一和第二多肽之间设计一个界面以进行异型寡聚化。优选的界面包含抗体恒定结构域的ch3结构域的至少一部分。据报道,fc序列的ch3结构域中的“把手入孔”突变大大减少了同型二聚体的形成(参见,例如merchant等人,1998,
nature biotechnology,16:677-681)。“凸起”是通过用较大的氨基酸侧链(例如,酪氨酸或色氨酸)来替换第一多肽界面上的小氨基酸侧链而构建的。任选地在第二多肽的界面上创建与凸起大小相同或相似的补偿性“内腔”,其通过用较小的氨基酸侧链(例如,丙氨酸或苏氨酸)来替换大氨基酸侧链。当在第一或第二多肽的界面处存在定位和尺寸适当的凸起或内腔时,仅需要分别在相邻界面处设计相应的内腔或凸起。可以通过合成手段例如改变编码多肽的核酸或者通过肽合成来制成凸起和内腔。关于把手入孔的进一步描述,参见美国专利5,731,168;5,807,706;5,821,333。
[0154]
利用“凸起入内腔”策略来制备异型多聚体的一般方法包括在一种或分别的宿主细胞中表达编码第一多肽的第一多核苷酸和编码第二多肽的第二多核苷酸,该第一多核苷酸已经从原始多核苷酸改变以编码凸起,该第二多核苷酸已经从原始多核苷酸改变以编码内腔。将多肽在共同的宿主细胞中表达,从宿主细胞培养物中回收异型多聚体,或者在分别的宿主细胞中表达,回收和纯化,然后形成异型多聚体。在一些实施方案中,所形成的异型多聚体是多聚体型抗体,例如双特异性抗体。
[0155]
嵌合分子
[0156]
本文公开了包含本文定义的抗原结合分子和异源部分的嵌合分子。
[0157]
在一个实施方案中,异源部分是可检测部分、半衰期延长部分或治疗部分。
[0158]
本发明涵盖的可检测部分包括例如本领域已知的适于诊断检测(包括体外检测和体内成像)的任何种类。例如,可检测部分可以是荧光团、放射性核素报告子、含金属的纳米颗粒或微颗粒、超声造影剂(例如,纳米气泡型或微气泡型)或光学成像染料。这也包括在磁共振成像(mri)和磁性颗粒成像(mpi)中可见的对比颗粒。例如,可以通过荧光偏振、荧光活化细胞分选和荧光显微术对荧光团进行检测和/或成像,这可以或不必与电喷雾电离-质谱法(esi-ms)检测以及荧光发射计算机断层扫描(flect)成像相结合。放射性核素报告子可以通过放射性核素(核)检测进行检测和成像,例如单光子发射计算机断层扫描(spect)、正电子发射断层扫描(pet)或闪烁成像。可以利用光学成像来检测含金属的纳米颗粒或微颗粒,包括通常与顺磁性纳米颗粒或微颗粒一起使用的mri,以及通常与超顺磁性颗粒一起使用的mpi。可以使用超声成像,包括对比增强超声(ceu),来检测超声造影剂。
[0159]
可检测标记物也可以是酶-底物标记物。酶通常可以催化显色底物的化学变化,这可以使用多种技术来测量。例如,该酶可以催化显色底物的化学变化,这种变化可以使用多种技术进行测量。例如,该酶可以催化底物的颜色变化,这可以通过分光光度法来测量。备选地,该酶可以改变底物的荧光或化学发光。用于对荧光变化进行定量的技术如上所述。化学发光底物通过化学反应变为电子激发态,然后可以发射可测量(例如,使用化学发光测量仪)的光或向荧光接受体提供能量。酶性标记物的实例包括萤光素酶(例如,萤火虫荧光素酶和细菌萤光素酶;第4,737,456号美国专利)、萤光素、2,3-二氢酞嗪二酮、苹果酸脱氢酶、脲酶、过氧化物酶如辣根过氧化物酶(hrpo)、碱性磷酸酶、β-半乳糖苷酶、葡萄糖淀粉酶、溶菌酶、糖类氧化酶(例如,葡萄糖氧化酶、半乳糖氧化酶和葡萄糖-6-磷酸脱氢酶)、杂环氧化酶(诸如,尿酸酶(unease)和黄嘌呤氧化酶)、乳过氧化物酶、微过氧化物酶等。
[0160]
酶-底物组合的实例包括,例如:
[0161]
1)辣根过氧化物酶(hrpo)利用过氧化氢来氧化染料前体(例如,邻苯二胺(opd)或3,3',5,5'-四甲基联苯胺盐酸盐(tmb));
[0162]
2)碱性磷酸酶(ap),以对硝基苯磷酸盐为显色底物;和
[0163]
3)β-d-半乳糖苷酶(β-d-gal),具有显色底物(例如,p-硝基苯-β-d-半乳糖苷酶)或荧光底物4-甲基伞形酮基-β-d-半乳糖苷。
[0164]
在本发明的另一实施方案中,不需要对抗原结合分子进行标记,可以使用与该抗原结合分子结合的标记抗体来检测其存在。本发明的抗原结合分子可以用于任何已知的测定方法,例如竞争性结合测定、直接和间接夹心测定、免疫组织化学和免疫沉淀测定。
[0165]
在一个实施方案中,嵌合分子包含至少一个异源部分,即“半衰期延长部分”。半衰期延长部分可以包括,例如,(i)xten多肽;(ii)fc;(iii)白蛋白;(iv)白蛋白结合多肽或脂肪酸;(v)人绒毛膜促性腺激素13亚基的c-末端肽(ctp);(vi)pas;(vii)hap;(viii)转铁蛋白;(ix)聚乙二醇(peg);(x)羟乙基淀粉(hes);(xi)聚唾液酸(psa);(xii)阻断嵌合分子与清除受体结合的清除受体或其片段;(xiii)低复杂度肽;(xiv)或者它们的任意组合。在一些实施方案中,半衰期延长部分包含fc区。在其它实施方案中,半衰期延长部分包含通过接头融合的两个fc区。示例性异源部分还包括,例如,fcrn结合部分(例如,与fcrn结合的完整fc区或其部分)、单链fc区(scfc区,例如,如描述于第20080260738号美国专利公布文件、wo 2008/012543和wo 2008/1439545中)或可加工的scfc区。在一些实施方案中,异源部分可以包括用于非多肽部分的附着位点,该非多肽部分例如聚乙二醇(peg)、羟乙基淀粉(hes)、聚唾液酸或者这些部分的任何衍生物、变体或组合。
[0166]
在一些实施方案中,至少一个异源部分是治疗部分。在某些实施方案中,治疗部分选自抗癌部分(例如,细胞抑制/毒性的,和/或抗增殖药物)、免疫治疗部分和抗炎部分。在一些实施方案中,该治疗剂可用于治疗癌症。有用的抗癌剂种类包括化学治疗剂,其代表性实例包括抗微管蛋白剂、奥瑞他汀类(auristatins)、dna小沟结合物、dna复制抑制剂、烷化剂(例如,铂配合物类,如顺铂、单(铂)、双(铂)和三核铂配合物以及卡铂)、蒽环类药物、抗生素类、抗叶酸剂、抗代谢物、钙调蛋白抑制剂、化疗增敏剂、倍癌霉素、依托泊苷、氟化嘧啶类、离子载体类、莱希菌素(lexitropsin)、美登木素生物碱、亚硝基脲、顺氯氨铂(platinol)、成孔化合物、嘌呤抗代谢物、嘌呤霉素、放疗增敏剂、雷帕霉素、类固醇类、紫杉烷类、拓朴异构酶抑制剂、长春花生物碱等。
[0167]
在一个实施方案中,治疗部分是奥瑞他汀,例如单甲基奥瑞他汀f(mmaf)或单甲基奥瑞他汀e(mmae)。
[0168]
在一个实施方案中,抗原结合分子通过缬氨酸-瓜氨酸(vc)接头与治疗部分相连。
[0169]
多核苷酸、构建体和宿主细胞
[0170]
本文公开了一种分离的多核苷酸,其包含编码如本文定义的抗原结合分子或如本文定义的嵌合分子的核酸序列。
[0171]
术语“多核苷酸”或“核酸”在本文中可互换使用,指的是核苷酸的聚合物,可以是mrna、rna、crna、cdna或dna。该术语通常指长度至少为10个碱基的核苷酸的聚合形式,核苷酸可以是核糖核苷酸或脱氧核苷酸或任一类型核苷酸的修饰形式。该术语包括单链和双链形式的dna。
[0172]
本文还公开了包含编码如本文所述的抗原结合分子的核酸的载体。
[0173]
所谓“载体”意指核酸分子,优选来源于例如质粒、噬菌体或病毒的dna分子,核酸序列可插入或克隆到该分子中。载体优选包含一个或多个独特的限制性位点,并且能够在
限定的宿主细胞(包括靶细胞或其组织或者祖细胞或其组织)中自主复制,或者可以与限定的宿主的基因组整合,使得克隆的序列是可复制的。相应地,载体可以是自主复制载体,即作为染色体外实体存在的载体,其复制独立于染色体复制,例如是线性或闭合环状质粒、染色体外元件、微染色体或人工染色体。载体可以包含用于确保自我复制的任何构件。备选地,载体可以是这样一种载体,当将其导入宿主细胞时,它会整合入基因组内并与整合入其中的染色体一起复制。载体系统可以包含单一载体或质粒、两种或更多种载体或质粒(它们合起来包含待导入宿主细胞基因组的全部dna)或者转座子。载体的选择通常取决于载体与该载体将要导入其中的宿主细胞的相容性。载体还可以包括选择标志物,例如抗生素抗性基因,其可以用于选出合适的转化子。这种抗性基因的实例为本领域技术人员所熟知。
[0174]
本文公开了一种构建体,其包含编码如本文定义的抗原结合分子或如本文定义的嵌合分子的核酸序列,该核酸序列与一个或多个调控序列可操作连接。
[0175]
术语“构建体”指的是一种重组基因分子,其包括来自不同来源的一个或多个分离的核酸序列。因此,构建体是嵌合分子,其中两个或更多个不同来源的核酸序列组装成单个核酸分子,并且包括含有以下成分的任何构建体,(1)核酸序列,其包括在自然界中未发现在一起的调控序列和编码序列(即,核苷酸序列的至少一种相对于其他核苷酸序列的至少一种是异源的),或(2)编码非天然邻接的功能性rna分子或蛋白质部分的序列,或(3)非天然邻接的启动子部分。代表性构建体包括任何重组核酸分子,例如质粒、粘粒、病毒、自主复制多核苷酸分子、噬菌体、或者线性或环状单链或双链dna或rna核酸分子,它们来源于任何来源,能够进行基因组整合或自主复制,包含其中一个或多个核酸分子已经可操作地连接的核酸分子。本发明的构建体通常包括用于指导也包含在构建体中的感兴趣核酸序列(例如目标核酸序列或调控物核酸序列)表达的必要元件。这种元件可以包括调控元件或调节序列,例如与感兴趣的核酸序列可操作地连接的启动子(以便指导该核酸序列的转录),并且经常还包括多腺苷酸化序列。在本发明的某些实施方案中,构建体可以包含在载体内。除了构建体的组分之外,载体还可以包括例如一种或多种可选择标志物、一个或多个复制起点(例如原核和真核起点)、至少一个多克隆位点和/或促进构建体稳定整合到宿主细胞基因组中的元件。两个或更多个构建体可以包含在单个核酸分子例如单个载体中,或者可以包含在两个或更多个分别的核酸分子例如两个或更多个分别的载体中。“表达构建体”通常包括至少一种调控序列,其与感兴趣的核苷酸序列可操作地连接。以这种方式,例如,在表达构建体中提供与待表达的核苷酸序列可操作地连接的启动子,用于在生物体或其部分(包括宿主细胞)中表达。对于实施本发明,用于制备和使用构建体和宿主细胞的常规组合物和方法是本领域技术人员所熟知的,参见,例如molecular cloning:a laboratory manual,第3版第1、2和3卷,j.f.sambrook,d.w.russell和n.irwin,cold spring harbor laboratory press,2000。
[0176]
如本文所用的所谓“调控元件”、“调控序列”、“调节序列”等,意指在特定宿主细胞中表达可操作地连接的编码序列所必需的核酸序列(如dna)。例如,适用于原核细胞的调控序列包括启动子,以及任选的顺式作用序列,如操纵子序列和核糖体结合位点。适用于真核细胞的调控序列包括转录调控序列如启动子、多腺苷酸化信号、转录增强子、翻译调控序列如翻译增强子和内部核糖体结合位点(ires)、调节mrna稳定性的核酸序列,以及将由转录的多核苷酸编码的产物导向细胞内的细胞内区室或细胞外环境的导向序列。
[0177]
本文公开了一种宿主细胞,其包含如本文定义的构建体。
[0178]
术语“宿主”、“宿主细胞”、“宿主细胞系”和“宿主细胞培养物”可互换使用,并且指的是已经导入外源核酸的细胞,包括这类细胞的子代。宿主细胞包括“转化子”和“转化细胞”,其包括原代转化细胞和由其衍生的后代,而不考虑传代次数。后代的核酸内容物可能与亲本细胞不完全相同,而可能含有突变。本文包括与在原始转化细胞中筛选或选择的具有相同功能或生物学活性的突变后代。宿主细胞是可用于产生本发明抗原结合分子的任何类型的细胞系统。宿主细胞包括培养细胞,例如哺乳动物培养细胞(如cho细胞、bhk细胞、ns0细胞、sp2/0细胞、yo骨髓瘤细胞、p3x63小鼠骨髓瘤细胞、per细胞、per.c6细胞或杂交瘤细胞)、酵母细胞、昆虫细胞和植物细胞,诸如此类,还包括包含在转基因动物、转基因植物或培养的植物或动物组织中的细胞。
[0179]
药物组合物
[0180]
本文公开了一种药物组合物,其包含如本文定义的抗原结合分子或如本文定义的嵌合分子,以及药学上可接受的载剂。
[0181]
所谓“药学上可接受的载剂”意指一种由非生物学上或其它方面不想要的物质组成的药物媒介物,即可以将该物质与选定的活性剂一起施用于受试者而不会导致任何或实质性不良反应。载剂可以包括赋形剂和其他添加剂,例如稀释剂、去污剂、着色剂、润湿剂或乳化剂、ph缓冲剂、防腐剂等。
[0182]
代表性的药学上可接受的载剂包括本领域普通技术人员已知的任何和所有溶剂、分散介质、包衣、表面活性剂、抗氧化剂、防腐剂(例如,抗细菌剂、抗真菌剂)、等渗剂、吸收延迟剂、盐类、防腐剂、药物、药物稳定剂、凝胶、粘合剂、赋形剂、崩解剂、润滑剂、甜味剂、矫味剂、染料等类似物质及其组合(参见,例如remington's pharmaceutical sciences,第18版mack printing company,1990,第1289-1329页,通过引用方式并入本文)。除非任何常规载剂与活性成分不相容,否则涵盖其在药物组合物中的用途。
[0183]
药物组合物可以是多种形式。这些包括,例如,液体、半固体和固体剂型,如液体溶液剂(例如,可注射和可输注的溶液剂)、分散剂或混悬剂、脂质体和栓剂。优选的剂型取决于拟用的施用方式和治疗应用。合适的药物组合物可以通过静脉内、皮下或肌内方式施用。在一些实施方案中,组合物是以可注射或可输注的溶液剂的剂型存在。优选的施用方式是胃肠外施用(例如,静脉内、皮下、腹膜内、肌内施用)。在特定的实施方案中,通过静脉内输注或注射来施用药物组合物。在其它实施方案中,通过肌内或皮下注射来施用药物组合物。
[0184]
如本文所用的,短语“胃肠外施用”和“通过胃肠外施用地”意思是除了肠内和局部施用以外的施用方式,通常通过注射,并且包括但不限于静脉内、肌内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、椎管内、硬膜外以及胸骨内注射和输注。
[0185]
用于胃肠外施用的制剂包括无菌水性溶液剂或非水性溶液剂、混悬剂和乳剂。非水性溶剂的实例为丙二醇、聚乙二醇、植物油如橄榄油,以及可注射有机酯类如油酸乙酯。水性载剂包括水、醇性/水性溶液、乳液或悬浮液,包括盐水和缓冲介质。在本发明中,药学上可接受的载剂包括但不限于0.01-0.1m,优选0.05m磷酸盐缓冲液或0.8%盐水。其他常见的胃肠外媒介物包括磷酸钠溶液、林格氏葡萄糖、葡萄糖和氯化钠、乳酸林格氏液或不挥发油类。静脉内媒介物包括流体和营养补充剂、电解质补充剂,例如基于林格氏葡萄糖的补充
剂等。还可以存在防腐剂和其他助剂,例如抗微生物剂、抗氧化剂、螯合剂和惰性气体等。
[0186]
更具体而言,适用于注射用途的药物组合物包括无菌水性溶液剂(如果是水溶性的)或分散剂,以及用于临时制备无菌可注射溶液剂或分散剂的无菌粉末。在这种情况下,组合物必须是无菌的并且应该是流体,以达到存在易注射性的程度。它在生产和储存条件下应该是稳定的,并且优选地将其保存为防止微生物如细菌和真菌的污染作用。载剂可以是含有例如水、乙醇、多元醇(例如,甘油、丙二醇、液态聚乙二醇等)及其合适混合物的溶剂或分散介质。例如,通过使用包衣如卵磷脂和/或通过保持所需的粒径,可以维持适当的流动性。在特定的实施方案中,可以将本公开的药剂与媒介物缀合,以用于细胞递送。在这些实施方案中,可以将药剂封装在合适的媒介物中,以帮助将药剂递送至靶细胞、以提高药剂的稳定性或者使药剂的潜在毒性降至最低限度。如熟练的技术人员将理解的,多种媒介物适用于递送本公开的药剂。合适的结构化流体递送系统的非限制性示例可以包括纳米颗粒、脂质体、微乳液、胶束体、树枝状聚合物和其他含磷脂的系统。将本公开的药剂并入递送媒介物的方法是本领域已知的。尽管下文给出了多种实施方案,但应理解,本领域已知的将如本文所述的抗原结合分子并入递送媒介物的其他方法也涵盖在内。
[0187]
调整剂量方案以提供最佳的期望应答(例如,治疗应答)。例如,可以施用单次推注,也可以在一段时间内施用多个分次剂量,或者可以根据治疗情况的紧急状态所指示按比例减少或增加剂量。可以在多种场合施用本公开的抗原结合分子。单次剂量之间的间隔可以是每天、每周、每月或每年。如通过测量患者中修饰多肽或抗原的血液水平所指示,间隔也可以是不规则的。备选地,可以将抗原结合分子作为缓释制剂来施用,在这种情况下,需要减少施用频次。剂量和频次根据多肽在患者中的半衰期而变化。
[0188]
为了便于施用和剂量的均一性,将组合物配制成剂量单位形式可能是有利的。如本文所用的“剂量单位形式”,指的是适合作为待治疗受试者的单位剂量的物理上的离散单位;每个单位含有预定量的活性化合物,其经计算与所需的药学上可接受的载剂一起产生期望的治疗效果。本发明剂量单位形式的规格取决于并直接依赖于以下方面:(a)活性化合物的独特特征和要达到的特定治疗效果,以及(b)对于个体中的治疗敏感性,配制这种活性化合物的技术中固有的局限性。
[0189]
抗原结合分子的剂量和治疗方案可由熟练的技术人员确定。在某些实施方案中,通过注射(例如,皮下或静脉内)来施用抗原结合分子,剂量为约0.01至50mg/kg,例如0.01至0.1mg/kg,例如约0.1至1mg/kg、约1至5mg/kg、约5至25mg/kg、约10至50mg/kg。给药方案可以从例如每周一次到每2、3或4周一次不等。
[0190]
应当注意的是,剂量值可以随着要缓解的病况的类型和严重程度而变化。还应理解的是,对于任何特定的受试者,具体的剂量方案应根据个体需要和管理或监督组合物施用的人的专业判断,随时间进行调整,并且本文阐述的剂量范围仅是示例性的,并非意在限制所要求保护的组合物的范围或实践。
[0191]
治疗方法
[0192]
本文提供了一种用于降低细胞(例如癌细胞)中alppl2的表达或活性的方法。本文提供了一种用于降低癌细胞中alppl2的表达或活性的方法,该方法包括使癌细胞与如本文定义的抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物接触。
[0193]
本文公开了一种用于降低癌细胞中alppl2的表达或活性的方法,该方法包括使癌
细胞与如本文定义的抗原结合分子或如本文定义的嵌合分子接触。
[0194]
如本文所用的术语“肿瘤”,指的是任何恶性或良性的赘生细胞生长和增殖,以及所有癌前和癌性细胞和组织。术语“癌症”和“癌性”指的是或描述了哺乳动物中的生理状况,其典型的部分特征是细胞生长不受控制。如本文所用的,术语“癌症”指的是非转移性和转移性癌症,包括早期和晚期癌症。术语“癌前”指的是通常在癌症之前或发展为癌症的病况或生长。所谓“非转移性”意指一种良性的癌症或者保留在原发部位的癌症,并且未扩散入淋巴或血管系统或原发部位以外的组织。总体来说,非转移性癌症是指任何0期、i期或ii期癌症,有时是iii期癌症。所谓“早期癌症”意指非侵袭性或非转移性癌症,或者被归类为0、i或ii期癌症的癌症。术语“晚期癌症”通常指的是iii期或iv期癌症,但也可指ii期癌症或ii期癌症的亚期。本领域技术人员会理解,将ii期癌症归类为早期癌症或晚期癌症取决于癌症的具体类型。癌症的说明性实例包括但不限于乳腺癌、前列腺或睾丸癌、卵巢癌、子宫颈癌、胰腺癌、结直肠癌、肺癌、肝细胞癌、胃癌、肝癌、膀胱癌、尿路癌、甲状腺癌、肾癌、癌、黑色素瘤、脑癌、非小细胞肺癌、头颈部鳞状细胞癌、子宫内膜癌、多发性骨髓瘤、直肠癌、间皮瘤、子宫内膜癌和食管癌。在一个示例性实施方案中,癌症是结直肠癌、子宫内膜癌、胃癌、间皮瘤、卵巢癌、胰腺癌或睾丸癌。
[0195]
本文提供了一种用于减少或抑制受试者中肿瘤的增殖、存活和活力的方法,该方法包括向受试者施用如本文定义的抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物。
[0196]
本文公开了一种用于减少或抑制受试者中肿瘤的增殖、存活和活力的方法,该方法包括向受试者施用如本文定义的抗原结合分子或如本文定义的嵌合分子。
[0197]
术语“患者”包括接受预防性或治疗性处理的人类和其他哺乳动物受试者。如本文所用的,术语“受试者”包括任何人类或非人动物。例如,本发明的方法可用于治疗患有癌症的受试者。在一个实施方案中,受试者是人类。术语“非人动物”包括所有脊椎动物,例如哺乳动物和非哺乳动物,如非人灵长类动物、羊、狗、牛、鸡、两栖动物、爬行动物等。例如,本发明的方法可用于治疗患有癌症的受试者。在一个实施方案中,受试者是人类。术语“非人动物”包括所有脊椎动物,例如哺乳动物和非哺乳动物,如非人灵长类动物、羊、狗、牛、鸡、两栖动物、爬行动物等。
[0198]
本文公开的方法可以包括向受试者施用“治疗有效量”的药剂(例如,抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物)。如本文所用的,术语“治疗有效量”在其含义内包括无毒但足够量的药剂或化合物以提供所需的治疗效果。所需的确切量将因受试者而异,这取决于多种因素,例如接受治疗的物种、受试者的年龄和总体状况、接受治疗的病况的严重程度、所施用的具体药剂和施用方式等。因此,无法规定一个确切的“有效量”。然而,对于任何给定的情况,本领域普通技术人员可以只通过常规实验来确定适当的“有效量”。
[0199]
在一个实施方案中,提供了一种治疗受试者中癌症的方法,其中该方法包括向受试者施用本文定义的抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物。
[0200]
本文公开了一种治疗受试者中癌症的方法,其中该方法包括向受试者施用本文定义的抗原结合分子或本文定义的嵌合分子。
[0201]
如本文所用的术语“治疗/处理”,可以指的是(1)防止或延迟病症的一种或多种症状的出现;(2)抑制病症或病症的一种或多种症状的发展;(3)缓解病症,即引起病症或病症的至少一种或多种症状的消退;和/或(4)引起病症的一种或多种症状的严重程度降低。
[0202]
在一个实施方案中,癌症是胃癌、卵巢癌或胰腺癌。
[0203]
本文公开了如本文定义的抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物用作药物。
[0204]
本文公开了如本文所定义的抗原结合分子或如本文所定义的嵌合分子用于治疗癌症。
[0205]
本文公开了抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物在制备用于治疗有需要的受试者的药物中的用途。受试者可以是患有癌症的受试者。
[0206]
本文公开了如本文定义的抗原结合分子或如本文定义的嵌合分子在制备用于治疗癌症的药剂中的用途。
[0207]
本文公开了治疗受试者中与不期望的alppl2表达相关的病症或病况的方法,其中该方法包括向受试者施用如本文定义的抗原结合分子、嵌合分子、多核苷酸、构建体、载体、宿主细胞或药物组合物。
[0208]
本文公开了治疗受试者中与不期望的alppl2表达相关的病症或病况的方法,其中该方法包括向受试者施用本文定义的抗原结合分子或本文定义的嵌合分子。
[0209]
在一个实施方案中,与不期望的alppl2表达相关的病症或病况是癌症。
[0210]
在一个实施方案中,癌症是实体癌。
[0211]
在一个实施方案中,癌症是子宫颈癌、结肠癌、子宫内膜癌、胃癌、卵巢癌或胰腺癌。
[0212]
试剂盒
[0213]
本文公开了一种用于检测癌症的试剂盒,该试剂盒包含本文定义的抗原结合分子或嵌合分子。
[0214]
诊断方法
[0215]
本文公开了一种确定受试者患癌症可能性的方法,其中该方法包括检测获自受试者的样品中的alppl2,其中与参照相比样品中alppl2水平的增加指示受试者患癌症的可能性。
[0216]
在一个实施方案中,该方法包括用本文定义的抗原结合分子或本文定义的嵌合分子检测alppl2。
[0217]
本文公开了一种治疗受试者中癌症的方法,其中该方法包括a)检测获自受试者的样品中的alppl2,其中与参照相比,样品中alppl2水平的增加指示受试者患癌症的可能性上升;并b)治疗发现患癌症可能性上升的受试者。
[0218]
在一个实施方案中,该方法包括用本文定义的抗原结合分子或本文定义的嵌合分子检测alppl2。
[0219]
在一个实施方案中,该方法包括用本文定义的抗原结合分子或本文定义的嵌合分子治疗受试者。
[0220]
本文公开了一种鉴定可能对抗alppl2抗体治疗作出响应的受试者的方法,该方法包括检测获自受试者的样品中的alppl2,其中alppl2水平的增加指示受试者可能对alppl2
抗体的治疗有响应。
[0221]
在一个实施方案中,该方法包括用本文定义的抗原结合分子或本文定义的嵌合分子检测alppl2。
[0222]
本文公开了一种鉴定和治疗可能对抗alppl2抗体治疗作出响应的受试者的方法,该方法包括a)检测获自受试者的样品中的alppl2,其中alppl2水平的增加指示受试者可能对alppl2抗体的治疗有响应;并b)治疗发现可能对alppl2抗体的治疗有响应的受试者。
[0223]
如本文所用的,“和/或”指的是并且涵盖一个或多个相关所列项目的任何和所有可能的组合,以及当解释为备选(或)时缺少组合。
[0224]
如在本技术中所使用的,单数形式的“一个(a)”、“一种(an)”和“所述或该(the)”包括复数指代,除非在上下文中另有明确说明。例如,术语“一种药剂”包括多个/种药剂,包括它们的混合物。
[0225]
所谓“约”意指数量、水平、值、数字、频次、百分比、尺寸、大小、量、重量或长度与参照数量、水平、值、数字、频次、百分比、尺寸、大小、量、重量或长度相差多达15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%。
[0226]
除非上下文另有要求,否则在整个本说明书和随后的声明中,单词“包含/包括(comprise)”以及一些变型诸如“包含/包括(comprises)”和“包含/包括(comprising)”将被理解为意味着包括所述的整数或步骤或者整数或步骤组,但不排除任何其它整数或步骤或者整数或步骤组。
[0227]
本说明书中对任何在先出版物(或从中得出的信息)或任何已知内容的引用不是也不应被视为确认或承认或以任何形式暗示,即该在先出版物(或从中得出的信息)或已知内容构成本说明书所涉及研究领域的公知常识的一部分。
[0228]
本领域技术人员将会理解,除了那些具体描述的内容之外,本文描述的本发明易于进行变化和修改。应当理解,本发明包括落入精神和范围内的所有这类变化和修改。本发明还包括在本说明书中单独或共同提及或指出的所有步骤、特征、组合物和化合物,以及任何两个或更多个所述步骤或特征的任何和所有组合。
[0229]
现在将参考以下实施例描述本发明的某些实施方案,这些实施例仅用于说明的目的,并非意在限制上文所述的通用性范围。
实施例
[0230]
靶标id和背景
[0231]
胃癌是东亚的一种常见疾病,其中79%的患者被诊断为iv期,五年生存率低于5%。一种新的细胞表面生物标志物alppl2被鉴定为治疗性抗体和配套诊断的靶标。通过严格的生物信息学分析,对来自19名胃癌患者的rna测序数据进行生物标志物鉴定。
[0232]
在免疫组织化学染色中使用市售抗alppl2抗体在6种胃癌细胞系中验证了alppl2蛋白表达。在过表达alppl2 mrna的胃癌细胞系中观察到强的膜染色,而在不过表达alppl2转录本的细胞系中未观察到明显的染色。还通过对2种胃肿瘤微阵列的免疫组织化学染色评估了临床患病率。对疾病的不同阶段和胃的不同区域的总共198个肿瘤核心进行染色。结果表明,198例中有32例出现alppl2膜染色,占16%。在相邻匹配和不匹配的正常组织中均未观察到明显的膜染色。
[0233]
抗体生成
[0234]
通过用抗原免疫家兔来产生针对人alppl2的抗体。通过直接从兔单一b细胞中克隆抗体基因来分离兔抗体。
[0235]
在筛选过程中,选择了与alppl2结合但不与在正常肠组织中表达的相关alpi结合的克隆(图1和2)。总共分离出36种对人alpp/alppl2具有高亲和力的克隆。可变区和互补决定区的氨基酸序列如表1和2所示。
[0236]
亲和力和特异性
[0237]
通过elisa和高通量流式细胞术来筛选和鉴定特异性克隆(图3)。用截短型(用于elisa筛选)或全长(用于facs筛选)alpi和alppl2转染兔肾细胞。
[0238]
进一步筛选出对alppl2/alpp具有特异性但对alpi没有特异性的克隆子集,用于使用生物膜干涉技术分析来进行亲和力测量(图3)。在该技术中,将来自兔b细胞的单一浓度的不同上清液克隆固定在蛋白a生物传感器上。然后将生物传感器与分析物一起孵育,以测量亲和力。
[0239]
通过将cdr移植到相同的骨架上工程化改造了现有技术中公开的可比的人源化单克隆抗体,并通过elisa评估与alppl2和alpi二者的结合。该可比的人源化单克隆抗体具有下列vh和v
l
序列:
[0240][0241]
合成基因并克隆到表达载体中用于产生重组抗体。图4中的表面等离子体共振数据表明,现有技术中公开的抗体显示出与alpi的非特异性结合,而本发明的抗体却不是这样。
[0242]
免疫组织化学(ihc)活性
[0243]
为了能够开发配套诊断,对抗体的ihc活性进行了评估(图5)。通过蛋白酶k消化进行抗原修复,而不是热介导的抗原修复,实现了检测。通过ihc,c36、c45和c130实现了alppl2+ve细胞系(sch)和福尔马林固定石蜡包埋(ffpe)的人类肿瘤组织中的检测。这表明这些抗体可以在患者分层中具有诊断应用,并在治疗alppl2/alpp+ve肿瘤方面具有治疗应用,包括胃癌、卵巢癌、结直肠癌、胰腺癌、子宫内膜癌、间皮瘤和睾丸癌。c36在除胎盘外的所有正常组织中均呈阴性染色,表明alppl/alpp在正常组织中无/低表达。这也表明了这些抗体在临床上的最佳治疗窗。
[0244]
非人灵长类动物(nhp)的交叉反应性
[0245]
进一步评估了抗体与非人灵长类动物直系同源物的交叉反应性(图6)。所选克隆显示出对恒河猴直系同源物的反应性。
[0246]
人源化克隆(亲和力、选择性和特异性)
[0247]
通过将cdr移植到人igg1骨架,对所选克隆(c4、c15、c131、c12、c18、c36和c53)进行人源化。使用表面等离子体共振显示,这些人源化克隆保留了高alpp/alppl2亲和力(图
7)。使用biacore t200对表面等离子体共振进行了研究。将配体(例如,alppl2或alpp)固定在生物传感器cm5芯片上,用链霉亲和素捕获。然后将装载有配体的传感器与不同浓度的分析物(重组表达的人源化抗体克隆)一起孵育,以测量亲和力。
[0248]
人源化克隆(c4、c36和c53)保持了对癌症特定的alppl2和/或alpp的选择性,但对广泛表达的alpi和alpl没有选择性(图13)。人源化克隆也对癌细胞具有特异性,但对正常的幼稚和受刺激的免疫细胞不具有特异性(图13)。
[0249]
人源化克隆(adcc)
[0250]
首先通过报告物或原代nk细胞与癌细胞系的共培养来评估抗体依赖性细胞毒性,从而测试人源化克隆的治疗功效(图8)。与其他克隆相比,c4在具有高和低靶标表达的两种胃癌细胞系中产生最强力的adcc诱导。在原代nk细胞与不同胃癌细胞系的共培养测定中证实了c4的效力。c4实现了对高表达细胞系的几乎完全杀伤,并显示出与靶标表达水平成比例的效力(最大%杀死和ec50)。另外,还在报告测定中测试了c4,并且证实了对不同卵巢癌和胰腺癌细胞系的adcc诱导。
[0251]
对人源化c4的fc区进一步改造以增强adcc。报告测定进一步证实了具有工程化fc的人源化c4更强力地诱导胃癌细胞系的adcc。
[0252]
人源化克隆(adc)
[0253]
评估了使用这些人源化抗体作为抗体-药物缀合物的适用性。首先,在与vc-mmaf缀合的二抗的存在下测试了这些抗体对胃癌细胞系的杀伤作用(图9)。次级adc测定揭示了克隆之间的一些效力差异;仅在具有高靶标表达的所选胃癌细胞系中观察到杀伤作用,而在其他细胞系中则没有。使用与vc-mmae缀合的相同抗体证实了这些结果。抗体与vc-mmae的初级缀合增强了在次级adc测定中观察到的对相同胃癌细胞系的杀伤作用。
[0254]
人源化克隆(t细胞衔接体)
[0255]
进一步例示了这些人源化抗体可以成功地适于用作t细胞衔接体,以诱导强效的t细胞介导的癌细胞杀伤(图10、图11和图12)。通过人源化克隆与抗cd3抗体的异二聚化,双特异性抗体实现了对胃癌、卵巢癌和胰腺癌细胞系的强效和特异性杀伤,而与靶标表达水平无关。尤其是,c4在pm浓度下实现了对多种癌细胞系的几乎完全杀伤。
[0256]
alppl2特异性克隆
[0257]
嵌合和人源化c53克隆表现出对alppl2而非alpp的结合特异性(图12)。嵌合c53对恒河猴直系同源物也具有交叉反应性。使用生物膜干涉技术比较人源化c53与人源化c36对alppl和alpp的结合亲和力。在该技术中,将生物素化配体(即alppl2或alpp)固定在sa生物传感器上。然后将装载有配体的传感器与不同浓度的分析物(重组表达的人源化抗体克隆)在缓冲液中一起孵育。通过生物膜干涉技术测定,人源化c53抗体表现出对alppl的nm级结合亲和力,但对alpp不是这样,而人源化c36对alppl2和alpp表现出相似的结合亲和力。
[0258]
进一步例示了人源化c53抗体在adcc中保持其杀伤效力,并适于用作t细胞衔接体来诱导强效的t细胞介导的癌细胞杀伤。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1