制备用于合成鞘氨醇-1-磷酸酯受体激动剂的中间体的方法与流程
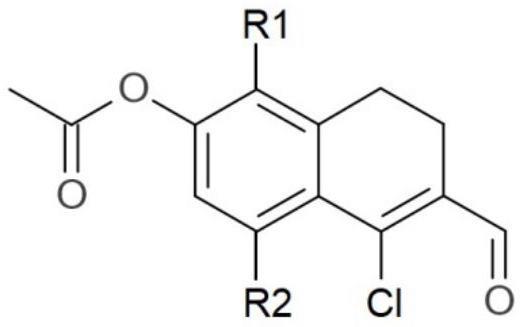
本发明涉及一种制备用于合成鞘氨醇-1-磷酸酯受体激动剂的主要中间体的方法。更具体地,本发明涉及一种能够在温和条件下用简单的工艺以高收率大规模生产下式5的中间化合物的新制备方法:[式5]其中,r1和r2各自独立地为氢、烷基、卤素、卤代烷基或烷氧基烷基。
背景技术:
1、鞘氨醇-1-磷酸酯(s1p)通过细胞内神经酰胺途径产生,其中神经酰胺为起始物质。神经酰胺通过两种途径产生,其中第一种途径为从头生物合成途径。神经酰胺还由细胞中的细胞膜成分鞘磷脂降解产生。各个组织中的s1p水平由两种生物合成鞘氨醇激酶(sphk)和两种生物可降解s1p磷酸酶(s1p溶解酶和溶血磷脂磷酸酶)控制。已知通过鞘氨醇激酶导致鞘氨醇磷酸化产生的s1p介导各种细胞应答,如细胞增殖、细胞骨架组织和迁移、粘附和紧密连接组装以及形态发生。s1p以与血浆蛋白(包括白蛋白)组合的形式以高水平(100-1000nm)存在于血浆中,而它以低水平存在于组织中。
2、s1p与g蛋白偶联受体s1p受体结合,以显示出各种生物功能。作为s1p受体亚型,迄今已知s1p1至s1p5,分别命名为内皮分化基因(edg)受体1、5、3、6和8。已知s1p受体参与多种生物功能,如白细胞再循环、神经细胞增殖、形态变化、迁移、内皮功能、血管调节和心血管发育。
3、近年来,许多研究已经发现通过这些受体的s1p信号传导过程在与多发性硬化相关的一系列反应(包括炎症反应和修复过程)中起重要作用,实际上已批准非选择性s1p1激动剂作为多发性硬化的治疗剂。s1p受体在许多与诱发多发性硬化相关的细胞中广泛表达。尤其,s1p1受体在免疫系统中起主要作用。s1p1受体主要表达于淋巴细胞如t细胞和b细胞的表面上并响应于s1p,从而参与淋巴细胞再循环。在正常条件下,体液中的s1p浓度高于淋巴组织,因此s1p浓度差异导致淋巴细胞离开淋巴组织,从而在输出淋巴循环后进行循环。然而,如果淋巴细胞中的s1p1受体被s1p1激动剂下调,就不会发生淋巴细胞从淋巴组织流出,从而减少自身侵袭性淋巴细胞的浸润,由此造成中枢神经系统(cns)的炎症和组织损伤。因此,获得对多发性硬化的治疗效果。已经批准非选择性s1p1激动剂芬戈莫德作为治疗多发性硬化的口服药物。出乎意料地,当它结合在欲激活的s1p1受体处时,所述受体被降解或从淋巴细胞表面内在化,因此它发挥功能性s1p1拮抗作用。
4、关于此类s1p受体,韩国专利申请公开第10-2014-0104376号公开了下式1的新化合物,所述化合物是有效的s1p受体激动剂:
5、[式1]
6、
7、其中,
8、x表示c或n,
9、r1表示h或任选取代的烷基,
10、r2表示h、任选取代的烷基、卤素、cn、cf3或cocf3,
11、w表示c、n、c-烷氧基、c-卤素或c-cn,
12、q表示ch2o或
13、s选自以下残基:
14、
15、其中
16、m和n独立地表示0、1、2或3,
17、r3至r10独立地表示h、烷基、卤素、卤代烷基或烷氧基烷基,
18、r11表示h、
19、r12表示oh、nh2、
20、在上述文献的一个具体示例中,公开了根据以下反应方案1的1-[1-氯-6-(3-氯-1-异丙基-1h-吲唑-5-基甲氧基)-3,4-二氢-萘-2-基甲基]-哌啶-4-甲酸的制备(反应方案1中的“sg35”是指“1-氯-6-羟基-3,4-二氢-萘-2-甲醛”)。
21、[反应方案1]
22、
23、在上述反应方案1中,制备1-氯-6-羟基-3,4-二氢-萘-2-甲醛的步骤可以如以下反应方案2所详述。
24、[反应方案2]
25、
26、首先,在0℃向6-甲氧基-3,4-二氢萘-1(2h)-酮溶解在甲苯中的溶液中滴加n,n-二甲基甲酰胺(dmf)和氧氯化磷(pocl3),然后在70℃搅拌6小时。将反应混合物倒入冰中并用乙酸乙酯萃取。有机层用盐水洗涤,干燥并浓缩,所得残余物通过硅胶柱色谱法(己烷:乙酸乙酯=20:1至10:1)纯化,得到1-氯-6-甲氧基-3,4-二氢-2-萘甲醛。
27、接下来,在0℃将氯化铝(alcl3)加入1-氯-6-甲氧基-3,4-二氢-2-萘甲醛在二氯甲烷中的溶液中,然后在50℃搅拌6小时。将反应混合物倒入冰中并用乙酸乙酯萃取。将有机层干燥并浓缩,所得残余物通过硅胶柱色谱法(己烷:四氢呋喃=5:1至3:1)纯化,得到1-氯-6-羟基-3,4-二氢-2-萘甲醛。
28、然而,在进行旨在获得1-氯-6-甲氧基-3,4-二氢-2-萘甲醛的维尔斯迈尔-哈克反应(vilsmeier-haack reaction)时,因在70℃的高温下反应而可能存在放热问题,并因总收率为80%而需要提高收率。此外,在旨在获得1-氯-6-羟基-3,4-二氢-2-萘甲醛的反应中,可能会因使用alcl3而存在反应器污染问题或因使用危险的试剂而存在安全问题。在使用alcl3时,可能因反应终止或副反应进展导致出现批处理失败而存在稳定性问题,并因总收率为70%而需要提高收率。
技术实现思路
1、技术问题
2、因此,本发明的技术问题是提供一种适合通过更简单的工艺以高收率大规模生产式5化合物的方法,所述式5化合物是合成优异的鞘氨醇-1-磷酸酯受体激动剂的关键中间体。
3、技术方案
4、为了解决上述技术问题,本发明提供了一种制备下式5的中间体化合物的方法,所述方法包括以下步骤:
5、i)通过使式2化合物与乙酰化剂和碱在有机溶剂中反应来制备式3化合物的步骤,
6、ii)通过式3化合物的维尔斯迈尔-哈克反应来制备式4化合物的步骤,以及
7、iii)通过从式4化合物除去乙酰基来制备式5化合物的步骤:
8、[式2]
9、
10、[式3]
11、
12、[式4]
13、
14、[式5]
15、
16、其中,
17、r1和r2各自独立地为氢、烷基、卤素、卤代烷基或烷氧基烷基。
18、下文详细描述了本发明。
19、根据本发明的一个实施方式,在上述式中,r1和r2各自独立地为氢、c1-c6烷基、卤素、卤代-c1-c6烷基或c1-c6烷氧基-c1-c6烷基。
20、根据本发明的另一个实施方式,在上述式中,r1和r2各自独立地为氢或c1-c4烷基。
21、在本发明的制备方法中,在步骤(i)中,通过使式2化合物与乙酰化剂和碱在有机溶剂中反应来制备式3化合物。
22、在根据本发明的另一个实施方式中,步骤(i)的有机溶剂可以是选自例如二氯甲烷(dcm)、二氯乙烷(dce)、甲苯、乙腈(acn)及其混合物的一种或多种。
23、在根据本发明的另一个实施方式中,步骤(i)的乙酰化剂可以是乙酰氯或乙酸酐。
24、在根据本发明的另一个实施方式中,步骤(i)的碱可以是选自三乙胺(tea)、n,n-二异丙基乙胺(dipea)、1,8-二氮杂双环(5.4.0)十一碳-7-烯(dbu)、氢氧化钠(naoh)、碳酸钾(k2co3)、碳酸钠(na2co3)及其混合物中的一种或多种。
25、在本发明的制备方法中,在步骤(ii)中,通过式3化合物的维尔斯迈尔-哈克反应来制备式4化合物。
26、在根据本发明的另一个实施方式中,步骤(ii)的维尔斯迈尔-哈克反应可以在30℃以下的温度下进行,更优选在20℃至25℃的温度下进行。
27、在本发明的制备方法中,在步骤(iii)中,通过从式4化合物除去乙酰基的脱保护来制备式5化合物。
28、在根据本发明的另一个实施方式中,除去乙酰基可以用例如k2co3来进行。
29、在根据本发明的另一个实施方式中,可以在室温下进行除去乙酰基的脱保护反应。
30、在根据本发明的另一个实施方式中,步骤(iii)制备的式5化合物可以直接结晶,例如通过滴加盐酸(hcl)而不进行如干燥或过滤等工艺。
31、本发明的效果
32、本发明的制备方法不使用会污染反应器的危险试剂如alcl3,并且不存在因反应终止或副反应进展而导致批处理失败的问题。因此,本发明的制备方法可以通过在保证安全性和稳定性的同时在室温下进行维尔斯迈尔-哈克反应和脱保护反应而在温和条件下以高收率大规模生产式5的中间体。
- 还没有人留言评论。精彩留言会获得点赞!