神经生长因子突变体的制作方法
神经生长因子突变体
1.本技术为申请号为201780017019.9、发明名称为“神经生长因子突变体”专利申请的分案申请。
技术领域
2.本发明涉及神经生长因子突变体,属于生物制药领域。
背景技术:
3.疼痛根据其神经生理学机制可分为感受性疼痛和神经病理性疼痛两类,前者直接由伤害性刺激引起,与组织损伤或炎症反应有关,又称炎症性疼痛;后者由躯体感觉神经系统的损伤或疾病直接造成的慢性疼痛。
4.神经生长因子(nerve growth factor,ngf)是意大利科学家levi-montlcini于1953年在小鼠肉瘤细胞内发现的第一个神经营养因子,ngf是一种具有神经元营养和促进突起生长双重生物学功能的一种神经细胞生长调节因子,它对中枢及周围神经元的发育、分化、生长、再生和功能特性的表达均具有重要的调控作用。ngf包含α、β、γ三个亚单位,β亚单位是活性区,由两条单链通过非共价键结合而成。levi-montalcini因为发现了ngf而获得了诺贝尔奖。目前,国内外已有多个ngf产品上市,临床上主要用于治疗神经系统发育不良,包括弱视、神经瘤、各种神经损伤及神经系统病变等疾病。
5.ngf存在于多种物种中,在雄性小鼠颌下腺、牛精浆、蛇毒、豚鼠前列腺和人胎盘组织中含量丰富。其中小鼠ngf与人ngf氨基酸序列同源性达到90%。考虑到鼠ngf应用于人体的种属差异性及小鼠作为原材料所具有的潜在的致病因子风险及人胎盘组织原材料的限制,发展基因工程技术制备重组人ngf(rhngf,recombinant human ngf)来取代提取的鼠ngf和人ngf具有很好的应用前景。
6.体内成熟的ngf以同源二聚体的形式存在,每条肽链包含120个氨基酸。人ngf基因位于1号染色体短臂上,完整的ngf外显子由241个氨基酸组成,通常称为prepro ngf前体,在内质网中prepro ngf前体的信号肽被切割下来,形成pro ngf前体(223个氨基酸),pro ngf前体在内质网中以同源二聚体形式存在,然后转移至高尔基体中,前体部分经furin酶切,形成成熟的ngf二聚体(单体含有120个氨基酸),被转运至细胞外,同时也有部分未经切割的pro ngf前体分泌至细胞外。
7.重组人源ngf虽然避免了一些潜在的致病风险,但在实际使用过程中仍然会存在很大问题:1)保持ngf生物活性,像其他蛋白质一样,ngf的生物活性依赖于其二级和三级结构,故在制备、纯化、存储及给药期间过程中保持其生物活性特别重要;2)ngf使用过程中会引起较严重的疼痛,部分病人无法耐受,故造成了使用上的部分受限。ngf参与了疼痛的病理生理过程,通过影响炎症介质的释放、离子通道的开放及促进神经纤维的生长导致疼痛,并通过调控离子通道及分子信号从而参与疼痛的发生发展。有学者推测ngf还可能通过促进致痛物质的表达导致疼痛,并在机体损伤后可改变神经元的出芽和再生。目前的研究发现:在人类中,不会引起痛觉过敏的最大剂量为0.03μg/kg(pettyet al.,1994
‑‑
29)。但是,
如此低的剂量限制了ngf的应用,同时也限制了其适应症的扩大,如用于中枢神经系统。
8.因此,为避免上述问题,需寻求一种可以减轻疼痛副作用甚至无痛的重组hngf,从而可加大使用剂量及受试人群,为扩大适应症以及应用于中枢神经系统提供了可能。
技术实现要素:
9.本发明的目的是提供一系列可以减轻疼痛副作用甚至无痛的神经生长因子突变体,即重组hngf。更优选地,提供一系列生物活性高且可以减轻疼痛副作用甚至无痛的神经生长因子突变体。为实现上述目的,本发明采用以下技术方案:
10.一种神经生长因子突变体,其特征在于,相对于亲本神经生长因子,所述突变体的突变位点包括:phe12glu、lys32gly、lys32leu、lys32tyr、arg59leu、arg59ala、asp65ala、asp65gly、lys74leu、lys88phe、lys88leu、lys88glu、lys88gly、gln96glu、arg114val、arg114phe、arg114gly、arg114leu、phe101ala或上述突变位点的任意组合;优选地,相对于亲本人神经生长因子;优选地,相对于亲本野生型人神经生长因子。
11.所述的神经生长因子突变体,为序列表seq id no:3至seq id no:21中任意一条所示的氨基酸序列。
12.编码所述的神经生长因子突变体的核苷酸序列。
13.所述的核苷酸序列,为序列表seq id no:22至seq id no:40所示的核苷酸序列。
14.本发明所述重组hngf突变体是在野生型hngf序列基础上进行单点突变得到的,其氨基酸序列及对应的编码核苷酸序列如下:
15.phe12glu:氨基酸序列为seq id no:3,编码核苷酸序列为seq id no:22;
16.lys32gly:氨基酸序列为seq id no:4,编码核苷酸序列为seq id no:23;
17.lys32leu:氨基酸序列为seq id no:5,编码核苷酸序列为seq id no:24;
18.lys32tyr:氨基酸序列为seq id no:6,编码核苷酸序列为seq id no:25;
19.arg59leu:氨基酸序列为seq id no:7,编码核苷酸序列为seq id no:26;
20.arg59ala:氨基酸序列为seq id no:8,编码核苷酸序列为seq id no:27;
21.asp65ala:氨基酸序列为seq id no:9,编码核苷酸序列为seq id no:28;
22.asp65gly:氨基酸序列为seq id no:10,编码核苷酸序列为seq id no:29;
23.lys74leu:氨基酸序列为seq id no:11,编码核苷酸序列为seq id no:30;
24.lys88phe:氨基酸序列为seq id no:12,编码核苷酸序列为seq id no:31;
25.lys88leu:氨基酸序列为seq id no:13,编码核苷酸序列为seq id no:32;
26.lys88glu:氨基酸序列为seq id no:14,编码核苷酸序列为seq id no:33;
27.lys88gly:氨基酸序列为seq id no:15,编码核苷酸序列为seq id no:34;
28.gln96glu:氨基酸序列为seq id no:16,编码核苷酸序列为seq id no:35;
29.arg114val:氨基酸序列为seq id no:17,编码核苷酸序列为seq id no:36;
30.arg114phe:氨基酸序列为seq id no:18,编码核苷酸序列为seq id no:37;
31.arg114gly:氨基酸序列为seq id no:19,编码核苷酸序列为seq id no:38;
32.arg114leu:氨基酸序列为seq id no:20,编码核苷酸序列为seq id no:39;
33.phe101ala:氨基酸序列为seq id no:21,编码核苷酸序列为seq id no:40。
34.一种长效化神经生长因子突变体,其中所述长效化神经生长因子突变体是由上述
任意所述的氨基酸序列得到的。
35.优选地,所述长效化神经生长因子突变体是通过化学修饰得到的,优选地所述长效化神经生长因子突变体为聚乙二醇和神经生长因子突变体的结合物。
36.优选地,所述长效化神经生长因子突变体是与其他蛋白融合得到的融合蛋白。优选地所述蛋白为人白蛋白,人白蛋白类似物,人白蛋白的片段,免疫球蛋白的fc部分,免疫球蛋白的fc部分的类似物,或免疫球蛋白的fc部分的片段。
37.优选地所述融合蛋白为神经生长因子突变体的c末端直接或通过肽接头与白蛋白或fc蛋白的n末端融合得到的。
38.一种表达载体,含有所述的核苷酸序列。
39.所述表达载体选自由dna载体和病毒载体所组成的组中。
40.所述dna载体选自由dna质粒载体、结合其的脂质体、结合其的分子耦联体和结合其的多聚物所组成的组中;优选地,所述dna质粒载体为真核细胞表达载体;所述病毒载体选自由腺相关病毒载体、慢病毒载体和腺病毒载体所组成的组中。
41.一种表达所述表达载体的方法,将所述的表达载体转染至宿主细胞,培养所得重组细胞表达得到神经生长因子突变体。
42.含有所述表达载体的宿主细胞。
43.所述的宿主细胞为哺乳动物细胞。
44.所述哺乳动物细胞为中国仓鼠卵巢细胞、人胚肾293细胞、cos细胞或hela细胞。
45.一种药物组合物,所述药物组合物含有药学上可接受的赋形剂,以及上述提及的神经生长因子突变体、上述提及的表达载体和上述提及的宿主细胞中的一种或几种。
46.本发明的药物可以制成注射剂、胶囊、片剂或粉剂等多种形式,上述各种剂型的药物均可以按照药学领域的常规方法制备。
47.所述药物组合物优选为注射液,所述注射液包括药学上可接受的赋形剂以及上述提及的神经生长因子突变体。
48.需要的时候,在上述药物组合物中还可以加入一种或多种药学上可接受的载体,所述载体包括药学领域常规的稀释剂、稳定剂、表面活性剂和防腐剂等。
49.所述的神经生长因子突变体用于制备治疗神经系统疾病的药物中的用途。所述神经系统疾病指与神经元退化或损伤相关的中枢和/或外周神经系统的疾病。神经系统疾病的具体例子包括但并不限于:alzheimer病、parkinson病、huntington舞蹈病、中风、als、外周神经病变和其他特征为神经元坏死或丧失的病症,无论是中枢的、外周的还是运动神经元(motorneuron),除了治疗因外伤、烧伤、肾衰竭或受伤造成的神经损伤之外。例如,与某些病症相关的外周神经病变如与糖尿病、aids或化疗相关的神经病变。
50.将神经生长因子突变体制备得到治疗神经系统疾病的药物可用于给病人施用。确切的使用剂量将取决于被治疗的疾病,而且可由该领域的技术人员用已知技术确定。另外,如本领域中所知,需要根据年龄、体重、一般健康状况、性别、饮食、施用时间、药物相互作用和疾病严重程度等情况加以调节,这可由该领域的技术人员通过常规试验而确定。此处提及的病人包括人和其他动物及生物体。因此,这些方法可用于人的治疗和兽用。
51.本发明的由神经生长因子突变体制备得到治疗神经系统疾病的药物的施用可用多种方法进行,其中包括但并不限于:口服、皮下、静脉、脑内、鼻内、透过皮肤、腹膜内、肌
内、肺内、阴道给药、直肠给药和眼内给药等。在某些情况下,比如在处理伤口时,可直接以溶液或喷雾形式施用。
52.本发明的药物组合物含有所述神经生长因子突变体,它处于适合给病人施用的形式。在优选例子中,药物组合物是水溶性形式,并且可以含有诸如载体、赋形剂、稳定剂、缓冲液、盐分、抗氧化剂、亲水聚合物、氨基酸、碳水化合物、离子或非离子表面活性剂、聚乙二醇或丙二醇等。所述神经生长因子突变体制备的药物也可以用本领域已知的技术以缓释形式植入,或者以微囊形式包埋。
53.所述的神经生长因子突变体用于制备有效减轻体重的药物中的用途。
54.所述的神经生长因子突变体用于制备长效化神经生长因子的用途。
55.本发明的优点在于:相对于现有技术中的野生型神经生长因子而言,可以减轻疼痛副作用甚至导致无痛,进一步地,部分神经生长因子突变体的生物活性会有明显提高。
56.以下结合附图和具体实施方式对本发明做进一步说明,并非对本发明的限定,凡依照本发明公开内容所进行的本领域等同替换,均属于本发明保护范围。
附图说明
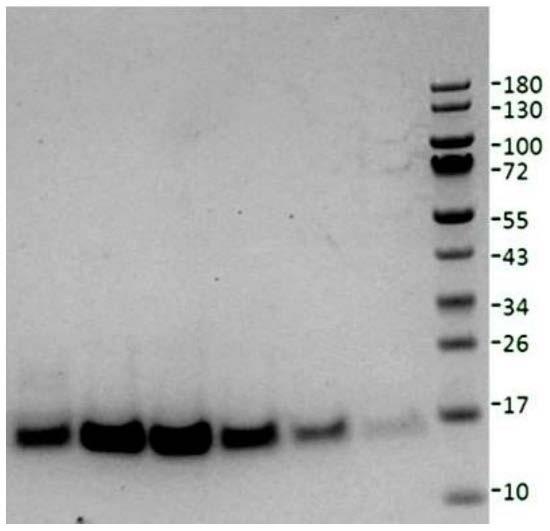
57.图1为实施例4 superdex75柱纯化的野生型hngf的sds page电泳结果
58.图2(a)和图2(b)为实施例5中突变体的活性测定结果
59.图3(a)和图3(b)为实施例7短期给药小鼠痛阈测定结果
60.图4(a)、图4(b)和图4(c)为实施例7长期给药小鼠痛阈测定结果
61.图5为实施例8小鼠行为学实验结果,分别注射突变体、野生型hngf,观测小鼠抬腿维持时间
具体实施方式
62.实施例1.野生型h ngf及其突变体的质粒构建
63.1、构建野生型hngf的dna序列表达质粒
64.合成野生型hngf的dna序列(序列表seq id no:1),使用引物(f:ggaattcatgtccatgttg(序列表seq id no:41),r:caagctttcaggctcttct(序列表seq id no:42))对目的序列进行pcr扩增,使用ecori(neb#r0101s)进行酶切后,将酶切产物使用hindiii(neb#r0104s)进行二次酶切。将pcdna3.1(-)表达载体使用同样的方法进行酶切。将酶切载体和pcr扩增目的片段进行琼脂糖凝胶电泳,切下目的片段,使用dna胶回收试剂盒(tiangen,#dp209-03)分别回收酶切后的载体和目的dna片段后,使用dna连接酶试剂盒(takara/6022)16℃连接1h,完成野生型hngf的质粒构建。
65.2、构建hngf突变体的dna序列表达质粒
66.同样上述方法,我们合成并构建了所有突变体的质粒。突变体的dna序列为序列表seq id no:22至seq id no:40所示的核苷酸序列。
67.实施例2、hngf及其突变体的质粒转化及提取
68.1、转化:
69.将上述实施例1构建好的hngf及其突变体质粒进行热激转化,将top10感受态细胞(天根/cb104-02)从-70℃冰箱取出后立即置于冰上解冻,取50ul用于转化。向其中加入2ul
质粒,轻弹混匀,冰浴30min。于42℃干浴90s,期间不要振荡离心管,取出后立即置于冰上2min。加入无抗lb/soc培养基500ul,150rpm/min,37℃摇床培养45min。将离心管内液体全部倒入lb平板上,均匀涂开。待平板晾干后,倒置于培养箱培养16h。
70.2、质粒大提
71.挑取上述2.1实验得到的单菌落接种于500ul lb液体培养基,37℃培养7h,同时菌液送检测序。将测序正确的菌液进行大量摇菌,将500ul菌液接种于500mllb培养基,37℃培养16h。4℃离心收集过夜培养的菌液,6000xg离心10分钟,充分弃去上清使用质粒大提试剂盒(购自qiagen,货号12163)大提质粒,测量浓度备用。
72.实施例3.野生型hngf及其突变体的表达
73.将上述实施例2大提得到的野生型hngf和及其突变体质粒转染293f细胞中,转染后第四日收集表达上清并定量。
74.实验步骤:
75.1、转染前一天,接种293f细胞,0.5
×
106/ml,共900ml,300ml/瓶。
76.2、转染当天计数,细胞密度约1.0
×
106/ml,活率99%以上。
77.3、转染:取36ml细胞培养基到125ml培养瓶;加360ug质粒,混匀;再加1080ug pei,混匀。室温静置15分钟;与细胞混匀,约12.3ml/瓶;37℃,8%co2,120rpm培养。
78.4、转染后第四日收集细胞上清,10000g离心20分钟。
79.5、收集上清,0.45um过滤,得到野生型hngf及其突变体的蛋白上清液。
80.6、sds-page检测,硝酸银染色定量。
81.实施例4.野生型hngf及其突变体的纯化
82.纯化上述实施例3中得到的ngf及其突变体的蛋白上清液。
83.1、阳离子交换层析:先使用乙酸和水调野生型hngf及其突变体的蛋白上清液至ph为4.0。cm sepharose ff层析柱用0.05mol/l乙酸盐缓冲液(ph4.0)充分平衡后上样,上样完成后,用平衡液冲洗至基线,用0.05mol/l tris-hc1(ph9.0)缓冲液洗脱杂峰至基线,再用0.05mol/ltris-hc1和0.05mol/l tris-hc1-0.4mol/l nacl(ph9.0)梯度洗脱,根据紫外吸收情况收集目标峰,在紫外检测仪上显示数字开始上升时开始收集,降为基线时停止收集目标蛋白峰。
84.2、疏水层析:butyl sepharose 4 ff层析柱经0.02mol/l磷酸盐(ph6.8)-1.5mol/l氯化钠缓冲液充分平衡。在步骤1收集的目标峰料液中加入氯化钠固体使料液中氯化钠的终浓度为1.5mol/l,待氯化钠充分溶解后上样,速度为120cm/h,上样完成后用平衡液冲洗至基线,然后用0.02mol/l磷酸盐(ph6.8)洗脱收集目标峰。
85.3、凝胶排阻层析:superdex 75 prep grade层析柱用ph6.8、0.05mol/l磷酸盐-0.15mol/l氯化钠缓冲液充分平衡后上样步骤/2中收集的目标峰,在紫外检测仪上显示数字从基线开始上升时开始收集,降为基线时停止收集目标蛋白峰。
86.superdex75柱纯化的野生型hngf的sds page如图1所示,说明制备得到的ngf纯度较高。将收集的野生型hngf及其突变体目标蛋白峰样品使用超滤管浓缩至0.4mg/ml,4℃保存用于后续实验。
87.实施例5.鸡胚法测定野生型hngf及其突变体活性
88.1、鸡胚背根神经节法测量野生型hngf及其突变体活性
89.将上述实施例4中得到的野生型hngf(氨基酸序列参见序列表)及其突变体(氨基酸序列参见序列表)样品进行稀释:a液:6ng提取的野生型hngf及其突变体样品加1ml无血清dmem培养液溶解;b液:取a液50μl加无血清dmem培养液4.95ml;c液:取b液60μl加无血清dmem培养液2.94ml(总量3ml)使终浓度为(3au/ml)。a、b液稀释在离心管中,c液在细胞瓶内,将c液作为1号瓶,再3倍梯度稀释为:2号、3号、4号、5号、6号待测液。每个待测液加入1个培养瓶,2ml/瓶。同时以无血清dmem培养液为空白对照,以购自中检院的标准品为阳性对照(参考品)。加入8日龄的鸡胚背根神经节后置于5%co2、37℃饱和湿度培养箱中,24小时后观察结果。
90.以生长最好时每毫升待测样品中ngf的含量作为1个活性单位(au)。从出现阴性对照结果的稀释度开始往回数第3和第4两个稀释度中取生长最好的作为判定终点计算效价。参考品为购自中检院的标准品,每支装量为1000au。
91.ngf比活的计算公式为:
92.待测样品的比活(au/mg)=参考品活性(au/ml)
×
[样品预稀释倍数
×
对应参考品稀释点处的活性(au/ml)/参考品实测活性(au/ml)]
[0093]
测活结果如图2(a)和图2(b)所示。结果表明,hngf突变体phe12glu,lys32leu,arg59leu,asp65ala,lys74leu,lys88leu,lys88gly,gln96glu,phe101ala,arg114leu,均保留了野生型的活性,甚至活性更高。
[0094]
实施例6.tf-1细胞法测定ngf及其突变体活性
[0095]
详细操作方法按照专利公开号为cn103376248a,专利名称为“神经生长因子活性定量测定方法”中实施例1中的方法进行操作,比活性检测结果见下表。
[0096]
表1
[0097]
样品名称细胞法比活(u/mg)野生型hngf43万lys74leu76.7万phe12glu62万lys88gly59万gln96glu43万
[0098]
实施例7.ngf及其突变体是否致痛(疼痛阈值)检测
[0099]
实验原理:筛选对痛觉反应正常的合格小鼠,注射一定剂量的ngf样品(野生型或其突变体),通过机械刺激测定小鼠曲爪反应疼痛阈值,进行统计分析,最终确定样品是否引起小鼠痛觉过敏。
[0100]
7-1、短期致痛情况观测
[0101]
一、实验材料
[0102]
动态足底触觉仪,意大利/ugo basile,型号37450。
[0103]
二、实验内容
[0104]
1、合格小鼠筛选
[0105]
订购spf级别cd-1小鼠,小鼠规格为雄性,体重30-35g。
[0106]
使用动态足底触觉仪[意大利/ugo basile,型号37450]筛选两足平均阈值在7.5-10之间且同一只小鼠左右脚阈值p值,p值》0.05的实验动物为合格小鼠。
[0107]
随机分组,分为实验组和空白对照组,实验组又按照不同样品及给药剂量分为小组,每组10只。
[0108]
2、ngf样品给药设计
[0109]
2.1野生型样品致痛剂量筛选
[0110]
药物配制:将阳性对照ngf野生型样品及各突变体样品均使用样品储备液(50mm pb,150mm nacl,ph6.8)进行稀释。
[0111]
空白对照:为ngf样品储备液。
[0112]
给药方式及剂量:小鼠左右脚足底皮下分别给药20ul;
[0113]
短期给药最低剂量为1.25μg/只,同时给予相应比较高的剂量以确定其致痛性,见图3(b)标注剂量。
[0114]
3、痛阈测
[0115]
在给药后分别在1个小时、2个小时进行机械阈值测定,并且记录数值,进行短期给药(2小时内)的观测。
[0116]
4、结果统计分析
[0117]
采用graphpad prism软件进行图表绘制及结果统计分析,比较各剂量组与对照组之间机械阈值是否有差异,分析野生型样品以及突变体样品的致痛性。
[0118]
由图3(a)可知,给药最低剂量为1.25μg/只时,对照组小鼠无疼痛表现,而野生型的阳性对照组,疼痛阈值在1h明显低于5以下,疼痛明显;而各突变体实验组疼痛阈值均在7左右,与阴性对照组比无明显差异,说明短期注射突变体基本无致痛性;
[0119]
由图3(b)可知,对照组与野生型的给药剂量为1.25μg/只,实验组给药剂量增加时,对照组小鼠无疼痛表现,而野生型的阳性对照组,疼痛阈值在1h明显低于5以下,疼痛明显;而各突变体实验组疼痛阈值均在7左右,与阴性对照组比无明显差异,说明加大给药剂量的情况下短期注射突变体也基本无致痛性。
[0120]
7-2长期致痛情况观测
[0121]
随机选择上述突变体中的三个1号(phe12glu)、2号(lys88gly、3号(arg114leu)进行长期致痛试验,除设定本次实验的3个给药剂量为:0.2μg/只、0.5μg/只、1.25μg/只,每天给药一次,连续3周,期间不间断的进行疼痛阈值的测定外,其余均按照7-1“短期致痛情况观测”中的方法进行。
[0122]
结果如图4(a)、4(b)和4(c)所示,表明:突变体phe12glu在14天内痛阈未明显降低,未见导致疼痛,14天后仅出现中剂量(0.5ug/只)短暂的疼痛;突变体lys88gly、突变体arg114leu在试验过程中均未出现明显的痛阈改变;而野生型ngf在17天以内三个剂量显示痛阈逐渐降低,逐渐出现疼痛感。可见,本发明的突变体较野生型具有显著的降低疼痛的优点。
[0123]
实施例8.野生型hngf及其突变体是否致痛的行为学检测
[0124]
野生型hngf及其突变体样品对小鼠关节给药,通过行为学观察小鼠抬腿时间以及次数来考察样品是否致痛。
[0125]
实验内容
[0126]
1、小鼠订购
[0127]
订购spf级别cd-1小鼠,小鼠规格为雄性,体重30-35g。随机分组,分为实验组、空
白对照组(简称对照组)及阳性对照组,各组根据剂量又分为七个小组,每个小组随机挑选6只。
[0128]
2、给药剂量与时间
[0129]
2.1给药剂量
[0130]
阳性对照:采用样品储备液(50mm pb,150mm nacl,ph6.8)稀释野生型hngf为1.25μg/10ul组;
[0131]
实验组:突变体药物配制方法同阳性对照,稀释突变体phe12glu、lys88gly及arg114leu为1.25μg/10ul组及0.5μg/10ul;
[0132]
空白对照:生理盐水。
[0133]
2.2给药方式
[0134]
在小鼠后腿关节内注射药品,每个关节腔给药10ul。
[0135]
2.3给药时间:
[0136]
每剂量组进行单次连续3-4天给药。即第一天上午10点,以及之后第2、3、4天相同时间点给药。
[0137]
3、行为学观察
[0138]
各实验组以及对照组当天给药后2、4小时进行观察,以及给药的第2、3、4天相同时间点进行观察。
[0139]
观察指标:2分钟内小鼠自发性抬腿的次数以及每次抬腿维持的时间(秒),计算抬腿维持累计时间。
[0140]
4、结果统计分析
[0141]
采用graphpad prism软件双因素方差分析抬腿维持时间,比较分析不同样品是否致痛。
[0142]
实验结果如图5所示:野生型hngf组在注射药物后的各检测时间点均能引起明显的疼痛,突变体各剂量组连续给药均没有抬腿行为或者疼痛异常现象,可确定不引起疼痛,卡方分析得知在各检测时间点阳性对照组与实验组均有明显差异。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1