一种用于异种移植供体猪多重病毒实时荧光检测的特异性引物、探针和试剂盒的制作方法
1.本发明属于核酸检测领域,本发明提供一种用于异种移植供体猪多重病毒的实时荧光检测方法,能够同时筛查供体猪内源性反转录病毒(perv),猪流感病毒(si)以及猪戊肝病毒(phev)rna的方法。
技术背景
2.目前器官移植面临的最大问题就是供体短缺,猪源性异种移植为大多数脏器功能衰竭又缺乏供体器官而死亡的患者提供了希望。然而随着猪供体器官移植到人体的同时,某些猪源病毒也有可能传染给人类并致病,猪巨细胞病毒(pcmv) 和猪淋巴性疱疹病毒(plhv)在很大程度是种特异性的,通常不会感染人细胞。猪adv和pcv2通常不会引起很严重的疾病,还没有传播到人类的报道。猪内源性逆转录病毒(porcine endogenous retrovirus,perv)已整合到猪的基因组中,它们会产生能够感染人类细胞的病毒颗粒,导致免疫缺陷和肿瘤,因此对异种移植构成特殊风险。猪流感是一种由甲型猪流感病毒(swine influenza a,si) 引起的猪呼吸系统疾病。中国卫生部门将原人感染猪流感称为甲型h1n1流感,猪戊肝病毒(porcine hepatitis e virus phev)在猪身体内不会引起明显的疾病,却是经粪-口途径传播的人兽共患病原体,临床上超过50%的急性肝炎病人为 hev所致。hev可以跨种间感染与传播,给人类健康和畜牧业生产造成巨大危害,并构成潜在的公共卫生问题。
3.perv有三种亚型,perv-a,perv-b和perv-c。perv-a和perv-b存在于所有猪基因组,在体外能感染人类;perv-c只存在部分猪基因组且只能感染猪。但是perv-a/c的重组型在人类细胞培养中有很强的感染性。因此perv的筛查检测应该涵盖三种病毒亚型。我们选择三型perv均高度保守的perv-gag基因 1332-1430区段设计通用型引物和特异性探针。
4.甲型猪流感病毒(si)分为三个亚型:h1n1,h1n2,h3n2,目前只有h1n1亚型可以感染多种动物,包括许多禽类和哺乳动物,具备了在人群中大流行的基本特征。我们设计能够检测甲型h1n1猪流感的引物和探针。
5.phev分为4个基因型,其中基因ⅰ型和ⅱ型仅感染人类;基因ⅲ型和ⅳ型为人畜共患病,其中猪为主要宿主,我们设计了能够筛查所有hev的通用型引物。
6.perv,si,phev均为rna病毒。本发明提供同时筛查供体猪内源性反转录病毒(perv),猪流感病毒(si)以及猪戊肝病毒(phev)的实时荧光pcr检测方法。
技术实现要素:
7.猪是目前公认的异种细胞、组织或器官移植研究的最佳供体,它具有与人类高度相似的基因组,且容易进行基因编辑和体外克隆。目前猪源性异种移植在全世界正处于临床前试验研究阶段。2020年1月2日《科学》杂志预测异种器官移植临床试验可能成为2020年度十大头条科学新闻。由于免疫抑制剂的大量使用,避免感染是决定移植手术成败和器官
移植后病人生存质量的关键因素。移植前筛选和鉴定健康供体猪和器官,对于降低移植后内源性病毒感染的风险十分重要。因此及早建立一个能快速检测异种器官移植多种病毒的方法对于器官供体猪和受体病人都有重要意义。实时荧光pcr技术是近年来发展迅速的一种核酸检测技术,通过检测与靶序列互补的特异探针荧光信号的动态变化以扩增曲线方式实时反映pcr的每个循环的扩增水平。
8.为实现上述目的,本发明的技术方案采用roche magnapure核酸试剂盒提取外周血或者呼吸道样本中的总核酸rna,使用一步法实时荧光逆转录-聚合酶链反应(real time rt-pcr)同时检测样本中perv,si,hev的rna数量。
9.本发明提供一种用于异种移植供体猪多重病毒实时荧光检测的特异性引物、探针,其特征在于,通过对已报导perv,si,hev的核酸序列进行比对分析,分别以perv-gag基因1332-1430区段(三型perv-abc均高度保守),si-ha基因, hev-orf3基因为扩增靶位点,选择无二级结构且高度保守的区段,根据引物探针设计的基本原则,利用引物分析软件和人工判断,并经多次实验优化后确定适合实时荧光定量real time-pcr(rt-pcr或qpcr)的多对引物和探针。
10.在本发明的一种实施方式中,
11.所述perv病毒正反向引物及探针序列分别是:
12.正向引物:5'-tgatcaggatgagagccgg-3',
13.反向引物:5'-ttaaaccatggctaataaaccaaga-3',
14.probe:5'-fam-tgccaaatcttgccacgtaaggatataggg bhq-3',
15.所述si病毒正反向引物及探针序列分别是:
16.正向引物:5'-gggaatatctcaaacctttcaaatg-3',
17.反向引物:5'-acaaaggtgtaacggcagcat-3',
18.probe:5'-fam-cgagtcatgattgggccatgaacttgt-3',
19.所述phev病毒正反向引物及探针序列分别是:
20.正向引物:5'-gtcaccccagaaaccacc-3',
21.反向引物:5'-ttcatccaaccaacccct-3',
22.probe:5'-fam-gcgaagggctgagaatca-bhq1-3',
23.上述三对荧光探针分别在5'端标记有荧光报告基团,3'端标记有荧光淬灭基团。
24.在本发明的一种实施方式中,所述荧光报告基团为fam;所述荧光淬灭基团为bhq。也可以根据特殊的荧光报告基团选择相对应的荧光淬灭基团进行不同方式的多种组合以适应众多厂家多通道荧光pcr仪器的不同需求。如荧光报告基团可以选择fam、vic、cy3、rox、cy5、tet、hex、joe等;淬灭基团选择与荧光基团相对应的淬灭基团如bhq系列、tamra、dabcyl等。
25.本发明第二目的在于提供一种用于异种移植供体猪多重病毒实时荧光检测的特异性试剂盒,试剂盒包括perv,si,hev反应混合液、rna人工内标(biolinebio38041)、阳性质控品、阴性质控品,所述反应混合液含有内标探针和如权利要求1至3任一所述的荧光rt-pcr引物和荧光探针。
26.在本发明的一种实施方式中,所述perv反应混合液由与perv-abc型靶多核苷酸的结合的正向引物,反向引物,和能够与靶多核苷酸结合并且两末端分别结合有荧光报告基
团(fam)和荧光淬灭基团的寡核苷酸探针组成,另外还有rt-pcr反应需要的逆转录混合液及人工内标扩增反应(特异探针报告基团为cy5)混合液,而si和hev混合液分别由与si和hev靶多核苷酸的结合的正向引物,反向引物,和能够与靶多核苷酸结合并且两末端分别结合有荧光报告基团(均为fam)和荧光淬灭基团的寡核苷酸探针组成,另外还有rt-pcr反应需要的逆转录混合液。
27.在本发明的一种实施方式中,其中阴性质控品为去离子水,阳性质控品为含有病毒特异序列的合成dna。
28.本发明还提供了一种用于异种移植供体猪多重病毒实时荧光检测的方法,试剂组成如下:
29.1)perv——abc型和人工内标反应混合液(50ul/管)1管
30.2)si反应混合液1管;
31.3)hev反应混合液1管;
32.4)阴性质控品(200ul/管)1管;
33.5)阳性质控品(perv,si,hev)各1管;
34.6)rna人工内标(biolinebio38041)1管:
35.所述rna人工内标不会干扰靶序列扩增的人工合成的内标,在核酸提取开始前加入每个标本和阴性质控中,完成与模板同时提取和一起扩增的每个步骤,监控样本提取和扩增中出现的任何抑制因子,确保反应过程的有效性。
36.其中1)反应混合液由与pervabc型靶多核苷酸的结合的正向引物,反向引物,和能够与靶多核苷酸结合并且两末端分别结合有荧光报告基团(fam)和荧光淬灭基团的寡核苷酸探针组成,另外还有rt-pcr反应需要的逆转录混合液及人工内标扩增反应(特异探针报告基团为cy5)混合液,2)和3)混合液分别由与si和hev靶多核苷酸的结合的正向引物,反向引物,和能够与靶多核苷酸结合并且两末端分别结合有荧光报告基团(均为fam)和荧光淬灭基团的寡核苷酸探针组成,另外还有rt-pcr反应需要的逆转录混合液。
37.其中阴性质控品为去离子水,阳性质控品为含有病毒特异序列的合成dna。
38.在本发明的一种实施方式中,包括以下步骤:
39.(l)rna提取:使用magnapurelc和罗氏magna核酸提取纯化试剂盒(rochecatn);05323738001),在推荐的操作程序下,可提取高纯度的rna。rna内部提取参照(iec:biolinebio38041)提取前加入标本中作为质量监控;
40.(2)rt-pcr反应:
41.按表1配方做反应混合液:
42.表1.反应混合液配方
43.反应混合物(ul)perv+人工内标sihev混和液151515rna模板101010总计252525
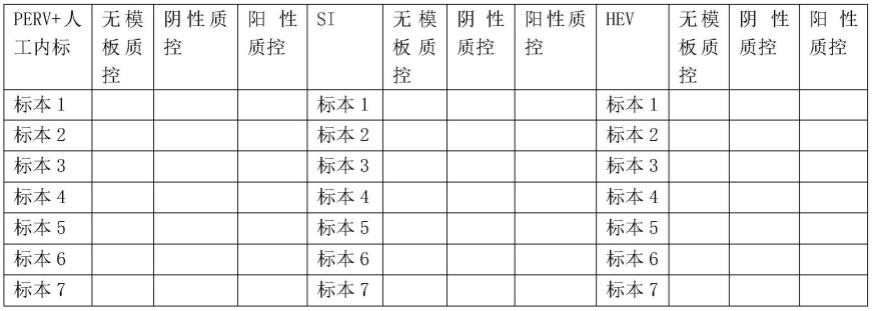
44.按表2方式安排96孔扩增板:
45.表2.96孔扩增板
[0046][0047]
(3)结果分析
[0048]
反应结束后保存检测数据文件。根据pcr扩增结果所得到的曲线,分析实验结果。
[0049]
(4)有效结果判断:
[0050]
1无模板质控没有靶基因和内标扩增信号
[0051]
2阴性质控没有靶基因扩增信号。
[0052]
3阳性质控有靶基因扩增信号(465-510)。
[0053]
4所有标本都有与阴性质控不超过2个ct(cycle of threshold)值的人工内标扩增信号(618-660)。超过2个ct,提示标本可能有在提取或者扩增环节有抑制因素影响,需要对原标本重复试验。
[0054]
本发明可以实现同时检测样本中perv,si,hev病毒的rna定量,与现有技术相比,本发明具有如下优点:
[0055]
1、将rna逆转录、dna扩增与检测三过程融合为一体,可以实时、动态快速监测rna,极大缩短了结果分析时间。2、采取一种封闭的检测模式,减少指数扩增后污染可能。3、荧光探针的使用,提高了检测靶多核苷酸的特异性。4、可以同时检测呼吸道样本、血清、肺组织等样品中的perv,甲型si和phev。5、为器官移植供体猪快速筛查提供高灵敏、高通量、实时定量的早期诊断证据,减少漏检、假阴性或假阳性结果,改善因感染导致的器官功能丧失,提高患者的生存质量和术后生存率。6、适合各种厂家生产或个人常用的核酸提取纯化试剂盒提取高纯度的全核酸;可根据众多厂家多通道荧光pcr仪器的不同需求选择特殊的荧光报告基团和与之相对应的荧光淬灭基团进行不同方式的多种组合;可以选用其他常用或个人不同喜好的内参照。
附图说明
[0056]
为了更清楚地说明本技术实施例的技术方案,下面将对本技术实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本技术的某些实施例,因此不应被看作是对范围的限定。
[0057]
图1为本技术实施例提供的显示灵敏度的检测结果的示意图;
[0058]
图2为本技术实施例提供的人工内标没有抑制的曲线的示意图。
具体实施方式
[0059]
实施例1敏感性:
[0060]
病毒检测试剂盒灵敏度实验
[0061]
显示灵敏度的检测结果。分别检测浓度为2500copies/ul、250copies/ul、25copies,2.5copies/ul的4份阳性质控品,浓度为2.5copies/ul的样本扩增曲线平直且与基线无交叉,没有ct值,可明确判定为阴性。阳性质控品样本阳性扩增曲线有明显指数增长
期,成s型,均明确判定为阳性。
[0062]
实施例2特异性
[0063]
本发明针对设计特异性引物和探针,可分别检测出perv,si,phev,没有交叉反应,说明本试剂盒具有良好的特异性。
[0064]
实施例3反应体系的建立与优化
[0065]
经多次重复试验确定反应条件:50℃逆转录10min,l个循环;94℃10min, 1个循环;最后94℃15s,55℃45s,45个循环。
[0066]
实施例4检测方法步骤
[0067]
根据国内外相关文献报道表明可检测的标本包括:血清(适用于perv,hev),外周全血(perv),呼吸道拭子样本和肺组织样品(适用于si)等。标本可立即用于测试,也可以保存于-70℃待测,保存期为6个月。
[0068]
(l)rna提取:使用magna pure lc和罗氏magna核酸提取纯化试剂盒(rochecat n);05323738001),或者其他公司生产的核酸提取试剂盒,或个人常用的核酸提取纯化方法,在推荐的操作程序下,可提取高纯度的rna。rna内部提取参照(iec:bioline bio38041)提取前加入标本中作为质量监控。
[0069]
(2)rt-pcr反应:
[0070]
按以下配方做反应混合液:
[0071]
反应混合物(ul)perv+人工内标sihev混和液151515rna模板101010总计252525
[0072] 按以下方式安排96孔扩增板:
[0073][0074]
(3)结果分析
[0075]
反应结束后保存检测数据文件。根据pcr扩增结果所得到的曲线,分析实验结果。
[0076]
有效结果判断:
[0077]
1无模板质控没有靶基因和内标扩增信号
[0078]
2阴性质控没有靶基因扩增信号。
[0079]
3阳性质控有靶基因扩增信号(465-510)。
[0080]
4所有标本都有与阴性质控不超过2个ct(cycle of threshold)值的人工内标扩
增信号(618-660)。超过2个ct,提示标本可能有在提取或者扩增环节有抑制因素影响,需要对原标本重复试验。
[0081]
实施例5人工内标没有抑制的曲线。
[0082]
e1-5为标本人工内标扩增曲线,相差小于2个ct值。
[0083]
没有模板的对照(ntc)没有人工内标扩增曲线。
[0084]
同理适用于其他rnasn p、gapdh、b2m、18srna、、tbp、β-actin、hprt 等管家基因的内参照。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1