磷酸二酯酶抑制剂的制备方法与流程
1.本发明属于医药技术领域,具体涉及磷酸二酯酶抑制剂的制备方法及制备中间体。
背景技术:
2.磷酸二酯酶9(phosphodiesterase 9)是pde家族中的重要一员,对cgmp具有非常高的选择性,其抑制剂用于治疗由于中枢神经系统紊乱导致的认知损害方面的疾病,比如老年痴呆症和精神分裂症、大脑的神经变性过程疾病。
3.6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈(即,wo2019062733a1的实施例71中的化合物107)是pde9的抑制剂。
4.wo2019062733a1的实施例71公开了下述制备方法,其包括以下步骤:
[0005][0006]
在1,7-二氮杂萘环的4和6位引入取代基时,需要进行偶联反应和亲核取代反应,
反应流程长,总收率低。在化合物107的制备过程中,需要使用中间体4,6-二氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈(结构如下)作为合成起点。
[0007][0008]
wo2019062733a1的制备例2公开了中间体4,6-二氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的制备方法,
[0009][0010]
其中需要使用15ml的三氯氧磷(密度为1.64g/cm3,分子量为153.33g/mol,即,24.6g,0.16mol,相当于7当量,而得到约0.7当量的目标产物。也就是说,为得到1当量的6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈,wo2019062733a1所公开的方法需要使用约30当量的三氯氧磷。
[0011]
wo2020182076a1公开了相同的制备中间体4,6-二氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的方法(第28页,制备例1,步骤3)。
[0012]
wo2020182076a1还公开了6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的制备方法(第29页,制备例2,步骤3)。根据该方法,制备1当量的6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈,需要使用5.13当量的三氯氧磷,而且还需要使用色谱分离方法。
[0013]
三氯氧磷毒性大,易爆炸,并且容易造成环境污染问题。因此希望在合成过程中尽量少使用三氯氧磷。在实际制药过程中,还希望工艺流程短,尽量避免提纯操作,以期提高收率。因此在后续对于合成放大的研究过程中,仍需要对合成工艺进行改进,期望能够更大程度的降低生产成本、减少三废产量,提高工艺安全系数。
技术实现要素:
[0014]
本发明的目的是,提供式(i)化合物的制备方法及制备中间体,和更进一步地,提供式(i')化合物的制备方法及制备中间体。
[0015]
本发明提供式(i)化合物的制备方法,其通过如下步骤制备:
[0016][0017]
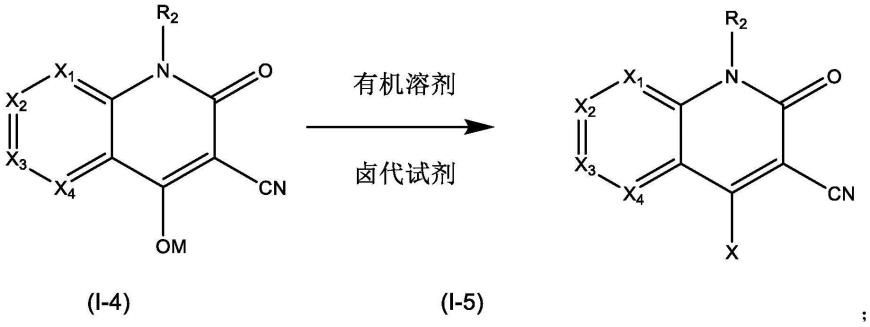
步骤(c'):于有机溶剂中,(i-4)与卤代试剂发生卤代反应得到(i-5):
[0018][0019]
步骤(d'):于有机溶剂中,(i-5)与(i-6)和碱发生亲核取代反应得(i'):
[0020][0021]
其中,x为卤素原子;m为碱金属离子;
[0022]
x1为ch,x2为n,x3为cr3,x4为ch;
[0023]
r3选自氢、氨基、氰基、卤素、羧基、c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、吗啉基、c
2-6
烯基、c
1-4
烷羰基、c
1-4
烷氨羰基、(c
1-6
烷基)2氨羰基、c
1-4
烷基磺酰基、c
1-4
烷基硫基、氨基羰基、环丙基、氮杂环丁烷基和哌嗪基,
[0024]
a)其中所述c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、c
2-6
烯基、c
1-4
烷羰基、c
1-4
烷氨羰基、(c
1-6
烷基)2氨羰基、c
1-4
烷基磺酰基、c
1-4
烷基硫基、氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、氨基、卤素、c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、环丙基、c
1-4
烷羰氧基、和
未被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代,
[0025]
b)其中所述环丙基、氮杂环丁烷基、吗啉基和哌嗪基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、卤素、c
1-4
烷基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、和c
1-4
烷羰氧基的基团取代;
[0026]
优选地,r3选自氢、卤素、c
1-4
烷基、c
1-4
烷氧基、吗啉基、c
2-6
烯基、c
1-4
烷氨羰基、(c
1-4
烷基)2氨羰基、和氨基羰基,
[0027]
a)其中所述c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基、(c
1-4
烷基)2氨羰基、和氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、和未被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代,
[0028]
b)其中所述吗啉基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基的基团取代;
[0029]
更优选地,r3选自氢、卤素、c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基、和氨基羰基,
[0030]
其中所述c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基、和氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、和未被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代;
[0031]
l为键;
[0032]
环a为4-7元单杂环基或7-12元螺杂环基,所述4-7元单杂环基的杂原子选自n,7-12元螺杂环基的杂原子选自o、n中的一种或两种的组合,且7-12元螺杂环基至少含有一个n,环a通过n原子与l相连接;
[0033]
优选地,环a为4-7元单杂环基,所述4-7元单杂环基的杂原子选自n,环a通过n原子与l相连接;
[0034]
更优选地,环a选自
[0035]
特别更优选地,环a为
[0036]
每个r1分别独立地选自氢、羟基、氰基、卤素、c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基,基中所述c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基未被取代或被羟基取代;
[0037]
优选地,每个r1分别独立地选自氢、c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基,其中所述c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基未被取代或被羟基取代;
[0038]
m为0、1或2;
[0039]
r2选自氢。
[0040]
本发明提供式(i')化合物的制备方法,其通过如下步骤制备:
[0041][0042]
步骤(c):于有机溶剂中,(i'-4)与卤代试剂发生卤代反应得到(i'-5):
[0043][0044]
步骤(d):于有机溶剂中,(i'-5)与(i'-6)和碱发生亲核取代反应得(i'):
[0045][0046]
其中,r1为c
1-6
烷基;
[0047]
x为卤素原子;
[0048]
m为碱金属离子。
[0049]
在本发明的一种实施方式中,(i')化合物的制备方法,其通过如下步骤制备:
[0050]
步骤(c):于有机溶剂中,(i'-4)与卤代试剂发生卤代反应得到(i'-5):
[0051][0052]
步骤(d):于有机溶剂中,(i'-5)与(i'-6)和碱发生亲核取代反应得(i'):
[0053]
[0054]
其中,r1为c
1-6
烷基;
[0055]
x为卤素原子;
[0056]
m为k
+
、na
+
、li
+
、cs
+
。
[0057]
在本发明的一种实施方式中,式(i')化合物的制备方法,还包括步骤(b),
[0058]
于有机溶剂中,(i'-3)与碱发生缩合反应得到(i'-4):
[0059][0060]
r1为c
1-6
烷基;优选甲基、乙基;
[0061]
r2为c
1-6
烷基;优选甲基、乙基;
[0062]
m为k
+
、na
+
、li
+
、cs
+
,优选k
+
、na
+
。
[0063]
在本发明的一种实施方式中,式(i')化合物的制备方法,还包括步骤(a),
[0064]
于有机溶剂中,式(i'-1)、(i'-2)和偶联试剂发生缩合反应得到(i'-3):
[0065][0066]
r1为c
1-6
烷基;优选甲基、乙基;
[0067]
r2为c
1-6
烷基;优选甲基、乙基。
[0068]
在本发明的一种实施方式中,
[0069]
步骤(a)所述的偶联试剂是1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、2-(7-氧化苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐、二环己基碳二亚胺中的一种或几种;
[0070]
步骤(b)所述的碱是氢氧化钾、氢氧化钠、甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾、甲醇钾中的一种或几种;
[0071]
步骤(c')和步骤(c)所述的卤代试剂是三氯氧磷、氯化亚砜、磺酰氯、三氯化膦、五氯化膦、三溴化磷、三溴氧磷、三光气、草酰氯中的一种或几种;
[0072]
步骤(d')和步骤(d)所述的碱是三乙胺、n,n-二异丙基乙胺、甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾中的一种或几种。
[0073]
在本发明的一种实施方式中,
[0074]
步骤(d')和步骤(d)所述的碱是三乙胺。
[0075]
在本发明的一种实施方式中,
[0076]
步骤(a)所述的有机溶剂是二氯甲烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、四氢呋喃中的一种或几种;优选为二氯甲烷;
[0077]
步骤(b)所述的有机溶剂是乙醇、四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、
n,n-二甲基乙酰胺中的一种或几种;优选为四氢呋喃;
[0078]
步骤(c')和步骤(c)所述的有机溶剂是乙腈、四氢呋喃、2-甲基四氢呋喃、氯仿、1,2-二氯乙烷中的一种或几种;优选为乙腈;
[0079]
步骤(d')和步骤(d)所述的有机溶剂是乙醇、四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺中的一种或几种;优选为乙醇。
[0080]
在本发明的一种实施方式中,
[0081]
步骤(a)所述的偶联试剂为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐;
[0082]
步骤(b)所述的碱是甲醇钾和乙醇钠中的一种或几种;
[0083]
步骤(c')和步骤(c)所述的卤代试剂为三氯氧磷;
[0084]
步骤(d')和步骤(d)所述的碱为三乙胺或n,n-二异丙基乙胺。
[0085]
在本发明的一种实施方式中,
[0086]
步骤(a)中,有机溶剂的用量为式(i'-1)的2-20倍体积,优选5-12倍体积;
[0087]
步骤(b)中,有机溶剂的用量为式(i'-3)的2-20倍体积,优选3-12倍体积;
[0088]
步骤(c')中,有机溶剂的用量为式(i-4)的2-20倍体积,优选4-10倍体积;
[0089]
步骤(c)中,有机溶剂的用量为式(i'-4)的2-20倍体积,优选4-10倍体积;
[0090]
步骤(d')中,有机溶剂的用量为式(i-5)的2-20倍体积,优选10-20倍体积。
[0091]
步骤(d)中,有机溶剂的用量为式(i'-5)的2-20倍体积,优选10-20倍体积。
[0092]
在本发明的一种实施方式中,
[0093]
所述步骤(a)的(i'-1)、(i'-2)和偶联试剂的摩尔比为1:(0.5-2):(1-2);
[0094]
所述步骤(b)的(i'-3)和碱的摩尔比为1:(1-5);
[0095]
所述步骤(c')的(i-4)和卤代试剂的摩尔比为1:(1-5);
[0096]
所述步骤(c)的(i'-4)和卤代试剂的摩尔比为1:(1-5);
[0097]
所述步骤(d')的(i-5)、(i-6)和碱的摩尔比为1:(0.5-2):(1-3);
[0098]
所述步骤(d)的(i'-5)、(i'-6)和碱的摩尔比为1:(0.5-2):(1-3)。
[0099]
在本发明的一种实施方式中,
[0100]
所述步骤(c')的(i-4)和卤代试剂的摩尔比为1:(1-3);
[0101]
所述步骤(c)的(i'-4)和卤代试剂的摩尔比为1:(1-3)。
[0102]
在本发明的一种实施方式中,
[0103]
所述步骤(c')的(i-4)和卤代试剂的摩尔比为1:1、1:1.1、1:1.2、1:1.5或1:2.3;
[0104]
所述步骤(c)的(i'-4)和卤代试剂的摩尔比为1:1、1:1.1、1:1.2、1:1.5或1:2.3。
[0105]
本发明还提供式(i')化合物的制备中间体,具有以下结构式:
[0106][0107]
r1为c
1-6
烷基;优选甲基、乙基;
[0108]
m为k
+
、na
+
、li
+
、cs
+
。
[0109]
在本发明的一种实施方式中,所述的制备中间体,其结构如下:
[0110][0111]
本发明还提供式(i')化合物的制备中间体可用于治疗或者预防由pde9介导的相关疾病的药物的合成。
具体实施方式
[0112]
本发明所述的“c
1-6
烷基”指含有1-6个碳原子的烃部分去除一个氢原子衍生的直链或支链的烷基,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、2-甲基丁基、新戊基、1-乙基丙基、正己基、异己基、4-甲基戊基、3-甲基戊基、2-甲基戊基、1-甲基戊基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、1,2-二甲基丁基、1,3-二甲基丁基、2,3-二甲基丁基、2-乙基丁基和1-甲基-2-甲基丙基等。所述“c
1-4
烷基”指含有1-4个碳原子的上述实例。
[0113]
本发明所述的“c
1-4
烷氧基”是指前文所定义的“c
1-4
烷基”通过氧原子与母体分子连接的基团,即“c
1-4
烷基-o
‑”
基团,如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基和叔丁氧基等。
[0114]
发明所述的“c
1-4
烷基氨基”、“(c
1-4
烷基)2氨基”、“(c
1-4
烷基)2氨羰基”、“c
1-4
烷基磺酰基”、“c
1-4
烷基硫基”分别指c
1-4
烷基-nh-、(c
1-4
烷基)(c
1-4
烷基)n-、(c
1-4
烷基)(c
1-4
烷基)n-c(o)-、c
1-4
烷基-s(o)
2-、c
1-4
烷基-s-。
[0115]
本发明所述的“4-6元杂环基”是指4-6元的至少一个环碳原子被选自o、s、n的杂原子替代的非芳香性的环状基团,优选1-3个杂原子,同时包括碳原子、氮原子和硫原子可以被氧代。
[0116]
本发明所述的“卤素”是指氟、氯、溴、碘等。
[0117]
本发明所述的“碱”,包括有机碱和无机碱。其中,有机碱包括但不限制于叔丁醇钠、叔丁醇钾、lihmds、甲醇钠、乙醇钠、甲醇钾。无机碱包括但不限制于氢氧化钾、氢氧化钠、氢氧化镁、氢氧化铷。
[0118]
本发明所述的“碱金属”,指在元素周期表中ⅰa族除氢(h)外的六个金属元素,即锂(li)、钠(na)、钾(k)、铷(rb)、铯(cs)、钫(fr)。
[0119]
本发明所述的“倍体积”是指溶解1g物质所需要的溶剂的体积(ml),例如,溶解1g式(i'-1)化合物所需要的溶剂为10ml,则称为10倍体积。
[0120]
特别地,本发明提供下列技术方案:
[0121]
技术方案1.式(i)化合物的制备方法,其特征在于,其通过如下步骤制备:
[0122][0123]
步骤(c'):于有机溶剂中,(i-4)与卤代试剂发生卤代反应得到(i-5):
[0124][0125]
步骤(d'):于有机溶剂中,(i-5)与(i-6)和碱发生亲核取代反应得(i):
[0126][0127]
其中,x为卤素原子;m为碱金属离子;
[0128]
x1为ch,x2为n,x3为cr3,x4为ch;
[0129]
r3选自氢、氨基、氰基、卤素、羧基、c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、吗啉基、c
2-6
烯基、c
1-4
烷羰基、c
1-4
烷氨羰基、(c
1-6
烷基)2氨羰基、c
1-4
烷基磺酰基、c
1-4
烷基硫基、氨基羰基、环丙基、氮杂环丁烷基和哌嗪基,
[0130]
a)其中所述c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、c
2-6
烯基、c
1-4
烷羰基、c
1-4
烷氨羰基、(c
1-6
烷基)2氨羰基、c
1-4
烷基磺酰基、c
1-4
烷基硫基、氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、氨基、卤素、c
1-4
烷基、c
1-4
烷氧基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基、环丙基、c
1-4
烷羰氧基和未
被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代,
[0131]
b)其中所述环丙基、氮杂环丁烷基、吗啉基和哌嗪基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、卤素、c
1-4
烷基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基和c
1-4
烷羰氧基的基团取代;
[0132]
l为键;
[0133]
环a为4-7元单杂环基或7-12元螺杂环基,所述4-7元单杂环基的杂原子选自n,7-12元螺杂环基的杂原子选自o、n中的一种或两种的组合,且7-12元螺杂环基至少含有一个n,环a通过n原子与l相连接;
[0134]
每个r1分别独立地选自氢、羟基、氰基、卤素、c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基,基中所述c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基未被取代或被羟基取代;
[0135]
m为0、1或2;
[0136]
r2选自氢。
[0137]
技术方案2.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0138]
r3选自氢、卤素、c
1-4
烷基、c
1-4
烷氧基、吗啉基、c
2-6
烯基、c
1-4
烷氨羰基、(c
1-4
烷基)2氨羰基和氨基羰基,
[0139]
a)其中所述c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基、(c
1-4
烷基)2氨羰基、和氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基和未被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代,
[0140]
b)其中所述吗啉基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基和(c
1-4
烷基)2氨基的基团取代;
[0141]
技术方案3.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0142]
r3选自氢、卤素、c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基和氨基羰基,
[0143]
其中所述c
1-4
烷基、c
1-4
烷氧基、c
2-6
烯基、c
1-4
烷氨羰基、和氨基羰基是未被取代的或任选被一至多个(例如1、2、3、4或5个,在满足化合价平衡的条件下)独立选自羟基、c
1-4
烷氧基、环丙基、氨基、c
1-4
烷基氨基、(c
1-4
烷基)2氨基和未被取代或被c
1-4
烷基取代的4-6元杂环基的基团取代。
[0144]
技术方案4.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0145]
环a为4-7元单杂环基,所述4-7元单杂环基的杂原子选自n,环a通过n原子与l相连接。
[0146]
技术方案5.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0147]
环a选自
[0148]
技术方案6.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0149]
环a为
[0150]
技术方案7.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0151]
每个r1分别独立地选自氢、c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基,其中所述c
1-4
烷基、c
1-4
烷氧基、吡唑基、噻唑基和三唑基未被取代或被羟基取代。
[0152]
技术方案8.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0153]
在步骤(c')中,所述的卤代试剂是三氯氧磷、氯化亚砜、磺酰氯、三氯化膦、五氯化膦、三溴化磷、三溴氧磷、三光气、草酰氯中的一种或几种。
[0154]
技术方案9.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0155]
在步骤(c')中,所述的卤代试剂是三氯氧磷。
[0156]
技术方案10.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0157]
在步骤(c')中,(i-4)和卤代试剂的摩尔比为1:(1-5)。
[0158]
技术方案11.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0159]
在步骤(c')中,(i-4)和卤代试剂的摩尔比为1:(1-3)。
[0160]
技术方案12.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0161]
在步骤(c')中,(i-4)和卤代试剂的摩尔比为1:(1.2-2.3)。
[0162]
技术方案13.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0163]
在步骤(c')中,(i-4)和卤代试剂的摩尔比为约1:1.5。
[0164]
技术方案14.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0165]
在步骤(d')中,所述的碱是三乙胺、n,n-二异丙基乙胺、甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾中的一种或几种。
[0166]
技术方案15.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0167]
在步骤(d')中,所述的碱是三乙胺或n,n-二异丙基乙胺。
[0168]
技术方案16.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0169]
在步骤(d')中,所述的碱是三乙胺。
[0170]
技术方案17.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0171]
在步骤(d')中,所述的碱是n,n-二异丙基乙胺。
[0172]
技术方案18.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0173]
在步骤(d')中,(i-5)、(i-6)和碱的摩尔比为1:(0.5-2):(1-3)。
[0174]
技术方案19.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0175]
在步骤(c')中,所述的有机溶剂是乙腈、四氢呋喃、2-甲基四氢呋喃、氯仿、1,2-二氯乙烷中的一种或几种。
[0176]
技术方案20.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0177]
在步骤(c')中,所述的有机溶剂是乙腈。
[0178]
技术方案21.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0179]
在步骤(d')中,所述的有机溶剂是乙醇、四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺中的一种或几种。
[0180]
技术方案22.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0181]
在步骤(d')中,所述的有机溶剂是乙醇。
[0182]
技术方案23.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0183]
在步骤(c')中,有机溶剂的用量为式(i'-4)的2-20倍体积。
[0184]
技术方案24.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0185]
在步骤(c')中,有机溶剂的用量为式(i'-4)的4-10倍体积。
[0186]
技术方案25.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0187]
在步骤(d')中,有机溶剂的用量为式(i'-5)的2-20倍体积。
[0188]
技术方案26.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0189]
在步骤(d')中,有机溶剂的用量为式(i'-5)的10-20倍体积。
[0190]
技术方案27.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0191]
在步骤(c')中,反应温度为40-160℃且不高于比溶剂沸点低5℃的温度,反应时间为1-36小时。
[0192]
技术方案28.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0193]
在步骤(c')中,反应温度为60-140℃且不高于比溶剂沸点低5℃的温度,反应时间为2-24小时。
[0194]
技术方案29.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0195]
在步骤(c')中,反应温度为80-120℃且不高于比溶剂沸点低5℃的温度,反应时间为4-12小时。
[0196]
技术方案30.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0197]
在步骤(d')中,反应温度为40-120℃且不高于比溶剂沸点低5℃的温度,反应时间为0.1-12小时。
[0198]
技术方案31.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0199]
在步骤(d')中,反应温度为50-110℃且不高于比溶剂沸点低5℃的温度,反应时间为0.5-6小时。
[0200]
技术方案32.根据前述技术方案中任一项所述的制备方法,其特征在于,
[0201]
在步骤(d')中,反应温度为60-100℃且不高于比溶剂沸点低5℃的温度,反应时间为1-3小时。
[0202]
技术方案33.式(i')化合物的制备方法,其特征在于,其通过如下步骤制备:
[0203][0204]
步骤(c):于有机溶剂中,(i'-4)与卤代试剂发生卤代反应得到(i'-5):
[0205][0206]
步骤(d):于有机溶剂中,(i'-5)与(i'-6)和碱发生亲核取代反应得(i'):
[0207][0208]
其中,r1为c
1-6
烷基;
[0209]
x为卤素原子;
[0210]
m为碱金属离子。
[0211]
技术方案34.根据技术方案33所述的制备方法,其特征在于在步骤(c)中,所述的卤代试剂是三氯氧磷、氯化亚砜、磺酰氯、三氯化膦、五氯化膦、三溴化磷、三溴氧磷、三光气、草酰氯中的一种或几种。
[0212]
技术方案35.根据技术方案33-34中任一项所述的制备方法,其特征在于在步骤(c)中,所述的卤代试剂是三氯氧磷。
[0213]
技术方案36.根据技术方案33-35中任一项所述的制备方法,其特征在于在步骤(c)中,(i'-4)和卤代试剂的摩尔比为1:(1-5)。
[0214]
技术方案37.根据技术方案33-36中任一项所述的制备方法,其特征在于在步骤(c)中,(i'-4)和卤代试剂的摩尔比为1:(1-3)。
[0215]
技术方案38.根据技术方案33-37中任一项所述的制备方法,其特征在于在步骤(c)中,(i'-4)和卤代试剂的摩尔比为1:(1.2-2.3)。
[0216]
技术方案39.根据技术方案33-38中任一项所述的制备方法,其特征在于在步骤(c)中,(i'-4)和卤代试剂的摩尔比为约1:1.5。
[0217]
技术方案40.根据技术方案33-39中任一项所述的制备方法,其特征在于在步骤(d)中,所述的碱是三乙胺、n,n-二异丙基乙胺、甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾中的一种或几种。
[0218]
技术方案41.根据技术方案33-40中任一项所述的制备方法,其特征在于在步骤(d)中,所述的碱是三乙胺或n,n-二异丙基乙胺。
[0219]
技术方案42.根据技术方案33-41中任一项所述的制备方法,其特征在于在步骤(d)中,所述的碱是三乙胺。
[0220]
技术方案43.根据技术方案33-42中任一项所述的制备方法,其特征在于在步骤(d)中,所述的碱是n,n-二异丙基乙胺。
[0221]
技术方案44.根据技术方案33-43中任一项所述的制备方法,其特征在于在步骤(d)中,(i'-5)、(i'-6)和碱的摩尔比为1:(0.5-2):(1-3)。
[0222]
技术方案45.根据技术方案33-44中任一项所述的制备方法,其特征在于在步骤(c)中,所述的有机溶剂是乙腈、四氢呋喃、2-甲基四氢呋喃、氯仿、1,2-二氯乙烷中的一种或几种。
[0223]
技术方案46.根据技术方案33-45中任一项所述的制备方法,其特征在于在步骤(c)中,所述的有机溶剂是乙腈。
[0224]
技术方案47.根据技术方案33-46中任一项所述的制备方法,其特征在于在步骤(d)中,所述的有机溶剂是乙醇、四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺中的一种或几种。
[0225]
技术方案48.根据技术方案33-47中任一项所述的制备方法,其特征在于在步骤(d)中,所述的有机溶剂是乙醇。
[0226]
技术方案49.根据技术方案33-48中任一项所述的制备方法,其特征在于在步骤(c)中,有机溶剂的用量为式(i'-4)的2-20倍体积。
[0227]
技术方案50.根据技术方案33-49中任一项所述的制备方法,其特征在于在步骤(c)中,有机溶剂的用量为式(i'-4)的4-10倍体积。
[0228]
技术方案51.根据技术方案33-50中任一项所述的制备方法,其特征在于在步骤(d)中,有机溶剂的用量为式(i'-5)的2-20倍体积。
[0229]
技术方案52.根据技术方案33-51中任一项所述的制备方法,其特征在于在步骤(d)中,有机溶剂的用量为式(i'-5)的10-20倍体积。
[0230]
技术方案53.根据技术方案33-52中任一项所述的制备方法,其特征在于,
[0231]
在步骤(c)中,反应温度为40-160℃且不高于比溶剂沸点低5℃的温度,反应时间为1-36小时。
[0232]
技术方案54.根据技术方案33-53中任一项所述的制备方法,其特征在于,
[0233]
在步骤(c)中,反应温度为60-140℃且不高于比溶剂沸点低5℃的温度,反应时间为2-24小时。
[0234]
技术方案55.根据技术方案33-54中任一项所述的制备方法,其特征在于,
[0235]
在步骤(c)中,反应温度为80-120℃且不高于比溶剂沸点低5℃的温度,反应时间为4-12小时。
[0236]
技术方案56.根据技术方案33-55中任一项所述的制备方法,其特征在于,
[0237]
在步骤(d)中,反应温度为40-120℃且不高于比溶剂沸点低5℃的温度,反应时间为0.1-12小时。
[0238]
技术方案57.根据技术方案33-56中任一项所述的制备方法,其特征在于,
[0239]
在步骤(d)中,反应温度为50-110℃且不高于比溶剂沸点低5℃的温度,反应时间为0.5-6小时。
[0240]
技术方案58.根据技术方案33-57中任一项所述的制备方法,其特征在于,
[0241]
在步骤(d)中,反应温度为60-100℃且不高于比溶剂沸点低5℃的温度,反应时间为1-3小时。
[0242]
技术方案59.技术方案1-58中任一项所述的制备方法,其特征在于,还包括步骤(b),
[0243]
于有机溶剂中,(i'-3)与碱发生缩合反应得到(i'-4):
[0244]
[0245]
r1为c
1-6
烷基;
[0246]
r2为c
1-6
烷基;
[0247]
m为k
+
、na
+
、li
+
、cs
+
。
[0248]
技术方案60.技术方案59所述的制备方法,其特征在于r1为甲基或乙基。
[0249]
技术方案61.技术方案59-60中任一项所述的制备方法,其特征在于r2为甲基或乙基。
[0250]
技术方案62.技术方案59-61中任一项所述的制备方法,其特征在于m为k
+
或na
+
。
[0251]
技术方案63.技术方案59-62中任一项所述的制备方法,其特征在于在步骤(b)中,所述的碱是氢氧化钾、氢氧化钠、甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾、甲醇钾中的一种或几种。
[0252]
技术方案64.技术方案59-63中任一项所述的制备方法,其特征在于在步骤(b)中,所述的碱是甲醇钾和/或乙醇钠。
[0253]
技术方案65.技术方案59-64中任一项所述的制备方法,其特征在于在步骤(b)中,(i'-3)和碱的摩尔比为1:(1-5)。
[0254]
技术方案66.技术方案59-65中任一项所述的制备方法,其特征在于在步骤(b)中,所述的有机溶剂是乙醇、四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺中的一种或几种。
[0255]
技术方案67.技术方案59-66中任一项所述的制备方法,其特征在于在步骤(b)中,所述的有机溶剂是四氢呋喃。
[0256]
技术方案68.技术方案59-67中任一项所述的制备方法,其特征在于在步骤(b)中,所述的有机溶剂的用量为式(i'-3)的2-20倍体积。
[0257]
技术方案69.技术方案59-68中任一项所述的制备方法,其特征在于在步骤(b)中,所述的有机溶剂的用量为式(i'-3)的3-12倍体积。
[0258]
技术方案70.技术方案59-69中任一项所述的制备方法,其特征在于,
[0259]
在步骤(b)中,反应温度为40-120℃且不高于比溶剂沸点低5℃的温度,反应时间为0.1-12小时。
[0260]
技术方案71.技术方案59-70中任一项所述的制备方法,其特征在于,
[0261]
在步骤(b)中,反应温度为50-120℃且不高于比溶剂沸点低5℃的温度,反应时间为0.5-6小时。
[0262]
技术方案72.技术方案59-71中任一项所述的制备方法,其特征在于,
[0263]
在步骤(b)中,反应温度为60-100℃且不高于比溶剂沸点低5℃的温度,反应时间为1-3小时。
[0264]
技术方案73.技术方案59-72中任一项所述的制备方法,其特征在于,还包括步骤(a),
[0265]
于有机溶剂中,式(i'-1)、(i'-2)和偶联试剂发生缩合反应得到(i'-3):
[0266][0267]
r1为c
1-6
烷基;
[0268]
r2为c
1-6
烷基。
[0269]
技术方案74.技术方案73所述的制备方法,其特征在于,
[0270]
r1为甲基或乙基;
[0271]
技术方案75.技术方案73-74中任一项所述的制备方法,其特征在于,
[0272]
r2为甲基或乙基。
[0273]
技术方案76.技术方案73-75中任一项所述的制备方法,其特征在于,
[0274]
在步骤(a)中,所述的偶联试剂是1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、2-(7-氧化苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐、二环己基碳二亚胺中的一种或几种。
[0275]
技术方案77.技术方案73-76中任一项所述的制备方法,其特征在于,
[0276]
在步骤(a)中,所述的偶联试剂是1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐。
[0277]
技术方案78.技术方案73-77中任一项所述的制备方法,其特征在于在步骤(a)中,(i'-1)、(i'-2)和偶联试剂的摩尔比为1:(0.5-2):(1-2)。
[0278]
技术方案79.技术方案73-78中任一项所述的制备方法,其特征在于,
[0279]
在步骤(a)中,所述的有机溶剂是二氯甲烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、四氢呋喃中的一种或几种。
[0280]
技术方案80.技术方案73-79中任一项所述的制备方法,其特征在于,
[0281]
在步骤(a)中,所述的有机溶剂是二氯甲烷。
[0282]
技术方案81.技术方案73-80中任一项所述的制备方法,其特征在于,
[0283]
在步骤(a)中,所述的有机溶剂的用量为式(i'-1)的2-20倍体积。
[0284]
技术方案82.技术方案73-81中任一项所述的制备方法,其特征在于,
[0285]
在步骤(a)中,所述的有机溶剂的用量为式(i'-1)的5-12倍体积。
[0286]
技术方案83.技术方案73-82中任一项所述的制备方法,其特征在于,
[0287]
在步骤(a)中,反应温度为10-40℃且不高于比溶剂沸点低5℃的温度,反应时间为0.1-12小时。
[0288]
技术方案84.技术方案73-83中任一项所述的制备方法,其特征在于,
[0289]
在步骤(a)中,反应温度为15-35℃且不高于比溶剂沸点低5℃的温度,反应时间为0.5-6小时。
[0290]
技术方案85.技术方案73-84中任一项所述的制备方法,其特征在于,
[0291]
在步骤(a)中,反应温度为20-30℃且不高于比溶剂沸点低5℃的温度,反应时间为1-3小时。
[0292]
技术方案86.式(i')化合物的中间体,其特征在于,具有以下结构式:
[0293][0294]
r1为c
1-6
烷基;
[0295]
m为k
+
、na
+
、li
+
、cs
+
。
[0296]
技术方案87.式(i')化合物的中间体,其特征在于,具有以下结构式:
[0297][0298]
r1为甲基或乙基;
[0299]
m为k
+
、na
+
、li
+
、cs
+
。
[0300]
技术方案88.中间体,其特征在于,其结构如下:
[0301][0302]
wo2019062733a1和wo2020182076a1公开的制备方法使用了一类1,2-二氢-2-氧代-3-氰基-1,7-二氮杂萘-4-醇化合物作为中间体,与卤代试剂进行卤代反应;与此不同,根据本发明的制备方法,可以使用一类1,2-二氢-2-氧代-3-氰基-1,7-二氮杂萘-4-醇碱金属盐化合物作为中间体,与卤代试剂进行卤代反应。如下实施例所举例说明的,本发明可以减少有毒有害的卤代试剂(如三氯氧磷)的用量。
[0303]
实施例
[0304]
以下通过具体实施例对本发明的上述内容作进一步的详细说明,但不应该理解为本发明上述主题的范围仅限于以下实施例。凡是基于本发明上述内容所实现的技术均属于本发明的范围。
[0305]
本文中使用的缩写如下:
[0306]“edci”是指:1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐。
[0307]“dipea”是指:n,n-二异丙基乙胺。
[0308]
参照wo2009093032a1的化合物23,实施例14进行制备。
[0309]
实施例1 式(i)化合物的制备
[0310][0311]
步骤1a:6-乙基-3-(氰基乙酰胺基)吡啶-4-甲酸乙酯的合成
[0312][0313]
将中间体6-乙基-3-氨基吡啶-4-甲酸乙酯(100g,514.84mmol,1.0eq)溶于二氯甲烷(1.00l),在冰浴条件下加入氰基乙酸(52.55g,617.81mmol,1.2eq),分批加入edci(148.03g,772.26mmol,1.5eq),25℃反应2小时,lc-ms检测反应完全。向反应液中加入h2o(1.00l),分液,有机相用h2o(2
×
500ml)洗,无水硫酸钠干燥,抽滤,滤液浓缩,粗品经甲基叔丁基醚(300ml)打浆得到产品(128g,收率:95.15%)。
[0314]
步骤1b:6-乙基-3-(氰基乙酰胺基)吡啶-4-甲酸乙酯的合成
[0315]
将中间体6-乙基-3-氨基吡啶-4-甲酸乙酯(500g,2.57mol,1.0eq)溶于二氯甲烷(6.00l),在冰浴条件下加入氰基乙酸(262.76g,3.09mol,1.2eq),分批加入edci(740.23g,3.86mol,1.5eq),25℃反应2小时,lc-ms检测反应完全。向反应液中加入h2o(5.00l),分液,水相用dcm(2
×
500ml)萃取,合并有机相,无水硫酸钠干燥,抽滤,滤液浓缩至1.0l,滴加至5.0l正庚烷中,大量固体析出,抽滤收集固体,50℃下烘干得到产品(658g,收率:98%)。
[0316]
步骤2a:3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钾的合成
[0317][0318]
将甲醇钾(2.95g,42.10mmol,1.1eq)分散到正庚烷(200ml)中,然后将体系内温升到80度,接着将中间体6-乙基-3-(氰基乙酰胺基)吡啶-4-甲酸乙酯(10g,38.27mmol,1.0eq)溶于四氢呋喃(30ml)中,滴加到上述加热体系中去,加完80℃反应2小时,lc-ms检测反应完全。关闭加热,让反应体系自然降温至室温,抽滤,滤饼干燥得到粗产品(10.4g,收率:107.29%)。
[0319]
步骤2b:3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钠的合成
[0320]
[0321]
将乙醇钠(2.86g,42.10mmol,1.1eq)分散到正庚烷(200ml)中,然后将体系内温升到80度,接着将中间体6-乙基-3-(氰基乙酰胺基)吡啶-4-甲酸乙酯(10g,38.27mmol,1.0eq)溶于四氢呋喃(30ml)中,滴加到上述加热体系中去,加完80℃反应2小时,lc-ms检测反应完全。关闭加热,让反应体系自然降温至室温,抽滤,滤饼干燥得到粗产品(10.3g,收率:113.43%)。
[0322]
步骤3a:6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0323][0324]
将中间体3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钾(5g,19.74mmol,1.0eq)溶于乙腈(50ml),室温下加入三氯氧磷(4.54g,29.61mmol,1.5eq),100℃反应8小时。将反应液降温,浓缩,加h2o(50ml),用10%氢氧化钠调ph值至6左右,有大量黄色固体析出,抽滤,烘干得粗品3.87g(收率:83.95%)。
[0325]
步骤3b:6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0326][0327]
将中间体3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钾(5g,19.74mmol,1.0eq)溶于乙腈(50ml),室温下加入三氯氧磷(3.63g,23.69mmol,1.2eq),100℃反应8小时。将反应液降温,浓缩,加h2o(50ml),用10%氢氧化钠调ph值至6左右,有大量黄色固体析出,抽滤,烘干得粗品3.47g(收率:75.27%)。
[0328]
步骤3c:6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0329][0330]
将中间体3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钾(10g,39.5mmol,1.0eq)溶于乙腈(100ml),室温下分批次加入三氯氧磷(13.93g,90.85mmol,2.3eq),100℃反应8小时。将反应液降温,浓缩,加h2o(500ml),用10%氢氧化钠调ph值至6左右,有大量黄色固体析出,抽滤,烘干得粗品7.18g(收率:77.87%)。
[0331]
步骤3d:6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0332][0333]
将中间体3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钠(5g,21.08mmol,1.0eq)溶于乙腈(50ml),室温下加入三氯氧磷(4.85g,31.62mmol,1.5eq),100℃反应8小时。将反应液降温,浓缩,加h2o(50ml),用10%氢氧化钠调ph值至6左右,有大量
黄色固体析出,抽滤,烘干得粗品3.72g(收率:75.46%)。
[0334]
步骤3e:6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0335][0336]
将中间体3-氰基-6-乙基-2-氧代-1,2-二氢-1,7-二氮杂萘-4-醇钾(120g,473.7mmol,1.0eq)溶于乙腈(1200ml),室温下分批次加入三氯氧磷(73.36g,478.48mmol,1.01eq),100℃反应8小时。将反应液降温,浓缩,加h2o(1200ml),用10%氢氧化钠调ph值至6左右,有大量黄色固体析出,抽滤,烘干得粗品;粗品加入2350ml四氢呋喃(thf),加入活性炭,升温回流过滤,滤液用乙酸异丙酯进行代蒸除去thf,冷却至室温后有大量固体析出,收集固体,烘干,得80.45g黄色固体(收率:72.7%)。
[0337]
步骤4a:6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0338][0339]
将中间体6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈(91g,390.3mmol,1.0eq)和4-甲基-4-甲氧基哌啶盐酸盐(70.89g,429.43mmol,1.1eq)溶于乙醇(1365ml)中,加入dipea(151.36g,1171.17mmol,3.0eq),80℃反应2小时,lc-ms检测反应完全。减压蒸除约75%的乙醇,加入水(2l),25℃搅拌1小时,抽滤,滤饼用乙醇(4l)回流溶解完全,抽滤,滤液浓缩至约1l,降温到10℃左右,抽滤,滤饼烘干得到产品(69g,收率:54.15%)。
[0340]1hnmr(400mhz,dmso-d6)δ(ppm):11.90(s,1h),8.58(s,1h),7.40(s,1h),3.59-3.61(m,4h),3.19(s,3h),2.78-2.84(m,2h),1.89-1.93(m,2h),1.77-1.82(m,2h),1.22-1.26(m,6h).
[0341]
分子式:c
18h22
n4o2分子量:326.40lc-ms(pos,m/z)=327.59[m+h]
+
.
[0342]
步骤4b:6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈的合成
[0343]
[0344]
将中间体6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈(15g,64.2mmol,1.0eq)和4-甲基-4-甲氧基哌啶盐酸盐(11.7g,70.62mmol,1.1eq)溶于乙醇(150ml)中,加入三乙胺(14.29g,141.23mmol,2.2eq),80℃反应2小时,lc-ms检测反应完全。减压蒸除约75%的乙醇,加入水(300ml),25℃搅拌1小时,抽滤,滤饼用乙醇(600ml)回流溶解完全,加入活性炭(2g),回流0.5h。抽滤,滤液浓缩至约400ml,降温到室温,抽滤,滤饼烘干得到产品(17.10g,收率:81.6%)。
[0345]
实施例2
[0346]
在步骤1中,edci被替换为2-(7-氧化苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐、或二环己基碳二亚胺,和二氯甲烷被替换为n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、或四氢呋喃,可以获得6-乙基-3-(氰基乙酰胺基)吡啶-4-甲酸乙酯。
[0347]
在步骤2a中,甲醇钾被替换为乙醇钠、氢氧化钾、氢氧化钠、甲醇钠、叔丁醇钠、或叔丁醇钾,和四氢呋喃被替换为乙醇、2-甲基四氢呋喃、n,n-二甲基甲酰胺、或n,n-二甲基乙酰胺,可以获得相应的产物。
[0348]
在步骤2b中,乙醇钠被替换为甲醇钾、氢氧化钾、氢氧化钠、甲醇钠、叔丁醇钠、或叔丁醇钾,和四氢呋喃被替换为乙醇、2-甲基四氢呋喃、n,n-二甲基甲酰胺、或n,n-二甲基乙酰胺,可以获得相应的产物。
[0349]
在步骤3a、3b、3c和3d中,乙腈被替换为四氢呋喃、2-甲基四氢呋喃、氯仿、或1,2-二氯乙烷;和三氯氧磷被替换为氯化亚砜、磺酰氯、三氯化膦、五氯化膦、三溴化磷、三溴氧磷、三光气、或草酰氯,可以获得6-乙基-4-氯-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈。
[0350]
在步骤4a中,n,n-二异丙基乙胺被替换为三乙胺、甲醇钠、乙醇钠、叔丁醇钠、或叔丁醇钾,和乙醇被替换为四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、或n,n-二甲基乙酰胺,可以获得6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈。
[0351]
在步骤4b中,三乙胺被替换为n,n-二异丙基乙胺、甲醇钠、乙醇钠、叔丁醇钠、或叔丁醇钾,和乙醇被替换为四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、或n,n-二甲基乙酰胺,可以获得6-乙基-4-(4-甲氧基-4-甲基哌啶-1-基)-2-氧代-1,2-二氢-1,7-二氮杂萘-3-甲腈。
[0352]
本发明的新的制备方法,具有以下优点:
[0353]
(1)与现有技术相比于,在维持相同或甚至更高收率的基础上,本发明能够显著降低卤代试剂如三氯氧磷的投料量。即在获得相同或甚至更高数量的目标产物的情况下,能够使用更少量的卤代试剂如三氯氧磷。从而减少了生产成本,且三废的产生量也明显降低。
[0354]
(2)在大规模工厂生产中,大量使用某些卤代试剂如三氯氧磷会造成在后处理过程的淬灭中瞬时产生巨大热量,处理不当有爆炸风险。本发明明显降低了这样的卤代试剂如三氯氧磷的投料量,从而相应降低了后处理过程中热能的产生,后处理系统的安全性得以提高,更适合大规模工厂生产。
[0355]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明保护的范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1