促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途的制作方法
促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途
1.本技术为下述原分案申请的分案申请:
2.原分案申请的申请日:2018年09月18日;
3.原分案申请的申请号:2021107606690;
4.原分案申请的发明名称:促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途;
5.该原分案申请为母案申请的分案申请:
6.母案申请的申请日:2018年09月18日;
7.母案申请的申请号:2018110919805;
8.母案申请的发明名称:促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途;本技术是申请人按照审查员的审查意见针对原分案申请的再次分案申请。
技术领域
9.本发明涉及多肽及其用途,具体涉及促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途。
背景技术:
10.肝脏是人体内最大的内脏器官(约占人体总质量的2.5%),同时也是中心代谢器官。发挥肝功能的主要是实质细胞,它们占到肝脏细胞总量的80%。肝细胞发挥了一系列作用,包括制造血浆、合成载体蛋白、对消化物的解毒、共轭及荷尔蒙的分泌、调节血脂与氨基酸的合成及代谢等。
11.细胞凋亡(apoptosis)是细胞在特定环境下的主动自杀过程。细胞凋亡是kerr等人1972年在研究肝脏局部缺血时观察到细胞调亡和死亡的两个不同图型。细胞凋亡的特征是细胞皱缩,细胞膜呈胞状突起,形成凋亡小体,核碎片和核dna降解等异常现象。细胞凋亡是临床许多疾病病理变化的主要特征,特别是在肝脏疾病中,肝细胞凋亡是引起肝脏损害的重要因素。肝细胞凋亡在肝脏病变机制中起着重要作用,死亡受体通路的紊乱被认为是激发急/慢性肝损伤发生的重要原因之一。近年来研究表明肝细胞凋亡广泛参与了多种肝病的病理过程,包括肝衰竭、病毒性肝炎、肝纤维化、肝硬化、酒精性肝病、非酒精性脂肪肝和自身免疫性肝病等。
12.肝衰竭(liver failure,lf)是由病毒、药物、酒精等多种因素引起的重型肝脏损害,导致其解毒、排泄、合成等功能发生严重障碍或失代偿,出现以凝血功能障碍、重度黄疸、腹水、肝性脑病甚至消化道出血等为主要表现的一组临床症候群,病死率极高,是肝病科临床常见的危急重症之一。《2012年版肝衰竭诊疗指南》根据其病理特征和疾病进程的不同,将肝衰竭分为急性肝衰竭(acute liver failure,alf)、亚急性肝衰竭(subacute liver failure,salf)、慢加急性(亚急性)肝衰竭(acute-on-chronic liver failure,aclf)和慢性肝衰竭(chronic liver failure,clf)。肝衰竭是临床急危重症,至今仍缺乏疗效确切的特效药物,因而成为世界性的难治病种之一,尽管人工肝和肝移植是行之有效的治疗方法,但是其昂贵的费用、肝源的紧缺及排斥反应等导致该治疗方法无法在我国得
到广泛的推广使用。
13.人hip/pap蛋白,又称再生蛋白3α(regenerating islet-derived protein iii-alpha),是由胰腺分泌的165个氨基酸组成的蛋白质。研究表明,hip/pap蛋白能防御肝细胞免于肿瘤坏死因子介导的程序性死亡,同时也是一种促有丝分裂剂,能促进肝细胞有丝分裂,从而促进肝细胞再生。现在人hip/pap蛋白一般经由重组表达系统(例如大肠杆菌)表达,纯化方法复杂,制备成本高。
14.多肽是由多个氨基酸通过一个氨基酸的氨基与另一个氨基酸的羧基脱水缩合而形成的化合物,其也可以来源于蛋白质水解的中间产物。多肽一般指由少于50个氨基酸脱水缩合而形成的化合物,而50个氨基酸以上的多肽通常称为蛋白质。多肽类药物具有分子量小、易于合成、副作用小、特异性强等特点,很少引起严重的免疫反应。
技术实现要素:
15.本发明的目的在于克服现有技术的不足之处而提供用于促进肝细胞增殖和/或抑制肝细胞凋亡的多肽及其用途。
16.为实现上述目的,本发明采取的技术方案为:促进肝细胞增殖和/或抑制肝细胞凋亡的多肽,其氨基酸序列选自seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6中的至少一种。
17.本发明促进肝细胞增殖和/或抑制肝细胞凋亡的多肽,其可以是seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6中任意一氨基酸序列所示的多肽,也可以是这6种多肽中任意两种以上(包括两种)多肽的组合。
18.上述seq id no:1~seq id no:6所示的多肽均衍生自人hip/pap蛋白。发明人在大量研究中发现,大部分衍生自人hip/pap蛋白的多肽片段都不具备生物活性,但意外的发现seq id no:1~seq id no:6所示的多肽具有与hip/pap相当或更优的促进肝细胞增殖和/或抑制肝细胞凋亡的活性。
19.作为本发明所述促进肝细胞增殖和/或抑制肝细胞凋亡的多肽的优选实施方式,所述多肽的氨基酸序列如seq id no:4所示。研究表明,如seq id no:1~seq id no:6所示的多肽以及hip/pap中,如seq id no:4所示的多肽促进肝细胞增殖和抑制肝细胞凋亡的作用最强,且其活性明显高于hip/pap。
20.另外,本发明还提供了上述多肽在制备用于促进肝细胞增殖或治疗由于肝细胞凋亡导致的疾病的产品中的用途。
21.作为本发明所述用途的优选实施方式,所述产品为药物。
22.作为本发明所述用途的优选实施方式,所述药物为液体剂型。
23.作为本发明所述用途的优选实施方式,所述促进肝细胞增殖为体内促进肝再生或体外促进肝细胞生长。
24.作为本发明所述用途的优选实施方式,所述由于肝细胞凋亡导致的疾病为肝衰竭、病毒性肝炎、肝纤维化、肝硬化、酒精性肝病、非酒精性脂肪肝或自身免疫性肝病。更优选地,所述肝衰竭为急性肝衰竭。
25.本发明的发明人通过体外细胞实验证实本发明seq id no:1~seq id no:6所示的多肽具有促进肝细胞增殖和抑制肝细胞凋亡的活性,因此本发明的多肽可以用于促进肝
细胞增殖或治疗肝细胞凋亡导致的疾病。研究显示,肝细胞凋亡的疾病包括肝衰竭,病毒性肝炎,胆汁淤积性肝损伤,酒精性肝损伤,非酒精性脂肪性肝炎,肝硬化,和毒素或药物介导的肝损伤等,由于本发明的多肽具有抑制肝细胞凋亡的活性,因此可以用于治疗上述疾病。本发明的多肽在急性肝衰竭动物模型中显示对急性肝衰竭的良好治疗效果,进一步证实其可用于肝细胞凋亡相关疾病的治疗。
26.最后,本发明还提供了一种促进肝细胞增殖和/或抑制肝细胞凋亡的药物,所述药物含有上述多肽。
27.作为本发明所述促进肝细胞增殖和/或抑制肝细胞凋亡的药物的优选实施方式,所述药物还包括药学上可接受的载体。本领域的技术人员可根据药物的剂型等对药学上可接受的载体进行常规选择。药物的剂型包括但不限于液体剂型、气体剂型、固体剂型等,作为本发明所述促进肝细胞增殖和/或抑制肝细胞凋亡的药物的优选实施方式,所述药物为液体剂型。本发明的药物可通过静脉注射或皮下注射来进行给药。
28.作为本发明所述促进肝细胞增殖和/或抑制肝细胞凋亡的药物的优选实施方式,所述促进肝细胞增殖为体内促进肝再生或体外促进肝细胞生长。
29.与现有技术相比,本发明的有益效果为:本发明提供了促进肝细胞增殖和/或抑制肝细胞凋亡的多肽,这些多肽长度为9至27个氨基酸,而hip/pap蛋白质的长度为165个氨基酸,本发明的多肽长度显著短于hip/pap蛋白质,但具有与hip/pap相当或更优的促进肝细胞增殖和/或抑制肝细胞凋亡的活性,并且本发明多肽具有分子量小、易于合成、免疫原性低等优点,因此本发明的多肽具有广阔的应用前景。
附图说明
30.图1为本发明多肽与hip/pap促进肝细胞增殖的活性比较结果图;
31.图2为本发明多肽与hip/pap抑制肝细胞凋亡的活性比较结果图;
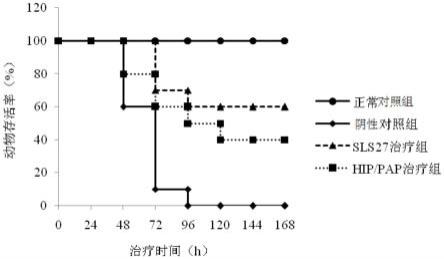
32.图3为本发明多肽与hip/pap治疗小鼠急性肝衰竭的生存率比较结果图。
具体实施方式
33.为更好地说明本发明的目的、技术方案和优点,下面将结合附图和具体实施例对本发明作进一步说明。
34.实施例1多肽
35.本发明促进肝细胞增殖和/或抑制肝细胞凋亡的多肽的一种实施例,本实施例的多肽如表1所示。
36.表1
37.名称序列号序列igl9seq id no:1iglhdptqgptq9seq id no:2ptqgtepnglhd9seq id no:3lhdptqgtesls27seq id no:4slsrstaflrwkdyncnvrlpyvckftayg25seq id no:5aygshcyalflspkswtdadlacqkvsv19seq id no:6vsvlsgaegsfvsslvksi
38.本实施例的上述多肽由深圳市泓翊科技有限公司采用固相合成工艺合成,纯度均>98%,各合成50mg。
39.实施例2检测体外促进肝细胞增殖的活性
40.本实施例中,人肝细胞系hl-7702购自atcc。
41.本实施例检测实施例1所述6种多肽以及hip/pap体外促进肝细胞增殖的活性的方法为:
42.取出冻存的hl-7702细胞,37℃水浴锅解冻复苏。在低速离心机上,以800rpm离心5分钟;吸去上清,然后用1ml培养基重悬细胞。
43.重悬细胞转移至新的培养瓶中,加入适量mem培养基,至于co2培养箱培养(培养条件5%co2、饱和湿度、37℃)。
44.待细胞生长至80%,消化细胞后吹打散细胞,计数,调整细胞浓度为1
×
105个/ml,加至96孔板,每孔100μl,即每孔细胞为1
×
104个。
45.待细胞贴壁后,加入不同药物处理,分别为igl9、ptq9、lhd9、sls27、ayg25、vsv19、hip/pap,每种药物设两个浓度(1μg/ml、10μg/ml),并以pbs作为阴性对照。
46.药物处理0、2、3、4、5天后,分别加入celltiter96aq单溶液细胞增殖检测试剂(promega,cat.no.g3582),比例为1/10。即100μl培养液加入10μl检测液。
47.孵育4小时后,酶标仪读板,测od490数据。
48.结果见图1,由图1可见,hip/pap及本发明多肽均具有促进肝细胞增殖的作用,且量效关系明显,本发明6种多肽的活性与hip/pap相当或更优,其中sls27促进肝细胞增殖的作用最强。
49.实施例3检测体外抑制肝细胞凋亡的活性
50.本实施例检测实施例1所述6种多肽以及hip/pap体外抑制肝细胞凋亡的活性的方法为:
51.人肝细胞hl-7702铺96孔板,细胞浓度为1
×
105个/ml,每孔100μl,即每孔细胞为1
×
104个。
52.每孔加入20ng/ml act d2处理30min、80ng/ml tnf-α处理48h,建立细胞凋亡模型。
53.加入相应的药物处理,分别为igl9、ptq9、lhd9、sls27、ayg25、vsv19、hip/pap,加药体积为10μl,每种药物两个浓度(终浓度分别为1μg/ml、10μg/ml)加入体积为10μl,并以同体积的pbs作为阴性对照。
54.药物处理24h后,每孔加入100μl 试剂(3/7assay promega公司提供,货号:g8090),在摇板机上以300-500rpm的转速轻柔混匀每孔的内容物约30秒。在室温(18-22℃)孵育30分钟到3小时。
55.在荧光发光仪(luminometer)(promega,glomax生物发光检测仪)上测量每个样品的荧光值。
56.结果见图2,由图2可见,hip/pap及本发明多肽均具有抑制肝细胞凋亡的作用,且量效关系明显,本发明6种多肽的活性与hip/pap相当或更优,其中sls27抑制肝细胞凋亡的作用最强。
57.实施例4动物模型中检测治疗急性肝衰竭的效果
58.本实施例检测实施例1所述6种多肽以及hip/pap治疗急性肝衰竭的效果的方法为:
59.选择实施例2、3中活性最高的多肽sls27进行体内活性研究,考察对小鼠急性肝衰竭模型的治疗作用。
60.8周龄雄性balb/c小鼠80只,随机分成四组,分别为正常对照组、阴性对照组、sls27治疗组和hip/pap治疗组,分别给予生理盐水、生理盐水、sls27多肽(2.5mg/kg)、hip/pap(2.5mg/kg),给药方式为尾静脉注射,注射体积为100μl。给药2d后给予5%的d-氨基半乳糖(d-gal,sigma)建立急性肝衰竭模型,剂量为1.0g/kg,正常对照组给予同等剂量的生理盐水。
61.小鼠注射d-gal 6h后,阴性对照组小鼠开始出现活动减少,饮食下降的现象,正常对照组及sls27、hip/pap治疗组则无明显变化;48h后,阴性对照组小鼠活动明显减少,并开始死亡,96h内死亡率达100%。治疗168h(7天)后,正常对照组小鼠存活率为100%,sls27治疗组和hip/pap治疗组小鼠存活率分别为60%和40%,阴性对照组则为0。与阴性对照组相比,sls27治疗组的动物存活率显著更高(p<0.01),且优于hip/pap组,说明sls27多肽的活性高于hip/pap。
62.最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1