一种有机化合物及其应用、包含其的有机电致发光器件的制作方法
本发明涉及一种含硼氮类有机化合物,属于有机发光材料,本发明还同时涉及该化合物在有机电致发光器件中的应用。
背景技术:
1、随着社会科学的不断进步与发展,显示技术在人们的生活中变得至关重要。有机电致发光二极管(oleds)由于其具有柔性、可弯曲、自发光、高对比度、大尺寸、低功耗等诸多优点而成为了目前主流的显示设备之一。
2、oleds的发光机理是电子和空穴在电激发下复合形成激子,激子服从概率统计分布,单线态激子大约占25%,三线态激子大约占75%。第一代发光技术统称为荧光技术,它是利用单线态激子发光;第二代发光技术统称为磷光技术,它是利用三线态激子发光,理论上可实现100%的内量子效率,但是构筑磷光染料所需要的重金属它不仅价格昂贵而且污染环境,因此目前普遍采用的是利用有机小分子构筑的第三代热激发延迟荧光技术,当单-三线态能级差很小时,三线态激子可以反向系间窜越至单线态,进而回迁至基态发光。其中作为三基色的红光以及绿光染料由于其电致发光效率较高,功耗低,成为了目前商业化显示设备的主流。然而,蓝光材料的色度以及寿命都达不到目前商业化的显示需求,蓝光器件仍然采用传统荧光材料来实现高的色纯度以及长的器件寿命。
3、近年来,日本的takuji hatakeyama以及junji kido等课题组报道了一系列基于硼氮共振型的热激发延迟荧光的有机小分子材料dabna-1(adv.mater.2016,28,2777–2781j.mater.chem.c,2019,7,3082-3089),该类化合物中硼原子、氮原子以及苯基,构成了刚性多环的芳香族共振骨架,因而具有较高的荧光量子产率。该类化合物与传统的蓝色荧光染料相比,发射光谱带隙更窄、色纯度较高。然而,刚性平面结构也导致了其单线态与三线态能级差较大,三线态到单线态的反向系间窜越较慢,激子在染料上复合后会引起严重的效率滚降,器件寿命较短。此外,过于平面的刚性结构往往也会导致因掺杂浓度过高进而导致发射光谱变宽以及红移等不利影响。
4、
5、现有的有机电致发光材料在发光性能方面还有很大的改进余地,业界亟需开发新的发光材料体系以满足商业化需求。硼氮共振型材料具有高色纯度和高发光效率的优点,引起了科研界和产业界的广泛关注。但是,由于外围取代基对其能级影响很小,即很难对材料的发光颜色进行调控,其光色也一直局限在天蓝光区域,大大限制这类材料在高分辨显示、全彩显示以及白光照明领域等的进一步应用。
6、随着oled产品逐步进入市场,人们对这类产品的性能有越来越高的要求。当前使用的oled材料和器件结构无法完全解决oled产品效率、寿命、成本等各方面的问题。本发明的研究人员通过认真思考和不断实验,发现了一种巧妙的分子设计方案,并在下文中详细地进行说明。令人惊讶地,本发明所揭示的化合物非常适合应用于oled并提升器件的性能和调节其发光颜色至深蓝光。
技术实现思路
1、为解决上述技术问题,本发明设计一类特定结构的可发射深蓝光的含硼氮结构的共振型荧光染料,并可以有效调节材料光色至深蓝光,同时能够提升器件效率及寿命。
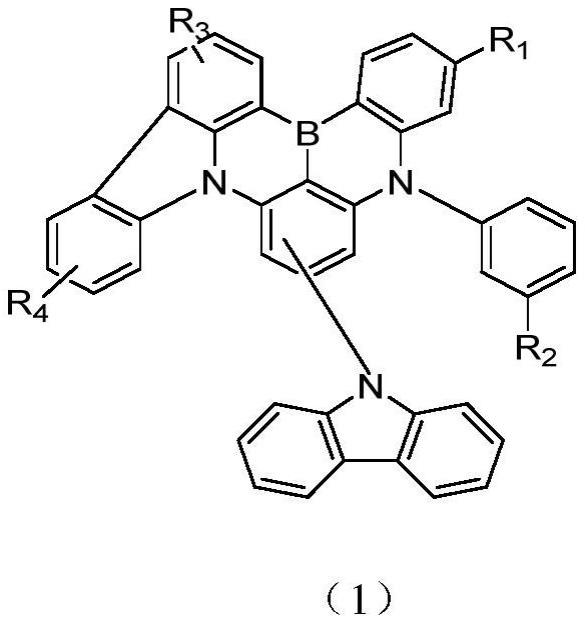
2、本发明提供了一种含硼氮类有机化合物,具有如通式(1)所示的结构:
3、
4、式(1)中:
5、环a、环b分别独立地表示取代或未取代的c5~c60芳环、取代或未取代的c3~c60杂环中的一种;
6、环a和环b中所述取代的取代基各自独立地选自卤素、未取代或r'取代的c1~c20直链或支链烷基、未取代或r'取代的c3~c20环烷基、未取代或r'取代的c1~c20烷氧基、未取代或r'取代的c1~c20烷基硅基、未取代或r'取代的c1~c20烷基氨基、氰基、硝基、羟基、氨基、未取代或r'取代的c6~c30芳基氨基、未取代或r'取代的c3~c30杂芳基氨基、未取代或r'取代的c6~c30芳氧基、未取代或r'取代的c3~c30杂芳氧基、未取代或r'取代的c6~c60芳基、未取代或r'取代的c3~c60杂芳基中的至少一种,环a和环b中所述取代的取代基各自独立地不连接,或相邻的2个取代基通过化学键连接成环;
7、r1和r2分别独立地选自取代或未取代的c1~c20直链或支链烷基、取代或未取代的c3~c20环烷基、取代或未取代的c1~c20烷氧基、取代或未取代的c1~c20烷基硅基、取代或未取代的c6~c60芳基氨基、取代或未取代的c3~c60杂芳基氨基、取代或未取代的c6~c30芳氧基、取代或未取代的c3~c30杂芳氧基、取代或未取代的c6~c60芳基、取代或未取代的c3~c60杂芳基中的一种;
8、l1选自单键、cr1r2、o原子、s原子、nr3中的一种;
9、r1、r2和r3分别独立地选自取代或未取代的c1~c20直链或支链烷基、取代或未取代的c3~c20环烷基、取代或未取代的c6~c60芳基、取代或未取代的c3~c60杂芳基中的一种;
10、x1、x2、x3分别独立地选自cr3或n,所述r3独立地选自氢、卤素、氰基、硝基、羟基、氨基、取代或未取代的c1~c20直链或支链烷基、取代或未取代的c3~c20环烷基、取代或未取代的c1~c20烷氧基、取代或未取代的c1~c20烷基硅基、取代或未取代的c6~c60芳基氨基、取代或未取代的c6~c60杂芳基氨基、取代或未取代的c6~c30芳氧基、取代或未取代的c3~c30杂芳氧基、取代或未取代的c6~c60芳基、取代或未取代的c3~c60杂芳基中的一种;所述相邻的两个r3之间连接成环或者不连接;
11、x1、x2、x3中至少一个为cr3,且该r3为式(a)所示的结构;
12、式(a)中:环c和环d分别独立地表示r”取代或未取代的c5~c30芳环、r”取代或未取代的c3~c30杂环中的一种,环c和环d中所述取代的取代基各自独立地不连接,或相邻的2个取代基通过化学键连接成环;
13、r1、r2、r3、r1、r2、r3中所述取代的取代基、r'和r”各自独立选自卤素、氰基、硝基、羟基、氨基、c1~c20直链或支链烷基、c3~c20环烷基、c1~c20烷氧基、c1~c20烷基硅基、c6~c30芳基氨基、c3~c30杂芳基氨基、c6~c30芳氧基、c3~c30杂芳氧基、c6~c60芳基或c3~c60杂芳基中的一种或两种的组合。
14、本发明中,所述的“取代或未取代”的基团,可以取代有一个取代基,也可以取代有多个取代基,当取代基为多个时,可以选自不同的取代基,本发明中涉及到相同的表达方式时,均具有同样的意义,且取代基的选择范围均如上所示不再一一赘述。
15、在本说明书中,ca~cb的表达方式代表该基团具有的碳原子数为a~b,除非特殊说明,一般而言该碳原子数不包括取代基的碳原子数。
16、在本说明书中,“-”划过的环结构的表达方式,表示连接位点于该环结构上任意能够成键的位置。
17、在本说明书中,“各自独立地”表示其主语具有多个时,彼此之间可以相同也可以不同。
18、本发明中,对于化学元素的表述,若无特别说明,通常包含其同位素的概念,例如“氢(h)”的表述,则包括其同位素1h(氕或者h)、2h(氘或者d)的概念;碳(c)则包括12c、13c等,不再赘述。
19、本发明中的杂原子,通常指选自n、o、s、p、si和se中的原子或原子团,优选选自n、o、s。
20、在本说明书中,作为卤素的例子可举出:氟、氯、溴、碘等。
21、在本发明中,若无特别说明,芳基和杂芳基均包括单环和稠环的情况。
22、本发明中,所述取代或未取代的c6-c60芳基包括单环芳基和稠环芳基,优选c6-c30芳基,进一步优选c6-c20芳基。所谓单环芳基是指分子中含有至少一个苯基,当分子中含有至少两个苯基时,苯基之间相互独立,通过单键进行连接,示例性地如:苯基、联苯基、三联苯基等。具体而言,所述联苯基包括2-联苯基、3-联苯基和4-联苯基;所述三联苯基包括对-三联苯基-4-基、对-三联苯基-3-基、对-三联苯基-2-基、间-三联苯基-4-基、间-三联苯基-3-基和间-三联苯基-2-基。稠环芳基是指分子中含有至少两个芳环,且芳环之间并不相互独立而是共用两个相邻的碳原子互相稠合的基团。示例性地如:萘基、蒽基、菲基、茚基、芴基、荧蒽基、三亚苯基、芘基、苝基、基、并四苯基及它们的衍生基团等。所述萘基包括1-萘基或2-萘基;所述蒽基选自1-蒽基、2-蒽基和9-蒽基;所述芴基选自1-芴基、2-芴基、3-芴基、4-芴基和9-芴基;所述芘基选自1-芘基、2-芘基和4-芘基;所述并四苯基选自1-并四苯基、2-并四苯基和9-并四苯基。所述芴的衍生基团选自9,9-二甲基芴基、9,9-二乙基芴基、9,9-二丙基芴基、9,9-二丁基芴基、9,9-二戊基芴基、9,9-二己基芴基、9,9-二苯基芴基、9,9-二萘基芴基、9,9’-螺二芴和苯并芴基。
23、本发明中提到的c3~c60杂芳基包括单环杂芳基和稠环杂芳基,优选c3-c30的杂芳基,进一步优选为c4-c20杂芳基,更优选为c5-c12杂芳基。单环杂芳基是指分子中含有至少一个杂芳基,当分子中含有一个杂芳基和其他基团(如芳基、杂芳基、烷基等)时,杂芳基和其他基团之间相互独立,通过单键进行连接,单环杂芳基可举出例如:呋喃基、噻吩基、吡咯基、吡啶基等。稠环杂芳基是指分子中至少含有一个芳杂环和一个具有芳香性的环(芳杂环或芳环),且二者之间并不相互独立而是共用两个相邻的原子互相稠合的基团。稠环杂芳基的例子可以举出:苯并呋喃基、苯并噻吩基、异苯并呋喃基、吲哚基、二苯并呋喃基、二苯并噻吩基、咔唑基、吖啶基、异苯并呋喃基、异苯并噻吩基、苯并咔唑基、氮杂咔唑基、吩噻嗪基、吩嗪基、9-苯基咔唑基、9-萘基咔唑基、二苯并咔唑基、吲哚并咔唑基等。
24、本发明中亚芳基的具体例,可以举出上述芳基的例子中去掉一个氢原子而得到的二价基团。亚芳基的碳个数包括但不限于c6、c8、c10、c12、c14、c16、c18、c20、c22、c24、c26、c28等。本发明中亚杂芳基的具体例,可以举出上述杂芳基的例子中去掉一个氢原子而得到的二价基团。
25、本发明中的芳氧基,可以举出上述芳基与杂芳基与氧组成的一价基团。
26、本发明中,芳基氨基代表一个或两个芳基取代氨基上的氢而形成的基团,其中所述芳基氨基的连接位点可以与芳基氨基中的芳基连接,也可以与芳基氨基中的n连接,所述芳基氨基中的芳基的示例性碳个数和具体基团与上述相同。
27、本发明中提到的c6~c30芳基氨基可举出例如:苯基氨基、甲基苯基氨基、萘基氨基、蒽基氨基、菲基氨基、联苯基氨基等。
28、本发明中提到的c3~c30杂芳基氨基可举出例如:吡啶基氨基、嘧啶基氨基、二苯并呋喃基氨基等。
29、本发明中提到的链状烷基,若无特别说明,包括直链烷基和支链烷基。具体而言,取代或未取代的c1-c30链状烷基,优选为取代或未取代c1-c16的链状烷基,更优选为取代或未取代的c1-c10的链状烷基。取代或未取代的c1-c10的链状烷基可举出例如:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、2-甲基丁基、正戊基、仲戊基、新戊基、正己基、新己基、正庚基、正辛基、2-乙基己基等。
30、本发明中,所述环烷基包括单环烷基和多环烷基;其中,单环烷基是指含有单个环状结构的烷基;多环烷基是指两个或者两个以上的环烷基通过共享一个或多个环上碳原子所组成的结构;所述c3-c20环烷基可举例如:环丙基、环丁基、环戊基、环己基、金刚烷基等。
31、在本说明书中,作为所述取代或未取代的c1-c20烷氧基优选取代或未取代的c1-c10烷氧基的,c1-c10烷氧基的例子可举出:甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、仲丁氧基、异丁氧基、叔丁氧基、戊氧基、异戊氧基、己氧基、庚氧基、辛氧基、壬氧基、癸氧基、十一烷氧基、十二烷氧基等,其中优选甲氧基、乙氧基、正丙氧基、异丙氧基、叔丁氧基、仲丁氧基、异丁氧基、异戊氧基,更优选甲氧基。
32、在本说明书中,作为所述取代或未取代的c1-c20硅烷基,作为所述取代或未取代的c1-c10硅烷基,c1-c10硅烷基的例子可以是被在上述c1~c10烷基中所例举的基团取代的甲硅烷基,具体可举出:甲基甲硅烷基、二甲基甲硅烷基、三甲基甲硅烷基、乙基甲硅烷基、二乙基甲硅烷基、三乙基甲硅烷基、叔丁基二甲基甲硅烷基、叔丁基二苯基甲硅烷基等基团。
33、需要说明的是,本技术中为了便于说明对各个基团/特征可能的作用分别进行了描述,但这并不表示这些基团/特征是孤立地起作用的。实际上,获得良好性能的原因本质上是整个分子的优化组合,是各个基团之间协同作用的结果,而不是单一基团的效果。
34、优选的,环a、环b中的至少一个具有如式(b)所示的结构:
35、
36、当环a为式(b)所示的结构时,所述环a通过共享化学键c或化学键d与式(1)的其他部分连接,当环b为式(b)所示的结构时,环b通过共享化学键c和共享化学键d与式(1)的其他部分连接;
37、式(b)中,所述z1、z2、z3和z4分别独立地选自cr4或n,所述r4独立地选自氢、卤素、未取代或r'取代的c1~c20直链或支链烷基、未取代或r'取代的c3~c20环烷基、未取代或r'取代的c1~c20烷氧基、未取代或r'取代的c1~c20烷基硅基、未取代或r'取代的c1~c20烷基氨基、氰基、硝基、羟基、氨基、未取代或r'取代的c6~c30芳基氨基、未取代或r'取代的c3~c30杂芳基氨基、未取代或r'取代的c6~c30芳氧基、未取代或r'取代的c3~c30杂芳氧基、未取代或r'取代的c6~c60芳基、未取代或r'取代的c3~c60杂芳基中的至少一种,所述相邻的两个r4之间连接成环或者不连接;
38、r'各自独立选自卤素、氰基、硝基、羟基、氨基、c1~c20直链或支链烷基、c3~c20环烷基、c1~c20烷氧基、c1~c20烷基硅基、c6~c30芳基氨基、c3~c30杂芳基氨基、c6~c30芳氧基、c3~c30杂芳氧基、c6~c60芳基或c3~c60杂芳基中的一种或两种的组合。
39、优选的,本发明的有机化合物具有如式(1-1)所示的结构:
40、
41、式(1-1)中,x1、x2、x3、r1、r2、l1、环c和环d的定义均与在权利要求1中的定义相同;
42、z1、z2、z3和z4的定义与在式(b)中的定义相同,z1’、z2’、z3’的定义与z1、z2、z3和z4的定义相同;
43、优选的,z1、z2、z3、z4、z1’、z2’、z3’分别独立地选自cr4或n,所述r4选自氢、卤素、未取代或r'取代的c1~c20直链或支链烷基、未取代或r'取代的c3~c20环烷基、未取代或r'取代的c1~c20烷氧基、未取代或r'取代的c1~c20烷基硅基、未取代或r'取代的c1~c20烷基氨基、氰基、硝基、羟基、氨基、未取代或r'取代的c6~c30芳基氨基、未取代或r'取代的c3~c30杂芳基氨基、未取代或r'取代的c6~c30芳氧基、未取代或r'取代的c3~c30杂芳氧基、未取代或r'取代的c6~c60芳基、未取代或r'取代的c3~c60杂芳基中的至少一种,所述相邻的两个r4之间连接成环或者不连接;
44、r'各自独立地选自卤素、c1~c10直链或支链烷基、c3~c10环烷基、c1~c10烷氧基、c1~c10烷基硅基、氰基、硝基、羟基、氨基、c6~c30芳基氨基、c3~c30杂芳基氨基、c6~c30芳氧基、c3~c30杂芳氧基、c6~c30芳基、c3~c30杂芳基中的一种或两种的组合。
45、优选的,所述式(1)、式(1-1)中,x1、x2、x3分别独立地选自cr3,且其中至少一个r3为式(a)所示的结构;
46、优选的,所述式(1)、式(1-1)中,x1、x2、x3分别独立地选自cr3,且其中至少一个r3为式(a)所示的结构,另两个r3为氢;
47、再优选的,所述x2为cr3且r3为式(a)所示的结构,所述x1和x3为cr3且r3为氢。
48、优选的,本发明的有机化合物具有如式(1-2)所示的结构:
49、
50、式(1-2)中,z1、z2、z3、z4、z1’、z2’、z3’、r1、r2、l1、环c和环d的定义均与在式(1-1)中的定义相同;
51、优选的,l1为单键
52、优选的,r1和r2分别独立地选自取代或未取代的c1~c20直链或支链链状烷基、取代或未取代的c3~c20环烷基中的一种;
53、优选的,r1和r2分别独立地选自c1~c20直链或支链烷基、c3~c20环烷基中的一种;
54、更优选的,r1和r2分别独立地选自甲基、乙基、异丙基、叔丁基、异丁基、特戊基、环丙基、环戊基或环己基中的一种;
55、最优选的,r1和r2分别独立地选自叔丁基或特戊基。
56、优选的,环c和环d中的至少一个具有如式(c)所示的结构:
57、
58、式(c)中,所述z5、z6、z7和z8分别独立地选自cr5或n,所述r5独立地选自氢或者卤素、氰基、硝基、羟基、氨基、c1~c20直链或支链烷基、c3~c20环烷基、c1~c20烷氧基、c1~c20烷基硅基、c6~c30芳基氨基、c3~c30杂芳基氨基、c6~c30芳氧基、c3~c30杂芳氧基、c6~c60芳基或c3~c60杂芳基中的一种或两种的组合,所述相邻的两个r5之间连接成环或者不连接;
59、优选的,所述z5、z6、z7和z8分别独立地选自cr5;
60、再优选的,所述z5、z6、z7和z8分别独立地选自cr5,且该r5选自氢或者c1~c20直链或支链烷基、c3~c20环烷基、c6~c60芳基或c3~c60杂芳基中的一种或两种的组合;
61、更优选的,所述z5、z6、z7和z8分别独立地选自cr5,且该r5选自氢。
62、优选的,具有如下式(1-3)所示的结构:
63、
64、式(1-3)中,r1、r2、l1的定义均与在式(1)中的定义相同;
65、z1、z2、z3、z4、z1’、z2’、z3’分别独立地选自cr4,所述r4选自氢、未取代或r'取代的c1~c20直链或支链烷基、未取代或r'取代的c3~c20环烷基、氰基、未取代或r'取代的c6~c30芳基氨基、未取代或r'取代的c3~c30杂芳基氨基、未取代或r'取代的c6~c60芳基、未取代或r'取代的c3~c60杂芳基中的至少一种,所述相邻的两个r4之间连接成环或者不连接;
66、所述r'各自独立地选自c1~c10直链或支链烷基、c3~c10环烷基、c1~c10烷氧基、c1~c10氰基、c6~c30芳基氨基、c3~c30杂芳基氨基、c6~c30芳基、c3~c30杂芳基中的一种或两种的组合。
67、优选的,所述z2、z2’分别独立地选自cr4,所述r4选自取代或未取代的c1~c10直链或支链烷基、取代或未取代的c3~c10环烷基中的一种;
68、优选的,所述z1、z2、z3、z4、z1’、z2’、z3’分别独立地选自cr4,且z2、z2’分别独立为cr4中的r4选自取代或未取代的c1~c10直链或支链烷基、取代或未取代的c3~c10环烷基中的一种;
69、再优选的,所述z1、z2、z3、z4、z1’、z2’、z3’分别独立地选自cr4,且z2、z2’分别独立为cr4中的r4选自取代或未取代的c1~c10链状烷基、取代或未取代的c3~c10环烷基中的一种,z1、z3、z4、z1’、z3’分别独立为cr4中的r4为氢;
70、最优选的,所述z1、z2、z3、z4、z1’、z2’、z3’分别独立地选自cr4,且z2、z2’分别独立为cr4中的r4选自甲基、乙基、异丙基、叔丁基、异丁基、特戊基、环丙基、环戊基或环己基,z1、z3、z4、z1’、z3’分别独立为cr4中的r4为氢。
71、再优选的,本发明的有机化合物具有如下式(1-3-1)所示的结构:
72、
73、最优选的,本发明的有机化合物具有如下式(1-4-1)、(1-4-2)或(1-4-3)所示的结构:
74、
75、其中,r1和r2的定义均与在式(1-3)中的定义相同,r41、r42、r41‘、r42‘、r41‘’和r42‘’的定义均与r4定义相同;
76、优选的,r5具有如式(1-4-1)所示的结构。
77、更进一步的,本发明的有机化合物可以优选出下述所示的具体结构化合物m1至m102,这些化合物仅为代表性的,并不限定本发明的范围:
78、
79、
80、
81、
82、
83、
84、本发明化合物的制备工艺简单易行,原料易得,适合于量产放大,非常适用于工业应用。
85、本发明化合物引入l1键连使得分子刚性更强,发光效率更高,b原子对位咔唑由于空间位阻作用可以抑制分子聚集,有利于寿命提升,同时由于咔唑基团具有良好的空穴传输性能,且homo能级更深,能防止载流子捕获,有助于降低电压。
86、作为本发明的另一个方面,还提供了一种如上所述的化合物在有机电致发光器件中的应用。具体说,本发明的上述化合物,具有优异的发光性能,能够给予三线态激子而实现较高的发光效率,同时基于其优良的载流子传输效率,适合作为发光染料使用。
87、当然,由于本发明的化合物也可以作为敏化剂与主体材料和染料一起实现良好的发光层。其应用的器件包括但不限于有机电致发光器件、光学传感器、太阳能电池、照明元件、有机薄膜晶体管、有机场效应晶体管、有机薄膜太阳能电池、信息标签、电子人工皮肤片材、片材型扫描器或电子纸,优选为有机电致发光器件。
88、本发明的还提供一种有机电致发光器件,所述有机电致发光器件包括第一电极、第二电极和插入所述第一电极和第二电极之间的至少一层或多个发光功能层,所述发光功能层中含有至少一种本发明所述的化合物。
89、本发明的有机电致发光器件,结构与现有的器件一致,例如包括阳极层、多个发光功能层和阴极层;所述多个发光功能层至少包括发光层,其中发光层中含有本发明的上述有机化合物。
90、采用本发明化合物制备的oled器件具有低启动电压、高发光效率和更优的使用寿命,能够满足当前面板、显示器制造企业对高性能材料的要求。
- 还没有人留言评论。精彩留言会获得点赞!