多酶偶联转化芳香族化合物的方法
本发明涉及生物化学领域,具体涉及一种多酶偶联转化芳香族化合物的方法。
背景技术:
1、多环芳香烃(polycyclic aromatic hydrocarbons,pah)是一类结构中由多个苯环组成的化合物,具有致癌性、致突变活性,在世界范围内受到严格的检疫。多环芳香烃(pah)大多是化石能源的副产品。由于化石能源是人类社会经济活动的能源基础,因此在可预见的未来,pah危害仍然受到广泛的关注。由于π电子共轭,芳香烃类化合物的分子势能较低,化学性质异常的稳定。而且芳香类化合物是非极性物质,大多数微溶或不溶于水。随着结构中苯环个数的增加,芳香烃类化合物的稳定性越强,极性越弱。所以,芳香类物质的降解是一个缓慢、复杂的过程。
2、萘是结构最简单的pah类物质,由两个苯环构成分子结构。萘及其衍生物都是重要的化工原料,在杀虫剂合成、印染和橡胶等工艺中具有广泛的应用。石油轻质化和煤焦化过程中可以产生大量含有萘及其衍生物的轻质循环油(lco),原油产业lco的年产量为5000万吨。lco是有价值的物质资源,裂解之后生成轻质芳烃(苯、甲苯和二甲苯),同时lco也是生态和健康的重大威胁。基于石油化工的可持续发展、以及环境保护理念的贯彻,萘等芳香烃的产生、治理都受到了严格的监管。然而,石化行业中产生的萘等芳香环物质主要使用高温、高压环境中的金属催化裂解,这种方法工艺复杂,并存在高污染、高耗能的缺点。相比较而言,生物法裂解pah能耗低,环境友好。
3、化石能源使用引起的另一个严重的环境威胁就是co2排放和温室效应。由于温室效应全球气候反常,极端的气象灾害发生的频率明显的增加。因此,减少co2的排放或者提高co2固定效率成为迫切的需求。通过非氧化型羧化酶催化,在酚类物质的羟基邻位插入羧基(kolbe–schmitt反应)是一类典型的固碳反应。kolbe–schmitt反应的逆反应显著,反应的转化率非常的低,通常使用高温、高压(~90bar,120–300℃),提高反应的转化率。这种工艺的能耗高,污染严重,而且碳排放非常的明显。酶催化这一过程,可以在温和的条件下进行,不需要大量的能量输入,但是逆反应明显,转化率低的问题难以避免。如果要提高酶催化反应固定co2的效率,必须解决逆反应的限制。
4、邻羧基苯甲醛是合成清热阵痛药物的一种重要的中间体。通常邻羧基苯甲醛由苯酚经溴化、水解而得。将苯酚加热、通入溴反应,然后加入水,进行水解,冷却,析出邻羧基苯甲醛。该工艺的步骤繁琐、可控性差,邻羧基苯甲醛的收率低、纯度差。邻苯二甲酸是燃料、聚酯树脂、涤纶、药物及增塑剂的中间体。传统上邻苯二甲酸的制备工艺比较复杂,使用林甲基苯甲酸、邻二甲苯或萘为原料,经过金属催化和强氧化剂制备。萘可用于制备邻羧基苯甲醛和邻苯二甲酸,然而工艺安全性和经济性还要进一步提高。
技术实现思路
1、本发明的目的是提供一种多酶偶联转化芳香族化合物的方法。
2、第一方面,本发明要求保护一种芳香族化合物的开环方法。
3、本发明要求保护的芳香族化合物的开环方法,可包括如下步骤:
4、(a1)芳香族化合物经单加氧酶催化,反应生成对应酚类化合物;
5、(a2)所述酚类化合物经羧化酶催化,反应生成含羧基芳香族化合物;
6、(a3)所述含羧基芳香族化合物经双加氧酶催化,反应生成羧酸类化合物;
7、(a4)所述羧酸类化合物经醛缩酶催化,反应生成丙酮酸和芳香醛酸类化合物;
8、(a5)所述丙酮酸和芳香醛酸类化合物经脱氢酶催化,反应生成二元羧酸类化合物。
9、在所述方法中,若所述芳香族化合物含有酚羟基,则跳过步骤(a1),直接进行步骤(a2)。
10、在所述方法中,各种酶的催化反应通过如下任一方式进行:1)向反应体系中直接加入相应酶;2)向反应体系中加入能够表达相应酶的细胞。
11、在本发明的具体实施方式中,能够表达所述单加氧酶的细胞为能够表达所述单加氧酶的大肠杆菌,如bl21 gold(de3);能够表达所述羧化酶的细胞为能够表达所述羧化酶的大肠杆菌,如bl21 gold(de3);能够表达所述双加氧酶的细胞为能够表达所述双加氧酶的大肠杆菌,如bl21 gold(de3);能够表达所述醛缩酶的细胞为能够表达所述醛缩酶的大肠杆菌,如bl21 gold(de3);能够表达所述脱氢酶的细胞为能够表达所述脱氢酶的大肠杆菌,如bl21 gold(de3)。
12、在步骤(a1)中,需要以nad(p)h提供还原力。
13、进一步地,所述以nad(p)h提供还原力可通过如下任一方式实现:1)向反应体系中直接加入nad(p)h;2)在所述反应体系中形成辅酶nad(p)h/nad(p)+循环。
14、更进一步地,在所述反应体系中形成辅酶nad(p)h/nad(p)+循环可通过如下任一方式实现:1)向反应体系中加入醇脱氢酶adh和nad(p)+;2)向反应体系中加入能够表达醇脱氢酶adh的细胞和nad(p)+;3)向反应体系中加入醇脱氢酶adh和nad(p)h;4)向反应体系中加入能够表达醇脱氢酶adh的细胞和nad(p)h;5)当步骤(a1)和步骤(a5)在同一反应体系中完成时,向反应体系中加入nad(p)h或nad(p)+。对于5),单加氧酶催化可使nad(p)h转化为nad(p)+,脱氢酶催化可使nad(p)+转化为nad(p)h,步骤(a1)有单加氧酶,步骤(a5)有脱氢酶,因此当步骤(a1)与步骤(a5)在同一反应体系中可以形成辅酶循环,只需再提供nad(p)h或者nad(p)+即可。下同。
15、在本发明的具体实施方式中,所述能够表达醇脱氢酶adh的细胞为能够表达醇脱氢酶adh的大肠杆菌,如bl21 gold(de3)。所述能够表达醇脱氢酶adh的细胞在所述反应体系中的加入量为0.5g细胞湿重/ml,nad(p)+或nad(p)h的加入量为30mm。
16、在步骤(a2)中,以hco3-或co2作为另一底物。
17、在步骤(a5)中,所述反应需要nad(p)+。
18、进一步地,所述反应中的nad(p)+可通过如下任一方式引入:1)向反应体系中直接加入nad(p)+;2)在所述反应体系中形成辅酶nad(p)h/nad(p)+循环。
19、更进一步地,在所述反应体系中形成辅酶nad(p)h/nad(p)+循环可通过如下方式实现:1)向反应体系中加入nad(p)h氧化酶和nad(p)+;2)向反应体系中加入nad(p)h氧化酶和nad(p)h;3)当步骤(a1)和步骤(a5)在同一反应体系中完成时,向反应体系中加入nad(p)h或nad(p)+。
20、在本发明的具体实施方式中,所述nad(p)h氧化酶(nox)的加入量为4.5u/ml,nad(p)+的加入量为0.5mm。
21、其中,所述芳香族化合物可为芳香烃化合物。
22、进一步地,所述芳香烃化合物可为多环芳香烃;
23、更进一步地,所述多环芳香烃可为萘。
24、在本发明的具体实施方式中,所述芳香族化合物为萘。
25、第二方面,本发明要求保护一种降解萘和/或固定co2的方法。
26、本发明要求保护的降解萘和/或固定co2的方法,可包括如下步骤:
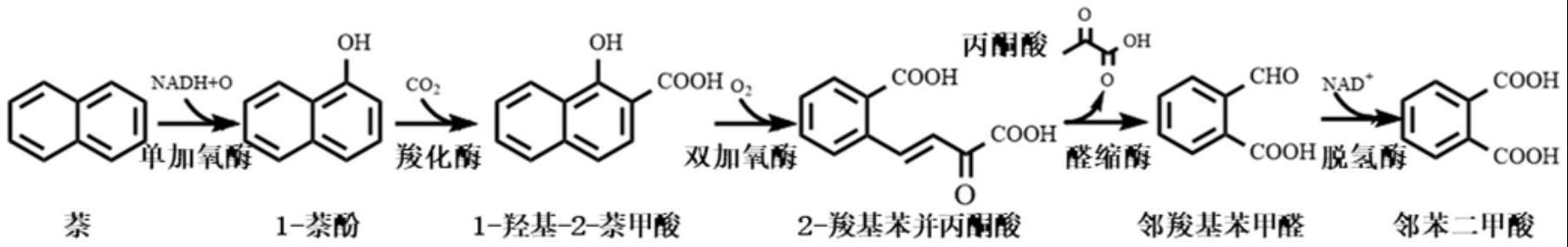
27、(a1)萘经单加氧酶催化,反应生成1-萘酚;
28、(a2)1-萘酚经羧化酶催化,反应生成1-羟基-2-苯甲酸;
29、(a3)1-羟基-2-苯甲酸经双加氧酶催化,反应生成2-羧基苯并丙酮酸;
30、(a4)2-羧基苯并丙酮酸经醛缩酶催化,反应生成邻羧基苯甲醛;
31、(a5)邻羧基苯甲醛经脱氢酶催化,反应生成邻苯二甲酸。
32、
33、在步骤(a1)中,需要以nad(p)h提供还原力。
34、进一步地,所述以nad(p)h提供还原力可通过如下任一方式实现:1)向反应体系中直接加入nad(p)h;2)在所述反应体系中形成辅酶nad(p)h/nad(p)+循环。
35、更进一步地,在所述反应体系中形成辅酶nad(p)h/nad(p)+循环可通过如下任一方式实现:1)向反应体系中加入醇脱氢酶adh和nad(p)+;2)向反应体系中加入能够表达醇脱氢酶adh的细胞和nad(p)+;3)向反应体系中加入醇脱氢酶adh和nad(p)h;4)向反应体系中加入能够表达醇脱氢酶adh的细胞和nad(p)h;5)当步骤(a1)和步骤(a5)在同一反应体系中完成时,向反应体系中加入nad(p)h或nad(p)+。对于5),单加氧酶催化可使nad(p)h转化为nad(p)+,脱氢酶催化可使nad(p)+转化为nad(p)h,步骤(a1)有单加氧酶,步骤(a5)有脱氢酶,因此当步骤(a1)与步骤(a5)在同一反应体系中可以形成辅酶循环,只需再提供nad(p)h或者nad(p)+即可。
36、在本发明的具体实施方式中,所述能够表达醇脱氢酶adh的细胞为能够表达醇脱氢酶adh的大肠杆菌,如bl21 gold(de3)。所述能够表达醇脱氢酶adh的细胞在所述反应体系中的加入量为0.5g细胞湿重/ml,nad(p)+或nad(p)h的加入量为30mm。
37、在步骤(a2)中,以hco3-或co2作为另一底物。
38、在所述方法中,各种酶的催化反应可通过如下任一方式进行:1)向反应体系中直接加入相应酶;2)向反应体系中加入能够表达相应酶的细胞。
39、在步骤(a5)中,所述反应需要nad(p)+。
40、进一步地,所述反应中的nad(p)+可通过如下任一方式引入:1)向反应体系中直接加入nad(p)+;2)在所述反应体系中形成辅酶nad(p)h/nad(p)+循环。
41、更进一步地,在所述反应体系中形成辅酶nad(p)h/nad(p)+循环可通过如下方式实现:1)向反应体系中加入nad(p)h氧化酶和nad(p)+;2)向反应体系中加入nad(p)h氧化酶和nad(p)h;3)当步骤(a1)和步骤(a5)在同一反应体系中完成时,向反应体系中加入nad(p)h或nad(p)+。
42、在本发明的具体实施方式中,所述nad(p)h氧化酶(nox)的加入量为4.5u/ml,nad(p)+的加入量为0.5mm。
43、在所述方法中,步骤(a1)-(a3)可以在同一个反应体系中经一步反应完成,所述反应体系记为反应体系i。
44、进一步地,所述反应体系i中含有1)萘、2)单加氧酶或能够表达所述单加氧酶的细胞、3)羧化酶或能够表达所述羧化酶的细胞、4)双加氧酶或能够表达所述双加氧酶的细胞、5)nad(p)h、6)hco3-或co2、7)反应缓冲液i。
45、更进一步地,在所述反应体系i中,萘的终浓度为15mm、nad(p)h的终浓度为60mm、hco3-的终浓度为50mm或在反应过程中向所述反应体系i中持续性通入co2。所述单加氧酶0.5mg/ml或能够表达所述单加氧酶的细胞0.5g细胞湿重/ml、所述羧化酶0.03-1u/ml(如1u/ml、0.03u/ml、0.14u/ml)或能够表达所述羧化酶的细胞0.5g细胞湿重/ml、所述双加氧酶9u/ml或能够表达所述双加氧酶的细胞0.5g细胞湿重/ml;余量为所述反应缓冲液i。
46、更进一步地,所述反应缓冲液i的ph可为6.5-8.0(如ph7.0-7.5)。具体可为磷酸钾缓冲液(ph7.0或ph7.5,100mm)。
47、更进一步地,所述反应的温度可为25-35℃(如30℃),反应时间为可3-12h(如12h)。
48、在所述方法中,步骤(a4)-(a5)可以在同一个反应体系中经一步反应完成,所述反应体系记为反应体系ii。
49、进一步地,所述反应体系ii中含有1)2-羧基苯并丙酮酸、2)醛缩酶或能够表达所述醛缩酶的细胞、3)脱氢酶或能够表达所述脱氢酶的细胞、4)nad(p)h、5)khco3、6)反应缓冲液ii。
50、在本发明的具体实施方式中,所述反应体系ii中还含有nad(p)h氧化酶,但是nad(p)h氧化酶不是必须的,其作用是产生nad(p)+,具体是脱氢酶催化的同时会将nad(p)+转化为nad(p)h,如果nad(p)+不够需要nad(p)h氧化酶催化nad(p)h来产生。
51、更进一步地,在所述反应体系ii中,2-羧基苯并丙酮酸的终浓度为10mm、nad(p)h的终浓度为15mm、khco3的终浓度为50mm。所述醛缩酶的浓度为0.75mg/ml、所述脱氢酶的浓度为18u/ml;余量为所述反应缓冲液ii。
52、在本发明的具体实施方式中,在所述反应体系ii中,所述nad(p)h氧化酶的浓度为4.5u/ml。
53、更进一步地,所述反应缓冲液ii的ph为6.5-8.0(如ph7.0-7.5)。具体可为磷酸钾缓冲液(ph7.0或ph7.5,100mm)。
54、更进一步地,所述反应的温度可为25-35℃(如30℃),反应时间为3-12h(如5.5h)。
55、在所述方法中,步骤(a2)-(a5)可以在同一个反应体系中经一步反应完成,所述反应体系记为反应体系iii。
56、进一步地,所述反应体系iii中含有1)1-萘酚、2)羧化酶或能够表达所述羧化酶的细胞、3)双加氧酶或能够表达所述双加氧酶的细胞、4)醛缩酶或能够表达所述醛缩酶的细胞、5)脱氢酶或能够表达所述脱氢酶的细胞、6)nad(p)h氧化酶或能够表达所述nad(p)h氧化酶的细胞、7)nad(p)+、8)khco3、9)反应缓冲液iii。
57、更进一步地,在所述反应体系iii中,所述1-萘酚的终浓度为7.5mm、所述nad(p)+的终浓度为0.5mm、所述khco3的终浓度为90mm。所述羧化酶的浓度为所述羧化酶0.03-1u/ml(如1u/ml、0.03u/ml、0.14u/ml)或能够表达所述羧化酶的细胞0.5g细胞湿重/ml、所述双加氧酶9u/ml或能够表达所述双加氧酶的细胞0.5g细胞湿重/ml、所述醛缩酶的浓度为0.75mg/ml、所述脱氢酶的浓度为18u/ml、所述nad(p)h氧化酶的浓度为4.5u/ml;余量为所述反应缓冲液iii。
58、更进一步地,所述反应缓冲液iii的ph为6.5-8.0(如ph7.0-7.5)。具体可为磷酸钾缓冲液(ph7.0或ph7.5,100mm)。
59、更进一步地,所述反应的温度为25-35℃(如30℃),反应时间为3-12h(如12h)。
60、第三方面,本发明要求保护如下任一方法:
61、方法i:一种以萘为底物生成邻羧基苯甲醛的方法,包括前文第二方面所述方法的步骤(a1)-(a4);
62、方法ii:一种以萘为底物生成邻苯二甲酸的方法,包括前文第二方面所述方法的步骤(a1)-(a5);
63、方法iii、一种以1-萘酚为底物生成邻羧基苯甲醛的方法,包括前文第二方面所述方法的步骤(a2)-(a4);
64、方法iv:一种以1-萘酚为底物生成邻苯二甲酸的方法,包括前文第二方面所述方法的步骤(a2)-(a5)。
65、第四方面,本发明要求保护成套酶。
66、本发明要求保护的成套酶为如下(b1)或(b2)或(b3)或(b4):
67、(b1)由羧化酶、双加氧酶和醛缩酶组成;
68、(b2)由单加氧酶、醇脱氢酶adh、羧化酶、双加氧酶和醛缩酶组成;
69、(b3)由羧化酶、双加氧酶、醛缩酶、脱氢酶和nad(p)h氧化酶组成;
70、(b4)由单加氧酶、醇脱氢酶adh、羧化酶、双加氧酶、醛缩酶、脱氢酶和nad(p)h氧化酶组成。
71、第五方面,本发明要求保护成套细胞。
72、本发明要求保护的成套细胞,为如下(c1)或(c2)或(c3)或(c4):
73、(c1)由能够表达羧化酶的细胞、能够表达双加氧酶的细胞、能够表达醛缩酶的细胞组成;
74、(c2)由能够表达单加氧酶细胞、能够表达醇脱氢酶adh细胞、能够表达羧化酶的细胞、能够表达双加氧酶的细胞、能够表达醛缩酶的细胞组成;
75、(c3)由能够表达羧化酶的细胞、能够表达双加氧酶的细胞、能够表达醛缩酶的细胞、能够表达脱氢酶的细胞和能够表达nad(p)h氧化酶的细胞组成;
76、(c4)由能够表达单加氧酶的细胞、能够表达醇脱氢酶adh的细胞、能够表达羧化酶的细胞、能够表达双加氧酶的细胞、能够表达醛缩酶的细胞、能够表达脱氢酶的细胞和能够表达nad(p)h氧化酶的细胞组成。
77、第六方面,本发明要求保护如下p1-p2中任一应用:
78、p1、前文第一方面所述方法或前文第四方面所述成套酶或前文第五方面所述成套细胞在降解芳香族化合物和/或固定co2和/或制备邻羧基苯甲醛和/或邻苯二甲酸中的应用;
79、p2、前文第一方面所述方法或前文第四方面所述成套酶或前文第五方面所述成套细胞在降解萘和/或固定co2和/或制备邻羧基苯甲醛和/或邻苯二甲酸中的应用。
80、在上述各方面中,所述单加氧酶可为来源于巨大芽孢杆菌(bacillusmegaterium)的单加氧酶突变体[p450 bm-3(a74g/f87v/l188q)]。进一步地,所述来源于巨大芽孢杆菌(bacillus megaterium)的单加氧酶突变体[p450 bm-3(a74g/f87v/l188q)]的氨基酸序列如seq id no.1所示。
81、在上述各方面中,所述羧化酶可为来源于米曲霉(aspergillus oryzae)的羧化酶,来源于根瘤菌(rhizobium sp.)的羧化酶,或来源于念珠毛孢子菌(trichosporonmoniliiforme)的羧化酶。进一步地,所述来源于米曲霉(aspergillus oryzae)的羧化酶的氨基酸序列如seq id no.2所示;所述来源于根瘤菌(rhizobium sp.)的羧化酶的氨基酸序列如seq id no.3所示;所述来源于念珠毛孢子菌(trichosporon moniliiforme)的羧化酶的氨基酸序列如seq id no.4所示。
82、在上述各方面中,所述双加氧酶可为来源于范巴伦氏分枝杆菌(mycobacteriumvanbaalenii pyr-1)的双加氧酶。进一步地,所述来源于范巴伦氏分枝杆菌(mycobacterium vanbaalenii pyr-1)的双加氧酶的氨基酸序列如seq id no.5所。
83、在上述各方面中,所述醛缩酶可为来源于恶臭假单胞菌(pseudomonas putida)的醛缩酶。进一步地,所述来源于恶臭假单胞菌(pseudomonas putida)的醛缩酶的氨基酸序列如seq id no.6所示。
84、在上述各方面中,所述脱氢酶可为来源于诺卡氏菌(nocardioides sp.kp7)的脱氢酶。进一步地,所述来源于诺卡氏菌(nocardioides sp.kp7)的脱氢酶的氨基酸序列如seq id no.7所示。
85、在上述各方面中,所述nad(p)h氧化酶可为来源于副兰乳杆菌(lactiplantibacillus pentosus)的nad(p)h氧化酶。进一步地,所述来源于副兰乳杆菌(lactiplantibacillus pentosus)的nad(p)h氧化酶的氨基酸序列如seq id no.8所示。
86、在上述各方面中,所述醇脱氢酶adh的氨基酸序列如seq id no.17所示。
87、在本发明中,所述单加氧酶、所述羧化酶、所述双加氧酶、所述醛缩酶、所述脱氢酶和nad(p)h氧化酶均是利用大肠杆菌作为宿主菌进行原核表达,然后进行ni柱纯化后得到的。具体可按照包括如下步骤的方法制备得到的:将表达所述单加氧酶、所述羧化酶、所述双加氧酶、所述醛缩酶、所述脱氢酶或nad(p)h氧化酶的大肠杆菌(如bl21 gold(de3))用终浓度为50μm的iptg进行诱导表达,表达条件为20~30℃诱导24h;离心收集细胞,重悬后破碎细胞,离心收集上清,过滤后进行ni柱纯化,脱盐,冷冻干燥,即得。
88、本发明公开了一种co2固定和萘裂解偶联反应的方法,该方法以羧化-双加氧偶联反应为核心,克服了酶催化羧化反应的热力学可逆性,极大地提高了固定co2的效率,并以此为核心搭建了新的萘降解反应路径,萘经过加氧酶生成1-萘酚,再经过羧化-双加氧偶联反应生成2-羧基苯并丙酮酸,再经过醛缩反应生成邻羧基苯甲醛或醛缩-脱氢偶联反应生成邻苯二甲酸,实现了萘的裂解开环和co2固定,以及邻羧基苯甲醛和邻苯二甲酸的制备。
89、与现有的非氧化型羧化反应相比,本发明具有以下优势:
90、1、通过羧化酶和加氧酶偶联,消除了产物抑制,羧化酶催化反应在正常的环境条件下即可进行,加大降低了羧化酶固定c的成本,提高了效率。
91、2、以萘为底物,构建了新的反应路径,将萘的降解和co2的固定偶联起来。
92、3、以萘为底物,设计了一种绿色、温和的合成邻羧基苯甲醛和邻苯二甲酸的方法。
93、4、本发明方法中不依赖底物和温度的驱动,反应条件温和、操作便利。
- 还没有人留言评论。精彩留言会获得点赞!