一种高区域高立体选择性的-4-烃基-4-氨基-2-氟-2-丁烯酸酯的合成方法
1.本发明涉及一种(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物的合成方法,属于单氟烯基羧酸酯类化合物技术领域。
背景技术:
2.由于氟原子独特的性质,具有潜在生物活性的含氟有机化合物的合成一直备受化学家和药物学家们的关注。单氟烯基结构作为酰胺键的生物电子等排体(scheme 1)由于其在体内不易被体内的酶识别水解,且分子中c=c双键存在不同的z或e构型,其作为多肽模拟物时可使多肽模拟物存在不同的空间结构,从而可以更好地研究其生物活性,具有更佳的模拟效果。此外,由于氟原子的引入,可以形成氢键,可提高药物与作用靶点的结合力,从而增强药物的活性。目前单氟烯基类化合物已被广泛应用于各种酶抑制剂和多肽模拟物的研究中(scheme 2)。
[0003][0004]
scheme 1酰胺键的生物电子等排体-单氟烯基结构
[0005][0006]
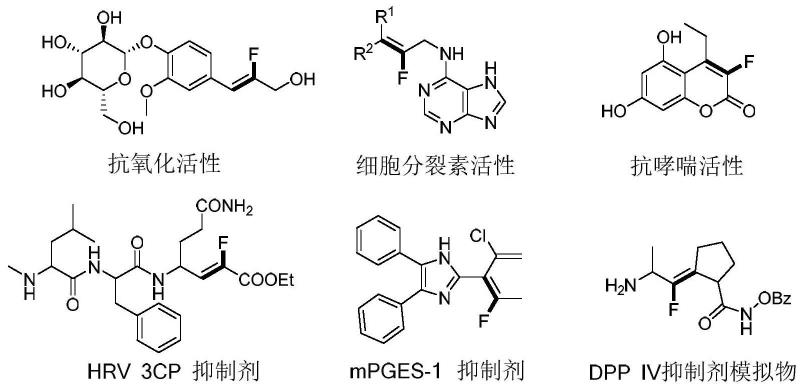
scheme 2具有生物活性的单氟烯基类化合物
[0007]
虽然现有技术中已有单氟烯基羧酸酯类化合物的合成,但是也存在制备工艺复杂,区域选择性和立体选择性差,产率低,底物普适性较窄,反应条件比较苛刻等缺陷。
技术实现要素:
[0008]
针对上述技术问题,本发明目的提供一种(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物合成方法。
[0009]
本发明提供了一种(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物的合成方法,其结构通式如下式(1)所示:
[0010][0011]
其中:取代基r1烷基或芳基,优选为苯基或取代的苯基,r2为h,乙基,苯基,r3为苯基、4-甲氧基苯基、4-二甲氨基苯基,4-三氟甲基苯基和2-萘基,或r2r3连接成环戊烷基;
[0012]
该类化合物的合成方法包括以下步骤:以化合物(2)α,α-二氟亚甲基-β-烯基羧酸酯为原料,加入胺(3),碱,钯催化剂和配体,发生脱氟氨基化反应,制得所述(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物,其反应过程如下式表述:
[0013][0014]
化合物(2)中,取代基r1烷基或芳基,r2为h,烷基或芳基,r3为烷基,芳基或r2r3连接成环烷基;
[0015]
所述金属钯催化剂为二价钯或零价钯,优选二价钯pd(oac)2。
[0016]
所述的配体为膦配体,优选dpephos。
[0017]
所述的碱为有机碱,优选et3n。
[0018]
所述α,α-二氟亚甲基-β-烯基羧酸酯与胺(3)的摩尔比为1∶(1~4),优选1∶2。
[0019]
所述钯催化剂与α,α-二氟亚甲基-β-烯基羧酸酯的摩尔比为(0.02~0.10)∶1,优选0.05∶1。
[0020]
所述配体与α,α-二氟亚甲基-β-烯基羧酸酯的摩尔比为(0.03~0.3)∶1,优选0.075∶1。
[0021]
所述碱与α,α-二氟亚甲基-β-烯基羧酸酯的摩尔比为(1~6)∶1,优选2∶1。
[0022]
所述脱氟氨基化反应的温度为常温10~40℃,优选常温。
[0023]
所述脱氟氨基化反应在惰性气体气氛中进行。
[0024]
本发明方法合成的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物可进一步采用柱层析的方法纯化。
[0025]
由于单氟烯基结构是酰胺键的生物电子等排体,因此许多含单氟烯基结构的化合物已被证明有多种药理活性,如抗癌、抗菌、抗hiv病毒以及治疗糖尿病等活性。因此通过本合成方法有望合成结构多样具有潜在生物活性的含氟化合物。本发明紧密围绕上述问题,通过金属钯催化下α,α-二氟亚甲基-β-烯基羧酸酯的脱氟氨基化反应高选择性合成一系列新型多肽模拟物-(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物。
[0026]
技术效果:相对于现有技术,本发明(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯类化合物合成方法是一种高效、简单、高区域、高立体选择性的合成方法,该串联反应选择性地在c18h19
o2nf[m+h]
+
:300.1391,found:300.1394.
[0035]
实施例2
[0036]
操作同前,反应过程如下
[0037][0038]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率91%。
[0039][0040]1h nmr(400mhz,chloroform-d)δ7.49-7.42(m,2h),7.42-7.34(m,2h),7.36-7.29(m,1h),6.81-6.72(m,2h),6.64-6.55(m,2h),6.28(dd,j
h-f
=32.2hz,j=9.5hz,1h),5.41(d,j=9.5hz,1h),4.26(q,j=7.1hz,2h),3.89-3.78(br,1h),3.73(s,3h),1.31(t,j=7.2hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.4(d,j
c-f
=35.5hz),152.7,147.5(d,j
c-f
=259.6hz),140.5,129.0,128.1,126.7,121.7(d,j
c-f
=9.8hz),115.0,114.8,62.0,55.6,53.7(d,j
c-f
=2.6hz),14.1.
19
f nmr(376mhz,chloroform-d)δ-126.7(d,j
h-f
=32.1hz).ir:3382,3063,2992,2936,2904,2828,1711,1676,1512,1456,1400,1368,1316,1245,1181,1069,1034,1010,902,890,810,758,703,551,515cm-1
.hrms(maldi):m/z calcd.for c
19h20
o3nf[m]
+
:329.1424,found:329.1422.
[0041]
实施例3
[0042]
操作同前,反应过程如下
[0043][0044]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯如下式,收率91%。
[0045][0046]1h nmr(400mhz,chloroform-d)δ7.51-7.46(m,2h),7.43-7.37(m,2h),7.37-7.31(m,1h),6.81-6.57(m,4h),6.31(dd,j
h-f
=32.3hz,j=9.5hz,1h),5.44(d,j=9.6hz,1h),
4.28(q,j=7.1hz,2h),3.88-3.65(br,1h),2.84(s,6h),1.33(t,j=7.2hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.5(d,j
c-f
=35.6hz),147.5(d,j
c-f
=259.0hz),144.8,140.8,138.6,129.1,128.0,126.8,122.1(d,j
c-f
=9.9hz),115.5,115.3,62.0,53.8,42.0,14.1.
19
f nmr(376mhz,chloroform-d)δ-126.9(d,j
h-f
=32.2hz).ir:3375,3071,3027,2992,2936,2797,1716,1679,1524,1452,1373,1368,1316,1305,1261,1229,1181,1157,1057,1005,942,902,858,807,755,699,591,543,519cm-1
.hrms(maldi):m/z calcd.for c
20h23
o2n2f[m]
+
:342.1742,found:342.1738.
[0047]
实施例4
[0048]
操作同前,反应过程如下
[0049][0050]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率76%。
[0051][0052]1h nmr(400mhz,chloroform-d)δ7.51-7.41(m,6h),7.41-7.36(m,1h),6.67(d,j=8.5hz,2h),6.32(dd,j
h-f
=31.7hz,j=9.5hz,1h),5.55(dd,j=9.5,4.9hz,1h),4.50(d,j=5.0hz,1h),4.31(q,j=7.1hz,2h),1.36(t,j=7.1hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.3(d,j
c-f
=35.2hz),149.0,148.0(d,j
c-f
=261.5hz),139.5(d,j
c-f
=2.0hz),129.3,124.8(q,j
c-f
=270.5hz),120.0(q,j
c-f
=32.7hz),112.7,62.2,52.5(d,j
c-f
=3.2hz),14.1.
19
f nmr(376mhz,chloroform-d)δ-61.1,-125.8(d,j
h-f
=31.5hz).ir:3398,3063,3027,2984,2928,1728,1679,1616,1532,1492,1449,1397,1373,1325,1277,1241,1189,1165,1113,1005,898,826,766,699,651,587,500cm-1
.hrms(dart):m/z calcd.for c
19h18
o2nf4[m+h]
+
:368.1265,found:368.1268.
[0053]
实施例5
[0054]
操作同前,反应过程如下:
[0055][0056]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率90%。
[0057][0058]1h nmr(400mhz,chloroform-d)δ7.73-7.66(m,2h),7.62(d,j=8.3hz,1h),7.56-7.48(m,2h),7.46-7.40(m,2h),7.40-7.33(m,2h),7.27-7.22(m,1h),6.94(dd,j=8.8,2.4hz,1h),6.84(d,j=2.4hz,1h),6.36(dd,j
h-f
=32.0hz,j=9.5hz,1h),5.65(d,j=9.5hz,1h),4.46-4.16(m,3h),1.34(t,j=7.1hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.4(d,j
c-f
=35.3hz),148.0(d,j
c-f
=260.0hz),144.0,140.1(d,j
c-f
=2.1hz),134.8,129.2,129.1,128.3,127.9,127.6,126.8,126.5,126.3,122.6,121.2(d,j
c-f
=9.8hz),118.0,106.0,62.1,53.0(d,j
c-f
=2.8hz),14.1.
19
f nmr(376mhz,chloroform-d)δ-126.2(d,j
h-f
=32.0hz).ir:3394,3063,2994,2891,1716,1679,1627,1595,1528,1472,1398,1369,1333,1310,1278,1233,1187,1063,1015,923,891,829,807,747,702,634,595,475cm-1
.hrms(maldi):m/zcalcd.for c
22h19
o2nf[m-h]
+
:348.1400,found:348.1394.
[0059]
实施例6
[0060]
操作同前,反应过程如下:
[0061][0062]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率63%。
[0063][0064]1h nmr(400mhz,chloroform-d)δ7.43-7.38(m,2h),7.37-7.32(m,2h),7.30-7.25(m,1h),6.22(dd,j
h-f
=32.5hz,j=9.7hz,1h),4.78(d,j=9.7hz,1h),4.25(qd,j=7.1,3.3hz,2h),2.85-2.35(m,2h),1.49(p,j=7.2hz,2h),1.41-1.33(m,2h),1.30(t,j=7.1hz,3h),0.90(t,j=7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.7(d,j
c-f
=35.8hz),147.5(d,j
c-f
=257.9hz),141.4(d,j
c-f
=2.0hz),128.8,127.8,127.0,122.6(d,j
c-f
=9.5hz),61.8,57.3(d,j
c-f
=2.2hz),47.5,32.2,20.4,14.1,14.0.
19
f nmr(376mhz,chloroform-d)δ-128.7(d,j
h-f
=32.6hz).ir:3446,2963,2931,2866,1737,1671,1564,1454,1371,1308,1234,1149,1104,1074,962,880,793,700,625,428cm-1
.hrms(maldi):m/z calcd.for c
16h22
o2nf[m-h]
+
:278.1563,found:278.1551.
[0065]
实施例7
[0066]
操作同前,反应过程如下:
[0067][0068]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率70%。
[0069][0070]1h nmr(400mhz,chloroform-d)δ7.39(d,j=7.0hz,2h),7.34(t,j=7.5hz,2h),7.30-7.24(m,1h),6.20(dd,j
h-f
=32.6hz,j=9.7hz,1h),4.97(d,j=9.7hz,1h),4.25(qd,j=7.2,2.5hz,2h),2.44(ddt,j=10.2,6.4,3.8hz,1h),1.92(dt,j=10.9,3.1hz,2h),1.77-1.66(m,2h),1.58(dt,j=11.9,3.4hz,1h),1.30(t,j=7.2hz,3h),1.25-1.01(m,6h).
13
c nmr(101mhz,chloroform-d)δ160.7(d,j
c-f
=35.7hz),147.2(d,j
c-f
=257.6hz),128.8,127.7,127.0,123.1(d,j
c-f
=9.7hz),61.8,54.0,53.6(d,j
c-f
=2.3hz),34.0,33.5,26.1,25.0(d,jc-f
=5.8hz),14.1.
19
f nmr(376mhz,chloroform-d)δ-129.1(d,j
h-f
=32.6hz).ir:3444,3323,3084,3063,2981,2929,2853,2662,2597,1735,1673,1601,1491,1452,1395,1372,1310,1230,1191,1147,1121,1073,1028,1016,968,890,861,793,766,700,630,591,548,428cm-1
.hrms(maldi):m/z calcd.for c
18h23
o2nf[m-h]
+
:304.1709,found:304.1707.
[0071]
实施例8
[0072]
操作同前,反应过程如下:
[0073][0074]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率82%。
[0075][0076]1h nmr(400mhz,chloroform-d)δ7.40-7.32(m,2h),7.21-7.13(m,2h),6.98-6.84(m,2h),6.74(t,j=7.3hz,1h),6.65-6.59(m,2h),6.27(dd,j
h-f
=32.2,j=9.5hz,1h),5.43(d,j=9.5hz,1h),4.25(q,j=7.2hz,2h),4.03(br,1h),3.80(s,3h),1.30(t,j=
7.1hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.4(d,j
c-f
=35.5hz),159.4,147.5(d,j
c-f
=259.4hz),146.5,132.3(d,j
c-f
=2.0hz),129.3,127.9,121.7(d,j
c-f
=9.7hz),118.4,114.4,113.5,62.0,55.3,52.3(d,j
c-f
=2.9hz),14.1.
19
f nmr(376mhz,chloroform-d)δ-126.9(d,j
h-f
=32.1hz).ir:3398,3056,2931,2836,1734,1674,1602,1510,1461,1371,1312,1248,1176,1128,1106,1032,901,830,751,692,577,510cm-1
.hrms(maldi):m/z calcd.for c
19h19
o3nf[m-h]
+
:328.1337,found:328.1344.
[0077]
实施例9
[0078]
操作同前,反应过程如下:
[0079][0080]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率46%。
[0081][0082]1h nmr(400mhz,chloroform-d)δ7.13-7.05(m,2h),6.68-6.60(m,1h),6.50(d,j=7.5hz,2h),5.84(dd,j
h-f
=33.5hz,j=9.5hz,1h),4.28(dt,j=9.4,7.0hz,1h),4.17(q,j=7.4hz,2h),3.59(s,1h),1.72-1.60(m,1h),1.60-1.46(m,1h),1.41-1.27(m,4h),1.23(t,j=7.1hz,3h),0.84(t,j=7.0hz,3h).
13
c nmr(101mhz,chloroform-d)δ160.5(d,j
c-f
=35.9hz),148.2(d,j
c-f
=256.9hz),146.8,129.4,123.3(d,j
c-f
=10.2hz),117.9,113.0,61.9,48.3(d,j
c-f
=2.3hz),35.0(d,j
c-f
=2.1hz),27.9,22.5,14.1,14.0.
19
f nmr(376mhz,chloroform-d)δ-128.1(d,j
h-f
=33.4hz).ir:3399,3085,3055,3022,2958,2871,1730,1672,1602,1503,1466,1443,1394,1371,1314,1257,1207,1180,1145,1089,1062,1019,992,887,869,766,749,692,510cm-1
.hrms(dart):m/z calcd.for c
16h23
o2nf[m+h]
+
:280.1704,found:280.1707.
[0083]
实施例10
[0084]
操作同前,反应过程如下:
[0085][0086]
所得到的(z)-4-烃基-4-氨基-2-氟-2-丁烯酸酯其结构如下式,收率73%。
[0087][0088]1h nmr(400mhz,chloroform-d)δ7.44-7.39(m,2h),7.37-7.29(m,2h),7.29-7.23(m,1h),6.34(dd,j
h-f
=32.6hz,j=10.4hz,1h),4.81(d,j=10.3hz,1h),4.27(qd,j=7.2,1.4hz,2h),2.61(dq,j=14.3,7.2hz,2h),2.50(dq,j=13.7,7.0hz,2h),1.32(t,j=7.1hz,3h),1.00(t,j=7.1hz,6h).
13
c nmr(101mhz,chloroform-d)δ160.6(d,j
c-f
=35.9hz),148.2(d,j
c-f
=258.0hz),141.0(d,j
c-f
=2.2hz),128.5,127.8,127.5,120.6(d,j
c-f
=10.0hz),61.8,59.3,43.2,14.1,11.8.
19
f nmr(376mhz,chloroform-d)δ-128.6(d,j
h-f
=32.6hz).ir:3449,3084,3063,3028,2973,2936,2874,2820,1739,1673,1603,1494,1467,1452,1386,1372,1308,1238,1199,1178,1123,1102,1075,1028,894,861,840,785,764,744,717,700,628,573,483,429cm-1
.hrms(maldi):m/z calcd.for c
16h21
o2nf[m-h]
+
:278.1564,found:278.1551.
[0089]
显而易见的是,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1