CREPT在前列腺癌分期、监测进展和/或判断预后中的用途
crept在前列腺癌分期、监测进展和/或判断预后中的用途
技术领域
1.本公开涉及肿瘤诊断和肿瘤标记物领域,具体涉及crept在前列腺癌分期、监测进展和/或判断预后中的用途。
背景技术:
2.前列腺癌是老年男性的常见疾病,据美国国家肿瘤研究所和国家卫生统计中心数据,2012年,前列腺癌的发病率已超过肺癌,在男性恶性肿瘤占第一位。
3.前列腺癌最初大多是雄激素依赖型,在手术或者药物去势治疗后,雄激素水平急剧下降,但是仍有约70%的患者会进展为去势抵抗型前列腺癌 (castration-resistant prostate cancer,crpc)。患者一旦进入去势抵抗型前列腺癌阶段,癌细胞增殖加速,导致肿瘤进展或转移,病情恶化并最终可能会导致死亡。由雄激素依赖型前列腺癌进展为雄激素非依赖型前列腺癌是前列腺癌致死的首要原因,但其中的机制极其复杂且尚不明确。众多研究表明,雄激素受体(androgen receptor,ar)在雄激素依赖型和雄激素非依赖型前列腺中均呈高表达且在前列腺癌的进展过程中扮演关键作用。
4.引用文献1(d lu et al.,crept accelerates tumorigenesis by regulatingthe transcription of cell-cycle related genes.cancer cell.21:92-104,2012)公开了相比癌旁组织,肿瘤细胞周期相关蛋白(cell-cycle-related andexpression-elevated protein in tumor,crept)在前列腺癌组织中高表达,并且亦有研究发现crept与ar相互作用,通过调控ar信号通路的转录活性促进前列腺癌的发生与转移。
5.然而,前列腺癌的发生、发展涉及复杂的信号通路或机制,了解分子对某一信号通路的调控功能,无法预测该分子可以应用于疾病的诊断、治疗。并且,目前尚未有研究报道crept尤其是其表达水平与前列腺癌的分期、疾病进展和预后相关性的报道。
6.前列腺癌的诊断主要依靠直肠指检、血清psa浓度测定和经直肠超声引导下的前列腺穿刺活检。确诊前列腺癌需要获得组织病理学诊断,在前列腺空芯针穿刺活检标本中发现癌组织是确诊前列腺癌的最常见方法。直肠指检联合血清psa测定是目前公认的早期发现前列腺癌最佳的初筛方法。ct、 mri、ect骨扫描和pet等其它影像学检查方法则有助于获得更准确的前列腺癌临床分期。前列腺癌的分期标准依据的是国际抗癌联盟和美国癌症联合会联合制定的tnm分期系统。tnm分期系统将肿瘤按照原发肿瘤、区域淋巴结和远处转移来分期。原发肿瘤用t表示,t1期是指检查没有发现的前列腺肿瘤,t2期是指肿瘤局限在前列腺包膜以内,t3期是指肿瘤已经超出前列腺包膜或者侵犯精囊,但没有侵犯其他器官,t4期是肿瘤已经侵犯周围其他器官。区域淋巴结用n表示,n0期是指淋巴结没有转移,n1期是指淋巴结发现转移。远处表示用m表示,m0是指没有远处转移,m1是指有远处转移。在前列腺癌的病理分级方面,目前最常使用gleason评分系统,其采用5级、 10分制。前列腺癌组织被分为主要分级区和次要分级区,每区的gleason分值在1-5,即每个形态分为5级,分别计为1-5分。gleason评分是把主要分级区和次要分级区的gleason分值相加,形成癌组织分级常数。gleason 1级(简称1级):癌肿极为罕见。其边界很清楚,膨胀型生长,几乎不侵犯基
质,癌腺泡很简单,多为圆形,中度大小,紧密排列在一起,其胞浆和良性上皮细胞胞浆极为相近。gleason 2级(2级):癌肿很少见,多发生在前列腺移行区,癌肿边界不很清楚,癌腺泡被基质分开,呈简单圆形,大小可不同,可不规则,疏松排列在一起。gleason 3级(3级):癌肿最常见,多发生在前列腺外周区,最重要的特征是侵润性生长,癌腺泡大小不一,形状各异,核仁大而红,胞浆多呈碱性染色。gleason 4级(4级):癌肿分化差,浸润性生长,癌腺泡不规则融合在一起,形成微小乳头状或筛状,核仁大而红,胞浆可为碱性或灰色反应。gleason 5级(5级):癌肿分化极差,边界可为规则圆形或不规则状,伴有浸润性生长,生长型式为片状单一细胞型或者是粉刺状癌型,伴有坏死,癌细胞核大,核仁大而红,胞浆染色可有变化。可以看出,这些前列腺癌的分级和分期过程繁琐,方法较为复杂,而且只有专业人士才能准确判断。因此,仍有待开发更简便、有效、客观的前列腺癌分期的判断方法或辅助判断方法,例如通过标志物的表达水平判断或辅助判断分期、进展的变化趋势。
技术实现要素:
7.发明要解决的问题
8.基于现有技术中存在的上述问题,本公开的目的在于提供一种灵敏特异地确定前列腺癌分期、监测进展和/或判断预后的生物标志物,具体是, crept在前列腺癌分期、监测进展和/或判断预后中的用途。
9.用于解决问题的方案
10.在本公开的一些方面中,提供了确定受试者样本中crept的表达水平的试剂的以下(i)~(iii)中任一用途:
11.(i)在制备用于检测前列腺癌分期的试剂/试剂盒中的用途;
12.(ii)在制备用于监测前列腺癌进展的试剂/试剂盒中的用途;
13.(iii)在制备用于判断前列腺癌预后的试剂/试剂盒中的用途。
14.在一些实施方案中,所述前列腺癌分期包括区分非转移型前列腺癌和转移型前列腺癌。
15.在一些实施方案中,所述前列腺癌分期包括区分前列腺癌的分化程度和 /或侵袭性。
16.在一些优选的实施方案中,所述分化程度和/或侵袭性是由gleason分级系统确定的分化程度和/或侵袭性。
17.在一些实施方案中,将所述受试者样本中crept的表达水平与参考量相比较,确定所述受试者中的前列腺癌分期。
18.在一些实施方案中,所述的前列腺癌包括腺癌、导管腺癌、尿路上皮癌、鳞状细胞癌和腺鳞癌中的一种或多种。
19.在一些实施方案中,所述的受试者包括哺乳动物;优选地,所述的受试者为人。
20.在一些任选的实施方案中,当检测前列腺癌分期时,所述受试者包括患有前列腺癌的受试者;当监测前列腺癌进展时,所述受试者包括患有良性的前列腺增生性病变或患有前列腺癌的受试者;当判断前列腺癌预后时,所述受试者包括正患有或者曾经患有前列腺癌的受试者。
21.在一些实施方案中,所述样本包括前列腺组织。
22.在一些任选的实施方案中,当检测前列腺癌分期时,所述样本包括前列腺癌组织;当检测前列腺癌进展时,所述样本包括良性的前列腺增生性病变组织或前列腺癌组织;当判断前列腺癌预后时,所述样本包括前列腺癌组织。
23.在一些实施方案中,在基因水平或蛋白水平确定crept的表达水平;任选地,当在基因水平确定crept的表达水平时,所述试剂包括引物和探针中的一种或多种;或者,当在蛋白水平确定crept的表达水平时,所述试剂包括抗体。
24.在本公开的另一些方面中,提供了一种用于检测前列腺癌的分期或监测进展的系统,其中,所述系统包括检测装置、计算装置和输出装置;
25.所述检测装置包括进样器和检测器,所述进样器用于采集来自受试者的样本,所述检测器用于检测所述样本中crept的表达水平;
26.所述计算装置包括存储器和处理器,所述存储器中存储有计算机程序,所述处理器被配置为执行所述存储器中存储的计算机程序,以实现如下判别:
27.当检测前列腺癌的分期时,将所述样本中crept的表达水平与参考量相比较,判别所述样本对应的受试者的前列腺癌分期;
28.当监测前列腺癌的进展时,将来自同一受试者的不同时间采集的样本中 crept的表达水平相比较,或者将样本中crept的表达水平与参考量相比较,判别样本对应的受试者的前列腺癌是否进展。
29.在一些实施方案中,所述输出装置用于输出所述检测装置的检测结果和/或所述计算装置的判别结果,所述输出装置包括显示器、打印机和音频输出装置中的至少一种;所述计算装置包括电脑主机、中央处理器和网络服务器中的至少一种。
30.在本公开的另一些方面中,提供了一种检测前列腺癌分期的方法,其包括:
31.a)确定待测样本中crept的表达水平;
32.b)将在步骤a)中测定的crept的表达水平与一种或多种参考量比较;
33.c)基于在步骤b)中获得的信息对所述待测样本中前列腺癌进行分期。
34.在本公开的另一些方面中,提供了一种监测前列腺癌进展的方法,其包括:
35.a)确定第一样本中crept的表达水平;
36.b)将在步骤a)中测定的crept的表达水平与一种或多种参考量比较;或者测定在第二样本中crept的表达水平,并将所述第一样本中的crept的表达水平与所述第二样本中的crept的表达水平比较;
37.c)基于在步骤b)中获得的信息监测前列腺癌进展;
38.其中,所述第一样本和所述第二样本为来自同一受试者的不同时间采集的样本。
39.发明的效果
40.本公开发现了crept可以应用于前列腺癌分期、监测进展和预后判断,对于前列腺癌的诊断、治疗具有重要意义。
附图说明
41.图1a和图1b为crept在人(图1a)和小鼠(图1b)前列腺正常和癌组织中的免疫组化染色结果。
42.图2为在geo数据库(https://www.ncbi.nlm.nih.gov/geo/)中分析前列腺增生组
织、前列腺内皮瘤和前列腺癌组织中的crept表达量。
43.图3为在geo数据库中分析非转移型前列腺癌组织与转移型前列腺癌组织中crept表达量。
44.图4为在tcga数据库分析gleason值与crept表达量的相关性。
45.图5a为在人的前列腺癌组织芯片中通过免疫组织化学实验检测crept 表达量。
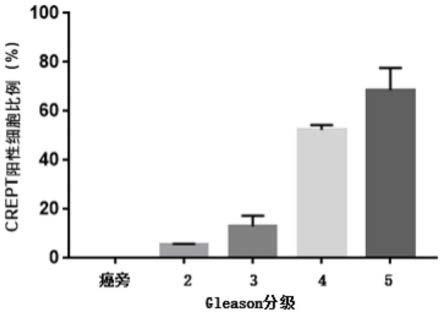
46.图5b是根据图5a免疫组化染色结果统计的crept阳性细胞数,选取3个视野,统计视野中crept阳性细胞数占总细胞数的比例,取平均值。
47.图6为tcga数据库中前列腺癌患者(n=593)crept低表达组(75%, n=366)和crept高表达组(25%,n=127)的无病生存率。
具体实施方式
48.以下,针对本公开的内容进行详细说明。以下所记载的技术特征的说明基于本公开的代表性的实施方案、具体例子而进行,但本公开不限定于这些实施方案、具体例子。需要说明的是:
49.本说明书中,使用“数值a~数值b”表示的数值范围是指包含端点数值 a、b的范围。
50.本说明书中,使用“基本上”或“实质上”表示与理论模型或理论数据的标准偏差在5%、优选为3%、更优选为1%范围以内。
51.本说明书中,使用“可以”表示的含义包括了进行某种处理以及不进行某种处理两方面的含义。
52.本说明书中,“任选的”或“任选地”是指接下来描述的事件或情况可发生或可不发生,并且该描述包括该事件发生的情况和该事件不发生的情况。
53.本说明书中,所提及的“一些具体/优选的实施方案”、“另一些具体/ 优选的实施方案”、“实施方案”等是指所描述的与该实施方案有关的特定要素(例如,特征、结构、性质和/或特性)包括在此处所述的至少一种实施方案中,并且可存在于其它实施方案中或者可不存在于其它实施方案中。另外,应理解,所述要素可以任何合适的方式组合在各种实施方案中。
54.本公开的术语“包括”和“具有”以及它们任何变形,意图在于覆盖不排他的包含。例如包含了一系列步骤的过程、方法、装置、产品或设备没有限定于已列出的步骤或模块,而是可选地还包括没有列出的步骤,或可选地还包括对于这些过程、方法、产品或设备固有的其它步骤。
55.在本公开中提及的“多个”是指两个或两个以上。“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b这三种情况。字符“/”一般表示前后关联对象是一种“或”的关系。
56.在本说明书中,术语“肿瘤”或“癌症”是指以肿瘤性或恶性细胞生长、增殖或转移为特征的任何医学病症,包括实体癌和如白血病的非实体癌。
57.在本说明书中,术语“前列腺癌”或“前列腺肿瘤”是指源于前列腺组织的癌症或肿瘤。
58.在本说明书中,在疾病(比如癌症或肿瘤)背景下的术语“阶段”是指指示疾病严重
性的疾病进展状态。
59.在本说明书中,术语“诊断”是指分子或病理状态、诸如癌症的疾病或病症的鉴定,或是指可能受益于特定治疗方案的癌症患者的鉴定。
60.在本说明书中,术语“分期”是指鉴定已经进展的疾病所处的具体阶段,在一些方面,“分期”是指用于将癌症(例如,前列腺癌)分级/描述的常用系统。在另一些方面,分期通常也是指确定肿瘤的范围和位置以开发适当的治疗策略并估计预后。具体地,分期是预测前列腺癌的严重程度及其进展,以及根据常规病程预计恢复前景的一种方法。
61.分期可以采用gleason分级系统。对于前列腺癌分期/分级,以gleason分级系统(gleason,d.f.,mellinger,g.t.,and veterans administration cooperativeurological research,g.(2017).prediction of prognosis for prostaticadenocarcinoma by combined histological grading and clinical staging.j urol 197,s134-s139.)应用的最为普遍,其是临床上治疗前列腺癌关键的参考指标之一(matoso,a.,and epstein,j.i.(2016).grading of prostate cancer:past, present,and future.curr urol rep 17,25.),同时也是最常用的前列腺癌评分/ 分期和预后系统。gleason分级系统采用与预后相关的5级、10分制,将一个视野下的经he染色的肿瘤组织按占总面积的多少分成主要形态和次要形态,每个形态分为5级,分别计为1-5分。最终,gleason分级的评分(值)为计算主要形态的分数与次要形态的分数之和。gleason总评分为2-4分属于分化良好癌;5-7分属于中等分化癌;8-10分属于较低分化癌。同时,2分是最无侵袭性的,10分是最有侵袭性的。在临床上,认为gleason总评分8-10极有可能为转移性前列腺癌。癌细胞可经血行、淋巴扩散或直接侵及邻近器官,如精囊腺。最常见的转移部位是淋巴结、肺和骨髓(alchin,d.r.,murphy,d.,andlawrentschuk,n.(2017).risk factors for gleason score upgrading followingradical prostatectomy.minerva urol nefrol 69,459-465.;humphrey,p.a.(2004). gleason grading and prognostic factors in carcinoma of the prostate.mod pathol 17,292-306.)。
62.在本说明书中,术语“预后”是指受益于治疗(比如癌症治疗)的益处的可能性的预测。在一些方面,预后通常涉及确定根据常规病程或病例的特性预计的恢复前景,例如确定发生前列腺癌的可能性、确定发生侵袭性前列腺癌的可能性、确定发生转移性前列腺癌的可能性和/或确定长期存活结果。在另一些方面,预后既包括判断疾病的特定后果(如康复、某种症状、体征、并发症),也包括提供时间线索(如预测某段时间内发生某种结局的可能性)。当从疾病演进过程的角度考虑时,预后包括例如缓解率、复发率、病残率。当从疾病终极状态的角度考虑时,预后包括例如治愈率、生存率、病死率。当从预后时间考虑时,预后包括例如近期病死率、远期病死率(参见刘振华主编的《肿瘤预后学》)。
63.在本说明书中,术语“预测”指患者有利或不利地对特定抗前列腺癌治疗将作出反应的可能性。在一个实施方案中,预测涉及这些反应的程度。在一个实施方案中,预测涉及患者在治疗(例如用特定治疗剂治疗)之后是否将存活或改善和/或存活或改善并且持续一段时间没有疾病进展的概率。
64.在本说明书中,“个体”或“受试者”为哺乳动物。哺乳动物包括但不限于驯养动物(例如母牛、绵羊、猫、狗和马)、灵长类动物(例如人类和非人灵长类动物如猴子)、兔、和啮齿动物(例如小鼠和大鼠)。在某些实施方案中,所述个体或受试者是人。
65.在本说明书中,术语“样本”是指可能包含需要进行分析的靶分子的任何物质,包括生物样本。如本文所用,“生物样本”是指从活的或病毒性(或朊病毒的)来源或其他大分子和生物分子来源获得的任何样本,并且包括可以从之获得核酸、蛋白质和/或其他大分子的受试者的任何细胞类型或组织。生物样本可以是直接从生物来源获得的样本或者是被处理的样本。例如,被扩增的分离的核酸构成生物样本。生物样本包括,但不限于,体液(例如血液、血浆、血清、脑脊髓液、滑液、尿液、汗液、精液、粪便、痰、眼泪、粘液、羊水等)、渗出液、骨髓样本、腹水、骨盆冲洗液、胸膜液、脊髓液、淋巴液、眼液、鼻、喉或生殖器拭子的提取物、消化组织的细胞悬浮液、或粪类物质的提取物、以及来自人、动物(例如非人哺乳动物)和植物的组织和器官样本,以及由此衍生出的加工样本。
66.本公开提供了一种可以用于前列腺癌分期检测、监测进展和预后判断的标记物,即crept。在本公开中,首先明确了crept蛋白在人和小鼠前列腺癌组织中是高表达的。其次发现随着前列腺癌的发生,组织中的crept的 mrna水平随之升高,且转移型前列腺癌组织中crept的mrna水平明显高于其它非转移型前列腺癌。根据前列腺癌特有的组织学分级方法,即gleason 分级法,分析tcga数据库中不同gleason分级/评分的前列腺癌组织中 crept的mrna水平发现,随着gleason分级/评分升高,crept的表达水平升高,二者呈现良好的正相关性。利用免疫组织化学实验在人的前列腺癌组织芯片中分析crept的表达量发现,高表达的crept促进前列腺癌的发展进程。最后,本公开分析发现crept高表达的前列腺癌患者的无病生存率明显低于crept低表达的前列腺癌患者。这些证据显示crept可以作为前列腺癌分期监测(分级诊断)、监测进展和预后判断的标记物。
67.以下是对本公开的技术方案详细的说明。
68.《crept用于检测前列腺癌分期》
69.在本公开的一些方面中,提供了确定受试者样本中crept的表达水平的试剂在制备用于检测/辅助判断前列腺癌分期的试剂/试剂盒中的用途。
70.在本公开的另一些方面中,还提供了一种检测/辅助判断前列腺癌分期的方法,其包括:
71.a)确定待测样本中crept的表达水平;
72.b)将在步骤a)中确定的crept的表达水平与一种或多种参考量比较;
73.c)基于在步骤b)中获得的信息对所述待测样本中前列腺癌进行分期。
74.在本公开的一些实施方案中,crept为引用文献1中公开的crept,其基因序列记载在ncbi数据库(https://www.ncbi.nlm.nih.gov/),识别号为: gene id:58490。在一些实施方案中,crept的表达水平可以是在基因水平上的表达水平,例如dna或mrna的水平。在另一些实施方案中,crept 的表达水平可以是蛋白水平上的表达水平。
75.可以理解,当在基因水平确定crept的表达水平时,示例性地,可以使用的试剂包括引物对和/或探针等。技术人员根据crept的核苷酸序列可以自行制备特异性的引物对和/或探针。当在蛋白水平确定crept的表达水平时,示例性地,可以使用的试剂可以是抗crept抗体。多克隆抗体或单克隆抗体等抗体均可用于实施本公开的技术方案。本领域技术人员也可以选择其他合适的试剂以及方法基于基因水平或蛋白水平确定crept的表达水平,本公开对于这样的试剂或方法没有特殊的限制。
76.当被用于确定或测量的crept时,术语“水平”、“表达水平”、“量”和“表达量”在本
文中可互换地使用。基因水平或蛋白水平的crept的表达水平或表达量包括crept基因或蛋白的绝对量、相对量或者其浓度,以及与其相关的任意值或参数。此类值或者参数包括通过直接测量获得的全部特定物理或化学性质的强度信号值,例如强度值。此外,还包括通过间接测量获得的全部值或者参数,例如,从生物读出系统中测定的表达水平。应当理解,与前述量或参数相关的值还可以通过全部的标准数学运算获得。
77.在本公开中,前列腺癌包括任何病理类型的前列腺癌,包括腺癌(腺泡腺癌)、导管腺癌、尿路上皮癌、鳞状细胞癌和腺鳞癌。在一些优选的实施方案中,前列腺癌包括腺癌。
78.在本公开的一些实施方案中,所述的待测样本来自受试者。在本公开的一些实施方案中,所述的受试者包括哺乳动物。在一些具体的实施方案中,所述的受试者包括人。
79.对于用于检测前列腺癌分期,在一些更具体的实施方案中,所述的受试者为患有前列腺癌的受试者。在本公开中,对于前列腺癌患者中前列腺组织 (尤其是癌组织)中的crept的表达水平进行测量,从而确定/辅助判断其前列腺癌分期(例如非转移或转移,gleason分级及其对应的侵袭性/分化性)。
80.在本公开的一些实施方案中,所述的样本包括前列腺组织,例如通过细针穿刺、穿刺活检或通过手术获得的前列腺组织。对于用于检测前列腺癌分期,在本公开的一些具体的实施方案中,所述的样本包括前列腺癌组织。
81.在本公开的一些实施方案中,前列腺癌分期包括区分非转移型前列腺癌和转移型前列腺癌。其中,在本公开中,非转移型前列腺癌为仅在患者前列腺原位发现肿瘤,未发现远端转移。转移型前列腺癌为除发现前列腺原位肿瘤外还存在远端器官的癌变。
82.如后文实施例3中所证实的,本公开发现,相对于患有非转移型前列腺癌的受试者的前列腺癌组织,患有转移型前列腺癌的受试者的前列腺癌组织中crept的表达水平显著增高。因此,crept的表达水平可以区分非转移型前列腺癌和转移型前列腺癌,以及判断/辅助判断转移型前列腺癌发生的可能性。
83.在本公开的另一些实施方案中,前列腺癌分期包括区分gleason分级和/ 或gleason评分。在一些实施方案种,前列腺癌分期还包括区分前列腺癌的分化程度和/或侵袭性。在一些优选的实施方案中,所述分化程度和/或侵袭性是由gleason分级系统确定的分化程度和/或侵袭性。在一些示例性的实施方案中,前列腺癌的分化程度包括分化良好癌、中等分化癌和较低分化癌。在本公开中,对于前列腺癌的分化程度和/或侵袭性的区分,可以通过gleason 分级系统的分级或评分进行,并且通常可以指导选择适当的治疗方法。示例性地,如前文所述,gleason评分为2-4分属于分化良好癌;5-7分属于中等分化癌;8-10分属于较低分化癌。技术人员也可以根据gleason评分的其他分数或分级划分分组。在本公开中,如后文实施例4和实施例5中所证实的,crept 表达水平与gleason评分具有相关性,gleason评分越高,前列腺癌组织中 crept表达量越高。
84.在一些更具体的实施方案中,前列腺癌分期包括区分中等分化癌 (gleason评分≤7)和较低分化癌(gleason评分>7)。如后文实施例4中所证实的,中等分化癌(gleason评分≤7)和较低分化癌(gleason评分>7)间,crept 表达水平存在显著性差异,如实施例4中所证明的。
85.在本公开的一些实施方案中,通过将确定的受试者样本中crept的表达水平与一种或多种参考量比较,进而确定所述受试者中前列腺癌分期、监测受试者中前列腺癌进展,
或预后判断。
86.在本公开中,“比较”包括将受试者样本中crept的表达水平与合适参考源的表达水平(参考量)相比较。可以理解,比较指对应的参数或者值的比较,例如,将绝对量与绝对参考量比较,而将浓度与参考浓度比较,或者将获自待测样本的强度信号与参考样本的相同类型强度信号比较。基于确定的受试者样本中crept的表达水平与参考量的比较,可以在待测受试者的样本中分期前列腺癌、监测进展或预后判断。
87.在一些实施方案中,术语“参考量”指允许在患有前列腺癌的受试者中分期前列腺癌、监测进展或预后判断的量。
88.在一些具体实施方案中,参考量可以来源于患不同阶段或分期的前列腺癌的受试者的样本。
89.在一些示例性的实施方案中,如果要区分非转移型前列腺癌和转移型前列腺癌,那么参考量可以来源于(i)患有非转移型前列腺癌的受试者的样本(例如,前列腺癌组织)和/或(ii)患有转移型前列腺癌的受试者的样本(例如,前列腺癌组织)。
90.在另一些示例性的实施方案中,如果要区分分化良好癌、中等分化癌和较低分化癌,那么参考量可以来源于(i)处于分化良好癌的受试者的样本(例如,前列腺癌组织),(ii)处于中等分化癌的受试者的样本(例如,前列腺癌组织),和/或(iii)处于较低分化癌的受试者的样本(例如,前列腺癌组织)。
91.在一些实施方案中,参考量可以是获自一组样本中crept的表达水平的平均值或中值。优选地,所述参考量来自前列腺组织样本。
92.在一些实施方案中,参考量还可以是获自处于前列腺癌的多种分期的受试者的代表性群体中crept的表达水平的平均值或中值。受试者的群体应当包含多个受试者,优选地,至少5、10、50、100、1,000或10,000个受试者。应当理解,待进行前列腺癌分期的受试者与受试者的群体中的受试者是同一物种。
93.在一些实施方案中,“参考量”可以通过测定一组参考受试者的crept 的表达水平获得,例如一组患非转移型前列腺癌的受试者、一组患转移型前列腺癌的受试者、或者包含待研究的受试者的群体;并通过合适的统计学方法,例如中值、平均值、分位数、pls-da、逻辑回归方法、随机森林分类 (random forest classification)或者其他给出阈值的方法计算参考量。阈值应当考虑前列腺癌分期的预期灵敏性和特异性的临床设定。
94.可以理解,可应用于受试者的参考量可以依据多种生理学参数而变化,例如年龄或者亚群,以及用于确定crept的表达水平的方法等。
95.在一些具体的实施方案中,如果区分非转移型前列腺癌和转移型前列腺癌,并且如果参考量获自(i)患非转移型前列腺癌的受试者和(ii)患转移型前列腺癌的受试者,可以基于待测样本的crept的表达水平与前述参考量之间的同一性或相似性的程度(定性或定量)实施前列腺癌的分期。在另一些具体的实施方案中,如果要区分分化良好癌、中等分化癌和较低分化癌,并且参考量获自(i)处于分化良好癌的受试者,(ii)处于中等分化癌的受试者和(iii)处于较低分化癌的受试者,同样地,可以基于待测样本的crept的表达水平与前述参考量之间的同一性或相似性的程度(定性或定量)实施前列腺癌的分期。在另一些具体的实施方案中,如果要区分不同gleason分级/评分的前列腺癌,参考量可以获自处于不同gleason分级/评分的前列腺癌的受试者,同样地,可以基于待测样本的crept的表达水
平与前述参考量之间的同一性或相似性的程度(定性或定量)实施前列腺癌的分期。
96.《crept用于监测前列腺癌进展》
97.本公开的另一些方面中,提供了确定受试者样本中crept的表达水平的试剂在制备用于监测/辅助监测前列腺癌进展的试剂/试剂盒中的用途。
98.本公开另一些方面还提供了一种监测/辅助监测前列腺癌进展的方法,其包括:
99.a)确定第一样本中crept的表达水平;
100.b)将在步骤a)中测定的crept的表达水平与一种或多种参考量比较;或者测定在第二样本中crept的表达水平,并将所述第一样本中的crept的表达水平与所述第二样本中的crept的表达水平比较;
101.c)基于在步骤b)中获得的信息监测前列腺癌进展;
102.其中,所述第一样本和所述第二样本为来自同一受试者的不同时间采集的样本。
103.在一些实施方案中,“前列腺癌进展”指前列腺癌从一个阶段转变到另一个阶段,在一些具体的实施方案中,转变到更晚期或转变到gleason分级/ 评分中更高的级别/评分,在另一些具体的实施方案中,转变到更早期或转变到gleason分级/评分中更低的级别/评分。优选地,转变到更晚期或转变到 gleason评分中更高的级别评分,例如从分化良好癌进展到中等分化癌或较低分化癌。又如从非转移型前列腺癌进展到转移型前列腺癌。在另一些实施方案中,“前列腺癌进展”还指由良性的前列腺增生性病变(例如,前列腺增生组织、前列腺上皮瘤)进展至恶性的前列腺癌。进展的分类和测定有益于进行有效的和合适的治疗性干预。
104.在一些实施方案中,所述待测样本来自受试者。对于用于监测前列腺癌进展,在一些实施方案中,所述的受试者包括患有良性的前列腺增生性病变的受试者。示例性地,所述良性的前列腺增生性病变包括良性的前列腺增生、前列腺上皮瘤等。在另一些实施方案中,所述的受试者包括患有前列腺癌的受试者。
105.对于用于监测前列腺癌进展,在一些实施方案中,所述的样本包括良性的前列腺增生性病变组织(例如,良性前列腺增生组织、前列腺上皮瘤组织),或者前列腺癌组织。
106.在一些具体的实施方案中,与第一样本中的crept的表达水平比较,在第二样本中crept的表达水平的增加,优选地,统计学显著的增加,指示了前列腺癌的进展。
107.在一些具体的实施方案中,所述第二样本在所述第一样本后1-2个月内、 2-4个月内、4-6个月内、6-12个月内、12-24个月内,和更优选地,24-48个月内获得。
108.在其他实施方案中,如上所述的,也可以将受试者样本中crept的表达水平与合适的参考量相比较,从而监测受试者前列腺癌的进展。
109.此外,本公开还涉及确定受试者样本中crept的表达水平的试剂在制备用于监测前列腺癌治疗或者针对前列腺癌进展的治疗有效性的试剂/试剂盒的用途。可以理解,有效的治疗应当导致受试者样本中crept的表达水平的降低,例如从患病或者晚期阶段到健康或者更早期的疾病阶段。
110.《crept用于前列腺癌预后判断》
111.在本公开的一些方面中,提供了确定受试者样本中crept的表达水平的试剂在制备用于判断/辅助判断前列腺癌预后的试剂/试剂盒中的用途。
112.在一些实施方案中,受试者是正患有前列腺癌的受试者、或者曾经患有前列腺癌
的受试者(而无论是否治愈)。
113.在一些具体实施方案中,预后是指无病生存率。
114.《检测系统和试剂盒》
115.本公开的一些方面中,提供了一种用于检测前列腺癌的分期或监测进展的系统,其中,所述系统包括检测装置、计算装置和输出装置;
116.所述检测装置包括进样器和检测器,所述进样器用于采集来自受试者的样本,所述检测器用于检测所述样本中crept的表达水平;
117.所述计算装置包括存储器和处理器,所述存储器中存储有计算机程序,所述处理器被配置为执行所述存储器中存储的计算机程序,以实现如下判别:
118.当检测前列腺癌的分期时,将所述样本中crept的表达水平与参考量相比较,判别所述样本对应的受试者的前列腺癌分期;
119.当监测前列腺癌的进展时,将来自同一受试者的不同时间采集的样本中 crept的表达水平相比较,或者将样本中crept的表达水平与参考量相比较,判别样本对应的受试者的前列腺癌是否进展。
120.在一些具体的实施方案中,所述输出装置用于输出所述检测装置的检测结果和/或所述计算装置的判别结果,所述输出装置包括显示器、打印机和音频输出装置中的至少一种;所述计算装置包括电脑主机、中央处理器和网络服务器中的至少一种。
121.在另一些方面,本公开提供过了一种用于检测前列腺癌的分期、监测进展和/或预后判断的试剂盒,其包括确定受试者样本中crept的表达水平的试剂。在一些实施方案中,所述的试剂盒还包括适合于测定由所述试剂确定的所述受试者样本中crept的表达水平的装置。
122.实施例
123.以下通过实施例进一步说明本公开,但不作为对本公开的限制。以下提供了本公开实施方案中所使用的具体材料及其来源。但是,应当理解的是,这些仅仅是示例性的,并不意图限制本公开,与如下试剂和仪器的类型、型号、品质、性质或功能相同或相似的材料均可以用于实施本公开。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
124.实施例1、crept在人及小鼠前列腺癌组织中的表达
125.本实施例利用免疫组织化学实验,样本来自于上海芯超公司购买人前列腺癌组织芯片,在同一患者的正常前列腺组织与前列腺癌组织中检测crept 的表达量,crept抗体已在专利cn102559601a中公开。实验方法:将组织用4%的多聚甲醛固定后,包埋在石蜡中,将切片置于65℃烤片机上烤片 30-40分钟,使石蜡熔化。将切片进行脱蜡处理:放入第一个100%二甲苯缸中,上下温和提拉约20次,静置5分钟;放入第二个100%二甲苯缸中,操作同上;放入第三个100%二甲苯缸中,操作同上。脱蜡完毕后将切片水化:放入第一个100%乙醇缸中,上下温和提拉约20次,静置2分钟;放入第二个 100%乙醇缸中,静置1分钟;放入90%乙醇缸中,静置1分钟;放入80%乙醇缸中,静置1分钟;放入70%乙醇缸中,静置1分钟。水化后洗片两次:第一次洗片:在灰缸中加双蒸水,上下温和提拉约20次;第二次洗片:在灰缸中加双蒸水,上下温和提拉约3次,静置1分钟。洗片后进行修复:在灰缸中加入柠檬酸钠缓冲液(ph=6),用高压锅煮沸20分钟;在室温下晾30分钟;双蒸水洗3次,上下轻提数次,静
置1分钟。然后封闭:在湿盒中,用封闭液处理10分钟;用pbst(含0.1%tween 20的pbs)洗3次,每次5分钟。接下来孵crept抗体:在湿盒中,用一抗专用稀释液按一定比例稀释抗体,封口膜封片,4℃孵育过夜,pbst洗3次,每次5分钟。再孵育二抗:用带有生物素标记二抗,室温孵育30分钟,pbst洗3次,每次5分钟。dab染色:滴加dab 染色液,在显微镜下观察染色程度,用水终止染色。苏木精液染细胞核5分钟,流水冲洗30分钟。最后将切片依次用75%乙醇,95%乙醇,100%乙醇处理各3分钟,二甲苯处理2分钟,中性树脂封片。扫描拍照并分析结果。结果显示,crept在人前列腺癌组织中呈高表达,在对应的正常前列腺组织中低表达。同样地,本实施例通过免疫组织化学实验比较了crept在小鼠(来自于本实验室构建转基因杂交小鼠(自发诱导前列腺癌)前列腺组织切片)前列腺癌组织与正常前列腺组织表达差异,实验结果表明,crept在小鼠的前列腺癌组织中表达量明显高于小鼠正常前列腺组织。
126.具体结果参见图1a和图1b。其中,图1a为人前列腺癌组织与正常前列腺组织中通过免疫组化检测crept的表达量的结果,人前列腺癌组织中 crept呈现高表达状态,而同一患者的正常前列腺组织则看不到crept的阳性染色结果。图1b为小鼠前列腺癌组织与正常前列腺组织进行crept免疫组化染色的结果,同样,小鼠列腺癌组织中crept呈现高表达状态,而小鼠的正常前列腺组织则看不到crept的阳性染色结果。
127.实施例2、随着前列腺癌的发生,组织中的crept的mrna水平随之升高
128.本实施例分析了gse6099 hs6-2-23-8(获自geo数据库)中crept分别在前列腺增生组织(bph)、前列腺上皮瘤(pin)和前列腺癌(pca)组织中的表达量,其mrna水平,也就是tpm(transcripts per kilobase per million mappedreads,每千个碱基的转录每百万映射读取的转录本)平均值分别为1.02686、 1.19313、1.27188(样本tpm值为数据库给出)。结果如图2所示,结果显示,随着前列腺癌的发生,组织中的crept的mrna水平随之升高。具体地,通过t检验,前列腺增生组织(bph)与前列腺上皮瘤(pin)间crept的mrna表达水平具有显著差异,p值为0.0136;同时,前列腺增生组织(bph)与前列腺癌 (pca)间crept的mrna表达水平具有显著差异,p值为0.0056。可见,crept 可以作为前列腺癌疾病进展预测的标志物。因此,根据tpm值和细胞中的 rna含量预测(本实施例中定义mrna含量=tpm值,单位为ng)creptmrna含量大于等于约1.02ng且小于约1.19ng时,患者可能发生前列腺增生;大于等于约1.19ng且小于约1.2ng时,可能发生前列腺上皮瘤;大于等于约 1.2ng时,患者有可能发展为前列腺癌。
129.实施例3、转移型前列腺癌组织中crept表达量升高
130.本实施例中进一步比较了gse6919 gds2546(获自geo数据库)中非转移型前列腺癌组织(pca)与转移型前列腺癌组织(met)中crept的mrna水平差异。结果如图3所示,非转移型前列腺癌组织中tpm平均值为0.416,转移型前列腺癌组织中tpm平均值为2.540(样本tmp值为数据库中给出)结果显示,转移型前列腺癌组织(met)中crept的mrna水平明显高于其在非转移型前列腺癌(pca)组织中的mrna水平(统计分析方法:t检验; p《0.0001)。由此,根据tpm值和细胞中的rna含量预测(本实施例定义 mrna含量=tpm值,单位为ng)crept mrna含量大于等于约2.54ng时,患者可能出现转移。
131.实施例4、gleason评分与crept表达量相关
132.根据前列腺癌特有的组织学分级方法-gleason分级法,本实施例分析了 tcga数据库(cancer genome atlas research)中不同gleason评分的前列腺癌组织中crept的
mrna水平。结果如图4所示,gleason评分6/7时,tpm平均值为3.21;gleason评分大于7时,tpm平均值为3.40(样本tmp值为数据库中给出)结果表明,随着gleason评分升高,crept的表达水平升高(统计分析方法:t检验;p《0.001;n(6/7)=338,n(》7)=213)。由此,根据tpm值和细胞中的rna含量预测(本实施例中定义mrna含量=tpm值,单位为ng) crept mrna含量大于等于约3.21ng且小于约3.40ng时,gleason评分为6/7; crept mrna含量大于等于约3.40ng时,gleason评分大于7。
133.实施例5、gleason分级越高,crept表达量越高
134.本实施例利用免疫组织化学实验在人的前列腺癌组织芯片中分析 crept的表达量,样本来自于上海芯超公司购买人前列腺癌组织芯片,编号为hproa180pg05,共有90个前列腺癌腺癌组织并配有对应gleason分级。根据dab染色可以统计出creot阳性细胞数,具体方法是选取三个视野统计crept阳性细胞数占总细胞数的比例,取平均值,统计结果表明,gleason 分级越高,crept阳性细胞数越高,肿瘤恶性程度越高。
135.结果参见图5a和图5b,在癌旁组织中,crept阳性细胞率为0;gleason 分级2、3、4、5级中crept阳性细胞率分别为5.3%、13%、52.3%、68.7%。说明高表达的crept促进前列腺癌的发展进程。由此预测,crept阳性细胞率大于约5%且小于约13%时,患者肿瘤很少见;crept阳性细胞率大于约13%且小于约52%时,肿瘤常见;crept阳性细胞率大于约52%且小于约68%时,癌肿分化差;crept阳性细胞率大于约68%时,癌肿分化极差。
136.实施例6、crept表达水平与前列腺癌预后相关
137.将tcga数据库中前列腺癌患者(n=593)分为crept mrna低表达组 (75%,n=366)和crept高表达组(25%,n=127),分析两组的无病生存率。结果如图6所示,crept mrna高表达的前列腺癌患者的无病生存率明显低于crept低表达的前列腺癌患者。
138.以上示例性实施方式所呈现的描述仅用以说明本公开的技术方案,并不想要成为毫无遗漏的,也不想要把本公开限制为所描述的精确形式。显然,本领域的普通技术人员根据上述教导做出很多改变和变化都是可能的。选择示例性实施方式并进行描述是为了解释本公开的特定原理及其实际应用,从而使得本领域的其它技术人员便于理解、实现并利用本公开的各种示例性实施方式及其各种选择形式和修改形式。本公开的保护范围意在由所附权利要求书及其等效形式所限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1