一种特异性检测病毒的试剂及其应用的制作方法
1.本发明属于生物医药领域,涉及一种特异性检测病毒的试剂及其应用。
背景技术:
2.禽流感(avian influenza,ai)是由禽流感病毒(avian influenza virus,aiv)引起的一种禽呼吸性的传染病,可感染多种家禽和野生鸟类,也可感染其他动物及人类(krammer f,smith g,fouchier r,et al.influenza[j].nature reviews disease primers,2018.),造成重大的社会生态危害,也可造成重大的社会经济损失。
[0003]
aiv属于正粘病毒科,甲型流感病毒属(influenzavirus a),属于单股负链核糖核酸(ribonucleicacid,rna),共8个节段编码10种蛋白质。病毒颗粒呈球形或多边形,有些也呈丝状。病毒颗粒直径大小约为80-120nm,但呈丝状的大小可达几百纳米,病毒基因组全长约为13.6kb,由8个结构蛋白:血凝素(hemagglutinin,ha)、神经氨酸酶(neuraminidase,na)、基质蛋白1(matrix protein 1,m 1)、基质蛋白2(matrix protein 2,m2)、核蛋白(nucleoprotein,np)、聚合酶碱性蛋白1(polymerase basic protein 1,pb1)、聚合酶碱性蛋白2(polymerase basic protein 2,pb2)、聚合酶酸性蛋白(polymerase acid protein,pa),组成病毒的基本结构。位于宿主细胞质中含两个非结构蛋白:ns1(non-structural protein 1,ns1)蛋白和ns2(non-structural protein 2,ns2)蛋白。ha作为整合i型囊膜糖蛋白主要参与介导血凝活性及抗体介导的病毒中和活性。na属于ii型囊膜糖蛋白,主要参与细胞受体睡液酸残释放病毒,并通过抗体介导的病毒中和作用阻止病毒在体内扩散。np主要为结构蛋白与病毒rna片段相关。m1是非糖基化结构蛋白,存在于病毒囊膜下。m2为整合的iii型囊膜糖蛋白。pb1、pb2和pa为多聚酶复合物,与病毒rna复制转录翻译有关。目前,已经在鸟类中发现了16种ha(hl-h16)和9种na(n1-n9)亚型的aiv,但是新的ha(h17和h18)和na(n10和n11)亚型仅在蝙蝠中有所发现。
[0004]
流感病毒感染宿主范围主要取决于流感病毒的血凝素蛋白与宿主细胞表面流感病毒受体的相互作用。目前普遍认为流感病毒的受体为唾液酸受体,可以分为唾液酸a-2,3-gal受体和唾液酸a-2,6-gal受体。一般认为禽流感病毒倾向于结合a-2,3受体,而人流感病毒倾向于结合a-2,6受体。宿主体内不同类型受体的分布差异是流感病毒跨物种传播的主要屏障。
[0005]
近期,国内发现禽h3n8亚型流感病毒感染人,而使用之前的季节性流感h3亚型检测引物无法检测出该病毒,设计新的检测方法对于实现感染人的h3n8病毒的检测具有重要的意义。
技术实现要素:
[0006]
为了弥补现有技术的不足,本发明的目的之一是提供一种感染人的h3n8病毒的检测试剂。
[0007]
本发明的目的之二是提供一种感染人的h3n8病毒的检测方法。
[0008]
本发明的目的之三是提供感染人的h3n8病毒的应用。
[0009]
为了实现上述目的,本发明采用如下技术方案:
[0010]
本发明第一方面提供了一种检测感染人的h3n8病毒的试剂,所述试剂包括特异性针对该病毒ha基因的引物。
[0011]
优选地,所述引物的序列如seq id no:5和seq id no:6所示。
[0012]
优选地,所述试剂还包括针对ha基因的寡核苷酸探针。
[0013]
优选地,所述寡核苷酸探针的序列如seq id:7所示。
[0014]
优选地,所述寡核苷酸探针或引物与可检测标记偶联。
[0015]
优选地,可检测标记选自放射性元素、酶、抗体或荧光化学物质。
[0016]
本发明第二方面提供了一种检测感染人的h3n8病毒的试剂,所述试剂包括特异性针对na基因的引物。
[0017]
优选地,所述引物的序列如seq id no:8和seq id no:9所示。
[0018]
优选地,所述试剂还包括针对na基因的寡核苷酸探针。
[0019]
优选地,所述寡核苷酸探针的序列如seq id:10所示。
[0020]
优选地,所述寡核苷酸探针或引物与可检测标记偶联。
[0021]
优选地,可检测标记选自放射性元素、酶、抗体或荧光化学物质。
[0022]
本发明第三方面提供了一种检测感染人的h3n8病毒的产品,所述产品包括本发明第一方面和/或本发明第二方面所述的试剂。
[0023]
优选地,所述产品包括本发明第一方面所述的试剂和本发明第二方面述的试剂。
[0024]
优选地,本发明第一方面和本发明第二方面所述的试剂位于一个容器中。
[0025]
优选地,本发明第一方面和本发明第二方面所述的试剂位于不同的容器中。
[0026]
优选地,所述产品还包括检测内参的试剂。
[0027]
优选地,所述产品还包括处理样本的试剂。
[0028]
本发明第四方面提供了本发明第一方面所述的试剂、本发明第二方面所述的试剂、本发明第三方面所述的产品在检测h3n8病毒中的应用。
[0029]
本发明第五方面提供了本发明第一方面所述的试剂、本发明第二方面所述的试剂、本发明第三方面所述的产品在制备检测感染人的h3n8病毒感染的产品中的应用。
[0030]
本发明第六方面提供了一种检测感染人的h3n8病毒的方法,包括:
[0031]
使权利要求1和/或权利要求2所述的试剂与待测样品接触,通过检测信号值指示h3n8病毒的存在或者含量。
[0032]
优选地,允许多核苷酸扩增的条件下使所述试剂与所述待测样品接触。
[0033]
优选地,所述待测样品选自环境样品或生物样品。
[0034]
本发明第七方面提供了一种感染人的h3n8病毒,所述病毒的ha基因序列如seq id no:1所示或seq id no:3所示;na基因的序列如seq id no:2或seq id no:4所示。
[0035]
本发明的第八发面提供了如下任一项所述的物质:
[0036]
1)多肽,所述多肽选自权利要求7所述的h3n8病毒的ha蛋白和/或na蛋白;
[0037]
2)核酸分子,所述核酸分子编码权利要求7所述的h3n8病毒的ha和/或na蛋白;
[0038]
3)载体,所述载体包括2)所述的核酸分子。
[0039]
本发明第九方面提供了本发明第七方面所述的病毒、本发明第八方面所述的物质
在制备针对h3n8的抗体中的应用。
[0040]
本发明第十方面提供了本发明第七方面所述的病毒、本发明第八方面所述的物质在制备疫苗中的应用。
[0041]
本发明的优点和有益效果:
[0042]
本发明提供了一种检测感染人的h3n8病毒的试剂及产品,所述试剂进行h3n8的检测具有较高的特异性。
附图说明
[0043]
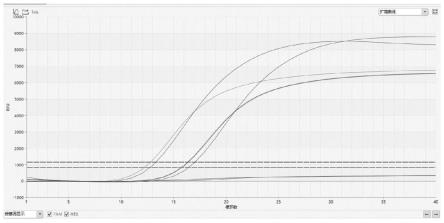
图1是不同地区来源的h3n8的检测结果图。
具体实施方式
[0044]
以下将对本发明进一步详细说明,应理解,所述用语旨在描述目的,而非限制本发明。
[0045]
术语“和/或”是指并且包括一个或多个相关联的所列项目的任何和所有可能的组合,以及在备选方案(或)中解释时缺少组合。
[0046]
在本发明中,术语“核酸”、“寡核苷酸”和“多核苷酸”可互换使用。核酸分子是由至少两个共价连接在一起的核苷酸组成的核苷酸聚合物。核酸分子是dna(脱氧核糖核苷酸)、rna(核糖核苷酸)以及重组rna和dna分子或使用核苷酸类似物产生的dna或rna类似物。核酸可以是单链或双链、线性或环状的。所述术语还涵盖核酸片段,例如可以使用所公开的提取方法回收的天然存在的rna或dna,或在体外人工合成的人工dna或rna分子。核酸的分子量也没有限制,可以在从数个碱基对(bp)到数百个碱基对如从约2个核苷酸到约1,000个核苷酸的范围内是任选的。作为非限制性示例,核酸分子可包含2个、3个、4个、5个、6个、7个、8个、9个、10个、12个、15个、20个、25个、30个、35个、40个、45个、50个、55个、60个、65个、70个、75个、80个、85个、90个、95个、100个、110个、120个、130个、140个、150个、200个、250个、300个、350个、400个、450个、500个、550个、600个、650个、700个、750个、800个、850个、900个或1,000个核苷酸。核酸可以是经化学修饰的,本发明中用于指核酸分子时意指一个或多个核苷酸被修饰,例如,非天然发生的核苷酸的结构修饰、被核苷类似物替代以及糖-磷酸骨架的化学修饰等。在一些示例中,经修饰的核酸分子可以包含非标准或修饰的核苷。
[0047]
优选地,如本发明中所表示的寡核苷酸引物在长度上具有15与35个之间的核苷酸,更优选在长度上具有15与30个之间的核苷酸,且最优选在长度上具有18与25个之间的核苷酸。优选地,寡核苷酸是单链寡脱氧核糖核苷酸。然而,由于自互补,寡核苷酸在某些条件下可以是部分双链(取决于例如寡核苷酸的序列、盐浓度以及温度)。
[0048]
在本发明中,术语“探针”是指蛋白(包括肽)、核酸、糖链(包括糖缀合物)、脂质(包括缀合的脂质)等生物聚合物。具体地,探针包括酶、激素、信息素、抗体、抗原、半抗原、肽、合成肽、dna、合成dna、rna、合成rna、dna/rna杂合体、pna、合成pna、神经节苷脂、寡核苷酸、适体、凝集素等。在本发明的上下文中,探针是包含与靶核酸序列特异性互补的核酸序列的核酸探针。
[0049]
在本发明中,术语“靶核酸”是指期望与待分析的感兴趣的分析物结合的天然或合成来源的核酸(例如dna或rna)序列。
[0050]
在本发明中,术语“互补的”通常是指特异性核苷酸双链化以形成规范的沃森-克里克碱基对,如本领域技术人员所理解的。例如,如果两条核酸链或两条核酸链的部分可以彼此形成完美的碱基配对双螺旋,则称它们是互补的或具有互补序列。术语“杂交”是指通过a和t与g和c之间的碱基配对进行的非共价键合。
[0051]
在一些实施方案中,探针包含短的单链寡核苷酸探针序列,其包含5-50个核苷酸、或5-30个核苷酸、或5-25个核苷酸、或10-25个核苷酸、或8-15个核苷酸、或10-20个核苷酸。作为非限制性示例,寡核苷酸探针序列可包含至少5个核苷酸、或至少6个核苷酸、或至少7个核苷酸、或至少8个核苷酸、或至少9个核苷酸、或至少10个核苷酸、或至少11个核苷酸、或至少12个核苷酸、或至少13个核苷酸、或至少14个核苷酸、或至少15个核苷酸、至少16个核苷酸、或至少17个核苷酸、或至少18个核苷酸、或至少19个核苷酸、或至少20个核苷酸、或至少21个核苷酸、或至少22个核苷酸、或至少23个核苷酸、或至少24个核苷酸、或至少25个核苷酸。
[0052]
单链寡核苷酸探针可以包含独特特异性寡核苷酸探针序列,其被设计为与靶核酸序列中存在的感兴趣的序列互补。探针序列可以通过互补序列与靶核酸序列的杂交来检测制备物中的靶核酸序列。在一些示例中,探针序列可以与互补靶序列有一个、两个、三个或更多个核苷酸不同。在一些实施方案中,核酸探针序列和靶序列之间的互补杂交不会影响靶核酸序列与分析物的结合。在其他示例中,靶核酸序列与感兴趣的分析物的结合不影响核酸探针序列的互补杂交。
[0053]
在本发明中,“引物”是指用作用于多核苷酸扩增的启动分子的天然存在的或合成的核苷酸聚合物。
[0054]
在本发明的实施方案中,扩增技术是本领域的技术人员所熟知的pcr或qpcr等。应理解,例如由于寡核苷酸序列与目标多核苷酸的序列片段之间的错配,引物可以不与目标序列100%互补。
[0055]
检测试剂
[0056]
本发明提供了一种检测感染人的h3n8病毒的试剂,所述试剂包括特异性针对该病毒ha基因的引物,所述引物靶向h3n8病毒特异性序列。
[0057]
在本发明的实施方案中,所述引物的序列具有seq id no:5和seq id no:6所示的序列或与其具有至少70%序列一致性的序列中的至少十二个连续核苷酸。
[0058]
在本发明的一些实施方案中,引物序列的一致性为至少80%。
[0059]
在本发明的一些实施方案中,引物序列的一致性为至少90%。
[0060]
在本发明的一些实施方案中,引物序列的一致性为至少95%。
[0061]
在本发明的一些实施方案中,引物序列的一致性为至少96%。
[0062]
在本发明的实施方案中,所述试剂还包括针对ha基因的寡核苷酸探针。
[0063]
在本发明的实施方案中,所述寡核苷酸探针的序列具有seq id:7所示的序列或与其具有至少70%序列一致性的序列中的至少十二个连续核苷酸。
[0064]
在本发明的另一实施方案中,提供了一种检测感染人的h3n8病毒的试剂,所述试剂包括特异性针对na基因的引物,所述引物靶向h3n8病毒特异性序列。
[0065]
在本发明的实施方案中,所述引物的序列具有seq id no:8和seq id no:9所示的序列或与其具有至少70%序列一致性的序列中的至少十二个连续核苷酸。
[0066]
在本发明的一些实施方案中,引物序列的一致性为至少80%。
[0067]
在本发明的一些实施方案中,引物序列的一致性为至少90%。
[0068]
在本发明的一些实施方案中,引物序列的一致性为至少95%。
[0069]
在本发明的一些实施方案中,引物序列的一致性为至少96%。
[0070]
在本发明的实施方案中,所述试剂还包括针对na基因的寡核苷酸探针。
[0071]
在本发明的实施方案中,所述寡核苷酸探针的序列具有seq id:10所示的序列或与其具有至少70%序列一致性的序列中的至少十二个连续核苷酸。
[0072]
在本发明的实施方案中,本发明所述的寡核苷酸探针或引物与可检测标记偶联。
[0073]
在本发明的一些实施方案中,可检测标记选自放射性元素、酶、抗体或荧光化学物质。
[0074]
在本发明的一些实施方案中,可检测标记选自荧光化学物质,荧光化学物质标记选自荧光素、花青染料、香豆素、藻红蛋白、藻胆蛋白、丹酰氯、镧系络合物或荧光染料。
[0075]
其中,所述荧光染料包括但不限于r-藻红蛋白、cy3、cy5、quasar 670、罗丹明、alexa或texas red。所述荧光素是6-fam(6-羧基荧光素)、tet(6-羧基-4,7,2
′7′‑
四氯荧光素)、joe(2,7-二甲氧基-4,5-二氯-6-羧基荧光素)或hex(6-羧基-2
′
,4
′
,7
′
,4,7-六氯荧光素)。
[0076]
在本发明中,本发明的寡核苷酸探针是用标记物质进行标记,以检测通过使用对应的寡核苷酸引物对扩增的产物。优选地,寡核苷酸探针与可检测标记偶连,该可检测标记选自由放射性元素、酶、抗体以及荧光化学物质组成的组。更优选地,本发明的寡核苷酸探针是用荧光化学物质进行标记,以便以高的灵敏度快速检测扩增产物。更优选地,本发明的寡核苷酸探针是用荧光化学物质以及猝灭剂进行双重标记。
[0077]
优选地,本发明的寡核苷酸探针具有用荧光物质(报告荧光染料)修饰的5
′
末端以及用猝灭剂(猝灭荧光染料)修饰的3
′
末端,或反之亦然。优选地,报告染料是荧光素(包括6-fam(6-羧基荧光素)、tet(6-羧基-4,7,2
′
,7
′‑
四氯荧光素)、joe(2,7-二甲氧基-4,5-二氯-6-羧基荧光素)以及hex(6-羧基-2
′
,4
′
,7
′
,4,7-六氯荧光素))、花青染料、香豆素、藻红蛋白、藻胆蛋白、丹酰氯、镧系络合物或荧光染料(诸如r-藻红蛋白、cy3、cy5、quasar 670、罗丹明、alexa或texas red)。猝灭荧光染料的实例包括罗丹明类荧光染料,诸如6-羧基四甲基罗丹明(tamra)、黑洞猝灭剂(bhq)bhq-1及2以及6-羧基-x-罗丹明(rox)。然而,此种标记及技术是本领域的技术人员熟知的。
[0078]
在本发明的一些实施方案中,所述可检测标记选自酶,酶包括辣根过氧化物酶(hrp)、酯酶、碱性磷酸酶(ap)、葡萄糖氧化酶、β-半乳糖苷酶或荧光素酶。酶标记是本领域的技术人员熟知的,并且任何酶试验均可无需再费周折而立即完成。基质也是本领域的技术人员熟知的,并且实例包括用于hrp的3,3'-二氨基联苯胺(dab)、3,3',5,5'-四甲基联苯胺(tmb)、2,2'-联氮双[3-乙基苯并噻唑啉-6-磺酸](abts)或邻苯二胺盐酸盐(opd),用于ap的氯化硝基四氮唑蓝(nbt)与5-溴-4-氯-3-吲哚磷酸(bcip)或对硝基苯磷酸盐(pnpp)或对氨基苯酚(pap)的组合、用于葡萄糖氧化酶的氯化硝基四氮唑蓝(nbt)以及用于β半乳糖苷酶的5-溴-4-氯-3-吲哚基-β-d-吡喃半乳糖苷(bcig或x-gal)。
[0079]
产品
[0080]
在本发明的一些实施方案中,本发明提供的检测感染人的h3n8病毒的产品包括前
面所述的针对ha基因的试剂。所述试剂包括特异性针对该病毒ha基因的引物和/或寡核苷酸探针。
[0081]
在本发明的一些实施方案中,本发明提供的检测感染人的h3n8病毒的产品包括前面所述的针对na基因的试剂。所述试剂包括特异性针对该病毒na基因的引物和/或寡核苷酸探针。
[0082]
在本发明的优选的实施方案中,本发明提供的检测感染人的h3n8病毒的产品包括前面所述的针对ha基因和na基因的检测试剂。
[0083]
作为一种可选择的实施方案中,针对ha基因和na基因的检测试剂位于一个容器中。
[0084]
作为一种可选择的实施方案,针对ha基因和na基因的检测试剂分别位于不同的单独容器中。
[0085]
在本发明的一些实施方案中,所述产品包括一个或多个对照样品,所述对照样品是rna、cdna或dna样品。
[0086]
在本发明的一些实施方案中,对照是阳性对照,其包括针对感染人的h3n8病毒的特异性rna、cdna或dna。
[0087]
在本发明的具体实施方案中,所述产品还包括说明书,其提供产品使用的信息。
[0088]
在本发明中,所述产品可以采用本领域的任何常规形式,包括但不限于试剂盒、芯片、试纸。
[0089]
在本发明中,“芯片”可以理解为任何三维形状。衬底可以是适用于如上所述的核酸固定的任何类型的材料。用作芯片衬底的材料可以具有期望的特性,包括光学特性,例如平整度、透明度、明确定义的光学吸收光谱、最小自发荧光、高反射率;和化学特性,例如允许共价连接的表面反应性。合适衬底的非限制性示例包括无机材料,例如硅、玻璃和陶瓷(例如低温共烧陶瓷(low-temperature cofired ceramic,ltcc))、聚合物衬底、复合材料和纸(nge等人,2013和wu等人,2013)。聚合物可以包括弹性体,例如聚二甲基硅氧烷(polydimethylsiloxane)(pdms;二甲硅油(dimethicone))、聚酯(例如热固性聚酯(thermoset polyester,tpe));热塑性聚合物,例如聚苯乙烯(ps)、聚碳酸酯(pc)、聚甲基丙烯酸甲酯(poly-methyl methacrylate,pmma)和聚乙二醇二丙烯酸酯(poly-ethylene glycol diacrylate,pegda)、全氟化合物/聚合物(例如全氟烷氧基(teflon pfa)、氟化乙烯丙烯(teflon fep)和多氟聚醚二醇甲基丙烯酸酯(polyfluoropolyether diol methacrylate,pfpe-dma))和聚氨酯(pu);和热固物(thermosets),以及聚酰亚胺和亚克力(acrylic)。纸、基于柔性纤维素的材料、复合材料,例如无定形材料、环烯烃聚合物(cop)、基于环烯烃单体和乙烯的聚合物,例如环烯烃共聚物(coc)。在一些示例中,芯片是塑料芯片:其具有出色的微加工性能,并且更容易整合到低成本的便携式分析系统中。
[0090]
在一些实施方案中,芯片可以被配置为与分析装置一起使用。在本发明中,术语“分析装置”通常是指被配置为用于进行至少一种分析,尤其是一种检测分析的任意装置。因此,分析装置通常可以是被配置为用于进行至少一种病毒核酸检测目的的任意装置。具体地,分析装置可以能够对样品中的至少一种病毒进行至少一种检测,例如,样品中病毒的存在和/或不存在。因此,分析装置通常可以是被配置为用于进行至少一种诊断目的如病毒感染的任意装置。
[0091]
预合成的核酸可以通过化学键合(例如,共价键合)和吸附固定在衬底上。公知的吸附方法包括包埋、共吸附和取代。基于化学反应的连接通常需要对核酸探针和表面二者进行复杂的化学修饰。执行许多处理步骤以将探针固定到衬底如聚合物塑料上。例如,可以对衬底的表面进行预处理以促进核酸探针的固定,包括引入官能性基团(例如,氨基、硫醇基、巯基(-sh)、磺酸基(-so3-)和羧基(-cooh))到衬底表面。dna寡核苷酸探针也可以通过sn2反应、结合缓冲液或通过uv暴露直接连接固定到未修饰的塑料衬底上。li等人用uv/臭氧照射pc以促进氨基修饰的dna探针的连接。kimura等人报道了uv诱导将用聚(dt)修饰的dna链和未公开的接头序列连接到pc、pmma和pet。
[0092]
检测方法
[0093]
本发明提供了检测感染人的h3n8病毒的方法,包括:
[0094]
使本发明上文所述的试剂与待测样品接触,通过检测信号值指示h3n8病毒的存在或者含量。
[0095]
在优选的实施方案中,允许多核苷酸扩增的条件下使所述试剂与所述待测样品接触,通过检测信号值指示h3n8病毒的存在或者含量。
[0096]
本领域的技术人员理解如本文中所用的术语“在允许多核苷酸扩增的条件下”。该术语涉及依赖模板的过程,其会导致核酸分子的量相对于其最初量增加。根据本发明,目的多核苷酸的扩增应允许通过被认为合适的及/或例如下文所述的任何方法对其进行检测。目的多核苷酸的扩增可以通过众所周知的方法、优选通过pcr执行,而且还可以通过逆转录酶pcr、实时pcr、逆转录酶实时pcr、templex-pcr、基于核酸序列的扩增(nasba)以及使用聚合酶及特异性寡核苷酸作为引物的等温扩增方法执行。上述扩增方法在本领域中众所周知。在本发明上下文中的pcr的优选实施方案将在实施例中进行描述。
[0097]
在一些实施方案中,所述扩增是pcr(聚合酶链反应)或实时pcr(聚合酶链反应)。
[0098]
当使用实时pcr时,使用“标准”制订校正曲线,这些“标准”是包含已知数量的目标核酸序列拷贝的样品。进行独立的反应,每一反应包含不同的标准。使用来自涉及不同标准量的每一反应的ct值制订ct与logn(起始拷贝数)的曲线图或“标准曲线”。
[0099]
通过将来自包含生物样品的反应的ct值插入到标准曲线上来确定生物样品中目标核酸序列的拷贝数。优选地,软件程序产生针对所有“标准”的ct与logn(起始拷贝数)的“标准曲线”,然后通过内插确定未知数的起始拷贝数。待测样品中目标基因序列的拷贝数的确定指示待测样品中病毒或病毒残余部分的数量。
[0100]
此种实时pcr方法需要至少三种寡核苷酸以对每一目标核酸序列进行分析。正向及反向寡核苷酸引物的序列与目标核酸序列的末端互补。探针序列与目标核酸序列的末端之间所发现的序列互补。当与目标杂交时,“正向引物”及“反向引物”为目标核酸序列的聚合酶催化的扩增提供模板。需要单链寡核苷酸探针进行目标检测。在此种方法中,两个反应合并成单一反应形式:用以检测特异性目标核酸序列的寡核苷酸探针杂交以及用以扩增目标核酸序列的pcr。通过荧光共振能量转移,猝灭剂减少寡核苷酸探针内的荧光报告基团的荧光发射。由于taq聚合酶的5'-3'外切核酸酶活性催化互补链合成,因此其将猝灭剂部分从结合寡核苷酸探针切除,从而由于报告因子不再被猝灭,导致探针的荧光发射增加。扩增反应期间的荧光信号的增加因此取决于荧光寡核苷酸探针及寡核苷酸引物二者与目标序列的杂交。
[0101]
优选地,采用多重形式来检测单一反应中的一个以上的目标核酸序列。例如,针对一个以上的目标基因的引物或针对同一目标基因上的不同位置的引物(具有连接至不同荧光报告因子的对应目标特异性探针)可以检测单一反应中的多个目标。更优选地,针对一个目标基因的引物(具有连接至不同荧光报告因子的两个对应目标特异性寡核苷酸探针)用于检测单一反应中的多个目标。
[0102]
在本发明中,所述待测样品选自环境样品或生物样品。
[0103]“环境样品”是指并未直接取自动物而是取自动物所居住的环境的样品。优选地,环境样品是空气过滤器样品、用于收集口腔液的绳样品、拖把垫或海绵样品。然而,环境样品可以是来自动物所居住的环境的任何其他样品,诸如来自地面、墙壁、门、嵌板、工作人员的衣物或喂食/饮水系统的拭子。
[0104]“生物样品”是指体液样品、分离的细胞样品或来自组织或器官的样品。体液样品可以通过公知的技术获得,并且优选地包括鼻样品或口腔液样品(诸如鼻拭子样品或口腔拭子样品或扁桃体拭子样品或口咽拭子样品等等)。可通过例如活组织检查从任何组织或器官获得组织或器官样品。优选地,组织样品是呼吸组织样品或肺样品。可通过诸如离心或细胞分选之类的分离技术从体液或组织或器官获得分离的细胞。
[0105]
病毒及其衍生产品
[0106]
在本发明中,流感病毒亚型指以血凝素(h或ha)和神经酰胺酶(n)病毒表面蛋白的各种组合为特征的甲型流感病毒变异体。根据本说明书,流感病毒亚型和来自这种病毒亚型的血凝素(ha)可按其h数字来指代,例如“h3亚型的ha”、“h3ha”或“h3流感病毒”。神经酰胺酶(na)可按其n数字来指代,例如“n8亚型的n8”、“n8流感病毒”。术语“亚型”具体包括每个亚型中的所有个体“毒株”,它们通常是由突变引起的,并且可能表现出不同的致病特征。这种毒株也可称为病毒亚型的各种“分离株”。因此,在本文中所用的术语“菌株”和“分离株”可互换使用。
[0107]
本发明发现了感染人的h3n8亚型病毒,所述病毒的ha基因序列如seq id no:1或seq id no:3所示;na基因的序列如seq id no:2或seq id no:4所示,该病毒目前保存于国家病原微生物保藏中心,毒株名称分别为nprc 2.3.280a/hunan-changsha/1000/2022(h3n8);nprc 2.3.279a/henan/4-10/2022(h3n8)。
[0108]
本发明同时提供了一种多肽,所述多肽具有与seq id no:1-4任一所示的序列编码的氨基酸序列相同的序列或者具有与seq id no:1-4任一所示的序列编码的氨基酸序列相同或者具有一定程度的序列一致性或序列同源性的序列。“同源性”可等同于“一致性”。
[0109]
本领域技术人员还将理解的是,多肽可以进行各种翻译后修饰。这些修饰的类型和程度常常取决于用于表达多肽的宿主细胞系以及培养条件。这样的修饰可以包括在糖基化、甲硫氨酸氧化、哌嗪二酮形成、天冬氨酸异构化和天冬酰胺脱酰胺化中的变化。常见修饰是由于羧肽酶的作用导致的羧基末端碱性残基(诸如赖氨酸或精氨酸)的缺失。
[0110]
通常,一个蛋白质中一个或多个氨基酸的修饰不会影响蛋白质或多肽的功能。本领域技术人员会认可改变单个氨基酸或小百分比的氨基酸或对氨基酸序列的个别添加、缺失、插入、替换是保守修饰,其中蛋白质的改变产生具有相似功能的蛋白质。提供功能相似的氨基酸的保守替换表是本领域公知的。
[0111]
本发明同时提供了核酸分子,所述核酸分子具有如seq id no:1-4任一所示的核
苷酸序列;或者具有与seq id no:1-4任一所示的核苷酸序列具有至少70%,优选80%,优选90%,优选95%,优选96%,优选97%,优选98%,优选99%的序列一致性或序列同源性的序列。
[0112]
本领域技术人员还将理解的是所述核酸分子可以进行密码子优化,“密码子优化”是指通过,用在所关注的脊椎动物(例如人)的基因中较频繁或最频繁使用的密码子置换至少一个、超过一个或大量天然序列的密码子,来改变核酸序列以增强在所述脊椎动物细胞中的表达,但核酸序列的改变不改变原始翻译蛋白质的氨基酸序列。各种物种对特定氨基酸的某些密码子呈现出特定的偏好。
[0113]
本发明同时提供了载体,所述载体包括前述的核酸分子。
[0114]
如本发明所用,术语“载体”是指可以将编码蛋白质的多核苷酸可操作地插入其中以引起所述蛋白质表达的媒介物。载体可用于转化、转导或转染宿主细胞,以使其在宿主细胞内表达携带的遗传元件。载体的实例包括质粒;噬菌粒;粘粒和人工染色体,如酵母人工染色体(yac)、细菌人工染色体(bac)或p1衍生的人工染色体(pac);噬菌体,如λ噬菌体或m13噬菌体;和动物病毒。用作载体的动物病毒的类别包括逆转录病毒(包括慢病毒)、腺病毒、腺相关病毒、疱疹病毒(例如单纯疱疹病毒)、痘病毒、杆状病毒、乳头状瘤病毒和乳多空病毒(例如sv40)。载体可以含有多种用于控制表达的元件,包含启动子序列、转录起始序列、增强子序列、选择元件和报告基因。另外,载体可以含有复制起点。术语“复制起点”是指当在载体中存在时其起始复制的序列。复制起点可被复制起始因子或替代地被dna解螺旋酶识别。载体还可以包括有助于其进入细胞的材料,包括但不限于病毒颗粒、脂质体或蛋白质包膜。
[0115]
应用
[0116]
本发明提供了前述的病毒或其衍生产品如多肽、核酸分子或载体在制备针对h3n8的抗体中的应用。通常情况下,病毒或其衍生产品作为免疫原免疫动物产生抗体。所述抗体包括但不限于单克隆抗体,多克隆抗体,具有多表位特异性的抗体,单链抗体,多特异性抗体和抗体片段。此类抗体可以是嵌合的,人源化的,人的和合成的。
[0117]
本发明提供了前述的病毒或衍生产品如多肽、核酸分子或载体在制备疫苗中的应用。
[0118]“疫苗”是指包括至少一种抗原的组合物,该至少一种抗原在注射了疫苗的宿主中引出免疫应答。此种免疫应答可以是针对本发明免疫原组合物的细胞及/或抗体介导的免疫应答。优选地,疫苗引起免疫应答,并且更优选地提供抵抗aiv感染的一种或多种临床症状的保护性免疫。宿主也可以被描述为“受试者”。优选地,本文中所描述或提及的任何宿主或受试者均为动物。
[0119]
通常,“疫苗”包括但不限于以下效果中的一种或多种:产生或激活专门针对本发明疫苗中所包括的一种或多种抗原的抗体、b细胞、辅助性t细胞、抑制性t细胞及/或细胞毒性t细胞及/或γ-δt细胞。进一步,宿主将显示保护性免疫应答或治疗应答。“保护性免疫应答”或“保护性免疫”将通过以下证明:受感染宿主通常所显示的临床症状减少或没有、恢复时间较快及/或传染性持续时间缩短或受感染宿主的组织或体液或排泄物中的病原体滴度降低。
[0120]
下面结合实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而
不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(new york:cold spring harborlaboratory press,1989)中所述的条件,或按照制造厂商所建议的条件。
[0121]
实施例1h3n8亚型病毒的分离及检测
[0122]
1、病料的采集与接种
[0123]
将取自湖南长沙的患者的咽拭子、河南驻马店患者的咽拭子分别置于含双抗的(青霉素和链霉素)磷酸盐缓冲液(pbs)中,震荡后取上清液接种于10日龄鸡胚,每个样品接种两个胚,于37℃孵育箱孵育,72h后用1%的鸡红细胞对鸡胚尿囊液进行血凝检测。对有血凝性样品用spf鸡胚纯化后进行鉴定,无血凝性但有呼吸道症状样品盲传1代。
[0124]
2、病毒的鉴定
[0125]
用spf鸡胚纯化有血凝性的样品,然后提取rna并反转录,并用流感病毒鉴定引物进行扩增,根据凝胶电泳结果鉴定其是否为禽流感。
[0126]
3、病毒rna的提取
[0127]
使用rna试剂盒说明书提取病毒rna。
[0128]
4、病毒rna反转录与pcr
[0129]
根据反转录试剂盒说明书,向病毒rna中加入流感病毒反转录通用引物进行反转录获得cdna,以cdna作为模板,使用通用引物对病毒全基因组片段进行扩增,将pcr产物进行琼脂糖凝胶电泳,并用胶回收试剂盒回收目的产物。
[0130]
5、病毒全基因组序列测定
[0131]
以胶回收产物为模板,利用测序引物以及测序试剂盒对病毒的全基因组序列进行测。
[0132]
6、结果
[0133]
检测结果显示,分离的病毒为h3n8亚型病毒,获取自湖南长沙患者的病毒的ha序列如seq id no:1所示,na序列如seq id no:2所示;获取自河南驻马店患者的病毒的ha序列如seq id no:3所示,na序列如seq id no:4所示。
[0134]
实施例2检测h3n8方法的确定
[0135]
1、收集样品
[0136]
采集于河南驻马店的人咽拭子样本。
[0137]
2、核酸提取
[0138]
使用病毒rna/dna提取试剂盒(货号:64t)提取核酸,具体步骤详见说明书。
[0139]
3、real-time pcr检测h3n8
[0140]
1)设计h3n8亚型的特异性引物探针,序列如下:
[0141]
针对ha基因的引物探针:
[0142]
h3-f-2022 5
’‑
ccattattgcattgaactacattctct-3’(seq id no:5)
[0143]
h3-r-2022 5
’‑
tgttgctgtaytgctgtctttcc-3’(seq id no:6)
[0144]
h3-p-2022 5
’‑
cctggcatttggccagartcttc-3’(seq id no:7)
[0145]
针对na基因的引物探针:
[0146]
n8-f-2022 5
’‑
agctccattgtgatgtgtgg-3’(seq id no:8)
[0147]
n8-r-2022 5
’‑
ggaagaacagctccatcgtg-3’(seq id no:9)
[0148]
n8-p-2022 5
’‑
actatgagattgccgactggtca-3’(seq id no:10)
[0149]
ha基因引物中的y代表兼并密码子:c/t;r代表兼并密码子:a/g;
[0150]
ha的探针为fam荧光标记的探针,na的探针为hex荧光标记的探针。
[0151]
2)real-time pcr检测
[0152]
(1)按照检测的标本数量计算所需pcr反应体系中各成分的体积数。核酸扩
[0153]
增反应液6.25μl/人份,h2o 11.25μl/人份,正向引物1μl/人份,正向引物1μl/人份,探针0.5μl/人份。将反应混合液加到96孔pcr板中,20μl/孔。
[0154]
(2)将位于取5μl的样本核酸,加入已分装好反应液的pcr板中,并设置阴
[0155]
性对照、阳性对照。阴性对照为h2o,阳性对照为环境h3n8的培养病毒a/环境/广西/04905/2022。
[0156]
(3)用光学封板膜将pcr板封好后,短暂离心,放入pcr仪中进行检测,其中,real-time pcr程序如下表所示,检测结束后,查看各检测孔的ct值和扩增曲线,保存实验记录,并导出实验结果。
[0157]
表1 real-time pcr程序
[0158][0159]
4、结果
[0160]
检测结果如表2所示,阴性对照的ct值为0,人样本中呈现显著的h3n8阳性。
[0161]
表2毒株的鉴定结果
[0162][0163]
实施例3不同地区h3n8亚型的检测
[0164]
采用实施例2的方法分别对河南驻马店感染人的h3n8亚型病毒(nprc2.3.279a/henan/4-10/2022)以及湖南感染人的h3n8亚型病毒(nprc 2.3.280a/hunan-changsha/1000/2022)进行检测。
[0165]
检测结果如图1所示,检测试剂能够检测出不同地区来源的感染人的h3n8亚型病毒,其中,图中靠左的两条曲线是河南来源的病毒株,右侧的两条曲线是湖南来源的病毒株。
[0166]
实施例4不同病毒亚型的交叉检测
[0167]
为了验证检测试剂的特异性,采用实施例2的方法对不同的病毒株(病毒株信息如表3所示)进行检测,检测结果如表4所示,检测试剂具有较高的特异性。
[0168]
表3病毒株信息
[0169]
型别毒株名称
h1n1-eaa/hunan/42443/2015h5n1a/environment/hubei-/00950/2013h5n6a/hubei/29578/2016h5n8a/astrakhan/3212/2020h7n9a/hunan/02650/2016h7n9-hpa/guangdong/17sf003/2016h9n2a/guizhou/13392/2020(h9n2)h10n3a/jiangsu/428/2021h1n1pdm09a/广东茂南/swl1536/2019h3n2a/cambodia/e0826360/2020bvb/四川旌阳/12048/2019byb/darwin/58/2019h3n8a/环境/广西/04905/2022
[0170]
表4不同毒株的鉴定结果
[0171]
[0172][0173]
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1