一种猴痘病毒特异性融合蛋白抗原及其制备方法和应用与流程
1.本发明涉及生物工程领域,尤其涉及一种猴痘病毒特异性融合蛋白抗原及其制备方法和应用。
背景技术:
2.猴痘病毒亦称猴天花,与天花病毒和牛痘病毒一样同属于正痘病毒,属于一种人畜共患病的病毒,其发源与非洲热带雨林,根据该病毒的毒力的不同以及危害程度不同,将其分为中非和西非两种病毒。猴痘病毒大小200-300nm,外周有30nm的外膜,内核为匀质的核心体,病毒可以独立复制。
3.一直以来,天花病毒和猴痘病毒被认为是两个最具有潜在生物恐怖威胁的病原。天花病毒由于全世界大规模的安全和廉价疫苗的应用,已经在70-80年代在全球被根除。猴痘病毒在人与人之间传播性差,致死率相对天花病毒较低,但是它的宿主群体广泛(啮齿动物),导致存在被基因修饰为更高毒株的危险性,所以继天花病毒之后猴痘病毒也成为重要的痘病毒传染病。
4.随着50年代初次发现猴痘病毒并命名,70-90年代也相继出现人畜感染的报道,但是一直未引起人类的重视。研发一种猴痘快速检测试剂盒以及检测抗原的工作迫在眉睫。
5.尽管在宿主嗜性和毒力存在差异,但是正痘病毒在病毒形态、生命周期和结构上表现出高度的相似性,蛋白组之间的同源性达到92-95%。因此,寻找一种能有效区分免疫天花病毒疫苗和猴痘病毒感染抗体的抗原显得更为重要,是影响猴痘检测准确性的重要因素。
6.目前,临床和科研过程中都需要针对猴痘病毒的建立特异性快速检测方法。但是,对于该病的病原学诊断方法主要为核酸检测试剂盒、临床症状等方法,而核酸检测试剂盒方法耗时长,临床症状速度慢,均不利于快速诊断。而目前市面上,尚未有猴痘病毒特异性抗原和快速检测方法。如何解决上述技术问题,是目前生物工程技术领域需要解决的技术问题。
技术实现要素:
7.针对上述问题,本发明提供了一种猴痘病毒特异性融合蛋白抗原、其编码基因、以及该抗原的制备方法和应用,该融合蛋白抗原的抗原性和特异性好,为猴痘病毒的快速诊断和这类疾病的防控提供了技术支持。
8.现有的猴痘病毒核酸检测可根据同源基因序列内的单核苷酸多态性的优势,区分猴痘病毒和其他痘病毒。但这种核酸检测需要在病毒仍然存在的情况下收集标本,在感染清除后样品不能用于诊断猴痘。由于先前天花疫苗接种引起的交叉反应性免疫反应,猴痘标准抗体检测的开发变得复杂。
9.考虑到过去的天花疫苗接种的抗牛痘igm抗体应该普遍不存在,所以对样品进行免疫球蛋白m(igm)抗体检测可以用于区分猴痘的感染。为解决本发明提出的上述技术问
题,从患者血清中快速准确检测猴痘状病毒igm抗体显得尤为重要。建立胶体金试纸条检测新型冠状病毒抗体,可有效反映个人的感染情况并做到及时监控,而最基础的是寻找一个猴痘病毒的特异性抗原。而病毒作为天然抗原,其存在风险性大、时效性不足的问题,因此需要研发出一种安全性高、特异性高、时效性高的重组抗原。
10.第一方面,为解决上述问题,本发明提供一种猴痘病毒特异性融合蛋白抗原,其特征在于,其氨基酸序列如seq id no:1所示。
11.上述猴痘病毒特异性融合蛋白抗原包括猴痘病毒b19r蛋白和b21r蛋白的2个优势线性抗原,所述2个优势线性抗原分别为b19r
37-181
和b21r
577-812
, b19r
37-181
位于b19r的第37个氨基酸到第181个氨基酸,b21r
577-812
位于b21r 的第577个氨基酸到第812个氨基酸。
12.申请人经过对猴痘病毒的基因组分析、不断研发和大量实验发现,b19r蛋白是一种ifn-a/b结合蛋白,在猴痘病毒中为352个氨基酸的蛋白,而在牛痘病毒中为一个截断的蛋白,缺失c段的部分氨基酸;而b21r蛋白在牛痘病毒中存在缺失,这个蛋白可以作为区分猴痘病毒和牛痘病毒疫苗候选蛋白。
13.基于上述两个蛋白的特点,申请人利用生物软件分析b19r和b21r氨基酸序列,优先选择b21r蛋白的抗原特异性较强的序列(即优势线性抗原 b21r
577-812
),并补充b19r的线性抗原位点(即优势线性抗原b19r
37-181
)重新组成一种特异性强且灵敏度高(避免漏检)的抗原位点,即得到氨基酸序列如 seq id no:1所示的猴痘病毒特异性融合蛋白抗原。
14.上述猴痘病毒特异性融合蛋白抗原包括序列如seq id no:1所示的氨基酸序列,也包括与seq id no:1所示的序列同源性大于98%或99%,且保持相同抗原活性的氨基酸序列,这些氨基酸序列可为seq id no:1所示序列的某位点氨基酸的替换、缺失或增加。
15.第二方面,本发明还提供一种基因,该基因编码上述猴痘病毒特异性融合蛋白抗原。本领域技术人员可根据本发明公开的猴痘病毒特异性融合蛋白抗原的氨基酸序列以及说明书中内容,基于本领域公知常识得到该抗原的编码基因。
16.可选地,本发明提供一种所述基因的序列,如seq id no:2所示。后续实施例中以seq id no:2所示的基因序列为例说明猴痘病毒特异性融合蛋白抗原的制备,但是其编码序列不限于如seq id no:2所示的基因序列,这也是本领域技术人员可根据本领域公知常识基于前述蛋白序列扩展得到的,属于本发明的保护范围。
17.第三方面,本发明还提供一种重组表达载体,其是将上述基因连接到表达载体所形成。通过基因工程的方法将前述基因酶切连接在目标表达载体,从而获得重组表达载体,并后续通过将该重组表达载体转化到工程菌中,通过诱导该基因的表达,从而得到含有猴痘病毒特异性融合蛋白抗原的发酵产物。
18.可选地,所述重组表达载体包括pet系列载体。优选地,所述表达载体为 pet41a质粒。
19.第四方面,本发明还提供一种重组工程菌,该重组工程菌中转化有上述的重组表达载体。
20.可选地,所述宿主菌为大肠杆菌bl21(de3)、大肠杆菌rosseta或者其他大肠杆菌突变表达菌株。
21.使用真核表达抗原存在抗原产量低、成本高以及在短时间难以放大产出等问题,因此,申请人选择大肠杆菌表达系统生产特异性猴痘病毒抗原,其具有制备简单、成本低
廉,易于短时间放大产出的优点,明显提高检测猴痘病毒的时效性。
22.第五方面,本发明还提供一种制备上述猴痘病毒特异性融合蛋白抗原的方法,其包括以下步骤:
23.对如前所述的重组工程菌进行发酵,诱导表达猴痘病毒特异性融合蛋白抗原,再对发酵产物进行分离和纯化,得到猴痘病毒特异性融合蛋白抗原。
24.优选地,所述方法包括以下步骤:
25.s1、重组表达载体的构建:将前述的基因克隆到表达载体中,得到重组表达载体;
26.s2、工程菌的构建:将得到的重组表达载体转入宿主菌,得到重组工程菌;
27.s3、工程菌的发酵:利用重组工程菌诱导表达猴痘病毒特异性融合蛋白抗原; s4、猴痘病毒特异性融合蛋白抗原的分离和纯化:分离和纯化步骤3得到的发酵产物,得到猴痘病毒特异性融合蛋白抗原。
28.上述猴痘病毒特异性融合蛋白抗原的纯化方法包括但不限于层析、透析或本领域已知的其它方法。
29.第六方面,本发明还提供上述猴痘病毒特异性融合蛋白抗原在制备猴痘病毒检测试剂、生产用于诱导针对猴痘病毒的免疫反应的药剂,或在生产用于预防猴痘病毒感染的药剂中的应用。基于猴痘病毒特异性融合蛋白抗原的特性,本领域技术人员结合本领域常识可知晓其在上述方面可进行应用。
30.上述应用包括所述猴痘病毒特异性融合蛋白抗原在制备猴痘病毒疫苗中的用途。
31.第七方面,本发明还提供一种试剂盒,其包括上述的猴痘病毒特异性融合蛋白抗原、编码猴痘病毒特异性融合蛋白抗原的基因、前述的重组表达载体或前述的重组工程菌。可根据上述抗原、基因以及表达载体和工程菌的用途,将其分别或者组合制成不同的试剂盒,满足不同的使用需求。
32.可选地,上述试剂盒为一种猴痘病毒抗体检测试剂盒,其包括上述猴痘病毒特异性融合蛋白抗原。本领域技术人员可根据本发明公开内容和本领域常识,利用上述猴痘病毒特异性融合蛋白抗原制备检测试剂盒,用于快速检测样品中的猴痘病毒,从而判断检测对象是否是猴痘病毒感染者。
33.本发明具有以下有益效果:
34.1、本发明首次提供一种猴痘病毒特异性融合蛋白抗原,并提供可高效表达该抗原的重组工程菌以及该抗原的制备方法,该方法的制备简单、成本低廉,易于短时间放大产出的优点,明显提高检测猴痘病毒的时效性。同时,该方法制备得到的猴痘病毒特异性融合蛋白抗原具有较好的抗原性和特异性,可有效区分猴痘和其他正痘病毒,提高检测的准确性。
35.2、可利用上述融合蛋白抗原制备对应的猴痘病毒检测试剂盒,该试剂盒能快速检测人体血清中的猴痘病毒抗体,并依此判断检测对象是否感染猴痘病毒,检测的特异性好,为猴痘病毒的快速诊断和这类疾病的防控提供了技术支持。
附图说明
36.图1为b19r的氨基酸序列分析结果;
37.图2为b21r的氨基酸序列分析结果;
38.图3为重组表达载体双酶切鉴定琼脂糖凝胶电泳图;其中泳道1为dna分子maker,
泳道2为构建重组表达载体用bamhi和xhoi双酶切后琼脂糖凝胶电泳图。
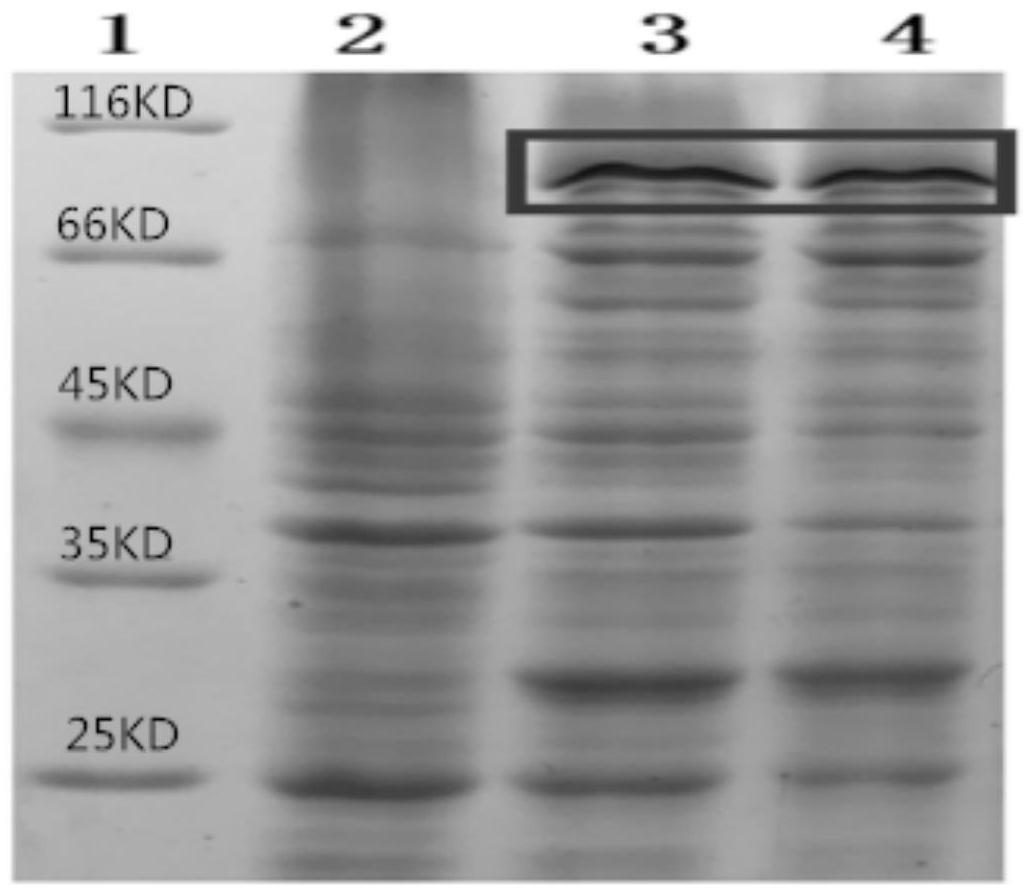
39.图4为重组工程菌阳性表达结果的sds-page结果图;
40.其中,泳道1为蛋白分子maker,泳道2为未诱导对照组,泳道3和4为诱导表达组。
具体实施方式
41.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。在本发明中,如无特殊说明,所采用的设备、原料等均可从市场购得或是本领域常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
42.本发明以猴痘病毒与其它正痘病毒差异性最大的b19r和b21r蛋白为基础,通过生物信息学软件对猴痘病毒b21r蛋白(ncbi序列号np_536609.1)和b19r (ncbi序列号np_536607.1)氨基酸的序列进行分析,将筛选得到的优势抗原表位按照一定顺序进行串联,构建并合成多表位融合抗原;同时,进行密码子优化后合成该蛋白的核酸序列,构建高效原核表达载体,纯化高纯度的重组蛋白。
43.为了使得本领域技术人员能够更加清楚地了解本技术的技术方案,以下将结合具体的实施例详细说明本技术的技术方案。
44.实验材料及方法
45.1、菌种与质粒:宿主菌采用bl21(de3),质粒采用pet41a,购自大连宝生物(takara)工程有限公司。
46.2、分子生物学试剂:限制性内切酶采用bamhⅰ和xhoi,t4连接酶为takara 的产品;质粒纯化试剂盒及dna片段琼脂糖凝胶回收试剂盒为德国qiagen的产品;iptg为promega的产品。其他试剂为进口或者国产分析纯试剂。
47.3、基因的合成和dna序列测序:由上海生工生物公司完成。
48.4、基因克隆方法:dna酶切、连接、电泳、质粒的提取纯化、蛋白的sds-page 分析等一般的分子克隆方法按常规方法进行。其他试剂盒的使用方法按说明书进行具体操作。
49.实施例1抗原表位的筛选
50.参考ncbi上公布的猴痘病毒b19r蛋白(ncbi序列号np_536607.1)和 b21r蛋白氨基酸序列(ncbi序列号np_536609.1),利用expasy、uniprot 等在线分析工具分析蛋白的二级结构和三级结构域,结合bepipred linearepitope prediction 2.0等在线软件分析线性抗原位点结果,在此技术上综合分析并筛选出猴痘病毒优势线性抗原。
51.筛选出的猴痘病毒b19r蛋白特异性线性抗原b19r
37-181
,位于该蛋白序列的第37个氨基酸到第181个氨基酸,b21r蛋白特异性线性抗原b21r
577-812
位于该蛋白序列的第577个氨基酸到第812个氨基酸。具体bepipred linearepitope prediction 2.0分析结果见图1和图2。
52.实施例2猴痘病毒特异性抗原表位基因获取
53.将编码上述优势抗原表位的两个基因按照一定的排列组合串联,具体顺序如下b19r
37-181
和b21r
577-812
,构建了含有2个多表位的融合抗原基因,经过稀有密码子在线软件对融合基因中的大肠杆菌稀有密码子进行分析,并用编码相同氨基酸的大肠杆菌偏爱密码
子核苷酸替换大肠杆菌的稀有密码子,使最终合成的多表位融合基因中不含有大肠杆菌的稀有密码子,最后得到猴痘病毒特异性融合蛋白抗原的核苷酸序列,该核苷酸序列如seq id no:2所示,接着在该序列两端分别增加bamh和xhoi限制性内切酶的酶切位点后,请上海生工生物公司合成上述添加酶切位点后的上述猴痘病毒特异性融合蛋白抗原核苷酸序列。
54.实施例3构建猴痘病毒特异性抗原的表达载体
55.1、实验方法:
56.使用试剂盒提取pet41a质粒,对该质粒进行bamhⅰ和xhoi双酶切,电泳后通过琼脂糖凝胶回收试剂盒回收双酶切后的大片段,同时用bamhⅰ和 xhoi双酶切猴痘病毒特异性融合蛋白抗原的编码基因,电泳后胶回收,-20℃备用。
57.将双酶切后的pet41a质粒和双酶切目的片段(猴痘病毒特异性融合蛋白抗原的编码基因)按1:3~1:10的比例混合,用t4连接酶16℃过夜连接,连接后即为重组表达载体,命名为pet41a-br。
58.实施例4重组表达载体的筛选和鉴定
59.1、将上述重组表达载体pet41a-br转化大肠杆菌bl21(de3),涂布含氨苄青霉素(60ug/ml)lb平板上,37℃恒温培养箱过夜。次日随机挑取5 个转化菌落和2个对照菌落(转化有质粒pet41a),分别提取质粒。
60.2、对提取的重组表达载体pet41a-br进行bamhⅰ和xhoi双酶切,酶切后进行琼脂糖凝胶电泳分析,由图3发现:第二泳道中电泳条带上能看见目的片段(猴痘病毒特异性融合蛋白抗原的编码基因)和载体片段,与预期目的条带1143bp和载体条带大小一致,结果显示构建重组表达载体成功,该菌即转化有重组表达载体pet41a-br的阳性重组工程菌。
61.实施例5阳性重组工程菌鉴定后高效表达
62.1、实验方法:
63.将鉴定阳性表达的工程菌和对照菌分别接种至2mllb培养基(添加 60ug/ml氨苄青霉素)的试管中,37℃恒温摇床振荡2h,加iptg(终浓度为 0.5mmol/l),继续30℃诱导6h。接着,离心并收集菌体,并进行sds-page 检测。
64.2、实验结果及分析
65.如图4的sds-page检测结果显示,pet41a-br表达的目的蛋白(猴痘病毒特异性融合蛋白抗原)的大小在66kd与116kd之间,75kd附近的位置,与expsy protparam在线软件预测结果75kd相符;且对照菌中无目的蛋白条带,该结果说明成功获得了表达猴痘病毒特异性融合蛋白抗原的重组工程菌。
66.实施例6表达蛋白的纯化
67.1、实验方法:
68.(1)将高效表达的重组工程菌在低温(4℃)条件下进行高速(12000rpm) 离心15min,将沉淀的菌体重悬于原菌液体积的1/10的0.01m pbs(ph7.4) 中,充分洗涤1次,高速(12000rpm)低温(4℃)离心15min,将沉淀重悬于原菌液体积的1/10的0.01m pbs(ph7.4)中,冰浴超声30min,12000rpm, 4℃离心20min,pet41a-br表达的蛋白以包涵体形式存在,收集沉淀为包涵体蛋白。
69.(2)将包涵体先用0.01m pbs(ph7.4)洗涤1次,然后用包涵体溶解液溶解(包涵体溶解液配方为50mmnah2po4
·
2h2o,500mm nacl,8m urea (尿素)),4℃溶解6h,12000rpm/
min,4℃离心20min,收集上清并将上清液经0.22um滤膜过滤后,得到蛋白质样品,用于后续纯化。
70.(3)纯化方法为:将前一步得到的蛋白质样品进行镍柱纯化(镍柱的规格是博格隆(上海)生物技术有限公司,货号aa0062),按0.5ml/min的流速使上述蛋白样品缓慢流过镍柱,用5倍柱床体积的包涵体溶解液洗涤层析柱。接着,流速不变,用10倍柱体积的洗杂缓冲液(配方为8murea,50mmnah2po4
·
2h2o,500mm nacl,20mm imid)洗掉杂蛋白;最后按照0.8ml/min 的流速用洗脱buffer(洗脱buffer采用8murea,50mm nah2po4
·
2h2o, 500mm nacl,500mm imid)洗脱目的蛋白,得到洗脱液。
71.(4)将洗脱液进行sds—page检测后,收集含有高纯度目的蛋白的洗脱液,并将其经urea梯度透析复性。
72.urea梯度透析复性的操作方法具体为,采用的复性液为20mm tris-hcl, 6m urea,ph9.0,逐渐降低复性液中的urea浓度为4m、2m、0m,每个梯度透析液的透析时间为2h,依次透析完后,用2l的20mm tris-hcl,ph9.0 透析48h,再对产物进行12000rpm/min,4℃离心20min,收集上清液即为目的融合蛋白(猴痘病毒特异性融合蛋白抗原)。
73.上述摇瓶发酵纯化方法制备得到的融合蛋白的纯度为90%,浓度为 2mg/ml,上述制备方法得到的融合蛋白的产量为每1l摇瓶发酵液产蛋白 10mg。
74.实施例7融合蛋白的多抗血清的制备
75.利用实施例6中纯化的猴痘病毒特异性融合蛋白抗原制备多抗血清,用该抗原和佐剂联合免疫新西兰大耳白兔的方式,制备并纯化获得的兔抗血清,再通过间接elisa法检测抗猴痘病毒特异性融合蛋白抗原的抗体的滴度。
76.1、主要试剂:完全弗氏佐剂和不完全弗氏佐剂为sigma公司产品,其他试剂为国产或进口分析纯试剂。
77.2、免疫程序
78.将实施例6纯化得到的融合蛋白作为免疫原,免疫5只新西兰大耳兔,每只免疫200ug抗原,免疫方式为背部多点免疫。第一次免疫使用1ml完全弗氏佐剂与400ug融合蛋白混合乳化,两周后第二次免疫,用1ml不完全弗氏佐剂和400ug融合蛋白混合乳化,免疫方式为背部多点免疫。三天后第三次免疫,用100ug的融合蛋白和相同体积的0.01mpbs(ph7.4)混合,免疫方式为腹腔免疫。三天后,同样免疫程序(即用100ug的融合蛋白和相同体积的0.01mpbs(ph7.4)混合进行腹腔免疫)免疫一次。
79.3、间接elisa测定兔抗血清的效价
80.最后一次免疫后三天,兔耳缘静脉取血,4000rpm离心10min获取兔抗血清。取融合蛋白用碳酸盐缓冲液(50mm,ph9.6)稀释后100ul/孔、100ng/ 孔的蛋白量包被酶联板,4℃过夜。次日20%小牛血清封闭,37℃水浴封闭2h,将兔抗血清梯度稀释作为一抗,37℃水浴孵育1h后,加1:5000二抗羊抗兔,加显色液显色。
81.实验结果显示,抗猴痘病毒特异性融合蛋白抗原的抗体的效价不低于 1:50000,这说明本发明提供的融合蛋白抗原具有较好的抗原性和特异性。
82.可以理解的是,对本领域普通技术人员来说,可以根据本发明的技术方案及本发明构思加以等同替换或改变,而所有这些改变或替换都应属于本发明所附的权利要求的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1