异烟肼半抗原衍生物、异烟肼人工抗原、杂交瘤细胞株、异烟肼单克隆抗体及应用的制作方法
1.本发明属于药物监测技术领域,具体涉及异烟肼半抗原衍生物、异烟肼人工抗原、杂交瘤细胞株、异烟肼单克隆抗体及应用。
背景技术:
2.异烟肼(isoniazid,inh,化学名为4-吡啶甲酰肼)具有抗菌杀菌的作用,是抗结核一线用药。inh经吸收后,需要在患者体内病灶部位达到一定的浓度才能起到抑制或杀灭结核分枝杆菌的作用。但inh有效治疗窗较窄,inh的浓度过低可能导致治疗失败或产生耐药,inh浓度过高时,又容易因高剂量和长期使用而引起肝、肾和神经等多方面的药物不良反应。因此,在inh用药过程中需进行血药浓度监测才能达到临床合理用药。
3.中国专利cn 110672576 a公开了一种利用量子点荧光猝灭法测定异烟肼的方法,但是该方法只能测试简单缓冲液中的异烟肼,如药品中的异烟肼含量。对于临床样本中异烟肼的测定,由于基质成分复杂,而难以测定。
4.中国专利cn 111848507 a公开了一种从异烟肼的酰肼基团部位进行衍生的半抗原结构,但是该衍生位点破坏了异烟肼与异烟肼主要代谢物(异烟酸和乙酰异烟肼等)的特征差异基团,反而暴露出来共有结构,会导致制备的抗体对代谢物存在交叉反应。文献(kam, s. tse, et al. "antibodies specific to isoniazid and isonicotinic acid." the journal of immunology 116.4 (1976): 965-969.)公开了对inh的酰肼基团部位进行衍生制备的异烟肼抗体,然而,其制备的抗体在检测inh中对异烟酸也存在显著的交叉反应。因此,开发满足inh的临床检测特异性的异烟肼抗体具有重要的意义。
技术实现要素:
5.有鉴于此,本发明提供了异烟肼半抗原衍生物、异烟肼人工抗原、杂交瘤细胞株、异烟肼单克隆抗体及应用。本发明提供的异烟肼半抗原衍生物与载体蛋白结合形成的异烟肼人工抗原免疫动物后产生的异烟肼单克隆抗体能够高灵敏度特异性识别异烟肼,满足异烟肼的临床检测特异性需求。
6.本发明提供一种异烟肼半抗原衍生物,具有式i所示结构:式i。
7.本发明提供了上述技术方案所述的异烟肼半抗原衍生物的制备方法,包括以下步骤:异烟肼和丙酮在碱性条件下进行缩合反应,得到中间体1;将所述中间体1、丁二酸单甲酯、过硫酸盐、三氟乙酸、金属盐催化剂和水混合,进行氧化脱羧反应,得到中间体2;将所述中间体2进行碱性水解反应后酸化,得到所述异烟肼半抗原衍生物;
。
8.本发明提供了一种异烟肼人工抗原,具有式ii所示结构:式ii;所述式ii中n为上述技术方案所述的异烟肼半抗原衍生物和载体蛋白的偶联比,n为1~40;所述式ii中的载体蛋白为具有免疫原性的蛋白质或多肽。
9.优选的,所述式ii中的载体蛋白包括血清白蛋、鸡卵清蛋白或牛甲状腺球蛋白。
10.本发明提供了上述技术方案所述异烟肼人工抗原的制备方法,包括以下步骤:将式i所示结构的异烟肼半抗原衍生物、有机胺盐类交联剂和极性溶剂混合进行活化,得到活化的异烟肼半抗原衍生物溶液;将所述活化的异烟肼半抗原衍生物溶液和载体蛋白的缓冲液混合进行酰胺化反应,得到式ii所示结构的异烟肼人工抗原。
11.本发明提供了一种产生异烟肼单克隆抗体的杂交瘤细胞株,所述杂交瘤细胞株的保藏编号为cgmcc no.:45165。
12.本发明提供了一种异烟肼单克隆抗体,由上述技术方案所述的杂交瘤细胞株产生。
13.本发明提供了上述技术方案所述的异烟肼半抗原衍生物和/或上述技术方案所述的异烟肼单克隆抗体在制备检测异烟肼中的应用。
14.本发明提供了一种异烟肼均相酶免疫检测试剂,包括独立分装的试剂r1和试剂r2;所述试剂r1包括酶底物和上述技术方案所述的异烟肼单克隆抗体;所述试剂r2包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和葡萄糖-6-磷酸脱氢酶的偶联物。
15.本发明提供了一种异烟肼磁微粒化学发光检测试剂,包括独立分装的磁微粒工作液和酶标工作液;所述磁微粒工作液包括磁珠和上述技术方案所述的异烟肼单克隆抗体;所述酶标工作液包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和血清碱性磷酸酶的偶联物。
16.本发明提供一种异烟肼半抗原衍生物,具有式i所示结构。本发明提供的异烟肼半抗原衍生物,将异烟肼如式i氮杂环相应结构位置上的h取代为-ch
2-ch
2-ch
2-cooh,羧基衍生位点远离酰肼特征结构,使得酰肼特征结构更好的暴露出来,从而实现对异烟肼的特异性识别,且以-ch
2-ch
2-ch
2-cooh作为偶联臂偶联蛋白得到的异烟肼抗原能够准确获得对异烟肼具有特异性结合能力的抗体,满足异烟肼的临床检测特异性、高灵敏度和准确性的需求。
17.本发明还提供了一种产生异烟肼单克隆抗体的杂交瘤细胞株,所述杂交瘤细胞株
的保藏编号分别cgmcc no.:45165。本发明提供的杂交瘤细胞株能够产生异烟肼单克隆抗体,产生的异烟肼单克隆抗体具有能够高灵敏度等效识别异烟肼的能力,同时具备优于现有已知抗体的特异性,与异烟肼主要代谢物(乙酰异烟肼、异烟酸、烟酰胺、氨基水杨酸)无明显的交叉反应,满足异烟肼的临床检测特异性、高灵敏度和准确性的需求。
18.本发明还提供了一种异烟肼单克隆抗体,由上述技术方案所述的产生异烟肼单克隆抗体的杂交瘤细胞产生。本发明的异烟肼单克隆抗体具有能够高灵敏度等效识别异烟肼的能力,同时具备优于已知抗体的特异性,与异烟肼对主要代谢物(乙酰异烟肼、异烟酸、烟酰胺、氨基水杨酸)无明显的交叉反应,满足异烟肼的临床检测特异性、高灵敏度和准确性的需求。
19.本发明还提供了上述技术方案所述的异烟肼单克隆抗体在制备检测异烟肼试剂中的应用。由于本发明的异烟肼单克隆抗体具有能够高灵敏度等效识别异烟肼的能力,使其能够应用于制备检测异烟肼的检测试剂(异烟肼均相酶免疫检测试剂和异烟肼磁微粒化学发光检测试剂),满足异烟肼的临床检测特异性、高灵敏度和准确性的需求。
附图说明
20.图1为实施例1制备的异烟肼半抗原衍生物的氢谱图;图2为实施例4磁微粒发光法得到的异烟肼定标曲线图;图3为实施例5构建的均相酶法同lc-ms法的测定异烟肼的结果比对图。
具体实施方式
21.本发明提供一种异烟肼半抗原衍生物,具有式i所示结构:式i。
22.本发明提供了上述技术方案所述的异烟肼半抗原衍生物的制备方法,包括以下步骤:异烟肼和丙酮在碱性条件下进行缩合反应,得到中间体1;将所述中间体1、丁二酸单甲酯、过硫酸盐、三氟乙酸、金属盐催化剂和水混合,进行氧化脱羧反应,得到中间体2;将所述中间体2进行碱性水解反应后酸化,得到所述异烟肼半抗原衍生物;。
23.在本发明中,如无特殊说明,所用原料均为本领域技术人员熟知的市售产品。
24.本发明异烟肼和丙酮在碱性条件下进行缩合反应,得到中间体1。
25.在本发明中,所述异烟肼和丙酮的质量比优选为(2~3):1,更优选为(2.7~2.8):1。
26.在本发明中,所述碱性条件优选由氢氧化物提供,所述氢氧化物优选包括naoh和koh中的一种或两种;所述氢氧化物优选以氢氧化物水溶液形式使用,所述氢氧化物水溶液的浓度优选为0.5~2mol/l,更优选为1~1.5mol/l;本发明对于所述氢氧化物的用量没有特
殊限定,能够将体系的ph值调节至12~13即可;在本发明的具体实施例中,所述异烟肼的质量与氢氧化物的物质的量之比优选为13.7g:0.04mol。
27.在本发明中,所述缩合反应的温度优选为40~55℃,更优选为45~50℃;所述缩合反应的时间优选为1~3h,更优选为2h。
28.完成所述缩合反应后,本发明优选将所得缩合反应液依次进行除丙酮、结晶和固液分离,将所得固体组分进行干燥,得到中间体1。本发明对于所述丙酮除去的方式没有特殊限定,能够将丙酮除去即可,具体如减压蒸馏。在本发明中,所述结晶用溶剂优选包为水,所述异烟肼和结晶用水的质量比优选为(10~15):1,更优选为(13~14):1。在本发明中,所述结晶的温度优选为10~15℃,更优选为12~13℃;所述结晶的时间优选为1~3h,更优选为2h。本发明对于所述固液分离的方式没有特殊限定,采用本领域技术人员熟知的固液分离方式即可,具体如过滤。在本发明中,所述干燥优选为真空干燥,所述真空干燥的温度优选为40~50℃,更优选为43~47℃。
29.得到中间体1后,本发明将所述中间体1、丁二酸单甲酯、过硫酸盐、三氟乙酸、金属盐催化剂和水混合,进行氧化脱羧反应,得到中间体2。
30.在本发明中,所述中间体1和丁二酸单甲酯的质量比优选为1:(0.7~0.8),更优选为1:0.76。在本发明中,所述过硫酸盐优选包括过硫酸铵和过硫酸钠中的一种或两种。在本发明中,所述中间体1和过硫酸盐的质量比优选为1:(5~10),更优选为1:(6~7)。在本发明中,所述中间体1和三氟乙酸的质量比优选为1:(0.5~1),更优选为1:0.65。在本发明中,所述中间体1和金属盐催化剂的质量比优选为1:(1.8~2.2),更优选为1:2;所述金属盐催化剂优选包括硝酸银。本发明对于所述水的用量没有特殊限定,能够保证氧化脱羧反应顺利进行即可,在本发明的具体实施例中,所述中间体1和水的质量比优选为1:30。
31.本发明对于所述混合没有特殊限定,能够将原料混合均匀即可,具体如过搅拌混合。
32.在本发明中,所述氧化脱羧反应的温度优选为20~25℃,更优选为22~23℃,所述氧化脱羧反应的时间优选为1~3h,更优选为2h。
33.完成所述氧化脱羧反应后,本发明优选还包括将所得氧化脱羧反应液进行有机溶剂萃取,将所得有机层进行浓缩,得到中间体2。在本发明中,所述萃取用有机溶剂优选包括乙酸乙酯。本发明对于所述浓缩的方式没有特殊限定,浓缩至恒重即可,具体如减压蒸馏。
34.得到中间体2后,本发明将所述中间体2进行碱性水解反应后酸化,得到所述异烟肼半抗原衍生物。
35.在本发明中,所述碱性水解反应优选在氢氧化物存在条件下进行,所述氢氧化物优选包括naoh和koh中的一种或两种;所述氢氧化物优选以氢氧化物水溶液形式使用,所述氢氧化物水溶液的浓度优选为0.5~2mol/l,更优选为1mol/l;本发明对于所述氢氧化物的用量没有特殊限定,能够将体系的ph值调节至11~13即可,ph值更优选为12。在本发明中,所述酸化用酸优选包括盐酸和硫酸中的一种或两种;所述盐酸的浓度优选为0.5~2mol/l,更优选为1mol/l;本发明对于所述酸的用量没有特殊限定,能够将体系的ph值调节至4~5即可,ph值更优选为4.5。
36.完成所述酸化后,本发明优选将所得酸化反应液依次进行结晶和固液分离,将所得固体组分进行干燥,得到所述异烟肼半抗原衍生物。在本发明中,所述结晶的温度优选为
10~15℃,更优选为12~13℃;所述结晶的时间优选为1~3h,更优选为2h。本发明对于所述固液分离的方式没有特殊限定,采用本领域技术人员熟知的固液分离方式即可,具体如过滤。在本发明中,所述干燥优选为真空干燥,所述干燥的温度优选为40~50℃,更优选为43~47℃;本发明对于所述干燥的时间没有特殊限定,干燥至恒重即可。
37.本发明提供一种异烟肼人工抗原,具有式ii所示结构:式ii;所述式ii中n为上述技术方案所述的异烟肼半抗原衍生物和载体蛋白的偶联比,所述n为1~40;所述式ii中的载体蛋白为具有免疫原性的蛋白质或多肽。
38.在本发明中,所述式ii中的载体蛋白优选包括血清白蛋、鸡卵清蛋白或牛甲状腺球蛋白,更优选为血清白蛋;所述血清蛋白优选包括牛血清白蛋白、人血清白蛋白或兔血清白蛋白,更优选为牛血清白蛋白。
39.本发明提供了上述技术方案所述的异烟肼人工抗原的制备方法,包括以下步骤:将式i所示结构的异烟肼半抗原衍生物、有机胺盐类交联剂和极性溶剂混合进行活化,得到活化的异烟肼半抗原衍生物溶液;将所述活化的异烟肼半抗原衍生物溶液和载体蛋白的缓冲液混合进行酰胺化反应,得到式ii所示结构的异烟肼人工抗原。
40.本发明将式i所示结构的异烟肼半抗原衍生物、有机胺盐类交联剂和极性溶剂混合进行活化,得到活化的异烟肼半抗原衍生物溶液。
41.在本发明中,所述有机胺盐类交联剂优选包括1-(3-二甲基氨基丙基)-3-乙基碳化二亚胺盐酸盐(edc)和n,n'-二环己基碳二亚胺和氯甲酸乙酯中的一种或两种,更优选为1-(3-二甲基氨基丙基)-3-乙基碳化二亚胺盐酸盐。在本发明中,所述异烟肼半抗原衍生物和有机胺盐类交联剂的质量比优选为1:(1~10),更优选为1:(1~5)。
42.在本发明中,所述极性溶剂优选为有机溶剂和水的混合溶剂,所述有机溶剂优选包括二甲基亚砜(dmso)、n,n-二甲基甲酰胺(dmf)和乙腈中的一种或几种;所述有机溶剂和水的体积比优选为1:(0.05~0.2),更优选为1:0.1。
43.在本发明中,所述混合优选包括以下步骤:将所述异烟肼半抗原衍生物溶解于有机溶剂中,得到异烟肼半抗原衍生物溶液;将所述有机胺盐类交联剂溶解于水中,得到交联剂溶液;将所述化学交联剂溶液加入所述异烟肼半抗原衍生物溶液中。在本发明中,所述异烟肼半抗原衍生物溶液的浓度优选为5~50mg/ml,更优选为10~30mg/ml。在本发明中,所述交联剂溶液的浓度优选为5~100mg/ml,更优选为50~100mg/ml。
44.在本发明中,所述活化的温度优选为4~40℃,更优选为20~30℃;所述活化的时间优选为1~20h,更优选为2~10h。
45.得到活化的异烟肼半抗原衍生物溶液后,本发明将所述活化的异烟肼半抗原衍生物溶液和载体蛋白的缓冲液混合进行酰胺化反应,得到式ii所示结构的异烟肼人工抗原。
46.在本发明中,所述载体蛋白的缓冲液优选为载体蛋白的磷酸盐缓冲液(pbs缓冲液)。在本发明中,所述载体蛋白的缓冲液中载体蛋白的浓度优选为4~20mg/ml,更优选为4~10mg/ml。在本发明中,所述pbs缓冲液的ph值优选为7.2~7.8,更优选为7.4。
47.在本发明中,所述异烟肼半抗原衍生物和载体蛋白的质量比优选为1:(1~3),更优选为1:2。
48.本发明对于所述混合没有特殊限定,能够将原料混合均匀即可,具体如搅拌混合。在本发明中,所述酰胺化反应的温度优选为4~40℃,更优选为20~30℃,所述酰胺化反应的时间优选为1~5h,更优选为2~3h;所述酰胺化反应优选在搅拌的条件下进行,本发明对所述搅拌的具体实施过程没有特殊要求。
49.所述酰胺化反应后,本发明优选还包括将所得酰胺化反应液进行透析纯化,得到所述异烟肼人工抗原。在本发明中,所述透析纯化使用的透析液优选为pbs缓冲液;所述pbs缓冲液的ph值优选为7.2~7.8,更优选为7.4。在本发明中,所述透析纯化使用的透析膜的截留分子量优选为3000~30000da,更优选为7000~15000da。在本发明中,所述透析纯化的次数优选为2~6次,更优选为3~4次。
50.在本发明中,所述异烟肼人工抗原优选保存于-70~-15℃条件下,更优选为-30~-20℃。
51.本发明还提供了一种产生异烟肼单克隆抗体的杂交瘤细胞株,所述杂交瘤细胞株(2c1)的保藏编号为cgmcc no.:45165,它保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏日期为2022年5月19日,保藏地址为北京市朝阳区北辰西路1号院3号,邮编为100101,分类名为杂交瘤细胞株。
52.在本发明中,所述产生异烟肼单克隆抗体的杂交瘤细胞株的制备方法优选包括以下步骤:对动物依次进行第一免疫和第二免疫,得到免疫动物;提取所述免疫动物的脾细胞并和sp2/0细胞进行融合,得到融合细胞;对所述融合细胞进行杂交瘤筛选。
53.本发明对动物依次进行第一免疫和第二免疫,得到免疫动物。在本发明中,所述动物优选包括小鼠、兔、山羊和绵羊中的一种或多种,更优选为小鼠。在本发明中,所述第一免疫的试剂优选为异烟肼人工抗原-pbs溶液和弗氏完全佐剂等体积混合乳化的溶液;所述异烟肼人工抗原-pbs溶液的浓度优选为1mg/ml。在本发明中,所述第一免疫的免疫次数优选为1次;每次第一免疫的免疫剂量优选为0.01~0.2mg/只。在本发明中,所述混合乳化的温度优选为15~30℃,更优选为20~25℃;所述混合乳化的时间优选0.1~1h,更优选为0.5h。在本发明中,所述第二免疫和第一免疫之间优选间隔2~6周。在本发明中,所述第二免疫的试剂优选为异烟肼人工抗原-pbs溶液和弗式不完全佐剂等体积混合乳化的溶液;所述异烟肼人工抗原-pbs溶液中异烟肼人工抗原与弗式不完全佐剂用量比优选为1mg:0.5~2ml,更优选为1mg:1~1.5ml;所述异烟肼人工抗原-pbs溶液的浓度优选为1mg/ml。在本发明中,所述第二免疫的次数优选为3~6次,更优选为4~5次;每次第二免疫的免疫剂量优选为0.01~0.2mg/只;两次第二免疫之间优选间隔1周。在本发明中,所述第一免疫的试剂和第二免疫的试剂中的pbs缓冲液的ph值独立地优选为7.2~7.8,更优选为7.4。
54.得到免疫动物后,本发明提取所述免疫动物的脾细胞并和sp2/0细胞进行融合,得到融合细胞。在本发明中,所述提取免疫动物的脾细胞优选在最后一次免疫的一周后进行。本发明对于所述融合没有特殊限定,采用本领域技术人员熟知的融合方法即可,具体如参考文献(national research council. "monoclonal antibody production." (1999).)
公开的方法进行。
55.得到融合细胞后,本发明对所述融合细胞进行杂交瘤筛选。在本发明的具体实施例中,所述杂交瘤筛选优选包括以下步骤:采用异烟肼-牛甲状腺球蛋白1ug/ml包被elisa 96孔板,对融合细胞进行效价及竞争测定。
56.在本发明中,所述杂交瘤时,本发明优选通过间接竞争elisa评估筛选不同杂交瘤细胞株获得的异烟肼抗体对异烟肼的特异性识别效率。
57.本发明还提供了一种异烟肼单克隆抗体,由上述技术方案所述杂交瘤细胞产生。在本发明中,所述异烟肼抗体分别命名为抗体2c1和抗体12w2。
58.在本发明中,由所述的产生异烟肼单克隆抗体的杂交瘤细胞产生异烟肼单克隆抗体的方法优选包括:依次进行腹水制备和protein a/g纯化。本发明对所述腹水制备和protein a/g纯化的操作不做具体限定,采用本领域技术人员熟知的技术手段即可。
59.本发明还提供了上述技术方案所述的异烟肼半抗原衍生物和/或上述技术方案所述所述的异烟肼单克隆抗体在制备检测异烟肼中的应用。
60.本发明提供一种异烟肼均相酶免疫检测试剂,包括独立分装的试剂r1和试剂r2;所述试剂r1包括酶底物和上述技术方案所述的异烟肼单克隆抗体;所述试剂r2包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和葡萄糖-6-磷酸脱氢酶的偶联物。
61.本发明提供的异烟肼均相酶免疫检测试剂包括独立分装的试剂r1。在本发明中,所述试剂r1包括酶底物和上述技术方案所述的异烟肼单克隆抗体。在本发明中,所述酶底物优选为葡萄糖-6-磷酸(g6p)。在本发明中,所述试剂r1中优选还包括tris缓冲液,所述tris缓冲液的ph值优选为8.0~8.5,更优选为8.0。
62.在本发明中,所述试剂r1的制备方法包括以下步骤:将烟酰胺腺嘌呤二核苷酸(nad)、酶底物和tris缓冲液混合,得到酶底物溶液;将所述酶底物溶液和异烟肼单克隆抗体混合,得到所述试剂r1。在本发明中,所述酶底物溶液中nad的浓度优选为10~30mmol/l,更优选为20mmol/l;所述酶底物溶液中酶底物的浓度优选为20~40mmol/l,更优选为30mmol/l。在本发明中,所述tris缓冲液的ph值优选为8.0~8.5,更优选为8.0。在本发明中,所述酶底物溶液中nad、酶底物和tris缓冲液的摩尔比优选为20:(25~35):(50~60),更优选为20:30:55。在本发明中,所述试剂r1中异烟肼单克隆抗体的质量百分含量优选为0.01~0.1%,更优选为0.05%。在本发明中,所述异烟肼抗体具体优选为抗体2c1和抗体12w2中的一种或两种,更优选为抗体2c1。
63.本发明提供的异烟肼均相酶免疫检测试剂包括独立分装的试剂r2。在本发明中,所述试剂r2包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和葡萄糖-6-磷酸脱氢酶的偶联物。在本发明中,所述异烟肼酶标偶联物的制备方法优选包括以下步骤:将葡萄糖-6-磷酸脱氢酶(g6pdh)的缓冲液、上述技术方案所述的异烟肼半抗原衍生物的有机溶液和有机胺盐类交联剂混合进行复合反应,得到异烟肼酶标偶联物。
64.在本发明中,所述g6pdh的缓冲液优选为g6pdh的pbs溶液;所述葡萄糖-6-磷酸脱氢酶的缓冲液中g6pdh的浓度优选为0.05~2mol/l,更优选为0.1mol/l;所述g6pdh的缓冲液中g6pdh的酶量和缓冲液的体积之比优选为600u:0.5~1.5ml,更优选为600u:1ml;所述pbs
缓冲液的ph值独立地优选为7.2~7.8,更优选为7.4。
65.在本发明中,所述异烟肼半抗原衍生物的有机溶液优选为异烟肼半抗原衍生物的dmso溶液;所述异烟肼半抗原衍生物的有机溶液中,异烟肼半抗原衍生物的质量和有机溶剂的体积之比优选为1mg:100~300μl,更优选为1mg:200μl。在本发明中,所述有机胺盐类交联剂的可选种类优选与前述有机胺盐类交联剂相同,在此不再赘述。在本发明中,所述异烟肼半抗原衍生物和有机胺盐类交联剂的质量比优选为(0.1~1):1,更优选为0.5:1。
66.在本发明中,所述复合反应的温度优选为5~40℃,更优选为20~30℃;所述复合反应的时间优选为1~3h,更优选为2h;所述复合反应优选在搅拌的条件下进行,本发明对所述搅拌的具体实施过程没有特殊要求。
67.完成所述复合反应后,本发明优选还包括将所得复合反应液依次进行透析纯化,得到异烟肼酶标偶联物。在本发明中,所述透析纯化使用的透析优选为pbs缓冲液;所述pbs缓冲液的ph值独立地优选为7.2~7.8,更优选为7.4。在本发明中,所述透析纯化使用的透析膜的截留分子量优选为7000~15000da。在本发明中,所述透析纯化的次数优选为2~6次,更优选为3~4次。
68.在本发明中,所述试剂r2中优选还包括tris缓冲液,所述tris缓冲液的ph值优选为8~8.5,更优选为8.5;本发明对于所述tris缓冲液的用量没有特殊限定,使得异烟肼酶标偶联物在tris缓冲液中的质量百分含量为0.01~0.1%,更优选为0.5%即可。在本发明中,所述试剂r2优选还包括复合缓冲液;所述复合缓冲液优选包括tris缓冲液、nacl和bsa,所述复合缓冲液中tris的浓度优选为25~200mmol/l,更优选为50~100mmol/l,nacl的质量百分数优选为0.5~1.8%,更优选为0.9~1.5%,bsa的浓度优选为1~10mg/ml,更优选为5~6mg/ml;所述复合缓冲液的ph值优选为7~9,更优选为8~8.5。在本发明中,所述试剂r2中异烟肼酶标偶联物的酶量优选为1~10u/ml,更优选为5~8u/ml。
69.在本发明中,所述试剂r2的制备方法优选包括以下步骤:将所述异烟肼酶标偶联物和tris缓冲液混合,得到所述试剂r2。
70.在本发明中,所述试剂r2中,所述异烟肼酶标偶联物的质量百分含量优选为0.01~0.1%,更优选为0.5%。
71.在本发明中,所述异烟肼酶标偶联物和tris缓冲液混合后,得到混合液,本发明优选对所述混合液进行稀释,得到所述试剂r2。在本发明中,所述稀释用稀释剂优选为所述复合缓冲液。
72.本发明采用上述技术方方案所述的异烟肼均相酶免疫检测试剂进行异烟肼检测的方法优选为:将待测样本和试剂r1进行反应,之后加入试剂r2进行继续反应,之后测试od340波长的升高速率。在本发明中,所述待测样本和试剂r1的体积比优选为1:(2~3),更优选为1:2.5。在本发明中,所述反应和继续反应的温度独立地优选为4~40℃,更优选为20~37℃;时间独立地优选为3~7min,更优选为5min。在本发明中,所述待测样本和试剂r2的体积比优选为1:(2~3),更优选为1:2.5。本发明对于所述测试od340波长的升高速率用仪器没有特殊限定,采用本领域技术人员熟知的仪器即可,在本发明的具体实施例中,优选采用日立7170全自动生化分析仪进行测试。
73.本发明提供一种异烟肼磁微粒化学发光检测试剂,包括独立分装的磁微粒工作液和酶标工作液;
所述磁微粒工作液包括磁珠和上述技术方案所述的异烟肼单克隆抗体;所述酶标工作液包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和血清碱性磷酸酶偶联物。
74.在本发明中,所述异烟肼磁微粒化学发光检测试剂,包括独立分装的磁微粒工作液。在本发明中,所述磁微粒工作液包括磁珠和上述技术方案所述的异烟肼单克隆抗体。在本发明的具体实施例中,所述磁珠具体优选为dynal beads m280 tosyl磁珠(ref: 30110d);所述dynal beads m280 tosyl磁珠优选购买于赛默飞生物。在本发明中,所述异烟肼单克隆抗体具体优选为抗体2c1和抗体12w2中的一种或两种,更优选为抗体2c1在本发明中,所述异烟肼单克隆抗体和磁珠的质量比优选为1:0.002~0.025,更优选为1:0.02。
75.在本发明中,所述磁微粒工作液优选还包括硼酸-硼砂(bb)缓冲液。在本发明中,所述bb缓冲液的摩尔的浓度优选为25~100mmol/l,更优选为50~60mmol/l;所述bb缓冲液的ph至优选为7~10,更优选为8~9。在本发明中,所述磁珠的质量和bb缓冲液的体积之比优选为1mg:0.01~0.1ml,更优选为1mg:0.04ml。
76.在本发明中,所述磁微粒工作液的制备方法优选包括以下步骤:将磁珠和硼酸-硼砂缓冲液混合后加入所述异烟肼单克隆抗体进行反应,得到磁珠-抗体混合溶液;除去所述磁珠-抗体的上清液,加入tbst缓冲液混合反应,得到包被有抗体的磁珠溶液;除去所述包被有抗体的磁珠溶液的上清液,加入tbst缓冲液进行稀释,得到所述磁微粒工作液。
77.本发明将磁珠和硼酸-硼砂缓冲液混合后加入所述异烟肼单克隆抗体进行反应,得到磁珠-抗体混合溶液。在本发明中,所述反应的温度优选为25~42℃,更优选为30~37℃;所述反应的时间优选为5~10h,更优选为8h;所述反应优选在震荡条件下进行。
78.得到磁珠-抗体混合溶液后,本发明除去所述磁珠-抗体的上清液,加入tbst缓冲液混合反应,得到包被有抗体的磁珠溶液。在本发明中,所述除去所述磁珠-抗体的上清液优选为磁分离。在本发明中,所述tbst缓冲液优选包括tris缓冲液、nacl和tw20(吐温20),所述tbst缓冲液中tris的浓度优选为20~200mmol/l,更优选为50~100mmol/l,nacl的质量百分数优选为0.5~1.8%,更优选为0.9~1.5%,tw20的质量百分数优选为0.05~0.5%,更优选为0.1~0.3%;所述tbst缓冲液的ph值优选为7.2~7.8,更优选为7.4。在本发明中,所述反应的温度优选为25~42℃,更优选为30~37℃;所述反应的时间优选为10~15h,更优选为12h。
79.得到包被有抗体的磁珠溶液后,本发明除去所述包被有抗体的磁珠溶液的上清液,加入tbst缓冲液进行稀释,得到所述磁微粒工作液。在本发明中,所述除去所述包被有抗体的磁珠溶液的上清液优选为磁分离。在本发明中,所述tbst缓冲液优选与前述tbst缓冲液相同,在此不再赘述。在本发明中,所述磁微粒工作液中包被有抗体的磁珠的浓度优选为0.3~0.5mg/ml,更优选为0.4mg/ml。
80.在本发明中,所述异烟肼磁微粒化学发光检测试剂,包括独立分装的酶标工作液;所述酶标工作液包括异烟肼酶标偶联物,所述异烟肼酶标偶联物为上述技术方案所述的异烟肼半抗原衍生物和血清碱性磷酸酶的偶联物。
81.在本发明中,所述异烟肼半抗原衍生物和血清碱性磷酸酶的偶联物的制备方法优
选与所述异烟肼半抗原衍生物和葡萄糖-6-磷酸脱氢酶的偶联物的制备方法相同,不同之处在,将g6pdh替换为血清碱性磷酸酶(alp),所述alp与异烟肼半抗原衍生物的质量比优选为1:(0.4~0.6),更优选为1:0.5。
82.在本发明中,所述酶标工作液优选还包括混合稀释液,所述混合稀释液优选包括mes、nacl、bsa、mgcl和水,所述混合稀释液中mes的浓度优选为25~200mmol/l,更优选为50~100mmol/l,nacl的质量百分数优选为0.5~1.8%,更优选为0.9~1.5%,bsa的浓度优选为1~10mg/ml,更优选为5~6mg/ml,mgcl的浓度优选为0.5~2mmol/l,更优选为1~1.5mmol/l;所述混合稀释液的ph值优选为7~9,更优选为7.6。在本发明中,所述酶标工作液中异烟肼酶标偶联物的浓度优选为0.1~4μg/ml,更优选为1~2μg/ml。
83.在本发明中,所述酶标工作液的制备方法优选包括以下步骤:将异烟肼酶标偶联物和混合稀释液混合,得到酶标工作液。本发明对于所述混合没有特殊限定,能够将原料混合均匀即可。
84.本发明采用上述技术方案所述的异烟肼磁微粒化学发光检测试剂对异烟肼样本进行测试的方法优选包括以下步骤:将待测异烟肼样本、磁微粒液工作液和酶标工作液混合,进行孵育反应,加入发光剂显色。
85.在本发明中,所述待测异烟肼样本优选包括异烟肼的校准品、异烟肼质控品和异烟肼临床样本中的一种或几种;所述待测异烟肼样本在使用前优选先进行进行稀释,得到待测异烟肼样本液;所述稀释剂优选为pbs缓冲液,所述pbs缓冲液的ph值独立地优选为7.2~7.8,更优选为7.4;所述稀释的倍数优选为10~20倍。在本发明中,所述待测异烟肼样本液、磁微粒液工作液和酶标工作液的体积比优选为1:(3~5):(4~6),更优选为1:4:5;在本发明中,所述孵育的温度优选为25~42℃,更优选为30~37℃;所述孵育反应的时间优选为4~6min,更优选为5min。完成所述孵育后,本发明优选还包括清洗,然后再加入发光液进行显色;所述清洗用溶剂优选为化学发光仪配套的清洗液。在本发明中,所述发光剂优选包括3-(2'-螺旋金刚烷)-4-甲氧基-4-(3"-磷酰氧基)苯-1,2-二氧杂环丁烷(amppd)。
86.为了进一步说明本发明,下面结合实施例对本发明提供的技术方案进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
87.实施例1具有式i所示结构的异烟肼半抗原衍生物的制备生物的制备
将13.7g异烟肼和40ml丙酮在搅拌条件下加入到naoh水溶液(naoh质量为5g,1mol/l),在50℃条件下搅拌反应2h。反应结束减压蒸出过量的丙酮,加水20ml,在12℃条件下保温结晶2h,过滤,将所得固体粉末在45℃条件下真空烘干,得到中间体1。
88.在10.0g中间体1中加入300ml水、64.0g过硫酸铵、6.5gtfa和20gagno3,在室温(25℃)条件下反应2h,加入乙酸乙酯30ml静置分层,取有机层减压浓缩蒸出乙酸乙酯,得到中间体2。
89.在中间体2中加水50ml,然后滴加naoh(1mol/l)调ph值至12,水解2h,用盐酸(1mol/l)调ph值至4.5,在10℃条件下保温结晶2h,过滤,将所得固体粉末在45℃条件下真空烘干,得到2-丙酸异烟肼(具有式i所示结构的异烟肼半抗原衍生物)。
90.图1为2-丙酸异烟肼的氢谱图。由图1可知,本发明成功制备得到具有式i所示结构的异烟肼半抗原衍生物。
91.实施例2异烟肼人工抗原制备取10mg实施例1制备的异烟肼半抗原衍生物,加入1ml的dmso溶解完全,得到异烟肼半抗原衍生物溶液;称取10mg1-(3-二甲基氨基丙基)-3-乙基碳化二亚胺盐酸盐,溶解在100μl水中,然后加入到异烟肼半抗原衍生物溶液中,室温反应1h,得到交联异烟肼半抗原衍生物溶液;称取牛甲状腺球蛋白20mg溶解在5ml的pbs中,得到牛甲状腺球蛋白溶液;将交联异烟肼半抗原衍生物溶液和牛甲状腺球蛋白溶液混合,室温搅拌2h,得到复合反应液,将复合反应液用pbs缓冲液(ph=7.4)透析(透析袋7000da)4次,得到具有式ii所示结构的异烟肼人工抗原,异烟肼人工抗原置于-20℃冷冻保存。
92.实施例3异烟肼鼠单克隆抗体的制备将实施例2制备的异烟肼人工抗原用pbs缓冲液稀释至1mg/ml,加入等体积的sigma弗氏完全佐剂,乳化完全,小鼠按照0.1mg/只的剂量机型首次注射免疫,间隔4周后再次增强免疫,采用1mg实施2制备的异烟肼人工抗原同sigma弗式不完全佐剂等体积混合乳化后进行增强免疫,免疫剂量为0.1mg/只,免疫4次后,取小鼠脾细胞和sp2/0融合,采用异烟肼-牛甲状腺球蛋白1μg/ml包被elisa96孔板,对融合细胞进行效价及竞争测定,筛选得到2株细胞(2c1,12w2),细胞上清的结果如表1所示:表1细胞上清的间接竞争elisa结果
由表1可知,2c1表现出对异烟肼最高的灵敏度及最好的特异性,ic
50
为5ng/ml,并且对异烟肼代谢物和类似物无交叉反应。适合于异烟肼药物浓度监测方法的建立。因此对2c1小鼠腹水制备,并proteina/g纯化,得到抗体2c1,用于后续异烟肼方法的建立。
93.2c1杂交瘤细胞株保藏编号为cgmccno.:45165。
94.实施例4磁微粒化学发光法异烟肼血药浓度检测方法的建立:1)将50mgdynalbeadsm280tosyl磁珠稀释于2mlbb缓冲液(50mm,ph=8.0)中,加入1mg异烟肼抗体2c1,混匀后,37℃震荡反应8h;2)磁吸去除上清,加入tbst缓冲液(50mmtris缓冲液+0.9wt%nacl+0.1wt%tw20和水,ph=7.4)于37℃条件下反应12h;3)磁吸去除上清,加入步骤2)中的tbst缓冲液稀释到0.4mg/ml,得到磁微粒工作液,2~8℃保存待用;4)将1mgalp溶解在1mlpbs中,加入0.5mg异烟肼半抗原衍生物溶液(溶解于100μldmso中),混合均匀,加入1mgedc固体,在室温条件下混匀2h,透析(7000da)到pbs缓冲液(ph=7.4)中,用混合稀释液(50mmmes+0.9wt%nacl+5mg/mlbsa+1mmmgcl2,ph=6.7)稀释到1μg/ml,得到酶标工作液。
95.5)反应程序:取10μl待测异烟肼样本(用pbs预稀释10倍),加入40μl磁微粒液工作液和50μl酶标工作液,于37℃条件下孵育反应5min,化学发光仪配套的清洗液进行清洗,加入amppd显色。
96.采用小牛血清基质(购买于康源生物)配置不同浓度的异烟肼的校准品,浓度分别为:0mg/ml、10mg/ml、50mg/ml、250mg/ml、1250mg/ml和6250mg/ml;制定标准曲线如表2和图2所示;并测定精密度和最低检出限以及对异烟肼代谢物和类似物的交叉反应,结果如表3和表4所示,其中,精密度是测得高低两个水平的质控(qc1低值质控和qc2高值质控)品各10次,计算得到。最低检出限是检测一个零值样本20次,检出限为平均值+2sd。
97.表2磁微粒发光法异烟肼定标曲线数据
由表2的数据绘制图2所示曲线,曲线的四参数方程式:y=(a-d)/[1+(x/c)b]+d;参数:a=39311477.419727,b=1.25042336927708,c=9.71549044683522,d=23166.6823551865,相关系数r2:0.9996。
[0098]
表3精密度和灵敏度在浓度为462ng/ml的异烟肼样本中加入不同浓度的交叉测试物,计算交叉反应率,结果如表4所示。
[0099]
表4交叉反应性表4结果表明,磁微粒发光法的异烟肼试剂对异烟肼对主要代谢物无明显的交叉反应,特异性好。
[0100]
由表2~4和图2表明采用2c1抗体制备的磁微粒发光法异烟肼测定试剂灵敏度高,特异性好。
[0101]
实施例5异烟肼均相酶免疫检测试剂的制备异烟肼均相酶免疫检测试剂包括两种独立封装的试剂,具体如下:试剂r1的制备:20 mm nad、30 mm葡萄糖-6-磷酸g6p、55 mm ph=8.0 的tris缓冲液溶解制成均相酶底物,加入0.05wt%的抗异烟肼特异性抗体2c1混合均匀,得到试剂r1。
[0102]
试剂r2的制备:0.1m ph=8.5的tris缓冲液中加入0.0wt5%实施例1制备的异烟肼半抗原衍生物-g6pdh酶标偶联物。
[0103]
其中异烟肼半抗原衍生物-g6pdh酶标偶联物是采用600u g6pdh溶解在1ml pbs中,加入0.5mg异烟肼半抗原衍生物(溶解在100μl dmso中),混合均匀,加入1mg edc固体,室温反应2h,透析(使用7000da透析袋)到pbs中,用复合缓冲液(100mm tris,0.9wt%nacl,5mg/ml bsa,ph=8.5)稀释到5u/ml,得到试剂r2。
[0104]
测试程序为:在20μl待测样本中加入50μl试剂r1,在37℃条件下反应5min,然后加入50μl试剂r2继续反应5min,采用日立7170全自动生化分析仪测定od340波长的升高速率。
[0105]
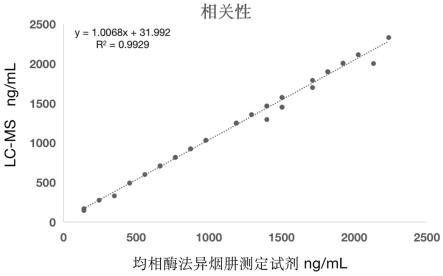
选取临床40例异烟肼尿液浓度样本,对比本发明构建的均相酶法同lc-ms法(参考文献:le thi luyen, ta manh hung, et al. "simultaneous determination of pyrazinamide, rifampicin, ethambutol, isoniazid and acetyl isoniazid in human plasma by lc-ms/ms method." journal of applied pharmaceutical science 8.09 (2018): 061-073.)的测定异烟肼结果进行比对,结果如图3所示,图3的结果表明,基于本发明制备的抗体建立的均相酶法测定异烟肼含量同lc-ms法相关性良好,符合临床需求。
[0106]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1