一种从酒茱萸中提取具有治疗关节炎作用的化合物的制备方法及其应用
1.本发明涉及医药领域,特别是一种从酒茱萸中提取具有治疗关节炎作用的化合物的制备方法及其应用。
背景技术:
2.山茱萸(cornus officinalis)为山茱萸科(cornaceae)山茱萸属(cornus)植物山茱萸 (cornus officinalis sieb.et zucc.)的干燥成熟的果肉,始载于《神农本草经》,主要分布于河南、陕西、浙江等省,是“滋补肝肾、涩精固脱”的名贵中药材。膝骨关节炎的重要病机在于肾虚血瘀,临床多采用补肾活血中药治疗,可取得较好疗效。酒茱萸作为山茱萸的炮制品,采用酒炖或酒蒸的方法生产(总则0213),是主要临床用药形式。现代研究表明,山茱萸炮制后可借酒温通,助力药势,降低其酸度,增强补益的功效,同时,炮制后可使有效成分更易煎出,进一步增强温补肝肾的功效,且酒萸肉煮水喝可有效缓解风湿性/类风湿性关节炎、关节疼痛等。本研究结合我国传统的入药习惯,对酒茱萸水提物进行了系统的化学成分研究。在薄层色谱法和高效液相色谱法的指导下,采用各种柱色谱分离技术,定向的富集、分离单体成分,运用各种波谱学方法,进行化合物的结构鉴定。获得具有显著治疗关节炎的结构新颖的化合物,为治疗关节炎提供疗效显著潜在药物,至今未见有公开报导。
技术实现要素:
3.针对上述情况,本发明的目的是提供一种从酒茱萸中提取具有治疗关节炎作用的化合物的制备方法及其应用,有效解决从酒茱萸中发现结构新颖的化合物,并实现新化合物在开发抗关节炎药物中的应用问题。
4.本发明解决的技术方案是,一种从酒茱萸中提取具有治疗关节炎作用的化合物,该化合物为compound 1:(r)-1
′‑
((5-formylfuran-2-yl)methyl)-4
′‑
methyl-3
′‑
hydroxysuccinate,分子式为 c
11h12
o7,不饱和度为6;分子结构式为:
[0005][0006]
其制备方法是,包括以下步骤:
[0007]
(1)取干燥的酒萸肉30kg,每次加入6~10倍重量体积、体积浓度30%~50%乙醇,重量体积是指固定体kg计,液体以l计,100℃加热回流提取2~5次,每次提取1~2h,合并提取液,减压回收至无醇味,加水分散成浓度相当于含生药量0.5g/ml~3g/ml的样品溶液;
[0008]
(2)将样品溶液上样于直径为20cm,径高比1:4~1:12的d101大孔吸附树脂柱,上样流速为0.3bv/h(bv指柱体积,1个柱体积为16~40l),用水洗脱2~4bv,弃去水洗液,用体积浓度30%乙醇洗脱2~8bv,流速为1~4bv/h,收集30%乙醇部位洗脱液,减压浓缩,得到
50℃相对密度1.1g/ml的浸膏(2.5~3.6kg);
[0009]
(3)将浸膏加水2.0~3.0l分散成悬浮液,每次用3.0~4.0l乙酸乙酯萃取3~6次,待静置分层完全,进行下一次萃取,合并萃取液,减压浓缩得到50℃相对密度为1.3g/ml的乙酸乙酯浸膏(300~450g);
[0010]
(4)乙酸乙酯浸膏经200~300目硅胶柱色谱,直径d=8~10cm,柱高h=18~25cm,用体积比100:0、100:5二氯甲烷-甲醇进行梯度洗脱,每个比例洗脱3~8个柱体积(1个柱体积为1000~2000ml),收集100:5洗脱液,减压浓缩回收溶剂,采用薄层色谱法检识,得到馏分fr.c(40~50g);
[0011]
(5)馏分fr.c经ods柱层析,直径d=4~6cm,柱高h=14~18cm,用体积比为10:90 甲醇-水洗脱4~8个柱体积(1个柱体积为175~500ml),收集洗脱液,减压浓缩回收溶剂,得馏分fr.c1(2.3~3.2g);
[0012]
(6)馏分fr.c1经sephadex lh-20柱层析,直径r=2~3cm,柱高h=100~150cm,用甲醇进行洗脱,流速1~2ml/min,薄层色谱法检识,合并相同馏分,得到馏分fr.c1-3(60~ 82mg);
[0013]
(7)采用半制备hplc,使用纳谱分析半制备柱(10mm
×
250mm,5μm,苏州纳谱分析技术有限公司),色谱条件16%~18%ch3cn/h2o,流速2.5~3.5ml/min,收集保留时间 tr=12~33min的馏分,对馏分进行制备纯化,得compound1(20~36mg)。
[0014]
本发明经鉴定,是一类从酒茱萸中提取的具有抗炎活性的新化合物,其制备方法易操作,导向性强,产品纯度99%以上,该化合物可有效用于制备抗炎的药物,开拓了酒茱萸的新用途和药用价值,经济和社会效益巨大。
附图说明
[0015]
图1为本发明化合物1分子结构式图。
[0016]
图2为本发明化合物1关键的hmbc及1h-1
h cosy相关图。
[0017]
图3为本发明化合物1的ecd相关图。
[0018]
图4为本发明的工艺流程图。
具体实施方式
[0019]
以下结合具体情况对本发明的具体实施方式作详细说明。
[0020]
实施例1
[0021]
本发明一种从酒茱萸中提取具有治疗关节炎作用的化合物的制备方法,包括以下步骤:
[0022]
(1)取干燥的酒萸肉30kg,每次加入8倍重量体积、体积浓度30%乙醇,100℃加热回流提取3次,每次提取2h,合并提取液,减压回收至无醇味,加水分散成浓度相当于含生药量2g/ml的样品溶液;
[0023]
(2)将样品溶液上样于直径为20cm,径高比1:10的d101大孔吸附树脂柱,上样流速为0.3bv/h(1个柱体积为34l),用水洗脱2bv,弃去水洗液,用体积浓度30%乙醇洗脱4bv,流速为2bv/h,收集30%乙醇部位洗脱液,减压浓缩,得到50℃相对密度1.1g/ml的浸膏 (3.2kg);
[0024]
(3)将浸膏加水3.0l分散成悬浮液,每次用3.5l乙酸乙酯萃取4次,待静置分层完全,进行下一次萃取,合并萃取液,减压浓缩得到50℃相对密度为1.3g/ml的乙酸乙酯浸膏 (409g);
[0025]
(4)乙酸乙酯浸膏经250目硅胶柱色谱,直径d=10cm,柱高h=18cm,用二氯甲烷洗脱4个柱体积,用体积比100:5二氯甲烷-甲醇洗脱6个柱体积(1个柱体积为1400ml),收集100:5洗脱液,减压浓缩回收溶剂,采用薄层色谱法检识,得到馏分fr.c(47.2g);
[0026]
(5)馏分fr.c经ods柱层析,直径d=5cm,柱高h=15cm,用体积比为10:90甲醇-水洗脱6个柱体积(1个柱体积为300ml),收集洗脱液,减压浓缩回收溶剂,得馏分fr.c1(3.0g);
[0027]
(6)馏分fr.c1经sephadex lh-20柱层析,直径r=2.6cm,柱高h=130cm,用甲醇进行洗脱,流速1ml/min,薄层色谱法检识,合并相同馏分,得到馏分fr.c1-3(80mg);
[0028]
(7)采用半制备hplc,使用纳谱分析半制备柱(10mm
×
250mm,5μm,苏州纳谱分析技术有限公司),色谱条件18%ch3cn/h2o,流速3ml/min,收集保留时间tr=12min的馏分,对馏分进行制备纯化,得compound1(32mg)。
[0029]
实施例2
[0030]
本发明一种从酒茱萸中提取具有治疗关节炎作用的化合物的制备方法,包括以下步骤:
[0031]
(1)取干燥的酒萸肉30kg,每次加入6倍重量体积、体积浓度50%乙醇,100℃加热回流提取2次,每次提取1h,合并提取液,减压回收至无醇味,加水分散成浓度相当于含生药量0.5g/ml的样品溶液;
[0032]
(2)将样品溶液上样于直径为20cm,径高比1:6的d101大孔吸附树脂柱,上样流速为 0.3bv/h(1个柱体积为24l),用水洗脱3bv,弃去水洗液,用体积浓度30%乙醇洗脱2bv,流速为3bv/h,收集30%乙醇部位洗脱液,减压浓缩,得到50℃相对密度1.1g/ml的浸膏(2.5kg);
[0033]
(3)将浸膏加水2l分散成悬浮液,每次用3l乙酸乙酯萃取3次,待静置分层完全,进行下一次萃取,合并萃取液,减压浓缩得到50℃相对密度为1.3g/ml的乙酸乙酯浸膏 (308g);
[0034]
(4)乙酸乙酯浸膏经200目硅胶柱色谱,直径d=8cm,柱高h=20cm,用二氯甲烷洗脱 4个柱体积,用体积比100:5二氯甲烷-甲醇洗脱6个柱体积(1个柱体积为1000ml),收集 100:5洗脱液,减压浓缩回收溶剂,采用薄层色谱法检识,得到馏分fr.c(42g);
[0035]
(5)馏分fr.c经ods柱层析,直径d=4cm,柱高h=14cm,用体积比为10:90甲醇-水洗脱8个柱体积(1个柱体积为175ml),收集洗脱液,减压浓缩回收溶剂,得馏分fr.c1(2.5g);
[0036]
(6)馏分fr.c1经sephadex lh-20柱层析,直径r=2.2cm,柱高h=120cm,用甲醇进行洗脱,流速2ml/min,薄层色谱法检识,合并相同馏分,得到馏分fr.c1-3(62mg);
[0037]
(7)采用半制备hplc,使用纳谱分析半制备柱(10mm
×
250mm,5μm,苏州纳谱分析技术有限公司),色谱条件16%ch3cn/h2o,流速3.5ml/min,收集保留时间tr=25min的馏分,对馏分进行制备纯化,得compound1(20mg)。
[0038]
实施例3
1300ml),收集100:5洗脱液,减压浓缩回收溶剂,采用薄层色谱法检识,得到馏分fr.c(45.6g);
[0053]
(5)馏分fr.c经ods柱层析,直径d=4.8cm,柱高h=14cm,用体积比为10:90甲醇
‑ꢀ
水洗脱4个柱体积(1个柱体积为250ml),收集洗脱液,减压浓缩回收溶剂,得馏分 fr.c1(2.8g);
[0054]
(6)馏分fr.c1经sephadex lh-20柱层析,直径r=2.6cm,柱高h=120cm,用甲醇进行洗脱,流速1ml/min,薄层色谱法检识,合并相同馏分,得到馏分fr.c1-3(79mg);
[0055]
(7)采用半制备hplc,使用纳谱分析半制备柱(10mm
×
250mm,5μm,苏州纳谱分析技术有限公司),色谱条件18%ch3cn/h2o,流速2.5ml/min,收集保留时间tr=20min的馏分,对馏分进行制备纯化,得compound1(27mg)。
[0056]
要指出的是,上述实施例仅是用于说明本发明的具体实施方式,以对该从酒茱萸中提取具有抗炎活性的化合物及其提取方法进行的详细描述,是说明性的,而不是用于限定本发明的保护范围,凡是在不脱离本发明总体构思下的变化和修改,均应属本发明的保护范围之内。
[0057]
本发明原料丰富,制备方法易操作,所制备的化合物为从酒茱萸中提取具有抗炎活性的 5-羟甲基糠醛衍生新化合物,开拓了酒茱萸的新用途,所得产品可有效用于制备抗炎药物,实现5-羟甲基糠醛衍生化合物在制备抗炎药物中的应用,并经实验取得了非常好的有益技术效果,有关实验资料如下:
[0058]
一、仪器和材料
[0059]
thermo evo 220spectrometer紫外光谱仪(thermo,waltham,ma,美国);
[0060]
bruker avⅲ500-nmr核磁共振仪(bruker,billerica,德国);
[0061]
thermo uplc-oribtrap-exploris120高分辨质谱仪(thermo,waltham,ma,美国);
[0062]
安东帕mcp 5100旋光仪(anton paar,graz,austria);
[0063]
清博华lc 52型半制备高效液相色谱仪(qbh,中国);
[0064]
hplc-5c18c制备柱(10
×
250mm,5um;suzhou,co.,ltd.,中国);
[0065]
cosmosil chiral 5c柱(10id
×
250mm,nacalai tesque,inc.,日本);
[0066]
柱层析硅胶(100-200目,200-300目,青岛海洋化工有限公司);d101型大孔树脂(上海摩速科学器材有限公司);葡聚糖凝胶sephadex lh-20(瑞典pharmacia公司);ods-c18 (日本ymc公司);
[0067]
所用试剂均为分析纯或色谱纯;
[0068]
氘代试剂:meod(cambridge isotope laboratories,usa);
[0069]
raw264.7细胞株来源于中国科学院(上海)细胞库;
[0070]
lps从美国sigma aldrich购买;
[0071]
dmem培养液和胎牛血清和胎牛血清(fbs)购自美国gibco公司;
[0072]
3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(mtt)和二甲基亚砜(dmso)购于美国 sigma-aldrich公司;
[0073]
二氧化碳培养箱(美国赛默飞公司,型号3111);
[0074]
酶标仪(美国赛默飞公司,型号multiskan fc);
[0075]
台式高速冷冻离心机(索福st-21,美国产);
[0076]
adventurer
tm
电子天平(奥豪斯国际贸易上海有限公司);
[0077]
洁净工作台,北京昌平长城空气净化设备工程公司;
[0078]
96孔板购于美国corning公司。
[0079]
二、结构鉴定
[0080]
化合物1(compound 1):黄色油状,纯度99.2%,易溶于甲醇等有机溶剂,遇香草醛
‑ꢀ
浓硫酸加热不显色。
[0081]
经ecd相关测试(见图3)和色谱鉴定,hresims准分子离子峰[m+na]
+
m/z 279.0597 (c
11h12
o7na计算值为279.0481),确定分子式为c
11h12
o7,不饱和度为6,旋光度[α]2
d5-2(c= 0.05,甲醇),uv光谱中在248nm处有最大吸收,红外光谱显示,结构存在1个羟基基团(3317 cm-1
),一个羰基(1656cm-1
),一个醛基(1656cm-1
)。1h-nmr谱和
13
c-nmr谱数据显示化合物存在一个亚甲基[δ
h 2.86(1h,dd,j=16.0,4.8hz,h-2'a),2.78(1h,dd,j=16.0,7.2hz, h-2'b,δ
c 39.9(c-2')];一个连氧亚甲基[δ
h 5.20(2h,s,h-7),δ
c 59.1(c-7)];一个连氧次甲基[δ
h 4.53(1h,dd,j=7.2,4.9hz,h-3’);δ
c 68.5(c-3’)],一个甲氧基[δ
h 3.72(3h,s,h-5’);δ
c 52.7 (c-5’)];两个烯烃质子信号[δ
h 7.38(1h,d,j=3.5hz,h-3),6.72(1h,d,j=3.5hz,h-4);δ
c 123.8(c-3),113.7(c-4)];一个醛基[δ
h 9.58(1h,s,h-6);δ
c 179.6(c-6)];两个sp2杂化的连氧季碳δ
c 154.4(c-2),157.2(c-5);两个酯羰基碳信号[δ
c 173.6(c-1'),175.9(c-4')]。详细信息见表1。根据其质谱和核磁数据,推断该化合物为5-羟甲基糠醛酯化衍生物。这一推断由1h-1
h-cosy谱和hmbc谱数据证实,1h-1
h-cosy谱显示h-2'与h-3'相关,h-3与h-4相关;hmbc谱显示h-3与c-2、c-4、c-5、c-6相关。结合其他1h-1
h-cosy谱和hmbc谱相关(见图2),最终确定化合物1的分子结构式如图1所示:
[0082][0083]
上述所得化合物经测定,鉴定为从酒茱萸中提取的一个5-羟甲基糠醛衍生化合物,即化合物1(compound 1)。
[0084]
化合物1的绝对构型是由实测ecd谱和计算ecd谱确定的。ecd光谱在191nm处表现出正的cotton效应,242nm处表现出负cotton效应。计算曲线与实验曲线吻合良好,但有轻微的峰移(见图3),表明化合物1的绝对构型为3'r。
[0085]
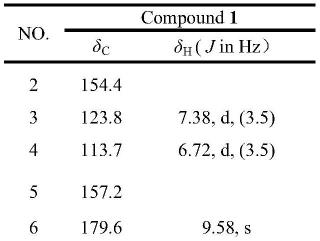
表1.化合物1的1h-and 13
c-nmr数据(500and 125mhzδin ppm,meod)
[0086]
[0087][0088]
三、活性试验
[0089]
1、体外抗炎实验
[0090]
采用griess法测定脂多糖(lps)诱导的raw264.7细胞产生no水平,评价化合物1 的抗炎活性。与模型组相比,化合物1能显著降低no的释放量(p《0.01),不呈浓度依赖性,表明其具有抗炎活性。
[0091]
化合物1的抗炎实验方法:将raw264.7细胞培养于dmem完全培养基(含10%新生牛血清)中,置37℃、5%co2培养箱内培养。选择对数生长期细胞用于实验。
[0092]
取对数生长期的raw264.7细胞,用完全培养基配成1
×
105个/ml的细胞悬浮液,接种于96孔板中,每孔加入100μl的细胞悬液,置37℃、5%co2培养箱内培养。24h后,弃去孔内上清液,分别加入100μl浓度为100、50、25、12.5、6.25、0mm,化合物1的完全培养基;即给药组和空白组,每组设置3个复孔,置37℃,含5%co2培养箱内培养。24小时后,每孔加入cck-8 10μl,用酶标仪在490nm处测定各孔od值。并计算细胞存活率,细胞存活率=(a测/a空)
×
100%。公式中:a测为药物组od值-空白组od值:a空为对照组od 值-空白组od值。每组重复3次独立实验。化合物1在浓度6.25-100μm时与空白组比较对 raw264.7细胞均无细胞毒活性,细胞活力均在100%以上。因此,选择25,50,100μm作为后续试验的浓度梯度。
[0093]
将处于对数生长期的细胞接种于24孔板(2
×
105个细胞/孔),37℃、5%co2环境的培养箱中培养12h后加入不同质量浓度的待测样品(最终质量浓度分别为25、50μm),温孵培养1h后加人1μg/ml lps。同时设空白对照组(培养基)、模型(lps+培养基)组、阳性药组(地塞米松+培养基)和药物作用组。继续温孵培养24h。每组重复3次独立实验。将上清液(100ml)与等体积格氏试剂混合,用酶联免疫检检测仪测定混合物在560nm处的od 值,计算no抑制率,结果见表2。
[0094]
表2化合物1对lps诱导的raw264.7细胞no水平影响(n=3)
[0095][0096][0097]
由表2可知,模型组no的释放量显著高于空白对照组(p《0.01),表明造模成功。与模型组相比,各浓度处理均能显著降低no的释放量(p《0.01),且呈浓度依赖性。由表2 可以看出,化合物1能够较好地抑制炎症因子no的生成。
[0098]
2、体内试验
[0099]
试验方法:48只sd大鼠,雄性,体质量(160
±
20)g,动物由济南朋悦实验动物繁育有限公司提供,实验动物许可证号:syxk(鲁)20210012。适应性喂养1周,随机分为6组,每组8只。除空白组其余大鼠均通过踝关节腔注射尿酸钠建立急性痛风性关节炎(aga)模型,具体为:大鼠用体积分数10%水合氯醛麻醉后,在右后踝关节处注射50μl尿酸钠混悬液 (20g
·
l-1
),正常组大鼠在相同部位注射50μl生理盐水,若大鼠受试关节在1h内肿胀度≥0.3ml即认为造模成功。造模后1h开始给药。给药组分别皮下注射高、低剂量(50mg/kg、 25mg/kg)制备的药物,阳性药组(白芍总苷胶囊)。对照组与模型组灌服等量生理盐水,连续给药3d。分别于造模后1h、6h、12h、24h、48h、72h观察大鼠步态变,采用爪肿测量仪测量各组大鼠右后踝关节标记以下的容积,作为肿胀度。
[0100]
制备的抗炎药物高、低剂量组均有显著的抗炎作用。空白组大鼠在整个实验过程中左后足趾各关节无红肿。模型组大鼠在造模1h后出现左后关节皮肤充血肿胀,模型大鼠的步态均不正常,步态评分均为所有时间点最高值。与模型组比较,给药组大鼠步态评分显著降低,差异具有统计学意义(p<0.05),踝关节肿胀减轻,pwt值提高,造模给药72h后,与空白组(0.03
±
0.01)相比,模型组大鼠足趾肿胀度0.30
±
0.02),化合物1高、低剂量组大鼠足趾肿胀度分别为0.13
±
0.09和0.23
±
0.06。从大鼠足趾肿胀度可以看出,制备的抗关节炎药物在50mg/kg和25mg/kg剂量下均可以显著抑制尿酸钠所致的大鼠急性关节炎症,具有很好的抗炎活性。并经临床对15例关节炎患者进行试用,结果证明,除1人无明显效果外,其余均为不同程度的治疗效果,抗炎有效率高达93%以上。
[0101]
综上所述,本发明原料丰富,制备方法易操作,所得产品质量好,纯度高达99.2%,试验表明,化合物1作为抗炎先导化合物,有效用于制备抗关节炎的药物中的应用,开拓了酒茱萸的药用价值和商业价值,具有巨大的开发应用前景,经济和社会效益巨大。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1