流式样本制备仪的制作方法
1.本发明涉及流式细胞仪的前置细胞样本制备领域,是一种对流式细胞术的改进。
背景技术:
2.流式细胞仪是一种被广泛应用于医疗和科研领域的检测设备,其用于检测细胞样品中被“标记”的关键细胞。近年来,流式细胞仪在中国各大医疗机构迅速普及,在血液检测、疾病诊断等领域发挥着重要作用。与此同时,流式细胞仪也逐渐走进中国各大高校和科研院所,已成为生命科学和医学研究的不可或缺的实验设备。
3.在使用“流式细胞仪”对细胞样品进行检测之前,必须对细胞进行标记,即“细胞样品制备”。在传统的实验室操作中,该操作通常由人工进行,程序十分繁琐,主要步骤如下。
4.实验人员首先需要人工将细胞样本制备成细胞悬液,例如将生物组织切碎,制备成细胞悬液,该过程极其繁琐耗时。
5.随后,根据不同的实验需求和细胞种类,实验人员需要向细胞悬液中加入裂解液、固定液等试剂,然后将载有细胞悬液的离心管放到混匀装置中进行混匀,该过程同样十分繁琐耗时。
6.接下来为“样本制备”的关键环节。实验人员需要往细胞悬液中加入“标记物”,随后放入混匀装置进行“孵化”,使得“标记物”与细胞充分结合。
7.接下来则为“样本制备”最繁琐的步骤,为了去除上述步骤中残留在细胞悬液中的标记物、裂解液、固定液等残留物质,获得纯净的、完成“标记”细胞,实验人员需要对细胞进行“洗涤”。传统人工“细胞洗涤”的步骤通常为:首先往细胞悬液中加入缓冲液;随后使用离心机使得纯净的细胞聚集到离心管底部,残留的液体悬浮在细胞上方;接下来人工使用移液枪将残留的液体吸走,留下纯净的细胞;由于上述步骤无法彻底“洗涤”干净细胞,聚集在底部的细胞必然夹杂着残留物,实验人员还需要加入缓冲液,即“重悬”细胞,再次重复上述步骤,直到细胞被“洗涤”干净。
8.上述人工“洗涤”操作存在巨大问题。首先,人工在使用“移液枪”将残留的液体吸走过程中,必然会带走一部分“纯净的细胞”,造成大量的细胞损失,这在原代细胞等众多涉及珍惜样本的流式实验中是不可接受的;同时,在使用离心机时,细胞受到巨大的“离心力”并被挤压在离心管壁上,这也会对细胞活性造成影响,导致细胞损失。第三,离心机体积过于庞大,无法集成进流式样本制备的自动化设备。因此,急需一种新的细胞“洗涤”技术来代替离心机。
9.如上所述,流式样本制备流程步骤多、时间长,极其耗费科研人员和医生的时间,阻碍科研的发展和医疗的诊断效率。另一方面,人工操作步骤繁琐,很容易出错,再加上不同实验人员的操作习惯不一样,很容易导致结果的不一致,无法得出可重复的、正确的实验数据,甚至导致疾病误诊。因此,急需一种自动化的仪器设备,来取代人工操作。
10.此外,传统人工操作中,细胞样品和各种有毒试剂很容易与人体接触,导致生物风险。
11.近年来,也有不少尝试,试图用自动化的方法来取代上述人工操作。例如美国贝克曼库尔特公司推出的prepplus 2设备。这一设备确实解决了一部分自动化操作,例如自动加液、自动混匀等,但并没有实现最繁琐的“细胞洗涤”的自动化,仍然需要人工大范围的介入。同时这一设备主要面向医疗场景,其“加液”和“混匀”环节采用闭环式自动化设计,不允许人工介入,并不能满足广大科研场景个性化、自动化的需求。
技术实现要素:
12.本发明提供了一种新的全自动细胞样本制备装置,用于流式细胞仪的前置样本处理本发明能够自动将裂解液、固定液等试剂加入细胞悬液,自动将抗体等标记物加入细胞悬液,自动完成细胞的混匀孵化操作,自动将细胞悬液与标记物进行混匀,自动对细胞样本进行洗涤,自动通过温控装置将各种试剂保持在规定的温度。
13.为了实现上述流式样本制备的自动化流程,本发明公开了一种流式样本制备装置,主要包括全自动加液组件、摇匀式细胞孵化组件、试剂贮存组件和细胞洗涤组件。
14.进一步的,所述全自动加液组件由三轴龙门导轨、自动注射枪头组成。所述全自动加液组件能够在整个装置中自由移动,能选择性地将特定体积的试剂从所述试剂贮存组件中转移到所述摇匀式细胞孵化组件中。
15.进一步的,所述摇匀式孵化组件包括温度控制组件、若干离心管孔和摇晃组件。所述若干离心管孔用于放置实验人员手动放入的盛有细胞样本的离心管。所述摇匀式孵化组件能以预定的时间、温度和频率对细胞进行孵化,使得抗体与细胞样本充分结合。
16.作为优选的,所述试剂贮存组件位于整个装置的一侧,用以贮存标记物、裂解液、固定液等试剂。
17.可选的,部分所述试剂贮存组件可以安装温度控制组件,以满足科研实验室的个性化的需求。
18.作为优选的,本发明还提供了一种新的洗涤装置。与上述(即人工使用离心机)的现有步骤的技术方法不同的是,本发明只对细胞悬液进行一次洗涤,该步骤发生在整个制备流程的最后,即在同一反应容器中进行了所有的样品和试剂架取和孵化步骤之后。根据本发明,细胞的固定、透化、细胞标记等步骤都在同一反应容器中进行,不一定按顺序进行,并没有任何中间的洗涤步骤。只有在细胞固定、透化和标记之后,细胞样本才会最终被送入全新的洗涤装置进行清洗,以消除残留物质。优选的是,此细胞洗涤装置利用了过滤技术而不是离心技术,因而可以被集成入本自动化设备,并且提高了细胞留存率。
附图说明
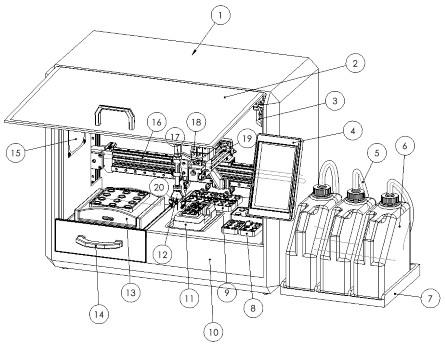
19.图1为本发明的立体空间结构示意图。
20.图2为本发明的正视图。
21.图3为本发明的侧视图。
22.图4为本发明的俯视图。
23.图5为本发明的立体空间结构示意图。
24.图6为摇匀式细胞孵化组件的立体空间结构示意图。
25.图7为全自动移液组件的立体空间结构示意图。
26.图8为带有温控装置的试剂贮存组件的立体空间结构示意图。
27.图9为试剂贮存组件的立体空间结构示意图。
28.附图标记说明。
29.1—设备外壳。
30.2—可开闭玻璃板。
31.3—细胞洗涤组件的缓冲液存放组件。
32.4—交互式显示器。
33.5—废液缸的导管。
34.6—废液缸。
35.7—废液缸的底座。
36.8—试剂贮存组件ⅰ。
37.9—试剂贮存组件ⅱ。
38.10—挡板。
39.11—带有控温装置的试剂贮存组件。
40.12—全自动移液组件。
41.13—摇匀式细胞孵化组件。
42.14—摇匀式细胞孵化组件的抽屉。
43.15—通风风扇。
44.16—全自动移液组件的x轴导轨。
45.17—细胞洗涤组件的移液针。
46.18—细胞洗涤组件。
47.19—全自动移液组件的y轴导轨。
48.20—全自动移液组件。
具体实施方式
49.以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
50.需要说明的是,本说明书中所引用的如“上”“下”“左”“右”“中间”及“一”等的用语,亦仅为便于叙述的明了,而非用以限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容下,当亦视为本发明可实施的范畴。
51.实施例。
52.以下结合附图和具体实施例,对本发明进行详细的结构和原理说明。
53.如图1,本实施例提供了一种流式细胞仪的前置样本制备装置,包括摇匀式细胞孵化组件13、全自动移液组件20、试剂贮存组件(ⅰ)8、试剂贮存组件(ⅱ) 9、带有控温装置的
试剂贮存组件11和细胞洗涤组件18。
54.实验开始时,实验人员需要手动将盛有细胞悬液的离心管放入摇匀式细胞孵化组件13的离心管孔中,然后将盛有裂解液的离心管放入试剂贮存组件8中,将盛有固定液的离心管放入试剂贮存组件9中,将盛有标记物悬液的离心管放入试剂贮存组件11中。
55.接下来设备开始自动工作。全自动移液组件20将自动移动至试剂贮存组件8上方,自动移液针管12会自动下降,插入盛有裂解液的离心管中,吸出裂解液,然后全自动移液组件20将会返回摇匀式细胞孵化组件13上方,将裂解液排入盛有样本悬液的某一离心管。然后,摇匀式细胞孵化组件13会根据用户设定的时间、频率和幅度开始摇晃,使得细胞样本和裂解液充分混匀。
56.然后,全自动移液组件20会重复上一步动作,将固定液从试剂贮存组件9转移到上一步的离心管中。然后,摇匀式细胞孵化组件13会根据用户设定的时间、频率和幅度开始摇晃,使得细胞样本和固定液充分混匀。
57.根据不同的实验要求,上述两步的动作可能会重复多次。
58.接下来,全自动移液组件20将自动移动至带有控温装置试剂贮存组件11上方,自动移液针管12会自动下降,插入盛有标记物悬液的离心管中,吸出标记物悬液,然后全自动移液组件20将会返回摇匀式细胞孵化组件13上方,将标记物悬液排入上一步的离心管中。然后,摇匀式细胞孵化组件13会根据用户设定的时间、频率和幅度开始摇晃,使得标记物和细胞样品充分结合。根据不同的实验要求,此步骤可能会重复多次,使得细胞带上不同种类的标记物。
59.然后,细胞洗涤组件18会移动到上一步的离心管上方,将包含杂质的细胞样本悬液吸入洗涤装置,利用抽压过滤原理去除杂质后,再将纯净的细胞样本悬液排回原来的离心管。
60.以上为针对摇匀式细胞孵化组件13中某一离心管中的细胞样本悬液的处理流程,在实际工作流程中,设备需要同时处理多个离心管中的样本悬液,因此上述步骤不一定连续进行。
61.在设备处理完细胞孵化组件13中所有离心管中的细胞样本悬液后,用户即可拉出细胞孵化组件13,取出里面的离心管,然后可将其放入流式细胞仪进行分析,流式样本制备流程结束。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1