一种人间充质干细胞分化成脂能力的检测方法与流程
本发明涉及生物,更具体地,本发明涉及一种人间充质干细胞分化成脂能力的检测方法。
背景技术:
1、人间充质干细胞(humanmesenchymalstemcells,hmscs)是近年来临床研究发展最为迅速的干细胞类型,其独特的生物学功能可归为三大类:多向分化潜能、免疫调控能力和组织再生功能。其中,多向分化潜能是指hmscs在特定体外诱导分化培养条件下,具有向内、中、外胚层不同细胞系列分化的潜能,表现为向骨、软骨、脂肪、肌、神经等细胞分化的能力。
2、hmscs作为治疗性细胞产品需通过质量控制满足包括基本生物学属性、安全性(微生物学安全性和生物学安全性)及生物学有效性在内的综合性质量要求。其中,生物学有效性是指间充质干细胞必须至少具备成脂、成骨、成软骨分化的能力,因此在其质量控制体系中需要对干细胞的上述分化能力进行检测、评价。目前成脂分化能力的评价方法主要为油红o染色法,该方法培养时间为21天,染色后通过图像软件对染色结果进行分析,所需周期长,仅为半定量分析,数据在分析过程中人为误差较大,不能客观反映hmscs的分化成脂能力。而近年来发展的通过检测细胞内成脂相关因子的mrna水平反映细胞分化成脂能力的相关研究,多为应用qrt-pcr技术检测成脂转录调控因子pparγ和c/ebpβ的表达,缺少成脂标志蛋白的检测,且检测时间长,数据不稳定,无法准确反映细胞的分化能力。因此,亟需开发一种可快速、规范、准确检测人间充质干细胞分化成脂能力的方法,以快速准确的评价细胞分化成脂的能力。
技术实现思路
1、基于上述问题,本发明的目的在于提供一种快速精确的定量检测方法,高效、客观、准确的检测hmscs的成脂分化能力,以解决传统方法存在的检测周期长,数据无法定量等问题。
2、为实现上述目的,本发明提供如下技术方案:
3、一方面,本发明提供一种人间充质干细胞分化成脂能力的检测方法,包括以下步骤:
4、(1)铺板:当干细胞培养瓶内的细胞融合率达到75-85%时,消化,离心,弃去上清液,加入适量培养基重悬细胞,计数,调整细胞密度,铺板;
5、(2)诱导:铺板后,当细胞融合度到90%以上时,更换诱导培养基,连续培养,取不同诱导时间点的诱导样品,低温保存;
6、其中所述诱导培养基为dmem/f12basic培养基中加入fbs、双抗、l-谷氨酰胺、地塞米松、ibmx、吲哚美辛、罗格列酮、胰岛素;
7、(3)检测:提取样品rna,并逆转录为cdna,以逆转录的cdna为模板,使用实时荧光定量pcr对目标基因和内参基因进行扩增检测;
8、(4)数据处理:同时测定样品中目标基因和内参基因的ct值,计算样品的目标基因相较空白样品的目标基因的相对表达倍数。
9、优选地,步骤(1)中铺板细胞密度为1×105cells/cm2。
10、优选地,步骤(1)中铺板所使用的为明胶包被板。
11、优选地,步骤(2)中所述诱导培养基中各添加成分的浓度分别为fbs10%(v/v),双抗1%(v/v),l-谷氨酰胺1%(v/v),地塞米松1μm,ibmx450μm,吲哚美辛100μm,罗格列酮2μm,胰岛素12μg/ml。
12、优选地,步骤(2)中诱导时间为7天和14天。
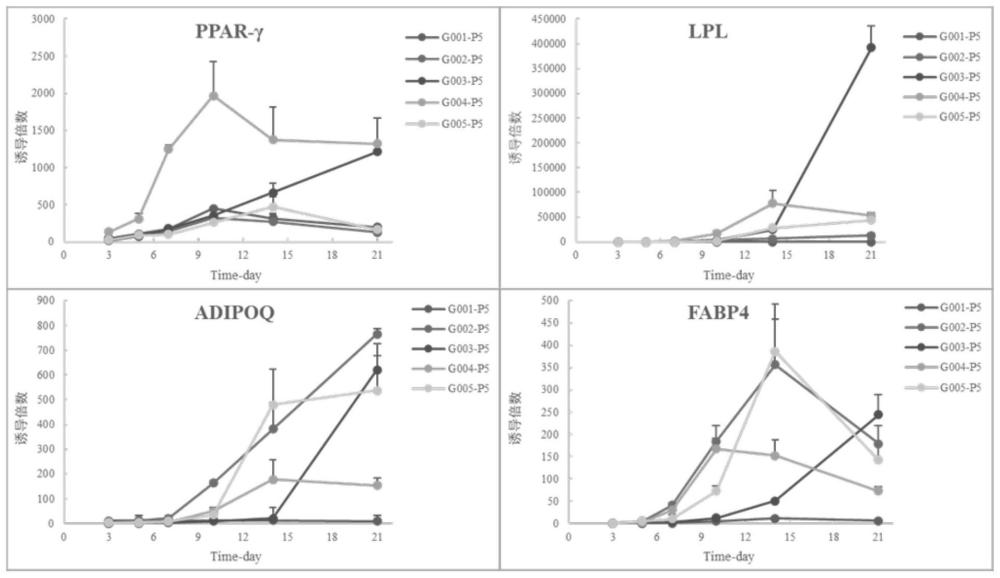
13、优选地,步骤(3)中所述检测的目标基因为:ppar-γ,lpl,adipoq,fabp4,内参基因为gapdh。以ppar-γ,lpl,adipoq,fabp4,gapdh为靶基因设计的pcr检测引物核苷酸序列如表1所示。
14、表1.引物组的具体信息
15、
16、
17、另一方面,本发明提供上述检测方法在干细胞质量控制中的应用。
18、与现有技术相比,本发明所使用的诱导体系、诱导方法可有效缩短诱导时间,检测周期更短,测定时使用的标志物和检测序列具有较高的特异性和灵敏度。本发明提供的整套检测方法可实现快速精确的定量检测,操作简便,检测周期短,灵敏度高,适用范围广,可用于不同来源、不同批次、不同代次干细胞的分化成脂能力的检测、评价,可作为标准化方法用于干细胞质量控制。
技术特征:
1.一种人间充质干细胞分化成脂能力的检测方法,包括以下步骤:
2.根据权利要求1所述的方法,其特征在于,步骤(1)中铺板细胞密度为1×105cells/cm2。
3.根据权利要求1所述的方法,其特征在于,步骤(1)中铺板所使用的为明胶包被板。
4.根据权利要求1所述的方法,其特征在于,步骤(2)中所述诱导培养基中各添加成分的浓度分别为fbs10%(v/v),双抗1%(v/v),l-谷氨酰胺1%(v/v),地塞米松1μm,ibmx450μm,吲哚美辛100μm,罗格列酮2μm,胰岛素12μg/ml。
5.根据权利要求1所述的方法,其特征在于,步骤(2)中诱导时间为7天和14天。
6.根据权利要求1所述的方法,其特征在于,步骤(3)中所述检测的目标基因为:ppar-γ,lpl,adipoq,fabp4,内参基因为gapdh。
7.根据权利要求6所述的方法,其特征在于,步骤(3)中以ppar-γ,lpl,adipoq,fabp4,gapdh为靶基因设计的pcr检测引物核苷酸序列如下所示:
8.权利要求1-7任一项所述的方法在干细胞质量控制中的应用。
技术总结
本发明提供了一种人间充质干细胞分化成脂能力的检测方法,通过诱导成脂培养基培养后,应用实时荧光定量PCR方法检测细胞内成脂转录因子及成脂标志蛋白的mRNA水平,实现对细胞分化成脂能力的定量评价。本发明的方法可实现快速精确的定量检测,检测周期短,灵敏度高,适用范围广,可用于不同来源、不同批次、不同代次干细胞的分化成脂能力的检测、评价,可作为标准化方法用于干细胞质量控制。
技术研发人员:慈小燕,闫凤英,丁凯,娄云云
受保护的技术使用者:天津和创生物技术有限公司
技术研发日:
技术公布日:2024/2/1
- 还没有人留言评论。精彩留言会获得点赞!