Masp1在筛选预防和/或治疗心血管疾病的药物中的应用的制作方法
masp1在筛选预防和/或治疗心血管疾病的药物中的应用
技术领域
1.本发明涉及masp1在筛选预防和/或治疗心血管疾病的药物中的应用,属于生物医药领域。
背景技术:
[0002]“心肌保护”近年来一直是心脏内、外科研究的热点。最近资料表明,缺血缺氧的心肌细胞内会发生许多变化,包括细胞内钙超载,自由基产生,膜损害,atp(adenosine triphosphate,atp)水平下降,氧耗竭等。
[0003]
为了干预心肌缺血及保护心肌,在近20年来研究了许多药物,如β-受体阻滞剂,钙拮抗剂,转换酶抑制剂,各种氧自由基清除剂等,但其对心肌的保护效果临床尚未肯定。现有治疗心肌缺血的药物,还没有一种能绝对减少心肌梗死,对抗心肌缺血。
[0004]
现有的各类心血管病治疗药物,除转换酶抑制剂具有阻滞生长因子产生,抑制蛋白质合成,减轻心肌肥厚的作用外,其它药物均无直接调节心肌生长、分化、修复的作用。近年来,国外已开始重视使用药物方法诱导心肌自身的保护能力,如转导基因促进心肌细胞再生等的研究。通过细胞外信号触发各种传递机制,调控心肌、血管细胞的增殖或重构。
[0005]
但是所有这些研究都处于动物试验或临床前研究阶段。因此,在体外循环心肌保护方法尚未完善的情况下,设计一种对机体无损害,又能于术前、术中及术后保护心肌的药物,对探索心肌缺血及再灌注损伤的防治,提供新的思路和途径,将有重要意义。
技术实现要素:
[0006]
本发明的目的是提供masp1在筛选预防和/或治疗心血管疾病的药物中的应用。为了实现以上上述目的,本发明提供了以下技术方案:
[0007]
技术方案一:检测masp1表达水平的检测试剂在筛选具有心肌保护作用的心血管疾病药物中的应用。
[0008]
技术方案二:检测masp1表达水平的检测试剂在筛选具有心肌保护作用的心肌缺血药物中的应用。
[0009]
技术方案三:检测masp1表达水平的检测试剂在筛选具有心肌保护作用的心肌缺血再灌注损伤药物中的应用。
[0010]
技术方案四:masp1在筛选预防和/或治疗心血管疾病的药物中的应用。
[0011]
技术方案五:masp1在筛选预防和/或治疗心肌缺血的药物中的应用。
[0012]
技术方案六:masp1在筛选预防和/或治疗心肌缺血再灌注损伤的药物中的应用。
[0013]
进一步地,所述masp1是作为药物的靶点,进而实现筛选心血管疾病、心肌缺血或心肌缺血再灌注损伤药物的目的。
[0014]
进一步地,所述药物为心肌肽。
[0015]
与现有技术相比,本发明的有益效果:
[0016]
本发明通过实验发现,masp1在心肌缺血再灌注模型组中表达下调,而使用心肌肽
后相对模型组表达上调,说明该分子可能对心肌损伤起到保护作用,心肌肽的作用可能与该分子介导的信号通路及生理机制相关。因此,masp1能够作为心肌肽作用的新靶点用于“心肌保护”的研究中。
附图说明
[0017]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0018]
图1为rna-seq展示masp1在各组动物组织中的fpkm值情况;
[0019]
图2为各模型组中masp1的mrna表达情况;
[0020]
图3为各模型组中masp1蛋白的表达和分布情况;
[0021]
图4为各模型组的病理状态;
[0022]
图5为各模型组细胞中纤维和炎性因子表达情况;
[0023]
图6为各模型组的细胞早期凋亡含量变化情况;
[0024]
图7为各模型组的细胞早期凋亡的水平变化情况;
[0025]
图8为各模型组的组织中ros含量变化情况;
[0026]
图9为各模型组的组织中ros的水平变化情况;
[0027]
图10为各模型组线粒体呼吸链复合物i的活性检测结果。
具体实施方式
[0028]
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
[0029]
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
[0030]
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
[0031]
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本发明说明书和实施例仅是示例性的。
[0032]
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
[0033]
实施例中心肌肽和masp1,本领域技术人员均可通过常规购买得到。
[0034]
实施例1
[0035]
1心肌肽的获取
[0036]
参考专利cn200610138176.9中实施例1的方法制备。
[0037]
2masp1的获取
[0038]
利用rna-seq对心肌缺血再灌注模型大鼠心肌组织进行测序,测序数据结果如图1所示。信号通路为complement and coagulation cascades;level 1:organismal systems;level 2:immune system。
[0039]
masp1作为靶点的信息:该基因编码丝氨酸蛋白酶,作为补体激活凝集素途径的组成部分。补体通路在先天和适应性免疫反应中发挥重要作用。编码的蛋白质作为酶原合成,当它与凝集素途径的病原体识别分子、甘露糖结合凝集素和ficolins复合时被激活。编码的蛋白还能切割纤维蛋白原和因子xiii,并可能参与凝血过程。该基因的剪接变体缺乏丝氨酸蛋白酶结构域,可作为补体途径的抑制剂。交替剪接会产生多个转录变体。
[0040]
3masp1作为新靶点的验证性实验
[0041]
3.1大鼠心肌缺血再灌注模型
[0042]
采用左冠状动脉前降支结扎法复制心梗模型。将模型组大鼠麻醉后颈部及胸前备皮,仰卧位固定于手术台中央,带上吸气面罩,将多导生理记录仪的电极分别插入大鼠左右上及左下肢,记录标准ⅱ导联心电图。于大鼠左胸第三、四肋间隙(可手按胸腔感知心脏跳动最明显的位置)作一斜行切口约1.5cm,止血钳逐层分离皮下肌肉组织后撑开胸腔,并用牵拉钩牵拉,暴露心脏。在体视显微镜视野下,剥离心包膜,持6/0无创缝合针丝线,于肺动脉圆锥与左心耳交界,距离冠状动脉起始点下方1~2mm处进针,深度1.0~1.5mm进行结扎。扎针进线后在上方放一根线径0.53mm,长5cm鱼线,活结结扎。即用干燥棉签清理胸腔,挤出胸腔内残余气体,并用3/0缝合线逐层缝合肌肉及皮肤,切口处进行局部消毒。观察1min后将大鼠放置在恒温电热毯上,待40min后轻抽鱼线再灌注。
[0043]
3.2实验分组
[0044]
1)正常大鼠组(nomal rat):sd大鼠;
[0045]
2)i/r模型大鼠组(model rat):心肌缺血再灌注损伤模型;
[0046]
3)治疗组:心肌肽治疗组(i/r模型+心肌肽),心肌缺血再灌注损伤模型sd大鼠,心肌肽注射液尾静脉注射;
[0047]
4)rage基因抑制剂干预治疗组:imasp1抑制剂+治疗组(imasp1+i/r模型+心肌肽):利用masp1抑制剂+心肌肽注射液,对心肌缺血再灌注损伤模型sd大鼠的尾静脉进行注射。每组6只大鼠,共24只。masp1抑制剂于模型前通过腹腔注射,注射后14d,开始心肌肽药物进行连续给药28天后处死动物并进行心肌组织解剖和处理。
[0048]
3.3实验检测内容
[0049]
1)苏木精-伊红染色法(hematoxylin-eosin staining)染色观察病理学变化:
[0050]
pbs冲洗心肌组织,取部分组织固定在10%中性福尔马林中,70%乙醇进行脱水并经过透明剂后浸蜡、包埋、切片和烤片。切片使用二甲苯和酒精梯度脱蜡后蒸馏水浸洗5min,放入mayer氏苏木素染液染色5min,清洗后再次浸入1%伊红染液染色5min,清洗后依次放入酒精和二甲苯后进行封片,晾干后于光学显微镜下观察拍照。
[0051]
2)qpcr法检测组织中masp1的表达水平:
[0052]
使用trizol法提取心肌组织总rna,紫外分光光度计测定od
260
/od
280
值以计算rna的纯度和浓度。构建逆转录反应体系将总rna进行逆转录为cdna,聚合酶链式反应pcr进行masp1的mrna表达检测,并利用2
‑△△
ct
方法计算表达数据。
[0053]
3)免疫组化(immunohistochemistry,ihc)法检测组织中masp1表达水平:
[0054]
心肌组织使用酒精进行梯度脱水和透明后,经过石蜡包埋、切片和烤片、脱蜡以及抗原修复后,将配制好的3%的过氧化氢滴加于切片组织上以阻断内源性过氧化物酶,室温孵育15min后,用pbs冲洗3次,在组织周围滴加稀释好的正常山羊血清进行血清封闭。添加一抗4℃孵育过夜后加酶标二抗,37℃孵育30min后加显色剂。冲洗后滴加新鲜配制的dab显色液,显微镜下观察,阳性信号为棕黄色或棕褐色,用自来水冲洗切片终止显色。harris苏木素复染后进行切片脱水、封片,晾干后可以在显微镜下观察及采集图像。
[0055]
4)蛋白质免疫印迹(western blot,wb)法检测组织masp1、蛋白表达情况:
[0056]
提取心肌组织总蛋白,使用bca法检测蛋白总浓度。制备蛋白样本和聚丙烯酰胺凝胶上样后进行电泳,以marker为对照进行切胶,将滤纸、pvdf膜剪成与凝胶尺寸大小相同,用甲醇浸泡pvdf膜15s。使膜由白色变为半透明后放入超纯水中,静置2min,将处理好的pvdf膜放入转膜缓冲液中平衡15min。按海绵垫,滤纸,凝胶,pvdf膜,滤纸,海绵垫的顺序叠加在一起,用玻璃棒赶走各层之间的气泡,放入转膜槽中,倒入转移缓冲液。将膜用tbst漂洗3次,后用5%的脱脂奶粉37℃缓慢震荡2h进行封闭。用封闭液稀释抗体至合适浓度孵育一抗,4℃过夜。一抗孵育结束后将pvdf膜放入以1∶5000稀释的hrp标记的兔二抗或者鼠二抗溶液中,37℃缓慢振荡孵育l h,tbst冲洗3次。在膜上加入适量的ecl发光液,利用一体式化学发光仪拍摄照片。
[0057]
5)线粒体能量代谢和功能检测:
[0058]
使用ros检测试剂盒(购于武汉伊莱瑞特生物科技股份有限公司)检测各组组织中ros含量,以蛋白浓度进行换算;
[0059]
使用线粒体膜电位检测试剂盒(购于北京索莱宝科技有限公司)检测各组线粒体膜电位;
[0060]
使用线粒体呼吸链复合体ⅰ活性检测试剂盒(购于江西江蓝纯生物试剂有限公司)检测各组线粒体呼吸链复合体i活性。
[0061]
3.4主要实验结果
[0062]
3.4.1 qpcr实验检测各组masp1的表达水平
[0063]
结果如图2所示,心肌缺血再灌注模型鼠组织中masp1的表达降低,使用心肌肽处理后表达相比模型组出现回升,使用masp1抑制剂处理后造模同时加入心肌肽处理masp1的表达相比模型+心肌肽治疗组出现降低,但仍高于模型组中的表达。说明心肌肽在心肌缺血再灌注模型中具有恢复masp1表达的功能。
[0064]
3.4.2免疫组化(ihc实验)实验检测各组中masp1蛋白的表达和分布
[0065]
结果如图3所示,心肌缺血再灌注大鼠模型组织切片中masp1的表达较正常大鼠明显降低,而使用心肌肽处理后的模型大鼠组织中masp1的表达出现上升,而使用masp1抑制剂预处理的模型大鼠同时使用心肌肽注射后,其表达较心肌肽治疗组降低。
[0066]
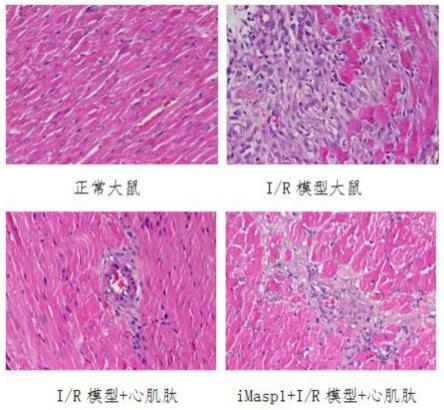
3.4.3 he染色观察各组病理状态
[0067]
结果如图4所示,心肌缺血再灌注模型大鼠相比正常大鼠心肌组织心肌细胞排布
不规则,细胞核/质比失衡,炎性细胞浸润增多;心肌肽处理后细胞排列明显规则,尽管仍有部分炎性细胞浸润;使用masp1抑制剂注射的模型动物加入心肌肽处理后同检测时间点相比,心肌肽处理组细胞尚未明显恢复均匀分布,毛细血管和炎性细胞增多。
[0068]
3.4.4 masson染色检测各组细胞中纤维和炎性因子
[0069]
结果如图5所示,心肌缺血再灌注模型大鼠心肌组织切片相比较正常大鼠切片胶原纤维排列紊乱,肌纤维减少,炎性因子浸润增多;而加入心肌肽处理后的模型动物心肌组织肌纤维有所恢复,胶原纤维变少,炎性浸润减少。使用masp1抑制剂注射的模型动物加入心肌肽处理后同检测时间点相比,心肌肽处理组肌纤维排列变得不规律,胶原纤维散布增多,且炎性浸润增加。
[0070]
3.4.5 jc-1线粒体膜电位检测细胞早期凋亡水平
[0071]
结果如图6-7所示,与正常大鼠相比,模型组大鼠相比正常大鼠流式红色荧光降低,绿色荧光增加。说明模型组大鼠心肌细胞早期凋亡增多;而加入心肌肽可以提高红光减少绿光,说明心肌肽可以抑制心肌细胞凋亡水平,增加其活性。当使用masp1抑制剂干预后的模型大鼠同时使用心肌肽注射液后,显示细胞凋亡水平高于心肌肽处理组,但仍低于模型组。
[0072]
3.4.6 ros试剂盒检测各模型组组织中ros含量
[0073]
结果如图8-9所示,心肌缺血再灌注模型组大鼠心肌组织ros水平显著高于正常大鼠,加入心肌肽后可以降低ros水平,而使用masp1抑制剂处理后的模型大鼠同时使用心肌肽注射液后ros的水平相比单独心肌肽处理组明显上升。
[0074]
3.4.7线粒体呼吸链复合物i活性检测
[0075]
结果如图10所示,模型组线粒体呼吸链复合物的活性相比正常大鼠组明显降低,而加入心肌肽后活性升高,使用masp1抑制剂预处理的动物模型同时心肌肽处理后,线粒体呼吸链复合物i活性有所降低。
[0076]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1