用于检测Sf9细胞DNA片段大小分布的引物对及检测方法与流程
用于检测sf9细胞dna片段大小分布的引物对及检测方法
技术领域
1.本发明涉及生物检测领域,尤其涉及用于检测sf9细胞dna片段大小分布的引物对及检测方法。
背景技术:
2.在基因治疗领域,人胚胎肾细胞(hek293)和杆状病毒表达载体(baculovirus expression vectors,bevs)/草地贪夜蛾卵巢细胞(spodoptera frugiperda cell,sf9)表达系统(bev-sf9)是用于生产基因治疗生物制品最主要的两个表达系统。尽管使用hek293是该行业金标准,但由于哺乳动物需贴壁生长导致放大生产困难。
3.昆虫细胞是新兴的生物制品生产基质,其中bev-sf9是最常用的昆虫细胞表达系统,该系统是以杆状病毒作为外源基因载体,以昆虫细胞作为宿主进行基因组自我扩增与目的蛋白表达。相较于hek293,sf9昆虫细胞可以在大规模反应器中高密度悬浮培养,而杆状病毒对于哺乳动物和植物是非致病性的,所以bev-sf9表达系统具有易于规模化生产、培养成本低、残留dna对脊椎动物的生物安全性高等优势,已陆续被研究用于生产重组蛋白、raav载体、亚单位疫苗、重组病毒样颗粒(vlp)等。
4.1983年,smith等首次使用bev-sf9表达系统获得重组蛋白,该方法被证明是一种经济可行的重组蛋白生产平台。
5.2002年,urabe等通过携带aav包装基因的重组杆状病毒感染sf9细胞来生产raav,产量远高于hek293表达系统,可达10
14
vg(vector genomes)/l,满足临床raav载体用量,为raav载体的生产提供了一种简单快捷、经济高效的方法。
6.2013年,由protein sciences corporation研制的全球第一支针对流感病毒的三价重组亚单位疫苗(recombination ha vaccine,rha vaccine)由美国食品药品监督管理局批准上市,用以预防流感病毒的大面积爆发,该疫苗即以bev-sf9作为表达系统。
7.2016年,fda又通过了覆盖率更高的四价流感疫苗。
8.而在新型冠状病毒大流行的背景下,截至2021年7月全球共有32个蛋白亚单元疫苗正在开展临床试验研究,截至2022年7月25日查找到10个新冠重组疫苗(sf9细胞)提交了临床试验登记。由此可见,sf9昆虫细胞在生物制品的生产中具有重要地位。
9.优质的生物制品能够帮助人类预防、治疗疾病,但是生产过程中引入的宿主细胞残留dna(host cell dna,hcd)会给使用者带来致瘤性、感染性和免疫原性风险。国内外监管机构对于疫苗中宿主细胞dna的残留量和残留dna片段的大小分布等有强烈的关注。
10.目前可见报道中对生物制品残留dna片段的分析方法主要有毛细管电泳和定量pcr法(qpcr)。毛细管电泳(capillary electrophoresis,ce)是粒子在高压电场驱动下,在毛细管中按其滴度或分配系数,进行高效、快速分离的一种电泳技术,分为芯片式毛细管电泳(chip ce)和毛细管阵列电泳(cae),可用于对核酸浓度和纯度的测定,检测灵敏度约为1~5pg/μl。定量pcr法(qpcr)是一种在dna扩增反应中,根据每个反应管内的荧光信号到达
设定的域值时所经历的循环数(ct值)和标准曲线浓度,从而定量分析未知样品核酸浓度的技术。相较于毛细管电泳法,qpcr法的检测限可达fg级别,具有更高的灵敏度,且qpcr法操作简便、样品通量较高,作为国际公认的残留dna的检测方法,目前分子生物学实验室已普遍具备qpcr的实验条件。尽管市场对sf9细胞基质生物制品中的宿主细胞残留dna片段有着迫切的定量分析需求,但到目前为止尚未见相关报道。
11.参考文献:[1]usami a,ishiyama s,enomoto c,et al.comparison of recombinant protein expression in a baculovirus system in insect cells(sf9)and silkworm[j].journal of biochemistry,2011,149(2):219-27.[2]shen x,hacker d l,baldi l,et al.virus-free transient protein production in sf9 cells[j].journal of biotechnology,2014,171:61-70.[3]urabe m,ding c,kotin r m.insect cells as a factory to produce adeno-associated virus type 2vectors[j].human gene therapy,2002,13(16):1935-43.[4]chen h.intron splicing
–
mediated expression of aav rep and cap genes and production of aav vectors in insect cells[j].molecular therapy,2008,16(5):924-30.[5]thompson c m,petiot e,mullick a,et al.critical assessment of influenza vlp production in sf9 and hek293 expression systems[j].bmc biotechnology,2015,15(1):1-12.[6]smith g e,fraser m j,summers m d.molecular engineering of the autographa californica nuclear polyhedrosis virus genome:deletion mutations within the polyhedrin gene[j].journal of virology,1983,46(2):584-93.[7]cox m,patriarca p a,treanor j.flublok,a recombinant hemagglutinin influenza vaccine[j].influenza&other respiratory viruses,2010,2(6):211-9.[8]meng f-y,gao f,jia s-y,et al.safety and immunogenicity of a recombinant covid-19vaccine(sf9 cells)in healthy population aged 18years or older:two single-center,randomised,double-blind,placebo-controlled,phase 1and phase 2trials[j].signal transduction and targeted therapy,2021,6(1):271.[9]药智网[z].https://db.yaozh.com/clinical?comprehensivesearchcontent=sf9&[10]lwer j.risk of tumor induction in vivo by residual cellular dna:quantitative considerations[j].journal of medical virology,2010,31(1):50-3.[11]peden k,sheng l,pal a,et al.biological activity of residual cell-substrate dna[j].developmental biology,2006,123:45-53.[12]klinman d m,yamshchikov g,ishigatsubo y.contribution of cpg motifs to the immunogenicity of dna vaccines[j].the journal of immunology,1997,158(8):3635-9.[13]krieg a m,yi a-k,matson s,et al.cpg motifs in bacterial dna trigger direct b-cell activation[j].nature,1995,374(6522):546-9.
[14]闫璐瑶.生物制品中宿主细胞残留dna检测的研究进展[j].国际生物制品学杂志,2021,44(3):5.[15]european pharmacopoeia commission.european pharmacopoeia 10.0[m].2019.[16]国家药典委员会.中华人民共和国药典2020年版三部[m].北京:中国医药科技出版社,2020.[17]olivier,vernay,eric,et al.comparative analysis of the performance of residual host cell dna assays for viral vaccines produced in vero cells[j].journal of virological methods,2019.[18]knezevic i,stacey g,petricciani j.who study group on cell substrates for production of biologicals,geneva,switzerland,11
–
12june 2007[j].biologicals,2008,36(3):203-11.[19]fda.guidance for industry:characterization and qualification of cell substrates and other biological materials used in the production of viral vaccines for infectious disease indications[s]2010,[20]国家药品监督管理局药品审评中心.基因治疗产品药学研究与评价技术指导原则(征求意见稿)[z].2020[21]united states pharmacopeia.general chapter,《1130》nucleic acid-based techniques—approaches for detecting trace nucleic acids(residual dna testing)(doc id:guid-373a1d1f-60dd-40e4-a922-1bdcc0c1aaf9_1_en-us)[z].usp-nf,rockville,md:united states pharmacopeia,2022.
技术实现要素:
[0012]
本发明是为了克服现有技术中对于sf9细胞残留dna的检测分析方法尚未完善,因此提供了一种用于定量检测sf9细胞dna片段大小分布的引物对及检测方法。
[0013]
为实现上述发明目的,本发明通过以下技术方案实现:在第一方面,本发明首先提供了一种用于检测sf9细胞dna片段大小分布的引物对,其至少包含4组引物对;其中:各引物对中的正向引物和反向引物分别特异性结合于sf9细胞基因组dna上seq id no:1所示区段;各组引物对扩增获得的扩增产物的长度分别为100bp以下、100-199bp、200-499bp以及499bp以上。
[0014]
作为优选,所述引物对选自以下引物对:第一引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第241-280位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第308-347位,并且所述引物对所扩增获得的扩增产物的长度为77-97bp;第二引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第210-247位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第308-347位,并且所述引物对所扩增获得的扩增产物的长度为108-128bp;第三引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列
的第238-279位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第442-482位,并且所述引物对所扩增获得的扩增产物的长度为215-235bp;第四引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第2-38位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第479-520位,并且所述引物对所扩增获得的扩增产物的长度为490-510bp。
[0015]
作为优选,所述引物对选自以下引物对:第一引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第251-270位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第318-337位,并且所述引物对所扩增获得的扩增产物的长度为87bp;第二引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第220-237位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第318-337位,并且所述引物对所扩增获得的扩增产物的长度为118bp;第三引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第248-269位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第452-472位,并且所述引物对所扩增获得的扩增产物的长度为225bp;第四引物对,其中的正向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第12-28位;所述反向引物结合于sf9细胞基因组dna上seq id no:1所示序列的第489-512位,并且所述引物对所扩增获得的扩增产物的长度为500bp。
[0016]
作为优选,所述第一引物对的正向引物如seq id no:5所示,反向引物如seq id no:7所示;所述第二引物对的正向引物如seq id no:3所示,反向引物如seq id no:7所示;所述第三引物对的正向引物如seq id no:4所示,反向引物如seq id no:8所示;所述第四引物对的正向引物如seq id no:2所示,反向引物如seq id no:9所示。
[0017]
在第二方面,本发明还提供了用于检测sf9细胞dna片段大小分布的引物对的组合,所述引物如上所示,且至少包括下述组合:所述第一引物对+所述第二引物对+所述第三引物对;所述第一引物对+所述第二引物对+所述第四引物对;所述第二引物对+所述第三引物对+所述第四引物对;所述第一引物对+所述第二引物对+所述第三引物对+所述第四引物对。
[0018]
在第三方面,本发明还提供了用于检测sf9细胞残留dna的检测试剂,所述检测试剂包括如上所述的引物对或者如上所述的引物对的组合。
[0019]
作为优选,所述检测试剂中还包括探针。
[0020]
作为优选,所述探针如seq id no:6所示,所述seq id no:6所示的序列结合于sf9细胞基因组dna上seq id no:1所示序列的第286-305位。
[0021]
将正向引物、反向引物以及探针组合后,即可获得所述检测试剂,在此本技术提出以下几种优选的组合方式。
[0022]
优选检测试剂组合1:正向引物如seq id no:5所示;反向引物如seq id no:7所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为87bp。
[0023]
优选检测试剂组合2:正向引物如seq id no:3所示;反向引物如seq id no:7所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为118bp。
[0024]
优选检测试剂组合3:正向引物如seq id no:4所示;反向引物如seq id no:8所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为225bp。
[0025]
优选检测试剂组合4:正向引物如seq id no:2所示;反向引物如seq id no:9所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为500bp。
[0026]
作为优选,所述检测试剂中的探针端部标记有荧光报告基团fam以及非荧光淬灭基团mgb。
[0027]
在第四方面,本发明还提供了用于检测sf9细胞残留dna的检测试剂盒,其包含所述的引物对或者引物对的组合或者所述的检测试剂。
[0028]
作为优选,所述检测试剂盒中还包括标准品对照。
[0029]
在第五方面,本发明还提供了一种sf9细胞残留dna的检测方法,所述方法包括:利用所述的引物对或者引物对的组合或者所述的检测试剂或者所述的检测试剂盒,对待测样品进行qpcr,并检测qpcr扩增产物。
[0030]
第六方面,本发明还提供了所述的引物对或者检测试剂或者检测试剂盒的用途,用于检测待测对象中是否存在sf9细胞残留dna及其片段大小分布。
[0031]
作为优选,基于上述用途,本发明还能够用于定量检测待测对象中sf9细胞残留dna片段。
[0032]
作为优选,所述待测对象选自基于sf9细胞基质培育制备的重组蛋白、raav载体、亚单位疫苗、重组病毒样颗粒(vlp)等中的任意一种。
[0033]
本发明具有以下有益效果:(1)本发明的目的是提供一种采用实时荧光定量pcr(real-time qpcr)技术定量检测sf9残留dna片段大小分布的引物对、方法和试剂盒,用于分析生物制品中间品、成品中的sf9残留dna片段大小分布,有利于改进工艺、提高产品质量,用于产品质量控制和放行。
[0034]
(2)利用所述引物对的pcr检测方法操作简便快捷,从获得样本到给出检测报告只需4h;灵敏度高,定量限均为30fg/rxn;(3)专属性强,能区分cho细胞、ns0细胞、vero细胞、293t细胞、毕赤酵母、e.coli、high five(high 5)昆虫细胞、苜蓿尺蠖核多角体病毒(acnpv)、重组腺相关病毒(raav)等干扰性dna。
附图说明
[0035]
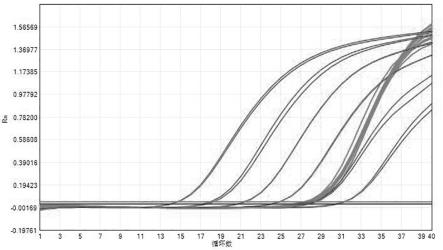
图1为体系1的标准曲线的扩增曲线。
[0036]
图2为体系1的线性关系图。
[0037]
图3为体系2的标准曲线的扩增曲线。
[0038]
图4为体系2的线性关系图。
[0039]
图5为体系3的标准曲线的扩增曲线。
[0040]
图6为体系3的线性关系图。
[0041]
图7为体系4的标准曲线的扩增曲线。
[0042]
图8为体系4的线性关系图。
[0043]
图9为体系1与体系2的专属性测试(干扰工程细胞/工程菌dna)的扩增曲线。
[0044]
图10为体系3与体系4的专属性测试(干扰工程细胞/工程菌dna)的扩增曲线。
[0045]
图11为体系1与体系2的专属性测试(干扰病毒相关dna)的扩增曲线。
[0046]
图12为体系3与体系4的专属性测试(干扰病毒相关dna a)的扩增曲线。
[0047]
图13为体系1的定量限测试的扩增曲线。
[0048]
图14为体系2的定量限测试的扩增曲线。
[0049]
图15为体系3的定量限测试的扩增曲线。
[0050]
图16为体系4的定量限测试的扩增曲线。
具体实施方式
[0051]
下面结合说明书附图以及具体实施例对本发明做进一步描述。本领域普通技术人员在基于这些说明的情况下将能够实现本发明。此外,下述说明中涉及到的本发明的实施例通常仅是本发明一部分的实施例,而不是全部的实施例。因此,基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
[0052]
本发明的引物对本发明所使用的术语“引物”具有本领域技术人员常规理解的意义。本发明的sf9细胞残留dna特异性引物不是针对外源基因本身或者病毒载体本身设计,而是针对sf9细胞残留dna的seq id no:1所示序列设计的。换言之,本发明的引物可以特异性结合于sf9细胞基因组dna的seq id no:1所示序列。
[0053]
其中sf9细胞基因组dna的seq id no:1所示序列具体如下所示:tctagacacacggcagtgtgtccgccaagttcgagcaaaaaaaccgacacaccggccgtgggttatattacacgaaccatttcgggccaagttcgacccacctataactcaaaatctattttatctacgcgtataaaatttctagtatctattgagatctacttacttatctaaaatacaaaatttcattaatgtacctattgtagatcttgagatattgacgtcagaaaatcgctatttttactatacactcactgactgactgactcactcactcatcaaaaacctagaccacttccaatagtcgtattgacttgaaatttggcatggaggtaggtatttaggtcaaggtaaaggaaaaaatctgaaaatggccaagtgtgagtcggttttaaaaataatgaaggtgtaaattcatacccctaaggaactaaaacaaaaaaattatctatatcttccaatggtcgtaccgacctaaaattcgttacgaaggtttgtatttagtcaaagtaaagtaaaa。
[0054]
鉴于本发明的教导和本领域的公知常识,本领域技术人员应该理解,针对seq id no:1所示序列可以设计多种引物对。因此,本发明的引物对不限于实施例中具体的到的引物对。
[0055]
在具体的实施方式中,正向引物如seq id no:2~5中的任意一项所示。
[0056]
seq id no:2所示序列具体为:ggcagtgtgtccgccaa,其结合于sf9细胞基因组dna上seq id no:1所示序列的第12-28位。
[0057]
seq id no:3所示序列具体为:gacgtcagaaaatcgcta,其结合于sf9细胞基因组dna上seq id no:1所示序列的第220-237位。
[0058]
seq id no:4所示序列具体为:acactcactgactgactgactc,其结合于sf9细胞基因组dna上seq id no:1所示序列的第248-269位。
[0059]
seq id no:5所示序列具体为:ctcactgactgactgactca,其结合于sf9细胞基因组
dna上seq id no:1所示序列的第251-270位。
[0060]
在具体的实施方式中,反向引物如seq id no:7~9中的任意一项所示。
[0061]
seq id no:7所示序列具体为:cctacctccatgccaaattt,其结合于sf9细胞基因组dna上seq id no:1所示序列的第318-337位。
[0062]
seq id no:8所示序列具体为:cggtacgaccattggaagata,其结合于sf9细胞基因组dna上seq id no:1所示序列的第452-472位seq id no:9所示序列具体为:actttgactaaatacaaaccttcg,其结合于sf9细胞基因组dna上seq id no:1所示序列的第489-512位。
[0063]
在具体的实施方式中,所述引物对选自以下引物对:所述第一引物对的正向引物如seq id no:5所示,反向引物如seq id no:7所示;所述第二引物对的正向引物如seq id no:3所示,反向引物如seq id no:7所示;所述第三引物对的正向引物如seq id no:4所示,反向引物如seq id no:8所示;所述第四引物对的正向引物如seq id no:2所示,反向引物如seq id no:9所示。
[0064]
引物对的组合:所述引物对如上所述第一引物对、第二引物对、第三引物对以及第四引物对所示,且至少包括下述组合:所述第一引物对+所述第二引物对+所述第三引物对;所述第一引物对+所述第二引物对+所述第四引物对;所述第二引物对+所述第三引物对+所述第四引物对所述第一引物对+所述第二引物对+所述第三引物对+所述第四引物对。
[0065]
本发明的探针:本文所述的术语“探针”具有本领域技术人员常规理解的意义,即一小段单链dna或者rna片段,用于检测与其互补的核酸序列。
[0066]
鉴于本发明的教导和本领域的公知常识,本领域技术人员应该理解,在知晓引物对的前提下,本领域技术人员可以根据正向引物和反向引物结合位点之间的模板序列自主设计探针,并检测该探针与引物对的技术效果。在具体的实施方式中,本领域普通技术人员可根据需要具体设计探针,所述探针可以处于液相中,也可以固定于固相上;可以在扩增前结合,也可以在扩增后结合。因此,本发明的探针并不限于实施例中具体公开的探针。本发明的引物对也不限于与实施例中具体公开的探针配对使用。
[0067]
在具体的实施方式中,本发明的探针如seq id no:6所示序列。
[0068]
seq id no:6所示序列具体为:fam-aacctagaccacttccaata-mgb,其结合于sf9细胞基因组dna上seq id no:1所示序列的第286-305位。
[0069]
本发明的检测试剂:本发明还提供用于定量检测sf9细胞残留dna的检测试剂,所述检测试剂包含本发明的引物对、探针以及实施pcr所需的其它成分,例如qpcr reaction buffer,dna稀释液,dna定量参考品,dna定量参考品。
[0070]
在具体的实施方式中:所述引物对,包含如上所述第一引物对、第二引物对、第三引物对以及第四引物。
[0071]
所述探针为如seq id no:6所示的序列。
[0072]
所述第一引物对、第二引物对、第三引物对以及第四引物与探针之间结合,在此本技术提出以下几种优选的组合方式。
[0073]
优选检测试剂组合1:正向引物如seq id no:5所示;反向引物如seq id no:7所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为87bp。
[0074]
优选检测试剂组合2:正向引物如seq id no:3所示;反向引物如seq id no:7所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为118bp。
[0075]
优选检测试剂组合3:正向引物如seq id no:4所示;反向引物如seq id no:8所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为225bp。
[0076]
优选检测试剂组合4:正向引物如seq id no:2所示;反向引物如seq id no:9所示,探针如seq id no:6所示,所述检测试剂所扩增获得的扩增产物长度为500bp。
[0077]
在具体的实施方式中,本发明的检测试剂的检测灵敏度达到30fg/rxn。
[0078]
在本发明的引物对或检测试剂的基础上,本发明还提供了用于检测sf9细胞残留dna的检测试剂盒,所述试剂盒中包括容器以及位于容器中的上述本发明引物对以及探针。
[0079]
在具体的实施方式中,本发明中的试剂还包括:qpcr reaction buffer、dna稀释液、dna定量参考品。
[0080]
在本发明的引物对或检测试剂的基础上,本发明进一步提供了sf9细胞残留dna的检测方法,所述方法包括利用如上所述的引物对或者如上所述的检测试剂,对待测样品进行qpcr检测。
[0081]
下面结合具体实施例,对本发明作进一步阐述,应理解,这些实施例仅用于说明本发明,而不用于限制本发明的范围,下列实施例中未注明具体条件的实验方法,通常按照常规条件,或者按照制造厂商所建议的条件,除非另外说明,否则百分比和份数按重量计算。
[0082]
【本发明所用的材料、仪器及方法】【材料】qpcr reaction buffer、dna稀释液、本发明引物对、本发明探针、sf9 dna定量参考品、cho dna定量参考品、vero dna定量参考品、human dna定量参考品、mdck dna定量参考品、e.coli dna定量参考品、毕赤酵母dna定量参考品、ns0 sp 2/0国家标准品、high 5dna原液均来自湖州申科生物技术有限公司;重组aav2病毒、重组aav5病毒、重组scaav2病毒,均购自云舟生物科技(广州)股份有限公司。
[0083]
本发明引物对以及本发明探针的序列如下表1所示。
[0084]
表1
[0085]
将引物对以及探针进行组合,得到如下表2所示的几种不同的体系。
[0086]
表2体系编号组合方式产物大小体系1seq id no:5、seq id no:6、seq id no:787bp体系2seq id no:3、seq id no:6、seq id no:7118bp体系3seq id no:4、seq id no:6、seq id no:8225bp体系4seq id no:2、seq id no:6、seq id no:9500bp。
[0087]
【仪器】shentek pcr实时荧光pcr检测系统,型号为96s。
[0088]
【方法】1.标准曲线样品准备用dna稀释液将sf9 dna定量参考品进行10倍梯度稀释,配制成300pg/μl、30pg/μl、3pg/μl、0.3pg/μl、0.03pg/μl、0.003pg/μl的标准品溶液。
[0089]
2.qpcr反应体系1)检测体系30μl:20μl qpcr反应液+10μl模板;2)设置反应程序:95℃预变性10min;95℃15s,60℃30s,72℃1min30 s,40个循环;反应体积30μl。
[0090]
3.数据分析扩增结束后,设置阈值线,读取标准曲线的扩增效率、斜率、r2以及各样品的检测值。
[0091]
4.结果判定1)标准曲线方程的相关系数r2应大于0.990,斜率在-3.1~-3.8(即扩增效率在83.3%~110.0%);2)无模板对照(ntc)和干扰性dna的ct值未检出或者≥35.00。vic信号为有效的“s”型扩增曲线。
[0092]
【具体实施例】实施例1-线性范围扩增四种不同片段检测体系的标准曲线,计算标准曲线相关系数(r2)和扩增效率(en)。结果表明,建立的四种不同片段检测体系的线性范围为3ng/rxn~30fg/rxn,标准曲线r2≥0.990,en为83.3%~110.0%,ntc ct值≥35.00,内部质控信号ct值≤32.00。
[0093]
其中体系1-体系4的标准曲线的扩增曲线以及线性关系图如图1~8所示,表3为四种不同片段检测体系的线性范围测试结果表。
[0094]
表3.四种不同片段检测体系的线性范围测试结果
[0095]
实施例2-专属性:评估生产常用的工程细胞/工程菌cho、vero、293t、mdck、ns0、high 5、e.coli、毕赤酵母的基因组dna,以及raav载体生产相关的重组苜蓿尺蠖核多角体病毒(acnpv)质粒dna提取纯化液、重组腺相关病毒2型(raav2)dna提取纯化液、重组腺相关病毒5型(raav5)dna提取纯化液、自身互补型aav2(self-complementary aav,scaav2)dna提取纯化液对sf9不同片段检测体系的干扰。其中,干扰工程细胞/工程菌dna的浓度为3ng/rxn,acnpv质粒dna的浓度为2.12
×
108copies/rxn,raav2/raav5/scaav2 dna提取纯化液的浓度为3ng/rxn。结果表明,所选的两类干扰dna的靶标信号未检出或检测ct值≥35.00,说明其对已建立的四组体系干扰较小,体系表现出较优的专属性。
[0096]
体系1与体系2的专属性测试(干扰工程细胞/工程菌dna)的扩增曲线如图9所示,体系3与体系4的专属性测试(干扰工程细胞/工程菌dna)的扩增曲线如图10所示,表4为四种不同片段检测体系的专属性测试(干扰工程细胞/工程菌dna)结果表。
[0097]
表4专属性测试结果(干扰工程细胞/工程菌dna)
[0098]
体系1与体系2的专属性测试(干扰病毒相关dna)的扩增曲线如图11所示,体系3与体系4的专属性测试(干扰病毒相关dna a)的扩增曲线如图12所示,表5为四种不同片段检测体系的专属性测试(干扰病毒相关dna)结果表。
[0099]
表5.专属性测试结果(干扰病毒dna)
[0100]
实施例3-定量限:扩增四种不同片段检测体系的标准曲线(3ng/rxn~30fg/rxn),同时测定各组在模板量为30fg/rxn的检测ct值(10复孔),将检测ct值代入标准曲线计算得到各孔检测浓度,计算10复孔检测浓度的变异系数(cv)和偏差。结果表明,各体系30fg/rxn检测浓度的cv和偏差均≤30.0%,定量限均为30fg/rxn。
[0101]
体系1~体系4的定量限测试的扩增曲线如图13~16所示,定量限检测结果如表6所示。
[0102]
表6.定量限检测结果
[0103]
综上所述,本发明提供了一种采用实时荧光定量pcr(real-time qpcr)技术定量检测sf9残留dna片段大小分布的引物对、方法和试剂盒,用于分析生物制品中间品、成品中的sf9残留dna片段大小分布,有利于改进工艺、提高产品质量,用于产品质量控制和放行。利用所述引物对的pcr检测方法操作简便快捷,从获得样本到给出检测报告只需4h;灵敏度高,定量限均为30fg/rxn;专属性强,能区分cho细胞、ns0细胞、vero细胞、293t细胞、毕赤酵母、e.coli、high five(high 5)昆虫细胞、苜蓿尺蠖核多角体病毒(acnpv)、重组腺相关病毒(raav)等干扰性dna。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1