3,3-二取代吲哚酮类化合物及其用途的制作方法
3,3-二取代吲哚酮类化合物及其用途
1.相关申请的交叉引用
2.本技术要求于2022年1月11日提交的pct/cn2022/071338的优先权,其全部内容在此通过引用并入本文。
技术领域
3.本发明属于医药领域,涉及3,3-二取代吲哚酮类化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物。本发明还涉及所述化合物的制备方法、包含所述化合物的药物组合物,以及所述化合物在预防和治疗相关癌症,例如乳腺癌、卵巢癌、子宫癌、宫颈癌或子宫内膜癌等中的作用。
背景技术:
4.乳腺癌是乳腺细胞成长失控导致的恶性疾病,在全球各个国家均具有高发病率。虽然随着医药技术的发展,当前乳腺癌的临床诊治已经得到了巨大改善,但根据《中国晚期乳腺癌规范诊疗指南(2020版)》,晚期乳腺癌患者的5年生存率仅有20%,总体中位生存时间仅有2~3年(中华肿瘤杂志,2020;42(10):781
·-797)。根据报道,中国每年约有27.24万乳腺癌新发患者,每年约有7.07万患者死于乳腺癌(ca cancer j clin.2016;66:115
–
132);美国每年约有28.42万乳腺癌新发患者,每年约有4.41万患者死于乳腺癌(ca cancer j clin.2021;71:7
–
33)。
5.根据雌激素受体(estrogen receptor,er)、孕激素受体(progesterone receptor,pr)、人上皮成长因子受体2(human epidermal growth factor receptor 2,her2)的表达背景,乳腺癌又可以分为多种亚型。在各种亚型中,er表达阳性患者在全部乳腺癌患者中占比约为79%(ca cancer j clin.2019;69:438
–
451),雌激素通过作用于er受体,驱动了乳腺癌细胞的增殖和存活。当前,靶向er信号通路的内分泌疗法是治疗er阳性肿瘤的主要治疗手段,包括雌激素竞争药物他莫昔芬、抑制雌激素产生的芳香化酶抑制剂来曲唑、er受体拮抗/降解剂氟维司群等。这些药物虽然展示了良好的治疗效果,但仍然有部分病人对药物不敏感,同时大部分在用药后会出现耐药性(nat rev clin oncol,2015sep;12(9):541-52)(nat rev clin oncol,2019may;16(5):296-311.)(cancer cell.2018sep10;34(3):427-438.e6.)。现有数据显示,耐药性一般在给药后7年内出现(sci transl med.2021jul21;13(603):eabf1383.)(nat rev clin oncol,2019may;16(5):296-311.)(ann oncol.2018aug1;29(8):1634-1657.)。
6.另外,近年也有新型机制的治疗药物例如cdk4/6抑制剂帕博西尼,可以用于er+/her2-乳腺癌患者的治疗(nat rev clin oncol,2016jul;13(7):417-30.),以及pi3kα抑制剂阿培利司,可以用于激素受体阳性/her2-乳腺癌的治疗(nat rev clin oncol,2019aug;16(8):466.)。这两类药单独用药作用较温和,一般需要与内分泌疗法合用,例如帕博西尼与来曲唑联用,而阿培利司一般与氟维司群联用;同时,这两类药获批用于her2-患者,不能用于全部er阳性患者;而且,这两类药物用药后也经常会出现耐药性。总体上,er+乳腺癌患
者仍然急需有效的治疗药物。
7.内分泌疗法耐药患者一般仍为er阳性,其中包括部分er发生突变(例如y537s和d538g)的患者,导致er信号的持续激活(cancer cell.2020apr 13;37(4):496-513.)(nat rev clin oncol,2015oct;12(10):573-83.)。在本技术中,我们使用er+的mcf乳腺癌细胞系(对他莫昔芬、氟维司群、帕博西尼等耐药或仅有部分反应)和er-的mda-mb-231乳腺癌细胞系,对一系列分子进行了检测,并发现了一些对er+细胞选择性杀伤并具有克服耐药潜力的新分子。
技术实现要素:
8.在一个方面,本发明提供了式(i)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物:
[0009][0010]
其中,
[0011]
r1选自c
3-10
环烷基、c
5-12
并环环烷基、5-10元杂芳基或5-10元杂环基;其任选地被1个、2个、3个、4个或5个r#取代;
[0012]
r#独立地选自h、卤素、-oh、-nh2、-cn、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、o-c
1-6
烷基、o-c
1-6
卤代烷基、c
3-7
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-7
环烷基或3-7元杂环基;
[0013]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o或c=s;
[0014]
r3、r4、r5和r6各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、-o-c
1-6
烷基或-o-c
1-6
卤代烷基;
[0015]
r7选自h、卤素、-oh、-cn、-nh2、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、o-c
1-6
烷基或o-c
1-6
卤代烷基。
[0016]
在另一个方面,本发明提供了一种药物组合物,所述药物组合物含有本发明化合物,和任选地药学上可接受的赋形剂,例如载体、佐剂或媒介物。
[0017]
在另一个方面,本发明提供了含有本发明化合物和药学上可接受的赋形剂的药物组合物,其还含有其它治疗剂。
[0018]
在另一个方面,本发明提供了本发明化合物在制备用于治疗和/或预防癌症的药物中的用途,优选地,所述癌症为er阳性癌症。
[0019]
在另一个方面,本发明提供了在受试者中治疗和/或预防癌症的方法,包括向所述受试者给药本发明化合物或本发明药物组合物,优选地,所述癌症为er阳性癌症。
[0020]
在另一个方面,本发明提供了本发明化合物或本发明药物组合物,其用于治疗和/或预防癌症,优选地,所述癌症为er阳性癌症。
[0021]
在具体实施方案中,本发明用于治疗和/或预防癌症。在另一具体实施方案中,本发明用于治疗和/或预防er阳性癌症。在另一具体实施方案中,本发明用于治疗和/或预防乳腺癌、卵巢癌、子宫癌、宫颈癌或子宫内膜癌。
[0022]
定义
[0023]
化学定义
[0024]
下面更详细地描述具体官能团和化学术语的定义。
[0025]
当列出数值范围时,既定包括每个值和在所述范围内的子范围。例如“c
1-6
烷基”包括c1、c2、c3、c4、c5、c6、c
1-6
、c
1-5
、c
1-4
、c
1-3
、c
1-2
、c
2-6
、c
2-5
、c
2-4
、c
2-3
、c
3-6
、c
3-5
、c
3-4
、c
4-6
、c
4-5
和c
5-6
烷基。
[0026]“c
1-6
烷基”是指具有1至6个碳原子的直链或支链饱和烃基团。在一些实施方案中,c
1-4
烷基和c
1-2
烷基是优选的。c
1-6
烷基的例子包括:甲基(c1)、乙基(c2)、正丙基(c3)、异丙基(c3)、正丁基(c4)、叔丁基(c4)、仲丁基(c4)、异丁基(c4)、正戊基(c5)、3-戊基(c5)、戊基(c5)、新戊基(c5)、3-甲基-2-丁基(c5)、叔戊基(c5)和正己基(c6)。术语“c
1-6
烷基”还包括杂烷基,其中一或多个(例如,1、2、3或4个)碳原子被杂原子(例如,氧、硫、氮、硼、硅、磷)替代。烷基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。常规烷基缩写包括:me(-ch3)、et(-ch2ch3)、ipr(-ch(ch3)2)、npr(-ch2ch2ch3)、n-bu(-ch2ch2ch2ch3)或i-bu(-ch2ch(ch3)2)。
[0027]“c
2-6
烯基”是指具有2至6个碳原子和至少一个碳碳双键的直链或支链烃基团。在一些实施方案中,c
2-4
烯基是优选的。c
2-6
烯基的例子包括:乙烯基(c2)、1-丙烯基(c3)、2-丙烯基(c3)、1-丁烯基(c4)、2-丁烯基(c4)、丁二烯基(c4)、戊烯基(c5)、戊二烯基(c5)、己烯基(c6),等等。术语“c
2-6
烯基”还包括杂烯基,其中一或多个(例如,1、2、3或4个)碳原子被杂原子(例如,氧、硫、氮、硼、硅、磷)替代。烯基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。
[0028]“c
2-6
炔基”是指具有2至6个碳原子、至少一个碳-碳叁键以及任选地一个或多个碳-碳双键的直链或支链烃基团。在一些实施方案中,c
2-4
炔基是优选的。c
2-6
炔基的例子包括但不限于:乙炔基(c2)、1-丙炔基(c3)、2-丙炔基(c3)、1-丁炔基(c4)、2-丁炔基(c4),戊炔基(c5)、己炔基(c6),等等。术语“c
2-6
炔基”还包括杂炔基,其中一或多个(例如,1、2、3或4个)碳原子被杂原子(例如,氧、硫、氮、硼、硅、磷)替代。炔基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。
[0029]“c
1-6
亚烷基”是指除去c
1-6
烷基的另一个氢而形成的二价基团,并且可以是取代或未取代的。在一些实施方案中,c
1-4
亚烷基、c
2-4
亚烷基和c
1-3
亚烷基是优选的。未取代的所述亚烷基包括但不限于:亚甲基(-ch
2-)、亚乙基(-ch2ch
2-)、亚丙基(-ch2ch2ch
2-)、亚丁基(-ch2ch2ch2ch
2-)、亚戊基(-ch2ch2ch2ch2ch
2-)、亚己基(-ch2ch2ch2ch2ch2ch
2-),等等。示例性的取代的所述亚烷基,例如,被一个或多个烷基(甲基)取代的所述亚烷基,包括但不限于:取代的亚甲基(-ch(ch3)-、-c(ch3)
2-)、取代的亚乙基(-ch(ch3)ch
2-、-ch2ch(ch3)-、-c(ch3)2ch
2-、-ch2c(ch3)
2-)、取代的亚丙基(-ch(ch3)ch2ch
2-、-ch2ch(ch3)ch
2-、-ch2ch2ch(ch3)-、-c(ch3)2ch2ch
2-、-ch2c(ch3)2ch
2-、-ch2ch2c(ch3)
2-),等等。
[0030]“c
0-6
亚烷基”是指化学键以及上述“c
1-6
亚烷基”。
[0031]“c
2-6
亚烯基”是指除去c
2-6
烯基的另一个氢而形成的二价基团,并且可以是取代或
未取代的。在一些实施方案中,c
2-4
亚烯基是特别优选的。示例性的未取代的所述亚烯基包括但不限于:亚乙烯基(-ch=ch-)和亚丙烯基(例如,-ch=chch
2-、-ch
2-ch=ch-)。示例性的取代的所述亚烯基,例如,被一个或多个烷基(甲基)取代的亚烯基,包括但不限于:取代的亚乙基(-c(ch3)=ch-、-ch=c(ch3)-)、取代的亚丙烯基(-c(ch3)=chch
2-、-ch=c(ch3)ch
2-、-ch=chch(ch3)-、-ch=chc(ch3)
2-、-ch(ch3)-ch=ch-、-c(ch3)
2-ch=ch-、-ch
2-c(ch3)=ch-、-ch
2-ch=c(ch3)-),等等。
[0032]“c
2-6
亚炔基”是指除去c
2-6
炔基的另一个氢而形成的二价基团,并且可以是取代或未取代的。在一些实施方案中,c
2-4
亚炔基是特别优选的。示例性的所述亚炔基包括但不限于:亚乙炔基(-c≡c-)、取代或未取代的亚丙炔基(-c≡cch
2-),等等。
[0033]“卤代”或“卤素”是指氟(f)、氯(cl)、溴(br)和碘(i)。
[0034]
因此,“c
1-6
卤代烷基”是指上述“c
1-6
烷基”,其被一个或多个卤素基团取代。在一些实施方案中,c
1-4
卤代烷基是特别优选的,更优选c
1-2
卤代烷基。示例性的所述卤代烷基包括但不限于:-cf3、-ch2f、-chf2、-chfch2f、-ch2chf2、-cf2cf3、-ccl3、-ch2cl、-chcl2、2,2,2-三氟-1,1-二甲基-乙基,等等。卤代烷基基团可以在任何可用的连接点上被取代,例如,1至5个取代基、1至3个取代基或1个取代基。
[0035]“c
3-10
环烷基”是指具有3至10个环碳原子和零个杂原子的非芳香环烃基团。在一些实施方案中,c
3-7
环烷基和c
3-6
环烷基是特别优选的,更优选c
5-6
环烷基。环烷基还包括其中上述环烷基环与一个或多个芳基或杂芳基稠合的环体系,其中连接点在环烷基环上,且在这样的情况中,碳的数目继续表示环烷基体系中的碳的数目。示例性的所述环烷基包括但不限于:环丙基(c3)、环丙烯基(c3)、环丁基(c4)、环丁烯基(c4)、环戊基(c5)、环戊烯基(c5)、环己基(c6)、环己烯基(c6)、环已二烯基(c6)、环庚基(c7)、环庚烯基(c7)、环庚二烯基(c7)、环庚三烯基(c7),等等。环烷基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。
[0036]“5-10元杂环基”是指具有环碳原子和1至5个环杂原子的5至10元非芳香环系的饱和或不饱和基团,其中,每个杂原子独立地选自氮、氧、硫、硼、磷和硅。“3-7元杂环基”是指具有环碳原子和1至3个环杂原子的3至7元非芳香环系的饱和或不饱和基团,其中,每个杂原子独立地选自氮、氧、硫、硼、磷和硅。在包含一个或多个氮原子的杂环基中,只要化合价允许,连接点可为碳或氮原子。在一些实施方案中,优选3-6元杂环基,其为具有环碳原子和1至3个环杂原子的3至6元非芳香环系;优选5-8元杂环基,其为具有环碳原子和1至3个环杂原子的4至8元非芳香环系;更优选5-6元杂环基,其为具有环碳原子和1至3个环杂原子的5至6元非芳香环系。杂环基还包括其中上述杂环基环与一个或多个环烷基稠合的环体系,其中连接点在环烷基环上,或其中上述杂环基环与一个或多个芳基或杂芳基稠合的环体系,其中连接点在杂环基环上;且在这样的情况下,环成员的数目继续表示在杂环基环体系中环成员的数目。示例性的包含一个杂原子的3元杂环基包括但不限于:氮杂环丙烷基、氧杂环丙烷基、硫杂环丙烷基(thiorenyl)。示例性的含有一个杂原子的4元杂环基包括但不限于:氮杂环丁烷基、氧杂环丁烷基和硫杂环丁烷基。示例性的含有一个杂原子的5元杂环基包括但不限于:四氢呋喃基、二氢呋喃基、四氢噻吩基、二氢噻吩基、吡咯烷基、二氢吡咯基和吡咯基-2,5-二酮。示例性的包含两个杂原子的5元杂环基包括但不限于:二氧杂环戊烷基、氧硫杂环戊烷基(oxasulfuranyl)、二硫杂环戊烷基(disulfuranyl)和噁唑烷-2-酮。示
例性的包含三个杂原子的5元杂环基包括但不限于:三唑啉基、噁二唑啉基和噻二唑啉基。示例性的包含一个杂原子的6元杂环基包括但不限于:哌啶基、四氢吡喃基、二氢吡啶基和硫杂环己烷基(thianyl)。示例性的包含两个杂原子的6元杂环基包括但不限于:哌嗪基、吗啉基、二硫杂环己烷基、二噁烷基。示例性的包含三个杂原子的6元杂环基包括但不限于:六氢三嗪基(triazinanyl)。示例性的含有一个杂原子的7元杂环基包括但不限于:氮杂环庚烷基、氧杂环庚烷基和硫杂环庚烷基。示例性的与c6芳基环稠合的5元杂环基(在本文中也称作5,6-双环杂环基)包括但不限于:二氢吲哚基、异二氢吲哚基、二氢苯并呋喃基、二氢苯并噻吩基、苯并噁唑啉酮基,等等。示例性的与c6芳基环稠合的6元杂环基(本文还指的是6,6-双环杂环基)包括但不限于:四氢喹啉基、四氢异喹啉基,等等。杂环基还包括上述杂环基与一个环烷基、杂环基、芳基或杂芳基共享一个或两个原子,形成桥环或螺环,只要化合价允许,共享的原子可为碳或氮原子。杂环基还包括上述杂环基与杂环基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。
[0037]“c
6-10
芳基”是指具有6-10个环碳原子和零个杂原子的单环或多环的(例如,双环)4n+2芳族环体系(例如,具有以环状排列共享的6或10个π电子)的基团。在一些实施方案中,芳基具有六个环碳原子(“c6芳基”;例如,苯基)。在一些实施方案中,芳基具有十个环碳原子(“c
10
芳基”;例如,萘基,例如,1-萘基和2-萘基)。芳基还包括其中上述芳基环与一个或多个环烷基或杂环基稠合的环系统,而且连接点在所述芳基环上,在这种情况下,碳原子的数目继续表示所述芳基环系统中的碳原子数目。芳基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代基或1个取代基取代。
[0038]“5-10元杂芳基”是指具有环碳原子和1-4个环杂原子的5-10元单环或双环的4n+2芳族环体系(例如,具有以环状排列共享的6或10个π电子)的基团,其中每个杂原子独立地选自氮、氧和硫。在含有一个或多个氮原子的杂芳基中,只要化合价允许,连接点可以是碳或氮原子。杂芳基双环系统在一个或两个环中可以包括一个或多个杂原子。杂芳基还包括其中上述杂芳基环与一个或多个环烷基或杂环基稠合的环系统,而且连接点在所述杂芳基环上,在这种情况下,碳原子的数目继续表示所述杂芳基环系统中的碳原子数目。在一些实施方案中,5-6元杂芳基是优选的,其为具有环碳原子和1-4个环杂原子的5-6元单环或双环的4n+2芳族环体系。示例性的含有一个杂原子的5元杂芳基包括但不限于:吡咯基、呋喃基和噻吩基。示例性的含有两个杂原子的5元杂芳基包括但不限于:咪唑基、吡唑基、噁唑基、异噁唑基、噻唑基和异噻唑基。示例性的含有三个杂原子的5元杂芳基包括但不限于:三唑基、噁二唑基(例如,1,2,4-噁二唑基)和噻二唑基。示例性的含有四个杂原子的5元杂芳基包括但不限于:四唑基。示例性的含有一个杂原子的6元杂芳基包括但不限于:吡啶基。示例性的含有两个杂原子的6元杂芳基包括但不限于:哒嗪基、嘧啶基和吡嗪基。示例性的含有三个或四个杂原子的6元杂芳基分别包括但不限于:三嗪基和四嗪基。示例性的含有一个杂原子的7元杂芳基包括但不限于:氮杂环庚三烯基、氧杂环庚三烯基和硫杂环庚三烯基。示例性的5,6-双环杂芳基包括但不限于:吲哚基、异吲哚基、吲唑基、苯并三唑基、苯并噻吩基、异苯并噻吩基、苯并呋喃基、苯并异呋喃基、苯并咪唑基、苯并噁唑基、苯并异噁唑基、苯并噁二唑基、苯并噻唑基、苯并异噻唑基、苯并噻二唑基、茚嗪基和嘌呤基。示例性的6,6-双环杂芳基包括但不限于:萘啶基、喋啶基、喹啉基、异喹啉基、噌琳基、喹喔啉基、酞嗪基和喹唑啉基。杂芳基基团可以被一或多个取代基任选取代,例如,被1至5个取代基、1至3个取代
基或1个取代基取代。
[0039]“c
5-12
并环环烷基”是指由两个或两个以上环状结构彼此共用两个相邻的碳原子所形成的5-12元环状基团,包括5-12元饱和并环环烷基和5-12元部分饱和并环环烷基。优选5-10元并环环烷基。5-12元饱和并环环烷基,是指该并环基为全部饱和的碳环,具体实例包括但不限于:二环[3.1.0]己烷基、二环[4.1.0]庚烷基、二环[2.2.0]己烷基、二环[3.2.0]庚烷基、二环[4.2.0]辛烷基、八氢并环戊二烯基、八氢-1h-茚基、十氢化萘基等。5-12元部分饱和并环环烷基,是指该并环中至少一个环为部分饱和的碳环,具体实例包括但不限于:双环[3.1.0]己-2-烯基、双环[4.1.0]庚-3-烯基、双环[3.2.0]庚-3-烯基、双环[4.2.0]辛-3-烯基、1,2,3,3a-四氢并环戊二烯基、2,3,3a,4,7,7a-六氢-1h-茚基、1,2,3,4,4a,5,6,8a-八氢化萘基、1,2,4a,5,6,8a-六氢化萘基等。
[0040]
上文定义的烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基等基团除去另一个氢而形成的二价基团统称为“亚基”。环烷基、杂环基、芳基和杂芳基等成环的基团统称为“环基”。
[0041]
本文定义的烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基等为任选取代的基团。
[0042]
示例性的碳原子上的取代基包括但不局限于:卤素、-cn、-no2、-n3、-so2h、-so3h、-oh、-or
aa
、-on(r
bb
)2、-n(r
bb
)2、-n(r
bb
)
3+
x-、-n(or
cc
)r
bb
、-sh、-sr
aa
、-ssr
cc
、-c(=o)r
aa
、-co2h、-cho、-c(or
cc
)2、-co2r
aa
、-oc(=o)r
aa
、-oco2r
aa
、-c(=o)n(r
bb
)2、-oc(=o)n(r
bb
)2、-nr
bb
c(=o)r
aa
、-nr
bb
co2r
aa
、-nr
bb
c(=o)n(r
bb
)2、-c(=nr
bb
)r
aa
、-c(=nr
bb
)or
aa
、-oc(=nr
bb
)r
aa
、-oc(=nr
bb
)or
aa
、-c(=nr
bb
)n(r
bb
)2、-oc(=nr
bb
)n(r
bb
)2、-nr
bb
c(=nr
bb
)n(r
bb
)2、-c(=o)nr
bb
so2r
aa
、-nr
bb
so2r
aa
、-so2n(r
bb
)2、-so2r
aa
、-so2or
aa
、-oso2r
aa
、-s(=o)r
aa
、-os(=o)r
aa
、-si(r
aa
)3、-osi(r
aa
)3、-c(=s)n(r
bb
)2、-c(=o)sr
aa
、-c(=s)sr
aa
、-sc(=s)sr
aa
、-sc(=o)sr
aa
、-oc(=o)sr
aa
、-sc(=o)or
aa
、-sc(=o)r
aa
、-p(=o)2r
aa
、-op(=o)2r
aa
、-p(=o)(r
aa
)2、-op(=o)(r
aa
)2、-op(=o)(or
cc
)2、-p(=o)2n(r
bb
)2、-op(=o)2n(r
bb
)2、-p(=o)(nr
bb
)2、-op(=o)(nr
bb
)2、-nr
bb
p(=o)(or
cc
)2、-nr
bb
p(=o)(nr
bb
)2、-p(r
cc
)2、-p(r
cc
)3、-op(r
cc
)2、-op(r
cc
)3、-b(r
aa
)2、-b(or
cc
)2、-br
aa
(or
cc
)、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
dd
基团取代;
[0043]
或者在碳原子上的两个偕氢被基团=o、=s、=nn(r
bb
)2、=nnr
bb
c(=o)r
aa
、=nnr
bb
c(=o)or
aa
、=nnr
bb
s(=o)2r
aa
、=nr
bb
或=nor
cc
取代;
[0044]raa
的每个独立地选自烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,或者两个r
aa
基团结合以形成杂环基或杂芳基环,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
dd
基团取代;
[0045]rbb
的每个独立地选自:氢、-oh、-or
aa
、-n(r
cc
)2、-cn、-c(=o)r
aa
、-c(=o)n(r
cc
)2、-co2r
aa
、-so2r
aa
、-c(=nr
cc
)or
aa
、-c(=nr
cc
)n(r
cc
)2、-so2n(r
cc
)2、-so2r
cc
、-so2or
cc
、-sor
aa
、-c(=s)n(r
cc
)2、-c(=o)sr
cc
、-c(=s)sr
cc
、-p(=o)2r
aa
、-p(=o)(r
aa
)2、-p(=o)2n(r
cc
)2、-p(=o)(nr
cc
)2、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,或者两个r
bb
基团结合以形成杂环基或杂芳基环,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
dd
基团取代;
[0046]rcc
的每个独立地选自氢、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,或者两个r
cc
基团结合以形成杂环基或杂芳基环,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
dd
基团取代;
[0047]rdd
的每个独立地选自:卤素、-cn、-no2、-n3、-so2h、-so3h、-oh、-or
ee
、-on(r
ff
)2、-n(r
ff
)2,、-n(r
ff
)
3+
x-、-n(or
ee
)r
ff
、-sh、-sr
ee
、-ssr
ee
、-c(=o)r
ee
、-co2h、-co2r
ee
、-oc(=o)r
ee
、-oco2r
ee
、-c(=o)n(r
ff
)2、-oc(=o)n(r
ff
)2、-nr
ff
c(=o)r
ee
、-nr
ff
co2r
ee
、-nr
ff
c(=o)n(r
ff
)2、-c(=nr
ff
)or
ee
、-oc(=nr
ff
)r
ee
、-oc(=nr
ff
)or
ee
、-c(=nr
ff
)n(r
ff
)2、-oc(=nr
ff
)n(r
ff
)2、-nr
ff
c(=nr
ff
)n(r
ff
)2、-nr
ff
so2r
ee
、-so2n(r
ff
)2、-so2r
ee
、-so2or
ee
、-oso2r
ee
、-s(=o)r
ee
、-si(r
ee
)3、-osi(r
ee
)3、-c(=s)n(r
ff
)2、-c(=o)sr
ee
、-c(=s)sr
ee
、-sc(=s)sr
ee
、-p(=o)2r
ee
、-p(=o)(r
ee
)2、-op(=o)(r
ee
)2、-op(=o)(or
ee
)2、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基、杂芳基,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
gg
基团取代,或者两个偕r
dd
取代基可结合以形成=o或=s;
[0048]ree
的每个独立地选自烷基、卤代烷基、烯基、炔基、环烷基、芳基、杂环基和杂芳基,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
gg
基团取代;
[0049]rff
的每个独立地选自氢、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,或者两个r
ff
基团结合形成杂环基或杂芳基环,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
gg
基团取代;
[0050]rgg
的每个独立地是:卤素、-cn、-no2、-n3、-so2h、-so3h、-oh、-oc
1-6
烷基、-on(c
1-6
烷基)2、-n(c
1-6
烷基)2、-n(c
1-6
烷基)
3+
x-、-nh(c
1-6
烷基)
2+
x-、-nh2(c
1-6
烷基)
+
x-、-nh
3+
x-、-n(oc
1-6
烷基)(c
1-6
烷基)、-n(oh)(c
1-6
烷基)、-nh(oh)、-sh、-sc
1-6
烷基、-ss(c
1-6
烷基)、-c(=o)(c
1-6
烷基)、-co2h、-co2(c
1-6
烷基)、-oc(=o)(c
1-6
烷基)、-oco2(c
1-6
烷基)、-c(=o)nh2、-c(=o)n(c
1-6
烷基)2、-oc(=o)nh(c
1-6
烷基)、-nhc(=o)(c
1-6
烷基)、-n(c
1-6
烷基)c(=o)(c
1-6
烷基)、-nhco2(c
1-6
烷基)、-nhc(=o)n(c
1-6
烷基)2、-nhc(=o)nh(c
1-6
烷基)、-nhc(=o)nh2、-c(=nh)o(c
1-6
烷基)、-oc(=nh)(c
1-6
烷基)、-oc(=nh)oc
1-6
烷基、-c(=nh)n(c
1-6
烷基)2、-c(=nh)nh(c
1-6
烷基)、-c(=nh)nh2、-oc(=nh)n(c
1-6
烷基)2、-oc(nh)nh(c
1-6
烷基)、-oc(nh)nh2、-nhc(nh)n(c
1-6
烷基)2、-nhc(=nh)nh2、-nhso2(c
1-6
烷基)、-so2n(c
1-6
烷基)2、-so2nh(c
1-6
烷基)、-so2nh2、-so2c
1-6
烷基、-so2oc
1-6
烷基、-oso2c
1-6
烷基、-soc
1-6
烷基、-si(c
1-6
烷基)3、-osi(c
1-6
烷基)3、-c(=s)n(c
1-6
烷基)2、c(=s)nh(c
1-6
烷基)、c(=s)nh2、-c(=o)s(c
1-6
烷基)、-c(=s)sc
1-6
烷基、-sc(=s)sc
1-6
烷基、-p(=o)2(c
1-6
烷基)、-p(=o)(c
1-6
烷基)2、-op(=o)(c
1-6
烷基)2、-op(=o)(oc
1-6
烷基)2、c
1-6
烷基、c
1-6
卤代烷基、c
2-c6烯基、c
2-c6炔基、c
3-c7环烷基、c
6-c
10
芳基、c
3-c7杂环基、c
5-c
10
杂芳基;或者两个偕r
gg
取代基可结合形成=o或=s;其中,x-为反离子。
[0051]
示例性的氮原子上取代基包括但不局限于:氢、-oh、-or
aa
、-n(r
cc
)2、-cn、-c(=o)r
aa
、-c(=o)n(r
cc
)2、-co2r
aa
、-so2r
aa
、-c(=nr
bb
)r
aa
、-c(=nr
cc
)or
aa
、-c(=nr
cc
)n(r
cc
)2、-so2n(r
cc
)2、-so2r
cc
、-so2or
cc
、-sor
aa
、-c(=s)n(r
cc
)2、-c(=o)sr
cc
、-c(=s)sr
cc
、-p(=o)2r
aa
、-p(=o)(r
aa
)2、-p(=o)2n(r
cc
)2、-p(=o)(nr
cc
)2、烷基、卤代烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基,或者连接至氮原子的两个r
cc
基团结合形成杂环基或杂芳基环,其中,每个烷基、烯基、炔基、环烷基、杂环基、芳基和杂芳基独立地被0、1、2、3、4或5个r
dd
基团
取代,且其中r
aa
、r
bb
、r
cc
和r
dd
如上所述。
[0052]
其它定义
[0053]
术语“癌症”包括但不限于下列癌症:乳腺癌、卵巢癌、子宫癌、宫颈癌或子宫内膜癌。
[0054]
本文所用的术语“治疗”涉及逆转、减轻、抑制该术语适用的障碍或病症的进展或者预防之,或者这类障碍或病症的一种或多种症状。本文所用的名词“治疗”涉及动词治疗的动作,后者是如刚才所定义的。
[0055]
本文所用的术语“药学上可接受的盐”表示本发明化合物的那些羧酸盐、氨基酸加成盐,它们在可靠的医学判断范围内适用于与患者组织接触,不会产生不恰当的毒性、刺激作用、变态反应等,与合理的益处/风险比相称,就它们的预期应用而言是有效的,包括(可能的话)本发明化合物的两性离子形式。
[0056]
药学上可接受的碱加成盐是与金属或胺生成的,例如碱金属与碱土金属氢氧化物或有机胺。用作阳离子的金属的实例有钠、钾、镁、钙等。适合的胺的实例有n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、n-甲基葡糖胺和普鲁卡因。
[0057]
酸性化合物的碱加成盐可以这样制备,按照常规方式使游离酸形式与足量所需的碱接触,生成盐。按照常规方式使盐形式与酸接触,再分离游离酸,可以使游离酸再生。游离酸形式在某些物理性质上多少不同于它们各自的盐形式,例如在极性溶剂中的溶解度,但是出于本发明的目的,盐还是等价于它们各自的游离酸。
[0058]
盐可以是从无机酸制备的硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、硝酸盐、磷酸盐、磷酸一氢盐、磷酸二氢盐、偏磷酸盐、焦磷酸盐、氯化物、溴化物、碘化物,酸例如盐酸、硝酸、硫酸、氢溴酸、氢碘酸、磷酸等。代表性盐包括:氢溴酸盐、盐酸盐、硫酸盐、硫酸氢盐、硝酸盐、乙酸盐、草酸盐、戊酸盐、油酸盐、棕榈酸盐、硬脂酸盐、月桂酸盐、硼酸盐、苯甲酸盐、乳酸盐、磷酸盐、甲苯磺酸盐、柠檬酸盐、马来酸盐、富马酸盐、琥珀酸盐、酒石酸盐、萘甲酸盐、甲磺酸盐、葡庚糖酸盐、乳糖酸盐、月桂基磺酸盐和羟乙磺酸盐等。盐也可以是从有机酸制备的,例如脂肪族一元与二元羧酸、苯基取代的烷酸、羟基烷酸、烷二酸、芳香族酸、脂肪族与芳香族磺酸等。代表性盐包括乙酸盐、丙酸盐、辛酸盐、异丁酸盐、草酸盐、丙二酸盐、琥珀酸盐、辛二酸盐、癸二酸盐、富马酸盐、马来酸盐、扁桃酸盐、苯甲酸盐、氯苯甲酸盆、甲基苯甲酸盐、二硝基苯甲酸盐、萘甲酸盐、苯磺酸盐、甲苯磺酸盐、苯乙酸盐、柠檬酸盐、乳酸盐、马来酸盐、酒石酸盐、甲磺酸盐等。药学上可接受的盐可以包括基于碱金属与碱土金属的阳离子,例如钠、锂、钾、钙、镁等,以及无毒的铵、季铵和胺阳离子,包括但不限于铵、四甲基铵、四乙基铵、甲胺、二甲胺、三甲胺、三乙胺、乙胺等。还涵盖氨基酸的盐,例如精氨酸盐、葡糖酸盐、半乳糖醛酸盐等(例如参见berge s.m.et al.,"pharmaceutical salts,”j.pharm.sci.,1977;66:1-19,引入此作为参考)。
[0059]
给药的“受试者”包括但不限于:人(即,任何年龄组的男性或女性,例如,儿科受试者(例如,婴儿、儿童、青少年)或成人受试者(例如,年轻的成人、中年的成人或年长的成人))和/或非人的动物,例如,哺乳动物,例如,灵长类(例如,食蟹猴、恒河猴)、牛、猪、马、绵羊、山羊、啮齿动物、猫和/或狗。在一些实施方案中,受试者是人。在一些实施方案中,受试者是非人动物。本文可互换使用术语“人”、“患者”和“受试者”。
[0060]“疾病”、“障碍”和“病症”在本文中可互换地使用。
[0061]
除非另作说明,否则,本文使用的术语“治疗”包括受试者患有具体疾病、障碍或病症时所发生的作用,它降低疾病、障碍或病症的严重程度,或延迟或减缓疾病、障碍或病症的发展(“治疗性治疗”),还包括在受试者开始患有具体疾病、障碍或病症之前发生的作用(“预防性治疗”)。
[0062]
通常,化合物的“有效量”是指足以引起目标生物反应的数量。正如本领域普通技术人员所理解的那样,本发明化合物的有效量可以根据下列因素而改变:例如,生物学目标、化合物的药代动力学、所治疗的疾病、给药模式以及受试者的年龄健康情况和症状。有效量包括治疗有效量和预防有效量。
[0063]
除非另作说明,否则,本文使用的化合物的“治疗有效量”是在治疗疾病、障碍或病症的过程中足以提供治疗益处的量,或使与疾病、障碍或病症有关的一或多种症状延迟或最小化的量。化合物的治疗有效量是指单独使用或与其它疗法联用时,治疗剂的量,它在治疗疾病、障碍或病症的过程中提供治疗益处。术语“治疗有效量”可以包括改善总体治疗、降低或避免疾病或病症的症状或病因、或增强其它治疗剂的治疗效果的量。
[0064]
除非另作说明,否则,本文使用的化合物的“预防有效量”是足以预防疾病、障碍或病症的量,或足以预防与疾病、障碍或病症有关的一或多种症状的量,或防止疾病、障碍或病症复发的量。化合物的预防有效量是指单独使用或与其它药剂联用时,治疗剂的量,它在预防疾病、障碍或病症的过程中提供预防益处。术语“预防有效量”可以包括改善总体预防的量,或增强其它预防药剂的预防效果的量。
[0065]“组合”以及相关术语是指同时或依次给药本发明化合物和其它治疗剂。例如,本发明化合物可以与其它治疗剂以分开的单位剂型同时或依次给药,或与其它治疗剂一起在单一单位剂型中同时给药。
[0066]
由随后的具体实施方案、实施例和权利要求,本发明的其它目的和优点将对于本领域技术人员显而易见。
具体实施方案
[0067]
本文中,“本发明化合物”指的是以下的式(i)化合物(包括子通式,例如式(i-1)、式(i-2)、式(ii)、式(ii-1)、式(ii-2)、式(iii)、式(iii-1)及式(iii-2)等)、或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,以及它们的混合物。
[0068]
在一个实施方案中,本发明涉及式(i)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物:
[0069][0070]
其中,
[0071]
r1选自c
3-10
环烷基、c
5-12
并环环烷基、5-10元杂芳基或5-10元杂环基;其任选地被1个、2个、3个、4个或5个r#取代;
[0072]
r#独立地选自h、卤素、-oh、-nh2、-cn、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、o-c
1-6
烷基、o-c
1-6
卤代烷基、c
3-7
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-7
环烷基或3-7元杂环基;
[0073]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o或c=s;
[0074]
r3、r4、r5和r6各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、-o-c
1-6
烷基或-o-c
1-6
卤代烷基;
[0075]
r7选自h、卤素、-oh、-cn、-nh2、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、o-c
1-6
烷基或o-c
1-6
卤代烷基。
[0076]
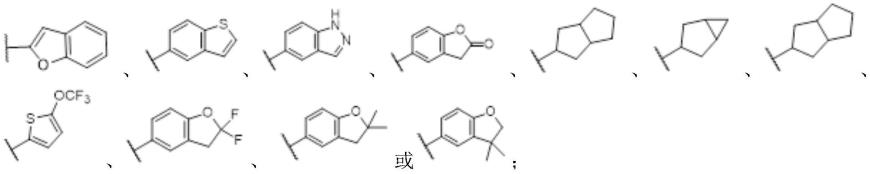
r1[0077]
在一个具体实施方式中,r1为c
3-10
环烷基;在另一个具体实施方式中,r1为c
5-12
并环环烷基;在另一个具体实施方式中,r1为5-10元杂芳基;在另一个具体实施方式中,r1为5-10元杂环基;在另一个具体实施方式中,r1为c
5-10
并环环烷基;在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为c
5-10
环烷基;在另一个具体实施方式中,r1为c
3-7
环烷基;在另一个具体实施方式中,r1为c
5-6
环烷基。
[0078]
在一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为在另一个具体实施方式中,r1为
[0090]
在一个具体实施方式中,r6为h;在另一个具体实施方式中,r6为卤素;在另一个具体实施方式中,r6为c
1-6
烷基;在另一个具体实施方式中,r6为c
1-4
烷基;在另一个具体实施方式中,r6为c
1-2
烷基;在另一个具体实施方式中,r6为c
2-6
烯基;在另一个具体实施方式中,r6为c
2-6
炔基;在另一个具体实施方式中,r6为c
1-6
卤代烷基;在另一个具体实施方式中,r6为-o-c
1-6
烷基;在另一个具体实施方式中,r6为-o-c
1-4
烷基;在另一个具体实施方式中,r6为-o-c
1-2
烷基;在另一个具体实施方式中,r6为-o-c
1-6
卤代烷基;在另一个具体实施方式中,r6为-o-c
1-4
卤代烷基;在另一个具体实施方式中,r6为-o-c
1-2
卤代烷基。
[0091]
r7[0092]
在一个具体实施方式中,r7为h;在另一个具体实施方式中,r7为卤素;在另一个具体实施方式中,r7为-oh;在另一个具体实施方式中,r7为-cn;在另一个具体实施方式中,r7为-nh2;在另一个具体实施方式中,r7为c
1-6
烷基;在另一个具体实施方式中,r7为c
1-4
烷基;在另一个具体实施方式中,r7为c
1-2
烷基;在另一个具体实施方式中,r7为c
2-6
烯基;在另一个具体实施方式中,r7为c
2-6
炔基;在另一个具体实施方式中,r7为c
1-6
卤代烷基;在另一个具体实施方式中,r7为-o-c
1-6
烷基;在另一个具体实施方式中,r7为-o-c
1-4
烷基;在另一个具体实施方式中,r7为-o-c
1-2
烷基;在另一个具体实施方式中,r7为-o-c
1-6
卤代烷基;在另一个具体实施方式中,r7为-o-c
1-4
卤代烷基;在另一个具体实施方式中,r7为-o-c
1-2
卤代烷基。
[0093]rs
[0094]
在一个具体实施方式中,rs为h;在另一个具体实施方式中,rs为c
1-4
烷基;在另一个具体实施方式中,rs为c
1-2
烷基;在另一个具体实施方式中,rs为c
1-4
卤代烷基;在另一个具体实施方式中,rs为c
1-2
卤代烷基;在另一个具体实施方式中,rs为o-c
1-4
烷基;在另一个具体实施方式中,rs为o-c
1-2
烷基;在另一个具体实施方式中,rs为o-c
1-4
卤代烷基;在另一个具体实施方式中,rs为o-c
1-2
卤代烷基。
[0095]
环a
[0096]
在一个具体实施方式中,环a为3-7元杂环基;在另一个具体实施方式中,环a为5-10元杂芳基;在另一个具体实施方式中,环a为5-6元杂环基;在另一个具体实施方式中,环a为5-6元杂芳基;
[0097]
在一个具体实施方式中,环a任选地被1个r#取代;在另一个具体实施方式中,环a任选地被2个r#取代;在另一个具体实施方式中,环a任选地被3个r#取代。
[0098]
环b
[0099]
在一个具体实施方式中,环b为c
6-10
芳基;在另一个具体实施方式中,环b为c
5-10
杂芳基。
[0100]
在一个具体实施方式中,环b任选地被1个r#取代;在另一个具体实施方式中,环b任选地被2个r#取代;在另一个具体实施方式中,环b任选地被3个r#取代。
[0101]
环c
[0102]
在一个具体实施方式中,环c为c
6-10
芳基;在另一个具体实施方式中,环c为c
5-10
杂芳基。
[0103]
在一个具体实施方式中,环c任选地被1个r#取代;在另一个具体实施方式中,环c任选地被2个r#取代;在另一个具体实施方式中,环c任选地被3个r#取代。
[0104]
r#
[0105]
在一个具体实施方式中,r#为h;在另一个具体实施方式中,r#为卤素;在另一个具体实施方式中,r#为-oh;在另一个具体实施方式中,r#为-nh2;在另一个具体实施方式中,r#为-cn;在另一个具体实施方式中,r#为c
1-6
烷基;在另一个具体实施方式中,r#为c
1-4
烷基;在另一个具体实施方式中,r#为c
1-2
烷基;在另一个具体实施方式中,r#为c
2-6
烯基;在另一个具体实施方式中,r#为c
2-6
炔基;在另一个具体实施方式中,r#为c
1-6
卤代烷基;在另一个具体实施方式中,r#为c
1-4
卤代烷基;在另一个具体实施方式中,r#为c
1-2
卤代烷基;在另一个具体实施方式中,r#为o-c
1-6
烷基;在另一个具体实施方式中,r#为o-c
1-6
卤代烷基;在另一个具体实施方式中,r#为c
3-7
环烷基;在另一个具体实施方式中,r#为c
3-5
环烷基;在另一个具体实施方式中,r#为3-7元杂环基;在另一个具体实施方式中,r#为5-6元杂环基。
[0106]
在一个具体实施方式中,同一碳原子上的两个r#一起形成c=o;在另一个具体实施方式中,同一碳原子上的两个r#一起形成c=s;在另一个具体实施方式中,同一碳原子上的两个r#一起形成c
3-7
环烷基;在另一个具体实施方式中,同一碳原子上的两个r#一起形成c
3-5
环烷基;在另一个具体实施方式中,同一碳原子上的两个r#一起形成3-7元杂环基;在另一个具体实施方式中,同一碳原子上的两个r#一起形成5-6元杂环基。
[0107]
在一个具体实施方式中,r#为f;在另一个具体实施方式中,r#为-ch3;在另一个具体实施方式中,r#为环丙烷;在另一个具体实施方式中,r#为-ocf3。
[0108]
以上任一具体实施方案中的任一技术方案或其任意组合,可以与其它具体实施方案中的任一技术方案或其任意组合进行组合。例如,r1的任一技术方案或其任意组合,可以与r2、r3、r4、r5、r6、r7、rs、环a、环b、环c和r#等的任一技术方案或其任意组合进行组合。本发明旨在包括所有这些技术方案的组合,限于篇幅,不再一一列出。
[0109]
在更具体的实施方案中,本发明提供了式(i-1)或(i-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物:
[0110][0111]
其中,
[0112]
r1选自c
3-10
环烷基、c
5-12
并环环烷基或5-10元杂芳基;其任选地被1个、2个或3个r#取代;
[0113]
r#选自h、卤素、-oh、-nh2、-cn、c
1-6
烷基、c
1-6
卤代烷基、o-c
1-6
烷基、o-c
1-6
卤代烷基、c
3-7
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-7
环烷基或3-7元杂环基;
[0114]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o或c=s;
[0115]
r3选自h、卤素、c
1-6
烷基或c
1-6
卤代烷基;
[0116]
r4选自h、卤素、-o-c
1-6
烷基或-o-c
1-6
卤代烷基;
[0117]
r5为h或卤素;
[0118]
r6为h或卤素;
[0119]
r7为-oh、-cn或-nh2。
[0120]
在更具体的实施方案中,本发明提供了上述式(i-1)或(i-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0121]
r1选自c
3-10
环烷基、c
5-10
并环环烷基、
[0122]rs
选自h、c
1-4
烷基、c
1-4
卤代烷基、o-c
1-4
烷基或o-c
1-4
卤代烷基;
[0123]
环a选自3-7元杂环基或5-10元杂芳基;
[0124]
环b为c
6-10
芳基或c
5-10
杂芳基;
[0125]
环c为c
6-10
芳基或c
5-10
杂芳基;
[0126]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0127]
r#选自h、卤素、c
1-4
烷基、c
1-4
卤代烷基、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0128]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o;
[0129]
r3选自c
1-2
烷基或c
1-2
卤代烷基;
[0130]
r4选自h或-o-c
1-2
烷基;
[0131]
r5为h;
[0132]
r6为h;
[0133]
r7为-oh。
[0134]
在更具体的实施方案中,本发明提供了上述式(i-1)或(i-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0135]
r1选自选自
[0136]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o;
[0137]
r3选自-cf3或-ch3;
[0138]
r4选自h或-och3;
[0139]
r5为h;
[0140]
r6为h;
[0141]
r7为-oh。
[0142]
在更具体的实施方案中,本发明提供了(ii)、(ii-1)或(ii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物:
[0143][0144]
其中,
[0145]
r1选自c
3-10
环烷基、c
5-10
并环环烷基或5-10元杂芳基;其任选地被1个、2个或3个r#取代;
[0146]
r#选自h、卤素、-oh、-nh2、-cn、c
1-6
烷基、c
1-6
卤代烷基、o-c
1-6
烷基、o-c
1-6
卤代烷基、c
3-7
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-7
环烷基或3-7元杂环基;
[0147]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o或c=s;
[0148]
r3选自c
1-6
烷基或c
1-6
卤代烷基;
[0149]
r4选自h、c
1-6
烷基、c
1-6
卤代烷基、-o-c
1-6
烷基或-o-c
1-6
卤代烷基。
[0150]
在更具体的实施方案中,本发明提供了上述(ii)、(ii-1)或(ii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0151]
r1选自c
3-10
环烷基、c
5-10
并环环烷基、
[0152]rs
选自h、c
1-4
烷基、c
1-4
卤代烷基、o-c
1-4
烷基或o-c
1-4
卤代烷基;
[0153]
环a选自3-7元杂环基或5-10元杂芳基;
[0154]
环b为c
6-10
芳基或c
5-10
杂芳基;
[0155]
环c为c
6-10
芳基或c
5-10
杂芳基;
[0156]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0157]
r#选自h、卤素、c
1-4
烷基、c
1-4
卤代烷基、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0158]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o;
[0159]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0160]
r4选自h、-o-c
1-4
烷基或-o-c
1-4
卤代烷基。
[0161]
在更具体的实施方案中,本发明提供了上述(ii)、(ii-1)或(ii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0162]
r1选自c
5-10
环烷基、c
5-10
并环环烷基、
[0163]rs
选自h、c
1-2
烷基或o-c
1-2
卤代烷基;
[0164]
环a选自5-6元杂环基或5-6元杂芳基;
[0165]
环b为c
6-10
芳基;
[0166]
环c为c
6-10
芳基;
[0167]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0168]
r#选自h、卤素、c
1-2
烷基或c
3-5
环烷基;或者同一碳原子上的两个r#一起形成c=o或c
3-5
环烷基;
[0169]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o;
[0170]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0171]
r4选自h或-o-c
1-2
烷基。
[0172]
在更具体的实施方案中,本发明提供了上述(ii)、(ii-1)或(ii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0173]
r1选自选自
[0174]
r2为h,或者与所连接的碳原子以及偕氢一起形成c=o;
[0175]
r3选自-cf3或-ch3;
[0176]
r4选自h或-och3。
[0177]
在更具体的实施方案中,本发明提供了式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物:
[0178][0179]
其中,
[0180]
r1选自c
3-10
环烷基或5-10元杂芳基;其中所述5-10元杂芳基可任选地被1个、2个或3个r#取代;
[0181]
r#选自h、卤素、-oh、-nh2、-cn、o-c
1-4
烷基、o-c
1-4
卤代烷基、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0182]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0183]
r4选自h、-o-c
1-4
烷基或-o-c
1-4
卤代烷基。
[0184]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶
剂合物,其中,
[0185]
r1选自c
3-10
环烷基、c
5-10
并环环烷基、
[0186]rs
选自h、c
1-4
烷基、c
1-4
卤代烷基、o-c
1-4
烷基或o-c
1-4
卤代烷基;
[0187]
环a选自3-7元杂环基或5-10元杂芳基;
[0188]
环b为c
6-10
芳基;
[0189]
环c为c
6-10
芳基;
[0190]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0191]
r#选自h、卤素、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0192]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0193]
r4选自h、-o-c
1-2
烷基或-o-c
1-2
卤代烷基。
[0194]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0195]
r1选自c
5-10
环烷基、c
5-10
并环环烷基、
[0196]rs
选自h、c
1-2
烷基或o-c
1-2
卤代烷基;
[0197]
环a选自5-6元杂环基或5-6元杂芳基;
[0198]
环b为c
6-10
芳基;
[0199]
环c为c
6-10
芳基;
[0200]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0201]
r#选自h、卤素或c
3-5
环烷基;或者同一碳原子上的两个r#一起形成c=o或c
3-5
环烷基;
[0202]
r3选自c
1-2
烷基或c
1-2
卤代烷基;
[0203]
r4选自h或-o-c
1-2
烷基。
[0204]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0205]
r1选自选自
[0206]
r3选自-cf3或-ch3;
[0207]
r4选自h或-och3。
[0208]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0209]
r1选自c
3-10
环烷基或5-10元杂芳基;其中所述5-10元杂芳基可任选地被1个、2个或3个r#取代;
[0210]
r#选自h、卤素、-oh、-nh2、-cn、o-c
1-4
烷基、o-c
1-4
卤代烷基、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0211]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0212]
r4选自h或-o-c
1-4
烷基。
[0213]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0214]
r1选自c
3-10
环烷基、优选c
3-10
环烷基、环烷基、
[0215]rs
选自h、c
1-4
烷基、c
1-4
卤代烷基、o-c
1-4
烷基或o-c
1-4
卤代烷基;
[0216]
环a选自3-7元杂环基(优选含氧原子的3-7元杂环基)或5-10元杂芳基;
[0217]
环b为c
6-10
芳基;
[0218]
环c为c
6-10
芳基;
[0219]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0220]
r#选自h、卤素、c
3-5
环烷基或3-7元杂环基;或者同一碳原子上的两个r#一起形成c=o、c=s、c
3-5
环烷基或3-7元杂环基;
[0221]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0222]
r4选自h或-o-c
1-4
烷基。
[0223]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0224]
r1选自c
5-10
环烷基、优选c
5-10
环烷基、环烷基、
[0225]rs
选自h、c
1-2
烷基或o-c
1-2
卤代烷基;
[0226]
环a选自5-6元杂环基(优选含氧原子的5-6元杂环基)或5-6元杂芳基;
[0227]
环b为c
6-10
芳基;
[0228]
环c为c
6-10
芳基;
[0229]
环a、环b和环c任选地被1个、2个或3个r#取代;
[0230]
r#选自h、卤素、=o或c
3-5
环烷基;
[0231]
r3选自c
1-2
烷基或c
1-2
卤代烷基;
[0232]
r4选自h或-o-c
1-2
烷基。
[0233]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0234]
r1选自选自
[0235]
r3选自-cf3或-ch3;
[0236]
r4选自h或-och3。
[0237]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0238]
r1选自c
3-10
环烷基或其中,环a为含氧原子的3-7元杂环基或5-10元杂芳基;
[0239]
r3选自c
1-4
烷基或c
1-4
卤代烷基;
[0240]
r4选自h或-o-c
1-4
烷基。
[0241]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0242]
r1选自c
5-10
环烷基或其中,环a为含氧原子的5-6元杂环基或5-6元杂芳基;
[0243]
r3选自c
1-2
烷基或c
1-2
卤代烷基;
[0244]
r4选自h或-o-c
1-2
烷基。
[0245]
在更具体的实施方案中,本发明提供了上述式(iii)、(iii-1)或(iii-2)化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中,
[0246]
r1选自
[0247]
r3选自-cf3或-ch3;
[0248]
r4选自h或-och3。
[0249]
在更具体的实施方案中,本发明提供了化合物,或其药学上可接受的盐、同位素变体、互变异构体、立体异构体、前药、多晶型、水合物或溶剂合物,其中所述化合物选自:
[0250][0251][0252]
本发明化合物可包括一个或多个不对称中心,且因此可以存在多种立体异构体形式,例如,对映异构体和/或非对映异构体形式。例如,本发明化合物可为单独的对映异构体、非对映异构体或几何异构体(例如顺式和反式异构体),或者可为立体异构体的混合物的形式,包括外消旋体混合物和富含一种或多种立体异构体的混合物。异构体可通过本领域技术人员已知的方法从混合物中分离,所述方法包括:手性高压液相色谱法(hplc)以及手性盐的形成和结晶;或者优选的异构体可通过不对称合成来制备。
[0253]
本发明化合物可以互变异构体形式存在。互变异构体为因分子中某一原子在两个位置迅速移动而产生的官能团异构体,互变异构体是一种特殊的官能团异构体,一对互变异构体可以互相转换,但通常以比较稳定的一种异构体为其主要的存在形式。最主要的例子为烯醇式和酮式互变异构体。
[0254]
本领域技术人员将理解,有机化合物可以与溶剂形成复合物,其在该溶剂中发生反应或从该溶剂中沉淀或结晶出来。这些复合物称为“溶剂合物”。当溶剂是水时,复合物称为“水合物”。本发明涵盖了本发明化合物的所有溶剂合物。
[0255]
术语“溶剂合物”是指通常由溶剂分解反应形成的与溶剂相结合的化合物或其盐的形式。这个物理缔合可包括氢键键合。常规溶剂包括包括水、甲醇、乙醇、乙酸、dmso、thf、乙醚等。本文所述的化合物可制备成,例如,结晶形式,且可被溶剂化。合适的溶剂合物包括药学上可接受的溶剂合物且进一步包括化学计量的溶剂合物和非化学计量的溶剂合物。在一些情况下,所述溶剂合物将能够分离,例如,当一或多个溶剂分子掺入结晶固体的晶格中时。“溶剂合物”包括溶液状态的溶剂合物和可分离的溶剂合物。代表性的溶剂合物包括水合物、乙醇合物和甲醇合物。
[0256]
术语“水合物”是指与水相结合的化合物。通常,包含在化合物的水合物中的水分子数与该水合物中该化合物分子数的比率确定。因此,化合物的水合物可用例如通式r
·
x h2o代表,其中r是该化合物,和x是大于0的数。给定化合物可形成超过一种水合物类型,包括,例如,单水合物(x为1)、低级水合物(x是大于0且小于1的数,例如,半水合物(r
·
0.5h2o))和多水合物(x为大于1的数,例如,二水合物(r
·
2h2o)和六水合物(r
·
6h2o))。
[0257]
本发明化合物可以是无定形或结晶形式(多晶型)。此外,本发明化合物可以以一种或多种结晶形式存在。因此,本发明在其范围内包括本发明化合物的所有无定形或结晶形式。术语“多晶型物”是指特定晶体堆积排列的化合物的结晶形式(或其盐、水合物或溶剂合物)。所有的多晶型物具有相同的元素组成。不同的结晶形式通常具有不同的x射线衍射图、红外光谱、熔点、密度、硬度、晶体形状、光电性质、稳定性和溶解度。重结晶溶剂、结晶速率、贮存温度和其他因素可导致一种结晶形式占优。化合物的各种多晶型物可在不同的条件下通过结晶制备。
[0258]
本发明还包括同位素标记的化合物(同位素变体),它们等同于式(i)所述的那些,但一个或多个原子被原子质量或质量数不同于自然界常见的原子质量或质量数的原子所代替。可以引入本发明化合物中的同位素的实例包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,分别例如2h、3h、
13
c、
11
c、
14
c、
15
n、
18
o、
17
o、
31
p、
32
p、
35
s、
18
f和
36
cl。含有上述同位素和/或其它原子的其它同位素的本发明化合物、其前体药物和所述化合物或所述前体药物的药学上可接受的盐都属于本发明的范围。某些同位素标记的本发明化合物、例如引入放射性同位素(例如3h和
14
c)的那些可用于药物和/或底物组织分布测定。氚、即3h和碳-14、即
14
c同位素是特别优选的,因为它们容易制备和检测。进而,被更重的同位素取代,例如氘、即2h,由于代谢稳定性更高可以提供治疗上的益处,例如延长体内半衰期或减少剂量需求,因而在有些情况下可能是优选的。同位素标记的本发明式(a)化合物及其前体药物一般可以这样制备,在进行下述流程和/或实施例与制备例所公开的工艺时,用容易得到的同位素标记的试剂代替非同位素标记的试剂。
[0259]
此外,前药也包括在本发明的上下文内。本文所用的术语“前药”是指在体内通过
例如在血液中水解转变成其具有医学效应的活性形式的化合物。药学上可接受的前药描述于t.higuchi和v.stella,prodrugs as novel delivery systems,a.c.s.symposium series的vol.14,edward b.roche,ed.,bioreversible carriers in drug design,american pharmaceutical association and pergamon press,1987,以及d.fleisher、s.ramon和h.barbra“improved oral drug delivery:solubility limitations overcome by the use of prodrugs”,advanced drug delivery reviews(1996)19(2)115-130,每篇引入本文作为参考。
[0260]
前药为任何共价键合的本发明化合物,当将这种前药给予患者时,其在体内释放母体化合物。通常通过修饰官能团来制备前药,修饰是以使得该修饰可以通过常规操作或在体内裂解产生母体化合物的方式进行的。前药包括,例如,其中羟基、氨基或巯基与任意基团键合的本发明化合物,当将其给予患者时,可以裂解形成羟基、氨基或巯基。因此,前药的代表性实例包括(但不限于)式(a)化合物的羟基、巯基和氨基官能团的乙酸酯/酰胺、甲酸酯/酰胺和苯甲酸酯/酰胺衍生物。另外,在羧酸(-cooh)的情况下,可以使用酯,例如甲酯、乙酯等。酯本身可以是有活性的和/或可以在人体体内条件下水解。合适的药学上可接受的体内可水解的酯基包括容易在人体中分解而释放母体酸或其盐的那些基团。
[0261]
本发明还提供药物制剂,包含治疗有效量的式(a)化合物或其治疗学上可接受的盐和其药学上可接受的载体、稀释剂或赋形剂。所有这些形式都属于本发明。
[0262]
药物组合物和试剂盒
[0263]
在另一方面,本发明提供了药物组合物,其包含本发明化合物(还称为“活性组分”)和药学上可接受的赋形剂。在一些实施方案中,所述药物组合物包含有效量的本发明化合物。在一些实施方案中,所述药物组合物包含治疗有效量的本发明化合物。在一些实施方案中,所述药物组合物包含预防有效量的本发明化合物。
[0264]
用于本发明的药学上可接受的赋形剂是指不会破坏一起调配的化合物的药理学活性的无毒载剂、佐剂或媒剂。可以用于本发明组合物中的药学上可接受的载剂、佐剂或媒剂包括(但不限于)离子交换剂、氧化铝、硬脂酸铝、卵磷脂、血清蛋白(如人类血清白蛋白)、缓冲物质(如磷酸盐)、甘氨酸、山梨酸、山梨酸钾、饱和植物脂肪酸的偏甘油酯混合物、水、盐或电解质(如硫酸鱼精蛋白)、磷酸氢二钠、磷酸氢钾、氯化钠、锌盐、硅胶、三硅酸镁、聚乙烯吡咯烷酮、基于纤维素的物质、聚乙二醇、羧甲基纤维素钠、聚丙烯酸酯、蜡、聚乙烯-聚氧丙烯-嵌段聚合物、聚乙二醇以及羊毛脂。
[0265]
用于给予本发明化合物的合适制剂将对于本领域普通技术人员而言是显而易见的,并且包括例如片剂、丸剂、胶囊、栓剂、锭剂、糖锭剂、溶液(特别是注射(皮下、静脉内、肌内)和输注(注射剂)用溶液)、酏剂、糖浆、扁囊剂、乳液、吸入剂或可分散粉剂。一种或多种药物活性化合物的含量的范围应该是作为整体的组合物的0.1至90wt%、优选0.5至50wt%,即,其量足以实现以下指定的剂量范围。如有必要,指定的剂量可每天给药若干次。
[0266]
本发明还包括试剂盒(例如,药物包装)。所提供的试剂盒可以包括本发明化合物、其它治疗剂,以及含有本发明化合物、其它治疗剂的第一和第二容器(例如,小瓶、安瓿瓶、瓶、注射器和/或可分散包装或其它合适的容器)。在一些实施方案中,提供的试剂盒还可以任选包括第三容器,其含有用于稀释或悬浮本发明化合物和/或其它治疗剂的药用赋形剂。在一些实施方案中,提供在第一容器和第二容器中的本发明化合物和其它治疗剂组合形成
一个单位剂型。
[0267]
给药
[0268]
本发明提供的药物组合物可以通过许多途径给药,包括但不限于:口服给药、肠胃外给药、吸入给药、局部给药、直肠给药、鼻腔给药、口腔给药、阴道给药、通过植入剂给药或其它给药方式。例如,本文使用的肠胃外给药包括皮下给药、皮内给药、静脉内给药、肌肉内给药、关节内给药、动脉内给药、滑膜腔内给药、胸骨内给药、脑脊髓膜内给药、病灶内给药、和颅内的注射或输液技术。
[0269]
通常,给予有效量的本文所提供的化合物。按照有关情况,包括所治疗的病症、选择的给药途径、实际给予的化合物、个体患者的年龄、体重和响应、患者症状的严重程度,等等,可以由医生确定实际上给予的化合物的量。
[0270]
当用于预防本发明所述病症时,给予处于形成所述病症危险之中的受试者本文所提供的化合物,典型地基于医生的建议并在医生监督下给药,剂量水平如上所述。处于形成具体病症的危险之中的受试者,通常包括具有所述病症的家族史的受试者,或通过遗传试验或筛选确定尤其对形成所述病症敏感的那些受试者。
[0271]
还可以长期给予本文所提供的药物组合物(“长期给药”)。长期给药是指在长时间内给予化合物或其药物组合物,例如,3个月、6个月、1年、2年、3年、5年等等,或者可无限期地持续给药,例如,受试者的余生。在一些实施方案中,长期给药意欲在长时间内在血液中提供所述化合物的恒定水平,例如,在治疗窗内。
[0272]
可以使用各种给药方法,进一步递送本发明的药物组合物。例如,在一些实施方案中,可以推注给药药物组合物,例如,为了使化合物在血液中的浓度提高至有效水平。推注剂量取决于通过身体的活性组分的目标全身性水平,例如,肌内或皮下的推注剂量使活性组分缓慢释放,而直接递送至静脉的推注(例如,通过iv静脉滴注)能够更加快速地递送,使得活性组分在血液中的浓度快速升高至有效水平。在其它实施方案中,可以以持续输液形式给予药物组合物,例如,通过iv静脉滴注,从而在受试者身体中提供稳态浓度的活性组分。此外,在其它实施方案中,可以首先给予推注剂量的药物组合物,而后持续输液。
[0273]
口服组合物可以采用散装液体溶液或混悬剂或散装粉剂形式。然而,更通常,为了便于精确地剂量给药,以单位剂量形式提供所述组合物。术语“单位剂型”是指适合作为人类患者及其它哺乳动物的单元剂量的物理离散单位,每个单位包含预定数量的、适于产生所需要的治疗效果的活性物质与合适药学赋形剂。典型的单位剂量形式包括液体组合物的预装填的、预先测量的安瓿或注射器,或者在固体组合物情况下的丸剂、片剂、胶囊剂等。在这种组合物中,所述化合物通常为较少的组分(约0.1至约50重量%,或优选约1至约40重量%),剩余部分为对于形成所需给药形式有用的各种载体或赋形剂以及加工助剂。
[0274]
对于口服剂量,代表性的方案是,每天一个至五个口服剂量,尤其是两个至四个口服剂量,典型地是三个口服剂量。使用这些剂量给药模式,每个剂量提供大约0.01至大约20mg/kg的本发明化合物,优选的剂量各自提供大约0.1至大约10mg/kg,尤其是大约1至大约5mg/kg。
[0275]
为了提供与使用注射剂量类似的血液水平,或比使用注射剂量更低的血液水平,通常选择透皮剂量,数量为大约0.01至大约20%重量,优选大约0.1至大约20%重量,优选大约0.1至大约10%重量,且更优选大约0.5至大约15%重量。
[0276]
从大约1至大约120小时,尤其是24至96小时,注射剂量水平在大约0.1mg/kg/小时至至少10mg/kg/小时的范围。为了获得足够的稳定状态水平,还可以给予大约0.1mg/kg至大约10mg/kg或更多的预载推注。对于40至80kg的人类患者来说,最大总剂量不能超过大约2g/天。
[0277]
适于口服给药的液体形式可包括合适的水性或非水载体以及缓冲剂、悬浮剂和分散剂、着色剂、调味剂,等等。固体形式可包括,例如,任何下列组份,或具有类似性质的化合物:粘合剂,例如,微晶纤维素、黄蓍胶或明胶;赋形剂,例如,淀粉或乳糖,崩解剂,例如,褐藻酸、primogel或玉米淀粉;润滑剂,例如,硬脂酸镁;助流剂,例如,胶体二氧化硅;甜味剂,例如,蔗糖或糖精;或调味剂,例如,薄荷、水杨酸甲酯或橙味调味剂。
[0278]
可注射的组合物典型地基于可注射用的无菌盐水或磷酸盐缓冲盐水,或本领域中已知的其它可注射的赋形剂。如前所述,在这种组合物中,活性化合物典型地为较少的组分,经常为约0.05至10%重量,剩余部分为可注射的赋形剂等。
[0279]
典型地将透皮组合物配制为含有活性组分的局部软膏剂或乳膏剂。当配制为软膏剂时,活性组分典型地与石蜡或可与水混溶的软膏基质组合。或者,活性组分可与例如水包油型乳膏基质一起配制为乳膏剂。这种透皮制剂是本领域中公知的,且通常包括用于提升活性组分或制剂的稳定的皮肤渗透的其它组份。所有这种已知的透皮制剂和组份包括在本发明提供的范围内。
[0280]
本发明化合物还可通过经皮装置给予。因此,经皮给药可使用贮存器(reservoir)或多孔膜类型、或者多种固体基质的贴剂实现。
[0281]
用于口服给予、注射或局部给予的组合物的上述组份仅仅是代表性的。其它材料以及加工技术等阐述于remington's pharmaceutical sciences,17th edition,1985,mack publishing company,easton,pennsylvania的第8部分中,本文以引用的方式引入该文献。
[0282]
本发明化合物还可以以持续释放形式给予,或从持续释放给药系统中给予。代表性的持续释放材料的描述可在remington's pharmaceutical sciences中找到。
[0283]
本发明还涉及本发明化合物的药学上可接受的制剂。在一个实施方案中,所述制剂包含水。在另一个实施方案中,所述制剂包含环糊精衍生物。最常见的环糊精为分别由6、7和8个α-1,4-连接的葡萄糖单元组成的α-、β-和γ-环糊精,其在连接的糖部分上任选包括一个或多个取代基,其包括但不限于:甲基化的、羟基烷基化的、酰化的和磺烷基醚取代。在一些实施方案中,所述环糊精为磺烷基醚β-环糊精,例如,磺丁基醚β-环糊精,也称作captisol。参见,例如,u.s.5,376,645。在一些实施方案中,所述制剂包括六丙基-β-环糊精(例如,在水中,10-50%)。
[0284]
药物联用
[0285]
目前本领域中已知的许多化学治疗剂可与本发明化合物组合使用。
[0286]
有待与本发明式(i)的化合物(包括化合物(i)的所有单独实施方案或通用子集)一起/组合使用或在如本文(上文和下文)所定义的医学用途、用途、治疗和/或预防方法中使用的药理学活性物质可选自以下中的任何一种或多种(优选在所有这些实施方案中仅使用一种另外的药理学活性物质):
[0287]
1.egfr和/或其突变体的抑制剂
[0288]
a.例如,阿法替尼、厄洛替尼、吉非替尼、拉帕替尼、西妥昔单抗、帕尼单抗、奥希替尼、奥莫替尼、egf-816;
[0289]
b.优选的是阿法替尼、奥希替尼和西妥昔单抗;
[0290]
c.最优选的是阿法替尼;
[0291]
2.erbb2(her2)和/或其突变体的抑制剂
[0292]
a.例如,阿法替尼、拉帕替尼、曲妥珠单抗、帕妥珠单抗;
[0293]
b.优选的是阿法替尼和曲妥珠单抗;
[0294]
c.最优选的是曲妥珠单抗;
[0295]
3.alk和/或其突变体的抑制剂
[0296]
a.例如,克唑替尼、阿来替尼、恩曲替尼、布加替尼;
[0297]
b.优选的是克唑替尼和阿来替尼;
[0298]
c.最优选的是克唑替尼;
[0299]
4.mek和/或其突变体的抑制剂
[0300]
a.例如,曲美替尼、考比替尼、比美替尼(binimetinib)、舍美替尼、瑞美替尼(refametinib);
[0301]
b.优选的是曲美替尼和考比替尼;
[0302]
c.最优选的是曲美替尼;
[0303]
5.kras g12c的抑制剂
[0304]
a.例如,ars-853(wo 2014/152588中的化合物v-64)、wo2016/044772中的实施例i-272;
[0305]
6.bcr-abl和/或其突变体的抑制剂
[0306]
a.例如,伊马替尼、达沙替尼、尼洛替尼;
[0307]
b.优选的是伊马替尼和尼洛替尼;
[0308]
c.最优选的是伊马替尼;
[0309]
7.fgfr1和/或fgfr2和/或fgfr3和/或其突变体的抑制剂
[0310]
a.例如,尼达尼布;
[0311]
8.ros1和/或其突变体的抑制剂
[0312]
a.例如,克唑替尼、恩曲替尼、洛拉替尼、色瑞替尼(ceritinib)、美瑞替尼(merestinib);
[0313]
b.优选的是克唑替尼和恩曲替尼;
[0314]
c.最优选的是克唑替尼;
[0315]
9.c-met和/或其突变体的抑制剂
[0316]
10.axl和/或其突变体的抑制剂
[0317]
11.ntrk1和/或其突变体的抑制剂
[0318]
12.ret和/或其突变体的抑制剂
[0319]
13.紫杉烷
[0320]
a.例如,紫杉醇、白蛋白结合型紫杉醇(nab-paclitaxel)、多西他赛;
[0321]
b.优选的是紫杉醇;
[0322]
14.含铂化合物
[0323]
a.例如,顺铂、卡铂、奥沙利铂;
[0324]
15.抗代谢药
[0325]
a.例如,5-氟尿嘧啶、卡培他滨、氟尿苷、阿糖胞苷、吉西他滨、三氟尿苷和替吡嘧啶(tipiracil)的组合(=tas102);
[0326]
b.优选的是吉西他滨;
[0327]
16.有丝分裂激酶抑制剂
[0328]
a.例如,cdk4/6抑制剂
[0329]
i.例如,帕博西尼、瑞博西尼、阿贝西利(abemaciclib);
[0330]
ii.优选的是帕博西尼和阿贝西利;
[0331]
iii.最优选的是阿贝西利;
[0332]
17.免疫治疗剂
[0333]
a.例如,免疫检查点抑制剂
[0334]
i.例如,抗-ctla4mab、抗-pd1mab、抗-pd-l1mab、抗-pd-l2mab、抗-lag3mab、抗-tim3mab;
[0335]
ii.优选的是抗-pd1mab;
[0336]
iii.例如,易普利姆玛、纳武单抗、派姆单抗、阿特利珠单抗、阿维鲁单抗(avelumab)、度伐鲁单抗、匹地利珠单抗(pidilizumab)、pdr-001(wo 2017/019896中公开且使用的bap049-克隆-e);
[0337]
iv.优选的是纳武单抗、派姆单抗和pdr-001;
[0338]
v.最优选的是派姆单抗;
[0339]
18.抗血管生成药
[0340]
a.例如,贝伐珠单抗、尼达尼布;
[0341]
b.最优选的是贝伐珠单抗;
[0342]
19.拓扑异构酶抑制剂
[0343]
a.例如,伊立替康、脂质体伊立替康、拓扑替康;
[0344]
b.最优选的是伊立替康;
[0345]
20.a-raf和/或b-raf和/或c-raf和/或其突变体的抑制剂
[0346]
a.例如,raf-709(=wo 2014/151616中的实施例131)、ly-3009120(=wo 2013/134243中的实施例1);
[0347]
21.erk和/或其突变体的抑制剂
[0348]
a.例如,乌利替尼(ulixertinib);
[0349]
22.细胞凋亡调节剂
[0350]
a.例如,对p53(优选功能性p53、最优选wt p53)与mdm2之间的相互作用的抑制剂(“mdm2抑制剂”);
[0351]
i.例如,hdm-201、nvp-cgm097、rg-7112、mk-8242、rg-7388、sar405838、amg-232、ds-3032、rg-7775、apg-115;
[0352]
ii.优选的是hdm-201、rg-7388和amg-232
[0353]
b.例如,parp抑制剂;
[0354]
c.例如,mcl-1抑制剂;
[0355]
23.mtor抑制剂
[0356]
a.例如,雷帕霉素、替西罗莫司、依维莫司、地磷莫司;
[0357]
24.表观遗传调节剂
[0358]
a.例如,bet抑制剂
[0359]
i.例如,jq-1、gsk 525762、otx 015(=mk8628)、cpi 0610、ten-010(=ro6870810);
[0360]
b.例如,cdk9抑制剂;
[0361]
25.igf1/2和/或igf1-r的抑制剂
[0362]
a.例如,珍妥珠单抗(xentuzumab)(wo 2010/066868中的抗体60833)、medi-573(=度司妥单抗(dusigitumab))。
[0363]
在本发明中,应理解,根据本发明的组合、组合物、试剂盒、方法、用途或用于所述用途的化合物可设想活性成分或组分的同时、并行、依次、相继、交替或单独给予。应当理解,sos1抑制剂化合物(例如,式(i)的化合物)和至少一种其他药理学活性物质可以依赖性地或独立地配制给予,例如像sos1抑制剂化合物(例如,式(i)的化合物)和至少一种其他药理学活性物质可以作为同一药物组合物/剂型的一部分给予或者优选以单独的药物组合物/剂型给予。
[0364]
实施例
[0365]
本发明所采用的试剂为直接购买的商业化试剂或经本领域熟知的常用方法合成。
[0366]
如下示例的具体反应路线或步骤为本发明所用,具体如下:
[0367]
实施例1
[0368]
关键中间体的制备
[0369]
中间体a1的合成
[0370][0371]
将4-溴苯酚a1-1(4.5g,26.0mmol)和3-溴-2-甲基丙-1-烯a1-2(2.9ml,28.6mmol)溶于100ml丙酮中,向反应液中加入碳酸钾(18.0g,260.1mmol)并在75℃下搅拌12小时,tlc检测反应完成,停止反应。过滤,滤液减压浓缩,加水(50ml),乙酸乙酯萃取,无水硫酸钠干燥,浓缩,得到无色油状物a1-3(5.8g),lc-ms:[m+h]
+
=227。
[0372]
将上步中间体a1-3(3.75g,16.5mmol)溶于50ml n,n-二乙基苯胺中,190℃下搅拌12小时。停止反应,向体系缓慢加入1n盐酸调节ph至7左右,乙醚萃取,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析分离(pe/ea=20/1)得到无色油状物a1-4(1.2g),收率:32%,lc-ms:[m+h]
+
=227。
[0373]
将上步中间体a1-4(1.2g,5.3mmol)溶于50ml二氯甲烷中,加入碘单质(270mg,1.1mmol),室温下反应12小时,停止反应。向反应液中加入饱和硫代硫酸钠水溶液调至无色,二氯甲烷萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,浓缩,得到无色油状物a1(1.0g),收率:83%,lc-ms:m+h
+
=227。
[0374]
中间体a2的合成
[0375][0376]
氮气保护下,将浓硫酸(3.8g,38mmol)逐滴滴加到原料a2-1(22.0g,117mmol)中,升温至40℃后逐滴缓慢加入原料a2-2(10.75ml,110mmol),继续反应2小时后停止反应。将反应液缓慢倒入50ml冰水中,二氯甲烷萃取,饱和碳酸氢钠水溶液洗涤,无水硫酸钠干燥,浓缩,正庚烷洗涤,抽滤,得到白色固体a2-3(15g),收率:46%。
[0377]
氮气保护下,将上步中间体a2-3(6.3g,23mmol)和盐酸吡啶(12.8g,103mmol)溶于喹啉(11.5g,88mmol)中,缓慢升温至175℃并搅拌16小时。冷却至室温,向反应液中缓慢加入浓度6n盐酸(120ml),乙醚萃取,有机相用饱和碳酸氢钠洗涤,无水硫酸钠干燥,浓缩,得到无色油状中间体a2(4.0g),收率:77%。
[0378]
中间体a3的合成
[0379][0380]
冰浴下,将四氢铝锂(1.35g,35.68mmol)溶于200ml乙醚中,缓慢滴加提前配置的a3-1(8.0g,29.7mmol)的乙醚溶液(100ml),滴毕,继续搅拌1小时。向反应液中加入20ml冰水和2.5m的氢氧化钠水溶液(4ml)淬灭反应,减压蒸除溶剂,向体系加入30ml冰水,乙酸乙酯萃取,无水硫酸钠干燥,浓缩,得到白色固体a3-2(6.5g),收率:96%,lc-ms:[m+h]
+
=227。
[0381]
冰浴下,将上步中间体a3-2(6.0g,26.6mmol)和diea(3.45g,26.6mmol)溶于120ml醋酸异丙酯中,缓慢滴加二氯亚砜(3.78g,31.9mmol),滴毕,继续反应1小时。向反应液中加入100ml冰水,乙酸乙酯萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,得到白色固体a3-3(6.0g),收率:93%,lc-ms:[m+h]
+
=245。
[0382]
冰浴,氮气保护下,将氯化铬(3.1g,20mmol)溶于40ml无水四氢呋喃中,缓慢滴加四氢铝锂的四氢呋喃溶液(10.1ml),搅拌15分钟后加入dmf(50ml)和异丙醇(3ml)。向体系中加入上步中间体a3-3(1.98g,8.1mmol)的dmf溶液(50ml),将反应液置于室温下反应12小时。停止反应,向反应液加水(300ml),正己烷萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析分离(pe/ea=21/1)得到白色固体a3-4(800mg),收率:47%,lc-ms:[m+h]
+
=211。
[0383]
冰浴,氮气保护下,将上步中间体a3-4(800mg,3.8mmol)溶于15ml二氯乙烷中,逐滴加入二乙基锌甲苯溶液(9.5ml),滴毕,加入氯碘甲烷(1.4ml,19mmol),继续搅拌1小时后,升温至65℃下反应3小时。冷却至室温,向反应液加入50ml饱和氯化铵水溶液,二氯甲烷萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析分离(pe/ea=100/1)得到无色油状物a3(280mg),收率:33%,lc-ms:[m+h]
+
=225。
[0384]
实施例2
[0385]
目标分子p1-p8的制备
[0386][0387]
氮气保护,在-78℃下,将原料p1-1(2.13g,9mmol)加入到100ml三口反应瓶中,10ml无水四氢呋喃溶解。向反应液中缓慢滴加正丁基锂(4.5ml,3.6mmol),滴毕,继续搅拌30分钟。缓慢向反应中滴加原料p1-2(645mg,3.0mmol)的thf(10ml)溶液,滴加完毕后,缓慢升至室温下继续反应2小时,lc-ms监测反应完成,停止反应。反应液用饱和氯化铵水溶液淬灭,乙酸乙酯萃取,有机相用饱和食盐水洗涤。无水硫酸钠干燥后,柱层析分离(洗脱剂pe/ea=3/1),得到淡黄色固体p1-3(384mg),收率34%,lc-ms:[m+h]
+
=374。
[0388]
氮气保护下,将上步中间体p1-3(384mg 1.04mmol)、对甲苯磺酸一水合物(1.5g,7.76mmol)和苯酚(487mg,5.18mmol)溶于10ml二氯乙烷中,90℃下回流反应2小时。停止反应,冷却至室温,过滤除去对甲苯磺酸盐,浓缩,柱层析分离(洗脱剂pe/ea=3/1),得到淡黄色固体p1(300mg,收率65%,lc-ms:[m+h]
+
=374。
[0389]1h nmr(400mhz,dmso-d6)δ11.34(s,1h),9.63(s,1h),7.60(d,j=7.9hz,1h),7.47(d,j=7.4hz,1h),7.39(dd,j=8.1,1.0hz,1h),7.22(td,j=7.9,3.3hz,2h),7.09
–
7.02(m,2h),6.83(dd,j=8.2,0.9hz,1h),6.81
–
6.74(m,2h).
[0390]
参照化合物p1的合成路线,采用类似的骨架结构,合成如下目标分子。
[0391]
[0392]
[0393][0394]
实施例2
[0395]
目标分子p9的制备
[0396][0397]
将原料p9-1(1.0g,7.29mmol),原料p9-2(1.23g,7.44mmol)和盐酸羟胺(1.55g,22.3mmol)溶于40ml水和2ml盐酸(浓度2m)中,加入无水硫酸钠(7.0g)。升温至55℃并反应3小时,lc-ms监测反应完成。停止反应,冷却至室温,乙酸乙酯萃取,无水硫酸钠干燥,浓缩,得到粗品p9-3。lc-ms:[m+h]
+
=209.3。
[0398]
冰浴下,将上步粗品溶于10ml浓硫酸中,升温至85℃下反应30分钟。lc-ms监测反应完成,将反应液缓慢倒入50ml冰水中,搅拌20分钟后抽滤,滤饼用水洗涤,干燥,得到黄色固体p9-4(450mg),两步收率:42%,lc-ms:[m+h]
+
=192.2。
[0399]
制作格氏试剂:将溴代环庚烷(1.0g 5.6mmol)溶于10ml无水四氢呋喃中;另取镁屑(0.41g,16.8mmol)和碘粒一颗,加入反应瓶中。向反应瓶中缓慢加入提前配置的溴代环庚烷溶液,快速升温至60℃引发反应。继续滴加溴代环庚烷的稀释液,滴毕,室温下搅拌1小时。格氏试剂浓度为0.56mmol/ml。
[0400]-50℃下,将中间体p9-4(100mg.0.35mmol)溶于5ml无水四氢呋喃中,缓慢加入新配置的格氏试剂(1.87ml),升温至室温,继续反应2小时。lc-ms监测反应完成,向体系加入饱和氯化铵水溶液30ml淬灭反应,乙酸乙酯萃取,无水硫酸钠干燥,浓缩,柱层析分离,得到中间体p9-5(50mg),收率:33%,lc-ms:[m+h]
+
=287.4。
[0401]
将上步中间体p9-5(50mg,0.17mmol),对甲苯磺酸(88mg,0.51mmol)和苯酚(32mg,0.34mmol)溶于8ml二氯乙烷中,升温至60℃反应1小时。lc-ms监测反应完成,向体系加入30ml水,二氯甲烷萃取,无水硫酸钠干燥,浓缩,柱层析分离,得到目标产物p9(18mg),收率:28%,lc-ms:[m+h]
+
=366。
[0402]1h nmr(400mhz,cdcl3)δ7.66(s,1h),7.27(s,1h),7.25(s,1h),7.09(d,j=8.3hz,1h),6.72(d,j=8.1hz,2h),6.57(d,j=8.3hz,1h),3.86(s,3h),2.62(t,j=9.8hz,1h),2.10(s,3h),1.78
–
1.45(m,12h).
[0403]
实施例3
[0404]
目标分子p2a和p2b的制备
[0405][0406]
将化合物p2经sfc手性拆分,得到化合物p2a和p2b。
[0407]
实施例4
[0408]
目标分子p10-p11的制备
[0409][0410]-78℃下,将原料p10-1(547mg,2.8mmol)溶于20ml无水四氢呋喃中,缓慢滴入1.6m浓度正丁基锂(1.74ml,2.8mmol),滴毕,继续搅拌1小时。向反应液中加入原料p1-2(300mg,1.39mmol),升温至室温反应1小时。加入30ml饱和氯化铵溶液淬灭反应,乙酸乙酯萃取,无水硫酸钠干燥,浓缩,柱层析分离,得中间体p10-2和p11-1的混合物(180mg),收率39%,lc-ms:[m+h]
+
=334。
[0411]
将上步混合物(180mg,0.54mmol)、苯酚(77mg,1.1mmol)和对甲苯磺酸(308mg,1.6mmol)溶于8ml二氯乙烷中,升温至60℃下反应1小时。lc-ms监测反应完全,停止反应,过滤,滤液浓缩,hplc色谱分离,得到化合物p10(9.5mg)和p11(12mg),lc-ms:[m+h]
+
=410。
[0412]
p10:1h nmr(400mhz,dmso-d6)δ11.18(s,1h),9.50(s,1h),7.98(d,j=2.2hz,1h),7.55(d,j=8.3hz,3h),7.38(d,j=2.0hz,1h),7.20(t,j=7.8hz,1h),7.09(dd,j=8.7,2.1hz,1h),7.03
–
6.96(m,2h),6.95
–
6.89(m,1h),6.78
–
6.65(m,2h).
[0413]
p11:1h nmr(400mhz,dmso-d6)δ11.22(s,1h),9.65(s,1h),7.59(dd,j=6.6,2.1hz,1h),7.53(d,j=8.1hz,1h),7.51
–
7.45(m,3h),7.35(d,j=7.5hz,1h),7.30(tt,j=7.4,5.8hz,2h),7.10(t,j=7.7hz,1h),6.95
–
6.90(m,2h),5.26(s,1h).
[0414]
实施例5
[0415]
目标分子p12的制备
[0416][0417]
氮气保护下,将原料p1-2(991mg,4.61mmol)和镁屑(142mg,5.8mmol)溶于20ml无水四氢呋喃中,加入一颗碘单质,快速升温至50℃引发反应,搅拌1小时。室温下缓慢加入原料p12-1(500mg 2.32mmol),滴毕,室温反应1小时。lc-ms监测反应完成,用40ml饱和氯化铵溶液淬灭反应,乙酸乙酯萃取,无水硫酸钠干燥,浓缩,柱层析分离,得中间体p12-2(300mg),收率:37%,lc-ms:m+h
+
=350。
[0418]
将中间体p12-2(300mg,0.86mmol)、苯酚(121mg,1.72mmol)和对甲苯磺酸(491mg,2.58mmol)溶于8ml二氯甲烷中,升温至60℃下反应1小时。停止反应,冷却至室温,过滤,滤液浓缩,柱层析分离,得到化合物p12(80mg),收率:22%,lc-ms:[m+h]
+
=426。
[0419]1h nmr(400mhz,dmso-d6)δ11.20(s,1h),9.50(s,1h),7.95(d,j=8.5hz,1h),7.75(d,j=5.4hz,1h),7.61(d,j=1.6hz,1h),7.56(dd,j=7.7,4.1hz,2h),7.44(d,j=5.4hz,1h),7.21(t,j=7.7hz,1h),7.15(dd,j=8.6,1.7hz,1h),7.00(d,j=8.7hz,2h),6.73(d,j=8.7hz,2h).
[0420]
实施例6
[0421]
目标分子p13的制备
[0422][0423]
氮气保护,-50℃下,将原料p13-1(1.14g,4.0mmol)溶于20ml无水四氢呋喃中,缓慢滴加2.5m浓度正丁基锂(1.6ml,4.0mmol),滴毕,在-50℃下搅拌1小时;将7-(三氟甲基)吲哚啉-2,3-二酮p1-2(430mg,2.0mmol)溶于4ml无水四氢呋喃中,并缓慢加入到上述反应液中,滴毕,升温至室温反应2小时。向体系中加入40ml饱和氯化铵水溶液淬灭反应,乙酸乙酯萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,浓缩,得到淡黄色固体p13-2(500mg),收率:59%,lc-ms:[m+h]
+
=424。
[0424]
氮气保护下,将上步中间体p13-2(423mg,1.0mmol)溶于15ml二氯乙烷中,加入苯并呋喃-2(3h)-酮p13-3(200mg,1.5mmol)和对甲苯磺酸(571mg,3.0mmol),升温至70℃反应30分钟,过滤,滤液浓缩,柱层析分离(pe/ea=5/1),得到白色固体p13(24mg),20%,lc-ms:[m+h]
+
=426。
[0425]1h nmr(400mhz,cdcl3)δ7.99(s,1h),7.49(d,j=8.0hz,1h),7.36(d,j=7.5hz,1h),7.20(d,j=7.0hz,2h),7.15(dd,j=8.5,2.1hz,1h),7.13
–
7.08(m,2h),7.03(d,j=8.4hz,1h),6.81
–
6.74(m,2h),5.17(s,1h),3.69(s,2h).
[0426]
实施例7
[0427]
目标分子h1的制备
[0428][0429]
氮气保护下,-78℃下,将原料h1-1(7.3g,30mmol)溶于24ml无水四氢呋喃中,缓慢滴加2.5m的正丁基锂(14.4ml,36mmol),滴毕,继续搅拌30分钟后,缓慢滴加提前配置好的p1-2(2.15g,10mmol)的四氢呋喃(20ml)溶液,滴加完毕,升温至室温继续反应2小时,停止反应。向反应液中加入30ml饱和氯化铵水溶液淬灭反应,乙酸乙酯萃取,有机相用饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析分离(pe/ea=3/1)得到黄色油状物h1-2(2.3g),收率:62%,lc-ms:[m+h]
+
=378。
[0430]
氮气保护下,将上步中间体h1-2(2.3g,6.10mmol)、对甲苯磺酸一水合物(8.12g,42.7mmol)和苯酚(2.87g,30.5mmol)溶于50ml二氯乙烷中,90℃下回流反应2小时。停止反应,冷却至室温,过滤除去对甲苯磺酸盐,浓缩,柱层析分离(pe/ea=3/1),得到淡黄色固体h1-3(2.0g),收率:72%,lc-ms:[m+h]
+
=454。
[0431]
将上步h1-3(50mg,0.11mmol)溶于5ml无水四氢呋喃中,加入硼烷二甲硫醚(0.2ml,0.4mmol),升温至50℃下反应10小时。冷却至室温,向反应液中加入2ml甲醇淬灭反应,浓缩,柱层析分离(pe/ea=4/1)得到化合物h1(20mg),收率:41%,lc-ms:[m+h]
+
=440。
[0432]1h nmr(400mhz,dmso-d6)δ9.35(s,1h),7.29
–
7.16(m,6h),6.95(d,j=8.7hz,2h),6.74
–
6.61(m,3h),6.23(s,1h),3.99(s,2h).
[0433]
参照化合物h1的合成路线,采用类似的骨架结构,合成如下目标分子。
[0434][0435]
实施例8
[0436]
化合物对于乳腺癌细胞增殖抑制的测试具体如下:
[0437]
mcf-7(雌激素受体表达阳性,于包含10%胎牛血清和1%青链霉素的mem培养基中培养)和mda-mb-231(雌激素受体表达阴性,于包含10%胎牛血清和1%青链霉素的l-15培养基中培养)乳腺癌细胞用于考察化合物对乳腺癌细胞的增殖抑制作用。
[0438]
将mcf-7和mda-mb-231细胞接种在384孔微板上(600/30μl),37℃、5%二氧化碳条件下温育过夜。使用echo 655(labcyte,model:655)在各孔中加入30nl不同浓度化合物并在37℃、5%co2孵育箱中温育3天。然后,每孔中加入30μl按照试剂盒说明书准备好的ctg试剂(promega,cat.no.:g7573)并振摇,在25℃避光孵育30分钟,使用envision仪器(perkinelmer,model:envision2105)扫描读板并记录信号值。
[0439]
使用以下公式计算抑制率(%):
[0440]
%inhibition=100-(signal
cmpd-signal
ave_bl
)/(signal
ave_vc-signal
ave_bl
)
×
100
[0441]
signal
ave_pc
:the average signal for the positive controls across the plate。
[0442]
signal
ave_vc
:the average signal for negative controls across the plate。
[0443]
使用graphpad8.0以非线性回归方程计算ic
50
:
[0444]
y=bottom+(top-bottom)/(1+10^((logic
50-x)
×
hillslope))
[0445]
x:抑制剂浓度的log对数值;y:抑制率%。
[0446]
化合物对于mcf-7细胞的抗增殖实验
[0447]
表1:化合物对于mcf-7细胞半数有效浓度抗增殖效果
[0448]
化合物mcf-7/ic
50
/nm化合物mcf-7/ic
50
/nmp1269*p219p2a20p2b》500p377p4207p5》500p6》500p738p8142p97p1047p11》500p1218p13》500p14121h1719*h2》500h3》500h4》500
[0449]
*:表示化合物与细胞孵育7天的结果
[0450]
以上结果表明:本发明对于er+阳性的乳腺癌具有良好的抑制效果。
[0451]
化合物对于非er阳性的mda-mb-231细胞的抗增殖实验
[0452][0453]
以上结果表明:本发明对于er-阴性的乳腺癌不具有抑制活性,体现了本发明对于雌激素受体阳性的乳腺癌的高选择性抑制。
[0454]
实施例10
[0455]
小鼠药代动力学评价实验
[0456]
以cd1雌性小鼠为受试动物,口服/静脉给药(口服给药量为10mg/kg,静脉为2mg/kg)。
[0457]
实验方案:口服组每组3只,静脉组每组三只。口服:收集给药前(0h)和给药后(0.25,0.5,1,2,4,8,24h)的血浆样品;静脉:收集给药前(0h)和给药后(0.083,0.25,0.5,1,2,4,8,24h)的血浆样品;用lc/ms/ms法分别测定小鼠口服和静脉给药后的血浆的血液浓度,采集的数据用ab sciex qtrap 6500软件计算,实验结果如下:
[0458][0459][0460]
以上实验结果表明,本发明化合物具有良好的口服吸收效果。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1