合成手性α-磷化合物的方法
合成手性
α-磷化合物的方法
技术领域
1.本发明专利涉及有机及药物合成领域,尤其是指一种通过廉价金属镍催化α-取代α,β-不饱和磷氧化物、磷酸酯、磷酸高效合成手性α-磷化合物的方法。
背景技术:
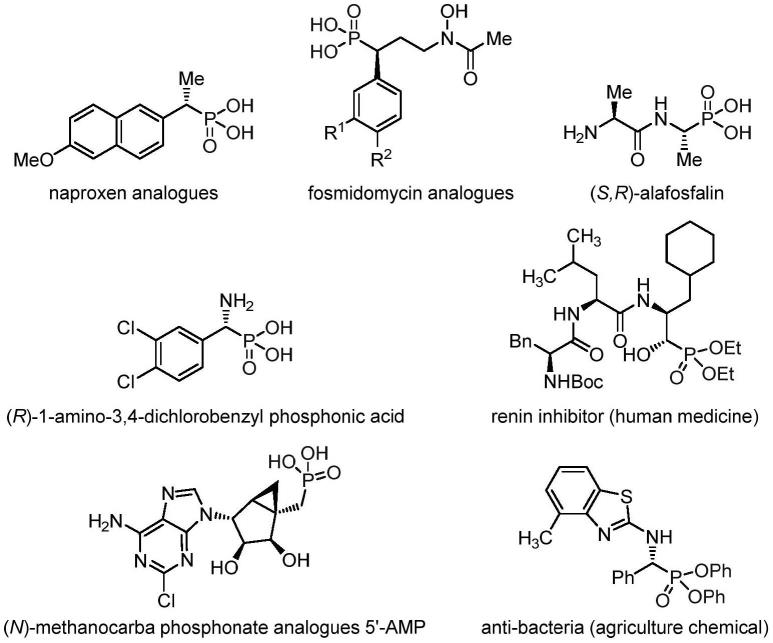
2.手性α-磷化合物不仅是许多医药、农药和生物活性分子的重要骨架,而且是获得手性有机磷化合物的重要中间体,例如非甾体抗炎剂萘普生类似物(+)-6-甲氧基-α-甲基-2-萘甲基磷酸具有良好消炎镇痛活性;膦胺霉素类似物能抑制恶性疟原虫生长;(s,r)-alafosfalin是一种高效的抗菌剂,能有效抵抗革兰氏阳性和革兰氏阴性微生物;(r)-1-amino-3,4-dichlorobenzylphosphonic acid能高效抑制苯丙氨酸解氨酶;(n)-methanocarba phosphonate analogues 5
’‑
amp是治疗心脏衰竭保护剂等。手性磷酸酯既能作为renin inhibitor(肾素抑制药),也可以作为anti-bacterial(抗菌剂)。
[0003][0004]
由于手性α-磷化合物在制药等领域具有重大的应用价值,人们对合成该类手性化合物的方法学进行了深入的研究,并且开发出了多种合成策略。目前,不对称氢化是最为直接和有效合成手性α-磷化合物的方法之一。在过去的数十年中,少数几例是利用贵重金属铑、铱、钌等金属与手性膦配体络合的催化剂对α-取代α,β-不饱和磷氧化物、磷酸酯、磷酸进行不对称氢化,得到手性α-磷化合物。但是,贵重金属催化体系面临价格昂贵、毒性重、地壳储量有限、重金属污染环境等困难,从而大大限制了该体系的工业化潜力。发展价格低廉、无毒或低毒且对环境友好、地球储量丰富的金属镍不对称催化氢化反应体系符合现代
化学可持续发展的要求和趋势,目前运用廉价金属镍催化体系进行不对称氢化实现手性α-磷化合物的合成方法尚未报道,充满挑战,需要致力于发展高效的催化体系。
[0005]
因此,研发一种易于工业化的合成手性α-磷化合物的方法显得很有必要。
技术实现要素:
[0006]
本发明旨在至少在一定程度上解决现有技术中存在的技术问题之一,由此,在本发明的第一方面,本发明提供一种合成手性α-磷化合物的方法,所述手性α-磷化合物由化合物1进行不对称氢化反应制备得到,所述化合物1制备所述手性α-磷化合物的反应式如下所示:
[0007][0008]
r3选自苯基、取代苯基、萘基、环己烷基中的一种,r’为c
1-c6的直链烷基或h,r1、r2分别独立地选自羟基、烷氧基、苯基和o-中的一种;优选地,所述取代苯基为卤素取代苯基、烷基取代苯基、烷氧基取代苯基或卤素烷基取代苯基。
[0009]
所述化合物1制备所述手性α-磷化合物使用的催化剂为手性配体(s,s)-ph-bpe与镍盐络合得到的催化剂。
[0010]
所述催化体系为廉价金属镍的催化体系。
[0011]
在本发明的一个或多个实施例中,控制不对称氢化反应温度为60~80℃。
[0012]
在本发明的一个或多个实施例中,反应在氢气气氛下进行,控制氢气压力为60~80大气压,控制反应时间为24~36小时。
[0013]
在本发明的一个或多个实施例中,所述催化剂由手性配体(s,s)-ph-bpe与镍盐经络合反应得到;
[0014]
所述手性配体(s,s)-ph-bpe的结构如下:
[0015][0016]
在本发明的一个或多个实施例中,所述络合反应在溶剂中进行,所述溶剂为醇,优选为甲醇或乙醇。
[0017]
在本发明的一个或多个实施例中,控制镍盐与手性配体(s,s)-ph-bpe的摩尔比为1:1~1.2。
[0018]
在本发明的一个或多个实施例中,控制所述络合反应的反应温度为15~35℃。
[0019]
在本发明的一个或多个实施例中,控制所述络合反应的反应时间为36小时。
[0020]
在本发明的一个或多个实施例中,所述镍盐为ni(oac)2。
[0021]
在本发明的一个或多个实施例中,合成手性α-磷化合物的方法,包括如下步骤:
[0022]
步骤1):手性配体(s,s)-ph-bpe与镍盐络合反应;
[0023]
步骤2):向步骤1)反应液中加入化合物1进行不对称氢化反应,即得到所述手性α-磷化合物。
[0024]
本发明的有益效果在于:
[0025]
1、本发明提供一种手性α-磷化合物的制备方法,其采用丰产廉价金属镍盐和商品化手性配体(s,s)-ph-bpe为催化体系,来源丰富,方便易得,价格低,催化活性、效率高,对映选择性好。
[0026]
2、本发明提供一种手性α-磷化合物的制备方法,其对绝大多数底物适用,均能实现100%完全转化和90%以上的对映选择性,并且,其原子经济性高,催化体系底物适用范围广,是目前首例通过丰产廉价金属催化氢化获得手性α-磷氧化物、α-磷酸酯和α-磷酸等α-磷化合物的方法,操作简单、环境友好,具有广阔的工业化前景。
具体实施方式
[0027]
以下结合具体实施例对本发明作进一步说明,但下列实施例仅用于说明本发明,而不应视为限制本发明的范围。以下实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行,使用的方法如无特别说明,均为本领域公知的常规方法,使用的耗材和试剂如无特别说明,均为市场购得。除非另有说明,本文中所用的专业与科学术语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法或材料也可应用于本发明中。
[0028]
本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围显然不限于下述的实施例,(+)-6-甲氧基-α-甲基-2-萘甲基磷酸、(s,r)-alafosfalin、(r)-1-amino-3,4-dichlorobenzylphosphonic acid、(n)-methanocarba phosphonate analogues 5
’‑
amp、上述renin inhibitor(肾素抑制药)和anti-bacterial(抗菌剂)同样可以由本发明所述的方法合成。在以下实施例中,用“mol%”表示的是该物质相对于α-取代α,β-不饱和磷氧化物、磷酸酯、磷酸类化合物的摩尔百分比。
[0029]
实施例1:从diphenyl(1-phenylvinyl)phosphine oxide制备(s)-diphenyl(1-phenylethyl)phosphine oxide
[0030][0031]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到diphenyl(1-phenylvinyl)phosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-diphenyl(1-phenylethyl)phosphine oxide(99%产率),产物经hplc分析,测得ee值(97%ee)。1h nmr(400mhz,chloroform-d)δ7.92
–
7.85(m,2h),7.58
–
7.50(m,3h),7.47
–
7.42(m,2h),7.37
–
7.34(m,1h),7.28
–
7.27(m,1h),7.25
–
7.15(m,6h),3.64
–
3.56(m,1h),1.58(dd,j=16.1,7.4hz,3h).
13
c nmr(101mhz,chloroform-d)δ137.8(d,j=5.5hz),132.3(d,j=14.5hz),131.7(d,j=2.8hz),131.4,131.3(d,j=2.8hz),131.1(d,j
=8.7hz),129.2(d,j=5.5hz),128.6(d,j=11.2hz),128.23,128.22,128.0(d,j=11.5hz),126.9(d,j=2.5hz),40.9(d,j=67.1hz),15.4(d,j=2.9hz).
31
p nmr(162mhz,cdcl3)δ33.61.
[0032]
另外,将催化剂载量降至2mol%时,反应底物diphenyl(1-phenylvinyl)phosphine oxide的量由0.1mmol增加至0.5mmol也能反应完全,以95%收率和97%ee获得目标产物。
[0033]
实施例2:从(1-(4-fluorophenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(4-fluorophenyl)ethyl)diphenylphosphine oxide
[0034][0035]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(4-fluorophenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(4-fluorophenyl)ethyl)diphenylphosphine oxide(99%产率),产物经hplc分析,测得ee值(98%ee)。1h nmr(400mhz,chloroform-d)δ7.93
–
7.87(m,2h),7.59
–
7.50(m,3h),7.48
–
7.42(m,2h),7.39
–
7.35(m,1h),7.30
–
7.27(m,2h),7.20
–
7.16(m,2h),6.89
–
6.85(m,2h),3.63
–
3.55(m,1h),1.55(dd,j=16.0,7.3hz,3h).
13
c nmr(101mhz,cdcl3)δ161.8(d,j=243.9hz),133.5,132.3,132.0,131.83,131.80,131.42,131.40,131.4,131.33,131.27,131.1,131.0,130.9,130.7,130.60,130.57,130.52,128.8,128.7,128.2,128.1,115.23,115.21,115.01,114.99,40.1(d,j=67.1hz),15.5(d,j=2.9hz).(due to c-p and c-f coupling and the complexity of the spectrum,doublets in the aromatic region cannot be assigned and they are listed as singlets).
31
p nmr(162mhz,cdcl3)δ33.52.
[0036]
实施例3:从(1-(3-fluorophenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(3-fluorophenyl)ethyl)diphenylphosphine oxide
[0037][0038]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(3-fluorophenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(3-fluorophenyl)ethyl)diphenylphosphine oxide(94%产率),产物经hplc分析,测得ee值(96%ee)。1h nmr(400mhz,chloroform-d)δ7.92
–
7.87(m,2h),7.59
–
7.45(m,5h),7.40
–
7.35(m,1h),7.30
–
7.26(m,2h),7.16
–
7.11(m,1h),7.01
–
6.92
(m,2h),6.87
–
6.82(m,1h),3.63
–
3.56(m,1h),1.56(dd,j=15.9,7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ162.6(d,j=246.0hz),140.5(dd,j=7.5,5.5hz),132.1(d,j=20.6hz),131.9(d,j=2.9hz),131.5(d,j=2.8hz),131.3(d,j=8.5hz),131.1(d,j=16.5hz),131.0(d,j=8.8hz),129.6(dd,j=8.3,2.1hz),128.8(d,j=11.3hz),128.2(d,j=11.5hz),124.9(dd,j=5.6,2.9hz),116.1(dd,j=22.0,5.5hz),113.9(dd,j=21.0,2.6hz),40.8(dd,j=66.9,1.7hz),15.4(d,j=2.9hz).
31
p nmr(162mhz,cdcl3)δ33.12.hrms(esi):[c
20h18
fop+h
+
]calc.325.1152,found 325.1146.
[0039]
实施例4:从(1-(2-fluorophenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(2-fluorophenyl)ethyl)diphenylphosphine oxide
[0040][0041]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(2-fluorophenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(2-fluorophenyl)ethyl)diphenylphosphine oxide(98%产率),产物经hplc分析,测得ee值(98%ee)。1h nmr(400mhz,chloroform-d)δ7.97
–
7.92(m,2h),7.75
–
7.73(m,1h),7.48(m,5h),7.36
–
7.31(m,1h),7.27
–
7.22(m,2h),7.14
–
7.07(m,2h),6.82
–
6.77(m,1h),4.14
–
4.07(m,1h),1.54(dd,j=15.8,7.3hz,3h).
13
c nmr(101mhz,cdcl3)δ159.7(dd,j=245.0,6.8hz),132.3(d,j=11.3hz),131.8(d,j=2.6hz),131.4(d,j=2.9hz),131.2(d,j=8.6hz),130.7(d,j=8.9hz),130.3(d,j=3.7hz),128.7(d,j=11.2hz),128.3(dd,j=8.4,2.4hz),128.0(d,j=11.7hz),125.4(dd,j=245.0,5.0hz),124.4(d,j=3.4hz),114.7(dd,j=23.2,1.8hz),31.1(dd,j=69.0,2.3hz),14.8(d,j=2.9hz).
31
p nmr(162mhz,cdcl3)δ33.53.hrms(esi):[c
20h18
fop+h
+
]calc.325.1152,found325.114.
[0042]
实施例5:从diphenyl(1-(m-tolyl)vinyl)phosphine oxide制备(s)-diphenyl(1-(m-tolyl)ethyl)phosphine oxide
[0043][0044]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到diphenyl(1-(m-tolyl)vinyl)phosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-diphenyl(1-(m-tolyl)ethyl)phosphine oxide(99%产率),产物经hplc分析,测得ee值(96%ee)。1h nmr(400mhz,chloroform-d)δ7.91
–
7.86(m,2h),7.57
–
7.50
(m,3h),7.47
–
7.42(m,2h),7.38
–
7.34(m,1h),7.28
–
7.24(m,1h),7.24
–
7.18(m,1h),7.09
–
6.96(m,4h),3.60
–
3.53(m,1h),2.22(s,3h),1.56(dd,j=16.1,7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ137.8(d,j=2.2hz),137.6(d,j=5.6hz),132.3(d,j=9.9hz),131.7(d,j=2.7hz),131.4(d,j=8.2hz),131.3(d,j=2.5hz),131.2(d,j=8.8hz),129.9(d,j=5.4hz),128.6(d,j=11.2hz),128.1(d,j=2.1hz),127.9(d,j=11.6hz),127.6(d,j=2.6hz),126.2(d,j=5.5hz),40.9(d,j=67.2hz),21.3,15.3(d,j=2.8hz).
31
p nmr(162mhz,cdcl3)δ33.78.
[0045]
实施例6:从(1-(4-methoxyphenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(4-methoxyphenyl)ethyl)diphenylphosphine oxide
[0046][0047]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(4-methoxyphenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(4-methoxyphenyl)ethyl)diphenylphosphine oxide(95%产率),产物经hplc分析,测得ee值(94%ee)。1h nmr(400mhz,chloroform-d)δ7.91
–
7.86(m,2h),7.55
–
7.43(m,5h),7.39
–
7.34(m,1h),7.29
–
7.26(m,2h),7.13
–
7.11(m,2h),6.74
–
6.72(m,2h),3.75(s,3h),3.60
–
3.53(m,1h),1.54(dd,j=16.1,7.3hz,3h).
13
c nmr(101mhz,cdcl3)δ158.5(d,j=2.5hz),131.7(d,j=2.4hz),131.4(d,j=9.0hz),131.2(d,j=8.9hz),130.2(d,j=5.4hz),129.5(d,j=5.7hz),128.6(d,j=11.2hz),128.1(d,j=11.5hz),127.9,113.7(d,j=2.0hz),55.1,40.9(d,j=67.3hz),15.5(d,j=2.4hz).
31
p nmr(162mhz,cdcl3)δ33.76.
[0048]
实施例7:从diphenyl(1-(4-(trifluoromethyl)phenyl)vinyl)phosphine oxide制备(s)-diphenyl(1-(4-(trifluoromethyl)phenyl)ethyl)phosphine oxide
[0049][0050]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到diphenyl(1-(4-(trifluoromethyl)phenyl)vinyl)phosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-diphenyl(1-(4-(trifluoromethyl)phenyl)ethyl)phosphine oxide(99%产率),产物经hplc分析,测得ee值(96%ee)。1h nmr(400mhz,chloroform-d)δ7.93
–
7.88(m,2h),7.60
–
7.51(m,3h),7.49
–
7.42(m,4h),7.40
–
7.33(m,3h),7.30
–
7.28(m,2h),3.71
–
3.63(m,1h),1.58(dd,j=15.9,7.3hz,3h).
13
c nmr
(101mhz,cdcl3)δ142.2(d,j=5.4hz),131.92(d,j=2.7hz),131.90(d,j=30.9hz),131.6(d,j=2.8hz),131.3(d,j=8.6hz),131.1,130.9(d,j=27.6hz),130.8,129.4(d,j=5.3hz),128.8(d,j=11.3hz),128.2(d,j=11.5hz),124.1(q,j=273.2hz),125.1(m),40.8(d,j=65.8hz),15.3(d,j=2.9hz).
31
p nmr(162mhz,cdcl3)δ32.93.
[0051]
实施例8:从(1-(4-pentylphenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(4-pentylphenyl)ethyl)diphenylphosphine oxide
[0052][0053]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(4-pentylphenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(4-pentylphenyl)ethyl)diphenylphosphine oxide(99%产率),产物经hplc分析,测得ee值(97%ee)。1h nmr(400mhz,chloroform-d)δ7.91
–
7.86(m,2h),7.57
–
7.50(m,3h),7.45
–
7.40(m,2h),7.37
–
7.33(m,1h),7.25
–
7.22(m,2h),7.11
–
6.98(m,4h),3.61
–
3.53(m,1h),2.51(t,j=7.7hz,2h),1.59
–
1.51(m,3h),1.32
–
1.22(m,6h),0.88(t,j=7.0hz,3h).
13
c nmr(101mhz,chloroform-d)δ141.5(d,j=2.7hz),134.7(d,j=5.7hz),132.4(d,j=20.0hz),131.7(d,j=2.7hz),131.4(d,j=15.7hz),131.4(d,j=8.4hz),131.22,131.2(d,j=6.2hz),129.0(d,j=5.4hz),128.6(d,j=11.1hz),128.3(d,j=2.1hz),127.9(d,j=11.5hz),40.5(d,j=67.2hz),35.4,31.3,31.0,22.5,15.3(d,j=2.6hz),14.0.
31
p nmr(162mhz,cdcl3)δ33.87.
[0054]
实施例9:从(1-(4-butylphenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(4-butylphenyl)ethyl)diphenylphosphine oxide
[0055][0056]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(4-butylphenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(4-butylphenyl)ethyl)diphenylphosphine oxide(99%产率),产物经hplc分析,测得ee值(99%ee)。1h nmr(400mhz,chloroform-d)δ7.91
–
7.86(m,2h),7.58
–
7.49(m,3h),7.44
–
7.33(m,3h),7.25
–
7.14(m,2h),7.10
–
6.98(m,4h),3.61
–
3.53(m,1h),2.52(t,j=7.7hz,2h),1.59
–
1.49(m,2h),1.34
–
1.25(m,1h),0.90(t,j=7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ141.5(d,j=2.9hz),134.7(d,j=5.8hz),132.4(d,j=20.5hz),131.6(d,j=2.7hz),131.4(d,j=8.3hz),131.2,131.1,129.0(d,j=5.4hz),
128.6(d,j=11.1hz),128.3(d,j=2.2hz),127.9(d,j=5.1hz),127.85,40.5(d,j=67.0hz),35.1,33.4,22.2,15.3(d,j=2.8hz),13.9.
31
p nmr(162mhz,cdcl3)δ33.88.
[0057]
实施例10:从(1-(4-ethylphenyl)vinyl)diphenylphosphine oxide制备(s)-(1-(4-ethylphenyl)ethyl)diphenylphosphine oxide
[0058][0059]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(4-ethylphenyl)vinyl)diphenylphosphine oxide(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(4-ethylphenyl)ethyl)diphenylphosphine oxide(95%产率),产物经hplc分析,测得ee值(98%ee)。1h nmr(400mhz,chloroform-d)δ7.91
–
7.86(m,2h),7.57
–
7.43(m,5h),7.38
–
7.34(m,1h),7.31
–
7.26(m,1h),7.25
–
7.20(m,1h),7.12
–
7.00(m,4h),3.62
–
3.55(m,1h),2.56(q,j=7.6hz,2h),1.56(dd,j=16.2,7.4hz,3h),1.17(t,j=7.6hz,3h).
13
c nmr(101mhz,chloroform-d)δ142.9(d,j=2.8hz),134.8(d,j=5.6hz),132.4(d,j=12.1hz),131.6(d,j=2.7hz),131.5(d,j=7.7hz),131.4(d,j=5.0hz),131.22,131.19,129.1(d,j=5.4hz),128.6(d,j=11.0hz),128.0(d,j=11.5hz),127.7(d,j=2.1hz),40.4(d,j=67.0hz),28.4,15.5,15.4(d,j=2.7hz).
31
p nmr(162mhz,cdcl3)δ33.78.hrms(esi):[c
22h23
op+h
+
]calc.335.1560,found 335.1553.
[0060]
实施例11:从(1,3-phenylenebis(ethene-1,1-diyl))bis(diphenylphosphine oxide)制备((1r,1'r)-1,3-phenylenebis(ethane-1,1-diyl))bis(diphenylphosphine oxide)
[0061][0062]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1,3-phenylenebis(ethene-1,1-diyl))bis(diphenylphosphine oxide)(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品((1r,1'r)-1,3-phenylenebis(ethane-1,1-diyl))bis(diphenylphosphine oxide)(99%产率),产物经hplc分析,测得ee值(》99%ee)。1h nmr(400mhz,chloroform-d)δ7.89
–
7.84(m,4h),7.56
–
7.48(m,6h),7.41
–
7.36(m,4h),7.32
–
7.28(m,3h),7.23
–
7.18(m,4h),7.10
–
7.05(m,2h),6.99
ꢀ‑
6.95(m,1h),3.57
–
3.50(m,2h),1.49(dd,j=16.1,7.3hz,1h),
13
c nmr(101mhz,chloroform-d)δ138.2(d,j=5.7hz),132.2(d,j=3.7hz),131.7(d,j=2.5hz),131.32,131.3,131.23,131.1(d,j=8.9hz),130.1(d,j=5.8hz),128.6(d,j=11.3hz),128.4,128.2(d,j=11.7hz),127.8(d,j=5.3hz),40.6
(d,j=67.5hz),15.8(d,j=2.8hz).
31
p nmr(162mhz,cdcl3)δ34.25.
[0063]
实施例12:从dimethyl(1-(o-tolyl)vinyl)phosphonate制备dimethyl(s)-(1-(o-tolyl)ethyl)phosphonate
[0064][0065]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-(o-tolyl)vinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-(o-tolyl)ethyl)phosphonate(99%产率),产物经hplc分析,测得ee值(96%ee)。1h nmr(400mhz,chloroform-d)δ7.48
–
7.46(m,1h),7.23
–
7.12(m,3h),3.69(d,j=10.6hz,3h),3.49(d,j=10.3hz,3h),3.56
–
3.40(m,1h),2.37(s,3h),1.56(dd,j=18.7,7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ136.2(d,j=8.2hz),136.0(d,j=6.6hz),130.4(d,j=2.5hz),127.8(d,j=4.7hz),126.9(d,j=3.2hz),126.3(d,j=3.2hz),53.3(d,j=6.9hz),52.8(d,j=7.4hz),33.1(d,j=138.4hz),19.9,15.8(d,j=5.0hz).
31
p nmr(162mhz,cdcl3)δ32.86.
[0066]
实施例13:从dimethyl(1-(4-chlorophenyl)vinyl)phosphonate制备dimethyl(s)-(1-(4-chlorophenyl)ethyl)phosphonate
[0067][0068]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-(4-chlorophenyl)vinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-(4-chlorophenyl)ethyl)phosphonate(95%产率),产物经hplc分析,测得ee值(90%ee)。1h nmr(400mhz,chloroform-d)δ7.30
–
7.26(m,4h),3.67(d,j=10.7hz,3h),3.54(d,j=10.6hz,3h),3.21
–
3.10(m,1h),1.55(dd,j=18.5,7.4hz,3h).
13
c nmr(101mhz,chloroform-d)δ136.2(d,j=7.0hz),133.0(d,j=3.9hz),129.9(d,j=6.6hz),128.7(d,j=2.9hz),53.4(d,j=7.0hz),52.9(d,j=7.2hz),37.4(d,j=138.6hz),15.4(d,j=5.2hz).
31
p nmr(162mhz,cdcl3)δ31.45.
[0069]
实施例14:从dimethyl(1-(2-chlorophenyl)vinyl)phosphonate制备dimethyl(s)-(1-(2-chlorophenyl)ethyl)phosphonate
[0070]
[0071]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-(2-chlorophenyl)vinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-(2-chlorophenyl)ethyl)phosphonate(97%产率),产物经hplc分析,测得ee值(84%ee)。1h nmr(400mhz,chloroform-d)δ7.62
–
7.59(m,1h),7.39
–
7.36(m,1h),7.29
–
7.27(m,1h),7.21
–
7.16(m,1h),3.97
–
3.86(m,1h),3.75(d,j=10.7hz,3h),3.54(d,j=10.6hz,3h)1.56(dd,j=18.4,7.4hz,3h).
13
c nmr(101mhz,chloroform-d)δ135.8(d,j=5.5hz),133.9(d,j=10.0hz),129.6(d,j=4.7hz),129.5(d,j=2.2hz),128.3(d,j=3.0hz),127.1(d,j=2.9hz),53.2(d,j=7.0hz),52.9(d,j=7.0hz),33.3(d,j=140.6hz),15.7(d,j=5.2hz).
31
p nmr(162mhz,cdcl3)δ31.73.
[0072]
实施例15:从dimethyl(1-phenylvinyl)phosphonate制备dimethyl(s)-(1-phenylethyl)phosphonate
[0073][0074]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-phenylvinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-phenylethyl)phosphonate(98%产率),产物经hplc分析,测得ee值(93%ee)。1h nmr(400mhz,chloroform-d)δ7.36
–
7.25(m,5h),3.62(d,j=10.6hz,3h),3.46(d,j=10.5hz,3h),3.26
–
3.09(m,1h),1.58(dd,j=18.6,7.4hz,3h).
13
c nmr(101mhz,chloroform-d)δ137.6(d,j=6.9hz),128.6(d,j=8.9hz),128.5,127.2(d,j=3.2hz),53.3(d,j=6.9hz),52.8(d,j=7.2hz),38.0(d,j=137.7hz),15.5(d,j=5.1hz).
31
p nmr(162mhz,cdcl3)δ32.16.
[0075]
实施例16:从dimethyl(1-(naphthalen-1-yl)vinyl)phosphonate制备dimethyl(s)-(1-(naphthalen-1-yl)ethyl)phosphonate
[0076][0077]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-(naphthalen-1-yl)vinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-(naphthalen-1-yl)ethyl)phosphonate(99%产率),产物经
hplc分析,测得ee值(86%ee)。1h nmr(400mhz,chloroform-d)δ8.09
–
8.07(m,1h),7.88
–
7.86(m,1h),7.80
–
7.78(m,1h),7.71
–
7.68(m,1h),7.57
–
7.48(m,3h),4.22
–
4.08(m,1h),3.69(d,j=10.7hz,3h),3.37(d,j=10.5hz,3h),1.71(dd,j=18.5,7.3hz,3h).
13
c nmr(101mhz,chloroform-d)δ133.8(d,j=1.9hz),133.6(d,j=6.6hz),131.5(d,j=7.2hz),129.0,127.8(d,j=3.6hz),126.3,126.0(d,j=6.4hz),125.6,125.5(d,j=3.7hz),122.9,53.4(d,j=7.0hz),52.9(d,j=7.6hz),31.9(d,j=137.5hz),16.2(d,j=5.3hz),
31
p nmr(162mhz,cdcl3)δ32.45.
[0078]
实施例17:从制备dimethyl(1-cyclohexylvinyl)phosphonate制备dimethyl(s)-(1-cyclohexylethyl)phosphonate
[0079][0080]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(1-cyclohexylvinyl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-cyclohexylethyl)phosphonate(99%产率),产物经hplc分析,测得ee值(97%ee)。1h nmr(400mhz,chloroform-d)δ3.74(s,3h),3.72(s,3h),1.82
–
1.74(m,3h),1.66
–
1.59(m,2h),1.29
–
1.22(m,5h),1.15
–
1.09(m,3h),0.92
–
0.81(m,2h).
13
c nmr(101mhz,chloroform-d)δ52.3(d,j=6.8hz),52.2(d,j=7.1hz),37.5(d,j=2.6hz),36.2(d,j=137.1hz),31.9(d,j=13.6hz),28.8(d,j=3.6hz),26.3(d,j=23.7hz),9.5(d,j=4.7hz).
31
p nmr(162mhz,cdcl3)δ37.25.
[0081]
实施例18:从dimethyl(e)-(1-phenylprop-1-en-1-yl)phosphonate制备dimethyl(s)-(1-phenylpropyl)phosphonate
[0082][0083]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到dimethyl(e)-(1-phenylprop-1-en-1-yl)phosphonate(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品dimethyl(s)-(1-phenylpropyl)phosphonate(95%产率),产物经hplc分析,测得ee值(97%ee)。1h nmr(400mhz,chloroform-d)δ7.35
–
7.27(m,5h),3.64(d,j=10.6hz,3h),3.42(d,j=10.4hz,3h),2.97
–
2.87(m,1h),2.24
–
1.89(m,2h),0.85(t,j=7.4hz,3h).
13
c nmr(101mhz,chloroform-d)δ135.8(d,j=6.7hz),129.2(d,j=6.9hz),128.5(d,j=2.5hz),127.2(d,j=3.1hz),53.3(d,j=7.0hz),52.6(d,j=7.3hz),46.1(d,j=136.5hz),23.1(d,j=3.4hz),12.4(d,j=16.1hz).
31
p nmr(162mhz,cdcl3)δ31.36.
[0084]
实施例19:从(1-(o-tolyl)vinyl)phosphonic acid制备(s)-(1-(o-tolyl)ethyl)phosphonic acid
[0085][0086]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(o-tolyl)vinyl)phosphonic acid(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(o-tolyl)ethyl)phosphonic acid(99%产率),产物经hplc分析,测得ee值(98%ee)。
[0087]
实施例20:从(1-(naphthalen-1-yl)vinyl)phosphonic acid制备(s)-(1-(naphthalen-1-yl)ethyl)phosphonic acid
[0088][0089]
在高纯氩气氛围下,将ni(oac)2(14.14mg,0.08mmol)和手性配体(s,s)-ph-bpe(44.58mg,0.088mmol)溶于无水六氟异丙醇(7.2ml)和无水甲醇(0.8ml)中,在15~35℃条件下搅拌36小时,得到澄清溶液。取250μl澄清溶液加入到(1-(naphthalen-1-yl)vinyl)phosphonic acid(0.1mmol)、六氟异丙醇(0.75ml)中。将反应体系置于高压釜中,在70℃和h2(70atm)条件下搅拌36小时。减压除去溶剂,柱层析分离(采取硅胶柱,洗脱剂:乙酸乙酯),得纯品(s)-(1-(naphthalen-1-yl)ethyl)phosphonic acid(99%产率),产物经hplc分析,测得ee值(92%ee)。
[0090]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1