一种7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛的制备方法与流程
1.本发明涉及精细化工合成技术领域,具体涉及一种7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛的制备方法。
背景技术:
2.7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛(以下简称c10醛酯)是c20+c10路线合成8
’‑
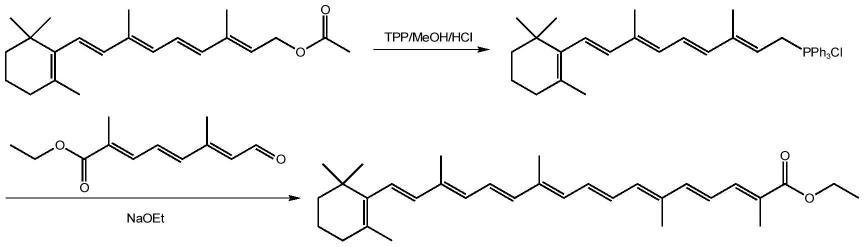
阿朴-β-胡萝卜酸乙酯(以下简称“阿朴酯”)的关键中间体。阿朴酯的该合成路线如式1所示,维生素a醋酸酯与三苯基膦、盐酸生成c20中间体后,继续与c10醛酯发生wittig反应,即可得到阿朴酯产品。
[0003][0004]
式1、阿朴酯的c20+c10合成路线
[0005]
根据文献和专利的报道,c10醛酯的合成方法主要有以下两种:
[0006]
(1)以roche维生素a醋酸酯的c14+c6路线副产物反式c6为原料,经过格氏、部分加氢,水解、wittig-horner以及氧化反应,一共五步反应得到c10醛酯(us3989758a、us3687990)。其合成路线如式2所示。
[0007][0008]
式2、c10醛酯的反式c6合成路线
[0009]
该方法使用了维生素a醋酸酯的副产物反式c6作为原料,比较经济。然而反应路线比较长,一共有五步反应,原子经济性比较差。工艺涉及格氏反应、部分加氢反应,wittig-horner反应,比较复杂。由于反式c6非常不稳定,在格氏反应中容易聚合,难以控制,反应收率很低,因此,路线总的收率也比较低。而且wittig-horner反应产生大量的含磷废水,处理成本较高。
[0010]
(2)以basf维生素a醋酸酯的c15+c5路线的c5作为原料,经过氧化、酯化水解、氯代、膦酯化、wittig-horner、氧化反应,一共六步反应得到c10醛酯(cn201210364500.4)其
合成路线如式3所示。
[0011][0012]
式3、c10醛酯的c5合成路线
[0013]
该方法与basf维生素a醋酸酯路线使用同样的原料c5,比较易得。然而反应路线比较长,一共有六步反应,原子经济性比较差,总反应收率偏低。工艺涉及氧化、氯代、膦酯化、wittig-horner反应,比较复杂。而且氧化步骤和wittig-horner反应都会产生大量的含磷废水,处理成本偏高。
[0014]
综述所述,c10醛酯的现有合成路线都存在以下缺点:
[0015]
(1)反应路线长,原子经济性差;
[0016]
(2)工艺复杂,总反应收率偏低;
[0017]
(3)需要处理大量的含磷废水,处理成本高。
[0018]
因此,本发明所要解决的是开发一条路线短,工艺简单、收率高,不产生的含磷废水的绿色环保的c10醛酯合成工艺。
技术实现要素:
[0019]
本发明所要解决的技术问题为:本发明提供了一种7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛的制备方法,该制备方法原料便宜易得,反应路线短,只需两步反应,收率高,原子经济性高;而且不产生含磷废水,大大降低了生产成本,能很好的解决c10醛酯的现有合成路线存在的缺点,带来较大的环保效益和经济效益,并且可以实现工业化生产。
[0020]
本发明的技术方案如下:
[0021]
一种7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛的制备方法,包括以下步骤:
[0022]
(1)在双催化剂的存在下,(e)-3-甲基戊-2-烯-4-炔-1-醇和甲基丙烯酸酯进行氢烯基化偶联反应得到c10醇酯;
[0023]
所述的双催化剂由铜催化剂和酸组成;
[0024]
(2)c10醇酯在tempo催化氧化体系中进行氧化反应,反应结束后经过后处理得到所述的7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛;
[0025]
所述的tempo催化氧化体系由tempo和助剂组成;
[0026]
反应式如下:
[0027][0028]
作为优选,步骤(1)中,所述的铜催化剂为亚铜盐,选自cu2so4,cucl,cubr,cuno3,cuac中的一种或者多种,进一步优选cu2so4,cuno3中的一种或者两种。cu2so4和cuno3效果比较理想,与亚铜的卤盐相比副反应更少,反应总收率更高。
[0029]
增加反应体系酸性有利于中间体c10醇酯的合成,作为优选,步骤(1)中,所述的酸选自hcl、hbr、硫酸、硝酸、磷酸、三氟乙酸中的一种或者多种,进一步优选为硫酸、磷酸、三氟乙酸中的一种或者多种。同盐酸、氢溴酸相比,硫酸、磷酸、三氟乙酸的副反应更少,三氟乙酸效果最为理想。
[0030]
作为优选,步骤(1)中,所述的氢烯基化偶联反应在以下溶剂中的一种或者多种中进行:
[0031]
苯、甲苯、二甲苯、三甲苯、庚烷、已烷、辛烷、二氯甲烷、三氯甲烷、氯仿或二氯乙烷等惰性溶剂,其中甲苯、二氯甲烷具有较好的经济效益和实验验证结果,进一步优选为甲苯或二氯甲烷。
[0032]
步骤(1)中,反应结束之后,后处理过程如下:
[0033]
用去离子水对反应液进行洗涤,除去催化剂,有机层用无水硫酸钠干燥,得到中间体c10醇酯溶液直接进入步骤(2)进行氧化反应。
[0034]
作为优选,步骤(2)中,所述的助剂为亚铜盐、三价铁盐或i2;其中,tempo/亚铜盐体系氧化效果比较理想,因此进一步优选tempo/亚铜盐体系,所述的亚铜盐为cu2so4,cucl,cubr,cuno3或cuac。
[0035]
作为优选,步骤(2)中,所述氧化反应的溶剂为:苯、甲苯、二甲苯、三甲苯、庚烷、已烷、辛烷、二氯甲烷、三氯甲烷、氯仿、二氯乙烷等惰性溶剂中的一种或者多种,其中甲苯、二氯甲烷具有较好的经济效益和实验验证结果,进一步优选甲苯或二氯甲烷。进一步地,步骤(2)氧化反应的溶剂与步骤(1)的氢烯基化偶联反应相同,步骤(1)的反应结束之后,反应溶剂可以不除去。
[0036]
作为优选,所述的后处理为重结晶,重结晶的溶剂选用醚类溶剂,c10醛酯在醚类溶剂中有一定的溶解度,且对温度敏感。作为进一步的优选,重结晶的溶剂可选择:甲醚、乙醚、异丙醚、叔丁基醚、异丁基醚、甲基叔丁基醚等,进一步异丙醚、甲基叔丁基醚具有较好的经济效益和实验验证结果。
[0037]
进一步的,本发明的7-烷氧羰基-3,7-二甲基-2,4,6-庚三烯醛的具体制备方法如下:
[0038]
(1)带搅拌、冷却回流装置的500ml四口烧瓶反应装置,置于低温循环槽内,先加入溶剂100g,60g甲基丙烯酸乙酯,催化剂m(铜催化剂)0.1-0.5g,催化剂l(酸催化剂)0.05-0.5g,常温条件下(25
±
2℃),缓慢滴加预冷至0-5℃的50g反式c6+50g溶剂混合液,在滴加过程中,反应体系温度上升,控温反应体系温度35-40℃,滴完保温30min。gc检测,甲基丙烯酸乙酯残留≤0.2%,视为合格。反应液加去离子水洗涤3次,100ml/次,除去催化剂m+l。有机层用无水硫酸钠干燥,得到中间体c10醇酯溶液;
[0039]
(2)在高压釜中加入c10醇酯溶液,0.1g tempo/0.1g助剂体系催化剂,控温30-80℃,搅拌下通入氧气/压缩空气,控压0.01-0.5mpa,反应10h。取样hplc检测,中间体c10醇酯
残留合格,停反应。氧化反应液加去离子水洗涤3次,100ml/次,除去催化剂。有机层c10醛酯溶液减压浓缩,浓缩温度≤80℃,回收溶剂。加300g结晶溶剂结晶,冷却至-10
±
1℃,析出c10醛酯粗品。c10醛酯粗品加入1.5-2倍量质量比的结晶溶剂,升温到回流30min,缓慢降温至-5
±
1℃,析晶2-4h,过滤,-0.1mpa,45-60℃,烘干,得到c10醛酯精品。
[0040]
与现有技术相比,本发明有如下优点:
[0041]
(1)本发明的反应路线短,两步反应就能得到目标产品,并且收率高,原子经济性好;
[0042]
(2)本发明的工艺简单,反应条件温和,设备投资小;
[0043]
(3)本发明的原料易得,有效利用了维生素a醋酸酯生产废料反式c6;生产过程无含磷废水,对环境友好。
具体实施方式
[0044]
c10醛酯的一般制备过程如下:
[0045]
(1)带搅拌、冷却回流装置的500ml四口烧瓶反应装置,置于低温循环槽内,先加入溶剂100g,60g甲基丙烯酸乙酯,催化剂m0.1g,催化剂l0.05g,常温条件下(25
±
2℃),缓慢滴加预冷至0-5℃的50g反式c6+50g甲苯混合液,在滴加过程中,反应体系温度上升,控温反应体系温度35~40℃,滴完保温30min。gc检测合格后。反应液加去离子水洗涤3次,100ml/次,除去催化剂m+l。有机层用无水硫酸钠干燥,检测水份≤100ppm,得到中间体c10醇酯溶液。
[0046]
(2)在高压釜中加入c10醇酯溶液,0.1gtempo/0.1g助剂体系催化剂,控温30-40℃,搅拌下通入压缩空气,控压0.1-0.5mpa,反应8-10h。取样hplc检测,中间体1c10醇酯残留≤0.5%,视为合格。停反应。反应液加去离子水洗涤3次,100ml/次,除去催化剂。有机层c10醛酯溶液减压浓缩,浓缩温度≤80℃,回收溶剂。加300g结晶溶剂结晶,冷却至-10
±
1℃,析出c10醛酯粗品。c10醛酯粗品加入1.5-2倍量质量比的异丙醚,升温到回流30min,缓慢降温至-5
±
1℃,析晶2-4h,过滤,-0.1mpa,45-60℃,烘干,得到c10醛酯精品,hplc检测纯度,以反式c6计算摩尔收率。
[0047]
下面结合具体实施例对本发明作进一步说明,但本发明的保护范围不限于此。
[0048]
实施例1-30
[0049]
实验设计催化剂m+l正交实验表(如下表),催化剂m+l投料量0.1g+0.05g,c10醇酯氧化催化体系0.1g tempo/0.1g助剂m(实施例中氧化反应的m选择与氢烯基化偶联反应相同),实验效果hplc检测纯度,以反式c6计c10醛酯的摩尔收率。
[0050][0051]
实验结果统计如下:
[0052][0053][0054]
实施例31-41
[0055]
不同反应溶剂,催化剂cu2so4+三氟乙酸:投料量0.1g+0.05g,c10醇酯氧化催化体系0.1g tempo/0.1g cu2so4,结晶溶剂异丙醚,实验效果hplc检测纯度,以反式c6计c10醛酯
的摩尔收率。实验结果如下:
[0056]
实验序号实验方案(反应溶剂)结晶溶剂产品纯度(%)摩尔收率(%)实例31苯异丙醚99.2193.98实例32甲苯异丙醚99.6095.77实例33二甲苯异丙醚99.3394.75实例34三甲苯异丙醚99.2993.28实例35庚烷异丙醚99.3192.79实例36已烷异丙醚98.7892.57实例37辛烷异丙醚98.5693.22实例38二氯甲烷异丙醚99.0492.35实例39三氯甲烷异丙醚98.5691.89实例40氯仿异丙醚99.0292.37实例41二氯乙烷异丙醚99.2393.26
[0057]
实施例42-44
[0058]
反应溶剂为甲苯,催化剂cu2so4+三氟乙酸:投料量0.1g+0.05g,不同的c10醇酯氧化催化体系,c10醇酯氧化催化体系0.1g tempo/0.1g助剂;结晶溶剂为异丙醚,实验效果hplc检测纯度,以反式c6计c10醛酯的摩尔收率。实验结果如下:
[0059][0060]
实施例45-50
[0061]
反应溶剂为甲苯,催化剂cu2so4+三氟乙酸:投料量0.1g+0.05g,c10醇酯氧化催化体系0.1g tempo/0.1g cu2so4,不同结晶溶剂,实验效果hplc检测纯度,以反式c6计c10醛酯的摩尔收率。实验结果如下:
[0062]
实验序号实验方案(结晶溶剂)反应溶剂产品纯度(%)摩尔收率(%)实例45甲醚甲苯98.9794.57实例46乙醚甲苯99.2394.50实例47异丙醚甲苯99.6795.82实例48叔丁基醚甲苯98.2693.29实例49异丁基醚甲苯98.5790.37实例50甲基叔丁基醚甲苯97.5290.41
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1