一种三氟甲基极化烯烃化合物及其制备方法
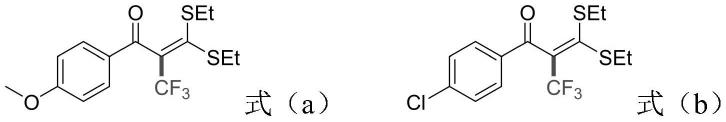
1.本发明属于有机合成化学技术领域,具体涉及一种三氟甲基极化烯烃化合物及其制备方法。
背景技术:
2.向药物分子框架中引入氟烷基可以显著改变其亲脂性、亲和力及代谢稳定性等(chem.soc.rev.2007,37,320
–
330.)。近些年以来,开发将氟烷基,特别是三氟甲基(cf3)引入有机分子中的方法引起了化学家们的广泛关注(chem.rev.2011,111,4475
–
4521.)。向极化烯烃中引入三氟甲基,以二硫缩烯酮为例,目前所用方法大都通过传统合成,即通过特殊的三氟甲基化试剂(org.lett.2018,20,3933-3937),或通过三氟甲基三甲基硅烷与多种添加剂结合的方式(chem.eur.j.2014,20,3439
–
3445)。利用光催化反应向其中引入三氟甲基的方法符合绿色合成发展理念,但至今鲜有报道。而通过co金属配合物调制的向极化烯烃中引入三氟甲基的反应也还待开发。
技术实现要素:
3.本发明的目的是为了提供一种三氟甲基极化烯烃化合物及其制备方法,该方法以co金属配合物为介导,利用绿色可持续发展的可见光能源,以实现温和、高效地向极化烯烃中引入三氟甲基,合成三氟甲基化极化烯烃。
4.为实现上述发明目的,本发明首先采用以下技术方案:
5.本发明首先提供一种三氟甲基极化烯烃化合物,结构式如式ⅰ所示:
[0006][0007]
式ⅰ中,r为甲氧基、氯或溴。
[0008]
本发明还提供一种三氟甲基极化烯烃化合物的制备方法,包括:
[0009]
向光反应管中加入式ⅱ所示的二硫缩烯酮、togni试剂、[co(ii)salen]配合物与光敏剂ir(ppy)3,随后在n2气氛中加入溶剂以及二异丙基乙胺,将光反应管置于蓝光led灯下照射反应后,分离纯化得到式ⅰ所示的三氟甲基极化烯烃化合物。
[0010][0011]
优选的是,所述的反应温度为25-30℃,反应时间为12-16h。
[0012]
优选的是,所述的蓝光led光源的光强为30w。
[0013]
优选的是,所述的式ⅱ所示的二硫缩烯酮与togni试剂的摩尔比为1:1.5。
[0014]
优选的是,所述的式ⅱ所示的二硫缩烯酮、二异丙基乙胺、[co(ii)salen]配合物、ir(ppy)3的摩尔比为1:2:(0.05~0.10):0.05。
[0015]
优选的是,所述的溶剂为甲醇。
[0016]
本发明的有益效果
[0017]
本发明提供一种三氟甲基极化烯烃化合物及其制备方法,该化合物的结构式如式ⅰ所示,该化合物是在蓝光led照射条件下,使光敏剂ir(ppy)3变为激发态,随后激发二异丙基乙胺,伴随着ir(ⅲ)转变为ir(ⅳ)。[co(ii)salen]配合物与生成的ir(ⅳ)发生单电子转移过程生成co(i)配合物,作为亲电性三氟甲基源的togni试剂与co(i)配合物结合生成[co(ⅲ)salen]配合物。由[co(ⅲ)salen]配合物进一步产生三氟甲基自由基和起始的[co(ii)salen]配合物。三氟甲基自由基与二硫缩烯酮结合,经氧化/去质子化反应得到目标三氟甲基化产物α-三氟甲基二硫缩烯酮。
[0018]
本发明的方法以简单易得的代表性极化烯烃二硫缩烯酮和togni试剂为原料,在光催化条件下,向反应体系中引入了三氟甲基,合成了一类α-三氟甲基二硫缩烯酮。与现有技术相对比,本发明具有原料廉价易得、方法简洁、后处理简单、反应条件温和、绿色实用等优点。
附图说明
[0019]
图1为本发明实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氢谱图;
[0020]
图2为本发明实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振碳谱图;
[0021]
图3为本发明实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氟谱图;
[0022]
图4为本发明实施例2制备得到的α-三氟甲基二硫缩烯酮化合物b的核磁共振氢谱图;
[0023]
图5为本发明实施例2制备得到的α-三氟甲基二硫缩烯酮化合物b的核磁共振碳谱图;
[0024]
图6为本发明实施例2制备得到的α-三氟甲基二硫缩烯酮化合物b的核磁共振氟谱图;
[0025]
图7为本发明实施例3制备得到的α-三氟甲基二硫缩烯酮化合物c的核磁共振氢谱图;
[0026]
图8为本发明实施例3制备得到的α-三氟甲基二硫缩烯酮化合物c的核磁共振碳谱图;
[0027]
图9为本发明实施例3制备得到的α-三氟甲基二硫缩烯酮化合物c的核磁共振氟谱图。
具体实施方式
[0028]
本发明首先提供一种三氟甲基极化烯烃化合物,结构式如式ⅰ所示:
[0029][0030]
式ⅰ中,r为甲氧基、氯或溴。优选结构如式(a)、式(b)、式(c)的结构:
[0031][0032][0033]
本发明还提供一种三氟甲基极化烯烃化合物的制备方法,包括:
[0034]
向光反应管中加入式ⅱ所示的二硫缩烯酮、togni试剂(3,3-二甲基-1-(三氟甲基)-1,2-苯并碘氧杂戊环)、[co(ii)salen]配合物(salen:n.n’亚乙基双(水杨基亚胺))与光敏剂ir(ppy)3,随后在n2气氛中加入溶剂以及二异丙基乙胺,将光反应管置于蓝光led灯下照射反应后,所述的反应温度优选为25-30℃,反应时间优选为12-16h,蓝光led光源的光强优选为30w,分离纯化得到式ⅰ所示的三氟甲基极化烯烃化合物。所述的式ⅱ所示的二硫缩烯酮与togni试剂的摩尔比优选为1:1.5;式ⅱ所示的二硫缩烯酮、二异丙基乙胺、[co(ii)salen]配合物、ir(ppy)3的摩尔比优选为1:2:(0.05~0.10):0.05。
[0035][0036]
反应式如下:
[0037][0038]
按照本发明,所述的式ⅱ所示的二硫缩烯酮的制备包括:
[0039]
向反应瓶中加入碳酸钾与r取代的苯乙酮,将其溶解于溶剂中,所述的溶剂优选为n,n-二甲基甲酰胺,优选在冰水浴中搅拌,0.5小时后,向反应体系中加入二硫化碳;1小时后,向体系中加入溴乙烷,加料完毕后,撤除冰水浴(0℃),置于室温下搅拌过夜。所述的r取代的苯乙酮投料为10mmol,各反应物的摩尔比为:r取代的苯乙酮/二硫化碳/氢化钠/溴乙烷=1/1.5/1.5/2.2。12小时后,将反应体系通过柱层析(石油醚/乙酸乙酯=10/1)分离得
到目标产物,产率:75~85%。
[0040]
本发明在可见光照射下、以二异丙基乙胺和[co(ii)salen]配合物为添加剂、以甲醇作溶剂、ir(ppy)3(ppy:三(2-苯基吡啶)合铱)为光敏剂,二硫缩烯酮与togni试剂的反应,以合成α-三氟甲基二硫缩烯酮。该方法实现了极化烯烃二硫缩烯酮的三氟甲基化反应,合成了多例三氟甲基化极化烯烃。本发明具有原料廉价易得、方法简洁、反应条件温和、绿色实用的优点。
[0041]
下面结合具体实施例对本发明做进一步详细的说明,实施例中涉及到的原料二硫缩烯酮为由商购原料的简单制备,其余原料均为商购获得。
[0042]
实施例1:的制备
[0043]
向35ml光反应管中加入3,3-双(乙硫基)-1-(4-甲氧基苯基)丙-2-烯-1-酮、togni试剂、[co(ii)salen]配合物与光敏剂ir(ppy)3,随后在n2气氛中加入溶剂甲醇(3ml)以及二异丙基乙胺。所述的步骤中二硫缩烯酮投料0.3mmol,各反应物的摩尔比为:二硫缩烯酮/togni试剂/二异丙基乙胺/[co(ii)salen]配合物/ir(ppy)3=1/1.5/2/0.05/0.05。将光反应管置于30w蓝光led灯下照射反应后,通过水浴/油浴控制温度于25℃,12h后,将反应体系通过柱层析(石油醚/乙酸乙酯=30/1)分离得到目标产物,产率:83%。
[0044]
实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氢谱图如图1所示;实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振碳谱图如图2所示;实施例1制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氟谱图如图3所示;
[0045]
谱图解析a:
[0046]1h nmr(600mhz,cdcl3):δ7.88(d,j=9.0hz,2h),6.96(d,j=9.0hz,2h),3.87,2.90(q,j=7.8hz,2h),2.73(q,j=7.2hz,2h),1.33(t,j=7.2hz,3h),1.08(t,j=7.2hz,3h).
13
c nmr(150mhz,cdcl3):δ188.3,164.3,147.1(q,j=3.6hz),134.9(q,j=30.5hz),131.7(2c),129.1,121.0(q,j=273.8hz),114.1(2c),55.5,28.4,28.3,15.0,14.6.
19
f nmr(470mhz,cdcl3):δ-55.65(s,3f).hrms(esi-tof)calcd for c
15h17
f3naos2(m+na)
+
373.0514.found 373.0509.
[0047]
实施例2:的制备
[0048]
向35ml光反应管中加入1-(4-氯苯基)-3,3-双(乙硫基)丙-2-烯-1-酮、togni试剂、[co(ii)salen]配合物与光敏剂ir(ppy)3,随后在n2气氛中加入溶剂甲醇(3ml)以及二异丙基乙胺。所述的步骤中二硫缩烯酮投料0.3mmol,各反应物的摩尔比为:二硫缩烯酮/togni试剂/二异丙基乙胺/[co(ii)salen]配合物/ir(ppy)3=1/1.5/2/0.05/0.05。将光反应管置于30w蓝光led灯下照射反应后,通过水浴/油浴控制温度于30℃,16h后,将反应体系通过柱层析(石油醚/乙酸乙酯=33/1)分离得到目标产物,产率:88%。
[0049]
实施例2制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氢谱图如图4所示;实施例2制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振碳谱图如图5所示;实施
例2制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氟谱图如图6所示;
[0050]
谱图解析b:
[0051]1h nmr(600mhz,cdcl3):δ7.85(d,j=8.4hz,2h),7.46(d,j=8.4hz,2h),2.91(q,j=7.2hz,2h),2.73(q,j=7.2hz,2h),1.33(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h).
13
c nmr(150mhz,cdcl3):δ188.5,148.6(q,j=3.5hz),140.5,134.6,133.9(q,j=30.9hz),130.5(2c),129.2(2c),120.9(q,j=273.9hz),28.6,28.5,15.0,14.5.
19
f nmr(470mhz,cdcl3):δ-55.63(s,3f).hrms(esi-tof)calcd for c
14h14
clf3naos2(m+na)
+
377.0013.found 377.0019.
[0052]
实施例3的制备
[0053]
向35ml光反应管中加入1-(4-溴苯基)-3,3-双(乙硫基)丙-2-烯-1-酮、togni试剂、[co(ii)salen]配合物与光敏剂ir(ppy)3,随后在n2气氛中加入溶剂甲醇(3ml)以及二异丙基乙胺。所述的步骤中二硫缩烯酮投料0.3mmol,各反应物的摩尔比为:二硫缩烯酮/togni试剂/二异丙基乙胺/[co(ii)salen]配合物/ir(ppy)3=1/1.5/2/0.1/0.05。将光反应管置于30w蓝光led灯下照射反应后,通过水浴/油浴控制温度于30℃,16h后,将反应体系通过柱层析(石油醚/乙酸乙酯=40/1)分离得到目标产物,产率:81%。
[0054]
实施例3制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氢谱图如图7所示;实施例3制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振碳谱图如图8所示;实施例3制备得到的α-三氟甲基二硫缩烯酮化合物a的核磁共振氟谱图如图9所示;
[0055]
谱图解析c:
[0056]1h nmr(600mhz,cdcl3):δ7.77(d,j=8.4hz,2h),7.63(d,j=8.4hz,2h),2.91(q,j=7.2hz,2h),2.73(q,j=7.2hz,2h),1.33(t,j=7.2hz,3h),1.05(t,j=7.2hz,3h).
13
c nmr(150mhz,cdcl3):δ188.7,148.7(q,j=3.6hz),135.0,133.9(q,j=30.9hz),132.1(2c),130.6(2c),129.3,120.9(q,j=273.8hz),28.6,28.5,15.0,14.5.
19
f nmr(470mhz,cdcl3):δ-55.61(s,3f).hrms(esi-tof)calcd for c
14h14
brf3naos2(m+na)
+
420.9514.found 420.9514.
[0057]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1