一种ω-转氨酶突变体及其应用
(一)本发明涉及一种ω-转氨酶突变体、编码基因,含有编码基因的载体、基因工程菌,以及其在微生物催化制备西他列汀中间体中的应用。
背景技术:
0、(二)背景技术
1、西他列汀(sitagliptin)为二肽基肽酶-4(dpp-4)抑制药,dpp-4是一个以同型二聚体形式存在于细胞膜上的多功能酶,它可以裂解包括胰高血糖素样肽-1和抑胃肽在内的多种肽类激素,而这两者与ii型糖尿病有着密切联系。dpp-4通过保护内源性肠降血糖素和增强其作用而控制血糖水平。葡萄糖依赖性促胰岛素释放肽(gip)和胰高血糖素样肽-1(glp-1),是针对膳食摄入而释放的肠降血糖素。
2、glp-1和gip能通过细胞内信号途径增加胰岛素合成及从胰岛β细胞的释放,glp-1亦能减少胰岛α细胞分泌胰高血糖素,使肝葡萄糖生成减少。但glp-1和gip均由dpp-4快速代谢,导致其促胰岛素作用丧失。
3、本药抑制肠降血糖素dpp-4的降解,故能增强glp-1和gip的功能,增加胰岛素释放并降低循环中胰高血糖素水平(此作用呈葡萄糖依赖性)。本药选择性抑制dpp-4,对dpp-8或dpp-9无抑制活性。此外,dpp-4抑制剂还可抑制gip、垂体腺苷酸环化酶激活多肽和胃泌素释放肽等参与调节血糖的其他肽类的降解。西他列汀能够血糖依赖性地增加胰岛素的分泌,降糖作用较为适中,不会引发低血糖的发生,并且无增加体重、恶心、呕吐等副作用。西他列汀的商品名为捷诺维(januvia),是由美国merck公司和codexis公司研制和开发,是首个获得fda批准用于治疗ⅱ型糖尿病的二肽基肽酶-iv(dpp-iv)抑制剂(2016年10月)。目前已在全世界70多个国家批准使用,据报道,2021年全球销售总额达到了30亿美元,是国际上药物销售额前20强的药物。
4、西他列汀及其中间体的合成既有完全化学法合成,也有化学法与酶法相结合的。对于化学-酶法而言关键就是要获得一种ω-转氨酶,其能够催化不对称转氨反应得到光学纯的西他列汀中间体。
5、国际专利wo201009950公开了codexis公司开发的工程化转氨酶(野生型来源于arthrobacter sp.),对溶剂dmso有很好的耐受性,但对醇类溶剂的耐受性不好;在酶催化反应中使用dmso,由于dmso沸点高,难以从反应体系中去除,使得反应产物在提纯过程中损失较大,导致成本较高。
6、美国专利us6699871公开了一种西他列汀中间体的化学合成方法,采用手性源来诱导出手性的alpha-氨基酸,而后通过重氮化反应产生beta-氨基酸来构建所需的手性中心。该路线所需的原料成本相对较高,反应较为麻烦,且产业化过程中工艺过程和产品质量都难以控制。
7、国际专利w02005003135公开了以s-苯甘氨酰胺来诱导催化氢化而合成手性胺的合成方法(默克公司)。该路线需要两次催化氢化,第一次所用的铂催化剂价格昂贵,第二次脱保护时需要用大量的pd(oh)2-c催化剂,成本较高,ee值为96%,需要进一步重结晶。
8、国际专利w02004087650公开了默克公司关于西他列汀中间体的合成路线,利用手性钌催化剂对酮进行不对称氢化构建手性醇,然后将手性醇转化成手性胺。该合成方法中,需要用到钌催化的不对称氢化,催化剂价格昂贵,总收率只有52%,工艺中用到高压氢气,立体选择性也不高。
9、国际专利w02007050485公开了默克公司关于西他列汀中间体的合成方法,采用了手性锗催化剂对烯胺的不对称氢化来合成手性胺,产率达到84%,ee值94%,但该方法需要用昂贵的锗手性催化剂,去除与回收也较为困难。
10、美国专利us8293507公开了coexis公司对节杆菌来源的转氨酶(ata117)进行改造得到的生物催化剂代替上述工艺中的锗催化剂,转氨得到的产物ee值达到99%。
11、以下专利对于合成西他列汀中间体的生产方法,公开了工艺路线。
12、中国专利cn107384887公开了何人宝等人筛选得到了一种源于唐菖蒲伯克霍尔德氏菌(burkholderia gladioli)的转氨酶,并对其进行了工程化改造。虽然cn107384887中公开的工程化转氨酶可直接以西他列汀前体酮为底物,但其活性不够高,需要用到50g/l的湿菌体才能达到较高的转化率,且反应体系中依然用dmso作为溶剂;高浓度的湿菌体使得反应体系成分极为复杂,对反应后处理和产物提出非常不利,同时dmso的去除也使得产物的分离收率受限。
13、中国专利cn102838511公开了浙江海翔药业关于西他列汀中间体的生产方法,采用格式试剂对手性环氧氯丙烷进行亲核取代,而后用氰化物进行取代水解合成beta-羟基酸,该方法总收率仅40%,而且采用剧毒氰化物,应用受限。
14、中国专利cn103014081公开了苏州汉酶公司利用转氨酶将3-碳基-4-(2,4,5-三氟苯基)-丁酸甲酯转氨化为(r)-3-氨基-4-(2,4,5-三氟苯基)-丁酸甲酯,但是并没有公开具体转氨酶的序列以及克隆方法。
15、中国专利cn105018440中,南京博优康远生物医药科技有限公司对分支杆菌(mycobacterium vanbaalenii)pyr-1来源的转氨酶进行改造得到的工程化转氨酶,用以合成一个相对简单的西他列汀中间体:r-3-氨基-4-(2,4,5-三氟苯基)-丁酸甲酯;虽然cn105018440中公开的工程化转氨酶对乙醇等醇类溶剂有很好的耐受性(所用溶剂为50%的乙醇,有利于产物的提纯),但催化活性不高,需要加入10g/l的酶蛋白,且转氨反应的产物需要经boc保护后才能进一步转化为boc保护的西他列汀,脱保护后得到西他列汀,整体收率不高,导致成本较高。
16、近年来,由于化学-酶法具有高选择性及环境优化的优势,逐步成为合成手性医药化学品及其中间体的首选方案。ω-转氨酶是生产西他列汀的关键酶。许多ω-转氨酶基因已被克隆,其中部分转氨酶的基因已在不同的宿主(大肠杆菌、毕赤酵母等)中表达,获得了酶活和选择性都较高的基因工程菌。尽管如此,对于r-型选择性转氨的天然ω-转氨酶报道很少,且这些ω-转氨酶催化的底物谱较窄,往往是为特定反应筛选的最适生物催化剂,因此大大限制了其应用范围。随着定向进化技术的发展,蛋白质工程越来越多地被用于改造酶的底物特异性,筛选具有较宽底物谱的新型转氨酶,研究其可以高效高选择性催化的手性药物及其中间体,不仅可以拓宽其应用范围,提升其应用潜力,也为实现工业化生产奠定基础。
技术实现思路
0、(三)
技术实现要素:
1、本发明目的是克服现有技术中用于合成西他列汀或其手性氨基中间体的工程化转氨酶的不足,提供一种直接以西他列汀前体酮为底物的、活性更好、对有机类溶剂耐受性更好、且热稳定性更好的工程化转氨酶——一种ω-转氨酶突变体、编码基因,含有编码基因的载体、基因工程菌,以及其在微生物催化制备西他列汀中间体中的应用。
2、本发明采用的技术方案是:
3、一种ω-转氨酶突变体,由seq id no.2所示氨基酸序列第275位、第115位、第97位进行单突变或多点联合突变获得。
4、seq id no.2所示的氨基酸序列组成的蛋白质可以从曲霉属真菌兰特(aspergillus lentulus)中分离获得,也可以从重组表达该蛋白质的表达转化体中分离获得,也可以人工合成获得。两条氨基酸序列或两条核苷酸序列之间的同一性均可通过本领域常用的算法得到,优选采用ncbi blastp和blastn软件根据默认参数计算得到。
5、所述突变体为下列之一或其中两种以上的组合:(1)第275位的甘氨酸突变成丙氨酸;(2)第115位的赖氨酸突变成甲硫氨酸;(3)第97位的赖氨酸突变成精氨酸。
6、优选的,所述突变体氨基酸序列如seq id no.4(突变体g275a)、6(突变体k115m)或8(突变体k97r/k115m)所示。
7、本发明所述氨基酸序列经过取代、缺失或添加一个或几个氨基酸残基且具有转氨酶活性的衍生的氨基酸序列具有至少95%同一性的蛋白质,均属于本发明的保护范围。
8、本发明还涉及编码所述的ω-转氨酶突变体的基因。
9、具体的,所述编码基因核苷酸序列如seq id no.3(编码seq id no.4所示突变体)或seq id no.5(编码seq id no.6所示突变体)或seq id no.7(编码seq idno.8所示突变体)所示。
10、由于核苷酸密码子的简并性,编码seq id no.4、6、8的氨基酸序列的多核苷酸序列不仅仅局限于seq id no.3、5、7。编码本发明的工程化转氨酶的核酸序列也可以是编码序列表中seq id no.4、6、8所示氨基酸序列的其他任何核酸序列。
11、本发明还涉及含有编码所述的ω-转氨酶突变体的基因的重组载体以及基因工程菌。
12、本发明还涉及所述ω-转氨酶突变体在微生物催化制备西他列汀中间体中的应用。具体为:构建含有所述转氨酶基因的重组载体,将所示重组载体转化至大肠杆菌中,获得的重组基因工程菌进行诱导培养,培养液分离得到含有重组转氨酶的菌体细胞,破碎后的转氨酶粗酶液以及纯化后转氨酶纯酶用于制备西他列汀中间体。所述催化剂包括转氨酶及其突变体纯酶、相应的重组基因工程菌湿菌体、粗酶液、粗酶粉、纯酶液、纯酶粉等其他形态。
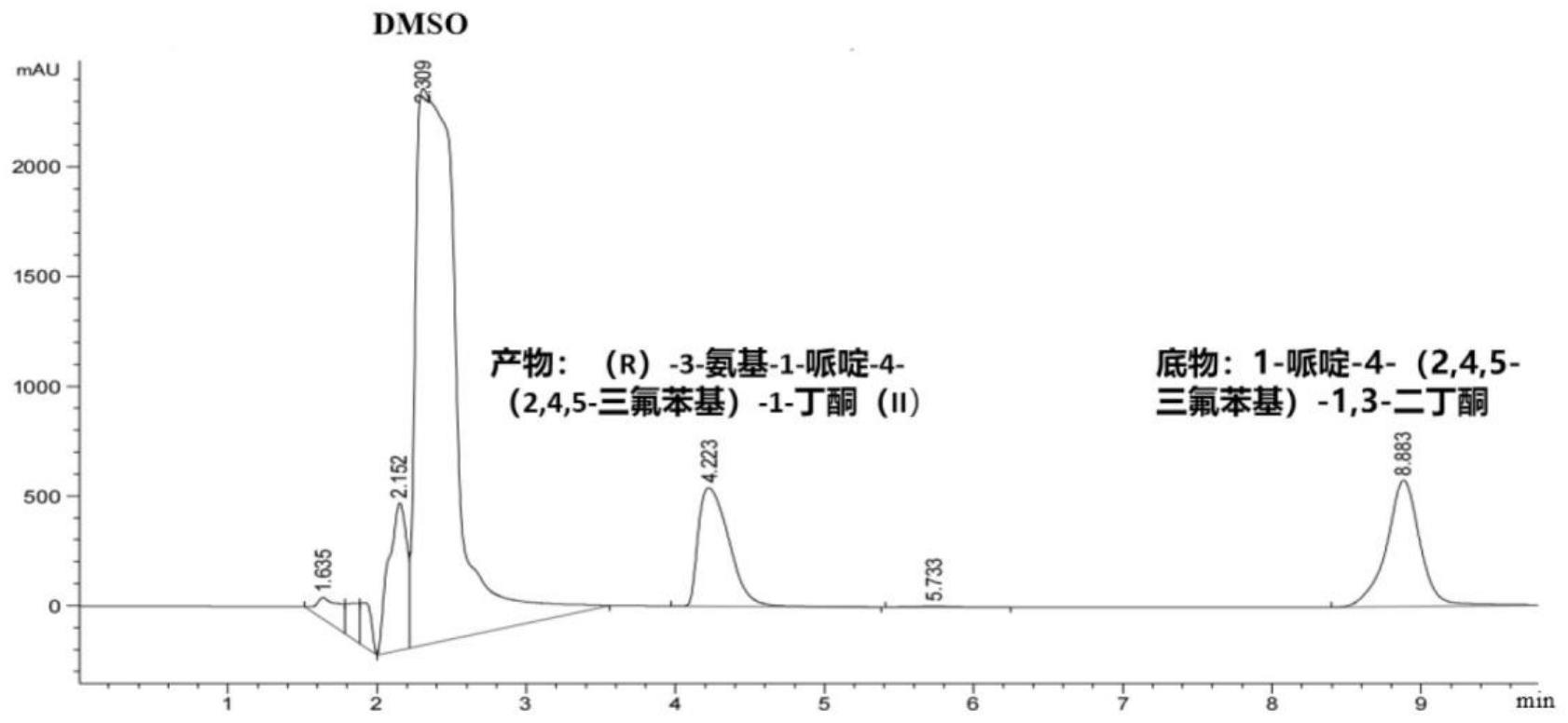
13、具体的,所述应用为:以1-哌啶-4-(2,4,5-三氟苯基)-1,3-二丁酮(i)为反应底物,含有所述ω-转氨酶突变体的湿菌体为生物催化剂,以二甲基亚砜(dmso)为助溶剂、以磷酸吡哆醛(plp)为辅酶、以异丙胺为辅底物,以ph 8~9三乙醇胺缓冲液为反应介质构成反应体系,在温度30~45℃、搅拌速度100~800r/min的条件下进行生物催化反应,反应结束后,反应液分离纯化获得(r)-3-氨基-1-哌啶-4-(2,4,5-三氟苯基)-1-丁酮(ii)。
14、
15、所述反应体系中,湿菌体用量为10~50g/l(优选50g/l),底物终浓度为50~200g/l,二甲基亚砜体积终浓度为10~20%(v/v),磷酸吡哆醛0.5~2g/l,异丙胺5~20g/l。
16、所述湿菌体可按如下方法制备:将含有ω-转氨酶突变体编码基因的重组大肠杆菌接种至含有50μg/ml卡那霉素的lb液体培养基,37℃,200rpm下培养12h,再以体积浓度1%接种量接种至新鲜的含有50μg/ml卡那霉素抗性的lb液体培养基中,于37℃,150rpm下培养至菌体od600达0.6~0.8,加入终浓度为0.1mm的iptg,28℃下诱导培养12h后,4℃、5000rpm离心20min,弃去上清液,收集沉淀,即获得所述的湿菌体。
17、本发明的有益效果主要体现在:针对己报道的不对称合成西他列汀及其中间体的总收率不高(一般低于50%),立体选择性偏低(产物e.e.值普遍低于90%)、金属催化剂昂贵、生物催化剂不能直接以西他列汀前体酮为底物的问题,本发明提供了来源于一种曲霉属真菌兰特(aspergillus lentulus)的转氨酶突变体(生物催化剂),以西他列汀中间体前体酮(如:1-哌啶-4-(2,4,5-三氟苯基)-1,3-二丁酮)为底物,同时异丙胺为氨基供体,磷酸吡多醛为辅酶,二甲基亚砜为助溶剂,进行生物催化反应、分离纯化制备高光学纯度的西他列汀中间体,该方法的总收率达到66.7%(包括转化得率及分离纯化收率),产物e.e.值达到99%(立体选择性高),具有较好应用前景。
- 还没有人留言评论。精彩留言会获得点赞!