2-氨基嘧啶衍生物作为激酶抑制剂及其制备和应用的制作方法
本发明属于医药,具体涉及2-氨基嘧啶衍生物及其用于制备癌症治疗药物的用途。
背景技术:
1、fms样酪氨酸激酶3(flt3)是一种iii型受体酪氨酸激酶,在造血作用和淋巴细胞增殖中发挥关键作用。flt3由一个n-端细胞外结构区、一个跨膜区以及一个细胞内激酶区(含一个近膜结构域及一个激酶催化域)所组成,其中细胞内激酶区的激酶催化域由一个n端、一个含有活化环的c端以及一个含有atp的结合位点的柔性激酶插入结构域所组成。flt3的天然配体包括血小板源性生长因子(pdgf)、集落刺激因子1(csf-1)和kit激酶配体(kl)(molecular cell,2004,13,169)。当flt3受体的细胞膜外结构域与配体结合后,flt3会与相应的配体形成二聚体复合物从而使活化环开启,此时底物蛋白连接到atp结合位点上从而催化底物蛋白的磷酸化,激活下游的磷脂酰肌醇-3-羟激酶(pi3k)通路和ras通路。研究证明flt3与src、grb2、shc和shp2等下游信号蛋白的激活直接相关(curr med chem,2008,15,3113)。
2、flt3的突变以及过度表达是造成多种恶性肿瘤、急性髓性白血病(aml)、急性淋巴细胞白血病(all)以及慢性髓性白血病(cml)的关键因素。aml的发病往往伴随着flt3的异常活化,flt3突变是造成其异常活化的主要原因。flt3-itd突变(近膜处的内部串联复制突变)在aml患者中最常见,大约30%的aml患者携带这种突变。此外,携带flt3氨酸激酶结构域(flt3-tkd)突变的aml患者占到5~10%。点突变最常见的是位于酪氨酸激酶结构域(flt3-tkd)的天冬氨酸-酪氨酸的突变(d835y)。与flt3-itd相似,flt-tkd突变同样导致下游增殖途径的激活。d835y点突变同样也是部分flt3(itd)抑制剂耐药的主要机制,如flt3抑制剂crenolanib耐药与d835y点突变相关。flt3突变的患者往往具有较差的预后。
3、早期flt3抑制剂如舒尼替尼(sunitinib)、索拉非尼(sorafenib)和来他替尼(lestaurtinib妥林(midostaurin)是第一种单药方案能短时效地降低flt3突变aml患者外周和骨髓原始细胞的数目的flt3激酶抑制剂。临床试验表明,在年轻初诊aml患者中,米哚妥林联合传统化疗对wt型和flt3突变都具有高的完全缓解率。但米哚妥林对flt3的选择性仍然不高,需与常规化疗方案联合以达到更显著的治疗效果。因此开发活性、选择性更高的flt3抑制剂仍然十分迫切。
4、细胞周期蛋白依赖性激酶(cdks)属于丝氨酸/苏氨酸蛋白激酶(ser/thrkinase),cdks家族主要参与调控细胞周期分裂、转录起始和某些特定代谢级联反应控制等。目前cdks总共有21种,其按功能可以分为两类:调控细胞周期型cdks和转录调控型cdks。其中cdk9的功能是转录调控,促进转录延伸,不参与细胞周期的调节。cdk9具有两个亚型42kda与55kda,可分别与细胞周期蛋白cyclin t1、cyclin t2a、cyclin t2b或cyclink形成二聚体,作为正性转录延长因子b(p-tefb)的主要组成部分。抑制cdk9则可以防止p-tefb活性复合物形成,抑制其延伸转录功能,从而阻断rna聚合酶ii转录延伸,抑制短寿命抗凋亡蛋白(如mcl-1,半衰期2~4h)的表达,最终导致癌细胞凋亡。研究表明,通过抑制cdk9可降低mcl-1、xiap、bcl-2等抗凋亡蛋白的表达(int j cancer.2012,130,1216)。
5、cdk9是临床针对血液系统肿瘤和淋巴瘤的热门靶点,目前已有多种药物进入临床实验阶段。cdk9抑制剂对all、aml、cml、nhl、mm等多种肿瘤细胞系有较强的生长抑制作用(mol cancer ther;13(6)june 2014)。flavopiridol是第一个进入临床实验阶段的cdk抑制剂,可以促进细胞周期阻滞,诱导肿瘤细胞凋亡,影响转录进程。flavopiridol对淋巴瘤效果显著,响应率80%以上;与阿糖胞苷和米托蒽醌合用,可使新诊断急性髓性白血病(aml)的缓解率达到75%(clin cancer res,2007,13(15),august 1)。
6、tg-02是tragara制药公司收购的针对血液肿瘤、小淋巴细胞瘤的cdk9抑制剂。在体外,tg-02可以通过mapk\erk5通路抑制mm的增殖并且诱导凋亡。目前,tg-02正在进行多项临床ⅰ期实验。已完成的临床试验显示tg-02可以影响白血病干细胞的增殖,并提高提高了其对化疗药物的敏感性。2015年11月,tragara公司宣布同香港李氏制药公司合作,共同对tg-02进行开发,用于治疗血液及实体肿瘤。
7、此外,进入临床研究的cdk9抑制剂还有dinaciclib、seliciclib、sns-032和rgb-286638等。
8、通过活性筛选,意外的发现本专利发明化合物具有显著的flt3和cdk9抑制活性,具有治疗flt3和cdk9相关疾病的潜力。
技术实现思路
1、本发明的目的是提供一种2-氨基嘧啶类蛋白激酶抑制剂。
2、本发明的另一个目的是提供所述的蛋白激酶抑制剂在制备预防或治疗flt3、cdk9激酶相关疾病药物的用途。
3、为实现本发明的目的,本发明的技术方案如下:
4、本发明所述的如式(i)所示的化合物、其立体异构体或其药学上可接受的盐,其特征在于:
5、
6、环a选自6~10元芳基或5~10元杂芳基;
7、环b选自6~10元芳基或5~10元杂芳基;
8、环c选自3~8元碳环或4~12元杂环基;
9、r1选自h、任选取代或未取代的c1-8直链或支链烷基、c3-8环烷基、c4-12杂环基、-nr11s(o)mr12、-nr11c=or12、-(ch2)ns(o)mr11、-(ch2)ns(o)mnr11r12、-(ch2)np(o)mr11、-(ch2)nc=onr11r12或-(ch2)nso=nr11;
10、r2选自h、氘、卤素、氰基、氨基、硝基、-c=oor11、-c=onhr11r12、-c=or11、任选取代或未取代的c1-4烷基、c3-8环烷基或c1-4烷氧基;
11、r3、r4、r5分别独立地选自h、氘、卤素、羟基、c1-4烷氧基、c1-8直链或支链烷基、c3-8环烷基、-cooh、-c=or11、-c=onr11r12、-(ch2)nnr11r12、-nr11cor12、-nr11s(o)mr12、-s(o)mr11、-s(o)mnr11r12或-(ch2)n-c4-12杂环基,所述c1-8直链或支链烷基、c3-c8环烷基或-(ch2)n-c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷氧基、c1-8直链或支链烷基、c3-8环烷基、-cooh、-c=or11、羟基取代的c1-8烷基、c1-2烷氧基取代的c1-8烷基、-c=onr11 r12、-(ch2)nnr11r12、-nr11cor12、-nr11s(o)mr12、-s(o)mr11、-s(o)mnr11r12或c4-12杂环基所取代;
12、或者,r3、r4和r5两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c3-8环烷基或c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷氧基、c1-8烷基、-cooh、-c=or11、羟基取代的c1-8烷基、-c=onr11r12、-(ch2)nnr11r12、-nr11cor12、-nr11s(o)mr12、-s(o)mr11、-s(o)mnr11r12所取代;
13、r6和r7各自独立地选自h、氘、氰基、c1-8直链或支链烷基或c3-8环烷基;
14、或者,r6和r7两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c3-8环烷基或c4-12杂环基可进一步被氘、卤素、羟基、c1-4烷氧基、-c=or11、c1-8烷基、-(ch2)n nr11r12或-nr11cor12所取代;
15、m选自0、1或2;
16、n选自0、1或2;
17、y选自c、o、s或n;
18、r8选自h、c1-4烷基、c3-8环烷基、c1-4烷氧基,或者不存在;
19、r9选自h、氘、卤素、氰基、c1-4烷基、c3-8环烷基、c1-4烷氧基,或者不存在;
20、r10选自h、氘、卤素、氰基、c1-4烷基、c3-8环烷基、c1-4烷氧基,或者不存在;
21、r11和r12各各自独立地选自h、任选取代或未取代的c1-4烷氧基、c1-8直链或支链烷基、c3-8环烷基、c4-12杂环基;
22、或者,r11和r12两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c3-8环烷基或c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷氧基、-c=or11、c1-8烷基、-(ch2)nnr11r12或-nr11cor12所取代。
23、本发明优选实施方案,其特征在于:
24、环a选自苯基、吡啶基、吡嗪基、嘧啶基、吡唑基、噁唑基、呋喃基、噻吩基或噻唑基;
25、环b选自噻吩基、噻唑基、呋喃基、咪唑基、吡唑基、吡咯基、噁唑基、苯基、吡啶基、吡嗪基、嘧啶基、哒嗪基、萘基、苯并呋喃基、苯并吡咯基、苯并噻唑基、苯并噻吩基、苯并咪唑基、苯并吡唑、苯并噁唑基、噻吩并吡咯基、环戊二烯并吡咯基、吡咯并吡咯基、吡咯并噻唑基、噻吩并噻唑基、吡唑并吡啶基、吡唑并嘧啶基、吡咯并哒嗪基、吡咯并嘧啶基或吡唑并嘧啶基;
26、环c选自
27、r1选自h、-nr11s(o)mr12、-nr11c=or12、-(ch2)ns(o)mr11、-(ch2)ns(o)mnr11r12、-
28、(ch2)nc=onr11r12或-(ch2)nso=nr11;
29、r2选自h、卤素、氰基、c1-4烷基或卤素取代的c1-4烷基;
30、r3、r4、r5分别独立地选自h、氘、卤素、c1-8直链或支链烷基、-c=or11、-(ch2)nnr11r12、-nr11cor12、-s(o)mr11或-(ch2)n-c4-12杂环基,所述c1-8直链或支链烷基或-(ch2)n-c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷基、c1-2烷氧基、-ch2oh、-ch2ch2oh或c4-6杂环基所取代;
31、或者,r3、r4和r5两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c4-12杂环基可进一步被羟基、氰基、甲基、乙基、-ch2oh或-ch2ch2oh所取代;
32、r6和r7各自独立地选自h、氘、c1-8直链或支链烷基或c3-8环烷基;
33、m选自0、1或2;
34、n选自0、1或2;
35、y选自o、s或n;
36、r8选自h、c1-4烷基、c1-4烷氧基,或者不存在;
37、r9选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
38、r10选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
39、r11和r12各自独立地选自h、任选取代或未取代的c1-4烷氧基、c1-8直链或支链烷基、c3-8环烷基、c4-12杂环基;
40、或者,r11和r12两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c3-8环烷基或c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷氧基、-c=or11、c1-8烷基、-(ch2)nnr11r12或-nr11cor12所取代;
41、条件是,式(i)化合物不包含以下结构:
42、
43、本发明优选实施方案,其特征在于:
44、环a选自苯基、吡啶基、吡嗪基;
45、环b选自噻吩基、噻唑基、呋喃基、咪唑基、吡咯基、苯基、吡啶基、萘基、苯并呋喃基、苯并噻吩基、苯并咪唑基、苯并噁唑基、苯并吡咯基、苯并噻唑基、噻吩并吡咯基、环戊二烯并吡咯基、吡咯并吡咯基、吡咯并噻唑基、噻吩并噻唑基、吡唑并吡啶基、吡唑并嘧啶基、吡咯并哒嗪基、吡咯并嘧啶基或吡唑并嘧啶基;
46、环c选自
47、r1选自h、-nr11s(o)mr12、-(ch2)ns(o)mr11、-(ch2)ns(o)mnr11r12、或-(ch2)nc=onr11r12;
48、r2选自h、卤素、氰基、c1-4烷基或卤素取代的c1-4烷基;
49、r3、r4、r5分别独立地选自h、氘、卤素、c1-8直链或支链烷基、-c=or11、-(ch2)nnr11r12、-nr11cor12或-(ch2)n-c4-12杂环基,所述c1-8直链或支链烷基或-(ch2)n-c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷基、c1-2烷氧基、-ch2oh、-ch2ch2oh或c4-6杂环基所取代;
50、或者,r3、r4和r5两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c4-12杂环基可进一步被羟基、氰基、甲基、乙基、-ch2oh或-ch2ch2oh所取代;
51、r6和r7各自独立地选自h、氘;
52、m选自0、1或2;
53、n选自0、1或2;
54、y选自o、s或n;
55、r8选自h、c1-4烷基、c1-4烷氧基,或者不存在;
56、r9选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
57、r10选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
58、r11和r12各自独立地选自h、c1-4烷氧基、c1-8直链或支链烷基、c3-8环烷基或c4-12杂环基、羟基取代的c1-8烷基、卤素取代的c1-8烷基或羟基取代的c4-12杂环基;
59、或者,r11和r12两两间连接,形成c3-8环烷基或c4-12杂环基,且所述的c3-8环烷基或c4-12杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷氧基、-c=or11、c1-8烷基、-(ch2)nnr11r12或-nr11cor12所取代。
60、本发明优选实施方案,其特征在于:
61、环a选自苯基、吡啶基或吡嗪基;
62、环b选自苯基或吡啶基;
63、环c选自
64、r1选自h、-nr11s(o)mr12、-(ch2)ns(o)mr11、-(ch2)ns(o)mnr11r12、或-(ch2)nc=onr11r12;
65、r2选自h、卤素、氰基、c1-4烷基或卤素取代的c1-4烷基;
66、r3、r4、r5分别独立地选自h、氘、卤素、c1-6烷基、-c=or11、-(ch2)nnr11r12、-nr11cor12或-(ch2)n-c4-6杂环基,所述c1-6烷基或-(ch2)n-c4-6杂环基可进一步被氘、卤素、羟基、氰基、c1-4烷基、c1-2烷氧基、-ch2oh、-ch2ch2oh、所取代;
67、或者,r3、r4和r5两两间连接,形成c3-5环烷基或c4-6杂环基,且所述的c4-6杂环基可进一步被氰基、甲基、乙基、羟基、-ch2oh或-ch2ch2oh所取代;
68、r6和r7各自独立地选自h、氘;
69、m选自0、1或2;
70、n选自0、1或2;
71、y选自o、s或n;
72、r8选自h、c1-4烷基、c1-4烷氧基,或者不存在;
73、r9选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
74、r10选自h、氰基、c1-4烷基、c1-4烷氧基,或者不存在;
75、r11和r12各自独立地选自h、甲氧基、乙氧基、甲基、乙基、丙基、丁基、环丙基、环丁基、环戊基、-ch2oh-ch2ch2oh-ch2chf2、
76、本发明优选实施方案,其特征在于:
77、环a选自苯基、吡啶基或吡嗪基;
78、环b选自苯基或吡啶基;
79、环c选自
80、r1选自h、-n(ch3)s(o)2ch3、-s(o)2ch3或-s(o)2nhc(ch3)3;
81、r2选自h、f、cl、br、氰基、甲基、乙基、丙基、丁基或cf3;
82、r3、r4、r5各自独立地选自h、氟、氯、溴、甲基、乙基、丙基、-ch2ch2oh、-coch3、-coch2oh、-ch2ch2och3、-n(ch3)2、-ch2n(ch3)2、
83、或者,r3、r4和r5两两间连接,形成c3-5环烷基或c4-6杂环基,且所述的c4-6杂环基可进一步被氰基、甲基、乙基、羟基、-ch2oh或-ch2ch2oh所取代;
84、r6和r7各自独立地选自h、氘;
85、y选自o或n;
86、r8选自h、甲基、乙基、丙基、丁基、甲氧基、乙氧基、丙氧基、丁氧基,或者不存在;
87、r9选自h、氰基、甲基、乙基、丙基、丁基、甲氧基、乙氧基、丙氧基、丁氧基,或者不存在;
88、r10选自h、氰基、甲基、乙基、丙基、丁基、甲氧基、乙氧基、丙氧基、丁氧基,或者不存在。
89、本发明实施方案,具有如下结构的化合物、其立体异构体或其药学上可接受的盐:
90、
91、
92、
93、
94、
95、
96、
97、
98、
99、本发明实施方案,具有如下结构的化合物、其立体异构体或其药学上可接受的盐:
100、
101、
102、
103、
104、
105、
106、
107、
108、
109、本发明实施方案,具有如下结构的化合物、其立体异构体或其药学上可接受的盐:
110、
111、
112、
113、
114、
115、本发明另一方面提供式(i)化合物或其药学上可接受的盐或酯或溶剂化物的制备方法,包括如下步骤:
116、方案一:式(i)化合物制备方法如下:
117、
118、式i-1化合物与式i-2化合物,在碱存在条件下得到式i-3化合物,所采用的溶剂选自三乙胺、diea、dmac、1,8-二氮杂双环[5.4.0]十一碳-7-烯、苯、甲苯、氯仿、正己烷、环己烷、二氯甲烷、1,2-二氯乙烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙醚、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选三乙胺、diea、dmac、1,8-二氮杂双环[5.4.0]十一碳-7-烯、n,n-二甲基甲酰胺;所采用的碱选自三乙胺、diea、1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾、碳酸钠、碳酸铯、氢氧化钠、氢氧化钾,优选三乙胺、diea、1,8-二氮杂双环[5.4.0]十一碳-7-烯;反应温度为0℃至100℃,优选50℃至70℃;
119、式i-3化合物与式i-4化合物,在金属催化剂存在条件下得到式(i)化合物,所采用的溶剂选自1,4-二氧六环、dmac、1-甲基-2吡咯烷酮、异丙醇、叔丁醇、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选1,4-二氧六环、四氢呋喃、甲苯、1-甲基-2吡咯烷酮、n,n-二甲基甲酰胺;所采用的碱选自碳酸钾、碳酸钠、碳酸铯、氢氧化钠、氢氧化钾、叔丁醇钠,优选碳酸钾、碳酸铯;所采用的金属催化剂为pd2(dba)3、pd(pph3)2cl2、pd(oac)2,优选pd2(dba)3;所采用的配体为xantphos(4,5-双二苯基膦-9,9-二甲基氧杂蒽)、xphos(2-二环己基磷-2',4',6'-三异丙基联苯)、dppf(双(二苯基膦基)二茂铁)、pcyp3(三环戊基膦四氟硼酸盐),优选xantphos;反应温度为50℃至130℃,优选90℃至110℃;
120、其中,环a、环b、环c、r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、m、n如式(i)化合物所定义。
121、方案二:式(i)制备方法也可如下:
122、
123、式i-1化合物与式i-2化合物,在碱存在条件下得到式i-3化合物,所采用的溶剂选自三乙胺、diea、dmac、1,8-二氮杂双环[5.4.0]十一碳-7-烯、苯、甲苯、氯仿、正己烷、环己烷、二氯甲烷、1,2-二氯乙烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙醚、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选三乙胺、diea、dmac、1,8-二氮杂双环[5.4.0]十一碳-7-烯、n,n-二甲基甲酰胺;所采用的碱选自三乙胺、diea、1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾、碳酸钠、碳酸铯、氢氧化钠、氢氧化钾,优选三乙胺、diea、1,8-二氮杂双环[5.4.0]十一碳-7-烯;反应温度为0℃至100℃,优选50℃至70℃;
124、式i-3化合物与式i-4化合物,在酸存在条件下得到式(i)化合物,所采用的溶剂选自甲醇、乙醇、异丙醇、正丁醇、叔丁醇、1-甲基-2吡咯烷酮、二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选乙醇、异丙醇、正丁醇;所采用的酸选自乙酸、三氟乙酸、甲磺酸、樟脑磺酸、硫酸、磷酸、硝酸,优选甲磺酸、樟脑磺酸;反应温度为40℃至110℃,优选60℃至90℃;
125、其中,环a、环b、环c、r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、m、n如式(i)化合物所定义。
126、本发明还提供式(i)化合物中间体式i-4的制备方法,
127、方案一:当环c为环庚烷时,式i-4-1的制备方法如下:
128、
129、式ii-1化合物与(甲氧基甲基)三苯基氯化磷,在碱存在条件下得到式ii-2化合物,所采用的溶剂选自1-甲基-2吡咯烷酮、二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选二氧六环、四氢呋喃;所采用的碱选自氢氧化钠、叔丁醇钾、钠氢、丁基锂,优选叔丁醇钾、钠氢;反应温度为-60℃至50℃,优选-40℃至30℃;
130、式ii-2化合物,在酸存条件下得到式ii-3化合物,所采用的溶剂选自1-甲基-2吡咯烷酮、二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选二氧六环、四氢呋喃;所采用的酸选自甲酸、乙酸、三氟乙酸、甲磺酸,优选甲酸;反应温度为50℃至100℃,优选60℃至80℃;
131、式ii-3化合物与式ii-8化合物,在酸存在条件下还原得到式ii-4化合物,所采用的溶剂选自二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选四氢呋喃;所采用的酸选自甲酸、乙酸、三氟乙酸,优选乙酸;所采用的还原剂为硼氢化钠、三乙酰氧基硼氢化钠、氰基硼氢化钠,优选三乙酰氧基硼氢化钠;反应温度为0℃至50℃,优选0℃至30℃;
132、式ii-4化合物在钯碳催化下经氢气还原得式i-4-1化合物;
133、其中,环b、r9、r10、r11、r12如式(i)化合物所定义。
134、方案二:当环c为环庚烷时,式i-4-2制备方法如下:
135、
136、式ii-1化合物与式ii-8化合物,在酸存在条件下还原得到式ii-6化合物,所采用的溶剂选自二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选四氢呋喃;所采用的酸选自甲酸、乙酸、三氟乙酸,优选乙酸;所采用的还原剂为硼氢化钠、三乙酰氧基硼氢化钠、氰基硼氢化钠,优选三乙酰氧基硼氢化钠;反应温度为0℃至50℃,优选0℃至30℃;
137、式ii-6化合物在钯碳催化下经氢气还原得式i-4-2化合物;
138、其中,环b、r9、r10、r11、r12如式(i)化合物所定义。
139、方案三:当环c为环己亚胺时,i-4-3制备方法如下:
140、
141、式iii-1化合物与nbs,在自由基引发剂过氧化二甲苯酰(bpo)存在条件下得到式iii-2化合物,所采用的溶剂选自苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈或它们中的一种或多种的混合溶剂,优选四氯化碳、氯仿;反应温度为30℃至100℃,优选50℃至90℃;
142、式iii-2化合物,在硝酸银存在条件下得到式iii-3化合物,所采用的溶剂选自水、丙酮、四氢呋喃、乙腈或它们中的一种或多种的混合溶剂,优选水、乙腈;反应温度为30℃至100℃,优选60℃至90℃;
143、式iii-3化合物与式iii-4化合物,在加热条件下得到式iii-5化合物,所采用的溶剂选自二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选四氢呋喃、二氧六环;反应温度为50℃至100℃,优选60℃至90℃;
144、式iii-5化合物在钯碳催化下经氢气还原得式iii-6化合物;
145、式iii-6化合物在碱催化下经三氟乙酸酐保护氨基得式iii-7化合物;
146、式iii-7化合物,在雷尼镍催化下经氢气还原得到式iii-8化合物,所采用的溶剂选自甲醇、乙醇、异丙醇、正丁醇、叔丁醇、1-甲基-2吡咯烷酮、二氧六环、苯、甲苯、氯仿、正己烷、环己烷、甲基叔丁基醚、四氯化碳、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酮、四氢呋喃、乙腈、n,n-二甲基甲酰胺或二甲亚砜或它们中的一种或多种的混合溶剂,优选甲醇;反应温度为0℃至60℃,优选30℃至40℃;
147、式iii-8化合物在碱存在条件下经水解得式i-4-3化合物,所采用的溶剂选自水、甲醇、乙醇、异丙醇、正丁醇、叔丁醇、二氧六环、四氢呋喃、乙腈或它们中的一种或多种的混合溶剂,优选甲醇、水;碱选自碳酸钾、碳酸钠、碳酸铯、氢氧化钠、氢氧化钾、叔丁醇钠,优选氢氧化钠;反应温度为50℃至100℃,优选60℃至90℃;
148、其中,环b、r9、r10如式(i)化合物所定义;
149、r13选自h、氘、卤素、氰基、c1-4烷基、c3-8环烷基或c1-4烷氧基。
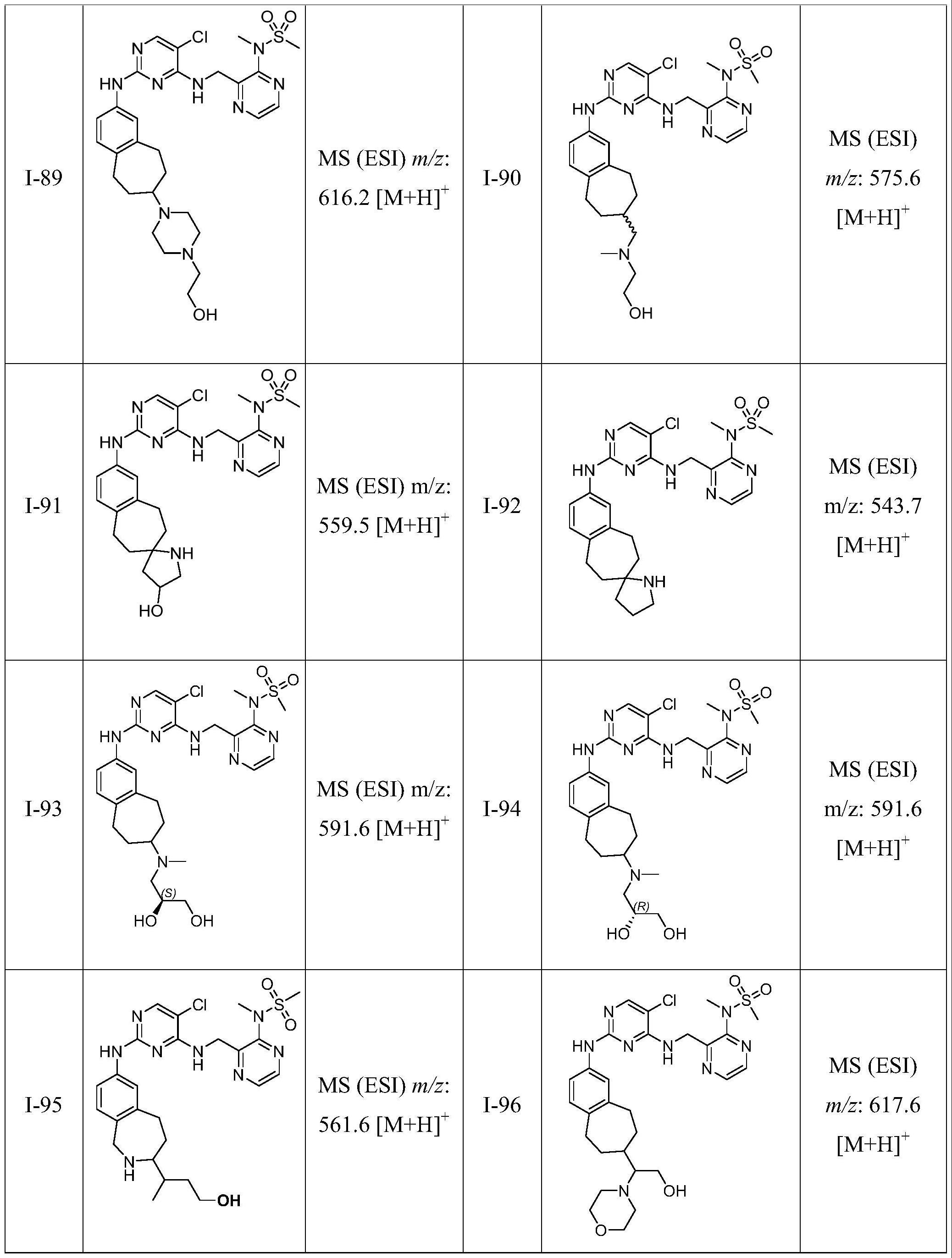
150、采用类似以上制备方法,可以制备得到以下化合物:
151、
152、
153、
154、
155、
156、
157、
158、
159、
160、
161、
162、
163、
164、
165、
166、
167、本发明还涉及一种药物组合物,其包含如式(i)所述的化合物、其立体异构体或其药学上可接受盐和可药用的载体。
168、本发明所述的药物组合物,其特征在于,所述药物组合物是胶囊剂、散剂、片剂、颗粒剂、丸剂、注射剂、糖浆剂、口服液、吸入剂、软膏剂、栓剂或贴剂。
169、本发明式(i)所述的化合物、其立体异构体或其药学上可接受盐或药物组合物在制备用于预防或治疗单独或部分地由flt3或者cdk9活性介导的疾病的治疗药物中的应用。
170、本发明式(i)所述的化合物、其立体异构体或其药学上可接受盐或药物组合物在制备用于预防或治疗单独或部分地由flt3或者cdk9活性介导的疾病的治疗药物中的应用,其特征在于,所述flt3或者cdk9活性介导的疾病为激酶相关的恶性肿瘤。
171、本发明式(i)所述的化合物、其立体异构体或其药学上可接受盐或药物组合物在制备用于预防或治疗单独或部分地由flt3或者cdk9活性介导的疾病的治疗药物中的应用,其特征在于,所述激酶相关的恶性肿瘤选自:卵巢癌、宫颈癌、结肠直肠癌、乳腺癌、胰腺癌、胶质瘤、胶质母细胞瘤、黑色素瘤、前列腺癌、白血病、淋巴瘤、非霍奇金淋巴瘤、胃癌、肺癌、肝细胞癌、胃肠道间质瘤、甲状腺癌、胆管癌、子宫内膜癌、肾癌、间变性大细胞淋巴瘤、多发性骨髓瘤、间皮瘤或者软组织肉瘤。
172、除非有相反陈述,下列用在说明书和权利要求书中的术语具有下述含义。
173、本发明中“芳基”指全碳单环或双环基团,“6~10元芳基”指含有6~10个碳的全碳芳基,例如苯基和萘基。所述芳基环可以稠合于杂芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为芳基环。
174、芳基可以是取代的或未取代的,当被取代时,取代基优选为一个或多个以下基团,独立地选自卤素、羟基、巯基、氰基、硝基、叠氮基、c1-8烷基、c3-8环烷基、3~8元杂环基、c1-8烷氧基、3-8元杂环基氧基。
175、本发明中“杂芳基”指包含1至4个杂原子的杂芳族体系,所述杂原子包括氮、氧和硫的杂原子,包括但不限于呋喃基、噻吩基、吡啶基、吡咯基、吡唑基、n-烷基吡咯基、嘧啶基、吡嗪基、咪唑基、四唑基等。
176、杂芳基可以是取代的或未取代的,当被取代时,取代基优选为一个或多个以下基团,独立地选自卤素、羟基、巯基、氰基、硝基、叠氮基、c1-8烷基、c3-8环烷基、3~8元杂环基、c1-8烷氧基、3~8元杂环基氧基。
177、本发明中“c1-8烷基”指包括1至8个碳原子的直链烷基和含支链烷基,烷基指饱和的脂族烃基团,例如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、1,1-二甲基丙基、1,2-二甲基丙基、2,2-二甲基丙基、1-乙基丙基、2-甲基丁基、3-甲基丁基、正己基、1-乙基-2-甲基丙基、1,1,2-三甲基丙基、1,1-二甲基丁基、1,2-二甲基丁基、2,2-二甲基丁基、1,3-二甲基丁基、2-乙基丁基、2-甲基戊基、3-甲基戊基、4-甲基戊基、2,3-二甲基丁基、正庚基、2-甲基己基、3-甲基己基、4-甲基己基、5-甲基己基、2,3-二甲基戊基、2,4-二甲基戊基、2,2-二甲基戊基、3,3-二甲基戊基、2-乙基戊基、3-乙基戊基、正辛基、2,3-二甲基己基、2,4-二甲基己基、2,5-二甲基己基、2,2-二甲基己基、3,3-二甲基己基、4,4-二甲基己基、2-乙基己基、3-乙基己基、4-乙基己基、2-甲基-2-乙基戊基、2-甲基-3-乙基戊基或其各种支链异构体等。
178、c1-8烷基可以是取代的或未取代的,当被取代时,取代基优选为一个或多个以下基团,独立地选自卤素、羟基、巯基、氰基、硝基、叠氮基、c1-8烷基、c3-8环烷基、3~8元杂环基、c1-8烷氧基或3~8元杂环基氧基。
179、本发明中“环烷基”指饱和单环烃取代基,“c3-8环烷基”指包括3至8个碳原子的单环环烷基,例如:单环环烷基的非限制性实施例包含环丙基、环丁基、环戊基、环己基、环庚基、环辛基等。
180、环烷基可以是取代的或未取代的,当被取代时,取代基优选为一个或多个以下基团,独立地选自卤素、羟基、巯基、氰基、硝基、叠氮基、c1-8烷基、c3-8环烷基、3~8元杂环基、c1-8烷氧基或3~8元杂环基氧基。
181、本发明中“杂环基”指饱和或部分不饱和单环或多环环状烃取代基,其中一个或多个环原子选自氮、氧或s(o)m(其中m是整数0、1、2)的杂原子,但不包括-o-o-、-o-s-或-s-s-的环部分,其余环原子为碳。“4~10元杂环基”指包含4至10个环原子的环基,“4~12元杂环基”指包含4至12个环原子的环基。单环杂环基的非限制性实施例包含氧杂环丁基、吡咯烷基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、高哌嗪基等。多环杂环基包括螺环、稠环和桥环的杂环基。
182、本发明中“烷氧基”指-o-(烷基),其中烷基的定义如上所述。“c1-8烷氧基”指含1-8个碳的烷基氧基,非限制性实施例包含甲氧基、乙氧基、丙氧基、丁氧基等。
183、“卤素”指氟、氯、溴或碘。
184、“药物组合物”表示含有一种或多种本文所述化合物或其生理学上可药用的盐或前体药物与其他化学组分的混合物,以及其他组分例如生理学可药用的载体和赋形剂。药物组合物的目的是促进对生物体的给药,利于活性成分的吸收进而发挥生物活性。
185、“”代表取代基的连接键。
186、本发明制备步骤中,所用试剂的缩写分别表示:
187、dcm 二氯甲烷
188、thf 四氢呋喃
189、ea 乙酸乙酯
190、pe 石油醚
191、dmf n,n-二甲基甲酰胺
192、cdi 羰基二咪唑
193、tbtu o-苯并三氮唑-n,n,n’,n’-四甲基脲四氟硼酸
- 还没有人留言评论。精彩留言会获得点赞!