包含成纤维细胞活化蛋白配体的化合物及其用途的制作方法
本发明涉及化合物;成纤维细胞活化蛋白(fap)抑制剂;分别包含所述化合物和抑制剂的组合物;分别用于疾病诊断方法的所述化合物、所述抑制剂和所述组合物;分别用于疾病治疗方法的所述化合物、所述抑制剂和所述组合物;分别用于疾病的诊断和治疗(也称作“治疗诊断(thera(g)nosis)”或“治疗诊断学(thera(g)nostics)”)方法的所述化合物、所述抑制剂和所述组合物;分别用于将效应物递送至表达fap的组织的方法中的所述化合物、所述抑制剂和所述组合物;分别使用所述化合物、所述抑制剂和所述组合物诊断疾病的方法;分别使用所述化合物、所述抑制剂和所述组合物治疗疾病的方法;分别使用所述化合物、所述抑制剂和所述组合物诊断和治疗疾病(也称作“治疗诊断”或“治疗诊断学”)的方法;分别使用所述化合物、所述抑制剂和所述组合物将效应物递送至表达fap的组织的方法。
背景技术:
1、尽管治疗选择越来越多,但癌症仍然是全球第二大死亡原因。治疗策略主要集中在靶向恶性癌细胞本身,而忽略了限制癌细胞治疗剂进入的始终存在的围绕肿瘤的微环境(tme)(valkenburg,et al.,nat rev clin oncol,2018,15:366)。tme是肿瘤团块的一部分,不仅包含异质的癌细胞群,还包含各种驻留和浸润的宿主细胞、分泌的因子和细胞外基质蛋白(quail,et al.,nat med,2013,19:1423)。在tme中发现的主要细胞类型是癌症相关成纤维细胞(caf)(kalluri,nat rev cancer,2016,16:582)。许多不同的细胞类型已被描述为caf的来源和起源,例如成纤维细胞、间充质干细胞、平滑肌细胞、上皮来源的细胞或内皮细胞(madar,et al.,trends mol med,2013,19:447)。caf表现出间充质样特征,并且通常是实体瘤团块中的主要细胞类型。caf作为肿瘤进展和体内平衡的参与者受到越来越多的关注(gascard,et al.,genes dev,2016,30:1002;lebleu,et al.,dis model mech,2018,11)。
2、近年来,成纤维细胞活化蛋白(fap)作为caf的标志物而广为人知(shiga,et al.,cancers(basel),2015,7:2443;pure,et al.,oncogene,2018,37:4343;jacob,et al.,curr mol med,2012,12:1220)。由于肿瘤内caf和间质的无所不在,fap被发现是放射性药物诊断的合适标志物和放射性药物治疗的合适靶点(siveke,j nucl med,2018,59:1412)。
3、成纤维细胞活化蛋白α(fap)是ii型跨膜丝氨酸蛋白酶和s9脯氨酰寡肽酶家族的成员(park,et al.,j biol chem,1999,274:36505)。最接近的家庭成员dpp4与fap有53%的同源性。与其它dpp酶(dpp4、dpp7、dpp8、dpp9)一样,fap具有后脯氨酸外肽酶活性。此外,fap具有内肽酶活性,类似于脯氨酰寡肽酶/内肽酶(pop/prep)。fap基因在不同物种中高度保守。人fap的胞外域与小鼠和大鼠fap具有90%的氨基酸序列相同性。小鼠fap与大鼠fap具有97%的序列相同性。
4、在结构上,fap是一种760个氨基酸的跨膜蛋白,包含一个短的n末端胞质尾区(6个氨基酸)、一个单一的跨膜结构域(20个氨基酸)和一个734个氨基酸的胞外域(aertgeerts,et al.,j biol chem,2005,280:19441)。这个胞外域由一个八叶β-螺旋(eight-bladedβ-propeller)和一个α/β水解酶结构域组成。催化三联体由ser624、asp702和his734组成,位于β-螺旋和水解酶结构域的界面。可通过β-螺旋域的中心孔或通过β-螺旋与水解酶结构域之间的狭窄空腔接近活性位点。fap单体没有活性,但与dpp4形成活性同二聚体以及异二聚体(ghersi,et al.,cancer res,2006,66:4652)。还有人描述了可溶的同二聚体fap(keane,et al.,febs open bio,2013,4:43;lee,et al.,blood,2006,107:1397)。
5、fap具有双重酶活性(hamson,et al.,proteomics clin appl,2014,8:454)。其二肽基肽酶活性允许裂解在脯氨酸残基后的n末端的两个氨基酸。通过其二肽基肽酶活性快速裂解的fap底物是神经肽y、肽yy、p物质和b型利钠肽。已表明胶原蛋白i和iii、成纤维细胞生长因子(fgf21)和α2-抗纤溶酶被fap的内肽酶活性裂解。虽然fap无法裂解天然胶原蛋白,但通过其它蛋白酶如基质金属蛋白酶的预消化促进fap进一步裂解胶原蛋白。胶原蛋白的加工可能影响癌细胞的迁移能力。除了通过细胞外基质的重塑增加癌细胞的侵润性外,还提出了其它几种fap介导的肿瘤促进作用,包括增殖和增加血管生成。此外,fap的间质表达与各种癌症的免疫监视脱逃有关,表明其在抗肿瘤免疫中的作用(pure,et al.,oncogene,2018,37:4343)。
6、fap在正常发育过程中短暂表达,但很少在健康的成年组织中表达。在转基因小鼠中,已证明fap由脂肪组织、骨骼肌、皮肤、骨骼和胰腺表达(pure,et al.,oncogene,2018,37:4343;roberts,et al.,j exp med,2013,210:1137)。然而,fap敲除小鼠具有健康的表型,表明在正常条件下具有多余的作用(niedermeyer,et al.,mol cell biol,2000,20:1089)。在活跃的组织重塑部位,包括伤口愈合、纤维化、关节炎、动脉粥样硬化和癌症,fap在间质细胞中高度上调(pure,et al.,oncogene,2018,37:4343)。
7、在单克隆抗体f19的使用下,于1990年首次报道了fap在90%的上皮癌的肿瘤间质中的表达(garin-chesa,et al.,proc natl acad sci u s a,1990,87:7235;rettig,etal.,cancer res,1993,53:3327)。表达fap的间质细胞被进一步鉴定为癌症相关成纤维细胞(caf)和癌症相关周细胞(cremasco,et al.,cancer immunol res,2018,6:1472)。恶性上皮细胞上的fap表达也有报道,但其意义仍有待确定(pure,et al.,oncogene,2018,37:4343)。下表1摘自busek et al.(busek,et al.,front biosci(landmark ed),2018,23:1933),总结了fap在各种恶性肿瘤中的表达,指示了肿瘤类型和细胞表达。
8、表1:在人恶性肿瘤中的fap表达(来自busek et al.)
9、
10、
11、
12、几乎所有癌和肉瘤都显示了fap在caf中的表达(pure,et al.,oncogene,2018,37:4343;busek,et al.,front biosci(landmark ed),2018,23:1933)。此外,caf存在于血液系统恶性肿瘤中(raffaghello,et al.,oncotarget,2015,6:2589)。因此,将fap用作治疗靶标不限于某些肿瘤实体。
13、许多表达fap的caf被描述为与不良预后相关。在广泛的人肿瘤适应症中,fap表达被描述为与较高的肿瘤等级和较差的总生存率相关(pure,et al.,oncogene,2018,37:4343)。
14、如上所述,表明存在于肿瘤微环境中的fap以及表达fap的细胞显著影响肿瘤进展(hanahan,etal.,cancer cell,2012,21:309)。此外,如下所述,由于其在肿瘤中的相对选择性表达,fap被视为治疗和诊断剂的合适靶标(siveke,j nucl med,2018,59:1412;christiansen,et al.,neoplasia,2013,15:348;zi,et al.,mol med rep,2015,11:3203)。
15、在发现后不久,fap就被用作癌症的治疗靶标。直到今天,已经探索了各种策略,包括例如fap酶活性的抑制、fap阳性细胞的消融或细胞毒性化合物的靶向递送。
16、在2007年,point therapeutics开发了fap和dpp4抑制剂talabostat(val-boro-pro,pt-100)(例如美国专利号6,890,904或公开的国际专利申请wo9916864中所述)。pennisi等人(pennisi,et al.,br jhaematol,2009,145:775)在多发性骨髓瘤动物模型以及癌症同源小鼠模型中观察到肿瘤生长减少。此外,已经开发并报道了几种其它的脯氨酰硼酸衍生物作为fap的推定选择性抑制剂。这些衍生物在生理ph值的水相环境中表现出不稳定性(coutts,et al.,j med chem,1996,39:2087)并且与其它酶具有非特异性反应性。
17、wo 2008/116054公开了六肽衍生物,其中化合物包含c-末端双氨基或硼酸官能团。
18、us2017/0066800公开了对fap有效的假肽抑制剂,例如m83。这些抑制剂在免疫缺陷小鼠的肺癌和结肠癌异种移植物中进行了评估。观察到肿瘤生长的抑制(jackson,etal.,neoplasia,2015,17:43)。这些假肽抑制脯氨酰寡肽酶(pop/prep)和fap的活性,因此排除了其作为特异性治疗性fap抑制剂的应用。
19、us2008/280856公开了一种基于纳摩尔硼酸的抑制剂。所述抑制剂显示出对fap和prep的双特异性抑制,从而排除了其作为特异性治疗性fap抑制剂的应用。
20、基于环状肽的fap抑制剂公开于例如wo 2016/146174和wo 2006/042282中。wo2016/146174公开了用于诊断和治疗表达fap的肿瘤的肽,显示出对fap的特异性,由此所述肽不识别密切相关的同源物dpp4。wo 2006/042282公开了治疗黑色素瘤的多肽。在裸鼠中,显示出对黑色素瘤生长和黑色素瘤转移的抑制作用。
21、wo 99/75151和wo 01/68708公开了人源化fap单克隆抗体f19(sibrotuzumab)。此外,wo 99/57151和wo 01/68708中公开了抗fap抗体f19及其人源化形式。开发方法涉及例如产生转化为二价衍生物的高亲和力、物种交叉反应性、fap特异性的scfv(brocks,etal.,mol med,2001,7:461)。在i期和ii期临床试验中,sibrotuzumab在转移性结直肠癌患者中显示出特异性肿瘤富集,但未能证明可测量的治疗活性,17名患者中只有2名病情稳定(hofheinz,et al.,onkologie,2003,26:44)。该f19抗体并未显示出阻断fap的任何细胞或蛋白酶功能,这可能解释了没有治疗效果的原因(hofheinz,et al.,onkologie,2003,26:44;scott,et al.,clin cancer res,2003,9:1639)。
22、us2018/022822公开了与人fap及其表位特异性结合的新分子,作为人源抗体和嵌合抗原受体(car),可用于治疗由fap诱发的疾病和病症。用抗fap抗体治疗携带常位同基因mc38结肠直肠肿瘤的小鼠降低肿瘤直径和转移数目。wo 2012/020006公开了在fc区带有修饰寡糖的糖工程化(glycoengineered)抗体。随后,根据wo 2014/161845,开发了对fap和dr5具有特异性的双特异性抗体。这些抗体在具有fap阳性间质的体外和体内临床前肿瘤模型中引起肿瘤细胞凋亡(brunker,etal.,mol cancer ther,2016,15:946)。wo 2015/118030中描述了靶向fap的抗体药物缀合物和免疫毒素。在应用抗hu/mofap hu36:溶细胞素adc候选物后,显示出体外毒性以及体内肿瘤生长抑制作用。目前尚不清楚这些抗体是否能够抑制fap活性。
23、jansen等人(jansen,et al.,j med chem,2014,57:3053;jansen,et al.,acsmed chem lett,2013,4:491)描述了基于(4-喹啉酰)甘氨酰-2-氰基吡咯烷的((4-quinolinoyl)glycyl-2-cyanopyrrolidine)小分子fap抑制剂,其显示出对相关的dpp和prep具有低纳摩尔抑制效力和高选择性,并在wo 2013/107820中公开。然而,这些化合物在结构上与本发明的化合物无关并且包括导致与fap共价结合的弹头。
24、近年来,开发了一些靶向fap的放射性药物方法,这些方法在本文中进行了示例性描述。
25、wo 2010/036814公开了通过抑制fap酶活性用作治疗剂或通过与fap结合用作放射性药物的fap小分子抑制剂。
26、wo 2019/083990公开了基于jansen等人(jansen,et al.,j med chem,2014,57:3053;jansen,et al.,acs med chem lett,2013,4:491)描述的小分子fap抑制剂的成像和放疗剂。此外,几位作者描述了基于jansen等人(jansen,et al.,j med chem,2014,57:3053;jansen,et al.,acs med chem lett,2013,4:491)描述的fap抑制剂的成像和放疗剂在癌症患者肿瘤中的选择性摄取(lindner,et al.,j nucl med,2018,59:1415;loktev,etal.,j nucl med,2018,59:1423;giesel,et al.,j nucl med,2019,60:386;loktev,etal.,j nucl med,2019,mar 8(epub ahead of print);giesel,et al.,eur j nucl medmol imaging,2019,46:1754;kratochwil,et al.,j nucl med,2019,60:801)。
27、对131i标记的人源化形式的f19抗体(sibrotuzumab)的临床评估显示了在结直肠癌或非小细胞肺癌患者中被肿瘤而不是被正常组织选择性摄取(scott,et al.,clincancer res,2003,9:1639)。这可能是由于抗体的循环时间长,使其不适用于涉及放射性核素的诊断、治疗或治疗诊断方法。
28、wo 2011/040972公开了识别人和鼠fap抗原的高亲和力抗体作为强力的放射免疫缀合物。esc11 igg1诱导表面fap的下调和内在化(fischer,et al.,clin cancer res,2012,18:6208)。wo 2017/211809公开了组织靶向性钍-227络合物,其中靶向部分对fap具有特异性。然而,抗体的长循环时间使其不适合涉及放射性核素的诊断、治疗或治疗诊断方法。
29、fap还被描述为涉及除肿瘤学适应症以外的其它疾病,其示例如下。
30、患者类风湿性关节炎关节中的成纤维细胞样滑膜细胞显示fap的表达显著增加(bauer,et al.,arthritis res ther,2006,8:r171;milner,et al.,arthritis resther,2006,8:r23)。在类风湿性关节炎中,间质细胞通过产生细胞外基质成分、募集浸润性免疫细胞和分泌炎症介质,在关节滑膜组织结构的组构中发挥重要作用。存在大量证据支持这些细胞在驱动炎症和关节损伤持续存在方面的作用(bartok,et al.,immunol rev,2010,233:233;turner,et al.,curr opin rheumatol,2015,27:175)。在类风湿性关节炎中,至少通过促进蛋白多糖损失和随后的软骨降解,fap在软骨转换中具有病理学作用(bauer,et al.,arthritis res ther,2006,8:r171;waldele,et al.,arthritis resther,2015,17:12)。因此,其可以作为患者分层的标志,用于对治疗成功进行评估和随访,或作为治疗靶标(bauer,et al.,arthritis res ther,2006,8:r171)。在小鼠中,使用99mtc标记的抗fap抗体的spect/ct成像证明了治疗反应(van der geest,et al.,rheumatology(oxford),2018,57:737;laverman,et al.,j nucl med,2015,56:778;van der geest,etal.,j nucl med,2017,58:151)。
31、此外,fap不仅被认为是损伤反应中活化的成纤维细胞的标志物(tillmanns,etal.,int j cardiol,2013,168:3926),而且还是伤口愈合过程中的重要参与者(ramirez-montagut,et al.,oncogene,2004,23:5435)。jing等人证明了大鼠烧伤后fap表达变化的时间依赖性过程(jing,et al.,nan fang yi ke da xue xue bao,2013,33:615)。在瘢痕疙瘩疤痕(常见的良性纤维增生性网状真皮病变)中抑制反应性创伤成纤维细胞中的fap活性可能提供预防疾病进展的治疗选择(dienus,et al.,arch dermatol res,2010,302:725)。
32、在纤维化疾病中,观察到fap表达上调,例如在特发性肺纤维化、克罗恩病和肝纤维化中。在克罗恩病(一种特征在于过度的、失衡的细胞外基质(ecm)沉积的慢性肠道炎性疾病)的离体模型中,观察到fap表达上调。fap抑制重建了细胞外基质稳态(truffi,etal.,inflamm bowel dis,2018,24:332)。egger等人(egger,et al.,eur j pharmacol,2017,809:64)使用肺纤维化鼠模型也进行了类似的观察。fap的抑制导致纤维化病理减少。fap也在慢性损伤肝脏的组织重塑区表达(wang,et al.,front biosci,2008,13:3168),肝星状细胞的fap表达与肝病的组织学严重程度相关(gorrell,et al.,adv exp med biol,2003,524:235)。因此,fap也是治疗肝纤维化的一个很有前景的靶标(lay,et al.,frontbiosci(landmark ed),2019,24:1)。
33、fap在动脉硬化病变中表达并在活化的血管平滑肌细胞中上调(monslow,et al.,circulation,2013,128:a17597)。monslow等人表明在动脉硬化病变中靶向抑制fap可以降低整体病变负担,抑制炎症细胞归巢,并经由其通过有利于富含基质的病变而非炎症来改变病变结构的能力来增加病变稳定性。更重要的是,大多数动脉硬化病变具有共同的致病特征:动脉粥样硬化斑块破裂引起动脉硬化病变(davies,et al.,br heart j,1985,53:363;falk,am j cardiol,1989,63:114e)。晚期动脉粥样硬化斑块中纤维帽的破裂是急性冠状动脉综合征的关键触发因素,可以导致心肌梗塞和心源性猝死。促进斑块不稳定的关键事件之一是纤维帽的降解,这将潜在的血栓形成斑块核心暴露于血流,从而导致血栓形成和随后的血管闭塞(farb,et al.,circulation,1996,93:1354;virmani,et al.,j amcoll cardiol,2006,47:c13)。brokopp等人表明fap有助于纤维帽中i型胶原蛋白分解(brokopp,et al.,eur heart j,2011,32:2713)。开发了放射性标记的示踪剂,并显示了其对动脉粥样硬化成像的适用性(meletta,et al.,molecules,2015,20:2081)。
技术实现思路
1、本发明所基于的问题是提供适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话。本发明所基于的另一个问题是提供适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话,从而所述化合物是fap活性的有力抑制剂;优选所述化合物的pic50等于或大于6.0。本发明所基于的另一个问题是提供在疾病诊断和/或治疗中适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话,其中病变细胞和/或病变组织表达fap。本发明所基于的再一个问题是提供一种化合物,所述化合物适于分别将诊断和/或治疗有效药剂递送至病变细胞和/或病变组织,更特别地是表达fap的病变细胞和/或病变组织,优选所述病变组织包含或含有癌症相关的成纤维细胞。另外,本发明所基于的问题是提供用于诊断疾病的方法、用于治疗和/或预防疾病的方法,以及用于组合地诊断与治疗疾病的方法;优选地,这种疾病是涉及表达fap的细胞和/或组织,更特别是表达fap的病变细胞和/或病变组织的疾病,优选所述病变组织包含或含有癌症相关的成纤维细胞。本发明所基于的另一个问题是提供用于鉴定个体的方法,其中所述个体对疾病的治疗可能有反应或可能没有反应;用于从一组个体选择个体的方法,其中所述个体对疾病的治疗可能有反应或可能没有反应。此外,本发明所基于的问题是提供含有具有上述特征的化合物的药物组合物。进一步地,本发明所基于的问题是提供适用于任何上述方法的药剂盒。
2、需要适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话。此外,需要适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话,从而所述化合物是fap活性的有力抑制剂;优选所述化合物的pic50等于或大于6.0。此外,需要在疾病诊断和/或治疗中适合作为诊断剂和/或药剂的化合物,特别是如果与诊断和/或治疗活性效应物缀合的话,其中病变细胞和/或病变组织表达fap。此外,需要一种化合物,其适于分别将诊断和/或治疗有效药剂递送至病变细胞和/或病变组织,更特别地是表达fap的病变细胞和/或病变组织,优选所述病变组织包含或含有癌症相关的成纤维细胞。另外,需要用于诊断疾病的方法、用于治疗和/或预防疾病的方法,以及组合地诊断和治疗疾病的方法;优选地,这种疾病是涉及表达fap的细胞和/或组织、更特别是表达fap的病变细胞和/或病变组织的疾病,优选所述病变组织包含或含有癌症相关的成纤维细胞。进一步地,需要用于鉴定个体的方法,其中所述个体对疾病的治疗可能有反应或可能没有反应;用于从一组个体选择个体的方法,其中所述个体对疾病的治疗可能有反应或可能没有反应。此外,需要含有具有上述特征的化合物的药物组合物。此外,需要适用于任何上述方法的药剂盒。本发明满足了这些需要。
3、这些和其它问题由所附权利要求的主题解决。
4、本发明所基于的这些和其它问题也由以下实施方案解决。
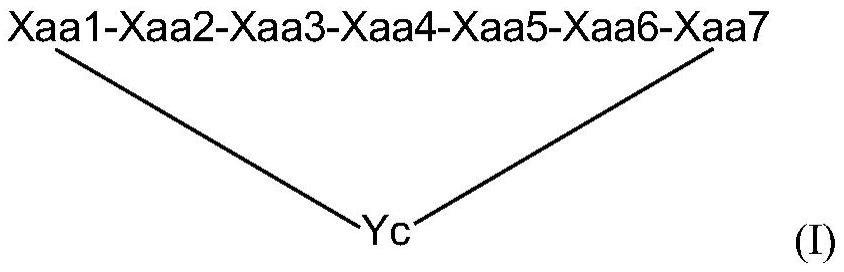
5、更具体而言,本发明所基于的问题在第一方面(其也是第一方面的第一实施方案)中通过包含式(i)的环状肽和连接于xaa1的n末端修饰基团a的化合物来解决:
6、
7、其中:
8、所述肽序列是以n末端至c末端的方向从左至右绘制的,
9、xaa1是式(ii)的氨基酸残基,
10、
11、其中:
12、r1a是-nh-,
13、r1b和r1c各自且彼此独立地是h或ch3,
14、n=0或1,
15、所述n末端修饰基团a共价连接于xaa1的氮原子,
16、xaa1的羰基共价连接于xaa2的氮;
17、xaa2是式(iii)、(iv)或(xx)的氨基酸残基,
18、
19、其中:
20、r2a、r2b、r2c各自且独立地选自(c1-c2)烷基和h,其中所述(c1-c2)烷基可以被选自oh、nh2、卤素、(c5-c7)环烷基的取代基取代,
21、p=0、1或2
22、v=1或2
23、w=1、2或3,以及
24、所述式(iv)的氨基酸任选地在所示的环位置3和/或4处被各自且独立地选自甲基、oh、nh2和f的一个或两个取代基取代;
25、xaa3是式(v)或(xx)的氨基酸残基,
26、
27、其中:
28、x3选自ch2、cf2、ch-r3b、s、o和nh,
29、p=1或2
30、v=1或2
31、w=1、2或3,
32、r3a是h、甲基、oh、nh2或f,
33、r3b是甲基、oh、nh2或f;
34、xaa4是式(vi)的氨基酸残基,
35、
36、其中:
37、r4a选自h、oh、cooh、conh2、x4和-nh-co-x4,其中x4选自(c1-c6)烷基、(c5-c6)芳基和(c5-c6)杂芳基,并且x4可以被各自且独立地选自甲基、conh2、卤素、nh2和oh的一个或两个取代基取代;
38、q=1、2或3,其中所述1个、2个或3个ch2-基团的一个或两个氢任选地各自且独立地被甲基、乙基、(c5-c6)芳基或(c5-c6)杂芳基取代,
39、r4b是甲基或h;
40、xaa5是结构(vii)的氨基酸残基,
41、
42、其中:
43、r5选自oh和nh2,以及
44、r=1、2或3;
45、xaa6是选自芳族l-α-氨基酸和杂芳族l-α-氨基酸的氨基酸的残基;
46、xaa7是式(ix)的氨基硫醇或氨基酸残基,
47、
48、其中:
49、r7a选自-co-、-cooh、-conh2、-ch2-oh、-(co)-nh-r7b、-(co)-(nr7c)-r7b和h,其中r7b和r7c各自且独立地是(c1-c4)烷基,以及
50、t是1或2;
51、yc是式(x)的环化元件,其存在或不存在,
52、
53、其中如果yc不存在,则xaal的s原子和xaa7的s原子彼此共价连接,形成式(xxii)的环状结构,
54、
55、其中:
56、n=0或1,
57、t=1或2,
58、以及
59、其中如果yc存在,则xaa1的s原子通过硫醚键连接至yc,并且xaa7的s原子通过硫醚键连接至yc,形成式(xxi)的环状结构,
60、
61、其中:
62、n=0或1,
63、t=1或2,
64、其中所述n-末端修饰基团a是保护基abl或氨基酸aaa。
65、在第一方面的第二实施方案(其也是第一方面的第一实施方案的一个实施方案)中,yc是式(xiii)的结构:
66、
67、其中rc1是h、(c1-c6)烷基或式(xi)、(xii)或(xxii)的结构,
68、
69、其中rc2是h或z基团,其中z基团包含螯合剂和任选存在的接头,
70、f=1、2、3、4、5或6,
71、g和h各自且彼此独立地是1或2,
72、i是0至36之间的整数,并且
73、k=1、2、3或4。
74、在第一方面的第三实施方案(其也是第一方面的第二实施方案的一个实施方案)中,rc2是包含螯合剂基团和任选存在的接头的z基团。
75、在第一方面的第四实施方案中(也是第一方面的第三实施方案的一个实施方案),所述接头选自ttds、o2oc、apac、gly、bal、gab、mamb、pamb、ppac、4amc、inp、sni、rni、nmg、cmp、peg6、peg12和其它peg-氨基酸,优选选自ttds、o2oc、apac、4amc、peg6和peg12,并且最优选所述接头选自ttds、o2oc和peg6。
76、在第一方面的第五实施方案(也是第一方面的第一、第二、第三和第四实施方案的一个实施方案)中,所述保护基abl选自ra1-c(o)-、ra1-s(o2)-、ra1-nh-c(o)-和ra1-o-c(o)-;其中ra1是任选被至多两个取代基取代的(c1-c8)烷基,所述取代基各自且独立地选自oh、f、cooh、(c3-c8)环烷基、芳基、杂芳基和(c3-c8)杂环,并且其中在(c1-c8)烷基中,一个-ch2-基团任选被-s-或-o-置换。
77、在第一方面的第六实施方案(也是第一方面的第五实施方案的一个实施方案)中,所述保护基abl是己酰基、buca、buur或戊磺酰基,优选所述保护基abl是己酰基或buur。
78、在第一方面的第七实施方案(也是第一方面的第一、第二、第三和第四实施方案的一个实施方案)中,所述氨基酸aaa是d-氨基酸残基或l-氨基酸残基,其均具有结构(xiv):
79、
80、其中:
81、ra2选自(c1-c6)烷基、修饰的(c1-c6)烷基、(c1-c3)烷基、修饰的(c1-c3)、(c3-c8)碳环、芳基、杂芳基和(c3-c8)杂环,其中在修饰的(c1-c6)烷基中,一个-ch2-基团被-s-或-o-置换,并且在修饰的(c1-c3)烷基中,一个h被oh、f或cooh取代,或两个h被f取代。
82、在第一方面的第八个实施方案(也是第一方面的第七个实施方案的一个实施方案)中,aaa选自nle、nle、met和met及其衍生物的氨基酸残基。
83、在第一方面的第九实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七和第八实施方案的一个实施方案)中,xaa1是选自cys、hcy和pen的d-氨基酸残基,或xaa1是选自cys、hcy和pen的l-氨基酸残基。
84、在第一方面的第十实施方案(也是第一方面的第九实施方案的一个实施方案)中,xaa1是选自cys和hcy的d-氨基酸残基,或者xaa1是选自cys和hcy的l-氨基酸残基。
85、在第一方面的第十一实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九和第十实施方案的一个实施方案)中,xaa2是选自pro、gly、nmg及其衍生物的氨基酸残基,其中xaa3是选自pro、hyp、tfp、cfp、dmp、aze和pip及其衍生物的氨基酸残基,其中xaa4是选自thr、hse、asn、gln和ser及其衍生物的氨基酸残基,其中xaa5是选自gln和glu及其衍生物的氨基酸残基,
86、其中xaa6是式(viiia)、(viiib)、(viiic)和(viiid)中任一式的氨基酸残基:
87、
88、其中:
89、r6a和r6b各自且独立地选自h、甲基、乙基、丙基和异丙基,
90、r6c代表0至3个取代基,每个这样的取代基各自且独立地选自cl、f、br、no2、nh2、cn、cf3、oh、or6d和c1-c4烷基,
91、r6d选自甲基、乙基、丙基和异丙基,
92、s是0或1,并且
93、其中xaa7是选自cys、cysol、aet、hcy、cys和hcy的氨基硫醇残基。
94、在第一方面的第十二实施方案(也是第一方面的第十一实施方案的一个实施方案)中,xaa6是式(viiia)的氨基酸残基,
95、
96、其中r6c代表0至2个取代基,每个这样的取代基各自且独立地选自cl、f、br、no2、nh2、cn、cf3、oh、o-r6d和甲基。
97、在第一方面的第十三实施方案(也是第一方面的第十二实施方案的一个实施方案)中,r6c表示0至1个取代基。
98、在第一方面的第十四实施方案(也是第一方面的第十三实施方案的一个实施方案)中,r6c代表在邻位或间位键合的1个取代基。
99、在第一方面的第十五实施方案(也是第一方面的第十三和第十四实施方案的一个实施方案)中,xaa6是选自phe、tyr、ocf和mcf的氨基酸残基。
100、在第一方面的第十六实施方案(也是第一方面的第十二、第十三、第十四和第十五实施方案、优选第一方面的第十五实施方案的一个实施方案)中,r6c各自且独立地选自cl、br、cf3和cn。
101、在第一方面的第十七实施方案(也是第一方面的第十二、第十三、第十四、第十五和第十六实施方案的一个实施方案)中,r6a和r6b各自为h。
102、在第一方面的第十八实施方案(也是第一方面的第十一实施方案的一个实施方案)中,xaa6是式(viiib)、(viiic)和(viiid)中任一式的氨基酸残基:
103、
104、其中r6c代表0至2个取代基,每个这样的取代基各自且独立地选自cl、f、br、no2、nh2、cn、cf3、oh、o-r6d和甲基。
105、在第一方面的第十九实施方案(也是第一方面的第十八实施方案的一个实施方案)中,r6c表示0至1个取代基,其中,如果存在,则所述取代基选自cl、f、br、no2、nh2、cn、cf3、oh、o-r6d和甲基。
106、在第一方面的第二十实施方案(也是第一方面的第十八和第十九实施方案的一个实施方案)中,s是0。
107、在第一方面的第二十一实施方案(也是第一方面的第十八、第十九和第二十实施方案的一个实施方案)中,r6c选自cl、br、cf3和cn。
108、在第一方面的第二十二实施方案(也是第一方面的第十八、第十九、第二十和第二十一实施方案的一个实施方案)中,r6a和r6b各自是h。
109、在第一方面的第二十三实施方案(也是第一方面的第十八、第十九、第二十和第二十二实施方案的一个实施方案)中,xaa6是选自由ppa、mpa、thi和1ni的氨基酸残基。
110、在第一方面的第二十四实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二和第二十三实施方案的一个实施方案)中,其中,xaa2是pro,xaa3是pro,xaa4是thr,xaa5是选自gln和glu的氨基酸残基,xaa6是phe,并且xaa7是选自cys和hcy的氨基硫醇残基。
111、在第一方面的第二十五实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三和第二十四实施方案的一个实施方案)中,所述化合物是式(li)(seq id no:50和51)、式(lii)(seq id no:52和53)、式(liii)(seq id no:54和55)或式(liv)的化合物:
112、
113、
114、其中x1是-nh-或-ch2-,以及y1是-nh2或-oh。
115、在第一方面的第二十六实施方案(也是第一方面的第一、第二、第三、第四、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三、第二十四和第二十五实施方案的一个实施方案)中,所述n-末端修饰基团a是氨基酸aaa,并且其中所述化合物包含共价连接至所述氨基酸aaa的z基团,其中所述z基团包含螯合剂和任选存在的接头,其中,如果存在该接头,则所述接头将所述螯合剂共价连接至所述氨基酸aaa,优选连接至所述氨基酸aaa的α-氮,优选所述接头与所述氨基酸aaa的α-氮之间的共价键接是酰胺。
116、在第一方面的第二十七实施方案(也是第一方面的第二十六实施方案的一个实施方案)中,所述接头选自ttds、o2oc、apac、gly、bal、gab、mamb、pamb、ppac、4amc、inp、sni、rni、nmg、cmp、peg6、peg12和其它peg-氨基酸,更优选ttds、o2oc、apac、4amc、peg6和peg12,并且最优选所述接头选自ttds、o2oc和peg6。
117、在第一方面的第二十八实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三、第二十四、第二十五、第二十六和第二十七实施方案的一个实施方案)中,氨基酸或肽连接至xaa7,其中该肽的大多数氨基酸是荷电的或极性的,并且所述肽的净电荷为-2、-1、0、+1或+2,优选所述肽选自式(xxxa-f)的肽:
118、xaa10-xaa11-xaa12-xaa13-xaa14-xaa15-xaa16(xxxa)
119、xaa10-xaa11-xaa12-xaa13-xaa14-xaa15(xxxb)
120、xaa10-xaa11-xaa12-xaa13-xaa14 (xxxc)
121、xaa10-xaa11-xaa12-xaa13 (xxxd)
122、xaa10-xaa11-xaa12 (xxxe)
123、xaa10-xaa11 (xxxf)
124、其中:
125、xaa10是asp、asp、bal、gly、gab、ser、nmg、bhf、lys、ttds或bhk,
126、xaa11是his、his、lys、ttds、arg、ape或ala,
127、xaa12是phe、nmf、tic、aic、mpa、amf、nmf、phe、lys、ape、ttds和ppa,
128、xaa13是arg、lys、ape、ttds或arg,
129、xaa14是asp、ala、asp、lys、ape或ttds,
130、xaa15是ttds、ape或lys,并且
131、xaa16是lys或ape,
132、其中,任选地,
133、xaa11和xaa12一起形成选自gab、pamb、cmp、pamb、mamb的单个氨基酸,并且任选地,xaa10、xaa11和xaa12一起形成选自gab、pamb、cmp、pamb和mamb的单个氨基酸,
134、条件是在式(xxxa-f)的肽中,如果存在,则ape是c末端构件,
135、并且其中所述连接至xaa7的氨基酸是xaa17,其中xaa17是asp、asp、bal、gly、gab、ser、nmg、bhf、lys、ttds或bhk,并且其中xaa17的α-cooh官能度以游离cooh-基团存在或以conh2-基团存在。
136、在第一方面的第二十九实施方案(也是第一方面的第二十八实施方案的一个实施方案)中,z-基团共价连接至所述肽或其中z-基团共价连接至xaa17,其中在每种情况下z基团均包含螯合剂和任选存在的接头。
137、在第一方面的第三十实施方案(也是第一方面的第二十九实施方案的一个实施方案)中,所述螯合剂共价连接至与xaa17连接的氨基酸,或者所述螯合剂共价连接至所述肽的c末端氨基酸,优选式(li)、(lii)、(liii)和(liv)的肽中任一者的c末端氨基酸。
138、在第一方面的第三十一实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三、第二十四、第二十五、第二十六、第二十七、第二十八、第二十九和第三十实施方案的一个实施方案)中,所述螯合剂选自dota、dotaga、nota、nodaga、noda-mpaa、hbed、teta、cb-te2a、dtpa、dfo、macropa、hopo、trap、thp、data、notp、sarcophagine、fsc、neta、h4octapa、pycup、nxs4-x(n4、n2s2、n3s)、hynic、99mtc(co)3-螯合剂,更优选dota、dotaga、nota、nodaga、noda-mpaa、hbed、cb-te2a、dfo、thp、n4,并且最优选dota、dotaga、nota和nodaga。
139、在第一方面的第三十二实施方案(也是第一方面的第三十一实施方案的一个实施方案)中,所述螯合剂是dota。
140、在第一方面的第三十三实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三、第二十四、第二十五、第二十六、第二十七、第二十八、第二十九、第三十、第三十一和第三十二实施方案的一个实施方案)中,所述化合物选自以下一组化合物:
141、下式的化合物h-met-[cys-pro-pro-thr-glu-phe-cys]-asp-his-phe-arg-asp-nh2(1001)(seq id no:4):
142、
143、下式的化合物hex-[cys-pro-pro-thr-glu-phe-cys]-asp-his-phe-arg-asp-nh2(1002)(seq id no:5):
144、
145、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-glu-phe-cys]-asp-nh2(1003)(seq id no:6):
146、
147、下式的化合物dota-nle-[cys-pro-pro-thr-glu-phe-cys]-asp-nh2(1004)(seqid no:7):
148、
149、下式的化合物dota-o2oc-nle-[cys-pro-pro-thr-glu-phe-cys]-asp-his-phe-arg-asp-nh2(1005)(seq id no:8):
150、
151、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-glu-phe-cys]-asp-his-phe-arg-asp-nh2(1006)(seq id no:9):
152、
153、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-glu-phe-cys]-asp-pamb-arg-nh2(1007)(seq idno:10):
154、
155、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-gln-phe-cys]-asp-nh2(1008)(seq id no:8):
156、
157、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-gln-phe-cys]-oh(1009)(seqid no:9):
158、
159、下式的化合物dota-ttds-nle-[cys-pro-pro-thr-gln-phe-cys]-bal-oh(1010)(seq id no:10):
160、
161、下式的化合物hex-[cys-pro-pro-thr-gln-phe-cys]-bhk(dota)-oh(1011)(seqid no:11):
162、
163、下式的化合物hex-[cys-pro-pro-thr-glu-phe-cys]-bhk(dota)-oh(1012)(seqid no:12):
164、
165、下式的化合物hex-[cys-pro-pro-thr-glu-phe-cys]-asp-lys(dota)-nh2(1013)(seq id no:16):
166、
167、下式的化合物buur-[cys-pro-pro-thr-glu-phe-cys]-bhk(dota)-oh(1014)(seqid no:17):
168、
169、下式化合物buur-[cys-pro-pro-thr-glu-phe-cys]-asp-lys(dota)-nh2(1015)(seq id no:18):
170、
171、下式的化合物hex-[cys-pro-pro-thr-gln-phe-cys]-asp-lys(dota)-nh2(1016)(seq id no:19):
172、
173、下式的化合物nodaga-ttds-nle-[cys-pro-pro-thr-gln-phe-cys]-bal-oh(1018)(seq id no:20):
174、
175、下式的化合物n4ac-ttds-nle-[cys-pro-pro-thr-gln-phe-cys]-bal-oh(1019)(seq id no:21):
176、
177、下式的化合物hex-[cys-pro-pro-thr-glu-phe-cys]-asp-lys(nodaga)-nh2(1020)(seq id no:22):
178、
179、下式的化合物hex-[cys-pro-pro-thr-glu-phe-cys]-asp-lys(n4ac)-nh2(1021)(seq id no:23):
180、
181、下式的化合物hex-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-nh2(2001)(seqid no:24):
182、
183、下式的化合物hex-[hcy-pro-pro-thr-gln-phe-hcy]-asp-nh2(2002)(seq idno:25):
184、
185、下式的化合物dota-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-nh2(2003)(seq id no:26):
186、
187、下式的化合物dota-o2oc-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-nh2(2004)(seq id no:27):
188、
189、下式的化合物dota-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-nh2(2005)(seq id no:28):
190、
191、下式的化合物dota-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-pamb-arg-nh2(2006)(seq id no:29):
192、
193、下式的化合物dota-ttds-nle-[cys(mli)-pro-pro-thr-glu-phe-cys]-asp-nh2(2007)(seq id no:30):
194、
195、下式的化合物dota-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-oh(2008)(seq id no:31):
196、
197、下式的化合物dota-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-bal-oh(2009)(seq id no:32):
198、
199、下式的化合物hex-[cys(mli)-pro-pro-thr-gln-phe-cys]-bhk(dota)-oh(2010)(seq id no:33):
200、
201、下式的化合物hex-[cys(mli)-pro-pro-thr-glu-phe-cys]-bhk(dota)-oh(2011)(seq id no:34):
202、
203、下式的化合物hex-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-lys(dota)-nh2(2012)(seq id no:35):
204、
205、下式的化合物buur-[cys(mli)-pro-pro-thr-gln-phe-cys]-bhk(dota)-oh(2013)(seq id no:36):
206、
207、下式的化合物buur-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-lys(dota)-nh2(2014)(seq id no:37):
208、
209、下式的化合物hex-[cys(mli(me))-pro-pro-thr-gln-phe-cys]-asp-lys(dota)-nh2(2015)(seq id no:38):
210、
211、下式的化合物dota-ttds-nle-[cys(mli(me))-pro-pro-thr-gln-phe-cys]-asp-nh2(2016)(seq id no:39):
212、
213、下式的化合物hex-[cys(mli(dota-ttd))-pro-pro-thr-gln-phe-cys]-asp-nh2(2017)(seq id no:40):
214、
215、下式的化合物hex-[cys(mli(dota-eda))-pro-pro-thr-gln-phe-cys]-asp-nh2(2018)(seq id no:41):
216、
217、下式的化合物hex-[cys(mli(dota-ttd))-pro-pro-thr-gln-phe-cys]-oh(2019)(seq id no:42):
218、
219、下式的化合物hex-[cys(mli(dota-ttd))-pro-pro-thr-glu-phe-cys]-asp-nh2(2020)(seq id no:43):
220、
221、下式的化合物nodaga-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-bal-oh(2021)(seq id no:44):
222、
223、下式的化合物n4ac-ttds-nle-[cys(mli)-pro-pro-thr-gln-phe-cys]-bal-oh(2022)(seq id no:45):
224、
225、下式的化合物hex-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-lys(nodaga)-nh2(2023)(seq id no:46):
226、
227、下式的化合物hex-[cys(mli)-pro-pro-thr-gln-phe-cys]-asp-lys(n4ac)-nh2(2024)(seq id no:47):
228、
229、下式的化合物hex-[cys(mli(nodaga-ttd))-pro-pro-thr-gln-phe-cys]-asp-nh2(2025)(seq id no:48):
230、
231、下式的化合物hex-[cys(mli(n4ac-ttd))-pro-pro-thr-gln-phe-cys]-asp-nh2(2026)(seq id no:9):
232、
233、在第一方面的第三十四实施方案(也是第一方面的第一、第二、第三、第四、第五、第六、第七、第八、第九、第十、第十一、第十二、第十三、第十四、第十五、第十六、第十七、第十八、第十九、第二十、第二十一、第二十二、第二十三、第二十四、第二十五、第二十六、第二十七、第二十八、第二十九、第三十、第三十一、第三十二和第三十三实施方案一个实施方案)中,所述化合物包含诊断活性核素或治疗活性核素,其中优选所述诊断活性核素是诊断活性放射性核素,更优选选自43sc、44sc、51mn、52mn、64cu、67ga、68ga、86y,89zr、94mtc、99mtc、111in、152tb、155tb、177lu、201tl、203pb、18f、76br、77br、123i、124i、125i,优选43sc、44sc、64cu、67ga、68ga、86y,89zr、99mtc、111in、152tb、155tb、203pb、18f、76br、77br、123i、124i、125i,并且最优选选自64cu、68ga、89zr、99mtc、111in、18f、123i、和124i,并且其中所述治疗活性核素是治疗活性放射性核素,更优选选自47sc、67cu、89sr、90y、111in、153sm、149tb、161tb、177lu、186re、188re、212pb、213bi、223ra、225ac、226th、227th、131i、211at,优选选自47sc、67cu、90y、177lu、188re、212pb、213bi、225ac、227th、131i、211at,并且最优选选自90y、177lu、225ac、227th、131i和211at。
234、更具体地,本发明所基于的问题在第二方面通过用于诊断疾病的方法中的根据第一方面的化合物得以解决,包括其任何实施方案、特别是其实施方案1至34。
235、更具体而言,本发明所基于的问题在第三方面通过用于治疗疾病的方法中的根据第一方面的化合物得以解决,包括其任何实施方案、特别是其实施方案1至34。
236、更具体地,本发明所基于的问题在第四方面通过用于鉴定个体的方法中的根据第一方面的化合物得以解决,包括其任何实施方案和特别是其实施方案1至34,其中所述个体对疾病的治疗可能有反应或可能没有反应,其中用于鉴定个体的方法包括使用根据第一方面的化合物(包括其任何实施方案)进行诊断方法。
237、更具体地,本发明所基于的问题在第五方面通过用于从一组个体者中选择个体的方法中的根据第一方面的化合物得以解决,包括其任何实施方案、特别是其实施方案1至34,其中所述个体对疾病的治疗可能有反应或可能没有反应,其中从一组个体中选择个体的方法包括使用根据第一方面的化合物(包括其任何实施方案)进行诊断方法。
238、更具体地,本发明所基于的问题在第六方面通过用于对一组个体进行分层的方法中的根据第一方面的化合物得以解决,包括其任何实施方案、特别是其实施方案1至34,所述分层方法将一组个体分为对疾病的治疗可能有反应的个体和对疾病的治疗可能没反应的个体,其中对一组个体进行分层的方法包括使用根据第一方面的化合物(包括其任何实施方案)进行诊断方法。
239、更具体地,本发明所基于的问题在第七方面通过组合物、优选药物组合物得以解决,其中所述组合物包含根据第一方面的化合物,包括其任何实施方案、特别是其实施方案1至34,以及药学上可接受的赋形剂。
240、更具体地,本发明所基于的问题在第八方面通过诊断个体疾病的方法得以解决,其中所述方法包括向所述个体施用诊断有效量的根据第一方面的化合物,包括其任何实施方案、特别是其实施方案1至34。
241、更具体地,本发明所基于的问题在第九方面通过治疗个体疾病的方法得以解决,其中所述方法包括向个体施用治疗有效量的根据第一方面的化合物,包括其任何实施方案、特别是实施方案1至34。
242、更具体地,本发明所基于的问题在第十方面通过药剂盒得以解决,所述药剂盒包含根据第一方面的化合物,包括其任何实施方案和特别是其实施方案1至34,一种或多种任选的赋形剂和任选存在的一种或多种装置,其中所述装置选自标记装置、纯化装置、操作装置、放射防护装置、分析装置或施用装置。
243、本领域技术人员将认识到本发明的一种或所述化合物是本文公开的任何化合物,包括但不限于任何上述实施方案和任何以下实施方案中描述的任何化合物。
244、本领域技术人员将认识到本发明的一种或所述方法是本文公开的任何方法,包括但不限于任何上述实施方案和任何以下实施方案中描述的任何方法。
245、本领域技术人员将认识到本发明的一种或所述组合物是本文公开的任何组合物,包括但不限于任何上述实施方案和任何以下实施方案中描述的任何组合物。
246、本领域技术人员将认识到本发明的一种或所述药剂盒是本文公开的任何药剂盒,包括但不限于任何上述实施方案和任何以下实施方案中描述的任何药剂盒。
247、本发明是基于本发明人的惊人发现,即本发明的化合物、更特别是其环状肽提供包含这种环状肽的化合物与成纤维细胞活化蛋白(fap)的高度特异性结合,因为迄今为止还没有描述具有纳摩尔亲和性的基于fap特异性环状肽的抑制剂。
248、此外,本发明是基于令人惊讶的发现,即螯合剂可以直接或间接地(即,使用接头)在三个不同位置与所述环状肽连接。第一个位置是具有式(x)结构的yc,其连接xaa1的s原子和xaa7的s原子,从而形成两个硫醚键;第二个位置是连接于式(i)的环状肽的xaa1的aaa,以及第三个位置是连接于xaa7的氨基酸或肽。令人惊讶的是,这种螯合剂的连接不显著影响本发明化合物与fap的结合以及本发明化合物对fap的抑制特性。在一个实施方案中,本发明涉及式(i)的环状肽,其中螯合剂(z基团)连接在如上定义的第一个、第二个或第三个位置中的仅一个位置。也在本发明范围内的是所述螯合剂在如上定义的第一个、第二个和第三个位置的任意组合处连接于式(i)的环状肽。更具体地,本发明还涉及式(i)化合物,其中z基团连接于如上定义的第一和第二个位置,其中z基团连接于如上定义的第一和第三个位置的式(i)化合物,其中z基团连接于如上定义的第二和第三个位置的式(i)化合物,以及其中z基团连接于如上定义的第一、第二和第三个位置的式(i)化合物。包含两个或三个z基团的这些化合物可以在本文公开的本发明的任何实施方案中实现。
249、最后,本发明人发现本发明的化合物在血浆中惊人地稳定,而且惊人地可以用作显像剂以及有效地缩小肿瘤。
250、如本文优选使用的表述烷基各自且独立地指饱和的直链或支链烃基,并且通常伴随指定其可以含有的碳原子数的修饰语。例如,表述(c1-c6)烷基各自且独立地指以下基团的任意一个:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、1-甲基丁基、1-乙基-丙基、3-甲基-丁基、1,2-二甲基-丙基、2-甲基-丁基、1,1-二甲基-丙基、2,2-二甲基丙基、正己基、1,1-二甲基-丁基以及含有六个饱和碳原子的烷基的任何其它异构体中的任一者。
251、在一个实施方案中以及如本文优选使用的,(c1-c2)烷基各自且独立地指甲基和乙基中任一者。
252、在一个实施方案中以及如本文优选使用的,(c1-c3)烷基各自且独立地指甲基、乙基、正丙基和异丙基中任一者。
253、在一个实施方案中以及如本文优选使用的,(c1-c4)烷基各自且独立地指甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基和叔丁基中任一者。
254、在一个实施方案中以及如本文优选使用的,(c1-c6)烷基各自且独立地指以下任一者:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、2-戊基、2-甲基-丁基、3-甲基-丁基、3-戊基、3-甲基-丁-2-基、2-甲基-丁-2-基、2,2-二甲基丙基、正己基、2-己基、2-甲基-戊基、3-甲基-戊基、4-甲基-戊基、3-己基、2-乙基-丁基、2-甲基-戊-2-基、2,2-二甲基-丁基、3,3-二甲基-丁基、3-甲基-戊-2-基、4-甲基-戊-2-基、2,3-二甲基-丁基、3-甲基-戊-3-基、2-甲基-戊-3-基、2,3-二甲基-丁-2-基和3,3-二甲基-丁-2-基中。
255、在一个实施方案中以及如本文优选使用的,(c1-c8)烷基是指具有1至8个碳原子的饱和或不饱和的直链或支链烃基。代表性的(c1-c8)烷基包括但并不限于以下任一者:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、2-戊基、2-甲基-丁基、3-甲基-丁基、3-戊基、3-甲基-丁-2-基、2-甲基-丁-2-基、2,2-二甲基丙基、正己基、2-己基、2-甲基-戊基、3-甲基-戊基、4-甲基-戊基、3-己基、2-乙基-丁基、2-甲基-戊-2-基、2,2-二甲基-丁基、3,3-二甲基-丁基、3-甲基-戊-2-基、4-甲基-戊-2-基、2,3-二甲基-丁基、3-甲基-戊-3-基、2-甲基-戊-3-基、2,3-二甲基-丁-2-基、3,3-二甲基-丁-2-基、正庚基、2-庚基、2-甲基-己基、3-甲基-己基、4-甲基-己基、5-甲基-己基、3-庚基、2-乙基-戊基、3-乙基-戊基、4-庚基、2-甲基-己-2-基、2,2-二甲基-戊基、3,3-二甲基-戊基、4,4-二甲基-戊基、3-甲基-己-2-基、4-甲基-己-2-基、5-甲基-己-2-基、2,3-二甲基-戊基、2,4-二甲基-戊基、3,4-二甲基-戊基、3-甲基-己-3-基、2-乙基-2-甲基-丁基、4-甲基-己-3-基、5-甲基-己-3-基、2-乙基-3-甲基-丁基、2,3-二甲基-戊-2-基、2,4-二甲基-戊-2-基、3,3-二甲基-戊-2-基、4,4-二甲基-戊-2-基、2,2,3-三甲基-丁基、2,3,3-三甲基-丁基、2,3,3-三甲基-丁-2-基、正辛基、2-辛基、2-甲基-庚基、3-甲基-庚基、4-甲基-庚基、5-甲基-庚基、6-甲基-庚基、3-辛基、2-乙基-己基、3-乙基-己基、4-乙基-己基、4-辛基、2-丙基-戊基、2-甲基-庚-2-基、2,2-二甲基-己基、3,3-二甲基-己基、4,4-二甲基-己基、5,5-二甲基-己基、3-甲基-庚-2-基、4-甲基-庚-2-基、5-甲基-庚-2-基、6-甲基-庚-2-基、2,3-二甲基-己-1-基、2,4-二甲基-己-1-基、2,5-二甲基-己-1-基、3,4-二甲基-己-1-基、3,5-二甲基-己-1-基、3,5-二甲基-己-1-基、3-甲基-庚-3-基、2-乙基-2-甲基-1-基、3-乙基-3-甲基-1-基、4-甲基-庚-3-基、5-甲基-庚-3-基、6-甲基-庚-3-基、2-乙基-3-甲基-戊基、2-乙基-4-甲基-戊基、3-乙基-4-甲基-戊基、2,3-二甲基-己-2-基、2,4-二甲基-己-2-基、2,5-二甲基-己-2-基、3,3-二甲基-己-2-基、3,4-二甲基-己-2-基、3,5-二甲基-己-2-基、4,4-二甲基-己-2-基、4,5-二甲基-己-2-基、5,5-二甲基-己-2-基、2,2,3-三甲基-戊基、2,2,4-三甲基-戊基、2,3,3-三甲基-戊基、2,3,4-三甲基-戊基、2,4,4-三甲基-戊基、3,3,4-三甲基-戊基、3,4,4-三甲基-戊基、2,3,3-三甲基-戊-2-基、2,3,4-三甲基-戊-2-基、2,4,4-三甲基-戊-2-基、3,4,4-三甲基-戊-2-基、2,2,3,3-四甲基-丁基、3,4-二甲基-己-3-基、3,5-二甲基-己-3-基、4,4-二甲基-己-3-基、4,5-二甲基-己-3-基、5,5-二甲基-己-3-基、3-乙基-3-甲基-戊-2-基、3-乙基-4-甲基-戊-2-基、3-乙基-己-3-基、2,2-二乙基-丁基、3-乙基-3-甲基-戊基、4-乙基-己-3-基、5-甲基-庚-3-基、2-乙基-3-甲基-戊基、4-甲基-庚-4-基、3-甲基-庚-4-基、2-甲基-庚-4-基、3-乙基-己-2-基、2-乙基-2-甲基-戊基、2-异丙基-戊基、2,2-二甲基-己-3-基、2,2,4-三甲基-戊-3-基和2-乙基-3-甲基-戊基。(c1-c8)烷基可以是未取代的,或者由一个或多个基团取代,所述基团包括但不限于(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
256、如本文优选使用的表述亚烷基是指饱和的直链或支链烃基,其中规定了两个取代点。其中两个取代点彼此相距最大的简单烷基链如甲烷-1,1-二基、乙烷-1,2-二基、丙烷-1,3-二基、丁烷-1,4-二基和戊烷-1,5-二基,也称为亚甲基(其也称为甲烷-1,1-二基)、亚乙基(其也称为乙烷-1,2-二基)、亚丙基(其也称为丙烷-1,3-二基)、亚丁基(其也称为丁烷-1,4-二基)和亚戊基(其也称为戊烷-1,5-二基)。
257、在一个实施方案中以及如本文优选使用的,(c1-c10)亚烷基各自且独立地指以下任一者:亚甲基、乙烷-1,2-二基、丙烷-1,3-二基、丙烷-1,2-二基、丁烷-1,4-二基、丁烷-1,3-二基、丁烷-1,2-二基、2-甲基-丙烷-1,2-二基、2-甲基-丙烷-1,3-二基、戊烷-1,5-二基、戊烷-1,4-二基、戊烷-1,3-二基、戊烷-1,2-二基、戊烷-2,3-二基、戊烷-2,4-二基、具有5个碳原子的任何其它异构体、己烷-1,6-二基、具有6个碳原子的任何其它异构体、庚烷-1,7-二基、具有7个碳原子的任何其它异构体、辛烷-1,8-二基、具有8个碳原子的任何其它异构体、壬烷-1,9-二基、具有9个碳原子的任何其它异构体、癸烷-1,10-二基和具有10个碳原子的任何其它异构体。优选地,(c1-c10)亚烷基各自且独立地指以下任一者:亚甲基、乙烷-1,2-二基、丙烷-1,3-二基、丁烷-1,4-二基、戊烷-1,5-二基、己烷-1,6-二基、庚烷-1,7-二基、辛烷-1,8-二基、壬烷-1,9-二基和癸烷-1,10-二基。(c1-c10)亚烷基可以是未取代的,或由一个或多个基团取代,所述基团包括但不限于(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
258、在一个实施方案中以及如本文优选使用的,(c3-c8)环烷基各自且独立地指环丙基、环丁基、环戊基、环己基、环庚基和环辛基中的任一者。
259、在一个实施方案中以及如本文优选使用的,(c5-c7)环烷基各自且独立地指环戊基、环己基和环庚基中的任一者。
260、在一个实施方案中以及如本文优选使用的,(c3-c8)碳环是指3元、4元、5元、6元、7元或8元饱和或不饱和非芳族碳环。代表性的(c3-c8)碳环包括但不限于以下任一者:-环丙基、-环丁基、-环戊基、-环戊二烯基、-环己基、-环己烯基、-1,3-环己二烯基、-1,4-环己二烯基、-环庚基、-1,3-环庚二烯基、-1,3,5-环庚三烯基、-环辛基和-环辛二烯基。(c3-c8)碳环基团可以是未取代的,或由一个或多个基团取代,所述基团包括但不限于(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
261、在一个实施方案中以及如本文优选使用的,(c3-c8)碳环基是指如上定义的(c3-c8)碳环基团,其中一个碳环基团氢原子由键替代。
262、在一个实施方案中以及如本文优选使用的,“芳基”是指碳环芳族基团。芳基的实例包括但不限于苯基、萘基和蒽基。
263、在一个实施方案中以及如本文优选使用的,(c5-c6)芳基是指包含5或6个碳原子的碳环芳族基团。碳环芳族基团可以是未取代的,或由一个或多个基团取代,所述基团包括但不限于-(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
264、在一个实施方案中以及如本文优选使用的,“杂芳基”是指杂环芳族基团。杂芳基的实例包括但不限于呋喃、噻吩、吡啶、嘧啶、苯并噻吩、苯并呋喃和喹啉。
265、在一个实施方案中以及如本文优选使用的,(c5-c6)杂芳基是指由5或6个环原子组成的杂环芳族基团,其中至少一个原子不同于碳,优选是氮、硫或氧。杂环芳族基团可以是未取代的,或由一个或多个基团取代,所述基团包括但不限于-(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
266、在一个实施方案中以及如本文优选使用的,(c3-c8)杂环基是指如上定义的(c3-c8)杂环基团,其中一个碳环基团氢原子由键替代。(c3-c8)杂环可以是未取代的,或由至多六个基团取代,所述基团包括(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
267、在一个实施方案中以及如本文优选使用的,亚芳基是指具有两个共价键的芳基基团并且可以是如以下结构所示的邻位、间位或对位构型:
268、
269、其中苯基可以是未取代的,或由四个基团取代,所述基团包括但不限于(c1-c8)烷基、-o-[(c1-c8)烷基]、-芳基、-co-r’、-o-co-r’、-co-or’、-co-nh2、-co-nhr’、-co-nr’2、-nh-co-r’、-so2-r’、-so-r’、-oh、-卤素、-n3、-nh2、-nhr’、-nr’2和-cn;其中每个r’独立地选自-(c1-c8)烷基和芳基。
270、在一个实施方案中以及如本文优选使用的,在本说明书书、包括权利要求书中的任何结构式或任何段落中未指定原子质量数的原子是未指定的同位素组合物、天然存在的同位素混合物或各个同位素。这特别适用于碳、氧、氮、硫、磷、卤素和金属原子,包括但不限于c、o、n、s、f、p、cl、br、at、sc、cr、mn、co、fe、cu、ga、sr、zr、y、mo、tc、ru、rh、pd、pt、ag、in、sb、sn、te、i、pr、pm、dy、sm、gd、tb、ho、dy、er、yb、tm、lu、sn、re、rd、os、ir、au、pb、bi、po、fr、ra、ac、th和fm。
271、在一个实施方案中以及如本文优选使用的,螯合剂(chelator)是能形成螯合物(chelate)的化合物,其中螯合物是化合物,优选其中金属或具有电子间隙或孤对电子的部分参与环形成的环状化合物。更优选地,螯合剂是这类其中单个配体在中心原子处占据多于一个配位位点的化合物。
272、在一个实施方案中以及如本文优选使用的,诊断活性化合物是适于或可用于诊断疾病的化合物。
273、在一个实施方案中以及如本文优选使用的,诊断剂或诊断活性剂是适于或可用于诊断疾病的化合物。
274、在一个实施方案中以及如本文优选使用的,治疗活性化合物适于或可用于治疗疾病的化合物。
275、在一个实施方案中以及如本文优选使用的,治疗剂或治疗活性剂是适于或可用于治疗疾病的化合物。
276、在一个实施方案中以及如本文优选使用的,治疗诊断活性化合物是适于或可用于诊断和治疗疾病的化合物。
277、在一个实施方案中以及如本文优选使用的,治疗诊断剂或治疗诊断活性剂是适于或可用于诊断和治疗疾病的化合物。
278、在一个实施方案中以及如本文优选使用的,治疗诊断法是用于组合诊断和治疗疾病的方法;优选地,用于治疗诊断法中的组合诊断和治疗活性化合物是放射性标记的。
279、在一个实施方案中以及如本文优选使用的,疾病的治疗是疾病的治疗和/或预防。
280、在一个实施方案中以及如本文优选使用的,涉及fap的疾病是这样的疾病,其中优选以上调方式表达fap的细胞包括但不限于成纤维细胞以及表达fap的组织或者含有或包含优选以上调方式表达fap的细胞例如成纤维细胞的组织是疾病和/或疾病症状的原因或一个原因,或者是疾病潜在病理的一部分。优选的表达fap的细胞是癌症相关成纤维细胞(caf)。在所述疾病的一个实施方案中,优选当与疾病的治疗(treatment)、正在治疗(treating)和/或疗法(therapy)结合使用时,分别影响所述细胞、所述组织和病理导致疾病和/或疾病症状的治愈、治疗或改善。在所述疾病的一个实施方案中,优选当与疾病的诊断(diagnosis)和/或正在诊断(diagnosing)结合使用时,对表达fap的细胞和/或表达fap的组织进行标记使得能将所述细胞和/或所述组织与健康的或不表达fap的细胞和/或健康的或不表达fap的组织加以区别或区分。更优选地,这种区别或区分分别形成所述诊断和正在诊断的基础。在其一个实施方案中,标记是指可检测标记与表达fap的细胞和/或表达fap的组织或含有这种表达fap的细胞的组织直接或间接的相互作用;更优选地,这种相互作用涉及或基于所述标记或携带这种标记的化合物与fap的相互作用。
281、在一个实施方案中以及如本文优选使用的,靶细胞是这样的细胞,其表达fap并且是疾病和/或疾病症状的原因或一个原因,或者是疾病潜在病理的一部分。
282、在一个实施方案中以及如本文优选使用的,非靶细胞是指这样的细胞,其不表达fap和/或不是疾病和/或疾病症状的原因或一个原因,或不是疾病潜在病理的一部分。
283、在一个实施方案中以及如本文优选使用的,瘤(neoplasm)是细胞的异常新生长。瘤中的细胞比正常细胞更快生长,如果不治疗则会继续生长。瘤可以是良性的或恶性的。
284、在一个实施方案中以及如本文优选使用的,肿瘤是团块病变,其可以是良性的或恶性的。
285、在一个实施方案中以及如本文优选使用的,癌症是恶性瘤。
286、在一个实施方案中以及如本文优选使用的,键连(linkage)是两个独立部分的两个原子的连接。优选的键连是一个化学键或多个化学键。更优选地,化学键是一个共价键或多个化学键。最优选地,键连是共价键或配位键。如本文优选使用的,配位键的一个实施方案是当金属被螯合剂结合时实现的键或一组键。根据连接的原子类型及其原子环境,产生不同类型的键连。这些键连类型由所述键连产生的原子排列类型定义。例如,包含胺的部分与包含羧酸的部分的连接导致称为酰胺的键连(其也称为酰胺键连,-co-n-,-n-co-)。本领域技术人员会认识到,产生键连的这个和以下实例仅是典型实例,决不是限制本技术的范围。本领域技术人员会认识到,包含异硫氰酸酯的部分与包含胺的部分的连接产生硫脲(其也称为硫脲键连,-n-cs-n-),包含c原子的部分与包含硫醇基团(-c-sh)的部分的连接产生硫醚(其也称为硫醚键连,-csc-)。优选与本发明的螯合剂和接头组合使用的键连及其原子排列的特征类型的非限制性列表见表2。
287、表2
288、
289、
290、在本发明的一些实施方案中,用于在螯合剂和接头之间或者直接在螯合剂与本发明的化合物之间形成键连的反应性基团的实例总结在表3中。然而,本领域技术人员会理解,在用于形成本发明缀合物的实施方案中可被实现的键连既不限于表3中的键连之一,也不限于形成这种键连的反应基团。
291、表3
292、
293、
294、以下是用于或适于在本发明缀合物的实施方案中使用的部分或结构之间形成键连的反应性基团和官能度:伯氨基或仲氨基、羧酸、活化的羧酸、氯、溴、碘、巯基、羟基、磺酸、活化的磺酸、磺酸酯如甲磺酸酯或甲苯磺酸酯、michael受体、应变烯烃(strainedalkene)如反式环辛烯、异氰酸酯、异硫氰酸酯、叠氮化物、炔烃和四嗪。
295、如本文优选使用的,术语“活化的羧酸”是指具有通式-co-x的羧酸基团,其中x是离去基团。例如,羧酸基团的活化形式可包括但不限于酰氯、对称或不对称酸酐、和酯。在一些实施方案中,活化的羧酸基团是具有五氟苯酚、硝基苯酚、苯并三唑、氮杂苯并三唑、硫酚或n-羟基琥珀酰亚胺(nhs)作为离去基团的酯。
296、如本文优选使用的,术语“活化的磺酸”是指具有通式-so2-x的磺酸基团,其中x是离去基团。例如,磺酸的活化形式可包括但不限于磺酰氯或磺酸酐。在一些实施方案中,活化的磺酸基团是具有氯作为离去基团的磺酰氯。
297、在一个实施方案中以及如本文优选使用的,术语“介导键连”是指建立一个键连或一种类型的键连,优选两个部分之间的键连。在优选的实施方案中,所述键连和键连的类型如本文所定义。
298、在本技术中提到由较低整数和较高整数表示的范围(例如1至4),此类范围表示所述较低整数、所述较高整数以及所述较低整数和所述较高整数之间的任何整数。到这种程度上,所述范围实际上是所述整数的个体化公开。在所述实例中,1至4的范围因此意味着1、2、3和4。
299、本发明的化合物通常含有如本文所提供的氨基酸序列。常规的氨基酸(也称为天然氨基酸)是根据其标准的三字母代码和一个字母缩写进行识别,如表4所示。
300、表4:常规氨基酸及其缩写
301、 氨基酸 3个字母的缩写 1个字母的缩写 丙氨酸 ala a 精氨酸 arg r 天冬酰胺 asn n 天冬氨酸 asp d 半胱氨酸 cys c 谷氨酸 glu e 谷氨酰胺 gln q 甘氨酸 gly g 组氨酸 his h 异亮氨酸 ile i 亮氨酸 leu l 赖氨酸 lys k 甲硫氨酸 met m 苯丙氨酸 phe f 脯氨酸 pro p 丝氨酸 ser s 苏氨酸 thr t 色氨酸 trp w 酪氨酸 tyr y 缬氨酸 val v
302、非常规氨基酸(也称为非天然氨基酸)是包含氨基和羧基而且不是常规氨基酸的任何类型的非低聚化合物。
303、用于构建本发明化合物的非常规氨基酸和其它构件的实例根据表5中其缩写或名称进行识别。一些构件的结构用将所述构件引入肽的示例性反应物(例如羧酸样)描绘,或者这些构件以完全连接到另一结构例如肽或氨基酸的残基示出。氨基酸的结构显示为明确的氨基酸,而不是氨基酸残基(它们以此方式在执行后呈现在肽序列中)。通常缩写,优选氨基酸的缩写代表相应的氨基酸或相应的氨基酸残基,如本领域技术人员所理解的。在一些实施方案中,构件或氨基酸残基可以通过缩写旁边的至少一个连字符识别,该连字符象征该部分共价结合到所述化合物的不同部分或结构,并且因此不是未结合的构件或氨基酸。
304、为清楚起见,还示出了由多于一个部分组成的一些较大的化学部分。
305、表5:非天然氨基酸及其它构件和化学部分的缩写、名称和结构
306、
307、
308、
309、
310、
311、
312、
313、
314、
315、
316、
317、
318、本领域技术人员会理解,本文提供的肽的氨基酸序列以典型的肽序列格式描述。例如,常规氨基酸的三个字母代码、或非常规氨基酸的代码、或其它构件的缩写表示所述氨基酸或构件在肽序列中的特定位置存在。每个氨基酸或构件的代码通过连字符(通常代表酰胺键)连接于序列中下一个和/或前一个氨基酸或构件的代码。
319、在氨基酸含有多于一个氨基和/或羧基的情况中,这个氨基酸的所有方向原则上都是可能的,但在α-氨基酸中,优选利用α-氨基和α-羧基,其它优选方向是明确指定的。
320、对于氨基酸,在其缩写中,第一个字母表示c-α-原子的立体化学(如果适用)。例如,大写的首字母表示肽序列中存在l型氨基酸,而小写的首字母表示肽序列中存在d型的相应氨基酸。
321、在一个实施方案中以及如本文优选使用的,芳族l-α-氨基酸是包含芳基基团的任何种类的l-α-氨基酸。
322、在一个实施方案中以及如本文优选使用的,杂芳族l-α-氨基酸是包含杂芳基的任何种类的l-α-氨基酸。
323、本领域技术人员会认识到,如果本文公开的化合物中存在立体中心,则不论这种立体中心是氨基酸基团的一部分还是本发明化合物的任何其它部分或基团。因此,本发明包括两种可能的立体异构体而且不仅包括外消旋化合物,还包括单独的对映异构体和/或非对映异构体。当希望化合物是单一对映体或非对映体时,其可以通过立体定向合成或通过拆分最终产物或任何方便的中间体来获得。最终产物、中间体或起始材料的拆分均可以通过本领域已知的任何合适的方法进行。参见例如e.l.eliel、s.h.wilen和l.n.mander的“stereochemistry of organic compounds”(wiley-lnterscience,1994)。
324、在本技术中,为了方便起见,在某些情况下,化合物的结构式表示某种异构体,但本发明包括所有异构体,如几何异构体、基于不对称碳的旋光异构体、立体异构体、互变异构体等。在本技术说明书中,为了方便起见,在某些情况下,化合物的结构式表示某种异构体,但本发明包括所有异构体,如几何异构体、基于不对称碳的旋光异构体、立体异构体、互变异构体等。
325、除非有相反说明,否则氨基酸序列在本文中以n末端至c末端方向呈现。
326、构成本发明的肽的氨基酸的衍生物可以如表6所示。在任何实施方案中,本发明的化合物的一个或多个氨基酸被相应的优选氨基酸的衍生物取代。
327、表6:本发明化合物中包含的优选氨基酸的衍生物示例
328、
329、给出了在以下某些实施方案中以及本文所用术语的优选用法。
330、线性肽
331、一般的线性肽通常如下所示从n末端至c末端方向书写:
332、nt-xaa1-xaa2-xaa3-xaa4-……xaan-ct;
333、其中:
334、1.xaax是如表5所示的、在特定序列位置x处的氨基酸或构件的缩写、描述符或符号,
335、2.nt是n末端基团,例如“h”(游离n末端氨基的氢),或特定终止羧酸的缩写(如“ac”表示乙酸),或通过连字符连接于n末端氨基酸代码(xaa1)的其它化学基团或化学基团的结构式,以及
336、3.ct是c末端基团,其通常是“oh”或“nh2”(作为末端羧酸或酰胺)或通过连字符连接于c末端氨基酸代码(xaan)的特定终止胺的缩写。
337、具有由特定构件或肽修饰的侧链的支链肽
338、一般的线性支链肽是如下所示从n末端至c末端方向书写的:
339、nt-xaa1-xaa2-xaa3(nt-xab1-xab2-……xabn)-……xaan-ct;
340、其中线性肽的描述中的陈述1至3适用于说明该支链肽主链中xaax、nt和ct。
341、分支的位置由xaax缩写后面的括号指定。分支通常出现在赖氨酸(lys)残基(或类似物)处,这意味着分支是通过酰胺键连接于赖氨酸的侧链ε-氨基官能团。
342、括号中的内容描述了肽分支“nt-xab1-xab2-……xabn”的序列/结构。其中:
343、1.xabx是表3所示的、在分支的特定序列位置x处的氨基酸或构件的缩写、描述符或符号,
344、2.nt是n末端基团,例如特定终止羧酸的缩写(如“ac”表示乙酸),或通过连字符连接于n末端氨基酸代码(xab1)的其它化学基团或化学基团的结构式,以及
345、3.分支xabn的最后构件,其通过其自身羧基官能团与这个赖氨酸的侧链氨基官能团(或类似残基)形成酰胺键,将分支与主链连接。
346、环状肽
347、示例性的一般的环状肽是如下所示从n末端至c末端书写的:
348、nt-xaa1-[xaa2-xaa3-xaa4-……xaan]-ct;
349、其中线性肽的描述中的陈述1至3适用于说明所述环状肽主链中xaax、nt和ct。肽环的特征由方括号指定。
350、1.左方括号表示在其侧链处环开始的构件(环起始残基),以及
351、2.右方括号表示在其侧链出环终止的构件(环终止残基)。
352、这两个残基之间连接的化学性质是:
353、1.酰胺键,其中在那些所示的残基中,一个残基在其侧链中含有氨基官能团(例如lys),而另一个残基在其侧链中含有羧基官能团(例如glu),或
354、2.二硫键,其中那些所示的残基/氨基酸含有巯基部分(例如cys)。
355、含有其它环化元件(yc)的环状肽
356、从n末端至c末端书写的一般的扩展的环状肽如下所示:
357、nt-xaa1-[xaa2(yc)-xaa3-xaa4-……xaan]-ct;
358、其中线性肽的描述中的陈述1至3适用于说明该环状肽主链中的xaax、nt和ct。此外,yc是环化元件。如在环状肽的情况中,环的特征由方括号指定,方括号表示环起始残基和环终止残基。
359、与环起始残基相邻的括号内容指定了在扩展的肽环内的环化元件yc。yc元件与所述残基的侧链相连。此外,yc元件与环终止残基的侧链相连。这些残基中的任一个与yc元件之间的键连的化学性质取决于相应氨基酸xaan的侧链官能团。如果xaan的侧链包含巯基(例如cys),则所述键连是硫醚。
360、如下所示的hex-[cys(mli(dota-ttd))-pro-pro-thr-gln-phe-cys]-asp-nh2(2017)的结构作为上述惯例的非限制性示例:
361、
362、其中:
363、1.hex对应通式中的nt。
364、2.cys、pro、pro、thr、gln、phe和cys对应于通式中的xaa1至xaa7。
365、3.asp是c-末端残基。
366、4.nh2对应于通式中的ct。
367、5.与序列中n末端半胱氨酸相邻的左方括号(,[‘)表示环在这个残基处开始(环起始残基)。
368、6.与序列中n末端半胱氨酸相邻的右方括号(,]‘)表示环在这个残基处终止(环终止残基)。
369、7.与指示为起始残基的cys相邻的括号内的“mli”指定环化元件yc。它进一步与指示为循环终止残基的cys结合。所述yc元件通过硫醚键连接至所述残基。
370、8.通过ttd接头将dota螯合剂连接至作为剩余连接点的mli残基的氮原子。这个dota-ttd直接写在“mli”后面的括号中。如果该连接点被氢原子取代,则不另外提及,而甲基取代基被提及为mli(me)。为了清楚起见,表5的化学结构列表中包含了“cys(mli(dota-ttd))”等术语。
371、在本发明的一个实施方案中,氨基酸或肽连接至xaa7,其中这个肽的大多数氨基酸是荷电的或极性的,并且所述肽的净电荷是-2、-1、0、+1或+2。
372、为了计算肽净电荷,带负电的氨基酸是在其侧链中带有酸性基团如-cooh或-so3h的氨基酸,其净电荷对应于酸性基团的数量,例如asp或glu的净电荷为-1。
373、对于这种计算,带正电荷的氨基酸是在其侧链中带有氨基或胍基等碱性基团的氨基酸,并且其净电荷对应于碱性基团的数量,例如lys或arg净电荷为+1。
374、极性氨基酸是在其侧链中带有极性基团的氨基酸。极性基团例如是conh2、oh、f、cl、cn和杂环,例如组氨酸中的咪唑。
375、极性氨基酸的净电荷为0。对于一些含氮杂环,在我们的计算中净电荷被认为是0,但公认的是根据环境的ph值,其可能会在平衡中质子化,因此在一定程度上带正电荷。
376、这个肽的大多数(50%或更多)氨基酸是荷电的或极性的。
377、优选地,正电荷或负电荷有时被极性或非极性氨基酸隔开。
378、在一些实施方案中,带负电荷的氨基酸的存在优选是在xaa10。
379、在一些实施方案中,带正电荷的氨基酸的存在优选是在xaa13,优选arg和arg。
380、根据本发明,本发明的化合物可包含z基团。z基团包含螯合剂和任选存在的接头。如优选使用的接头是将分子的两个部分分开的元件、部分或结构。在本发明中,接头基团与螯合剂基团以及z所连接的本发明化合物的相应部分二者形成共价键。接头基团原则上可以是能与螯合剂基团和本发明化合物的一部分在指定位置形成键的任何化学基团。
381、接头的一个重要性质或特征是其将螯合剂和本发明化合物的环状肽部分隔开。这在环状肽的靶结合能力被螯合剂的紧密接近损害的情况下尤其重要。然而,其最扩展的构象异构体中的总接头长度不应超过优选不超过最优选不超过
382、在优选的实施方案中,接头是-[x]a-,其中a是1至10的整数,每个x是单独的构件,其通过选自以下的官能团独立地连接于其在序列中的相邻基团:酰胺键、脲键、氨基甲酸酯键、酯键、醚键、硫醚键、磺酰胺键、三唑和二硫键。
383、x1与螯合剂连接以及与x2(如果存在)连接,或在指定位置与本发明化合物连接。xa与xa-1(如果存在)连接,以及在指定位置与本发明化合物连接。
384、更优选的接头基团类型由-[x]a-表示,其中a是1至10的整数,优选a是1至8、1至6、1至5、1至4或1至3的整数,每个x是单独的构件,其通过选自以下的官能团独立地连接于其在序列中的相邻基团:酰胺键、脲键、氨基甲酸酯键、酯键、醚键、硫醚键、磺酰胺键、三唑键和二硫键。
385、在一个实施方案中,所述构件x具有通式(8),
386、
387、其中:
388、片段lin2(如果存在)和片段lin3(如果存在)各自且独立地选自-co-、-nr10-、-s-、-co-nr10-、-cs-nr10-、-o-、-琥珀酰亚胺-和-ch2-co-nr10-;条件是lin2或lin3中至少之一通过碳原子与r9连接,以及所有含氮片段的氮原子与r9连接;
389、其中r10选自氢和(c1-c4)烷基;以及
390、其中r9选自-(c1-c10)亚烷基-、-(c3-c8)碳环-、-亚芳基-、-(c1-c10)亚烷基-亚芳基-、-亚芳基-(c1-c10)亚烷基-、-(c1-c10)亚烷基-亚芳基-(c1-c10)亚烷基-、-(c1-c10)亚烷基-(c3-c8)碳环-、-(c3-c8)碳环-(c1-c10)亚烷基-、-(c1-c10)亚烷基-(c3-c8)碳环-(c1-c10)亚烷基-、-(c3-c8)杂环-、(c1-c10)亚烷基-(c3-c8)杂环-、-(c3-c8)杂环-(c1-c10)亚烷基-、-(c1-c10)亚烷基-(c3-c8)杂环-(c1-c10)亚烷基-、-(ch2ch2o)r-和-(ch2)s-(ch2ch2o)r-(ch2)t-;
391、以及其中:
392、r是来自1、2、3、4、5、6、7、8、9和10的任何整数;
393、s是来自0、1、2、3和4的任何整数;以及
394、t是来自0、1、2、3和4的任何整数。
395、优选地,除了x1和螯合剂之间的键连之外,所述键连是酰胺键。更优选地,构件x2至xa独立地选自氨基酸、二羧酸和二胺,各自的键连是酰胺。
396、在一个实施方案中,构件x2至xa优选是氨基酸,其中所述氨基酸选自常规和非常规氨基酸。在一个实施方案中,氨基酸选自β-氨基酸、γ-氨基酸、δ-氨基酸、ε-氨基酸和ω-氨基酸之一。在进一步的实施方案中,氨基酸是环状氨基酸或线性氨基酸。本领域技术人员会理解,在具有立体中心的氨基酸的情况下,所有立体异构形式均可用于构件x中。
397、在一个实施方案中,构件x2至xa优选是氨基酸,其中所述氨基酸选自在氨基与羧基的间距方面不同的氨基酸。这种氨基酸一般可以表示如下:
398、
399、在本发明范围内,此类氨基酸不被进一步取代。然而,此类氨基酸被进一步取代也在本发明范围内;优选地,所述取代是co-nh2和/或ac-nh-。
400、可用作构件x的这种氨基酸(结构32)的代表是甘氨酸(gly)、β-丙氨酸(bal)、γ-氨基丁酸(gaba)、氨基戊酸、氨基己酸以及具有至多10个ch2基团的同系物。
401、更优选用作构件x的此类氨基酸(结构33)的代表是3-氨基甲基-苯甲酸、4-氨基甲基-苯甲酸、邻氨基苯甲酸、3-氨基苯甲酸和4-氨基苯甲酸。
402、相关构件是通过用cooh替代nh2而衍生自氨基酸(结构32+33)的二胺,优选用作构件x的是二氨基乙烷、1,3-二氨基丙烷、1,4-二氨基丁烷、1,5-二氨基戊烷、3-氨基甲基苯胺、4-氨基甲基苯胺、1,2-二氨基苯、1,3-二氨基苯和1,4-二氨基苯。
403、相关构件是通过用nh2替代cooh而衍生自氨基酸(结构32+33)的二羧酸,更优选用作构件x的是丙二酸、琥珀酸、戊二酸、己二酸、邻苯二甲酸、对苯二甲酸、间苯二甲酸以及2-、3-或4-羧基苯乙酸。
404、在进一步的实施方案中,所述氨基酸是含有聚醚(优选作为主链)的氨基酸。优选地,所述聚醚是聚乙二醇并且由最多30个单体单元组成,并由此是peg-氨基酸。优选地,与不包含所述聚醚的氨基酸相比,包含所述聚醚的氨基酸显示亲水性增加。如果并入构件x中并最终并入接头基团[x]a中,则结果通常是亲水性增加。这种氨基酸的优选实施方案描述如下,其中应认识到此类氨基酸可包含0、1、2、3、4、5、6、7、8、9、10、11或12个氧化乙烯部分:
405、
406、优选的含乙二醇的氨基酸是ttds(n-(3-{2-[2-(3-氨基丙氧基)-乙氧基]-乙氧基}-丙基)-琥珀酸)和o2oc([2-(2-氨基-乙氧基)-乙氧基]-乙酸),其结构式如下:
407、
408、在优选的实施方案中,所述接头包含选自以下的仅一个特定氨基酸的寡聚体或单体:ttds、o2oc、apac、gly、bal、gab、mamb、pamb、ppac、4amc、inp、sni、rni、nmg、cmp、peg6、peg12、peg-氨基酸,更优选所述接头是单体的。
409、在另一个优选的实施方案中,所述接头包含选自ttds、o2oc、apac、gly、bal、gab、mamb、pamb、peg6、peg12和peg-氨基酸的一个构件x2,以及另一个构件x1,其直接结合x2的氨基氮并通过选自如下的键连直接连接于螯合剂:酰胺键、脲键、氨基甲酸酯键、酯键、醚键、硫醚键、磺酰胺、三唑和二硫键。在这种情况下,x1用作衔接子以介导由螯合剂提供的不同种类的连接官能团与氨基酸x2的氮原子的键连,因为x1为螯合剂的键连提供相关的互补官能度。
410、然而,接头的使用通常是有目的的。在某些情况下,为了保持高生物活性,需要将较大的部分与生物活性分子隔开。在其它情况下,接头的引入有机会通过引入极性或多个电荷来调整分子的物理化学性质。在某些情况下,如果可以将螯合剂与生物活性化合物组合而无需此类接头,则这可能是一种优势和成就。特别是在其中螯合剂连接于式(x)的yc上的本发明化合物中,通常无需使用任何所示的接头就能在形成两个硫醚键的情况下很好地进行xaa1的s原子和xaa7的s原子的连接。
411、在一个实施方案中,本发明的化合物包含螯合剂。优选地,所述螯合剂是本发明化合物的一部分,由此所述螯合剂直接或间接连接至本发明化合物。优选地,本发明化合物中的螯合剂的间接连接是通过接头实现的。优选的螯合剂是形成优选包含至少一种放射性金属核素的金属螯合物的螯合剂。所述至少一种放射性金属核素优选可用于或适合于诊断和/或治疗和/或治疗诊断用途,并且更优选可用于或适合于成像和/或放射治疗。
412、在本发明的一个实施方案中,所述螯合剂是本文所定义的z基团的一部分,由此此类z基团包含螯合剂和任选存在的接头。本领域技术人员应当理解,z基团可以连接在本文公开的本发明化合物的三个不同位置处。尽管本发明的化合物可以在两个或甚至所有三个这样的位置处包含z基团,但优选本发明的化合物仅包含一个z基团。
413、原则上可用于和/或适用于本发明的实践(包括疾病的诊断和/或治疗)的螯合剂是本领域技术人员已知的。各种各样的相应螯合剂是可用的其已被综述,例如banerjee等人(banerjee,et al.,dalton trans,2005,24:3886)及其中的参考文献(price,et al.,chem soc rev,2014,43:260;wadas,et al.,chem rev,2010,110:2858)。所述螯合剂包括但不限于线性、环状、大环状、四吡啶、n3s、n2s2和n4螯合剂,如us 5,367,080 a、us 5,364,613 a、us 5,021,556 a、us 5,075,099 a和us 5,886,142 a中所述。
414、适用于实践本发明的代表性的螯合剂(在本文也称作螯合物)及其衍生物包括但不限于:99mtc(co)3-螯合剂,aazta,bat,cdta,dta,dtpa,cy-dta,dtcbp,chx-a"-dtpa,cta,cyclam,cyclen,teta,sarcophagine,cpta,teama,crown,cyclen,do3a,do2a,trita,data,dfo,data(m),data(p),data(ph),data(pph),dedpa,h4octapa,h2dedpa,h5decapa,h2azapa,h2chx dedpa,dfo-chx-mal,dfo-p-scn,dfo-1ac,dfo-bac,p-scn-bn-dfo,dfo-pphe-ncs,dfo-hopo,dfc,二膦,dota,dotaga,dota-mfco,dotam-一元酸,硝基-dota,硝基-pa-dota,p-ncs-bz-dota,pa-dota,dota-ncs,dota-nhs,cb-do2a,pcta,p-nh2-bn-pcta,p-scn-bn-pcta,p-scn-bn-dota,dotma,nb-dota,h4nb-dota,h4tce-dota,3,4,3-(li-1,2-hopo),tren(me-3,2-hopo),tce-dota,dotp,doxp,p-ncs-dota,p-ncs-trita,trita,teta,3p-c-depa,3p-c-depa-ncs,p-nh2-bn-oxo-do3a,p-scn-bn-tcmc,tcmc,4-氨基丁基-dota,叠氮基-单酰胺-dota,bcn-dota,丁炔-dota,bcn-dota-ga,doa3p,do2a2p,do2a(反式-h2do2a),do3a,do3a-硫醇,do3atbu-n-(2-氨基乙基)乙酰胺,do2ap,cb-do2a,c3b-do2a,hp-do3a,dota-nhs-酯,马来酰亚胺-dota-ga,马来酰亚胺-单-酰胺-dota,马来酰亚胺-dota,nh2-dota-ga,nh2-peg4-dota-ga,p-nh2-bn-dota,p-no2-bn-dota,p-scn-bn-dota,p-scn-bz-dota,ta-dota,ta-dota-ga,otta,doxp,tsc,dtc,dtcbp,ptsm,atsm,fsc,h2atsm,h2ptsm,dp44mt,dpc,bp44mt,qt,混合的缩氨基硫脲-苯并噻唑,缩氨基硫脲-苯乙烯基吡啶四配位基配体h2l2-4,hbed,hbed-cc,dmhbed,dmehpg,hbed-nn,shbed,br-me2hbed,bpca,heha,bf-heha,去铁酮,thp,hopo,hynic(2-肼基烟酰胺),nhs-hynic,hynic-kp-dppb,hynic-ko-dppb,(hynic)(tricine)2,(hynic)(edda)cl,p-eddha,aim,aima,iam b,mama,mama-dgal,mama-mgal,mama-da,mama-had,macropa,macropaquin,macroquin-so3,nxs4-x,n2s2,n3s,n4,mag3b,nota,nodaga,scn-bz-nota-r,not-p(notmp),notam,p-ncs-nota,tacn,tacn-tm,neta,neta-单胺,pscn-phpr-ne3ta,c-ne3ta-ncs,c-neta-ncs,3p-c-neta,nodasa,nopo,noda,no2a,n-苄基-noda,noda-mpaa,c-nota,bcnot-单胺,马来酰亚胺基-单-酰胺-nota,no2a-叠氮化物,no2a-丁炔,no2ap,no3ap,n-nota,oxo-do3a,p-nh2-bn-nota,p-nh2-bn-氧代-do3a,p-no2-bn-环烯,psc,p-scn-bn-nota,notp,p-scn-bn-氧代-do3a,trap,pepa,bf-pepa,pycup,pycup2a,pycup1a1bn,pycup2bn,resca,sarar-r,diamsar,ambasar-r,siamsar,sar,tachpyr,tachpyr-(6-me),tam a,tam b,tame,tame-hex,thp-ph-ncs,thp-ncs,thp-tate,ntp,h3thp,thpn,cb-te2a,pcb-te1a1p,teta-nhs,cpta,cpta-nhs,cb-te1k1p,cb-te2a,te2a,h2cb-te2a,te2p,cb-te2p,mm-te2a,dm-te2a,,2c-teta,6c-teta,bat,bat-6,nhs-bat酯,ssbat,scn-chx-a-dtpa-p,scn-teta,tmt-胺,p-bz-htcpp。
415、hynic、dtpa、edta、dota、teta、基于双氨基双硫醇(bat)的螯合剂在us 5,720,934中公开;去铁胺(dfo)在(doulias,et al.,free radic biol med,2003,35:719)中公开,四吡啶和n3s、n2s2和n4螯合剂在us 5,367,080 a、us 5,364,613 a、us 5,021,556 a、us 5,075,099 a、us 5,886,142 a中公开,其中所有参考文献均以其整体通过引用并入本文。6-氨基-6-甲基全氢-1,4-二氮杂环庚烷-n,n’,n″,n″-四乙酸(aazta)在pfister等人(pfister,et al.,ejnmmi res,2015,5:74)中公开,去铁酮,即1,2-二甲基-3,4-羟基吡啶酮,以及六齿三(3,4-羟基吡啶酮)(thp)在cusnir等人(cusnir,et al.,int jmol sci,2017,18)中公开,基于单胺-单酰胺二硫醇(mama)的螯合剂在demoin等人(demoin,et al.,nucl med biol,2016,43:802)中公开,macropa及类似物在thiele等人(thiele,et al.,angew chem int ed engl,2017,56:14712)中公开,1,4,7,10,13,16-六氮杂环十六烷-n,n’,n”,n”’,n””,n””’-六乙酸(heha)和pepa类似物在price和orvig(price,et al.,chemsoc rev,2014,43:260)中公开,pycup及类似物在boros等人(boros,et al.,mol pharm,2014,11:617)中公开,n,n-双(2-羟基苄基)乙二胺-n,n-二乙酸(hbed)、1,4,7,10-四(氨基甲酰基甲基)-l,4,7,10-四氮杂环十二烷(tcm)、2-[(羧甲基)]-[5-(4-硝基苯基-1-[4,7,10-三-(羧甲基)-1,4,7,10-四氮杂环十二烷-1-基]戊-2-基)-氨基]乙酸(3p-c-depa)、cb-te2a、te2a、te1a1p、diamsar、1-n-(4-氨基苄基)-3,6,10,13,16,19-六氮杂二环[6.6.6]-二十烷-1,8-二胺(sarar)、neta、n,n0,n00三(2-巯乙基)-1,4,7-三氮杂环壬烷(tacn-tm)、{4-[2-(双-羧甲基-氨基)-乙基]-7-羧甲基-[1,4,7]三氮杂壬-1-基}-乙酸(neta)、二亚乙基三胺五乙酸(dtp)、3-({4,7-二-[(2-羧基-乙基)-羟基-磷酰基甲基]-[1,4,7]三氮杂壬-1-基甲基}-羟基-磷酰基)-丙酸(trap)、nopo、h4octapa、shbed、bpca、3,6,9,15-四氮杂双环[9.3.1]-十五烷-1(15),11,13-三烯-3,6,9,-三乙酸(pcta)及1,4,7,10,13-五氮杂环十五烷-n,n’,n”,n”’,n””-五乙酸(pepa)在price和orvig(price,et al.,chem soc rev,2014,43:260)中公开,1-羟基-2-吡啶酮配体(hopo)在allott等人(allott,et al.,chemcommun(camb),2017,53:8529)中公开,[4-羧甲基-6-(羧甲基-甲基-氨基)-6-甲基-[1,4]二氮杂环庚烷-1-基]-乙酸(data)在tornesello等人(tornesello,et al.,molecules,2017,22:1282)中公开,四(氨甲基)甲烷(tam)及类似物在mcauley 1988(mcauley,et al.,canadian journal of chemistry,1989,67:1657)中公开,六齿三(3,4-羟基吡啶酮)(thp)及类似物在ma等人(ma,et al.,dalton trans,2015,44:4884)中公开。
416、现有技术中描述了一些上述螯合剂的诊断和/或治疗性应用。例如,2-肼基烟酰胺(hynic)已广泛用于在共配体存在下掺入99mtc和186,188re(schwartz,et al.,bioconjugchem,1991,2:333;babich,etal.,j nucl med,1993,34:1964;babich,et al.,nucl medbiol,1995,22:25);dtpa用于中以络合111in,而且一些修饰描述在文献中(li,etal.,nucl med biol,2001,28:145;brechbiel,et al.,bioconjug chem,1991,2:187);dota型螯合剂在放射治疗中的应用由tweedle等人(us pat 4,885,363)描述;螯合三价同位素金属的其它多氮杂(polyaza)大环由eisenwiener等人(eisenwiener,et al.,bioconjug chem,2002,13:530)描述;n4-螯合剂例如99mtc-n4-螯合剂在靶向cck-2受体的小促胃液素(minigastrin)情况中已经用于肽标记(nock,et al.,j nucl med,2005,46:1727)。
417、在一个实施方案中,金属螯合剂选自但不限于dota、dotaga、nota、nodaga、noda-mpaa、hbed、teta、cb-te2a、dtpa、dfo、macropa、hopo、trap、thp、data、notp、sarcophagine、fsc、neta、h4octapa、pycup、nxs4-x(n4、n2s2、n3s)、hynic、99mtc(co)3--螯合剂及其类似物,其中:
418、dota表示1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸,
419、dotaga表示1,4,7,10-四氮杂环十二烷,1-(戊二酸)-4,7,10-三乙酸,
420、nota表示1,4,7-三氮杂环壬烷三乙酸,
421、nodaga表示1,4,7-三氮杂环壬烷-n-戊二酸-n',n"-二乙酸,
422、noda-mpaa表示1,4,7-三氮杂环壬烷-1,4-二乙酸-甲基苯基乙酸,
423、hbed表示双(2-羟基苄基)乙二胺二乙酸,
424、teta表示1,4,8,11-四氮杂环十二烷-1,4,8,11-四乙酸,
425、cb-te2a表示4,11-双-(羧甲基甲基)-1,4,8,11-四氮杂二环[6.6.2]-十六烷,
426、dtpa表示二亚乙基三胺五乙酸,
427、chx-a”-dtpa表示[(2-{[2-(二-羧甲基-氨基)-环己基]-羧甲基-氨基}-乙基)-羧甲基l-氨基]-乙酸,
428、dfo表示除铁灵(desferal)或去铁胺(desferrioxamine)型螯合剂组,非限制性实例的化学名称是n-[5-({3-[5-(乙酰基-羟基-氨基)-戊基氨基甲酰基]-丙酰基}-羟基-氨基)-戊基]-n'-(5-氨基-戊基)-n'-羟基-琥珀酰胺,
429、macropa表示n,n’-双[(6-羧基-2-吡啶基)甲基]-4,13-二氮杂-18-冠,
430、hopo表示十八烷羟基吡啶酮类型螯合剂组,非限制性实例的结构在下文示出,
431、trap表示3-({4,7-双-[(2-羧基-乙基)-羟基-磷酰基甲基]-[1,4,7]三氮杂壬-1-基甲基}-羟基-磷酰基)-丙酸,
432、thp表示六齿三(3,4-羟基吡啶酮),
433、data表示[4-羧甲基-6-(羧甲基-甲基-氨基)-6-甲基-[1,4]二氮杂环庚烷-1-基]-乙酸,
434、notp表示1,4,7-三氮杂环壬烷-n,n’,n”-三(亚甲基膦)酸),
435、sarcophagine表示3,6,10,13,16,19-六氮杂二环[6.6.6]二十烷,
436、fsc表示3,15,27-三氨基-7,19,31-三羟基-10,22,34-三甲基-1,13,25-三氧杂-7,19,31-三氮杂-环三十六烷-9,21,33-三烯-2,8,14,20,26,32-六酮,
437、neta表示{4-[2-(双-羧甲基-氨基)-乙基]-7-羧甲基-[1,4,7]三氮杂环壬烷-1-基}-乙酸,
438、ne3ta表示{4-羧甲基-7-[2-(羧甲基-氨基)-乙基]-[1,4,7]三氮杂环壬烷-1-基}-乙酸,
439、h4octapa表示n,n’-(6-羧基-2-吡啶基甲基)-n,n’-二乙酸-1,2-乙二胺,
440、pycup表示1,8-(2,6-吡啶二亚甲基)-1,4,8,11-四氮杂环十四烷,
441、hynic表示6-肼基-烟酸,
442、nxs4-x(n4,n2s2,n3s)表示一组具有n原子(碱性胺或非碱性酰胺)和硫醇为供体的四齿螯合剂,其稳定tc-配合物,尤其是tc(v)-氧代配合物。一个代表性的非限制性实例mag3的结构如下所示,以及
443、n4表示n,n'-双-(2-氨基-乙基)-丙烷-1,3-二胺,
444、99mtc(co)3-螯合剂表示二齿或三齿螯合剂,其能与锝三羰基片段形成稳定络合物,
445、并且其化学结构如下所示:
446、
447、
448、在优选的实施方案中,所述金属螯合剂选自dota、dotaga、nota、nodaga、noda-mpaa、dtpa、chx-a”-dtpa、cb-te2a、n4及其类似物。
449、在更优选的实施方案中,所述金属螯合剂选自dota、dotaga和nodaga及其类似物。
450、在甚至更优选的实施方案中,所述金属螯合剂是dota及其类似物。
451、本领域技术人员意识到,理论上可以使用所述螯合剂,不论本发明的化合物是否用于或适合用于诊断或治疗。这个理论在国际专利申请wo 2009/109332 a1中概述。
452、本领域技术人员会进一步意识到,如果没有另外说明,则所述螯合剂在本发明化合物中的存在包括所述螯合剂与任何金属络合物配偶体(即理论上可以被所述螯合剂络合的任何金属)络合的可能。明确提及的本发明化合物的螯合剂或与本发明化合物相关的通用术语螯合剂是指未络合的螯合剂本身,或是指结合任何金属络合物配偶体的螯合剂,其中所述金属络合物配偶体是任何放射性或非放射性金属络合物配偶体。优选所述螯合剂金属络合物,即金属络合物配偶体所结合的螯合剂,其是稳定的螯合剂金属络合物。
453、非放射性螯合剂金属络合物有多种应用,例如用于评估如稳定性或活性等难以确定的性质。一个方面是金属络合物配偶体的放射性形式的冷变体(例如实施例中描述的非放射性镓、镥或铟络合物)可以充当放射性化合物的替代物。此外,它们是在体外或体内鉴定代谢物以及评估本发明化合物的毒性性质的有价值的工具。此外,螯合剂金属络合物可用于结合测定中,利用一些具有不同配体的金属络合物(例如铕盐)荧光特性。
454、螯合剂可以是合成的或商购的,具有多种(可能已经被激活的)与肽或氨基酸缀合的基团。
455、螯合剂与本发明各化合物的氨基-氮直接缀合对于选自以下组中的螯合剂是完全可能的:dtpa、dota、dotaga、nota、nodaga、noda-mpaa、hbed、teta、cb-te2a、dtpa、dfo、data、sarcophagine和n4,优选dtpa、dota、dotaga、nota、nodaga、noda-mpaa、cb-te2a和n4。在这方面优选的键连是酰胺键。
456、异硫氰酸酯官能化螯合剂与本发明各化合物的氨基-氮直接缀合对于选自以下组中的螯合剂是完全可能的:dota、dotaga、nota、nodaga、dtpa、chx-a”-dtpa、dfo和thp,优选dota、dotaga、nota、nodaga、dtpa和chx-a”-dtpa。在这方面优选的键连是硫脲键。
457、作为螯合剂与氨基-氮直接缀合的理想前体的螯合剂上的官能团是本领域技术人员已知的,并且包括但不限于羧酸、活化的羧酸,例如活性酯如nhs-酯、五氟苯酚-酯、hobt-酯和hoat-酯、异硫氰酸酯。
458、作为螯合剂与羧基直接缀合的理想前体的螯合剂上的官能团是本领域技术人员已知的,并且包括但不限于烷基氨基和芳基氨基氮。相应的螯合剂试剂是用于可商购的一些螯合剂,例如用于具有烷基氨基或芳基氨基氮的dota。
459、作为螯合剂与硫醇基团直接缀合的理想前体的螯合剂上的官能团是本领域技术人员已知的,并且包括但不限于马来酰亚胺氮。相应的螯合剂试剂是可商购的一些螯合剂,例如用于具有马来酰亚胺氮的dota。
460、作为螯合剂与叠氮基团直接缀合的理想前体的螯合剂上的官能团是本领域技术人员已知的,并且包括但不限于无环和环状炔烃。相应的螯合剂试剂是可商购的一些螯合剂,例如用于具有炔丙基或丁炔基的dota。
461、作为螯合剂与炔基直接缀合的理想前体的螯合剂上的官能团是本领域技术人员已知的,并且包括但不限于烷基和芳基吖嗪。相应的螯合剂试剂是可商购的一些螯合剂,例如用于具有叠氮丙基的dota。
462、本领域技术人员意识到,要分别考虑待治疗的疾病和/或待诊断的疾病和/或分别考虑待治疗和待诊断的患者和患者组的特性,来选择与或者待与本发明的化合物连接的放射性核素。
463、在本发明的一个实施方案中,所述放射活性核素也称为放射性核素。放射性衰变是不稳定原子的原子核通过发射电离粒子(电离辐射)而失去能量的过程。有不同类型的放射性衰变。当具有一种类型原子核的原子(称为母体放射性核素)转变为具有不同状态的原子核或包含不同数量的质子和中子的原子核时,导致能量衰减或损失。这些产物中的任何一个都被命名为子体核素。在某些衰变中,母体和子体是不同的化学元素,因此衰变过程会导致核嬗变(产生新元素的原子)。例如,放射性衰变可以是α衰变、β衰变和γ衰变。当原子核喷射出一个α粒子(氦核)时,发生α衰变。这是最常见的发射核子的过程,但在更罕见的衰变类型中,原子核可以喷射质子,或其它元素的特定核子(在这个过程中称为簇衰变)。在质子变成中子的过程中或者相反,在原子核发射电子(β--衰变)或正电子(β+-衰变)和一种类型中微子时,发生β衰变。相比之下,存在不会导致嬗变的放射性衰变过程。受激核的能量可以在γ衰变中以γ射线的形式发射,或用于通过与受激核在称为内部转换的过程中相互作用而喷射轨道电子,或用于从电子壳层吸收内部原子电子,从而核质子转变为中子导致为电子俘获(ec)的过程中发射电子中微子,或者在称为同质异能跃迁(it)的过程中可以在不改变质子和中子数量的情况下发射。一种形式的放射性衰变,即自发裂变(sf),仅在非常重的化学元素中发现,导致自发分解成较小的原子核和一些孤立的核粒子。
464、在本发明的优选实施方案中,所述放射性核素可用于标记本发明的化合物。
465、在本发明的一个实施方案中,所述放射性核素适合与螯合剂络合,形成放射性核素螯合物络合物。
466、在另一个实施方案中,本发明化合物的一个或多个原子具有非天然同位素组成,优选这些原子是放射性核素;更优选碳、氧、氮、硫、磷和卤素的放射性核素:这些放射性原子通常是本发明化合物的氨基酸(在某些情况下是含卤素的氨基酸)和/或构件(以及在某些情况下是卤化构件)的一部分。
467、在本发明的一个优选实施方案中,所述放射性核素具有允许诊断和/或治疗性医学用途的半衰期。具体而言,所述半衰期为1分钟至100天。
468、在本发明的优选实施方案中,所述放射性核素具有允许诊断和/或治疗性医学用途的衰变能。具体地,对于γ发射同位素,对于诊断用途而言,衰变能为0.01至4mev,优选0.08至0.4mev。对于正电子发射同位素,对于诊断用途而言,平均衰变能为0.2至3mev,优选0.2至1mev。对于对于β-发射同位素,对于治疗用途而言,平均衰变能为0.02至3mev,优选0.1至1mev。对于α发射同位素,对于治疗用途而言,衰变能为3至8mev,优选3.9至6.4mev。
469、在本发明的优选实施方案中,所述放射性核素是工业生产的,以用于医学用途。具体来说,所述放射性核素可达到gmp质量。
470、在本发明的优选实施方案中,放射性核素的放射性衰变后的子体核素与诊断和/或治疗性医学用途相容。此外,子体核素是稳定的,或以不干扰或甚至支持诊断和/或治疗性医学用途的方式进一步衰变。可结合本发明使用的代表性放射性核素总结在表7中。
471、表7:相关放射性核素的关键性质-半衰期、衰变辐射类型、最高概率跃迁的衰变能(β衰变的平均能量)和绝对强度(来源:https://www-nds.iaea.org/relnsd/vcharthtml/vcharthtml.html;访问日期:2020年9月4日)。
472、
473、
474、
475、
476、
477、
478、
479、
480、
481、
482、
483、
484、
485、
486、
487、
488、
489、
490、
491、
492、
493、
494、
495、
496、
497、
498、
499、
500、
501、
502、
503、
504、
505、
506、
507、
508、
509、
510、
511、
512、
513、
514、
515、
516、
517、
518、
519、
520、
521、
522、
523、
524、
525、
526、
527、
528、
529、
530、
531、
532、在本发明的一个实施方案中,所述放射性核素用于诊断。优选地,所述放射性同位素选自但不限于43sc、44sc、51mn、52mn、64cu、67ga、68ga、86y、89zr、94mtc、99mtc、111in、152tb、155tb、177lu、201tl、203pb、18f、76br、77br、123i、124i、125i。更优选地,所述放射性核素选自43sc、44sc、64cu、67ga、68ga、86y、89zr、99mtc、111in、152tb、155tb、203pb、18f、76br、77br、123i、124i、125i。甚至更优选地,所述放射性核素选自64cu、68ga、89zr、99mtc、111in、18f、123i和124i。然而,本领域技术人员意识到,所述放射性核素的用途不限于诊断目的,而是包括在与本发明的化合物缀合时在治疗和治疗诊断中的用途。
533、在本发明的一个实施方案中,所述放射性核素用于治疗。优选地,所述放射性同位素选自47sc、67cu、89sr、90y、111in、153sm、149tb、161tb、177lu、186re、188re、212pb、213bi、223ra、225ac、226th、227th、131i、211at。更优选地,所述放射性同位素选自47sc、67cu、90y、177lu、188re、212pb、213bi、225ac、227th、131i、211at。甚至更优选地,所述放射性核素选自90y、177lu、225ac、227th、131i和211at。然而,本领域技术人员意识到,所述放射性核素的用途不限于治疗目的,而是包括在与本发明的化合物缀合时在诊断和治疗诊断中的用途。
534、在一个实施方案中,本发明的化合物以药学可接受的盐的形式呈现。
535、本发明化合物的“药学可接受的盐”优选是酸盐或碱盐,其被本领域普遍认为适用于与人或动物组织接触而无过度毒性或致癌性,并且优选没有刺激性、过敏反应或者其它问题或并发症。此类盐包括碱性残基如胺的无机酸盐和有机酸盐,以及酸性残基如羧酸的碱金属盐或有机盐。本发明的化合物能够形成内盐,其也是药学上可接受的盐。
536、合适的药学上可接受的盐包括但不限于酸的盐,例如盐酸、磷酸、氢溴酸、苹果酸、乙醇酸、富马酸、硫酸、氨基磺酸、磺胺酸、甲酸、甲苯磺酸、甲磺酸、苯磺酸、乙二磺酸、2-羟基乙基磺酸、硝酸、苯甲酸、2-乙酰氧基苯甲酸、柠檬酸、酒石酸、乳酸、硬脂酸、水杨酸、戊二酸、抗坏血酸、双羟萘酸、琥珀酸、富马酸、马来酸、丙酸、羟基马来酸、氢碘酸、苯乙酸、链烷酸如乙酸、hooc-(ch2)n-cooh,其中n是0至4的任何整数,即0、1、2、3、或4等。类似地,药学上可接受的阳离子包括但不限于钠、钾、钙、铝、锂和铵。本领域普通技术人员将认识到本文提供的化合物的其它药学上可接受的盐。一般而言,可通过任何常规化学方法从含有碱性或酸性部分的母体化合物合成药学上可接受的酸或碱盐。简而言之,可以通过使这些化合物的游离酸或碱形式与化学计算量的合适碱或酸在水中、在有机溶剂中或在两者的混合物中反应来制备这种盐。一般来说,优选使用非水介质,如乙醚、乙酸乙酯、乙醇、异丙醇或乙腈。
537、本发明化合物的“药学上可接受的溶剂化物”优选是通过一种或多种溶剂分子与本发明化合物的一个或多个分子缔合形成的本发明化合物的溶剂化物。优选地,所述溶剂是本领域通常认为适合用于与人或动物的组织接触而没有过度毒性或致癌性,并且优选没有刺激性、过敏反应或者其它问题或并发症的溶剂。此类溶剂包括有机溶剂,如醇、醚、酯和胺。
538、本发明化合物的“水合物”是通过一个或多个水分子与本发明化合物的一个或多个分子缔合而形成。这种水合物包括但不限于半水合物、一水合物、二水合物、三水合物和四水合物。与水合物组成无关,所有水合物通常被认为是药学上可接受的。
539、本发明化合物对fap具有高结合亲和性,以及对fap具有高抑制活性。由于这种高结合亲和性,本发明的化合物作为靶向剂以及如果与另一部分缀合时作为靶向部分是有效的、有用的和/或适合的。如本文优选使用的,靶向剂是与靶分子相互作用的制剂,所述靶分子在此情况中是所述fap。就本发明的化合物由此靶向的细胞和组织而言,表达所述fap的任何细胞和组织分别被靶向或可以被靶向。
540、在一实施方案中,所述化合物与成纤维细胞活化蛋白(fap)相互作用,优选与具有seq id no:1的氨基酸序列的人fap或其同系物相互作用,其中所述同系物的氨基酸序列与fap具有相同性,所述相同性为seq id no:1的氨基酸序列的至少85%。在优选的实施方案中,所述相同性为90%,优选95%、96%、97%、98%或99%。
541、可以如本领域技术人员已知的那样确定两个核酸分子之间的相同性。更具体地,基于指定的程序参数,可以使用序列比较算法来计算测试序列相对于参考序列的序列同源性百分比。测试序列优选是这样的序列或蛋白质或多肽,其相对于不同的蛋白质或多肽,被称为是相同的,或被测试是否相同以及如果相同,在多大程度上相同,其中这种不同的蛋白质或多肽也被称为参考序列并且优选是野生型的蛋白质或多肽,更优选是seq id no:1的人fap。
542、用于比较的序列的最佳比对可以例如通过smith&waterman的局部同源算法(smith,et al.,advances in applied mathematics,1981,2:482)、通过needleman&wunsch的同源比对算法(needleman,et al.,j mol biol,1970,48:443)、通过pearson&lipman的相似性搜索方法(pearson,et al.,proc natl acad sci u s a,1988,85:2444)、通过这些算法的计算机化执行程序(gap,bestfit,fasta和tfasta,在wisconsin genetics软件包中,genetics computer group,575science dr.,madison,wis.),或通过目视检查而进行。
543、适用于确定序列相同性百分比的算法的一个实例是在局部序列比对检索基本工具中使用的算法(以下称为“blast”),见例如altschul等人,1990(altschul,et al.,j molbiol,1990,215:403)和altschul et al.,1997(altschul,et al.,nucleic acids res,1997,25:3389)。用于执行blast分析的软件可通过国家生物技术信息中心(以下简称ncbi)公开获得。mcginnis等人(mcginnis,et al.,nucleic acids res,2004,32:w20)描述了使用得自ncbi的软件确定序列相同性的默认参数,所述软件例如是blastn(用于核苷酸序列)和blastp(用于氨基酸序列)。
544、在本发明的范围内,本发明的化合物用于或供用于治疗如本文公开的疾病的方法。这种方法优选包括向有需要的个体施用治疗有效量的本发明化合物的步骤。这种方法包括但不限于治愈性或辅助性癌症治疗。其在不可能治愈且以局部疾病控制或症状缓解为目的的情况中用作姑息治疗,或在治疗具有生存获益的情况中用作治疗性治疗且其可以是治愈性的。
545、治疗本文公开的疾病的方法包括治疗本文公开的疾病,包括肿瘤和癌症,并且可以用作主要疗法或用作二线、三线、四线或最终疗法。将本发明的化合物与其它治疗方法联合使用也在本发明范围内。本领域技术人员众所周知,包括治愈性、辅助性、新辅助性、治疗性或姑息性治疗等的精确治疗意图将取决于肿瘤类型、位置和阶段以及患者的总体健康状况。
546、在本发明的一实施方案中,所述疾病选自:瘤nos,良性瘤,不确定良性还是恶性的瘤,恶性瘤,转移性瘤,不确定原发还是转移的恶性瘤,良性肿瘤细胞,不确定良性或恶性的肿瘤细胞,恶性肿瘤细胞,小细胞型恶性肿瘤,巨细胞型恶性肿瘤,梭形细胞型恶性肿瘤,上皮瘤nos,良性上皮肿瘤,原位癌nos,癌nos,癌转移nos,癌扩散,良性上皮瘤,恶性上皮瘤,大细胞癌nos,未分化型癌nos,间变型癌nos,多形性癌,巨细胞和梭形细胞癌,巨细胞癌,梭形细胞癌,假肉瘤,多角细胞癌,球状细胞癌,微小瘤,小细胞癌nos,燕麦形细胞癌,小细胞癌,梭形细胞型、乳头状和鳞状细胞瘤,乳头状瘤nos,原位乳头状癌,乳头状癌nos,疣状乳头状瘤,疣状癌nos,鳞状细胞乳头状瘤,乳头状鳞状细胞癌,倒置乳头状瘤,乳头状瘤病nos,原位鳞状细胞癌nos,鳞状细胞癌nos,鳞状细胞癌转移nos,角化型鳞状细胞癌nos,大细胞非角化型鳞状细胞癌,小细胞非角化型鳞状细胞癌,梭形细胞型鳞状细胞癌,腺样鳞状细胞癌,不确定基质侵袭的原位鳞状细胞癌,微浸润型鳞状细胞癌,queyrat增殖性红斑,bowen病,淋巴上皮癌,基底细胞瘤,基底细胞肿瘤,基底细胞癌nos,多中心基底细胞癌,硬斑病型基底细胞癌,纤维上皮型基底细胞癌,基底鳞状癌,异型癌,jadassohn表皮内上皮瘤,毛上皮瘤,毛囊瘤,外毛根鞘瘤,毛母质瘤,移行细胞乳头状瘤和癌,移行细胞乳头状瘤nos,尿路上皮乳头状瘤,原位移行细胞癌,移行细胞癌nos,施奈德乳头状瘤,倒置型移行细胞乳头状瘤,施奈德癌,梭形细胞型移行细胞癌,基底细胞样癌,泄殖腔癌,乳头状移行细胞癌,腺瘤和腺癌,腺瘤nos,支气管腺瘤nos,原位腺癌,腺癌nos,转移性腺癌nos,硬腺癌,皮革状囊胃,表浅扩散性腺癌,肠型腺癌,扩散型癌,单形性腺瘤,基底细胞腺瘤,胰岛细胞腺瘤,胰岛细胞癌,胰岛瘤nos,恶性胰岛瘤,胰高血糖素瘤,恶性胰高血糖素瘤nos,胃泌素瘤nos,恶性胃泌素瘤,混合型胰岛细胞和外分泌腺癌,胆管腺瘤,胆管癌,胆管囊腺瘤,胆管囊腺癌,肝细胞腺瘤,肝细胞癌nos,良性肝胆管瘤,肝细胞癌合并胆管癌,小梁腺瘤,小梁腺癌,胚胎性腺瘤,外分泌腺真皮圆柱瘤,腺样囊性癌,筛状癌,腺瘤性息肉nos,腺瘤性息肉中的腺癌,管状腺瘤nos,管状腺癌,腺瘤性结肠息肉病,腺瘤性结肠息肉病中的腺癌,多发性腺瘤性息肉,实体癌nos,单纯癌,类癌瘤nos,恶性类癌瘤,类癌瘤银质瘤nos,恶性类癌瘤银质瘤,类癌瘤非银质瘤nos,恶性类癌瘤非银质瘤,恶性黏液类癌,复合类癌,肺腺瘤病,细支气管-肺泡腺癌,肺泡腺瘤,肺泡腺癌,乳头状腺瘤nos,乳头状腺癌nos,绒毛状腺瘤nos,绒毛状腺瘤中腺癌,绒毛状腺癌,管状绒毛状腺瘤,嫌色细胞腺瘤,嫌色细胞癌,嗜酸细胞腺瘤,嗜酸细胞癌,混合型嗜酸细胞-嗜碱细胞腺瘤,混合型嗜酸细胞-嗜碱细胞癌,亲氧性腺瘤,亲氧性腺癌,嗜碱细胞腺瘤,嗜碱细胞癌,透明细胞腺瘤,透明细胞腺癌nos,肾性肿瘤,肾细胞癌,透明细胞腺纤维瘤,颗粒细胞癌,主细胞腺瘤,水透明细胞腺瘤,水透明细胞腺癌,混合细胞腺瘤,混合细胞腺癌,脂肪腺瘤,滤泡状腺瘤,滤泡状腺癌nos,高分化型滤泡状腺癌,小梁型滤泡状腺癌,微滤泡腺瘤,大滤泡腺瘤,乳头状和滤泡状腺癌,无包膜硬化型癌,多发性内分泌腺瘤,肾小球旁肿瘤,肾上腺皮质腺瘤nos,肾上腺皮质癌,紧凑细胞型肾上腺皮质腺瘤,重度色素变异型肾上腺皮质腺瘤,透明细胞型肾上腺皮质腺瘤,肾小球细胞型肾上腺皮质腺瘤,混合细胞型肾上腺皮质腺瘤,子宫内膜样腺瘤nos,子宫内膜样腺瘤,交界性恶性肿瘤,子宫内膜样癌,子宫内膜样腺纤维瘤nos,子宫内膜样腺纤维瘤交界性恶性肿瘤,恶性子宫内膜样腺纤维瘤,附件和皮肤附属器肿瘤,皮肤附属器腺瘤,皮肤附属器癌,汗腺腺瘤,汗腺肿瘤nos,汗腺腺癌,顶泌腺瘤,顶泌腺癌,小汗腺顶螺旋体瘤,小汗腺螺旋腺瘤,汗腺囊瘤,乳头状汗腺囊瘤,乳头状汗腺腺瘤,汗管瘤nos,皮脂腺瘤,皮脂腺癌,蜡样腺瘤,蜡样腺癌,粘液表皮样肿瘤赘生物,粘液表皮样肿瘤,粘液表皮样囊性癌,粘液性和浆液性肿瘤,囊腺瘤nos,囊腺癌nos,浆液性囊腺瘤nos,浆液性囊腺瘤交界性恶性肿瘤,浆液性囊腺癌nos,乳头状囊腺瘤nos,乳头状囊腺瘤交界性恶性肿瘤,乳头状囊腺癌nos,乳头状浆液性囊腺瘤nos,乳头状浆液性囊腺瘤交界性恶性肿瘤,乳头状浆液性囊腺癌,浆液性表面乳头状瘤nos,浆液性表面乳头状瘤交界性恶性肿瘤,浆液性表面乳头状癌,粘液性囊腺瘤nos,粘液性囊腺瘤交界性恶性肿瘤,粘液性囊腺癌nos,乳头状粘液性囊腺瘤nos,乳头状粘液性囊腺瘤交界性恶性肿瘤,乳头状粘液性囊腺癌,粘液性腺瘤,粘液性腺癌,腹膜假粘液瘤,产生粘蛋白的腺癌,印戒细胞癌,转移的印戒细胞癌,导管,小叶和髓质肿瘤,非浸润性导管内癌nos,浸润性导管癌,粉刺性癌,非浸润性粉刺性癌nos,青少年乳腺癌,导管内乳头状瘤,非浸润性导管内乳头状腺癌,囊内乳头状腺瘤,非浸润性囊内癌,导管内乳头状瘤病nos,乳晕下导管乳头瘤病,髓样癌nos,髓样癌伴淀粉样基质,髓样癌伴淋巴样基质,原位小叶癌,小叶癌nos,浸润性导管癌,炎性癌,乳腺佩吉特病,佩吉特病和乳腺浸润性导管癌,乳腺外佩吉特病,腺泡细胞肿瘤赘生物,腺泡细胞腺瘤,腺泡细胞肿瘤,腺泡细胞癌,复杂上皮肿瘤,腺鳞癌,腺淋巴瘤,腺癌伴鳞状上皮化生,腺癌伴软骨和骨化生,腺癌伴梭形细胞化生,腺癌伴大汗腺化生,良性胸腺瘤,恶性胸腺瘤,特化性腺瘤,性索间质瘤,泡膜细胞瘤nos,膜细胞癌,黄体瘤nos,颗粒细胞瘤nos,恶性颗粒细胞瘤,颗粒细胞膜细胞瘤,良性雄性细胞瘤,男性母细胞瘤nos,恶性男性母细胞瘤,间质细胞瘤,男性细胞瘤,管状男性母细胞瘤nos,支持细胞癌,具有脂质储存的管状男性母细胞瘤,良性支持细胞瘤,支持细胞瘤nos,恶性支持细胞瘤,门细胞瘤,卵巢脂质细胞瘤,肾上腺剩余肿瘤,副神经节瘤和血管球瘤,副神经节瘤nos,恶性副神经节瘤,交感神经副神经节瘤,副交感神经节瘤,颈静脉球瘤,主动脉体瘤,颈动脉体瘤,肾上腺外副神经节瘤nos,恶性肾上腺外副神经节瘤,嗜铬细胞瘤nos,恶性嗜铬细胞瘤,血管球肉瘤,血管球肿瘤,血管球瘤,痣和黑色素瘤,色素痣nos,恶性黑色素瘤nos,结节性黑色素瘤,气球状细胞痣,气球细胞黑色素瘤,晕痣,鼻部纤维性丘疹,真皮内痣,巨细胞痣,无色素痣,无黑素性黑素瘤,交界痣,交界痣恶性黑色素瘤,癌前黑色素沉着病nos,恶性癌前黑色素沉着病,哈金森黑色素雀斑,哈金森黑色素雀斑中恶性黑色素瘤,浅表扩散性黑色素瘤,皮内痣,复合痣,巨大色素痣,巨大色素痣中恶性黑色素瘤,上皮样和梭形细胞痣,上皮样细胞黑色素瘤,梭形细胞黑色素瘤nos,梭形细胞黑色素瘤a型,梭形细胞黑色素瘤b型,混合上皮样和梭形细胞黑色素瘤,蓝色痣nos,恶性蓝色痣,细胞蓝痣,软组织肿瘤和肉瘤nos,软组织肿瘤,良性肉瘤nos,肉瘤病nos,梭形细胞肉瘤,巨细胞肉瘤,小细胞肉瘤,上皮样细胞肉瘤,纤维瘤性肿瘤,纤维瘤nos,纤维肉瘤nos,纤维粘液瘤,纤维粘液肉瘤,骨膜纤维瘤,骨膜纤维肉瘤,筋膜纤维瘤,筋膜纤维肉瘤,婴儿纤维肉瘤,弹性纤维瘤,侵袭性纤维瘤病,腹部纤维瘤病,成纤维性纤维瘤,纤维性组织细胞瘤nos,非典型纤维性组织细胞瘤,恶性纤维性组织细胞瘤,纤维黄瘤nos,非典型纤维黄瘤,恶性纤维黄瘤,皮肤纤维瘤nos,隆突性皮肤纤维瘤,皮肤纤维肉瘤nos,粘液瘤,粘液瘤nos,粘液肉瘤,脂肪瘤,脂肪瘤nos,脂肪肉瘤nos,纤维脂肪瘤,高分化型脂肪肉瘤,纤维粘液脂肪瘤,粘液样脂肪肉瘤,圆细胞脂肪肉瘤,多形脂肪肉瘤,混合型脂肪肉瘤,肌内脂肪瘤,梭形细胞脂肪瘤,血管平滑肌脂肪瘤,血管平滑肌脂肪肉瘤,血管脂肪瘤nos,浸润性血管脂肪瘤,骨髓脂肪瘤,蛰伏脂瘤,成脂细胞瘤病,肌瘤性肿瘤,平滑肌瘤nos,血管内平滑肌瘤,平滑肌肉瘤nos,上皮样平滑肌瘤,上皮样平滑肌肉瘤,细胞平滑肌瘤,奇异型平滑肌瘤,血管肌瘤,血管肌肉瘤,肌瘤,肌肉瘤,横纹肌瘤nos,横纹肌肉瘤nos,多形性横纹肌肉瘤,混合型横纹肌肉瘤,胎儿横纹肌瘤,成人横纹肌瘤,胚胎性横纹肌肉瘤,腺泡横纹肌肉瘤,复杂的混合和间质肿瘤,子宫内膜间质肉瘤,淋巴管内间质肌病,腺肌瘤,多形性腺瘤,混合瘤,恶性mullerian混合瘤nos,中胚层混合瘤,中胚层肾瘤,肾母细胞瘤nos,上皮性肾母细胞瘤,间叶性肾母细胞瘤,肝母细胞瘤,癌肉瘤nos,胚胎型癌肉瘤,肌上皮瘤,良性间质瘤,间质瘤nos,恶性间充质瘤,胚胎肉瘤,纤维上皮肿瘤,布伦纳瘤nos,布伦纳瘤,交界性恶性肿瘤,恶性布伦纳瘤,纤维腺瘤nos,管内型纤维腺瘤nos,管周型纤维腺瘤,腺纤维瘤nos,浆液性腺纤维瘤,粘液性腺纤维瘤,细胞管内纤维腺瘤,叶状囊肉瘤nos,恶性叶状囊肉瘤,幼年纤维腺瘤,滑膜肿瘤,良性滑膜瘤,滑膜肉瘤nos,梭形细胞型滑膜肉瘤,上皮细胞型滑膜肉瘤,双相型滑膜肉瘤,透明细胞肌腱和腱膜肉瘤,间皮瘤,良性间皮瘤,恶性间皮瘤,良性纤维间皮瘤,恶性纤维间皮瘤,良性上皮样间皮瘤,恶性上皮样间皮瘤,双相型良性间皮瘤,双相型恶性间皮瘤,腺瘤样肿瘤nos,生殖细胞肿瘤,无性细胞瘤,精原细胞瘤nos,未分化型精原细胞瘤,精母细胞性精原细胞瘤,生殖细胞瘤,胚胎癌nos,内胚窦瘤,多胚瘤,性腺胚细胞瘤,良性畸胎瘤,畸胎瘤nos,恶性畸胎瘤nos,畸胎癌,未分化型恶性畸胎瘤,中间型恶性畸胎瘤,皮样囊肿,恶性转化的皮样囊肿,甲状腺肿样卵巢瘤,恶性甲状腺肿样卵巢瘤,间质类癌,滋养细胞肿瘤,葡萄胎nos,侵袭性葡萄胎,绒毛膜癌,绒毛膜癌合并畸胎瘤,恶性滋养细胞畸胎瘤,中肾瘤,良性中肾瘤,中肾肿瘤,恶性中肾瘤,输卵管内膜瘤,血管肿瘤,血管瘤nos,血管肉瘤,海绵状血管瘤,静脉血管瘤,蔓状血管瘤,枯否细胞肉瘤,良性血管内皮瘤,血管内皮瘤nos,恶性血管内皮瘤,毛细血管瘤,肌内血管瘤,卡波西肉瘤,血管角质瘤,疣状角化性血管瘤,良性血管外皮细胞瘤,血管外皮细胞瘤nos,恶性血管外皮细胞瘤,血管纤维瘤nos,成血管细胞瘤,淋巴管肿瘤,淋巴管瘤nos,淋巴管肉瘤,毛细淋巴管瘤,海绵状淋巴管瘤,囊性淋巴管瘤,淋巴管肌瘤,淋巴管肌瘤增生,血管淋巴管瘤,骨瘤和骨肉瘤,骨瘤nos,骨肉瘤nos,成软骨细胞型骨肉瘤,成纤维细胞型骨肉瘤,毛细血管扩张型骨肉瘤,佩吉特骨病中的骨肉瘤,近皮质骨肉瘤,骨样骨瘤nos,成骨细胞瘤,软骨肿瘤,骨软骨瘤,骨软骨瘤病nos,软骨瘤nos,软骨瘤病nos,软骨肉瘤nos,近皮质软骨瘤,近皮质软骨肉瘤,成软骨细胞瘤nos,恶性成软骨细胞瘤,间叶性软骨肉瘤,软骨粘液样纤维瘤,巨细胞肿瘤,骨巨细胞肿瘤nos,恶性骨巨细胞瘤,软组织巨细胞瘤nos,软组织恶性巨细胞瘤,各种骨肿瘤,尤文氏肉瘤,长骨釉质瘤,骨化纤维瘤,牙源性肿瘤,良性牙源性肿瘤,牙源性肿瘤nos,恶性牙源性肿瘤,牙质瘤,牙骨质瘤nos,良性成牙骨质细胞瘤,牙骨质化纤维瘤,巨大牙骨质瘤,牙瘤nos,组合性牙瘤,混合性牙瘤,成釉细胞纤维性牙瘤,成釉细胞性牙肉瘤,腺瘤样牙源性肿瘤,钙化性牙源性囊肿,成釉细胞瘤nos,恶性成釉细胞瘤,牙成釉细胞瘤,牙源性鳞状细胞肿瘤,牙源性粘液瘤,牙源性纤维瘤nos,成釉细胞纤维瘤,成釉细胞纤维肉瘤,钙化上皮牙源性肿瘤,其它肿瘤,颅咽管瘤,松果体瘤,松果体细胞瘤,松果体母细胞瘤,黑色素神经外胚层肿瘤,脊索瘤,胶质瘤,恶性胶质瘤,脑胶质瘤病,混合性胶质瘤,室管膜下血管内膜样胶质细胞瘤,室管膜下巨细胞星形细胞瘤,脉络丛乳头状瘤nos,恶性脉络丛乳头状瘤,室管膜瘤nos,变性型室管膜瘤间,乳头状室管膜瘤,粘液乳头状室管膜瘤,星形细胞瘤nos,间变性型星形细胞瘤,原生质星形细胞瘤,肥胖型星形胶质细胞瘤,纤维状星形细胞瘤,毛细胞型星形细胞瘤,成胶质细胞瘤nos,极性海绵状母细胞瘤,星形母细胞瘤,成胶质细胞瘤nos,巨细胞成胶质细胞瘤,具有肉瘤成分的成胶质细胞瘤,原始极性成胶质细胞瘤,少突神经胶质细胞瘤nos,间变型少突神经胶质细胞瘤,成少突神经胶质细胞瘤,成神经管细胞瘤nos,促结缔组织增生性髓母细胞瘤,髓成肌细胞瘤,小脑肉瘤nos,怪细胞肉瘤,神经上皮瘤样肿瘤,神经节瘤,成神经节细胞瘤,神经节瘤病,成神经细胞瘤nos,髓质上皮瘤nos,畸胎样髓上皮瘤,神经上皮瘤nos,海绵状神经母细胞瘤,神经节神经胶质瘤,神经节神经胶质瘤,pacinian肿瘤,视网膜母细胞瘤nos,分化型视网膜母细胞瘤,未分化型视网膜母细胞瘤,嗅觉神经源性肿瘤,感觉神经细胞瘤,嗅神经母细胞瘤,感觉神经上皮瘤,脑膜瘤,脑膜瘤nos,脑膜瘤病nos,恶性脑膜瘤,脑膜瘤性脑膜瘤,纤维性脑膜瘤,砂粒体型脑膜瘤,血管瘤性脑膜瘤,成血管细胞性脑膜瘤,血管外皮细胞性脑膜瘤,过渡型脑膜瘤,乳头状脑膜瘤,脑膜的肉瘤病,神经鞘肿瘤,神经纤维瘤nos,神经纤维瘤病nos,神经纤维肉瘤,黑色素型神经纤维瘤,丛状神经纤维瘤,神经鞘膜瘤nos,神经鞘瘤病,恶性神经鞘膜瘤,神经瘤nos,颗粒细胞肿瘤和腺泡状软组织肉瘤,颗粒细胞肿瘤nos,恶性颗粒细胞肿瘤,腺泡状软组织肉瘤,淋巴瘤nos或弥漫型、良性淋巴瘤肿瘤,恶性淋巴瘤nos,非霍奇金型恶性淋巴瘤,未分化细胞型恶性淋巴瘤nos,干细胞型恶性淋巴瘤,曲核细胞型恶性淋巴瘤nos,淋巴肉瘤nos,淋巴浆细胞型恶性淋巴瘤,免疫母细胞型恶性淋巴瘤,混合淋巴细胞-组织细胞型恶性淋巴瘤nos,中心母细胞-中心细胞弥漫型恶性淋巴瘤,恶性淋巴瘤滤泡中心细胞nos,淋巴细胞高分化型恶性淋巴瘤nos,淋巴细胞中等分化型恶性淋巴瘤nos,中心细胞型恶性淋巴瘤,滤泡中心细胞分裂型恶性淋巴瘤nos,淋巴细胞低分化型恶性淋巴瘤nos,幼淋巴细胞淋巴肉瘤,恶性淋巴瘤中心母细胞型nos,滤泡中心细胞非裂型恶性淋巴瘤,网状细胞肉瘤,网状细胞肉瘤nos,多形性细胞型网状肉瘤,结节型网状肉瘤,霍奇金病,霍奇金病nos,淋巴细胞优势型霍奇金病,混合细胞型霍奇金病,淋巴细胞耗竭型霍奇金病nos,淋巴细胞耗竭弥漫性纤维化型霍奇金病,淋巴细胞耗竭网状型霍奇金病,结节硬化型症霍奇金病,结节硬化型霍奇金病细胞期,霍奇金病副肉芽肿,霍奇金病肉芽肿,霍奇金肉瘤,结节或滤泡型淋巴瘤,结节型恶性淋巴瘤nos,混合淋巴细胞-组织细胞结节型恶性淋巴瘤,中心母细胞型-中心细胞滤泡型恶性淋巴瘤,淋巴细胞高分化结节型恶性淋巴瘤,淋巴细胞中等分化结节型恶性淋巴瘤,滤泡中心细胞分裂滤泡型恶性淋巴瘤,淋巴细胞低分化结节型恶性淋巴瘤,中心母细胞型滤泡型恶性淋巴瘤,滤泡中心细胞非分裂滤泡型恶性淋巴瘤,蕈样真菌病,蕈样真菌病,sezary病,各种网状内皮组织瘤,小神经胶质细胞瘤,恶性组织细胞增多病,组织细胞性髓性网状细胞增生症,letterer-siwe病,浆细胞肿瘤,浆细胞骨髓瘤,良性浆细胞瘤,浆细胞瘤nos,恶性浆细胞瘤,肥大细胞肿瘤,肥大细胞瘤nos,肥大细胞肉瘤,恶性肥大细胞增多症,burkitt肿瘤,burkitt肿瘤,白血病,白血病nos,急性白血病nos,亚急性白血病nos,慢性白血病nos,非白血性白血病nos,复合型白血病,复合白血病,淋巴性白血病,淋巴性白血病nos,急性淋巴性白血病,亚急性淋巴性白血病,慢性淋巴性白血病,非白血性淋巴性白血病,幼淋巴细胞性白血病,浆细胞性白血病,浆细胞白血病,红白血病,红白血病,急性红细胞增多症,慢性红细胞增多症,淋巴肉瘤细胞性白血病,淋巴肉瘤细胞白血病,髓系白血病,髓系白血病nos,急性髓系白血病,亚急性髓系白血病,慢性髓系白血病,非白血性髓系白血病,中性粒细胞性白血病,急性早幼粒细胞白血病,嗜碱性粒细胞性白血病,嗜碱性粒细胞白血病,嗜酸性粒细胞性白血病,嗜酸性粒细胞白血病,单核细胞白血病,单核细胞白血病nos,急性单核细胞白血病,亚急性单核细胞白血病,慢性单核细胞白血病,非白血性单核细胞白血病,其它白血病,肥大细胞白血病,巨核细胞白血病,巨核细胞骨髓组织增生病,骨髓性肉瘤,毛细胞白血病,各种骨髓增生和淋巴增生性疾病,真性红细胞增多症,急性全髓白血病,慢性骨髓增生性疾病,骨髓硬化伴髓样化生,特发性血小板增多症,慢性淋巴增生性疾病。
547、在本发明的一实施方案中,所述疾病选自胰腺肿瘤,胰腺腺癌,胰头肿瘤,胰体肿瘤,胰尾肿瘤,胰管肿瘤,胰岛肿瘤,胰颈肿瘤,前列腺肿瘤,前列腺腺癌,前列腺腺体,神经内分泌肿瘤,乳腺癌,乳房中央部分肿瘤,乳房内上象限,乳房内下象限,乳房外上象限,乳房外下象限,乳房腋尾,乳房的重叠病变,青少年乳腺癌,甲状旁腺肿瘤,骨髓瘤,肺癌,小细胞肺癌,非小细胞肺癌,主支气管肿瘤,肺上叶肿瘤,肺中叶肿瘤,肺下叶肿瘤,结直肠癌,升结肠肿瘤,结肠肝曲肿瘤,横结肠肿瘤,结肠脾曲肿瘤,降结肠肿瘤,乙状结肠肿瘤,结肠的重叠病变,小肠肿瘤,肝脏肿瘤,肝细胞腺瘤,肝细胞癌,肝胆管瘤,联合的肝细胞癌和胆管癌,肝母细胞瘤,卵巢癌,肉瘤,骨肉瘤,纤维肉瘤,胃肠道间质瘤,胃肠道,胃癌,甲状腺癌,甲状腺髓样癌,甲状腺,肾细胞癌,肾盂肿瘤,膀胱肿瘤,膀胱癌,膀胱三角的肿瘤,膀胱顶肿瘤,膀胱侧壁肿瘤,膀胱后壁肿瘤,输尿管口肿瘤,脐尿管肿瘤,膀胱的重叠病变,基底细胞癌,基底细胞肿瘤赘生物,基底细胞肿瘤,基底细胞癌,多中心基底细胞癌,基底细胞样癌,基底细胞腺瘤,鳞状细胞癌,口腔鳞状细胞癌,喉鳞状细胞癌,宫颈癌,外子宫颈肿瘤,子宫颈的重叠病变,子宫颈治肿瘤,子宫峡部肿瘤,子宫肿瘤,卵巢肿瘤,食管肿瘤,食管胸段肿瘤,食管腹段肿瘤,食管上三分之一肿瘤,食管中三分之一肿瘤,食管下三分之一肿瘤,食管的重叠病变,子宫内膜癌,头颈癌,淋巴瘤,恶性间皮瘤,间皮肿瘤,间皮瘤,纤维间皮瘤,纤维间皮瘤,上皮样间皮瘤,上皮样间皮瘤,十二指肠癌,神经内分泌肿瘤,肺神经内分泌肿瘤,胰腺神经内分泌肿瘤,前肠神经内分泌肿瘤,中肠神经内分泌肿瘤,后肠神经内分泌肿瘤,胃肠胰神经内分泌肿瘤神经内分泌肿癌,乳腺神经内分泌肿瘤,卵巢神经内分泌肿瘤,睾丸癌,胸腺癌,胃肿瘤,胃底肿瘤,胃体肿瘤,胃窦肿瘤,幽门肿瘤,胃小弯肿瘤,胃大弯肿瘤,胃重叠病变,副神经节瘤,神经节瘤,黑色素瘤,恶性黑色素瘤,结节性黑色素瘤,无色素性黑色素瘤,浅表扩散性黑色素瘤,上皮样细胞黑色素瘤,梭形细胞黑色素瘤,混合上皮样和梭形细胞黑色素瘤。
548、在又一实施方案中,前述适应症可以出现在选自以下的器官和组织:外上唇,外下唇,外唇nos,上唇粘膜,下唇粘膜,唇粘膜nos,唇连合处,唇重叠病变,舌底nos,舌背侧面nos,舌边缘,舌腹侧面nos,舌前2/3nos,舌扁桃体,舌重叠病变,舌nos,上牙龈,下牙龈,牙龈nos,口前底,口侧底,口底重叠病变,口底nos,硬腭,软腭nos,悬雍垂,腭重叠病变,腭nos,颊粘膜,口腔前庭,磨牙后区,口其它和非特定部分的重叠病变,口nos,腮腺,颌下腺,舌下腺,大唾液腺重叠病变,大唾液腺nos,扁桃体窝,扁桃体柱,扁桃体重叠病变,扁桃体nos,会厌谷,会厌前面,侧壁口咽,口咽后壁,鳃裂,口咽的重叠病变,口咽nos,鼻咽上壁,鼻咽后壁,鼻咽侧壁,鼻咽前壁,鼻咽的重叠病变,鼻咽nos,梨状隐窝,环状软骨后区,杓状会厌皱襞喉咽面,喉咽后壁,喉咽的重叠病变,喉咽nos,咽nos,咽喉,咽部淋巴环,唇口腔和咽部重叠病变,食管颈段,食管胸段,食管腹段,食管上三分之一,食管中三分之一,食管下三分之一,食管的重叠病变,食管nos,贲门,胃底,胃体,胃窦,幽门,胃小弯nos,胃大弯nos,胃的重叠病变,胃nos,十二指肠,空肠,回肠,麦克尔憩室,小肠的重叠病变,小肠nos,盲肠,阑尾,升结肠,结肠肝曲,横结肠,结肠脾曲,降结肠,乙状结肠,结肠的重叠病变,结肠nos,直肠乙状结肠交界处,直肠nos,肛门nos,肛管,泄殖腔源性区,直肠肛门和肛管的重叠病变,肝脏,肝内胆管,胆囊,肝外胆管,肝胰管壶腹,胆道的重叠病变,胆道nos,胰头,胰体,胰尾,胰管,胰岛,胰颈,胰腺的重叠病变,胰腺nos,肠道nos,消化系统的重叠病变,胃肠道nos,鼻腔,中耳,上颌窦,筛窦,额窦,蝶窦,副鼻窦的重叠病变,副鼻窦nos,声门,声门上,声门下,喉软骨,喉的重叠病变,喉nos,气管,主支气管,肺上叶,肺中叶,肺下叶,肺的重叠病变,肺nos,胸腺,心脏,前纵隔,后纵隔,纵隔nos,胸膜nos,心脏纵隔和胸膜的重叠病变,上呼吸道nos,呼吸系统和胸内器官的重叠病变,呼吸道nos,上肢长骨关节,上肢短骨关节,下肢长骨关节,下肢短骨关节,四肢骨关节和关节软骨的重叠病变,四肢骨nos,颅面骨,下颌骨,脊柱,肋骨胸骨锁骨,盆骨,骨关节和关节软骨的重叠病变,骨nos,血液,骨髓,脾脏,网状内皮系统nos,造血系统,唇部皮肤nos,眼睑nos,外耳,面部皮肤,头皮颈部皮肤,躯干皮肤,上肢皮肤,下肢皮肤,头颈部周围神经,肩臂部周围神经,腿部周围神经,胸部周围神经,腹部周围神经,盆部周围神经,周围神经干,周围神经和自主神经系统的重叠病变,自主神经系统nos,腹膜后腔,腹膜,腹膜nos,腹膜后腔和腹膜的重叠病变,头部结缔组织,臂部结缔组织,腿部结缔组织,胸部结缔组织,腹部结缔组织,盆部结缔组织,躯干结缔组织nos,皮下结缔组织和其它软组织的重叠病变,结缔组织nos,乳头,乳房中央部分,乳房内上象限,乳房内下象限,乳房外上象限,乳房外下象限,乳房腋尾,乳房的重叠病变,乳房nos,大阴唇,小阴唇,阴蒂,外阴的重叠病变,外阴nos,阴道nos,子宫颈内膜,子宫颈外膜,子宫颈的重叠病变,子宫颈,子宫峡部,子宫内膜,子宫肌层,子宫底,子宫体的重叠病变,子宫体,子宫nos,卵巢,输卵管,阔韧带,圆韧带,子宫旁组织,子宫附件,沃尔夫氏体,女性生殖器官的重叠病变,女性生殖道nos,包皮,阴茎,阴茎体,阴茎的重叠病变,阴茎nos,前列腺,隐睾,下降睾丸,睾丸nos,附睾,精索,阴囊nos,鞘膜,男性生殖器官的重叠病变,男性生殖器官nos,肾nos,肾盂,输尿管,膀胱三角区,膀胱顶,膀胱侧壁,膀胱后壁,输尿管口,脐尿管,膀胱的重叠病变,膀胱nos,尿道,尿道旁腺,泌尿器官的重叠病变,泌尿系统nos,结膜,角膜,视网膜,脉络膜,睫状体,泪腺,眼眶nos,眼和附属器的重叠病变,眼nos,脑膜,脊膜,脑膜nos,大脑,额叶,颞叶,顶叶,枕叶,脑室,小脑nos,脑干,脑的重叠病变,脑nos,脊髓,马尾神经,嗅神经,视神经,听神经,颅神经nos,脑和中枢神经系统重叠病变,神经系统nos,甲状腺,肾上腺皮质,肾上腺髓质,肾上腺nos,甲状旁腺,脑垂体,颅咽管,松果体,颈动脉体,主动脉体,内分泌腺及相关结构的重叠病变,内分泌腺nos,头面部或颈部nos,胸部nos,腹部nos,盆部nos,上肢nos,下肢nos,其它不明确的部位,不明确部位的重叠病变,头面颈部淋巴结,胸腔内淋巴结,腹内淋巴结,腋下淋巴结,腿部淋巴结,腹股沟区淋巴结,盆腔淋巴结,多区域淋巴结,淋巴结nos,原发部位不明。
549、用本技术公开和要求保护的化合物治疗的个体可以联合其它非手术抗增殖(例如抗癌)药物疗法进行治疗。在一个实施方案中,所述化合物可以与抗癌化合物例如细胞生长抑制化合物联合施用。细胞抑制化合物是抑制细胞生长和/或增殖的化合物(例如,小分子、核酸或蛋白质)。在一些实施方案中,细胞抑制化合物针对肿瘤的恶性细胞。在其它实施方案中,细胞抑制化合物是抑制血管平滑肌细胞或成纤维细胞生长和/或增殖的化合物。
550、与本技术公开和权利要求的化合物联合使用的合适的抗增殖药物或细胞抑制化合物包括抗癌药。许多可以使用的抗癌药物是公知的,包括但不限于:阿西维辛(acivicin);阿柔比星(aclarubicin);盐酸阿考达唑(acodazole hydrochloride);阿克罗宁(acronine);阿多来新(adozelesin);阿地白介素(aldesleukin);六甲蜜胺(altretamine);安波霉素(ambomycin);乙酸阿美蒽醌(ametantrone acetate);氨鲁米特(aminoglutethimide);安吖啶(amsacrine);阿那曲唑(anastrozole);氨茴霉素(anthramycin);天冬酰胺酶(asparaginase);曲林菌素(asperlin);阿扎胞苷(azacitidine);阿扎替派(azetepa);阿佐霉素(azotomycin);巴马司他(batimastat);苄替哌(benzodepa);比卡鲁胺(bicalutamide);盐酸比生群(bisantrene hydrochloride);二甲磺酸双奈法德(bisnafide dimesylate);比折来新(bizelesin);硫酸博来霉素(bleomycin sulfate);布喹那钠(brequinar sodium);溴匹立明(bropirimine);白消安(busulfan);放线菌素c(cactinomycin);卡普睾酮(calusterone);卡醋胺(caracemide);卡贝替姆(carbetimer);卡铂(carboplatin);卡莫司汀(carmustine);盐酸卡柔比星(carubicin hydrochloride);卡折来新(carzelesin);西地芬戈(cedefingol);苯丁酸氮芥(chlorambucil);西罗霉素(cirolemycin);顺铂(cisplatin);克拉屈滨(cladribine);crisnatol mesylate;环磷酰胺(cyclophosphamide);阿糖孢苷(cytarabine);达卡巴嗪(dacarbazine);放线菌素d(dactinomycin);盐酸柔红霉素(daunorubicinhydrochloride);地西他滨(decitabine);右奥马铂(dexormaplatin);地扎胍宁(dezaguanine);甲磺酸地扎胍宁(dezaguanine mesylate);地吖醌(diaziquone);多西他赛(docetaxel);阿霉素(doxorubicin);盐酸阿霉素(doxorubicin hydrochloride);屈洛昔芬(droloxifene);柠檬酸屈洛昔芬(droloxifenecitrate);丙酸屈他雄酮(dromostanolone propionate);达佐霉素(duazomycin);依达曲沙(edatrexate);盐酸依氟鸟氨酸(eflornithine hydrochloride);依沙芦星(elsamitrucin);恩洛铂(enloplatin);恩普氨酯(enpromate);依匹哌啶(epipropidine);盐酸表阿霉素(epirubicin hydrochloride);厄布洛唑(erbulozole);盐酸依索比星(esorubicinhydrochloride);雌莫司汀(estramustine);雌莫司汀磷酸钠(estramustinephosphatesodium);依他硝唑(etanidazole);依托泊苷(etoposide);磷酸依托泊苷(etoposidephosphate);艾托卜宁(etoprine);盐酸法倔唑(fadrozole hydrochloride);法扎拉滨(fazarabine);芬维a胺(fenretinide);氟尿苷(floxuridine);磷酸氟达拉滨(fludarabine phosphate);氟尿嘧啶(fluorouracil);氟西他宾(fluorocitabine);磷喹酮(fosquidone);福司曲星钠(fostriecin sodium);吉西他滨(gemcitabine);盐酸吉西他滨(gemcitabine hydrochloride);羟基脲(hydroxyurea);盐酸伊达比星(idarubicinhydrochloride);异环磷酰胺(ifosfamide);伊莫福新(ilmofosine);干扰素α-2a;干扰素α-2b;干扰素α-n1;干扰素α-n3;干扰素β-i a;干扰素γ-i b;异丙铂(iproplatin);盐酸伊立替康(irinotecanhydrochloride);醋酸兰瑞肽(lanreotide acetate);来曲唑(letrozole);醋酸亮丙瑞林(leuprolideacetate);盐酸利阿唑(liarozolehydrochloride);洛美曲索钠(lometrexol sodium);洛莫司汀(lomustine);盐酸洛索蒽醌(losoxantrone hydrochloride);马索罗酚(masoprocol);美登素(maytansine);盐酸氮芥(mechlorethamine hydrochloride);醋酸甲地孕酮(megestrol acetate);醋酸美伦孕酮(melengestrol acetate);美法仑(melphalan);美诺立尔(menogaril);巯嘌呤(mercaptopurine);甲氨蝶呤(methotrexate);甲氨蝶呤钠(methotrexate sodium);氯苯氨啶(metoprine);美妥替哌(meturedepa);米丁度胺(mitindomide);米托卡星(mitocarcin);mitocromin;米托洁林(mitogillin);米托马星(mitomalcin);丝裂霉素(mitomycin);米托司培(mitosper);米托坦(mitotane);盐酸米托蒽醌(mitoxantronehydrochloride);霉酚酸(mycophenolic acid);尼拉帕利(niraparib);诺考达唑(nocodazole);诺加霉素(nogalamycin);奥拉帕利(olaparib);奥马铂(ormaplatin);奥昔舒仑(oxisuran);紫杉醇(paclitaxel);培门冬酶(pegaspargase);培利霉素(peliomycin);戊氮芥(pentamustine);硫酸培洛霉素(peplomycin sulfate);培磷酰胺(perfosfamide);哌泊溴烷(pipobroman);哌泊舒凡(piposulfan);盐酸吡罗蒽醌(piroxantrone hydrochloride);普卡霉素(plicamycin);普洛美坦(plomestane);卟吩姆钠(porfimer sodium);泊非霉素(porfiromycin);泼尼莫司汀(prednimustine);盐酸丙卡巴肼(procarbazine hydrochloride);嘌呤霉素(puromycin);盐酸嘌呤霉素(puromycinhydrochloride);吡唑呋喃菌素(pyrazofurin);利波腺苷(riboprine);罗谷亚胺(rogletimide);卢卡帕利(rucaparib);沙芬戈(safingol);盐酸沙芬戈(safingolhydrochloride);司莫司汀(semustine);辛曲秦(simtrazene);sparfosate sodium;司帕霉素(sparsomycin);盐酸锗螺胺(spirogermanium hydrochloride);螺莫司汀(spiromustine);螺铂(spiroplatin);链霉黑素(streptonigrin);链脲佐菌素(streptozocin);磺氯苯脲(sulofenur);他拉唑帕利(talazoparib);他利霉素(talisomycin);紫杉醇;泰索帝(taxotere);替可加兰钠(tecogalan sodium);喃氟啶(tegafur);盐酸替洛蒽醌(teloxantrone hydrochloride);替莫卟吩(temoporfin);替尼泊苷(teniposide);替罗昔隆(teroxirone);睾内酯(testolactone);硫咪嘌呤(thiamiprine);硫鸟嘌呤(thioguanine);噻替派(thiotepa);噻唑呋林(tiazofurin);替拉扎明(tirapazamine);盐酸拓扑替康(topotecan hydrochloride);柠檬酸托瑞米芬(toremifene citrate);乙酸曲托龙(trestolone acetate);磷酸曲西立滨(triciribinephosphate);三甲曲沙(trimetrexate);三甲曲沙葡糖醛酸酯(trimetrexateglucuronate);盐酸妥布氯唑(tubulozole hydrochloride);乌拉莫司汀(uracilmustard);乌瑞替派(uredepa);伐普肽(vapreotide);维利帕尼(velaparib);维替泊芬(verteporfin);硫酸长春花碱(vinblastine sulfate);硫酸长春新碱(vincristinesulfate);长春地辛(vindesine);硫酸长春地辛(vindesine sulfate);硫酸长春匹定(vinepidine sulfate);硫酸长春甘酯(vinglycinate sulfate);硫酸长春罗新(vinleurosine sulfate);酒石酸长春瑞滨(vinorelbine tartrate);硫酸长春罗定(vinrosidine sulfate);硫酸长春利定(vinzolidine sulfate);伏氯唑(vorozole);折尼铂(zeniplatin);净司他丁(zinostatin);和盐酸佐柔比星(zorubicin hydrochloride)。
551、其它抗癌药物包括但不限于:20-epi-1,25二羟基维生素d3;5-乙炔基尿嘧啶;阿比特龙(abiraterone);酰基富烯;腺环戊醇(adecypenol);阿多来新(adozelesin);all-tk拮抗剂;氨莫司汀(ambamustine);amidox;氨磷汀(amifostine);氨基乙酰丙酸(aminolevulinic acid);氨柔比星(amrubicin);阿那格雷(anagrelide);穿心莲内酯(andrographolide);血管生成抑制剂;拮抗剂d;拮抗剂g;antarelix;抗背化形态发生蛋白-1(anti-dorsalizing morphogenetic protein-1);抗雌激素;抗瘤酮(antineoplaston);反义寡核苷酸;甘氨酸阿非迪霉素(aphidicolin glycinate);凋亡基因调节剂;凋亡调节剂;无嘌呤酸;ara-cdp-dl-ptba;精氨酸脱氨酶;asulacrine;阿他美坦(atamestane);阿莫司汀(atrimustine);axinastatin 1;axinastatin 2;axinastatin 3;阿扎司琼(azasetron);阿扎毒素(azatoxin);重氮酪氨酸(azatyrosine);浆果赤霉素(baccatin)iii衍生物;balanol;巴马司他(batimastat);bcr/abl拮抗剂;benzochlorins;苯甲酰星形孢菌素(benzoylstaurosporine);β-内酰胺衍生物;β-alethine;betaclamycinb;桦木酸;bfgf抑制剂;双吖丙啶基精胺(bisaziridinylspermine);双奈法德(bisnafide);bistratene a;breflate;布朵替坦(budotitane);丁硫氨酸亚砜胺(buthionine sulfoximine);钙泊三醇(calcipotriol);钙磷酸蛋白(calphostin)c;喜树碱衍生物;canarypox il-2;卡培他滨(capecitabine);甲酰胺-氨基-三唑;羧基酰胺三唑;carest m3;carn 700;软骨衍生的抑制剂;酪蛋白激酶抑制剂(icos);粟树精胺(castanospermine);cecropin b;西曲瑞克(cetrorelix);二氢卟吩(chlorins);氯代喹喔啉磺酰胺(chloroquinoxaline sulfonamide);西卡前列素(cicaprost);顺式卟啉;氯米芬(clomifene)类似物;克霉唑(clotrimazole);collismycin a;collismycin b;康普瑞汀(combretastatin)a4;康普瑞汀类似物;conagenin;crambescidin 816;crisnatol;cryptophycin 8;cryptophycin a衍生物;curacin a;cyclopentanthraquinones;cycloplatam;cypemycin;阿糖胞苷ocfosfate;溶细胞因子;细胞抑素(cytostatin);达昔单抗(dacliximab);脱氢膜海鞘素b(dehydrodidemnin b);德舍瑞林(deslorelin);dexifosfamide;右雷佐生(dexrazoxane);右维拉帕米(dexverapamil);膜海鞘素b(didemnin b);didox;diethylnorspermin;二氢-5-氮杂胞苷;9-二氢紫杉醇(dihydrotaxol,9-);dioxamycin;二苯基螺莫司汀(spiromustine);二十二醇(docosanol);多拉司琼(dolasetron);去氧氟尿苷(doxifluridine);屈大麻酚(dronabinol);倍癌霉素(duocarmycin)sa;依布硒啉(ebselen);依考莫司汀(ecomustine);依地福新(edelfosine);依决洛单抗(edrecolomab);eflomithine;榄香烯(elemene);乙嘧替氟(emitefur);表阿霉素(epirubicin);依立雄胺(epristeride);雌莫司汀类似物;雌激素激动剂;雌激素拮抗剂;依他硝唑(etanidazole);磷酸依托泊苷(etoposide);依西美坦(exemestane);非格司亭(filgrastim);非那雄胺(finasteride);夫拉平度(flavopiridol);氟卓斯汀(flezelastine);氟甾酮(fluasterone);氟达拉滨(fludarabine);fluorodaunorunicin hydrochloride;福酚美克(forfenimex);福美司坦(formestane);福莫司汀(fotemustine);gadolinium texaphyrin;硝酸镓;加洛他滨(galocitabine);加尼瑞克(ganirelix);明胶酶抑制剂;谷胱甘肽抑制剂;hepsulfam;heregulin;六亚甲基二乙酰胺;金丝桃素(hypericin);伊班膦酸(ibandronic acid);艾多昔芬(idoxifene);伊决孟酮(idramantone);伊莫福新(ilmofosine);伊洛马司他(ilomastat);咪唑并吖啶酮类(imidazoacridones);咪喹莫特(imiquimod);免疫刺激肽;胰岛素样生长因子-i受体抑制剂;干扰素激动剂;干扰素;白介素;碘苄胍(iobenguane);碘阿霉素(iododoxorubicin);甘薯苦醇(ipomeanol),4-;伊立替康(irinotecan);伊罗普拉(iroplact);伊索拉定(irsogladine);isobengazole;isohomohalicondrin b;伊他司琼(itasetron);jasplakinolide;kahalalide f;片螺素-n三醋酸酯;兰瑞肽(lanreotide);雷拉霉素(leinamycin);来格司亭(lenograstim);硫酸香菇多糖(lentinan sulfate);来普他汀(leptolstatin);白血病抑制因子;白细胞α干扰素;亮丙瑞林(leuprolide)+雌激素+黄体酮;亮丙瑞林(leuprorelin);左旋咪唑(levamisole);利阿唑(liarozole);线性聚胺类似物;亲脂性二糖肽;亲脂性铂化合物;lissoclinamide 7;洛铂(lobaplatin);蚯蚓磷脂(lombricine);洛美曲索(lometrexol);氯尼达明(lonidamine);洛索蒽醌(losoxantrone);洛伐他汀(lovastatin);洛索立宾(loxoribine);勒托替康(lurtotecan);lutetium texaphyrin;lysofylline;裂解肽;美坦辛(maitansine);mannostatin a;马立马司他(marimastat);马索罗酚(masoprocol);乳腺丝抑蛋白(maspin);基质溶素(matrilysin)抑制剂;基质金属蛋白酶抑制剂;merbarone;meterelin;蛋氨酸酶(methioninase);甲氧氯普胺(metoclopramide);mif抑制剂;米非司酮(mifepristone);米替福新(miltefosine);米立司亭(mirimostim);错配的双链rna;米托胍腙(mitoguazone);二溴卫矛醇(mitolactol);丝裂霉素(mitomycin)类似物;米托萘胺(mitonafide);mitotoxin成纤维细胞生长因子-皂草素;莫法罗汀(mofarotene);molgramostim;单克隆抗体,人绒毛膜促性腺激素;单磷酰脂a+分支杆菌细胞壁sk;莫哌达醇(mopidamol);多药耐药基因抑制剂;基于多肿瘤阻抑物1的疗法;氮芥抗癌化合物;mycaperoxide b;分支杆菌细胞壁提取物;myriaporone;n-乙酰地那林(dinaline);n-取代的苯甲酰胺;那法瑞林(nafarelin);nagrestip;纳洛酮+喷他佐辛;napavin;naphterpin;那托司亭(nartograstim);奈达铂(nedaplatin);奈莫柔比星(nemorubicin);奈立膦酸(neridronic acid);中性肽链内切酶;尼鲁米特(nilutamide);二左霉素(nisamycin);氮氧化物调节剂;硝基氧抗氧化剂;nitrullyn;o6-苄基鸟嘌呤;奥曲肽(octreotide);okicenone;寡核苷酸;奥那司酮(onapristone);昂丹司琼(ondansetron);昂丹司琼(ondansetron);oracin;口服细胞因子诱导剂;奥沙特隆(osaterone);奥沙利铂(oxaliplatin);oxaunomycin;紫杉醇(paclitaxel)类似物;紫杉醇衍生物;palauamine;棕榈酰根瘤菌素(palmitoylrhizoxin);帕米膦酸(pamidronic acid);人参炔三醇(panaxytriol);帕诺米芬(panomifene);parabactin;帕折普汀(pazelliptine);培门冬酶(pegaspargase);peldesine;戊聚糖聚硫酸钠;喷司他丁(pentostatin);pentrozole;全氟溴烷(perflubron);培磷酰胺(perfosfamide);紫苏醇(perillyl alcohol);phenazinomycin;乙酸苯酯;磷酸酶抑制剂;沙培林(picibanil);盐酸毛果芸香碱(pilocarpine hydrochloride);吡柔比星(pirarubicin);吡曲克辛(piritrexim);placetin a;placetin b;纤溶酶原激活物抑制剂;铂络合物;铂化合物;铂-三胺络合物;卟吩姆钠(porfimer sodium);甲基丝裂霉素(porfiromycin);丙基双-吖啶酮;前列腺素j2;蛋白酶体抑制剂;基于蛋白a的免疫调节剂;蛋白质激酶c抑制剂;蛋白质激酶c抑制剂,microalgal;蛋白质酪氨酸磷酸酶抑制剂;嘌呤核苷磷酸化酶抑制剂;羟基茜草素(purpurins);吡唑并吖啶(pyrazoloacridine);pyridoxylated血红蛋白聚氧乙烯缀合物;raf拮抗剂;雷替曲塞(raltitrexed);雷莫司琼(ramosetron);ras法尼基蛋白转移酶抑制剂;ras抑制剂;ras-gap抑制剂;脱甲基化瑞替普汀(retelliptine);re 186依替膦酸铼;利索新(rhizoxin);核酶;rii retinamide;罗希吐碱(rohitukine);罗莫肽(romurtide);罗喹美克(roquinimex);rubiginone b1;ruboxyl;saintopin;sarcnu;sarcophytol a;沙格司亭(sargramostim);sdi 1模拟物;衰老衍生的抑制剂1;有义寡核苷酸;信号转导抑制剂;信号转导调节剂;单链抗原结合蛋白;sizofuran;索布佐生(sobuzoxane);硼卡钠;苯乙酸钠;solverol;生长调节素结合蛋白;索纳明(sonermin);sparfosic acid;spicamycin d;螺莫司汀(spiromustine);斯耐潘定(splenopentin);海绵抑制素(spongistatin)1;角鲨胺(squalamine);干细胞抑制剂;干细胞分裂抑制剂;stipiamide;溶基质素抑制剂;sulfinosine;强效血管内皮肽拮抗剂;suradista;苏拉明(suramin);苦马豆素(swainsonine);合成的葡糖氨基葡聚糖;他莫司汀(tallimustine);他莫昔芬甲碘化物(tamoxifen methiodide);牛磺莫司汀(tauromustine);他扎罗汀(tazarotene);替可加兰钠(tecogalan sodium);替加氟(tegafur);tellurapyrylium;端粒酶抑制剂;替莫唑胺(temozolomide);四氯十氧化物(tetrachlorodecaoxide);tetrazomine;thaliblastine;沙利度胺(thalidomide);thiocoraline;血小板生成素;血小板生成素模拟物;胸腺法新(thymalfasin);促胸腺生成素受体激动剂;胸腺曲南(thymotrinan);甲状腺刺激激素;tinethyl etiopurpurin;二氯二茂钛(titanocene dichloride);topsentin;托瑞米芬(toremifene);全能干细胞因子;翻译抑制剂;维甲酸(tretinoin);三乙酰尿苷;曲西立滨(triciribine);托烷司琼(tropisetron);妥罗雄脲(turosteride);酪氨酸激酶抑制剂;tyrphostins;ubc抑制剂;乌苯美司(ubenimex);泌尿生殖窦衍生生长抑制因子;尿激酶受体拮抗剂;variolin b;载体系统,红细胞基因治疗;维拉雷琐(velaresol);藜芦胺(veramine);verdins;长春瑞滨(vinorelbine);vinxaltine;vitaxin;扎诺特隆(zanoterone);亚苄维c(zilascorb);以及净司他丁斯酯(zinostatin stimalamer)。
552、本技术公开和权利要求的化合物还可以与以下任何治疗联合使用:
553、联合聚(adp-核糖)聚合酶(parp)抑制剂的治疗,所述抑制剂是一类针对靶向具有缺陷的dna损伤修复的癌症的化疗剂(yuan,et al.,expert opin ther pat,2017,27:363)。这种parp抑制剂包括但不限于奥拉帕尼(olaparib)、rupacarib、velaparib、尼拉帕尼(niraparib)、talazoparib、pamiparib、iniparib、e7449和a-966492。
554、联合导致dna单链和双链断裂修复的信号传导途径和机制如核因子-κb信号传导的抑制剂(pilie,et al.,nat rev clin oncol,2019,16:81;zhang,et al.,chin jcancer,2012,31:359)的治疗。这种抑制剂包括但不限于atm和atr激酶、检查点激酶1和2、dna依赖性蛋白激酶和wee1激酶的抑制剂(pilie,et al.,nat rev clin oncol,2019,16:81)。
555、联合免疫调节剂(khalil,et al.,nat rev clin oncol,2016,13:394)、癌症疫苗(hollingsworth,et al.,npj vaccines,2019,4:7)、免疫检查点抑制剂(例如pd-1、pd-l1、ctla-4抑制剂)(wei,et al.,cancer discov,2018,8:1069)、细胞周期蛋白-d-激酶4/6抑制剂(goel,et al.,trends cell biol,2018,28:911)、能结合肿瘤细胞和/或转移瘤并能诱导抗体依赖性细胞毒性(adcc)的抗体(kellner,et al.,transfus med hemother,2017,44:327)、t细胞或nk细胞结合剂(例如双特异性抗体)(yu,et al.,j cancer res clinoncol,2019,145:941)、使用扩增的自体或同种异体免疫细胞(例如嵌合抗原受体t(car-t)细胞)的细胞疗法(khalil,et al.,nat rev clin oncol,2016,13:394)的治疗。免疫检查点抑制剂包括但不限于纳武单抗(nivolumab)、伊匹单抗(ipilimumab)、派姆单抗(pembrolizumab)、阿特珠单抗(atezolizumab)、阿维鲁单抗(avelumab)、德瓦鲁单抗(durvalumab)和西米普利单抗(cemiplimab)。
556、根据本发明,所述化合物可以在其它抗癌化合物之前、同时或之后施用。施用时间表可以涉及以交替方式施用不同的药剂。在其它实施方案中,可以在用其它疗法治疗之前和期间、或期间和之后、或之前和之后递送所述化合物。在一些情况下,在施用其它抗增殖治疗之前超过24小时施用所述化合物。在其它实施方案中,可以向个体施用多于一种抗增殖疗法。例如,个体可以接受本发明化合物,组合手术和至少一种其它抗增殖化合物。或者,所述化合物可以与多于一种抗癌药物组合施用。
557、在一个实施方案中,本发明的化合物用于检测过表达fap的细胞和组织,由此通过将可检测标记、优选可检测放射性核素缀合于本发明化合物来实现此类检测。在优选的实施方案中,检测到的细胞和组织是患病细胞和组织和/或是疾病的原因和/或疾病的症状,或者是疾病基础病理的一部分。在进一步优选的实施方案中,患病细胞和组织引起肿瘤学指征(例如赘生物、肿瘤和癌症)或非肿瘤学指征(例如炎性疾病、心血管疾病、自身免疫性疾病和纤维化疾病)和/或是其一部分。
558、在另一个实施方案中,本发明的化合物用于治疗过表达fap的细胞和组织。在一个优选的实施方案中,所治疗的细胞和组织是患病细胞和组织和/或是疾病的原因和/或疾病症状,或者是疾病基础病理的一部分。在进一步优选的实施方案中,患病细胞和组织引起肿瘤学指征(例如赘生物、肿瘤和癌症)和/或是肿瘤学指征的一部分,并且治疗活性是通过将治疗活性效应物与本发明的化合物、优选治疗活性放射性核素缀合来实现。在进一步优选的实施方案中,患病细胞和组织引起非肿瘤学指征(例如,炎性疾病、心血管疾病、自身免疫性疾病和纤维化疾病)和/或是非肿瘤学指征的一部分,并且治疗活性通过抑制fap的酶促活性来实现。
559、在进一步的实施方案中,特别是如果所述疾病是非肿瘤疾病或非肿瘤学指征(例如炎性疾病、心血管疾病、自身免疫疾病和纤维化疾病),则以治疗有效量施用本发明的化合物;优选地,本发明的化合物不包含治疗活性核素。有效量是足以在施用该化合物的个体中提供治疗或医学上期望的结果或效果的化合物剂量。有效量将随所治疗的具体病症、所治疗个体的年龄和身体状况、病症的严重程度、治疗的持续时间、同时或联合治疗的性质(如果有的话)、具体的施用途径以及卫生从业者知识和专业知识范围内的类似因素而变化。例如,就针对治疗患有以异常细胞增殖为特征的病症的个体的方法而言,抑制增殖的有效量将是足以减少或完全停止异常细胞增殖、从而减缓或停止细胞团例如肿瘤的发生或进展的量。如实施方案中所使用的,“抑制”涵盖所有前述内容。
560、在其它实施方案中,治疗有效量将是在手术或药物治疗后延长微转移的休眠或稳定任何残余原发肿瘤细胞所需的量。
561、一般而言,当使用不含治疗活性放射性核素的未缀合化合物时,治疗有效量将随着个体的年龄、状况和性别以及个体疾病的性质和程度而变化,所有这些都可以由本领域普通技术人员之一确定。剂量可由医生或兽医调整,特别是在发生任何并发症的情况下。治疗有效量通常为但不限于0.1μg/kg至约2000mg/kg、或1.0μg/kg至约1000mg/kg、或约0.1mg/kg至约500mg/kg、或约1.0mg/kg至约100mg/kg的范围,每日一剂或多剂施用,持续一天或多天。如果需要,活性化合物的有效日剂量可以分为两个、三个、四个、五个、六个或更多个亚剂量的形式施用,例如全天以适当的间隔分开施用,任选以单位剂型施用。在一些实施方案中,施用所述化合物超过7天、超过10天、超过14天和超过20天。在其它实施方案中,所述化合物在数周或数月的时间内施用。在其它实施方案中,所述化合物隔日递送。例如,每两天、或每三天、或每四天、或每五天、或每六天、或每周、或每月递送药剂。
562、在一个优选的实施方案中,本发明的化合物用于治疗和/或预防疾病,其中这种治疗是放射性核素疗法。
563、优选地,放射性核素治疗利用或基于由放射性核素发射的不同形式的辐射。这种辐射可以例如是光子辐射、电子辐射(包括但不限于β-粒子和auger电子)、质子辐射、中子辐射、正电子辐射、α-粒子或离子束辐射。根据所述放射性核素发射的粒子或辐射的种类,放射性核素治疗可以例如区分为光子放射性核素治疗、电子放射性核素治疗、质子放射性核素治疗、中子放射性核素治疗、正电子放射性核素治疗、α-粒子放射性核素治疗或离子束放射性核素治疗。所有这些形式的放射性核素治疗都包括在本发明中,并且所有这些形式的放射性核素治疗都可以通过本发明的化合物来实现,优选条件是放射性核素连接于本发明的化合物上,更优选作为效应物提供这种辐射。
564、放射性核素疗法优选通过破坏细胞的dna来起作用。这种损伤是由光子、电子、质子、中子、正电子、α粒子或离子束直接或间接电离构成dna链的原子引起的。间接电离是水电离的结果,形成自由基,特别是羟基自由基,然后破坏dna。
565、在最常见的放射性核素治疗形式中,大部分辐射效应是通过自由基产生的。由于细胞具有修复dna损伤的机制,因此断裂双链dna被证明是改变细胞特性的最重要技术。由于癌细胞通常是未分化的并且类似于干细胞,因此与大多数健康的分化细胞相比,癌细胞繁殖更多,并且修复亚致死损伤的能力减弱。所述dna损伤是通过细胞分裂遗传的,对癌细胞的损伤不断累积,导致其死亡或繁殖速度减慢。
566、氧是一种有效的放射增敏剂,通过形成损伤dna的自由基来提高给定剂量辐射的效力。因此,可以使用高压氧气瓶,携带增氧的血液代用品,诸如米索硝唑(misonidazole)和甲硝唑(metronidazole)的缺氧细胞放射增敏剂,以及诸如替拉扎明(tirapazamine)的缺氧细胞毒素。
567、选择放射性剂量时要考虑的其它因素包括患者是否正在接受化疗、是否在手术前或手术后进行放射治疗、以及手术的成功程度。
568、出于几个重要原因,总放射性剂量可以被分成几部分,即随着时间的推移分散在一次或多次治疗中。分成几部分可以使正常细胞有时间恢复,而肿瘤细胞在分部之间的修复效率通常较低。分成几部分还允许在一次治疗期间处于细胞周期的相对放射抗性阶段的肿瘤细胞在给予下一次分部之前循环进入周期的敏感阶段。类似地,长期或急性缺氧且因此具有更强抗辐射能力的肿瘤细胞可能会在各分部分之间重新充氧,从而提高对肿瘤细胞的杀伤力。
569、众所周知,不同的癌症对放射治疗的反应不同。癌症对辐射的反应通过其辐射敏感性来描述。对辐射高度敏感的癌细胞会被适度剂量的辐射迅速杀死。这些包括白血病、大多数淋巴瘤和生殖细胞肿瘤。
570、区分具体肿瘤的放射敏感性(在某种程度上是实验室测量)与实际临床实践中通过内部递送的放射性剂量对癌症的“治愈性”是很重要的。例如,白血病通常无法通过放射疗法治愈,因为其是全是传播的。如果淋巴瘤局限于身体的某一部位,那么它可能是可以根治的。同样,许多常见的、中等放射反应性的肿瘤如果处于早期阶段,可以用治疗剂量的放射性治疗。例如,这适用于非黑色素瘤皮肤癌、头颈癌、非小细胞肺癌、宫颈癌、肛门癌、前列腺癌。
571、肿瘤对放射治疗的反应也与其大小有关。由于复杂的原因,非常大的肿瘤对放射的反应不如较小的肿瘤或微观疾病。人们使用各种策略来克服这种影响。最常见的技术是放射治疗前的手术切除。这种情况最常见于采用广泛局部切除或乳房切除术随后进行辅助放疗的乳腺癌治疗中。另一种方法是在根治性放射性核素治疗之前通过新辅助化疗缩小肿瘤。第三种技术是通过在放射治疗过程中给予某些药物来增强癌症的放射敏感性。放射增敏药物的实例包括但不限于顺铂、尼莫唑(nimorazole)和西妥昔单抗(cetuximab)。
572、术中放疗是一种特殊类型的放疗,其是在手术切除癌症后立即进行。这种方法已应用于乳腺癌(靶向术中放射治疗)、脑肿瘤和直肠癌。
573、放射性核素治疗本身是无痛的。许多低剂量姑息治疗的副作用很小或没有副作用。较高剂量的治疗可能会在治疗期间(急性副作用)、治疗后数月或数年内(长期副作用)或重新治疗后(累积副作用)引起不同的副作用。副作用的性质、严重程度和持续时间取决于接受放射的器官、治疗本身(放射性核素的类型、剂量、分级、同步化疗)和患者。
574、在本发明的范围内,本发明的用于治疗疾病的方法可以实现本领域已知的上述策略中的每一个和任何策略,并且其构成本发明的进一步的实施方案。
575、本发明的化合物用于诊断本文公开的疾病的方法中也在本发明的范围内。此类方法优选包括向有需要的个体施用诊断有效量的本发明化合物的步骤。
576、根据本发明,成像方法选自闪烁成像、单光子发射计算机断层显像(spect)和正电子发射断层显像(pet)。
577、在本发明的优选实施方案中,包含来自n4螯合剂家族的螯合剂、更优选螯合tc放射性核素的根据本发明的化合物特别适合用于使用spect的方法和程序中。在其一个实施方案中,来自n4螯合剂家族的螯合剂是n4ac。
578、在本发明的优选实施方案中,包含螯合剂nodaga、更优选螯合ga放射性核素的根据本发明的化合物特别适合用于使用pet的方法和程序中。
579、闪烁成像是核医学中使用的诊断测试或方法的一种形式,其中放射性药物被细胞、组织和/或器官内化,优选在体内内化,并且由所述内化的放射性药物发射的辐射被外部检测仪(γ相机)捕获以形成并显示二维图像。与此相反,spect和pet形成并显示三维图像。因此,spect和pet被归类为与闪烁成像不同的技术,尽管它们也使用γ相机来检测内部辐射。闪烁成像不同于外部辐射穿过身体形成图像的诊断性x射线扫描。
580、单光子发射断层显像(spect)是一种使用γ射线的核成像技术。它们与使用γ相机的常规核医学平面成像非常相似。在spect扫描之前,患者会被注射放射性标记的发射γ射线的化学物质,扫描仪可以检测到这种射线。计算机从γ相机收集信息并将其转换为二维横截面。这些横截面可以重新加在一起以形成器官或组织的三维图像。spect涉及检测由放射性标记化学物质提供的放射性核素单独和连续发射的γ射线。为了获取spect图像,使γ相机围绕患者旋转。在旋转期间的定义点获取投影,通常每3至6度获取一次。在大多数情况下,使用完整的360度旋转来获得最佳重建。获得每个投影所需的时间也各不相同,但通常为15至20秒。总扫描时间为15至20分钟。多头γ相机速度更快。由于spect采集与平面γ相机成像非常相似,因此可以使用相同的放射性药物。
581、正电子发射断层显像(pet)是一种非侵入性诊断成像技术,用于测量人体内细胞的生化状态或代谢活动。pet的独特之处在于它可以生成人体基本生物化学或功能的图像。x射线、ct扫描或mri等传统诊断技术可生成身体解剖或结构的图像。这些技术的前提是可以看到与疾病相关的任何结构或解剖学变化。生化过程也会因疾病而改变,并且可能发生在解剖学发生任何重大变化之前。pet是一种成像技术,可以可视化其中一些早期生化变化。pet扫描仪依靠患者发出的辐射来创建图像。每位患者都会服用微量的放射性药物,这种药物要么与人体使用的天然物质非常相似,要么与受体或分子结构特异性结合。随着放射性同位素经历正电子发射衰变(也称为正β衰变)时,会发射正电子,即电子的反粒子对应物。在行进几毫米后,正电子遇到电子并湮灭,产生一对沿相反方向移动的湮灭(γ)光子。当它们到达扫描装置中的闪烁材料时,会被检测到,产生一束光,并被光电倍增管或硅雪崩光电二极管检测到。该技术依赖于对光子对的同时或同步检测。不成对到达(即在几纳秒内到达)的光子将被忽略。所有重合都被转发到图像处理单元,在此使用图像重建程序生成最终图像数据。
582、spect/ct和pet/ct是spect和pet与计算机断层显像(ct)的组合。组合这些方式的关键益处是提高读者的信心和准确性。对于传统的pet和spect,从异常区域发射的光子数量有限,产生的背景水平非常低,因此很难在解剖学上定位该区域。添加ct有助于从解剖学角度确定异常区域的位置,并对这代表疾病的可能性进行分类。
583、在本发明的范围内,本发明的诊断疾病的方法可以实现本领域已知的上述策略中的每一个和任何策略,并且其构成本发明的进一步的实施方案。
584、本发明的化合物可用于对患者进行分层,即在患者群体内创建子集,提供关于患者将如何响应给定药物的更详细信息。通过鉴定最有可能对新疗法产生反应的患者群子集,分层可以是将临床试验从阴性或中性结果转变为阳性结果的关键组成部分。
585、分层包括识别一组具有共同“生物学”特征的患者,为患者选择最佳治疗方案,并在风险评估、风险预防和实现最佳治疗结果方面实现最佳可能结果。
586、本发明的化合物可用于尽早评估或检测特定疾病(这是诊断性用途)、发生疾病的风险(这是易感性/风险性用途)、疾病的演变包括惰性与侵袭性(这是预后用途),并且可以用于预测对给定治疗的反应和毒性(这是预测用途)。
587、本发明的化合物用于治疗诊断方法中也在本发明的范围内。治疗诊断学的概念是将治疗剂与相应的诊断测试相结合,可增加治疗药物的临床应用。治疗诊断学的概念变得越来越有吸引力,并被广泛认为是通过帮助医生识别可能从特定治疗中受益的患者来提高药物治疗效率的关键,从而避免不必要的治疗。
588、治疗诊断学的概念是将治疗剂与诊断测试相结合,使医生能够识别那些将从给定的治疗中受益最多的患者。在一个实施方案中并且如本文优选使用的,本发明的化合物用于患者的诊断,即原发性肿瘤团块以及潜在的局部和远处转移的鉴定和定位。此外,可以确定肿瘤体积,特别是利用三维诊断方式,例如spect或pet。仅选择那些具有fap阳性肿瘤团块并因此可能受益于给定治疗的患者进行特定治疗,从而避免不必要的治疗。优选地,此类疗法是使用本发明的化合物的fap靶向疗法。在一种特定实施方案中,应用化学上相同的肿瘤靶向诊断,优选地用于闪烁成像的成像诊断、pet或spect以及放射治疗。此类化合物仅在放射性核素上有所不同,因此通常具有非常相似(即使不相同)的药代动力学特征。这可以使用螯合剂和诊断或治疗放射性金属来实现。或者,这可以使用用于放射性标记的前体和用诊断或治疗放射性核素进行放射性标记来实现。在一种实施方案中,优选通过本领域技术人员已知的诊断性放射性核素的辐射量化和随后的剂量测定以及与易受副作用影响的器官相比在肿瘤中药物浓度的预测来使用诊断性成像。因此,实现了对患者真正个体化的药物剂量治疗。
589、在一个实施方案中并且如本文优选使用的,所述治疗诊断方法仅用一种治疗诊断活性化合物来实现,例如用发射诊断可检测的辐射(例如正电子或伽马射线)以及治疗有效辐射(例如电子或α粒子)的放射性核素标记的本发明化合物。
590、本发明还考虑了一种在术中鉴定/公开个体中表达fap的患病组织的方法。此类方法使用本发明的化合物,其中此类本发明化合物优选包含诊断活性剂作为效应物。
591、根据本发明的另一个实施方案,本发明的化合物、特别是如果与放射性核素络合,可以用作任何其它肿瘤治疗的辅助剂或佐剂,所述其它肿瘤治疗包括作为大多数孤立的实体癌的主要治疗方法的手术、涉及使用电离辐射以试图治愈或改善癌症症状的放射治疗,使用近距离放射治疗形式的密封内部源或外部源、化疗例如烷化剂、抗代谢物、蒽环类药物、植物生物碱、拓扑异构酶抑制剂,以及其它抗肿瘤药物、调节肿瘤细胞行为而不直接攻击这些细胞的激素治疗、直接靶向某些类型癌症的分子异常的靶向药物,包括单克隆抗体和酪氨酸激酶抑制剂、血管生成抑制剂、免疫疗法、癌症疫苗接种、姑息治疗(包括行动)以减少身体、情感、精神和社会心理困扰,改善患者的生活质量,以及替代治疗,包括不属于常规医学的多样化的医疗保健系统、实践和产品。
592、在本发明方法的一个实施方案中,所述个体是患者。在一个实施方案中,患者是已被诊断为患有或疑似患有疾病或处于患有或发生疾病风险中的个体,其中所述疾病是如本文所述的疾病,并且优选是涉及fap的疾病。
593、在实施其中使用放射性核素并且更特别地连接到本发明化合物或其一部分的治疗和诊断方法时分别使用的剂量,将根据例如待治疗的特定病症而变化,例如肿瘤类型的已知放射敏感性、肿瘤的体积和所需的治疗。一般来说,所述剂量是基于每个器官的放射性分布和观察到的靶标吸收来计算的。可以一次或多次施用γ发射复合物以进行诊断成像。在动物中,指定的剂量范围可以是0.1μg/kg至5mg/kg的与例如1-200mbq的111in或89zr络合的本发明化合物。本发明化合物的β-发射络合物可以在几个时间点施用,例如持续1至3周或更长时间。在动物中,指定的剂量范围可以是0.1μg/kg至5mg/kg的与例如1-200mbq 90y或177lu络合的本发明化合物。在较大的哺乳动物例如人中,指定的剂量范围是0.1-100μg/kg的与例如10-400mbq 111in或89zr络合的本发明化合物。在较大的哺乳动物例如人中,指定的剂量范围是0.1-100μg/kg的与例如10-5000mbq 90y或177lu络合的本发明化合物。
594、另一方面,本发明涉及包含本发明化合物的组合物,特别是药物组合物。
595、本发明的药物组合物包含至少一种本发明的化合物和任选一种或多种的载体物质、赋形剂和/或佐剂。所述药物组合物可另外包含例如水、缓冲剂如中性缓冲盐水或磷酸盐缓冲盐水、乙醇、矿物油、植物油、二甲亚砜、碳水化合物如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇、蛋白质、佐剂、多肽或氨基酸如甘氨酸、抗氧化剂、螯合剂如edta或谷胱甘肽和/或防腐剂中的一种或多种制剂。此外,一种或多种其它活性成分可以但非必需包含在本发明的药物组合物中。
596、本发明的药物组合物可以配制用于任何合适的施用途径,包括例如局部施用,例如透皮或经眼、口服、含服、鼻、阴道、直肠或肠胃外施用。本文使用的术语胃肠外包括皮下、皮内、血管内例如静脉内、肌内、鞘内和腹膜内注射,以及任何类似的注射或输注技术。优选的施用途径是静脉内施用。
597、在本发明的一个实施方案中,包含放射性核素的本发明化合物通过任何常规途径施用,特别是静脉内施用,例如以注射溶液或悬浮液的形式静脉内施用。本发明的化合物还可以有利地通过输注施用,例如通过输注30至60分钟。
598、根据肿瘤的部位,本发明的化合物可以在尽可能靠近肿瘤部位的位置施用,例如通过导管施用。这种施用可以直接施用于肿瘤组织或周围组织或进入血管中。本发明的化合物还可以按剂量、优选以分开的剂量重复施用。
599、根据本发明的优选实施方案,本发明的药物组合物包含稳定剂,例如自由基清除剂,其抑制本发明化合物的自放射分解。合适的稳定剂包括例如血清白蛋白、抗坏血酸、视黄醇、龙胆酸或其衍生物,或氨基酸输注溶液,例如用于肠胃外蛋白质喂养,优选不含电解质和葡萄糖,例如可商购的氨基酸输注液,如ke nephro。优选抗坏血酸和龙胆酸。
600、本发明的药物组合物可以包含另外的添加剂,例如将ph值调节到7.2至7.4之间的制剂,例如乙酸钠或乙酸铵或na2hpo4。优选地,将稳定剂进入到本发明的非放射性化合物中,并且在稳定剂的存在下在室温下或优选在40至120℃的温度下进行放射性核素的引入,例如与放射性核素的络合。所述络合可以方便地在无空气条件下进行,例如在在n2或ar下进行。络合后可向所述组合物中进入另外的稳定剂。
601、本发明化合物的排泄,特别是当效应物是放射性核素时,基本上通过肾脏进行。进一步保护肾脏免受放射性蓄积可以通过施用赖氨酸或精氨酸或具有高含量赖氨酸和/或精氨酸的氨基酸溶液来实现,例如可商购的氨基酸溶液例如-14或-10,在注射本发明的化合物之前或与本发明的化合物一起施用,特别是如果效应物是放射性核素的话。还可以通过施用血浆扩张剂例如佳乐施(gelofusine)来实现对肾脏的保护,代替或补充氨基酸输注。还可以通过施用利尿剂来保护肾脏,利尿剂提供强制利尿的手段,从而提高排尿率。此类利尿剂包括高效髓袢利尿剂、噻嗪类、碳酸酐酶抑制剂、保钾利尿剂、保钙利尿剂、渗透性利尿剂和低效能利尿剂。除了本发明的化合物之外,本发明的药物组合物还可以包含至少一种这些另外的化合物,其旨在或适合于肾脏保护,优选对施用了本发明的化合物的个体的肾脏保护。
602、本领域技术人员应当理解,本文公开的本发明的化合物用于各种方法中。本领域技术人员还应当理解,本发明的组合物和本发明的药物组合物可以同等地用于所述各种方法中。本领域技术人员还应当理解,本文公开的本发明的组合物和药物组合物用于各种方法中。本领域技术人员同样应当理解,本发明的化合物可以同等地用于所述各种方法中。
603、本领域技术人员将认识到,本发明的组合物和本发明的药物组合物除了本发明的化合物之外还含有一种或多种其它化合物。就本文公开的这种一种或多种另外的化合物作为本发明的组合物和/或本发明的药物组合物的一部分而言,应当理解这种一种或多种另外的化合物可以与本发明的化合物分开施用给暴露于本发明方法的个体或本发明方法的个体。所述一种或多种另外的化合物的这种施用可以在施用本发明的化合物之前、同时或之后进行。本领域技术人员还应当认识到,在本发明的方法中,除了本发明的化合物之外,还可以为个体施用一种或多种另外的化合物。所述一种或多种另外的化合物的这种施用可以在施用本发明的化合物之前、同时或之后进行。就本文公开的这种一种或多种另外的化合物作为本发明方法的一部分施用而言,应当理解这种一种或多种另外的化合物是本发明的组合物和/或药物组合物的一部分。本发明的化合物和一种或多种另外的化合物可以包含在相同或不同的制剂中,这也在本发明的范围内。本发明的化合物和一种或多种另外的化合物不包含在同一制剂中,而是包含在含有包含本发明化合物的第一制剂和包含一种或多种另外的化合物的第二制剂的同一包装中,其中制剂的类型可以相同或可以不同。
604、在本发明的范围内,本发明的组合物和/或本发明的药物组合物中包含多于一种类型的本发明的化合物。在本发明的方法中使用、优选施用多于一种类型的本发明化合物也在本发明的范围内。
605、应当意识到,本发明的组合物和本发明的药物组合物可以以常规方式制备。
606、由于放射性衰变,放射性药物的放射性含量随着时间推移而减少。对于放射性药物诊断而言,放射性核素的物理半衰期通常很短。在这些情况下,最终的制备必须在施用于患者之前不久完成。用于断层显像的正电子发射放射性药物(pet放射性药物)尤其如此。这通常导致使用半成品,例如放射性核素发生器、放射性前体和药剂盒。
607、优选地,本发明的药剂盒除了包含一种或多于一种本发明的化合物之外,通常还包含以下至少一项:使用说明,最终制备和/或质量控制,一种或多种任选的赋形剂,一种或多种用于标记程序的可选试剂,任选具有或不具有屏蔽容器的一种或多种放射性核素,以及任选一种或多种装置,其中所述装置选自包括标记装置、纯化装置、分析装置、处理装置、辐射防护装置或施用装置等。
608、用于一般处理和运输放射性药物容器的被称为“pigs”的屏蔽容器具有多种用于保持放射性药物容器的构造,例如瓶子、小瓶、注射器等。一种形式通常包括允许接近持有的放射性药物容器的可移除盖。当容器盖就位时,辐射暴露是可以接受的。
609、标记装置选自开放反应器、封闭反应器、微流体系统、纳米反应器、小柱、压力容器、小瓶、温度可控反应器、混合或摇动反应器及其组合。
610、纯化装置优选选自离子交换色谱柱或装置、尺寸排阻色谱柱或装置、亲和色谱柱或装置、气相或液相色谱柱或装置、固相萃取柱或装置、过滤装置、离心瓶柱或装置。
611、分析装置优选选自测试装置,以确定所述放射性标记的化合物的身份、放射化学纯度、放射性核素纯度、放射性含量和比放射性。
612、处理装置优选选自由用于混合、稀释、分配、标记、注射和施用放射性药物于个体的装置。
613、使用辐射防护装置是为了保护医生和其它人员在使用治疗或诊断放射性核素时免受辐射。辐射防护装置优选选自具有辐射吸收材料的防护屏障的装置,所述辐射吸收材料选自铝、塑料、木材、铅、铁、铅玻璃、水、橡胶、塑料、布,确保与辐射源保持适当距离的装置,减少放射性核素暴露时间的装置,限制放射性物质被吸入、摄入或以其它方式进入体内的装置以及提供这些措施组合的装置。
614、施用装置优选选自注射器、屏蔽注射器、针头、泵和输注装置。注射器护罩通常是中空的圆柱形结构,其容纳注射器的圆柱形主体,并由铅或钨制成,具有铅玻璃窗,允许操作者观察注射器柱塞和注射器内的液体体积。
615、现在参考以下附图和实施例进一步示例说明本发明,从这些附图和实施例中可以得到进一步的特征、实施方案和优点,其中:
616、图1显示人成纤维细胞活化蛋白(fap)(seq id no:1)、人二肽基肽酶4(ddp4)(seqid no:2)和人脯氨酰内肽酶(prep)(seq id no:3)的氨基酸序列。
617、包括以下实施例以为本领域普通技术人员提供实践本公开主题的代表性实施方案的指导。根据本公开和本领域技术人员的一般水平,本领域技术人员可以理解以下实施例仅是示例性的,并且可以在不脱离本发明的范围的情况下对目前公开的主题进行多种改变、修改和变更。下面的合成描述和具体实施例仅用于示例说明的目的,并且不应被解释为以任何方式限制通过其它方法制备本公开的化合物。
618、实施例
619、本技术中以及具体的以下实施例使用的缩写如下:
620、
621、
622、
623、
624、实施例1:材料和方法
625、通过以下实施例进一步示例说明材料和方法以及一般方法。
626、溶剂:
627、溶剂按指定质量使用,无需进一步纯化。乙腈(超级,hplc,vwr-用于分析目的;prepsolv,merck-用于制备目的);二氯甲烷(合成级,roth);乙酸乙酯(合成级,roth);n,n-二甲基甲酰胺(肽合成级,biosolve);1-甲基-2-吡咯烷酮(肽级,iris biotech),1,4-二烷(特纯级,roth);甲醇(p.a.,merck)。
628、水:milli-q plus,millipore,脱矿物质。
629、化学品:
630、化学品根据或类似于文献程序合成或购自sigma-aldrich-merck(deisenhofen,germany)、bachem(bubendorf,switzerland)、vwr(darmstadt,germany)、novabiochem(merck group,darmstadt,germany)、acros organics(分销公司fisher scientificgmbh,schwerte,germany)、iris biotech(marktredwitz,germany)、amatek chemical(jiangsu,china)、roth(karlsruhe,deutschland)、molecular devices(chicago,usa)、biochrom(berlin,germany)、peptech(cambridge,ma,usa)、synthetech(albany,or,usa)、pharmacore(high point,nc,usa)、pcas biomatrix inc(saint-jean-sur-richelieu,quebec,canada)、alfa aesar(karlsruhe,germany)、tianjin nankai hecheng s&t co.、ltd(tianjin,china)、chematech(dijon,france)和anaspec(san jose,ca,usa)或其它公司,并按指定质量使用,无需进一步纯化。
631、boc4n4ac-oh根据文献程序合成(maecke et al.chem.eur.j.,2010,16,7,2115)。
632、
633、细胞:
634、ht29(ecacc目录号91072201)和wi-38(ecacc目录号90020107)购自ecacc,表达人fap的hek293细胞(q12884)由inscreenex gmbh(braunschweig,germany)使用重组酶介导的盒式交换(rmce)生产。nehlsen等人描述了rmce程序(nehlsen,et al.,bmc biotechnol,2009,9:100)。
635、hplc/ms分析
636、通过注射5μl样品溶液进行hplc/ms分析,对所有色谱图使用2步梯度(12分钟内5-65%的b,随后0.5分钟内65-90%,a:在水中0.1% tfa,b:在acn中0.1% tfa)。rp柱来自agilent(poroshell120型,2.7μm,ec-c18,50×3.00mm,流量0.8ml,室温hplc);质谱仪:agilent 6230lc/tof-ms,esi电离。masshunter qualitative analysis b.07.00sp2用作软件。在λ=230nm进行uv检测。保留时间(rt)以十进制表示(例如1.9分钟=1分钟54秒),指的是在uv光谱仪中的检测。为了评估观察到的化合物质量,使用了“通过分子式查找化合物(find compounds by formula)”功能。特别是,使用单个“化合物的中性质量(以道尔顿为单位)(neutral mass of a compound(in units of daltons))”值和相应的同位素分布模式来确认化合物的身份。质谱仪的准确度约为±5ppm。
637、制备型hplc:
638、使用反相色谱柱(来自phenomenex的kinetex 5μxb-c18 150×30mm或rlrp-s8μ,150×25mm)作为固定相进行制备型hplc分离。使用在水中0.1% tfa(a)和在acn中0.1% tfa(b)作为流动相,将其以线性二元梯度混合。梯度描述为:“30分钟内10至40%的b”,这意味着在30分钟内运行从10% b(相应的90%a)到40% b(相应的60% a)的线性梯度。流速在30-50ml/min的范围内。用于纯化本发明化合物的典型梯度从5-25% b开始,30分钟后在35-50% b结束,并且结束时和开始时的b百分比之间的差异为至少10%。常用的梯度是“30分钟内15%至40% b”。
639、自动/半自动固相合成的一般程序:
640、在tetras肽合成仪(advanced chemtech)上以50μmol和100μmol规模进行肽和聚酰胺的自动固相分析。手动步骤在配备玻璃料的塑料注射器中进行(材料pe,rolandvetter laborbedarf ohg,ammerbuch,germany)。除非另有说明,所述方案中的试剂量对应于100μmol规模。
641、固相合成是在聚苯乙烯(与1,4-二乙烯基苯(ps)或二(乙二醇)二甲基丙烯酸酯(deg)交联)、chemmatrix(cm)或tentagel(tg)树脂上进行。树脂接头是三苯甲基、wang和rink酰胺。
642、树脂加载:
643、在三苯甲基接头的情况下,如下进行第一构件的连接(树脂加载)。将树脂(聚苯乙烯(ps)三苯甲基氯,初始加载:1.8mmol/g)在dcm(5ml)中溶胀30分钟,随后用dcm(3ml,1分钟)洗涤。然后将树脂用相应构件(0.5mmol,5eq.)和dipea(350μl,3.5mmol,35eq.)在dcm(4ml)中的混合物处理1小时。然后将树脂用甲醇(5ml,5分钟)和dmf(3ml,2×1分钟)洗涤。
644、在wang接头的情况下,使用预加载的树脂(聚苯乙烯(ps)和tentagel(tg))。
645、在rink酰胺接头的情况下,第一残基与树脂(cm,deg)的连接采用与链组装相同的程序进行,如下所述。
646、alloc/allyl-脱保护:
647、在dmf中溶胀后,树脂用dmf和dcm洗涤。通过使氮气流穿过搅拌的溶剂来使dcm脱氧。用无氧溶剂洗涤树脂三次。然后将在无氧dcm中2ml 2m巴比妥酸溶液和在无氧dcm中1ml25μm四(三苯基膦)钯(0)溶液添加到树脂中。将树脂搅拌1小时,然后用dcm、meoh、dmf、在dmf中5% dipea、在dmf中5%二硫代氨基甲酸盐、dmf和dcm洗涤(每个洗涤步骤重复3次,每次用3ml洗涤1分钟)。
648、fmoc-脱保护:
649、在dmf中溶胀后,树脂用dmf洗涤,然后用哌啶/dmf(1:4,3ml,2和20分钟)处理,随后用dmf(3ml,5×1分钟)洗涤。
650、dde-脱保护:
651、在dmf中溶胀后,树脂用dmf洗涤,然后用水合肼/dmf(2/98,3ml 2×10分钟)处理,随后用dmf(3ml,5×1分钟)洗涤。
652、mtt-脱保护:
653、在dcm中溶胀后,树脂用dcm洗涤,然后用hfip/dcm(7/3,4-6ml,4小时)处理,随后用dcm(3ml,3×1分钟)、dmf(3ml,3×1ml)和dipea(在dmf中0.9m,3ml,1分钟)洗涤。
654、试剂溶液:
655、构件(在dmf或nmp中0.3m),dipea(在dmf中0.9m),hatu(在dmf中0.4m),乙酸酐(在dmf中0.75m)
656、偶联:构件/氨基酸的偶联(链组装):
657、除非另有说明,否则构件结构单元的偶联如下进行:随后添加相应构件的溶液(1.7ml,5eq.)、dipea溶液(1.15ml,10eq.)和hatu溶液(1.25ml,5eq.)后,将树脂摇动45分钟。如果需要,用dmf(3ml,1分钟)洗涤树脂并重复偶联步骤。
658、末端乙酰化:
659、添加dipea溶液(1.75ml,16eq.)和乙酸酐溶液(1.75ml,13eq.)后,将树脂摇动10分钟。然后用dmf(3ml,6×1分钟)洗涤树脂。
660、裂解方法a:从高酸不稳定树脂中裂解受保护的片段
661、序列组装完成后,树脂最后用dcm(3ml,4×1分钟)洗涤,然后真空干燥。然后用hfip/dcm(7/1,4ml,4小时)处理树脂并将收集的溶液蒸发至干燥。将残余物用制备型hplc纯化或不经进一步纯化而使用。
662、裂解方法b:未保护片段的裂解(完全树脂裂解)
663、序列组装完成后,树脂最后用dcm(3ml,4×1分钟)洗涤,真空干燥过夜并用tfa、edt、水和tips(94/2.5/2.5/1)处理2小时(除非另有说明)。然后将裂解溶液倒入mtbe和环己烷的冷冻混合物中(1/1,与裂解溶液体积相比过量10倍),在4℃下离心5分钟,收集沉淀并在真空中干燥。在纯化或进一步改性之前,将残余物从水/乙腈中冻干。
664、裂解方法c:溶液中肽保护基团的裂解
665、将受保护/部分受保护的化合物溶解在tfa、水和tips(95/2.5/2.5)中2小时(除非另有说明)。然后将裂解溶液倒入mtbe和环己烷的冷冻混合物中(1/1,与裂解溶液体积相比过量10倍),在4℃下离心5分钟,收集沉淀并在真空中干燥。在纯化或进一步改性之前,将残余物从水/乙腈中冻干。
666、更多相关的fmoc固相肽合成方法在“fmoc solid phase peptide synthesis”editors w.chan,p.white,oxford university press,usa,2000中详细描述。化合物名称适当地使用mestrenova version 12mnova iupac name plugin(mestrelab research,s.l.)或autonom version 2.2(beilstein informationssysteme 1988-1998,beilstein institut für literatur der organischen chemie licensed to beilsteinchemiedaten and software gmbh命名。
667、化合物的制备:
668、制备本发明化合物的具体实施方案通过使用上文公开的一般方法和公开的方法或本领域技术人员已知的其它方法来制备。除非另有说明,否则所有起始材料和试剂均为标准商业级,并且无需进一步纯化即可使用,或者通过常规方法由这种材料容易地制备。有机合成领域的技术人员根据本公开内容将认识到起始材料和反应条件可以变化,包括用于生产本发明所涵盖的化合物的附加步骤。用于形成不同环状结构的一般方法在下面的单独部分中公开。
669、本发明化合物的一种通用合成路线包括:
670、1.具有两个硫醇部分的线性肽前体的固相肽合成法(spps)。
671、2.该线性肽前体通过使用以下方式的硫醇位点特异性环化:
672、a.二溴或双(苯硫基)-马来酰亚胺衍生物,或
673、b.通过二硫化物直接氧化环化。
674、环化方法方案2a):用马来酰亚胺衍生物环化
675、将粗制肽材料溶解在磷酸盐缓冲液(0.1m,ph=6)和乙腈的1:1混合物中。向所得混合物中加入相应的3,4二溴马来酰亚胺在乙腈中的溶液。当通过lc-ms判断环化反应完成时,加入tfa并将反应溶液进行冷冻干燥。所述反应中使用的溶剂体积、3,4-二溴马来酰亚胺的量和tfa的体积取决于用于合成线性肽前体的树脂的量-每50μmol初始使用的树脂使用60ml的溶剂混合物、14.0mg(55μmol)的3,4-二溴马来酰亚胺和50μl tfa。
676、环化方法方案2b):二硫化物环化
677、将粗制肽材料溶解在乙腈和乙酸铵缓冲液(0.1m,ph 6)的1:1混合物中。向溶液中加入[pt(en)2cl2]cl2(二氯双-(乙二胺)-氯化铂(iv))。通过分析lc-ms判断环化反应完成后,加入tfa并将反应溶液冷冻干燥。反应中使用的溶剂体积、pt试剂量和tfa体积取决于用于合成线性肽前体的树脂量-每50μmol初始使用的树脂使用60ml溶剂混合物、22.8mg(50μmol)pt试剂和50μl tfa。
678、在用马来酰亚胺衍生物环化的情况下,充分理解并证明所选择的优选马来酰亚胺衍生物可能包含螯合剂或z-基团。配备有螯合剂的马来酰亚胺试剂的合成可以通过标准合成方法来进行,如下文的一个实施例所证明的。这些3,4-二溴马来酰亚胺试剂可直接用于环化方法2a)。
679、a)n-(dota-2-氨基乙基)-3,4-二溴马来酰亚胺
680、
681、按照标准固相合成程序,将三苯甲基氯树脂加载乙二胺。将dota(tbu)3-oh溶解在dmf中,并加入dipea和hatu。将这个溶液搅拌5分钟并加入加载的树脂中,将其搅拌16小时。反应中使用的dmf和dipea的体积以及dota(tbu)3-oh和hatu的量取决于所用树脂的量-每0.9mmol初始使用的树脂使用5ml dmf、470μl(2.7mmol)的dipea、773mg(1.35mmol)的dota(tbu)3-oh和513mg(1.35mmol)的hatu。使用每0.9mmol树脂15ml的二氯甲烷(94%)、tfa(5%)和三异丙基硅烷(1%)混合物从树脂上裂解30分钟。用碳酸铵溶液(1m)中和所得溶液。减压蒸发dcm并将残余物冻干。将残余物溶于水中并用乙酸乙酯萃取,用盐水洗涤,用硫酸镁干燥并蒸发。根据文献程序(et al.,tetrahedron lett.,2013,54:3493)使粗制产物与3,4-二溴-n-甲氧基羰基马来酰亚胺反应,得到其三叔丁基酯形式的标题化合物。在tfa、二氯甲烷和三异丙基硅烷的15:4:1混合物中进行叔丁基保护基的去除。根据分析lc-ms判断完成后,减压蒸发溶剂。hrms(esi):针对c22h32br2n6o9,m/z[m+h]+计算值为685.0685,实测值为685.0958。lc-ms(梯度:5分钟内5-65乙腈/水):rt=2.0分钟。
682、与3,4-二硫酚马来酰亚胺类似,根据文献程序制备相应的二硫酚马来酰亚胺衍生物(etal.,tetrahedron lett.,2013,54:3493)。
683、以与合成方法a类似的方式,可以用螯合剂和活化的马来酰亚胺部分选择性地装饰几种其它二胺。
684、本领域技术人员将容易理解,一些螯合剂在一些情况下可以有利地在与这些类型的试剂的环化反应期间完全或部分受保护地使用,并且随后所述保护基在相应环化产物的最终纯化之前被裂解。
685、本发明的化合物可以通过不同的策略来制备,例如使用这些通用方法。相应实施例的相关合成方法列于表8的列中。相关方法简述如下:
686、方法a(无螯合剂或n末端螯合剂-二硫化物,c末端酰胺)
687、·在rink酰胺树脂上进行固相肽合成,
688、·将裂解后的粗制材料根据方法2b)环化。
689、方法b(无螯合剂或n末端螯合剂-环化的马来酰亚胺,c末端酰胺)
690、·在rink酰胺树脂上进行固相肽合成,
691、·将裂解后的粗制材料根据方法2a)环化。
692、方法c(螯合剂与氨基酸侧链中的氨基结合-二硫化物,c末端酰胺)
693、·利用一个侧链带有alloc保护基的氨基酸在rink酰胺树脂上进行固相肽合成,
694、·序列组装完成后:进行alloc脱保护和螯合剂偶联作为受保护的构件
695、·将裂解后的粗制材料根据方法2b)环化。
696、方法d(螯合剂与氨基酸侧链中的氨基结合-环化的马来酰亚胺,c末端酰胺)
697、·利用一个侧链带有alloc保护基的氨基酸在rink酰胺树脂上进行固相肽合成,
698、·序列组装完成后:alloc脱保护和螯合剂偶联作为受保护的构件,
699、·将裂解后的粗制材料根据方法2a)环化。
700、方法e(n末端螯合剂-二硫化物,c末端酸)
701、·在三苯甲基树脂上进行固相肽合成,
702、·将裂解后的粗制材料根据方法2b)环化。
703、方法f(n末端螯合剂-环化的马来酰亚胺,c末端酸)
704、·在三苯甲基树脂上进行固相肽合成,
705、·将裂解后的粗制材料根据方法2a)环化。
706、方法g(马来酰亚胺螯合剂-环化的马来酰亚胺,c末端酰胺)
707、·在rink酰胺树脂上进行固相肽合成,
708、·将裂解后的粗制材料根据方法2a)用配有螯合剂的马来酰亚胺试剂环化。
709、方法h(马来酰亚胺螯合剂-环化的马来酰亚胺,c末端酸)
710、·在三苯甲基树脂上进行固相肽合成,
711、·将裂解后的粗制材料根据方法2a)用配有螯合剂的马来酰亚胺试剂环化。
712、方法i(与氨基酸侧链氨基结合的螯合剂-二硫化物-c末端酸)
713、·在三苯甲基树脂上进行固相肽合成,
714、·将裂解后的粗制材料根据方法2b)环化,
715、·使用n-羟基琥珀酰亚胺活化的螯合剂将螯合剂与dmso中纯化的肽中间体偶联。
716、方法k(螯合剂与氨基酸侧链中的氨基结合-环化的马来酰亚胺-c末端酸)
717、·在三苯甲基树脂上进行固相肽合成,
718、·将裂解后的粗制材料根据方法2a)环化,
719、·使用n-羟基琥珀酰亚胺活化的螯合剂将螯合剂与dmso中纯化的肽中间体偶联。
720、实施例2:本发明化合物的dota-过渡金属络合物的制备
721、a.从包含未络合dota的相应肽制备包含dota-过渡金属络合物的肽的一般程序
722、将在以下溶液中包含未络合的dota的0.1mm肽溶液用在水中的0.1mm相应金属盐溶液稀释:
723、·0.4m乙酸钠,ph=5(缓冲液a)(在cu(ii)、zn(ii)、in(iii)、lu(iii)或ga(iii)络合物的情况下),或
724、·0.1m乙酸铵,ph=8(缓冲液b)(在eu(iii)络合物的情况下),
725、由此将肽与金属的摩尔比调节至1:3。以如下条件搅拌溶液:
726、·在50℃搅拌20分钟(本文也称为条件a)(在in(iii)、lu(iii)、ga(iii)、zn(ii)或cu(ii)络合物的情况下),或
727、·在室温下过夜(本文也称为条件b)(在eu(iii)络合物的情况下)。
728、然后将该溶液进行:
729、·hplc纯化(本文也称为纯化方法a),或
730、·固相萃取(本文也称为纯化方法b)。
731、在固相萃取的情况下,将250mg varian bondesil-env置于15ml聚苯乙烯注射器中,用甲醇(1×5ml)和水(2×5ml)预洗。然后将反应溶液加到柱上。此后用水进行洗脱(2×5ml,以去除多余的盐),5ml的50% acn溶液作为第一级分,接下来的每个级分均用在含有0.1% tfa的水中的5ml的50% acn洗脱。
732、在任一情况下(hplc纯化或固相萃取),将含有纯产物的级分合并并冷冻干燥。
733、实施例3:facs结合测定
734、为了测定根据本发明的化合物与表达fap的细胞的结合,建立了竞争性facs结合测定。
735、将表达fap的人wi-38成纤维细胞(ecacc)在包含15%胎牛血清、2mm l-谷氨酰胺和1%非必需氨基酸的emem中培养。将细胞用accutase(biolegend,#bld-423201)分离并在facs缓冲液(包括1% fbs的pbs)中洗涤。将细胞在facs缓冲液中稀释至终浓度为100,000个细胞/ml,将200μl细胞悬液移至u形非结合96孔平板(greiner)中。将细胞在冰冷的facs缓冲液中洗涤并与3nm的cy5标记的化合物(h-met-[cys(3mebn)-pro-pro-thr-glu-phe-cys]-asp-his-phe-arg-asp-ttds-lys(cy5so3)-nh2)在存在肽浓度增加的条件下在4℃温育1小时。将细胞用facs缓冲液洗涤两次并重悬于200μl的facs缓冲液中。在attune nxt流式细胞仪中分析细胞。中值荧光强度(cy5通道)通过attune nxt软件计算并针对肽浓度作图。使用activitybase软件进行四参数逻辑(4pl)曲线拟合和pic50计算。对于根据本发明的每种化合物,这个测定以及根据实施例4进行的fap蛋白酶活性测定的结果列于表8中(在实施例4中示出)。pic50类别a表示pic50值>7.0,类别b表示pic50值在6.1和7.0之间,并且类别c表示pic50值≤6.0。
736、实施例4:fap蛋白酶活性测定
737、为了测定实施例13的肽的抑制活性,建立了基于fret的fap蛋白酶活性测定。
738、将重组人fap(r&d systems,#3715-se)在测定缓冲液(50mm tris、1m nacl、1mg/ml bsa,ph 7.5)中稀释至3.6nm的浓度。将25μl fap溶液与25μl的3倍连续稀释的测试化合物混合,并在白色96孔proxiplate(perkin elmer)中温育5分钟。作为特异性fap底物,使用fret肽hilytefluortm488-vs(d-)p sqg k(520)-nh2(bainbridge,et al.,sci rep,2017,7:12524)。加入在测定缓冲液中稀释的25μl的30μm底物溶液。所有溶液在使用前均在37℃平衡。在spectramax m5读板器中在37℃以动力学模式测量5分钟底物裂解和荧光增加(485nm激发和538nm发射)。通过softmax pro软件计算rfu/sec,并根据肽浓度作图。使用activitybase软件进行四参数逻辑(4pl)曲线拟合和pic50计算。表8中给出了本发明每种化合物的这个测定的结果。pic50类别a代表pic50值>7.0,类别b代表pic50值在6.1和7.0之间,并且类别c代表pic50值≤6.0。
739、如表8所示,本发明的化合物在facs结合测定和fap蛋白酶活性测定中均显示出惊人的优异结果。
740、除此之外,还可以轻松发现sar数据,该数据表明具有缀合的螯合剂的化合物与不含螯合剂但肽序列相似的化合物具有非常相似的活性。例如,化合物(1005)在n末端具有螯合剂和接头(dota-ttds-nle),是pic50>8的最高活性类别。在n末端不具有螯合剂和接头的相应化合物(具有n末端h-met-的化合物(1001)及具有n末端hex-的化合物(1002))与包含螯合剂的化合物(1005)相比呈现所有相似的活性。
741、对于本发明的马来酰亚胺环状化合物发现了类似的关系:例如,化合物(2004)和(2005)在n-末端具有螯合剂和接头(分别为dota-o2oc和dota-ttds-nle),并且是在pic50>7的最高活性类别。与包含螯合剂的化合物(2004)和(2005)相比,在n-末端没有螯合剂和接头的相应化合物((2001)和(2002)均具有n-末端hex-)表现出所有相似的活性。
742、这意味着来自不含螯合剂的化合物的活性数据可预测包含螯合剂的化合物的活性。如果螯合剂根据其它指定的可能性与本发明的化合物缀合(即在c-末端氨基酸或肽及在本发明的马来酰亚胺环状化合物的情况下在马来酰亚胺的氮原子,例如化合物(2017)、(2018)、(2019)和(2020)),则也观察到这种现象。
743、表8:化合物id、序列、计算质量、实测质量以及facs结合和fap活性测定的pic50类别
744、
745、
746、
747、在说明书、权利要书求、序列表和/或附图中公开的本发明的特征可以单独和以其任意组合作为以各种形式实现本发明的材料。
748、参考文献
749、本文引用的每个文件和任何文件的公开内容均通过引用并入。
750、
751、
752、
753、
754、
755、
756、
757、
758、
759、
760、
761、
762、
763、
764、
765、
766、
767、
768、
769、
770、
771、
772、
773、
774、
775、
776、
777、
778、
779、
780、
781、
782、
783、
784、
785、
786、
787、
788、
789、
790、
- 还没有人留言评论。精彩留言会获得点赞!