用于延长生物分子半衰期的化合物和方法与流程
本发明属于延长蛋白的血浆半衰期领域,特别涉及开发可用于此目的的白蛋白的新结合物。
背景技术:
1、将实验室实验转化为体内环境以评估分子的安全性和疗效需要考虑其他参数。对于暴露于全身循环的产品,最重要的变化是产品在血管血流中停留的影响。管理在血液中的停留时间是必要的,可以通过使用白蛋白这种最丰富的循环蛋白作为临时载体来提供这种管理。这可以通过将感兴趣的化合物通过与所述化合物融合或缀合的特定配体瞬时连接至血清白蛋白来实现。
技术实现思路
1、本发明涉及包含sac7d蛋白的变体或sac7d家族蛋白的变体的多肽,特别是与白蛋白结合的aho7c,以及其特别用于延长在体内与其结合的分子(包括肽或多肽)的半衰期。
2、这种变体与人和鼠血清白蛋白均结合,这对于加快产品的临床开发以及从动物到人的转化具有重要意义。事实上,大多数血清白蛋白结合物在小鼠和人之间不会发生交叉反应。此外,亲和力很重要,从而保证变体与血清白蛋白的强结合(和低周转率)(因此增加与变体相连的生物分子的血清半衰期)。这些变体还与血清白蛋白的表位结合,该表位不会妨碍血清白蛋白与fcr的结合,因而不会妨碍血清白蛋白/与生物分子相关联的变体复合物的再循环,这对增加与生物分子相关联的变体的血清半衰期很有意义。该变体是一种小蛋白,不会消除与其相关联的生物分子自身的生物活性。
3、特别地,在某些实施方案中,所述变体基于sac7d蛋白,并且包含seq id no:45、seq id no:46、seq id no:47、seq id no:48、seq id no:49、seq id no:50、seq id no:51、seq id no:52、seq id no:53、seq id no:54、seq id no:55、seq id no:56、seq idno:57、seq id no:58、seq id no:59、seq id no:60、seq id no:61、seq id no:62、seq idno:63、seq id no:64或seq id no:65。在某些实施方案中,所述变体基于ahoc蛋白,并且包含seq id no:66、seq id no:67、seq id no:68、seq id no:69、seq id no:70、seq id no:71、seq id no:72、seq id no:73、seq id no:74、seq id no:75、seq id no:76、seq idno:77、seq id no:78、seq id no:79、seq id no:80、seq id no:81、seq id no:82、seq idno:83、seq id no:84、seq id no:85或seq id no:86。在说明书和序列表之间存在差异的情况下,说明书中提到的序列是优先的。
4、特别地,变体包含seq id no:38或seq id no:38的氨基酸1-54。
5、特别地,变体包含选自以下的序列:seq id no:48、seq id no:51、seq id no:55、seq id no:58、seq id no:62、seq id no:65以及这些序列的氨基酸1-57。
6、特别地,变体包含选自以下的序列:seq id no:69、seq id no:72、seq id no:76、seq id no:79、seq id no:83、seq id no:86以及这些序列的氨基酸1-55。
7、本发明还涉及编码变体的核酸、包含变体和活性物质的多肽、生产方法、以及变体单独或与活性物质组合的用途。
8、特别地,本发明涉及
9、—本文公开的多肽,其包含与人和小鼠血清白蛋白结合的sac7d家族成员的变体。
10、—本文公开的多肽,其中与人和小鼠血清白蛋白结合的sac7d家族成员的变体缀合至有机分子。
11、—本文公开的多肽,其中与人和小鼠血清白蛋白结合的sac7d家族成员的变体缀合至另一多肽。
12、—本文公开的多肽,其中另一多肽是sac7d家族蛋白的另一变体。
13、—编码本文公开的多肽的核酸分子。
14、—包含本文公开的核酸分子的表达载体。
15、—包含本文公开的核酸分子、或本文公开的表达载体的宿主细胞。
16、—药物组合物,其包含本文公开的多肽、本文公开的核酸、本文公开的表达载体或本文公开的宿主细胞以及药学上可接受的载体。
17、—用于产生本文公开的多肽的方法,包括
18、(a)培养细胞培养物,其中细胞已经被本文公开的表达载体转化,
19、和
20、(b)回收多肽。
21、—本文公开的多肽作为药物。
22、—本文公开的多肽用于治疗或预防疾病,其中所述变体与治疗或预防疾病的活性物质相关联。
23、发明详述
24、需要注意的是,上面指出的序列可以在其n末端包含甲硫氨酸,但如果不包含列在每个序列n末端的这样的甲硫氨酸,也可以实施本发明。类似地,位于蛋白末端的氨基酸可以被省略。特别地,位于sac7d的残基l58之后的氨基酸(位于seq id no:16的l60之后的残基)可以省略。因此,变体可以包含seq id no:45至seq id no:65中任一个的氨基酸1-57、1-58、1-59、1-60、1-61、1-62或1-63。
25、当基于aho7c支架时,变体可包含seq id no:66至seq id no:86中任一个的氨基酸1-55、1-56、1-57或1-58。
26、这种变体能够融合至生物分子和/或缀合至小化学实体,延长分子的血浆半衰期,从而提高疗效或生物利用度,或允许使用较少的量。需要这种半衰期延长的典型分子是小化学分子(例如,抗癌的细胞毒性剂,如奥瑞他汀或多柔比星)、肽(胰岛素类似物,如glp-1)、小蛋白支架如来自嗜酸热硫化叶菌(sulfolobus acidocaldarius)的sac7d(以及类似物,如aho7c或sso7d)衍生物、抗体模拟物,如亲和体(affibodies)、亲和素(affilins)、affimers、alphabodies、anticalins、avimers、darpins、fynomer、kunits结构域肽、单体、蛋白a的z结构域、γb结晶、泛素、半胱氨酸蛋白酶抑制剂(cystatin)、脂质运载蛋白、膜受体的结构域、锚蛋白重复基序、fyn的sh3结构域、蛋白酶抑制剂的kunits结构域、纤连蛋白的第10个iii型结构域、3或4螺旋束蛋白、犰狳重复结构域、富含亮氨酸的重复结构域、pdz结构域、sumo或sumo样结构域、免疫球蛋白样结构域、磷酸酪氨酸结合结构域、普列克底物蛋白(pleckstrin)同源结构域、src同源2结构域或合成肽配体、抗体片段(包括fab、vhh、scfv)、酶、治疗性核酸,如反义寡核苷酸、sirna、shrna。
27、这对于以下生物分子是特别感兴趣的:旨在中和循环分子(如细胞因子(例如,il-17、tnf-α…)、生长因子、激素、抗菌肽、补体因子、凝血因子)的生物分子;还有与循环细胞(如免疫细胞(t淋巴细胞、巨噬细胞、抗原呈递细胞...))相互作用以进行中和、募集或激活的生物分子;需要扩散到组织和器官中的生物分子,因此受益于在脉管系统中的长期暴露,以加强外渗和/或组织摄取,例如脑摄取、肝脏、肺或骨骼靶向的情况;类似地,在循环中长时间的停留有利于更强地向实体瘤扩散,从而增强抗肿瘤活性(例如,当中和pd-l1或egf-r时);具有抗菌或抗病毒活性以治愈更普遍的感染的败血症的分子。
28、根据变体所融合的生物分子,融合产物可用于治疗癌症、代谢性疾病(如糖尿病)、神经系统疾病、炎性疾病和自身免疫性疾病(如类风湿性关节炎、银屑病、狼疮或多发性硬化症),或酶缺乏症,特别是脑部酶缺乏症。
29、生物分子(多肽或有机分子)优选具有生物活性。这表明该生物分子与受试者体内存在的分子(受体、配体、抗原等)相互作用,有利地为受试者提供有益效果(治愈、缓解、减轻症状、减少与待治疗疾病相关的标记物(例如,在病毒感染的情况下减少病毒载量))。事实上,活性物质是旨在用于制造医药产品(或诊断产品)的物质或物质的混合物,在生产过程中使用时,成为该产品的活性成分,旨在发挥药理、免疫或代谢作用,以恢复、纠正或改变生理功能或进行医学诊断。
30、应当注意的是,本说明书公开了sac7d的变体,但是该教导也适用于sac7d家族的其他蛋白。这些教导也适用于如wo 2007139397中所公开的其他ob折叠结构域。本发明也适用于sh3结构域,其是一种约60个氨基酸残基的小的蛋白结构域,最初被描述为病毒适体(adaptor)蛋白v-crk中的保守序列,在pfam数据库中以pf00018描述。sh3结构域具有特征性的β桶状折叠,其由排列为两个紧密堆积的反向平行β片层的五或六个β链组成。接头区可以包含短的螺旋。需要注意的是,ob折叠和sh3结构域具有同源性,考虑到这些结构域的序列和结构的知识,可以确定在任何ob折叠或sh3结构域中,哪些氨基酸对应于如下面公开的sac7d的氨基酸。
31、wo 2012069654描述了产生与白蛋白结合的darpins(包含ankryn重复)以改善感兴趣分子的药代动力学或药效学。
32、ep1930342描述了ob折叠蛋白变体的分离。
33、wo 2012150314描述了将与感兴趣的靶标的结合潜力从一个sac7d家族蛋白转移到另一个sac7d家族蛋白的可能性。
34、ep3483180描述了sac7d变体-抗体复合物。
35、robinson等人(nature,1998年第392卷,第6672期,202-205)描述了sac7d及其与dna的结合。
36、基于sac7d家族共有序列(seq id no:16)的变体描述
37、本文公开了sac7d家族特定成员的变体。鉴于sac7d家族蛋白序列的相似性(如图1所示)以及可能将突变从一个蛋白带入到另一个蛋白的事实,可以将突变绘制在sac7d家族的共有序列中。
38、在序列seq id no:17—seq id no:37中,在位置8-10、22、27、30、32、42、46和48处表示为x或xaa的氨基酸如表2所示。表示为x(或xaa)的其他氨基酸如表1或表3所示(其中“-”指无氨基酸)。
39、表1.seq id no:17–seq id no:37中氨基酸的描述。
40、
41、
42、表1中公开的氨基酸对应于观察到的sac7d家族蛋白的变异,也如图1所示。
43、表2中公开的氨基酸对应于本文公开的变体中参与白蛋白结合的氨基酸。值得注意的是,这些变体与野生型蛋白在以下氨基酸上存在进一步差异:
44、位置23:存在w;位置25:存在l;位置34:存在k;位置44:存在y。
45、发明人已证明这些氨基酸对于与白蛋白的结合很重要(氨基酸的改变会大大降低与白蛋白结合的能力或与白蛋白的亲和力)。相反,根据表2,可以修饰来自优化的结合物的其他氨基酸(seq id no:20、seq id no:23、seq id no:27、seq id no:30、seq id no:34或seq id no:37)。特别地,已经注意到,用其他氨基酸替换在这些结合物的位置22、27、30、32、42或48处的氨基酸基本上不改变结合或其特征。对于这些结合物中位置8和10的氨基酸,它们可以分别被疏水性/芳香族和极性/带电氨基酸改变,如表2中所列。
46、还表明,共有序列(不参与结合)的d17(天冬氨酸)可以被e(谷氨酸)替换。这在上述序列中得到体现(seq id no:20、seq id no:23,在位置17处含有x;seq id no:27和seqid no:30,含有d17;seq id no:34和seq id no:37,含有e17)。
47、表2.seq id no:17-seq id no:37中表示为xaa的氨基酸的描述。
48、
49、需要注意的是,该表用于上述序列,用于它们含有的xaa。对于一些序列,在表2的一些位置处指定了氨基酸,因此表中的行不适用。
50、如上所述,seq id no:17-37的位置1处的甲硫氨酸可以省略。seq id no:17-37的氨基酸61-68也可以省略。
51、在一个实施方案中,多肽包含seq id no:17或表3的序列之一的氨基酸2-60。
52、表3.基于sac7d家族蛋白共有序列的变体序列的列表。
53、
54、
55、x的性质在表1和表2中提供。位置17的x可以是e或d。
56、基于sac7d和aho7c的变体描述
57、sac7d和aho7c是具有很大相似性的蛋白。
58、seq id no:87对应于sac7d(seq id no:1)的氨基酸2-66和aho7c(seq id no:14)的氨基酸3-60比对后的共有序列。起始氨基酸已被省略,因为它们在蛋白结构中不是必需的。
59、xkvkfkykgeekevdxskikkvwrvgkmxsftyddngktgrgavsekdapkellxxxxxxxxxx(seqid no:87)
60、在该共有序列中,x(或xaa)如表4所示。
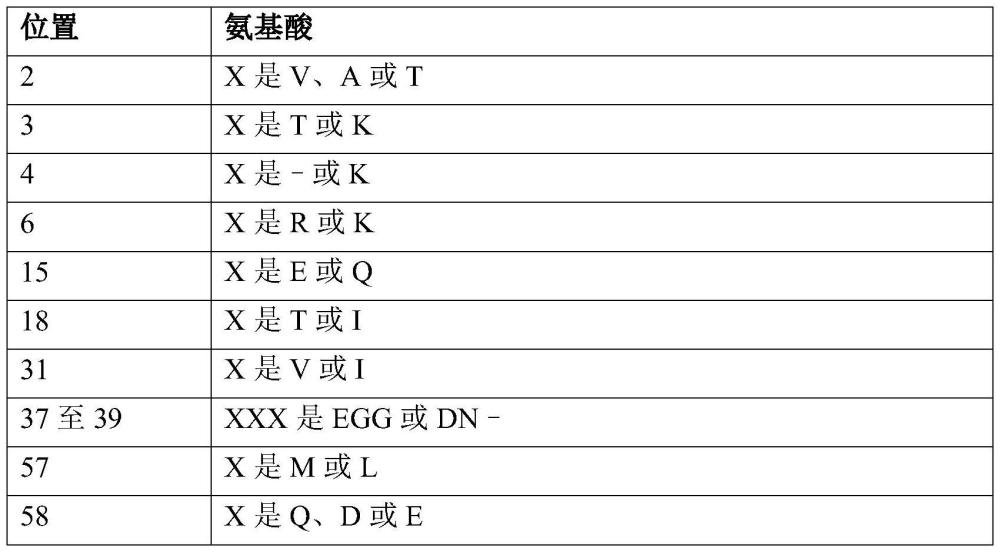
61、表4.在seq id no:87和seq id no:38-44中表示为xaa的氨基酸的描述。
62、
63、此类变体表示为
64、表5:基于sac7d-aho7c共有序列的变体的序列。
65、
66、
67、x表示的氨基酸进一步描述于表4、表6和表7中
68、表6.在seq id no:38-seq id no:86中表示为xaa的氨基酸的描述。
69、
70、需要注意的是,该表用于上述序列,用于它们含有的xaa。对于一些序列,在表6的一些位置处指定了氨基酸,因此表中的行不适用。
71、在这些序列中,在变体上一些不参与结合的氨基酸也可以进行修饰(具体参见seqid no:38-seq id no:86)。它们表示在表7中。
72、表7.在seq id no:36-44、seq id no:45-51和seq id no:66-72中表示为xaa的氨基酸。
73、 位置 氨基酸 15 xaa是d或e 36 xaa是n或q 56 xaa是m或l
74、在位置56处的xaa仅存在于seq id 45-51中。
75、基于sac7d(seq id no:1)的变体的描述
76、与人和小鼠血清白蛋白结合的sac7d的变体由seq id no:45至seq id no:65描述。
77、在这些序列中,sac7d蛋白的起始甲硫氨酸(m)已被省略。申请人确实已经证明,当删除该氨基酸时,蛋白的活性没有改变。同样,可以从变体中省略最后7个氨基酸并保留活性。
78、因此,由seq id no:45至seq id no:65中任一个的氨基酸1-57描述的蛋白也是根据本发明的变体。还可以引用由seq id no:45至seq id no:65中任一个的氨基酸1-58、1-59、1-60、1-61、1-62、1-63描述的蛋白,其也是根据本发明的变体。
79、因此,该多肽包含seq id no:45至seq id no:65中任一个,或基于这些序列的任何截短的蛋白,并且如上所述。
80、此类变体表示为
81、表8:基于sac7d的变体的序列。
82、
83、
84、x表示的氨基酸进一步描述于表6和表7中。
85、如上所述,可以修饰sac7d的d16(其位于seq id no:45-65的位置15,因为sac7d中存在的m1已被省略)、sac7d的n37(本文位于位置36)或sac7d的m57(本文位于位置56),如表7中公开的。
86、至于sac7d/aho7c的共有序列,可以预见任何取代的组合(编号是相对于seq idno:45-65),尽管序列表并未全部描述它们:
87、
88、如上所述,这些序列均含有突变的氨基酸w21、l23、k32、y41(分别对应于seq idno:1的位置22、24、33和42,其含有n末端甲硫氨酸),与sac7d中天然存在的氨基酸不同。
89、申请人确实发现这些氨基酸存在于与血清白蛋白结合的各种变体中,并且这种修饰导致结合的降低(亲和力损失或结合损失)。在表6中提到的条件下,其他氨基酸可以是可变的。
90、非常感兴趣的变体由seq id no:47、seq id no:48、seq id no:50、seq id no:51、seq id no:54、seq id no:55、seq id no:57、seq id no:58、seq id no:61、seq idno:62、seq id no:64和seq id no:65描述。
91、特别地,非常感兴趣的变体由seq id no:48、seq id no:51、seq id no:55、seqid no:58、seq id no:62和seq id no:65描述,
92、seq id no:62(命名为f06)以及seq id no:55是特别令人感兴趣的。需要注意的是,seq id no:62的l56可以被m56替换。
93、seq id no:58(命名为b11)以及seq id no:65也特别令人感兴趣。
94、基于aho7c(seq id no:14)的蛋白描述
95、与人和小鼠血清白蛋白结合的aho7c的变体由seq id no:66至seq id no:86描述。如上所述,这种蛋白与sac7d非常相似。本文还显示和提醒sac7d的突变可以从sac7d带入到另一个蛋白(wo 2012/150314)。
96、在这些序列中,aho7c蛋白的起始甲硫氨酸和丙氨酸(ma)(seq id no:14)已被省略。申请人确实已经证明,当删除这些氨基酸时,蛋白的活性没有改变。同样,可以从变体中省略最后4个氨基酸并保留活性。
97、因此,由seq id no:66至seq id no:86中任一个的氨基酸1-55描述的蛋白也是根据本发明的变体。还可以引用由seq id no:66至seq id no:86中任一个的氨基酸1-56、1-57、1-58描述的蛋白,其也是根据本发明的变体。
98、因此,该多肽包含seq id no:66至seq id no:86中任一个,或基于这些序列的任何截短的蛋白,并且如上所述。
99、此类变体表示为
100、表9:基于ao7c的变体的序列。x表示的氨基酸进一步描述于表6和表7中。
101、
102、
103、
104、如上所述,可以修饰aho7c的d17(其位于seq id no:66-86的位置15,因为aho7c中存在的m1a2已被省略),或aho7c的n38(本文位于位置36),如表7中公开的。
105、至于sac7d/aho7c的共有序列,可以预见任何取代的组合(编号是相对于seq idno:66-86),尽管序列表并未将其全部描述:
106、
107、如上所述,这些序列均含有突变的氨基酸w21、l23、k32、y41(分别对应于seq idno:14的位置23、25、34和43,seq id no:14在n末端含有甲硫氨酸和丙氨酸),与aho7c中天然存在的氨基酸不同。
108、申请人确实发现这些氨基酸存在于与血清白蛋白结合的各种变体中,并且这种修饰导致结合的降低(亲和力损失或结合损失)。在表6中提到的条件下,其他氨基酸可以是可变的。
109、非常感兴趣的变体由seq id no:68、seq id no:69、seq id no:71、seq id no:72、seq id no:75、seq id no:76、seq id no:78、seq id no:79、seq id no:82、seq idno:83、seq id no:85和seq id no:86描述。
110、特别地,非常感兴趣的变体由seq id no:69、seq id no:72、seq id no:76、seqid no:79、seq id no:83和seq id no:86描述,
111、seq id no:83(基于f06)特别令人感兴趣。
112、seq id no:86(基于b11)也特别令人感兴趣。
113、在一个具体实施方案中,多肽包含与人血清白蛋白(hsa)结合的sac7d家族蛋白的变体。
114、在一个具体实施方案中,与hsa结合的sac7d家族蛋白的变体与另一个蛋白或多肽连接或融合(本文也表示为相关联)。
115、本发明还涉及包含编码本文所述多肽的dna序列的遗传构建体、包含此类遗传构建体的载体和在其基因组中包含此类遗传构建体(核酸或载体)的宿主细胞。
116、本发明还涉及用于产生本文公开的多肽的方法,包括由以下组成的步骤
117、a.培养细胞培养物,其中细胞已经通过公开的遗传构建体进行转化,
118、和
119、b.回收多肽。
120、本发明还涉及本文公开的多肽用作药物。
121、本发明还涉及一种融合蛋白,其包含与具有治疗活性的多肽或蛋白质融合的本文公开的变体,所述融合蛋白用作药物。
122、本发明还涉及治疗需要其的受试者的方法,包括向受试者施用治疗量的本文公开的多肽,特别是当受试者患有癌症、代谢性疾病(如糖尿病)、神经系统疾病、炎性疾病或自身免疫性疾病(如类风湿性关节炎、银屑病、狼疮或多发性硬化症),或酶缺乏症,特别是脑部酶缺乏症。施用于受试者的多肽包含与人血清白蛋白结合的sac7d家族蛋白的变体,所述变体与对于待治疗的疾病具有治疗活性的蛋白或肽融合。例如,中和白介素17以治疗银屑病的蛋白;中和肿瘤坏死因子α用于治疗类风湿性关节炎的蛋白;阻止程序性死亡配体1与其癌细胞表面受体相互作用的蛋白、中和应激抗性因子,如热休克蛋白(特别是hsp 110)的蛋白。
123、治疗量(或有效量)是足以实现有益或期望结果(如临床结果)的量,因此取决于其应用的环境。在向患有本文公开的疾病的患者施用包含结合hsa的变体以及具有治疗活性的肽或多肽的多肽的情况下,试剂的有效量是,例如,相较于与未施用试剂所获得的反应,足以实现治愈患者、改善患者的病状、加速患者治愈的量。它也可以是阻止或减缓疾病进展的量。它可以是允许疾病消退、或与特定疾病相关的生物标志物消退的量。
124、具有治疗活性的试剂(或治疗剂)是在以有效量施用至患有疾病的受试者后改善受试者的病状、或减少与疾病相关的生物标记物的试剂。
125、需注意,sac7d的序列为:
126、mvkvkfkykgeekevdtskikkvwrvgkmvsftyddngktgrgavsek dapkelldmlaraerekk(seq id no:1)。
127、本文公开的与hsa结合的变体在对应于sac7序列的位置7、8、9、21、22、24、26、29、31、33、40、42、44和46(seq id no:38-86的位置6、7、8、20、21、23、25、28、30、32、39、41、43和45)处含有突变。在一些变体中可以保留seq id no 1中位置21的赖氨酸。在一些变体中,还可以保留seq id no 1中位置8处的赖氨酸、seq id no 1中位置26、29、31、40或46处的天然氨基酸或seq id no 1中位置43处的苯丙氨酸。
128、然而,与天然序列(即seq id no 1中的w22、l24、k33和y42(seq id no 38-86中的w21、l23、k32和y41))相比,变体含有至少4个突变的氨基酸,优选至少6个、更优选至少9个、或至少或恰好12个突变的氨基酸。
129、当与hsa结合的sac7d家族蛋白的变体与另一个蛋白或多肽连接或融合时是优选的。
130、它可以与sac7d家族蛋白的另一个变体、肽或抗体结合或融合(如wo 2019096797中所述)。
131、特别地,sac7d家族蛋白的其他变体可以结合il-17(参见wo 2019096797)或tnf-α(参见wo 2020074402)。
132、在另一个实施方案中,多肽缀合至有机分子。
133、还允许获得包含编码上述多肽的dna序列的遗传构建体、包含此类遗传构建体的载体和在其基因组中包含此类遗传构建体的宿主细胞。此类载体还包括允许多肽转录和翻译的元件(如启动子、终止子、增强子……)。
134、可以进行用于产生多肽的方法,包括培养其中细胞已经被遗传构建体转化的细胞培养物,和回收多肽。
135、还可以将所公开的多肽作为药物,特别是包含与has结合的变体的多肽,所述与has结合的变体与另一个具有治疗活性的肽或多肽融合。
136、需要注意的是,上面指出的序列可以在其n末端包含甲硫氨酸,但在不包含列在每个序列n末端的甲硫氨酸时,也可以实施本发明。类似地,位于蛋白末端的氨基酸可以被省略。特别地,位于sac7d的残基l58之后的氨基酸(位于seq id no:16的l60之后的残基)可以省略。
137、应当注意的是,本说明书公开了sac7d的变体作为示例,但该教导也适用于sac7d家族的其他蛋白。这些教导也适用于如wo 2007139397中所公开的其他ob折叠结构域。特别地,提及wo2012150314,其证明可以使用图1中所示的比对,将突变从sac7d家族的一个序列带入到另一序列。本发明也适用于sh3结构域,其是一种约60个氨基酸残基的小的蛋白结构域,最初被描述为病毒适体(adaptor)蛋白v-crk中的保守序列,在pfam数据库中以pf00018描述。sh3结构域具有特征性的β桶状折叠,其由排列为两个紧密堆积的反向平行β片层的五或六个β链组成。接头区可以包含短的螺旋。需要注意的是,ob折叠和sh3结构域具有同源性,考虑到这些结构域的序列和结构的知识,可以确定在任何ob折叠或sh3结构域中,哪些氨基酸对应于如下面公开的sac7d的氨基酸。
138、sac7d蛋白家族
139、sac7d家族被定义为与sac7d蛋白有关,并对应于从极端细菌中分离的7kda的dna结合蛋白家族。本文将其公开为ob折叠结构域的代表性种类,其优选用于本发明的上下文中。由于sh3结构域与ob折叠结构域具有同源性,所以与sac7d相关的教导也适用于sh3支架。
140、在wo 2008/068637中特别描述了这些蛋白和该家族。因此,在本发明的上下文中,当蛋白具有序列seq id no:1至seq id no:15之一、或当其具有与序列seq id no:16对应的序列时,其属于sac7d家族,所述序列seq id no:16是共有序列(获自seq id no:1至seqid no:9和seq id no:12至seq id no:15。在该共有序列中,破折号–表示无氨基酸,蛋白不具有相同的大小)。这种sac7d家族特别包括源自嗜酸热硫化叶菌(sulfolobusacidocaldarius)的sac7d或sac7e蛋白、源自硫磺矿硫化叶菌(sulfolobus solfataricus)的sso7d蛋白、源自头寇岱硫化叶菌(sulfolobus tokodaii)的dbp7蛋白(也称为sto7蛋白)、源自希氏硫化叶菌(sulfolobus shibatae)的ssh7b蛋白、源自希氏硫化叶菌(sulfolobus shibatae)的ssh7a蛋白、源自勤奋金属球菌(metallosphaera sedula)的mse7、源自嗜铜金属球菌(metallosphaera cuprina)的mcu7、源自好客嗜酸两面菌(acidianus hospitalis)的aho7a或aho7b或aho7c、源自冰岛硫化叶菌(sulfolobusislandicus)的sis7a或sis7b,以及源自硫磺矿硫化叶菌(sulfolobus solfataricus)的p7ss蛋白。鉴于sac7d家族蛋白序列的广泛相似性,可以直接和容易地鉴定出与sac7d的给定氨基酸对应的除sac7d之外的另一个蛋白的氨基酸。特别地,还可以使用wo 2008/068637的教导,其显示(在图中)和解释(在说明书中)这样的蛋白是可叠加的(superimposable)。
141、wo 2012/150314显示,来自sac7d家族的一个蛋白的突变,可以被带入同一家族的另一个蛋白上。这种便携性(portability)解释了从sac7d家族的一个蛋白的突变体开始,产生sac7d家族另一个蛋白的突变体。第一突变体可以特别地通过进行wo 2008/068637的方法获得。因此,有可能具体地使用wo 2012/150314和图1的教导,从该家族的任何其他蛋白的突变体开始,获得sac7d家族的任何蛋白的突变体。作为说明,对于sac7d的突变体,可以使用图1的序列比对,将sac7d突变体的突变氨基酸引入另一个蛋白的支架内。作为说明,从本文公开的sac7d变体获得的aho7c的变体描述为seq id no:66至seq id no:86。
142、为获得变体而在野生型蛋白序列中引入的突变残基的数量优选在4至25之间,或更具体地在4至22之间。因此,与野生型ob折叠蛋白(或结构域)相比,可以获得优选具有至少4个,更优选至少5个,更优选至少6个,更优选至少7个或8个,甚至更优选至少10个,但通常小于25个,更优选小于22个,甚至更优选小于20个或小于15个或14个取代氨基酸的变体。应注意,本文考虑所有和任何范围(如5-20或7-25等)。特别优选的范围是4-17和6-17、4-11、4-12、5-12、6-12、4-14和6-14。
143、优选地,相对于野生型ob折叠结构域,在ob折叠结构域的结合位点处,使7、8、9、10、11、12、13或14个氨基酸突变。将这些突变引入对应于sac7d(seq id no:1)的v2、k3、k5、k7、y8、k9、g10、e11、k13、e14、t17、k21、k22、w24、v26、g27、k28、m29、s31、t33、y34、d36、n37、g38、k39、t40、r42、a44、s46、e47、k48、d49、a50和p51的氨基酸处,优选引入对应于k7、y8、k9、k21、k22、w24、v26、m29、s31、t33、t40、r42、a44和s46的氨基酸中。
144、特别地,当突变的氨基酸数量是7至14之间(包括端值)时,是令人感兴趣的。特别地,变体还可以包含如上所述的氨基酸插入。
145、如所示,sac7d家族蛋白是源自嗜酸热硫化叶菌(sulfolobus acidocaldarius)的sac7d或sac7e、源自硫磺矿硫化叶菌(sulfolobus solfataricus)的sso7d、源自头寇岱硫化叶菌(sulfolobus tokodaii)的dbp7(也称为sto7)、源自希氏硫化叶菌(sulfolobusshibatae)的ssh7b、源自希氏硫化叶菌(sulfolobus shibatae)的ssh7a、源自勤奋金属球菌(metallosphaera sedula)的mse7、源自嗜铜金属球菌(metallosphaera cuprina)的mcu7、源自好客嗜酸两面菌(acidianus hospitalis)的aho7a或aho7b或aho7c、源自冰岛硫化叶菌(sulfolobus islandicus)的sis7a或sis7b以及源自硫磺矿硫化叶菌(sulfolobussolfataricus)的p7ss。sac7d、sso7d、sac7e、ssh7b、ssh7a、dbp7、sis7a(3个等位基因)、mse7、mcu7、aho7a、aho7b、aho7c和sto7d蛋白的各个序列分别由seq id no:1至seq id no:15表示。
146、该sac7d家族蛋白的变体可以称为nanofitin。因此,本发明优选实施于seq idno:1至seq id no:15表示的蛋白的变体、或具有序列seq id no:16的蛋白,特别是sac7d的变体。
147、sac7d蛋白与ob折叠蛋白和sh3结构域的连接
148、ob折叠蛋白是本领域已知的。它们特别描述在上面引用的文件以及arcus(curropin struct biol.2002年1月;12(6):794-801)。ob折叠为具有五个beta(β)片层的圆柱体形式。大多数ob折叠蛋白使用其天然配体的相同结合界面,所述天然配体可以是寡糖、寡核苷酸、蛋白、金属离子或催化底物。该结合界面主要包括位于β片层中的残基。位于环中的某些残基也可以参与ob折叠蛋白与其天然配体的结合。因此,申请wo2007/139397和wo2008/068637以及arcus文件(2002,同上引文)描述了用于结合其天然配体的ob折叠蛋白结构域。
149、特别地,文件wo 2008/068637精确地描述了如何识别ob折叠蛋白的结合结构域。使用网站wu-blast2(http://www.ebi.ac.uk/blast2/index.html)(lopez等人,2003,nucleic acids res 31,3795-3798)、t-coffee(http://www.ch.embnet.org/software/tcoffee.html)(notredame等人,2000,j mol biol 302,205-217)和dali lite(http://www.ebi.ac.uk/dalilite/)(holm和park,2000,bioinformatics 16,566-567),通过叠加具有ob折叠结构域的蛋白的几个序列和3d结构,可以识别出结合结构域的位置,特别是可以被修饰的氨基酸。将sac7d的序列(seq id no:1)作为参考,这些是残基v2、k3、k5、k7、y8、k9、g10、e11、k13、e14、t17、k21、k22、w24、v26、g27、k28、m29、s31、t33、y34、d35、d36、n37、g38、k39、t40、g41、r42、a44、s46、e47、k48、d49、a50和p51,优选是k7、y8、k9、k21、k22、w24、v26、m29、s31、t33、t40、r42、a44和s46。使用图1中所示的比对,可以在每种蛋白中识别出与sac7d的这些氨基酸相对应的氨基酸。
150、wo 2008/068637描述可以使用dali网站(http://www.ebi.ac.uk/dali/interactive.html)(holm和sander,1998,nucleic acids res 26,316-319)进行ob折叠蛋白或结构域(该申请中使用了10个结构域,包括sac7d)的3d结构的叠加。因此,对于任何ob折叠蛋白(或任何ob折叠结构域),很容易识别出参与到结合位点中并与上述sac7d氨基酸对应的氨基酸。因此,提供可以在这些蛋白之一中进行突变的氨基酸,使得可以识别出对应于任何其他ob折叠结构域的氨基酸。
151、还要注意的是,ob折叠结构域类似于sh3结构域,因此可以识别出在sh3结构域中的sac7d氨基酸的等同物。
152、ob折叠或sh3结构域的示例
153、可以根据本发明使用的ob-折叠蛋白的非限制性示例是sac7d、sso7d、seb的n末端结构域(papageorgiou等人,1998)、志贺样毒素iie的链a(pdb 2bosa)、人嗜中性白细胞激活素肽2(nap-2,pdb 1tvxa)、棕色固氮菌(azotobacter vinelandii)(pdb 1h9j)的钼结合蛋白(modg)、spe-c的n末端结构域(roussel等人,1997)、大肠杆菌志贺样毒素的b5亚基(kitov等人,2000)、cdc13(mitton-fry等人,2002)、人y盒蛋白yb-1的冷休克dna结合结构域(kloks等人,2002)、大肠杆菌无机焦磷酸酶eppase(samygina等人,2001)或(arcus,2002)文章的表3中列出的任何蛋白,如1krs(赖氨酰-trna合成酶lyss,大肠杆菌)、1c0aa(asp-trna合成酶,大肠杆菌)、1b8aa(asp-trna合成酶,p.kodakaraensis)、1lyla(赖氨酰-trna合成酶lysu,大肠杆菌)、1quqa(复制蛋白a,32kda亚基,人)、1quqb(复制蛋白a,14kda亚基,人)、1jmca(复制蛋白a,70kda亚基(rpa70)片段,人)、lotc(端粒末端合蛋白,o.nova)、3ulla(线粒体ssdna结合蛋白,人)、1prtf(百日咳毒素s5亚基,百日咳杆菌(b.pertussis))、1bcpd(百日咳毒素s5亚基(atp结合型),百日咳杆菌)、3chbd(霍乱毒素,霍乱弧菌(v.cholerae))、1tiid(热不稳定毒素,大肠杆菌)、2bosa(verotoxin1/志贺毒素,b五聚体,大肠杆菌)、1br9(timp2,人)、1an8(超抗原spe-c,化脓性链球菌(s.pyogenes))、3seb(超抗原spe,金黄色葡萄球菌(s.aureus))、1aw7a(中毒休克综合征毒素,金黄色葡萄球菌)、1jmc(主要冷休克蛋白,大肠杆菌)、1bkb(起始翻译因子5a,p.aerophylum)、1sro(pnp酶的s1 rna结合结构域,大肠杆菌)、1d7qa(起始翻译因子1,e1f1a,人)、1ah9(起始翻译因子1,if1,大肠杆菌)、1b9ma(mo依赖性转录调控物mode,大肠杆菌)、1ckma(rna鸟苷酸转移酶,小球藻病毒,pbcv-1)、1a0i(atp依赖性dna连接酶,噬菌体t7)、1snc(葡萄球菌核酶,金黄色葡萄球菌)、1hjp(dna解旋酶ruva亚基,n端结构域,大肠杆菌)、1pfsa(基因v蛋白,假单胞菌噬菌体pf3)、1gvp(基因v蛋白,丝状噬菌体(f1,m13))、1gpc(基因32蛋白(gp32)核心,噬菌体t4)、1wgja(无机焦磷酸酶,酿酒酵母(s.cerevisiae))和2prd(无机焦磷酸酶,极端嗜热菌(t.thermophilus))。
154、具有sh3结构域的蛋白的非详尽示例是信号转导适体蛋白、cdc24、cdc25、pi3激酶、磷脂酶、ras gtp酶激活蛋白、vav原癌基因、grb2、p54 s6激酶2(s6k2)、sh3d21、c10orf76(可能的)、stac3、某些肌球蛋白、shank1、2、3、arhgap12、c8orf46、tango1、整合酶、粘着斑激酶(fak、ptk2)、富含脯氨酸的酪氨酸激酶(pyk2、cadtk、ptk2β)或trip10(cip4)。
155、生产已鉴定的变体
156、可以通过本领域已知的任何分子遗传方法,将鉴定的变体的序列克隆到任何合适的载体中。
157、包含核苷酸序列的这些重组dna构建体与载体(例如质粒、噬菌粒、噬菌体或病毒载体)组合使用,其中所述核苷酸序列编码包含上述变体的多肽。
158、可以通过sambrook等人,1989(sambrook j,fritschi ef和maniatis t(1989)molecular cloning:a laboratorymanual,cold spring harbor laboratory press,newyork)中描述的技术生产这些重组核酸分子。或者,例如,可以使用合成仪化学合成dna序列。
159、本发明的重组构建体包含能够表达rna的表达载体,因此从上述遗传序列中生产蛋白。因此,载体可以进一步包含调控序列,包括与本文公开的遗传序列的开放阅读框(orf)可操作地连接的合适的启动子。载体可以进一步包含选择性标记物序列,如抗生素抗性基因。当细菌用作表达宿主时,可能还需要特异性的起始信号和细菌分泌信号以有效地翻译编码序列。
160、分子的生产
161、用载体来转染或转化细胞,所述载体包含编码含有上述公开的变体的多肽的序列。
162、在此类表达和有利地分泌蛋白的条件下培养细胞。细胞的培养条件是通常用于重组抗体产生的条件,是本领域已知的。如果需要,本领域技术人员也可以优化本领域已知的此类条件。kunert和reinhart(appl microbiol biotechnol.2016;100:3451-3461)综述了这些方法并提供对其充足的参考。
163、可以使用细菌、噬菌体(shukra等人,eur j microbiol immunol(bp).2014;4(12):91-98)或真核生产系统。
164、应该更优选使用真核细胞以获得适当的翻译后修饰,如糖基化。
165、特别地,可以使用cho(中国仓鼠卵巢)细胞、per.c6细胞(人细胞系,pau等人,vaccine.2001 21;19(17-19):2716-21)、hek 293b细胞(人胚胎肾细胞293)、ns0细胞(非分泌型鼠骨髓瘤来源的细胞系)或eb66细胞(鸭细胞系valneva,法国里昂)。
166、本公开还提供含有至少一个dna构建体的宿主细胞,所述dna构建体编码包含本文公开的变体的多肽。宿主细胞可以是可获得表达载体的任何细胞。如上所述,宿主细胞可以是高等真核宿主细胞(如哺乳动物细胞)、低等真核宿主细胞(如酵母细胞)或原核细胞(如细菌细胞)。
167、通过本领域已知的任何方法(如磷酸钙转染、脂质转染、deae、葡聚糖介导的转染、电穿孔或噬菌体感染)将重组构建体引入宿主细胞。这些载体可以插入宿主细胞的基因组中,也可以保持为基因组外载体(如细菌人工染色体或酵母人工染色体)。当引入细胞基因组中时,这种引入可以是使用本领域已知方法的随机或靶向的引入(同源重组等)。
168、细菌宿主和表达
169、通过将重组dna序列与合适的翻译起始和终止信号一起插入具有功能性启动子的可操作阅读相(reading phase),构建用于细菌使用的有用的表达载体。载体将包含一种或多种表型选择性标记物和复制起点,以确保载体的维持,并且如果需要,提供在宿主内的扩增。
170、用于转化的合适的原核宿主包括大肠杆菌、枯草芽孢杆菌(bacillus subtilis)、鼠伤寒沙门氏菌(salmonella typhimurium)和假单胞菌属(pseudomonas)、链霉菌属(streptomyces)和葡萄球菌属(staphylococcus)内的各种物种。
171、真核宿主和表达
172、真核宿主细胞的示例包括脊椎动物细胞、昆虫细胞和酵母细胞。特别地,可以使用上述细胞。
173、按照本领域已知的方法来培养经转化的或转染的细胞,并(根据是否分泌多肽)从细胞内或细胞外级分中回收多肽。
174、分子的分离
175、可以通过各种已知分离方法中的任一种,利用蛋白的物理或化学特性,从细胞内或细胞外级分中分离出产生的重组蛋白并纯化。
176、特别地,可以使用以下方法,如沉淀、切向流动过滤、超滤、各种类型的液相色谱法(如分子筛色谱法(凝胶过滤)、吸附色谱法、离子交换色谱法和亲和色谱法)、透析及其组合。
177、通常,任何已知并和用于纯化重组多肽的方法都适用于纯化本文公开的分子。
178、如果在重组序列中引入了标签(如聚组氨酸标签),则可以使用该标签纯化分子。但是,优选利用亲和性来纯化分子。
179、特别地,可以利用以下事实:此处生产的分子与特定靶标结合,并使用任何亲和性方法(亲和柱、facs、珠)分离这样的分子。
180、本文公开的分子的一个特别优点是:它们不需要被糖基化使其具有活性,因此可以在任何类型的细胞中生产,而不是必须在真核细胞中生产。它们特别易于在细菌细胞中生产。
181、变体的修饰
182、上述的具有结合人血清白蛋白和小鼠血清白蛋白能力的变体,可以通过本领域已知的任何方法进行修饰。
183、制备包含变体的多肽
184、可以制备dna序列,其含有两个编码序列,一个编码序列用于本文公开的变体,另一个编码序列用于感兴趣的蛋白或肽(特别是具有治疗活性的蛋白或肽)。因此,所得的表达的蛋白是包含两种蛋白的多肽。载体可以以这样的方式构建,使得载体包含编码接头的序列,所述接头位于表达多肽中的两种蛋白之间。
185、因此,本发明还涵盖包含与hsa结合的ob折叠蛋白(优选sac7d家族)的蛋白的变体的多肽,其连接(优选通过如上所述的胺结合)至另一个蛋白或多肽。
186、在一个具体实施方案中,其他蛋白或多肽包含sac7d家族蛋白的另一个变体。
187、特别令人感兴趣的是:
188、—一种多肽,其包含与hsa结合的sac7d家族的ob折叠蛋白的变体,所述变体(在n或c末端)与结合白介素-17的sac7d家族的ob折叠蛋白的变体融合,所述多肽中和白介素-17与其受体的相互作用以治疗自身免疫性疾病,如银屑病或银屑病性关节炎。
189、—一种多肽,其包含与hsa结合的sac7d家族的ob折叠蛋白的变体,所述变体(在n或c末端)与结合程序性死亡配体1的sac7d家族的ob折叠蛋白的变体融合,所述多肽中和程序性死亡配体1与其同源受体相互作用以治疗癌症,如实体瘤(乳腺癌、肺癌、肾癌、胰腺癌等)。
190、—一种多肽,其包含与hsa结合的sac7d家族的ob折叠蛋白的变体,所述变体(在n-或c-末端)与结合热休克蛋白110的sac7d家族的ob折叠蛋白的变体融合,所述多肽中和热休克蛋白110诱导细胞对应激的抗性的能力和诱导巨噬细胞极化的能力,从而缓解对抗癌药物的抗性和/或其自身引发抗癌活性。
191、—一种多肽,其包含与hsa结合的sac7d家族的ob折叠蛋白的变体,所述变体(在n或c末端)与结合肿瘤坏死因子α的sac7d家族的ob折叠蛋白的变体融合。这种多肽作为tnfα介导的炎性信号的抑制剂发挥作用,有助于减少疾病(如类风湿性关节炎、克罗恩病和更常见的炎性肠疾病)中的炎症。
192、在另一个实施方案中,其他蛋白或多肽是抗体。在该实施方案中,ob折叠结构域的变体融合至免疫球蛋白单体的至少一条重链或轻链,优选在轻链或重链的n或c末端处。在另一个实施方案中,变体可以与重链或轻链两者融合。
193、为了获得这样的化合物,可以使用包含选自以下的dna序列的遗传构建体:
194、a.编码抗体重链的序列,在其3'端与编码ob折叠蛋白的变体的序列融合(可能具有编码接头的序列);
195、b.编码抗体重链的序列,在其5'端与编码ob折叠蛋白的变体的序列融合(可能具有编码接头的序列);
196、c.编码抗体轻链的序列,在其3'端与编码ob折叠蛋白的变体的序列融合(可能具有编码接头的序列);
197、d.编码抗体轻链的序列,在其5'端与编码ob折叠蛋白的变体的序列融合(可能具有编码接头的序列)。
198、可以在抗体链(重链和/或轻链)的n末端和/或c末端进行融合。值得注意的是,尤其是当使用小的ob折叠结构域(约70个氨基酸)(如来自sac7d家族的蛋白)时,就可以获得具有抗体结构的分子(两条轻链配对两条重链,这种二聚体配对在一起),其具有抗体区以及进一步地具有由修饰的ob折叠结构域组成的结合区。
199、在一个具体的实施方案中,本文公开的蛋白的抗体部分是igg分子。
200、在另一个实施方案中,本文公开的蛋白的抗体部分是iga分子。
201、在另一个实施方案中,本文公开的蛋白的抗体部分是igm分子。
202、在另一个实施方案中,本文公开的蛋白的抗体部分是igd分子。
203、在另一个实施方案中,本文公开的蛋白的抗体部分是ige分子。
204、抗体可以是人抗体、啮齿动物抗体(如小鼠抗体或大鼠抗体)、猫抗体、狗抗体、鸡抗体、山羊抗体、骆驼科动物抗体(如骆驼抗体、美洲驼抗体、羊驼抗体或纳米体)、鲨鱼抗体或来自任何其他物种的抗体。抗体可以是嵌合的或人源化的抗体。如wikipedia所提醒,人源化的抗体是来自非人物种的抗体,其蛋白序列已被修饰以增加其与人天然产生的抗体变体的相似性。嵌合抗体包含来自不同物种的序列。
205、当抗体作为本文公开分子的一部分时,其优选是包含两条相同的重链(约400至500个氨基酸,通常约450个氨基酸)和两条相同的轻链的抗体。因此,抗体包含相同的fab可变区。因此,该抗体是单特异性抗体,其中抗体的两个部分(轻链和重链的组合)都与相同的抗原表位结合。
206、然而,抗体可以呈现不同的重链和/或轻链。特别地,在一些实施方案中,抗体是双特异性抗体。因此,术语“抗体”既涵盖具有相同重链和轻链的上述“经典抗体”,也涵盖具有多于一种特异性的工程化的抗体。
207、在一个具体实施方案中,抗体呈现来自一个抗体的一条重链和轻链,以及来自另一个抗体的另一条重链和轻链。
208、抗体可以与选自以下的靶标结合:
209、细胞表面受体:胰岛素受体、低密度脂蛋白受体相关蛋白1、转铁蛋白受体、表皮生长因子受体、表皮生长因子受体变体iii、血管内皮生长因子受体1、血管内皮生长因子受体2、her2、her3、her4、pmsa、igf-1r、gitr、rage、cd28。
210、细胞表面蛋白:间皮素、epcam、cd19、cd20、cd38、cd3、tim-3、cea、cmet、icam1、icam3、madcam、a4b7、cd7、cd4、cd138、整合素如αvβ6、α4β7、α4β1、αeβ7。
211、血管生成因子和生长因子:vegf、血管生成素2、hgf、pdgf、egf、gm-csf、hb-egf、tgf。
212、免疫检查点抑制剂或激活剂:pd-1、pd-l1、ctla4、cd28、b7-1、b7-2、icos、icosl、b7-h3、b7-h4、lag3、kir、4-1bb、ox40、cd27、cd40l、tim3、a2ar。
213、循环蛋白:tnfα、il23、il12、il33、il4、il13、il5、il6、il4、ifng、il17、rankl、bace1、α突触核蛋白、tau、淀粉样蛋白。
214、因此特别预见
215、—一种多肽,其包含如上公开的结合hsa的变体以及与il-17或il-17r结合的抗体(例如,伊赛克珠单抗(ixekizumab)或布罗达鲁单抗(brodalumab)),用于治疗自身免疫性疾病,如银屑病。
216、—一种多肽,其包含如上公开的结合hsa的变体以及与pd-l1结合的抗体(如阿特珠单抗(atezolizumab)、阿维鲁单抗(avelumab)或多伏罗单抗(durvalumab)),用于治疗癌症,如肾癌、肺癌、乳腺癌、胰腺癌和各种类型的血癌,如多发性骨髓瘤、淋巴瘤。
217、—一种多肽,其包含如上公开的结合hs a的变体以及与egfr结合的抗体(如,西妥昔单抗、帕尼单抗(panitumumab)、扎鲁土木单抗(zalutumumab)、尼妥珠单抗(nimotuzumab)和马妥珠单抗(matuzumab)),用于治疗实体瘤。
218、可替选地,多肽可以包含如上公开的变体和生物活性分子,如促红细胞生成素、干扰素、溶酶体障碍酶(lysosomal disorder enzyme)或依那西普(etanercept)。
219、在另一个实施方案中,ob折叠结构域的变体(特别是sac7d家族蛋白的变体)与有机分子缀合。这可以通过本领域已知的任何方法来完成。特别地,可以将分子化学连接至蛋白。作为分子,可以列举出抗增殖剂(细胞毒性剂和细胞抑制剂),包括细胞毒性化合物(例如,广谱的)、血管生成抑制剂、细胞周期进程抑制剂、pbk/m-tor/akt通路抑制剂、mapk信号传导通路抑制剂、激酶抑制剂、蛋白伴侣抑制剂、hdac抑制剂、parp抑制剂、wnt/hedgehog信号传导通路抑制剂、rna聚合酶抑制剂和蛋白酶体抑制剂。也可以使用抗炎分子。
220、可以特别提及dna结合或烷基化药物,如蒽环类药物(阿霉素、表柔比星、伊达比星、柔红霉素)及其类似物、烷基化剂,如加利车霉素、放线菌素、丝裂霉素(mitromycine)、吡咯并苯二氮杂卓等。也可以列举细胞周期进程抑制剂,如cdk抑制剂、rho激酶抑制剂、检查点激酶抑制剂、极光激酶抑制剂、plk抑制剂和ksp抑制剂。也可以列举沙利度胺及其衍生物来那度胺和泊马度胺。为了治疗炎性疾病,还可以使用环氧合酶-2抑制剂、5-脂氧合酶抑制剂、槲皮素和/或白藜芦醇作为与包含变体的多肽缀合的分子。
221、因此特别预见
222、—一种多肽,其包含如上公开的结合hsa的变体和janus激酶抑制剂,用于治疗炎性疾病,特别是克罗恩病。
223、—一种多肽,其包含如上公开的结合hsa的变体和阿霉素,用于治疗实体瘤,如胰腺癌、卵巢癌、肺癌、肾癌、肝癌、乳腺癌。
224、也在上面公开令人感兴趣的和优选的分子。
225、变体的用途
226、这些变体可以特别用于治疗方法,尤其是使用具有治疗此类疾病的活性的生物分子,用于治疗癌症、代谢性疾病(如糖尿病)、神经系统疾病、炎性疾病和自身免疫性疾病(如类风湿性关节炎、银屑病、狼疮或多发性硬化症),或酶缺乏症(特别是脑部酶缺乏症)。
227、因此,本发明涉及治疗癌症、代谢性疾病(如糖尿病)、神经系统疾病、炎性疾病和自身免疫性疾病(如类风湿性关节炎、银屑病、狼疮或多发性硬化症)或酶缺乏症(特别是脑部酶缺乏症)的方法,包括向需要其的受试者施用治疗量的与分子(针对待治疗的疾病具有治疗效果的多肽或其他分子)融合的本文公开的ob折叠的变体(特别是sac7d家族蛋白的变体)。
228、如本文所用,术语“治疗量”或“有效量”是足以实现有益或期望结果(如临床结果)的量,“有效量”取决于其应用的上下文。有效量是提供治疗改善同时使副作用或不利作用最小化的量。对于癌症而言,治疗改善可以是实体瘤中肿瘤大小的消退、受试者生活质量的改善、组合治疗的疗效的改善。
229、可以通过本领域的任何方法施用变体。
230、特别地,可以注射变体。在另一个实施方案中,可以局部应用变体(在患者的皮肤或眼睛上),如wo 2014/173899中所公开。在另一个实施方案中,可以口服施用变体,如wo2016/062874中所公开的。
231、变体或含有变体的多肽也可用于诊断方法。特别地,此类变体或多肽可以与本领域已知的任何标记物连接并用于成像方法中。
- 还没有人留言评论。精彩留言会获得点赞!