结合TROP2的抗体及其用途的制作方法
发明领域本技术大体上涉及分离的单克隆抗体,特别是小鼠源、嵌合或人源化的单克隆抗体,或其抗原结合部分,其与人trop2结合,具有高亲和力和功能性。还提供编码该抗体或其抗原结合部分的核酸分子,用于表达该抗体或其抗原结合部分的表达载体、宿主细胞和方法。本技术还提供可以包含该抗体或其抗原结合部分的双特异性分子、免疫偶联物、嵌合抗原受体、溶瘤病毒和药物组合物,以及使用这些的治疗方法。
背景技术:
1、trop2是一种跨膜糖蛋白,又称为表皮糖蛋白1(egp-1)、膜成分表面标志物-1(m1s1)、肿瘤相关钙离子信号转导子2(tacstd2)和胃肠道抗原733-1(ga733-1)。各trop2分子由疏水性前导肽、胞外结构域、跨膜结构域和胞质尾部组成。胞质尾部含有高度保守的磷脂酰肌醇4,5-二磷酸(pip2)结合序列和位于303位的丝氨酸磷酸化位点(zaman s et al.,(2019)onco targets ther.12:1781-1790)。trop2的结合搭档包括ifg-1、claudin-1、claudin-7、周期蛋白d1和pkc(shvartsur a et al.,(2015)genes cancer.6(3-4):84-105)。
2、trop2在正常组织中低水平表达,在例如胚胎器官发育和胎儿生长中起作用,而在所有癌症类型中均发现trop2表达上调,无论正常对应物的基线trop2水平如何(mustatarc et al.,(2013)cell reports.5(2):421-432;guerra e et al.,(2012)plos one.7(11):e49302;trerotola m et al.,(2013)oncogene.32(2):222-233)。研究显示,trop2表达所依赖的一些转录因子与癌症发展相关,例如tp63/tp53l和wilm肿瘤1(wt1),且已证实trop2参与许多与肿瘤发生相关的细胞信号通路。例如,trop2信号通路,通过β-连环蛋白信号通路,来调节细胞的自我更新和增殖,并因而促进癌细胞的干细胞样特性(stoyanova tet al.,(2012)genes dev.26(20):2271-2285)。trop2的过表达促进宫颈癌、卵巢癌、结肠癌和甲状腺癌的肿瘤侵袭,敲降trop2降低癌细胞侵袭(guan h et al.,(2017)bmccancer.17(1):486;liu t et al.,(2013)plos one.8(9):e75864;wu b et al.,(2017)exp ther med.14(3):1947-1952;zhao p et al.,(2018)oncol lett.15(3):3820-3827)。最近,进一步发现trop2信号转导会调节细胞迁移的信号通路。例如,据报道,trop2调节β1整合素的功能,以促进前列腺癌的转移(trerotola m et al.,(2013)cancerres.73(10):3155-3167)。
3、临床上,trop2高表达与例如肝门胆管癌、宫颈癌、和胃癌的不良预后相关。在一项包括2,569例患者的元分析中,trop2表达的增加在统计学上与一些实体瘤的较差总生存期以及无病生存期结果相关(fong d et al.,(2008)br j cancer.99(8):1290-1295;ning set al.,(2013)j gastrointest surg.17(2):360-368;liu t et al.,(2013)plos one.8(9):e75864;zhao w et al.,(2016)oncotarget.7(5):6136-6145;zeng p et al.,(2016)sci rep.6:33658)。trop2作为肿瘤标志物的作用也正在一些临床试验中测试。
4、由于其结构特点以及与癌症的相关性,trop2已成为有吸引力的治疗靶点。已制备出多个trop2抗体,且发现其中一些在异种移植小鼠模型中抑制乳腺癌进展和诱导细胞凋亡(lin h et al.,(2014)int j cancer.134(5):1239-1249)。然而,很可能由于其高内化速率,没有抗体表现出作为裸抗体的治疗价值,直到2015年ikeda等人发现了具有更高结合亲和力和更低内化活性的pr1e11(ikeda m et al.,(2015)biochem biophys rescommun.458(4):877-82)。在后来的研究中,pr1e11经确定在体内诱导有效的抗体依赖性细胞毒性,推测这与较高的细胞表面停留期相关(ikeda m et al.,(2016)anticancerres.36(11):5937-5944)。当前,大多数处于临床前和临床试验中的trop2靶向治疗剂都是抗体-药物偶联物(adc),包括ds-1062a、immu-132和pf-06664178,迄今为止在实体瘤治疗中取得了一些令人鼓舞的结果,且毒性较为有限(zaman s et al.,(2019)同上)。已开发出一种含有强效dna拓扑异构酶i抑制剂(dxd)的新型trop2导向抗体-药物偶联物(adc),datopotamab deruxtecan(dato-dxd,ds-1062a),并已在临床前模型中评估了其抗肿瘤活性和安全性(daisuke okajima et al.,mol cancer ther,2021dec;20(12):2329-2340)。
5、需要另外的具有低内化活性以用作裸抗体、或具有高内化活性以用于adc制备的trop2抗体。
6、本技术中对于任何文件的引用或标识,并不是承认这些文件是本发明的现有技术。
技术实现思路
1、本技术提供分离的单克隆抗体,例如小鼠源、嵌合或人源化的单克隆抗体,或其抗原结合部分,其结合trop2(例如人trop2),与现有技术trop2抗体例如赛妥珠单抗(sacituzumab,immu-132的抗体部分)相比,具有相当的(如果不是更高的话)与人和/或猴trop2的结合亲和力/能力、以及更高或更低的内化活性。
2、本技术的抗体或其抗原结合部分可以用于多种应用,包括体外trop2蛋白检测以及trop2相关疾病(例如癌症)的治疗。
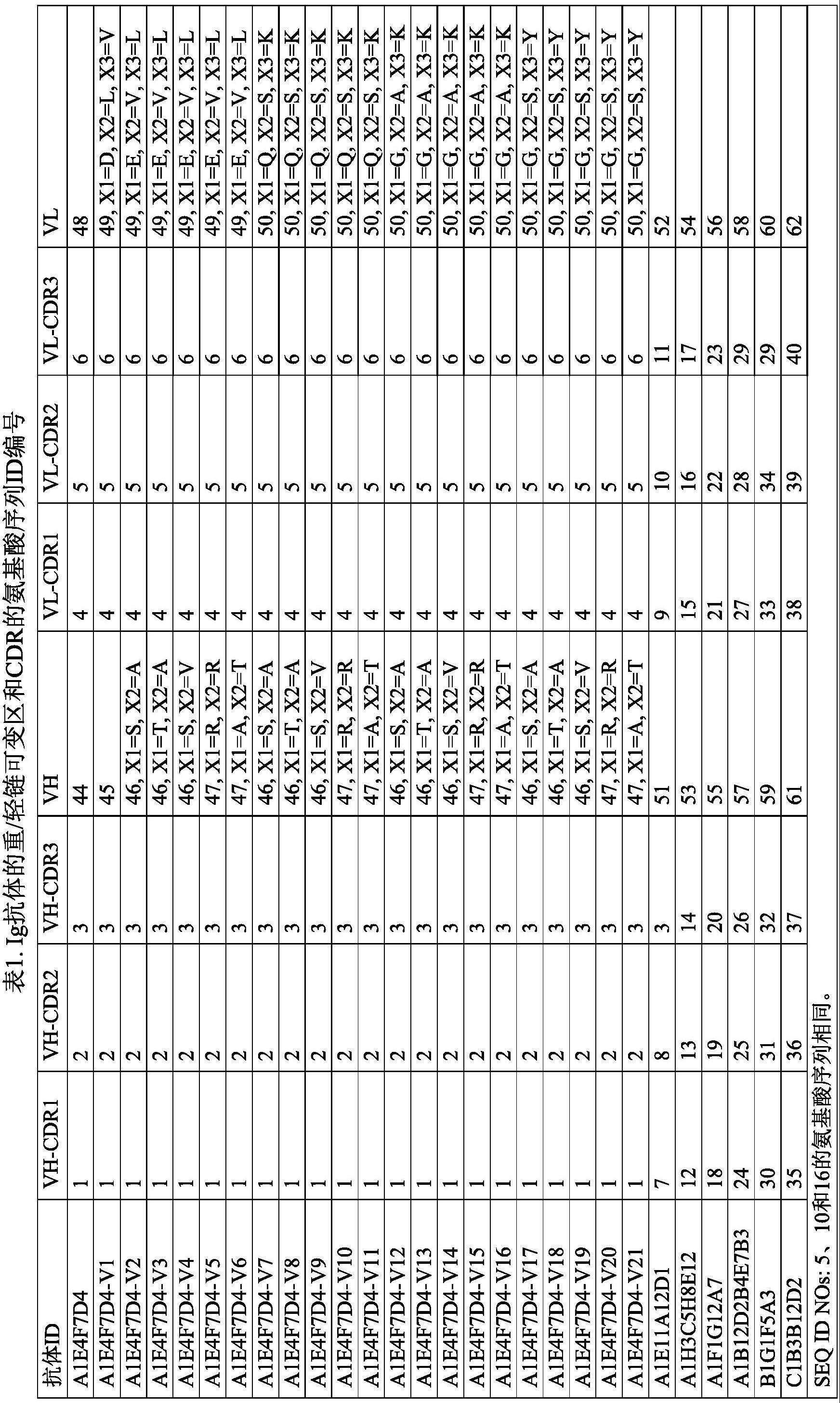
3、因此,在一个方面,本技术涉及结合trop2的分离的单克隆抗体(例如,小鼠源、嵌合或人源化抗体)或其抗原结合部分,其包含(i)重链可变区,其可以包含vh cdr1区、vhcdr2区和vh cdr3区,其中该vh cdr1区、vh cdr2区和vh cdr3区可以分别包含与(1)seq idnos:1、2和3;(2)seq id nos:7、8和3;(3)seq id nos:12、13和14;(4)seq id nos:18、19和20;(5)seq id nos:24、25和26;(6)seq id nos:30、31和32;或(7)seq id nos:35、36和37具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列;和/或ii)轻链可变区,其可以包含vl cdrl区、vlcdr2区和vl cdr3区,其中该vl cdrl区、vl cdr2区和vl cdr3区可以分别包含与(1)seq idnos:4、5和6;(2)seq id nos:9、10和11;(3)seq id nos:15、16和17;(4)seq id nos:21、22和23;(5)seq id nos:27、28和29;(6)seq id nos:33、34和29;或(7)seq id nos:38、39和40具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
4、本技术的分离的单克隆抗体或其抗原结合部分可以包含具有vh cdr1区、vh cdr2区和vh cdr3区的重链可变区,和具有vl cdr1区、vl cdr2区和vl cdr3区的轻链可变区,其中vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3可以分别包含与(1)seq idnos:1、2、3、4、5和6;(2)seq id nos:7、8、3、9、10和11;(3)seq id nos:12、13、14、15、16和17;(4)seq id nos:18、19、20、21、22和23;(5)seq id nos:24、25、26、27、28和29;(6)seqid nos:30、31、32、33、34和29;或(7)seq id nos:35、36、37、38、39和40具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
5、本技术的分离的单克隆抗体或其抗原结合部分可以包含重链可变区,其可以包含与seq id nos:44、45、46(x1=s、x2=a;x1=t、x2=a;x1=s、x2=v)、47(x1=r、x2=r;x1=a、x2=t)、51、53、55、57、59或61具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。seq id nos:44和47(x1=a、x2=t)的氨基酸序列可以分别由seq id nos:41和42的核苷酸序列编码。
6、本技术的分离的单克隆抗体或其抗原结合部分可以包含轻链可变区,其可以包含与seq id nos:48、49(x1=d、x2=l、x3=v;x1=e、x2=v、x3=l)、50(x1=q、x2=s、x3=k;x1=g、x2=a、x3=k;x1=g、x2=s、x3=y)、52、54、56、58、60或62具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。seq id nos:48和50(x1=g、x2=a、x3=k)的氨基酸序列可以分别由seq idnos:43和63的核苷酸序列编码。
7、本技术的分离的单克隆抗体或其抗原结合部分可以包含重链可变区和轻链可变区,重链可变区和轻链可变区可以分别包含与(1)seq id nos:44和48;(2)sew id nos:45和49(x1=d、x2=l、x3=v);(3)seq id nos:46(x1=s、x2=a)和49(x1=e、x2=v、x3=l);(4)seq id nos:46(x1=t、x2=a)和49(x1=e、x2=v、x3=l);(5)seq id nos:46(x1=s、x2=v)和49(x1=e、x2=v、x3=l);(6)seq id nos:47(x1=r、x2=r)和49(x1=e、x2=v、x3=l);(7)seq id nos:47(x1=a、x2=t)和49(x1=e、x2=v、x3=l);(8)seq id nos:46(x1=s、x2=a)和50(x1=q、x2=s、x3=k);(9)seq id nos:46(x1=t、x2=a)和50(x1=q、x2=s、x3=k);(10)seq id nos:46(x1=s、x2=v)和50(x1=q、x2=s、x3=k);(11)seq idnos:47(x1=r、x2=r)和50(x1=q、x2=s、x3=k);(12)seq id nos:47(x1=a、x2=t)和50(x1=q、x2=s、x3=k);(13)seq id nos:46(x1=s、x2=a)和50(x1=g、x2=a、x3=k);(14)seq id nos:46(x1=t、x2=a)和50(x1=g、x2=a、x3=k);(15)seq id nos:46(x1=s、x2=v)和50(x1=g、x2=a、x3=k);(16)seq id nos:47(x1=r、x2=r)和50(x1=g、x2=a、x3=k);(17)seq id nos:47(x1=a、x2=t)和50(x1=g、x2=a、x3=k);(18)seq idnos:46(x1=s、x2=a)和50(x1=g、x2=s、x3=y);(19)seq id nos:46(x1=t、x2=a)和50(x1=g、x2=s、x3=y);(20)seq id nos:46(x1=s、x2=v)和50(x1=g、x2=s、x3=y);(21)seq id nos:47(x1=r、x2=r)和50(x1=g、x2=s、x3=y);(22)seq id nos:47(x1=a、x2=t)和50(x1=g、x2=s、x3=y);(23)seq id nos:51和52;(24)seq id nos:53和54;(25)seq id nos:55和56;(26)seq id nos:57和58;(27)seq id nos:59和60;或(28)seqid nos:61和62具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
8、本技术的分离的单克隆抗体或其抗原结合部分可以包含通过二硫键连接的重链和轻链,重链可以包含重链可变区和重链恒定区,轻链可以包含轻链可变区和轻链恒定区,其中重链可变区的c端与重链恒定区的n端相连,轻链可变区的c端与轻链恒定区的n端相连,其中重链可变区和轻链可变区可以包含上述的氨基酸序列,该抗体或其抗原结合部分与trop2结合。重链恒定区可以是具有增强的fcr结合力的重链恒定区,例如具有seq idno.:64(xi=r、x2=e、x3=m;x1=k、x2=d、x3=l)所示氨基酸序列的人igg1恒定区,或其功能片段。轻链恒定区可以是具有例如seq id no.:65所示氨基酸序列的人κ恒定区,或其功能片段。重链恒定区也可以是基因改造成具有增强的fcr结合亲和力的人igg2或igg4恒定区,或其功能片段。seq id nos:64和65的氨基酸序列可分别由seq id nos:74和75的核苷酸序列编码。
9、在一些实施方式中,本技术的抗体可以包含两条重链和两条轻链,或者由两条重链和两条轻链组成,其中各重链可以包含上述重链恒定区、重链可变区或cdr序列,各轻链可以包含上述轻链恒定区、轻链可变区或cdr序列,其中抗体与trop2结合。本技术的抗体可以是全长抗体,例如igg1、igg2或igg4同种型的。在其他实施方式中,本技术的抗体或其抗原结合部位可以是单链可变片段(scfv)抗体、或抗体片段例如fab或f(ab')2片段。
10、本技术还提供双特异性分子,其可以包含本技术抗体或其抗原结合部分,与具有不同于该抗体或其抗原结合部分的结合特异性的第二功能基团(例如,第二抗体)连接。本技术还提供免疫偶联物,例如抗体-药物偶联物,其可以包含本技术的抗体或其抗原结合部分,与治疗剂例如细胞毒素(例如,sn-38)相连。在另一方面,本技术的抗体或其抗原结合部分可以作为嵌合抗原受体(car)的一部分。还提供免疫细胞,其可以包含抗原嵌合受体,例如t细胞和nk细胞。还提供配备有本技术的抗体或其抗原结合部分的溶瘤病毒。
11、抗体或其抗原结合部分、免疫偶联物、或双特异性分子可以经放射性标记并应用于临床成像,以例如,追踪/检测trop2+肿瘤/癌症的分布,包括转移性trop2+肿瘤/癌症的分布。放射性标记物包括,但不限于,3h。
12、本技术还提供编码本技术抗体或其抗原结合部分、双特异性分子、免疫偶联物、或car的核酸分子,以及可包含该核酸分子的表达载体、和可包含该表达载体的宿主细胞。还提供采用该宿主细胞制备本技术的trop2抗体或其抗原结合部分、双特异性分子、免疫偶联物、或car的方法,其可以包括(i)在该宿主细胞中表达目标分子、以及(ii)从宿主细胞或其细胞培养物中分离目标分子的步骤。
13、还提供药物组合物,其可以包含本技术的抗体或其抗原结合部分、免疫偶联物、双特异性分子、溶瘤病毒、car或car-t细胞、核酸分子、表达载体或宿主细胞,以及药学上可接受的载体。在一些实施方式中,药物组合物还可以包含用于治疗特定疾病的治疗剂,例如抗癌剂。
14、在另一方面,本技术提供一种在有需求的受试者中治疗与trop2(例如,trop2过量表达/信号转导)相关的疾病的方法,其可以包括向受试者施用治疗有效量的本技术药物组合物。疾病可以是肿瘤或癌症。肿瘤可以是实体瘤或非实体瘤,包括,但不限于,乳癌、结直肠癌、胃腺癌、食管癌、肝细胞癌、非小细胞肺癌、小细胞肺癌、卵巢上皮癌、前列腺癌、胰腺导管腺癌、头颈癌、鳞状细胞癌、肾细胞癌、膀胱肿瘤、宫颈癌、子宫内膜癌、滤泡状甲状腺癌、和多形性胶质母细胞瘤。在一些实施方式中,可以进一步施用至少一种其他的抗癌抗体,例如vista抗体、pd-1抗体、pd-l1抗体、lag-3抗体、ctla-4抗体、tim3抗体、stat3抗体、和/或ror1抗体。在某些实施方式中,受试者是人。
15、在另一方面,本技术提供一种在有需求的受试者中进行癌症成像的方法,包括向受试者施用本技术的放射性标记的trop2抗体或其抗原结合部位、免疫偶联物、或双特异性分子。该方法可以用于追踪/检测trop2高表达的肿瘤或癌症的分布,包括,但不限于,食管鳞状细胞癌、结直肠癌、胰腺癌、结肠癌、甲状腺乳头状癌、乳癌、和膀胱癌。在某些实施方式中,受试者是人。
16、基于以下具体描述和实施例,当前公开内容的其他特征和优势之处将会是明晰的,具体描述和实施例不应解读为限制性的。在本技术中引用的所有文献、genbank条目、专利和已公开专利申请的内容通过引用的方式明确地包含在本文中。
17、因而,本技术的目标是不在本技术中包含任何先前已知的产品、制造该产品的工艺或使用该产品的方法,从而申请人保留权利,并在此公开对任何先前已知的产品、过程或方法的弃权声明。需要进一步指出的是,本技术并不打算在本技术的范围内包含任何不符合uspto(35u.s.c.§112,第一段)或epo(epc,第83条)书面描述要件和可实施性要求的产品、工艺、或产品制造方法或产品使用方法,从而申请人保留权利,并在此公开对任何先前描述的产品、产品制备工艺、或产品使用方法的弃权声明。在本发明的实施中,符合epc第53条(c)和epc细则第28条(b)和(c)是有利的。明确保留对本技术同族或任何其他同族或任何第三方在先申请中涉及本技术人任何已授权专利的主题的任何实施方式做出明确的弃权声明的所有权利。本文中的任何内容都不应被解释为承诺。
18、应当注意的是,在本技术中,特别是在权利要求和/或段落中,术语例如“包含”、“包括”等可以具有美国专利法所赋予的意义;例如它们可以表示“包含在内”等;且术语例如“基本由...组成”或“基本由...构成”具有美国专利法所赋予的意义,例如它们允许没有明确表述的元素的存在,但将现有技术中存在的元素、或影响本发明基本或新特性的元素排除在外。
- 还没有人留言评论。精彩留言会获得点赞!