具有增强的针对外切核酸酶的抗性的线性DNA的制作方法
本发明涉及线性双链dna产物,其在每条链中内部位置处包含核酸酶抗性核苷酸。另外,本发明还涉及包含所述线性双链dna产物的复合分子、纳米粒、组合物和文库。还提供了用于产生和使用所述线性双链dna产物的方法。
背景技术:
1、天然核酸在生物环境中易于酶促降解。外切核酸酶通过水解多核苷酸链3’末端或5’末端处的磷酸二酯键从多核苷酸链末端切割单核苷酸。例如,外切核酸酶iii从多核苷酸链的3’末端除去单核苷酸,而外切核酸酶viii以5’至3’方向切割多核苷酸链。同时,在多核苷酸链内的磷酸二酯键被内切核酸酶的作用切割。
2、已经做出了相当大的努力以通过产生能够抵抗胞外和胞内核酸酶消化的核酸类似物来延长核酸的有效分子寿命。提出的解决方案之一包括使用硫代磷酸酯核苷酸(即2’-脱氧核苷酸-5’-(α-硫代)-三磷酸)。
3、硫代磷酸酯核苷酸包含硫原子而不是非桥接氧原子。这些经修饰核苷酸显示出与相应未经修饰核苷酸相当的物理和化学特征,但对外切核酸酶消化具有抗性。因此,并入硫代磷酸酯官能团可延长核酸分子的半衰期。
4、硫代磷酸酯修饰用于核酸药物开发计划。在治疗性核酸中,硫代磷酸酯核苷酸被并入到短的单链多核苷酸链中。例如,反义寡核苷酸福米韦生(fomivirsen)是用于治疗巨细胞病毒视网膜炎的21聚体硫代磷酸酯寡脱氧核苷酸(stein and castanotto,“fda-approved oligonucleotide therapies in 2017.”molecular therapy 25.5(2017):1069-1075)。类似地,哌加他尼(pegaptanib)(商标名macugen)是用于治疗视网膜年龄相关性黄斑变性的具有硫代磷酸酯3’-3’脱氧胸苷帽的短(27个核苷酸)适配体。
5、硫代磷酸酯修饰还已用于在线性双链多核苷酸链(例如双链dna)的背景下对多核苷酸链的末端进行加帽以提高对外切核酸酶消化的抗性(putney et al.“a dna fragmentwith an alpha-phosphorothioate nucleotide at one end is asymmetricallyblocked from digestion by exonuclease iii and can be replicated in vivo.”proceedings of the national academy of sciences 78.12(1981):7350-7354)。为了对多核苷酸链的末端进行加帽,将末端用限制酶消化并用dna聚合酶与脱氧核糖核苷酸三磷酸(deoxyribonucleotide triphosphate,dntp)的混合物处理,至少一种类型的所述脱氧核糖核苷酸三磷酸是与突出链(overhanging strand)中的核苷酸互补的硫代磷酸酯核苷酸。由于dna聚合酶以5’至3’方向添加核苷酸,因此该处理的结果是这样的平端多核苷酸片段,其具有位于每条链的3’末端(即在“帽”中)的硫代磷酸酯核苷酸。
6、美国专利us10350307 b2描述了将硫代磷酸酯核苷酸并入到包含多个串联重复序列的环状双链多联体dna中。美国专利us10350307 b2的多联体dna产物在单个环状产物中提供了表达序列的多个拷贝以产生用于蛋白质表达的改进的系统。美国专利us10350307b2的多联体dna产物的尺寸和多分散性质使其不太适合用于纳米粒产生和/或病毒或非病毒载体的组装。
7、因此,存在适合于rna产生和蛋白质表达的具有增强的对核酸酶消化(例如外切核酸酶消化)的抗性的线性双链dna产物的需要。另外,仍然需要适合于纳米粒产生、和/或病毒或非病毒载体组装以及文库产生的具有增强的对核酸酶消化的抗性的线性双链dna产物。
技术实现思路
1、本发明提供了具有增强的对核酸酶消化的抗性的线性双链dna产物。本发明基于dna产物中核酸酶抗性核苷酸(即受保护核苷酸)的存在。优选地,线性双链dna产物包含一个或更多个对外切核酸酶(例如外切核酸酶iii)消化具有抗性的核苷酸。还更优选地,线性双链dna产物在dna产物的一条链中或每条链中内部位置处包含对外切核酸酶(例如外切核酸酶iii)消化具有抗性的核苷酸。线性双链dna产物可包含盒。盒可包含编码序列。在一条链中或每条链中内部位置处的受保护核苷酸的位置可在盒外。受保护核苷酸的位置确保了盒在外切核酸酶消化(例如外切核酸酶iii消化)时保持完整。外切核酸酶抗性核苷酸(即受保护核苷酸)可以是硫代磷酸酯核苷酸。
2、本发明人已出乎意料地发现了用于产生具有增强的对核酸酶消化的抗性的线性双链dna产物的方法。具体地,线性双链dna产物具有增强的对外切核酸酶消化(例如外切核酸酶iii消化)的抗性。增强的对外切核酸酶消化的抗性延长了线性双链dna产物在细胞中的寿命(即线性双链dna产物具有增强的对胞内外切核酸酶的抗性)和在无细胞系统中的寿命(即线性双链dna产物具有增强的对胞外外切核酸酶的抗性)。另外,本发明人已发现了用于在每条dna链的3’末端和5’末端二者有效引入受保护核苷酸的方法,其提供了免受切割3’末端核苷酸的外切核酸酶(例如外切核酸酶iii)和切割5’末端核苷酸的外切核酸酶(例如外切核酸酶viii)的消化的保护。因此,当与不包含受保护核苷酸的线性双链dna产物相比,本发明的线性双链dna产物具有延长的体内表达。
3、本发明的线性双链dna产物具有另外的有利特性,例如基本上缺乏细菌骨架和/或抗生素抗性基因。缺乏这些特征在例如用于细胞治疗的细胞递送系统(例如病毒载体或纳米粒)的产生中特别有益。缺乏这些特征使得本发明的线性双链dna产物特别适合用于药物组合物。
4、出乎意料的是,本发明人已发现了用于产生具有增强的对核酸酶消化的抗性的线性双链dna产物的方法,其允许有效产生大量具有增强的对外切核酸酶消化的抗性的线性双链dna产物。产物的大规模制备可在无细胞系统中进行,这导致产生包含不含细菌污染物(例如在细胞裂解之后剩余)的线性双链dna产物的纯样品。
5、重要的是,本发明的线性双链dna产物可用于产生改进的细胞递送系统,例如病毒载体或纳米粒。这是因为本技术的发明人已发现了用于产生具有低分散性并且包含目的基因单个拷贝的线性双链dna产物的方式。使用包含目的基因(或目的基因的集合)的一个拷贝的具有低分散性的线性双链dna产物促进了产生均匀的细胞递送系统(即较低分散的细胞递送系统),例如纳米粒,这在提高的细胞摄取和更高的转染效率方面高度有益。
6、1.线性双链dna产物
7、本发明提供了包含有义链和反义链的线性双链dna产物,其中所述线性双链dna产物在每条链中内部位置处包含一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)。
8、内部位置可以是在线性双链dna产物中除在有义链和反义链的3’末端和5’末端上的最后一个核苷酸之外的任何位置。内部位置可位于远离线性双链dna产物的每条链的3’末端和/或5’末端至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、30、40、50、75或100个核苷酸处。内部位置可位于远离线性双链dna产物的每条链的3’末端和/或5’末端至少7个核苷酸处。优选地,内部位置位于远离线性双链dna产物的每条链的3’末端和/或5’末端至少10个核苷酸处。在线性双链dna产物中,内部位置可位于远离有义链的3’末端和5’末端至少7个核苷酸处。优选地,在线性双链dna产物中,内部位置位于远离有义链的3’末端和5’末端至少10个核苷酸处。在线性双链dna产物中,内部位置可位于远离反义链的3’末端和5’末端至少7个核苷酸处。优选地,在线性双链dna产物中,内部位置可位于远离反义链的3’末端和5’末端至少10个核苷酸处。在线性双链dna产物中,内部位置可位于远离每条链的3’末端至少7个核苷酸处。优选地,在线性双链dna产物中,内部位置可位于远离每条链的3’末端至少10个核苷酸处。在线性双链dna产物中,内部位置可位于远离每条链的5’末端至少7个核苷酸处。优选地,在线性双链dna产物中,内部位置可位于远离每条链的5’末端至少10个核苷酸处。
9、线性双链dna产物在靠近dna产物每条链末端的位置处可不包含受保护(例如硫代磷酸酯)核苷酸。受保护(例如硫代磷酸酯)核苷酸可以不是有义和/或反义链的自3’末端和/或5’末端起第1、第2、第3、第4、第5、第6、第7、第8、第9和/或第10个核苷酸。线性双链dna产物可在有义和/或反义链的自3’末端和/或5’末端起第1至3、1至4、1至5、1至6、1至7、1至8、1至9、1至10、1至12、1至14、1至16、1至18或1至20位中的任一者处不包含受保护(例如硫代磷酸酯)核苷酸。优选地,线性双链dna产物在有义和/或反义链的自3’末端和/或5’末端起的第1至9位不包含受保护(例如硫代磷酸酯)核苷酸。线性双链dna产物在有义链的自3’末端和/或5’末端起第1至9位可不包含受保护(例如硫代磷酸酯)核苷酸。线性双链dna产物在反义链的自3’末端和/或5’末端起第1至9位可不包含受保护(例如硫代磷酸酯)核苷酸。例如,在有义链中的第一受保护(例如硫代磷酸酯)核苷酸可以是从有义链的5’末端开始计数的第6个核苷酸。例如,在反义链中的第一受保护(例如硫代磷酸酯)核苷酸可以是从反义链的3’末端开始计数的第10个核苷酸。第一受保护(例如硫代磷酸酯)核苷酸在每条链中的位置可以不同。例如,线性双链dna产物可在从有义链的3’末端开始计数的第8位处和从反义链的3’末端开始计数的第12位处包含第一受保护(例如硫代磷酸酯)核苷酸。类似地,线性双链dna产物可包含受保护(例如硫代磷酸酯)核苷酸,其位于从有义链的3’末端开始计数的第8位、从有义链的5’末端开始计数的第6位、从反义链的3’末端开始计数的第12位以及从反义链的5’末端开始计数的第7位处。第一受保护(例如硫代磷酸酯)核苷酸在每条链中的位置可以是相同的。例如,线性双链dna产物可在从有义链的3’末端开始计数的第8位和从反义链的3’末端开始计数的第8位处包含第一受保护(例如硫代磷酸酯)核苷酸。线性双链dna产物可包含第一受保护(例如硫代磷酸酯)核苷酸,其是从有义和/或反义链的3’末端和/或5’末端开始计数的第6、第8或第10个核苷酸。线性双链dna产物在从有义和/或反义链的3’末端和/或5’末端开始计数的第1至6位处可不包含第一受保护(例如硫代磷酸酯)核苷酸。因此,内部位置可以是在线性双链dna产物内除在有义链和反义链的3’末端和5’末端的最后6、8或10个核苷酸之外的任何位置。线性双链dna产物可包含第一受保护(例如硫代磷酸酯)核苷酸,其是从有义和/或反义链的3’末端和/或5’末端开始计数的第7个核苷酸。优选地,线性双链dna产物可包含第一受保护(例如硫代磷酸酯)核苷酸,其是从有义和/或反义链的3’末端和/或5’末端开始计数的第10个核苷酸。
10、本文中所述的线性双链dna产物可包含盒。因此,本发明还提供了包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含一个或更多个受保护(例如硫代磷酸酯)核苷酸。
11、本文中使用的术语“单个盒”在线性双链dna产物的背景下旨在涵盖不包含多盒或不由多盒组成的线性双链dna产物。换言之线性双链dna产物仅包含单个盒,所述单个盒可包含目的基因的单个编码序列。单个盒可不包含多个串联重复序列和/或多联体dna或者不由多个串联重复序列和/或多联体dna组成。例如,本文中所述的线性双链dna产物可不包含通过已知方法产生的多联体dna或者不由通过已知方法产生的多联体dna组成,例如如在美国专利us10350307 b2中所述。本文中使用的术语“单个盒”旨在涵盖目的dna序列的单个拷贝,例如编码序列的单个拷贝。因此,“单个盒”可不涵盖这样的盒,其包含串联连接的相同dna序列的多个拷贝或由串联连接的相同dna序列的多个拷贝组成。单个盒可包含目的基因的集合。例如,单个盒可包含至少二、三、四或五个目的基因的序列。目的基因在单个盒中可以不相同。
12、盒可包含编码序列。编码序列可编码目的基因,例如编码蛋白质的基因。对于蛋白质表达,可将包含编码序列的盒连接到包含启动子的至少一部分的载体或质粒中,使得启动子的一部分与编码序列可操作地连接(例如启动子可在编码序列的上游)。载体或质粒还可包含成簇规则间隔短回文重复(clustered regularly interspaced shortpalindromic repeat,crispr)系统的指导rna(guide rna,grna)。盒可包含启动子和编码序列的至少一部分。盒可包含启动子和编码序列。盒可包含启动子、编码序列、核糖体结合位点和翻译终止序列。盒可另外包含辅助蛋白质表达的序列,例如帽非依赖性翻译元件。盒可包含(或编码)修复模板(或编辑模板)。修复模板(或编辑模板)可用于crispr-cas介导的同源定向修复(homology directed repair,hdr)。盒可编码crispr指导rna。盒可以是哺乳动物表达盒。启动子可以是cmv启动子。盒还可包含增强子。盒还可包含报道基因,例如egfp报道基因或萤光素酶报道基因。盒还可包含同聚序列,例如polya、polyc、polyt或polyg序列。同聚序列的长度可为3至200个核苷酸。同聚序列可用于促进盒的纯化,在这种情况下,同聚序列的长度可为4至12个核苷酸,或长度可为5至10个核苷酸。同聚序列可用于提高mrna表达,在这种情况下,同聚序列的长度可为10至200个核苷酸,优选长度为80至150个核苷酸。同聚序列的长度可为至少10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190或200个核苷酸。优选地,同聚序列的长度为至少100个核苷酸。还更优选地,同聚序列的长度为至少120个核苷酸。例如,同聚序列可包含具有至少120个核苷酸的polya序列。
13、受保护(例如硫代磷酸酯)核苷酸在线性双链dna产物中的位置可使得盒被保护免受核酸酶(例如外切核酸酶iii)消化。因此,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
14、(a)盒的5’末端核苷酸;
15、(b)盒的3’末端核苷酸;和
16、(c)盒外的一个或更多个核苷酸。
17、本文中使用的术语“盒的5’末端核苷酸”旨在涵盖盒的每条链的5’末端核苷酸。因此,在线性双链dna产物中,盒通常包含有义链的5’末端核苷酸和反义链的5’末端核苷酸。
18、本文中使用的术语“盒的3’末端核苷酸”旨在涵盖盒的每条链的3’末端核苷酸。因此,在线性双链dna产物中,盒通常包含有义链的3’末端核苷酸和反义链的3’末端核苷酸。
19、本文中使用的术语“盒外”旨在涵盖不是盒的一部分的任何核苷酸。这包括包含于线性双链dna产物中并且还不构成盒的一部分的任何核苷酸。术语“盒外n个核苷酸”或“远离盒的n个核苷酸”旨在描述位于从盒末端朝向线性双链dna产物末端的n个核苷酸的核苷酸。例如,术语“盒外2个核苷酸”在核苷酸的内部位置的背景下意指描述在盒外并且远离盒的最后一个核苷酸两个核苷酸的核苷酸。例如,在序列:5’-aaaaaacataaaa(seq id no:1)中,其中盒从核苷酸“t”开始(以5’至3’方向),术语“盒外2个核苷酸”是指“c”核苷酸。因此,术语“盒外至少2个核苷酸”或“远离盒至少2个核苷酸”意指描述在盒外并且远离盒的最后一个核苷酸至少两个核苷酸的核苷酸。在以上实例中,“远离盒至少2个核苷酸”的核苷酸将是选自5’-aaaaaac的任何核苷酸。类似地,术语“远离盒的5’末端至少2个核苷酸”意指描述在盒外并且远离盒的5’末端的最后一个核苷酸至少两个核苷酸的核苷酸。在以上实例中,在盒的5’末端的最后一个核苷酸是“t”,并且“远离盒的5’末端至少2个核苷酸”的核苷酸将是选自5’-aaaaaac的任何核苷酸。
20、内部位置可不位于盒的第二个与倒数第二个核苷酸之间。内部位置可以是在线性双链dna产物中除在有义链和反义链的3’末端和5’末端上的最后一个核苷酸之外和除位于盒的第二个与倒数第二个核苷酸之间的核苷酸之外的任何位置。内部位置可位于盒外并且远离线性双链dna产物的每条链的3’末端和/或5’末端至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、30、40、50、75或100个核苷酸和/或远离盒的每条链的3’末端和/或5’末端(即盒外)至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、30、40、50、75或100个核苷酸。优选地,内部位置位于盒外并且远离线性双链dna产物的每条链的3’末端和/或5’末端至少6个、至少8个或至少10个核苷酸和/或远离盒的每条链的3’末端和/或5’末端至少6个、至少8个或至少10个核苷酸(即盒外至少6个、至少8个或至少10个核苷酸)。优选地,盒在远离盒的3’末端和/或5’末端(即盒外)的有义链和/或反义链的第1至2、1至3、1至4、1至5、1至6、1至7、1至8、1至9、1至10、1至12、1至14、1至16、1至18或1至20位中任一者处不包含硫代磷酸酯核苷酸。优选地,每条链中的内部位置位于远离线性双链dna产物的末端至少6个核苷酸处并且不位于盒的第二个与倒数第二个核苷酸之间。优选地,每条链中的内部位置位于远离线性双链dna产物的末端至少10个核苷酸处并且不位于盒的第二个与倒数第二个核苷酸之间。优选地,每条链中的内部位置位于远离线性双链dna产物的末端至少6个核苷酸并且远离盒的末端至少6个核苷酸(即,盒外至少6个核苷酸)处。优选地,每条链中的内部位置位于远离线性双链dna产物的末端至少10个核苷酸并且远离盒的末端至少10个核苷酸(即,盒外至少10个核苷酸)处。线性双链dna产物可在内部位置处包含第一硫代磷酸酯核苷酸,所述内部位置是除在有义链和反义链的3’末端和5’末端上的最后一个核苷酸之外的位置,只要该位置位于盒外至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、30、40或50个核苷酸即可。例如,线性双链dna产物可包含第一硫代磷酸酯核苷酸,其是从有义和/或反义链的3’末端和/或5’末端计数的至少第6、第8或第10个核苷酸,只要这些位置不位于盒的第二个与倒数第二个核苷酸之间即可。优选地,线性双链dna产物可包含第一硫代磷酸酯核苷酸,其是从有义和/或反义链的3’末端和/或5’末端计数的至少第6、第8或第10个核苷酸,只要这些位置位于盒外即可。线性双链dna产物可包含第一硫代磷酸酯核苷酸,其是从有义和/或反义链的3’末端和/或5’末端计数的至少第6、第8或第10个核苷酸,只要这些位置位于盒外至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、30、40或50个核苷酸即可。优选地,线性双链dna产物可包含第一硫代磷酸酯核苷酸,其是从有义和/或反义链的3’末端和/或5’末端计数的至少第6、第8或第10个核苷酸,只要这些位置位于盒外至少6、8或10个核苷酸即可。
21、线性双链dna产物可在每条链中内部位置处包含至少2、3、4、5、6、7、8、9或10个受保护(例如硫代磷酸酯)核苷酸。优选地,线性双链dna产物在每条链中内部位置处包含至少2个受保护(例如硫代磷酸酯)核苷酸。
22、本发明提供了包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个核酸酶抗性核苷酸(即受保护核苷酸),其中在每条链中内部位置处的至少两个核酸酶抗性核苷酸选自:
23、(a)盒的5’末端核苷酸;
24、(b)盒的3’末端核苷酸;和
25、(c)盒外的一个或更多个核苷酸;并且
26、其中盒包含编码序列。
27、本发明提供了包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
28、(a)盒的5’末端核苷酸;
29、(b)盒的3’末端核苷酸;和
30、(c)盒外的一个或更多个核苷酸;并且
31、其中盒包含编码序列。
32、线性双链dna产物可对核酸酶消化具有抗性,或者可具有提高的或增强的对核酸酶消化的抗性。线性双链dna产物可对外切核酸酶消化具有抗性,或者具有提高的或增强的对外切核酸酶消化的抗性。线性双链dna产物可对通过切割3’末端核苷酸的外切核酸酶(例如外切核酸酶iii)和/或切割5’末端核苷酸的外切核酸酶(例如外切核酸酶viii)的消化具有抗性,或者具有提高的或增强的对通过切割3’末端核苷酸的外切核酸酶(例如外切核酸酶iii)和/或切割5’末端核苷酸的外切核酸酶(例如外切核酸酶viii)的消化的抗性。术语“提高的”或“增强的”在对酶消化的抗性的背景下是指当与不通过本文中所述的方法产生的dna产物相比时,对酶消化的更高抗性。例如,当与不包含受保护核苷酸(例如硫代磷酸酯核苷酸)的产物相比时。
33、硫代磷酸酯核苷酸在线性双链dna产物的有义链中的位置可使得一个或更多个硫代磷酸酯核苷酸位于盒的上游(即朝向dna产物的有义链的5’末端)。
34、在线性双链dna产物的有义链中:
35、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸;和/或
36、(b)至少两个硫代磷酸酯核苷酸中的一个可在有义链的第一区中,其中有义链的第一区在盒的5’。
37、硫代磷酸酯核苷酸在线性双链dna产物的有义链中的位置可使得一个或更多个硫代磷酸酯核苷酸位于盒的下游(即朝向dna产物的有义链的3’末端)。
38、在线性双链dna产物的有义链中:
39、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸;和/或
40、(b)至少两个硫代磷酸酯核苷酸中的一个可在有义链的第二区中,其中有义链的第二区在盒的3’。
41、硫代磷酸酯核苷酸在线性双链dna产物的反义链中的位置可使得一个或更多个硫代磷酸酯核苷酸位于盒的上游(即朝向dna产物的反义链的5’末端)。
42、在线性双链dna产物的反义链中:
43、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸;和/或
44、(b)至少两个硫代磷酸酯核苷酸中的一个可在反义链的第一区中,其中反义链的第一区在盒的5’。
45、硫代磷酸酯核苷酸在线性双链dna产物的反义链中的位置可使得一个或更多个硫代磷酸酯核苷酸位于盒的下游(即朝向dna产物的反义链的3’末端)。
46、在线性双链dna产物的反义链中:
47、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸;和/或
48、(b)至少两个硫代磷酸酯核苷酸中的一个可在反义链的第二区中,其中反义链的第二区在盒的3’。
49、硫代磷酸酯核苷酸在线性双链dna产物的有义链和反义链二者中的位置可使得至少一个硫代磷酸酯核苷酸位于盒的下游,并且至少一个硫代磷酸酯核苷酸位于每条链中盒的上游。
50、在线性双链dna产物中:
51、(a)在有义链中,至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸,和/或至少两个硫代磷酸酯核苷酸中的一个可在有义链的第一区中,其中有义链的第一区在盒的5’;
52、(b)在有义链中,至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,和/或至少两个硫代磷酸酯核苷酸中的一个可在有义链的第二区中,其中有义链的第二区在盒的3’;
53、(c)在反义链中,至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸,和/或至少两个硫代磷酸酯核苷酸中的一个可在反义链的第一区中,其中反义链的第一区在盒的5’;和
54、(d)在反义链中,至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,和/或至少两个硫代磷酸酯核苷酸中的一个可在反义链的第二区中,其中反义链的第二区在盒的3’。
55、本文中使用的术语“有义链的第一区”旨在涵盖线性双链dna产物的有义链的一部分,所述一部分在线性双链dna产物的5’末端与有义链中盒的第一个5’核苷酸之间。例如,在有义链序列:5’-aaaaaacataaaa-3’(seq id no:1)中,其中盒以5’至3’方向从核苷酸“t”开始,术语“有义链的第一区”是指5’-aaaaaaca-3’区。
56、术语“反义链的第一区”旨在涵盖线性双链dna产物的反义链的一部分,所述一部分在线性双链dna产物的5’末端与反义链中盒的第一个5’核苷酸之间。例如,在反义链序列:5’-aaaaaacataaaa-3’(seq id no:1)中,其中盒以5’至3’方向从核苷酸“t”开始,术语“反义链的第一区”是指5’-aaaaaaca-3’区。
57、术语“有义链的第二区”旨在涵盖线性双链dna产物的有义链的一部分,所述一部分在线性双链dna产物的3’末端与有义链中盒的第一个3’核苷酸之间。例如,在有义链序列:5’-aaaaaacataaaa-3’(seq id no:1)中,其中盒以3’至5’方向从核苷酸“t”开始,术语“有义链的第二区”是指5’-aaaa-3’区。
58、术语“反义链的第二区”旨在涵盖线性双链dna产物的反义链的一部分,所述一部分在线性双链dna产物的3’末端与反义链中盒的第一个3’核苷酸之间。例如,在反义链序列:5’-aaaaaacataaaa-3’(seq id no:1)中,其中盒以3’至5’方向从核苷酸“t”开始,术语“反义链的第二区”是指5’-aaaa-3’区。
59、线性双链dna产物可在盒上游(即朝向dna产物的有义链的5’末端)包含多个硫代磷酸酯核苷酸。例如,线性双链dna产物可在盒上游包含至少2、3、4、5、6、7、8、9或10个硫代磷酸酯核苷酸。优选地,在盒上游的至少2个硫代磷酸酯核苷酸。因此,硫代磷酸酯核苷酸在线性双链dna产物的有义链中的位置可使得至少两个硫代磷酸酯核苷酸位于盒的上游。
60、在线性双链dna产物的有义链中:
61、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在有义链的第一区中,其中有义链的第一区在盒的5’;或者
62、(b)至少两个硫代磷酸酯核苷酸可在有义链的第一区中,其中有义链的第一区在盒的5’。
63、线性双链dna产物可在盒下游(即朝向dna产物的3端)包含多个硫代磷酸酯核苷酸。例如,线性双链dna产物可在盒下游包含至少2、3、4、5、6、7、8、9或10个硫代磷酸酯核苷酸,优选在盒下游的至少2个硫代磷酸酯核苷酸。因此,硫代磷酸酯核苷酸在线性双链dna产物的有义链中的位置可使得至少两个硫代磷酸酯核苷酸位于盒的下游。
64、在线性双链dna产物的有义链中:
65、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在有义链的第二区中,其中有义链的第二区在盒的3’;或者
66、(b)至少两个硫代磷酸酯核苷酸可在有义链的第一区中,其中有义链的第一区在盒的3’。
67、硫代磷酸酯核苷酸在线性双链dna产物的反义链中的位置可使得至少两个硫代磷酸酯核苷酸位于盒的上游(即朝向dna产物的反义链的5’末端)。
68、在线性双链dna产物的反义链中:
69、(a)至少两个硫代磷酸酯核苷酸中的一个是盒的5’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个在反义链的第一区中,其中反义链的第一区在盒的5’;或者
70、(b)至少两个硫代磷酸酯核苷酸在反义链的第一区中,其中反义链的第一区在盒的5’。
71、硫代磷酸酯核苷酸在线性双链dna产物的反义链中的位置可使得至少两个硫代磷酸酯核苷酸位于盒的下游(即朝向dna产物的反义链的3’末端)。
72、在线性双链dna产物的反义链中:
73、(a)至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在反义链的第二区中,其中反义链的第二区在盒的3’;或者
74、(b)至少两个硫代磷酸酯核苷酸可在反义链的第二区中,其中反义链的第二区在盒的3’。
75、线性双链dna产物的每条链可包含多个硫代磷酸酯核苷酸。例如,线性双链dna产物可在盒上游和下游包含至少2、3、4、5、6、7、8、9或10个硫代磷酸酯核苷酸。硫代磷酸酯核苷酸在线性双链dna产物的有义链和反义链二者中的位置可使得至少两个硫代磷酸酯核苷酸位于盒的下游,并且至少两个硫代磷酸酯核苷酸位于每条链中的盒的上游。
76、在线性双链dna产物中:
77、(a)在有义链中:
78、i.至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在有义链的第一区中,其中有义链的第一区在盒的5’;或者
79、ii.至少两个硫代磷酸酯核苷酸可在有义链的第一区中,其中有义链的第一区在盒的5’;
80、(b)在有义链中:
81、i.至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在有义链的第二区中,其中有义链的第二区在盒的3’;或者
82、ii.至少两个硫代磷酸酯核苷酸可在有义链的第二区中,其中有义链的第二区在盒的3’;
83、(c)在反义链中:
84、i.至少两个硫代磷酸酯核苷酸中的一个可以是盒的5’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在反义链的第一区中,其中反义链的第一区在盒的5’;或者
85、ii.至少两个硫代磷酸酯核苷酸可在反义链的第一区中,其中反义链的第一区在盒的5’;并且
86、(d)在反义链中:
87、i.至少两个硫代磷酸酯核苷酸中的一个可以是盒的3’末端核苷酸,并且至少两个硫代磷酸酯核苷酸中的一个可在反义链的第二区中,其中反义链的第二区在盒的3’;或者
88、ii.至少两个硫代磷酸酯核苷酸可在反义链的第二区中,其中反义链的第二区在盒的3’。
89、线性双链dna产物可对核酸酶消化具有抗性,或者可具有提高的或增强的对核酸酶消化的抗性。线性双链dna产物可对3’末端外切核酸酶消化(例如通过外切核酸酶iii)和/或5’末端外切核酸酶消化(例如通过外切核酸酶viii)具有抗性。线性双链dna产物可在5’末端或5’末端区域包含受保护核苷酸(例如硫代磷酸酯核苷酸)。优选地,线性双链dna产物任选地在每条链中的5’末端或5’末端区域包含硫代磷酸酯核苷酸。线性双链dna产物可在每条链中的5’末端处或5’末端区域包含硫代磷酸酯核苷酸。由于大多数外切核酸酶,例如外切核酸酶iii,从多核苷酸链的3’末端除去核苷酸,因此线性双链dna产物可在3’末端或在3’末端区域包含受保护核苷酸。优选地,线性双链dna产物任选地在每条链中在3’末端或3’末端区域包含硫代磷酸酯核苷酸。线性双链dna产物可在3’末端或3’末端区域包含至少一个硫代磷酸酯核苷酸以及在5’末端或5’末端区域包含至少一个硫代磷酸酯核苷酸。线性双链dna产物可在每条链的3’末端或3’末端区域以及5’末端或5’末端区域包含硫代磷酸酯核苷酸。
90、硫代磷酸酯核苷酸可为不同类型。例如,线性双链dna产物可在3’末端或3’末端区域包含一个或更多个α-s-datp(即2’-脱氧腺苷-5’-(α-硫代)-三磷酸)以及在5’末端或5’末端区域包含一个或更多个α-s-dgtp(即2’-脱氧鸟苷-5'-(α-硫代)-三磷酸)。或者,在线性双链dna产物中的所有硫代磷酸酯核苷酸可为相同类型。例如,线性双链dna产物可在3’末端或3’末端区处包含一个或更多个α-s-datp以及在5’末端或5’末端区域包含一个或更多个α-s-datp。
91、线性双链dna产物可以是至少100、200、300、400、500、600、700、800、900、1000、2000、3000、4000、5000、6000、7000、8000、9000、10000、11000、12000、13000、14000或15000个碱基对长。优选地,线性双链dna产物为至少500或至少1000个碱基对长。
92、线性双链dna产物可在每条链中内部位置处包含多个硫代磷酸酯核苷酸。例如,线性双链dna产物可在每条链中内部位置处包含至少2、4、6、8、10、12、14、16、18、20、30、40、50、60、70、80、90、100、125、150、175、200、250、300、350、400、450或500个硫代磷酸酯核苷酸。优选地,线性双链dna产物在每条链中内部位置处包含至少2个硫代磷酸酯核苷酸。
93、在每条链中内部位置处的硫代磷酸酯核苷酸的量可取决于线性双链dna产物的长度。因此,线性双链dna产物可包含硫代磷酸酯核苷酸与总核苷酸之比为以下的硫代磷酸酯核苷酸:至少0.0001、至少0.0025、至少0.01至少0.025、至少0.05、至少0.075、至少0.10、至少0.12、至少0.15、至少0.25、至少0.35、至少0.5或至少0.75。线性双链dna产物可包含硫代磷酸酯核苷酸与总核苷酸之比为以下的硫代磷酸酯核苷酸:小于1、小于0.9、小于0.8、小于0.65、小于0.5、小于0.4、小于0.3、小于0.2、小于0.1、小于0.075或小于0.05。线性双链dna产物可包含硫代磷酸酯核苷酸与总核苷酸之比为以下的硫代磷酸酯核苷酸:0.0001至1、0.0025至0.75、0.025至0.65、0.025至0.15或0.25至0.50。优选地,硫代磷酸酯核苷酸与总核苷酸之比为0.025至0.15。线性双链dna产物可包含硫代磷酸酯核苷酸与总核苷酸之比为以下的硫代磷酸酯核苷酸:0.005至0.3、0.0075至0.2、0.01至0.15、0.01至0.10、0.02至0.08、0.03至0.07、0.04至0.06或0.05至0.075。优选地,硫代磷酸酯核苷酸与总核苷酸之比为0.01至0.10。优选地,硫代磷酸酯核苷酸与总核苷酸之比为约0.02、约0.025、约0.05、约0.075、约0.08、约0.10、约0.12、约0.15或约0.25。还更优选地,硫代磷酸酯核苷酸与总核苷酸之比为约0.025或约0.05。如在实施例中所示的,硫代磷酸酯核苷酸与总核苷酸之比为约0.025则足以提供增强的对外切核酸酶消化的抗性。如在实施例中所示的,硫代磷酸酯核苷酸与总核苷酸之比为约0.05或约0.075则在提供增强的对外切核酸酶消化的抗性中特别有效(如由表达水平所示的;参见实施例7和8)。此外,如在实施例中所示.比率为约0.05则特别适合于目的基因的体内表达(参见实施例10)。
94、在每条链中内部位置处的硫代磷酸酯核苷酸的量可以不同。例如,如果线性双链dna产物包含总共1000个核苷酸,并且硫代磷酸酯核苷酸与总核苷酸之比为0.1,则线性双链dna产物包含100个硫代磷酸酯核苷酸,其中75个可位于有义链中并且25个位于dna产物的反义链中。例如,在线性双链dna产物中100%的硫代磷酸酯核苷酸可位于有义链中。或者,在线性双链dna产物中100%的硫代磷酸酯核苷酸可位于反义链中。在线性双链dna产物中,有义链可包含硫代磷酸酯核苷酸总数目的至少90%、80%、70%、60%、50%、40%、30%、20%或10%。在线性双链dna产物中,反义链可包含硫代磷酸酯核苷酸总数目的至少90%、80%、70%、60%、50%、40%、30%、20%或10%。有义链和反义链可包含相等数目的硫代磷酸酯核苷酸。优选地,在线性双链dna产物中,有义链和反义链各自包含硫代磷酸酯核苷酸总数目的50%。
95、线性双链dna产物可包含突出端。例如,线性双链dna产物可包含5’突出端或3’突出端。线性双链dna产物可包含一个平端或更多个平端。线性双链dna产物可包含:5’突出端和平端、两个5’突出端、3’突出端和平端、两个3’突出端、或者5’突出端和3’突出端。
96、突出端可具有至少3个核苷酸(优选4至8个核苷酸)。突出端可在线性双链dna产物的有义链或反义链中。
97、有义链可具有这样的3’突出端,其具有至少1个核苷酸、至少2个核苷酸、2至8个核苷酸、2至7个核苷酸、2至6个核苷酸、2至5个核苷酸、2至4个核苷酸、2至3个核苷酸、3至8个核苷酸、3至7个核苷酸、3至6个核苷酸、3至5个核苷酸、3至4个核苷酸、4至8个核苷酸、4至7个核苷酸、4至6个核苷酸、4至5个核苷酸、5至8个核苷酸、6至8个核苷酸、6至7个核苷酸或7至8个核苷酸。优选地,有义链具有这样的3’突出端,其具有4至8个核苷酸。
98、有义链可具有这样的5’突出端,其具有至少1个核苷酸、至少2个核苷酸、2至8个核苷酸、2至7个核苷酸,2至6个核苷酸、2至5个核苷酸、2至4个核苷酸、2至3个核苷酸、3至8个核苷酸、3至7个核苷酸、3至6个核苷酸、3至5个核苷酸、3至4个核苷酸、4至8个核苷酸、4至7个核苷酸、4至6个核苷酸、4至5个核苷酸、5至8个核苷酸、6至8个核苷酸、6至7个核苷酸或7至8个核苷酸。优选地,有义链具有这样的5’突出端,其具有4至8个核苷酸。
99、反义链可具有这样的3’突出端,其具有至少1个核苷酸、至少2个核苷酸、2至8个核苷酸、2至7个核苷酸、2至6个核苷酸、2至5个核苷酸、2至4个核苷酸、2至3个核苷酸、3至8个核苷酸、3至7个核苷酸、3至6个核苷酸、3至5个核苷酸、3至4个核苷酸、4至8个核苷酸、4至7个核苷酸、4至6个核苷酸、4至5个核苷酸、5至8个核苷酸、6至8个核苷酸、6至7个核苷酸或7至8个核苷酸。优选地,反义链具有这样的3’突出端,其具有4至8个核苷酸。
100、反义链可具有这样的5’突出端,其具有至少1个核苷酸、至少2个核苷酸、2至8个核苷酸、2至7个核苷酸,2至6个核苷酸、2至5个核苷酸、2至4个核苷酸、2至3个核苷酸、3至8个核苷酸、3至7个核苷酸、3至6个核苷酸、3至5个核苷酸、3至4个核苷酸、4至8个核苷酸、4至7个核苷酸、4至6个核苷酸、4至5个核苷酸、5至8个核苷酸、6至8个核苷酸、6至7个核苷酸或7至8个核苷酸。优选地,反义链具有这样的5’突出端,其具有4至8个核苷酸。
101、本领域技术人员将理解,有义链和反义链的突出端可以是上述突出端长度的任何组合。在线性双链dna产物中的突出端不需要具有相同的长度。在线性双链dna产物中的突出端可具有相同的长度。
102、在线性双链dna产物中的每个突出端和/或平端可包含一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)。有义链的突出端和/或平端可包含一个或更多个受保护核苷酸。反义链的突出端和/或平端可包含一个或更多个受保护核苷酸。在每条链中的5’突出端、3’突出端和/或平端可包含一个或更多个受保护核苷酸。优选地,5’突出端包含一个或更多个硫代磷酸酯核苷酸。优选地,3’突出端包含一个或更多个硫代磷酸酯核苷酸。优选地,5’突出端、3’突出端和/或平端包含一个或更多个硫代磷酸酯核苷酸。还更优选地,在线性双链dna产物中的每个突出端和/或平端包含一个或更多个硫代磷酸酯核苷酸。在线性双链dna产物中的每个突出端和/或平端可包含至少两个受保护(例如硫代磷酸酯)核苷酸。有义链的突出端和/或平端可包含至少两个受保护核苷酸。反义链的突出端和/或平端可包含至少两个受保护核苷酸。在线性双链dna产物中的每个突出端和/或平端可包含至少三个、四个或五个受保护(例如硫代磷酸酯)核苷酸。有义链的突出端和/或平端可包含至少三个、四个或五个受保护核苷酸。反义链的突出端和/或平端可包含至少三个、四个或五个受保护核苷酸。5’突出端和/或3’突出端可包含至少2、3、4或5个受保护核苷酸。优选地,5’突出端和/或3’突出端包含至少2个受保护核苷酸,例如硫代磷酸酯核苷酸。还更优选地,每个突出端和/或平端包含至少2个受保护核苷酸,例如硫代磷酸酯核苷酸。
103、本文中使用的术语“硫代磷酸酯核苷酸”是指具有改变的磷酸骨架的核苷酸,其中,糖部分通过硫代磷酸酯键连接。在寡核苷酸序列的磷酸骨架中,硫代磷酸酯键包含硫原子作为非桥接氧原子的替代物。该修饰使得核苷酸间键联对核酸酶降解具有抗性。
104、本文中使用的术语“受保护核苷酸”或“核酸酶抗性核苷酸”旨在涵盖提供或增强对核酸酶消化(尤其是外切核酸酶消化)的抗性的任何类型的分子。尽管线性双链dna产物在本文中主要描述为包含硫代磷酸酯核苷酸,但本领域技术人员将理解,线性双链dna产物可替代地包含提供对核酸酶消化(例如外切核酸酶iii消化)的抗性的任何分子。例如,线性双链dna产物可包含核酸酶抗性核苷酸,即提供或提高对核酸酶(例如外切核酸酶)的抗性的经修饰核苷酸。线性双链dna产物可包含提供或提高对核酸酶(例如外切核酸酶)消化的抗性的肽、多肽或蛋白质。线性双链dna产物可包含2’-o-甲基核苷酸或2’-o-甲氧基乙基(moe)核苷酸。
105、本发明提供了包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒和在每条链中内部位置处的至少两个moe核苷酸,其中在每条链中内部位置处的至少两个moe核苷酸选自:
106、(a)盒的5’末端核苷酸;
107、(b)盒的3’末端核苷酸;和
108、(c)盒外的一个或更多个核苷酸;并且
109、其中盒包含编码序列。
110、对外切核酸酶消化具有抗性的核苷酸(即受保护核苷酸)可以是至少一种类型的硫代磷酸酯核苷酸。例如,至少一种类型的硫代磷酸酯核苷酸是α-s-datp(即2’-脱氧腺苷-5’-(α-硫代)-三磷酸)、α-s-dctp(即2’-脱氧胞苷-5’-(α-硫代)-三磷酸)、α-s-dgtp(即2’-脱氧鸟苷-5’-(α-硫代)-三磷酸)、α-s-dttp(即2’-脱氧胸苷-5’-(α-硫代)-三磷酸)、α-s-dutp(即2’-脱氧尿苷-5’-(α-硫代)-三磷酸)和/或尿苷2,3’-硫代环磷酸酯(uridine 2’,3’-cyclophosphorothioate),优选α-s-datp、α-s-dgtp或α-s-dttp。
111、线性双链dna产物可包含至少两种类型的硫代磷酸酯核苷酸。例如,至少两种类型的硫代磷酸酯核苷酸是:α-s-datp和α-s-dctp、α-s-datp和α-s-dgtp、α-s-datp和α-s-dttp、α-s-dctp和α-s-dgtp、α-s-dctp和α-s-dttp或者α-s-dgtp和α-s-dttp。
112、线性双链dna产物可包含至少三种类型的硫代磷酸酯核苷酸。例如,至少三种类型的硫代磷酸酯核苷酸是:
113、(a)α-s-datp、α-s-dctp和α-s-dgtp;
114、(b)α-s-datp、α-s-dctp和α-s-dttp;
115、(c)α-s-datp、α-s-dgtp和α-s-dttp;或者
116、(d)α-s-dctp、α-s-dgtp和α-s-dttp。
117、线性双链dna产物可包含至少四种类型的硫代磷酸酯核苷酸。例如,至少四种类型的受保护核苷酸是α-s-datp、α-s-dctp、α-s-dgtp和α-s-dttp。
118、硫代磷酸酯核苷酸可以是sp-异构体、rp-异构体或sp-与rp-异构体二者的混合物。
119、对外切核酸酶消化具有抗性的核苷酸(即受保护核苷酸)可以是至少一种类型,或者至少两种、三种或四种类型的moe核苷酸。例如,moe核苷酸可以是2’-o-甲氧基-乙基鸟苷、2’-o-甲氧基-乙基胞苷、2’-o甲氧基-乙基腺苷和/或2’-o-甲氧基-乙基胸苷。
120、在线性双链dna产物中受保护核苷酸的并入的量可基于本领域已知的方法确定。例如,可进行引物延伸测定以评估受保护核苷酸相比于未受保护核苷酸的并入率。例如,通过聚合酶的模板/引物分子的单核苷酸延伸可在存在提高浓度的与模板的第一碱基互补的受保护和未受保护核苷酸的情况下进行评价。在线性(非饱和)条件下的并入效率可用于确定与天然未受保护核苷酸相比受保护核苷酸的并入程度。
121、2.复合分子
122、线性双链dna产物还可包含功能部分。
123、本发明提供了复合分子,其包含本文中所述的线性双链dna产物和功能部分。任选地,功能部分是结合分子或探针。
124、本发明提供了复合分子,其包含:
125、(a)线性双链dna产物,所述线性双链dna产物包含有义链和反义链,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸;和
126、(b)功能部分。
127、优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
128、i.盒的5’末端核苷酸;
129、ii.盒的3’末端核苷酸;和
130、iii.盒外的一个或更多个核苷酸。
131、本发明还提供了复合分子,其包含:
132、(a)线性双链dna产物,所述线性双链dna产物包含有义链和反义链,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
133、i.盒的5’末端核苷酸;
134、ii.盒的3’末端核苷酸;和
135、iii.盒外的一个或更多个核苷酸;并且
136、其中盒包含编码序列;和
137、(b)功能部分。
138、功能部分可在多核苷酸链的3’和/或5’末端(或端区)处。功能部分可与线性双链dna产物的5’突出端、3’突出端和/或平端连接或结合。功能部分可通过共价键或非共价键或者通过核酸杂交与线性双链dna产物的5’突出端、3’突出端和/或平端连接或结合。功能部分可直接或间接(例如通过接头分子)与线性双链dna产物连接或结合。功能部分可通过与线性双链dna产物结合和/或通过与接头分子结合或退火来连接或结合,所述接头分子与线性双链dna产物结合。接头分子可以是生物聚合物(例如核酸分子)或合成聚合物。接头分子可包含一个或更多个乙二醇和/或聚(乙)二醇(例如六-乙二醇或五-乙二醇)单元。
139、线性双链dna产物可包含两个功能部分;在多核苷酸链的3’末端处的第一功能部分和在多肽链的5’末端处的第二功能部分。第一功能部分可与线性双链dna产物的5’突出端、3’突出端和/或3’末端的平端连接或结合。第二功能部分可与线性双链dna产物的5’突出端、3’突出端和/或5’末端的平端连接或结合。两个功能部分可相同或不同。例如,第一功能部分可以是促进dna产物的检测和/或测序的条码(barcode),第二功能部分可以是核靶向序列。
140、功能部分可以是探针。本文中使用的术语“探针”是指可变长度(例如3至1000个碱基长)的dna、rna或dna/rna嵌合体的片段,其用于检测与探针中序列互补的靶核苷酸序列的存在。通常来说,探针与这样的单链核酸杂交:所述单链核酸的碱基序列允许由于在探针与靶标之间的互补性引起的探针-靶标碱基配对。因此,功能部分可以是dna序列、rna序列或dna/rna嵌合体序列。本文中使用的术语“互补”是指根据watson/crick配对规则的核苷酸序列的配对。例如,序列5′-gcggtccca-3′的互补序列为5′-tgggaccgc-3′。互补序列还可以是与dna序列互补的rna序列。
141、功能部分可以是结合分子。术语“结合分子”是指能够与本文中所述的线性双链dna产物结合和/或能够与另外的分子或靶标结合的任何分子。结合分子可以是蛋白质、多肽或肽。结合分子可以是抗体,例如单克隆抗体或多克隆抗体。结合分子可以是抗体片段。
142、功能部分可通过与捕获分子(例如通过蛋白质-蛋白质相互作用结合的捕获抗体)结合来促进dna产物的检测。功能部分可与细胞靶标(例如细胞受体)结合。
143、功能部分可以是标签。因此,本发明的线性双链dna产物的有义链可在5’末端或3’末端处包含标签以用于检测。作为替代或补充,本发明的线性双链dna产物的反义链可包含在5’末端或3’末端处的标签以用于检测。“标签”可以是使得能够通过物理、化学和/或生物方式检测双链核酸分子的任何化学实体。标签可以是发色团、荧光团和/或放射性分子。
144、功能部分可以是靶向序列。靶向序列可以是用于将dna产物靶向至细胞中的特定位置的可变长度的dna或rna片段。靶向序列可用于由于增强的dna产物核输入而提高的非病毒基因递送的转染效率。例如,靶向序列可以是dna核靶向序列(即针对内源性dna结合蛋白质的识别序列),例如sv40增强子序列(优选在盒的下游)。
145、为促进dna产物的检测和/或定量,功能部分可包含荧光团、放射性化合物或条码。
146、可使用条码来测量与线性双链dna产物的存在、不存在和/或水平相对应的信号。条码可包含至少一个与条码化部分连接的结合部分,其中条码化部分包含至少一个核苷酸(即其中条码化部分包含长度为至少一个核苷酸的核苷酸序列),并且其中结合部分能够与线性双链dna产物的3’突出端、5’突出端或平端结合。结合部分能够与线性双链dna产物的3’和/或5’末端结合。可通过确定条码的条码化部分的存在、不存在和/或水平(例如通过测序或pcr)来测量信号。条码化部分可包含至少2、3、4、5、6、7、8、9或10个核苷酸。条码可包含至少2个结合部分(例如第一结合部分和第二结合部分)。例如,与第一条码化部分连接的第一结合部分可与线性双链dna产物的3’末端连接,并且与第二条码化部分连接的第二结合部分可与线性双链dna产物的5’末端连接。3’末端和5’末端可包含3’突出端、5’突出端或平端。
147、可使用荧光团(即经荧光标记的分子)来测量与dna产物的存在、不存在和/或水平相对应的信号,所述荧光团与线性双链dna产物的3’突出端、5’突出端或平端连接或结合。可通过流式细胞术和/或荧光激活细胞分选来测量信号。
148、功能部分还可促进dna测序。例如,功能部分可以是测序衔接子。术语“测序衔接子”旨在涵盖一个或更多个核酸结构域,所述核酸结构域包含由以下目的测序平台使用的核酸序列(或其互补序列)的至少一部分:例如由提供的测序平台(例如hiseqtm、miseqtm和/或genome analyzertm测序系统)、oxford nanoporetm technologies(例如minion测序系统)、ion torrenttm(例如ion pgmtm和/或ion protontm测序系统)、pacificbiosciences(例如pacbio rs ii测序系统);life technologiestm(例如solid测序系统)、roche(例如454gs flx+和/或gs junior测序系统)或任何其他的目的测序平台。
149、3.递送颗粒
150、任何或所有的线性双链dna产物或复合分子均可通过递送颗粒(例如纳米粒)递送至细胞。
151、本发明提供了特别适合用于基因治疗的纳米粒(或纳米粒文库)。本发明提供了线性双链dna产物、复合分子、纳米粒、组合物或文库,其用于基因治疗。
152、纳米粒(或纳米粒文库)可用于通过递送编码治疗性蛋白质的dna产物或通过递送可用于基因编辑的dna产物(例如crispr系统的基因)来治疗疾病。因此,纳米粒可用作递送系统以用于多种应用。递送可在体外或在体内。
153、治疗性基因的有效细胞内化是用于基因递送的纳米粒的成功临床应的关键过程。因此,本发明提供了用于细胞内化的纳米粒(或纳米粒文库)。
154、本发明提供了包含本文中所述的线性双链dna产物、复合分子或文库的纳米粒。因此,本发明提供了包含线性双链dna产物的纳米粒,所述线性双链dna产物包含有义链和反义链,其中所述线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
155、(a)盒的5’末端核苷酸;
156、(b)盒的3’末端核苷酸;和
157、(c)盒外的一个或更多个核苷酸。
158、本发明还提供了包含线性双链dna产物的纳米粒,所述线性双链dna产物包含有义链和反义链,其中所述线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
159、(a)盒的5’末端核苷酸;
160、(b)盒的3’末端核苷酸;和
161、(c)盒外的一个或更多个核苷酸;并且
162、其中盒包含编码序列。
163、本发明还提供了纳米粒文库,其中每个纳米粒包含线性双链dna产物,并且其中线性双链dna产物具有低分散性。术语“低分散性”在纳米粒(或纳米粒文库)的背景下旨在涵盖具有基本上相同尺寸(即多核苷酸链中碱基的数目)的线性双链dna产物。换言之,相对于纳米粒文库中其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%,优选小于5%。这些dna产物导致形成均匀纳米粒或均匀纳米粒的集合(即文库)。相反,包含多分散性dna产物的纳米粒(例如,如通过在美国专利us10350307 b2中描述的方法产生的)将具有不同的尺寸和形状(即较高的分散性)。纳米粒的均匀性(和/或低分散性)对转化和/或转染特别有益,并且在内化和药物释放过程中发挥关键作用。
164、本发明还提供了纳米粒文库,其包含如本文中所述的线性双链dna产物的文库。
165、纳米粒可包含线性双链dna产物的至少一个拷贝。纳米粒可包含线性双链dna产物的至少2、3、4、5、6、7、8、9、10个拷贝。纳米粒文库中的每个纳米粒可包含线性双链dna产物的至少一个拷贝。纳米粒文库中的每个纳米粒可包含线性双链dna产物的至少2、3、4、5、6、7、8、9、10个拷贝。纳米粒文库中的每个纳米粒可包含线性双链dna产物的相同量的拷贝。纳米粒文库中的每个纳米粒可包含线性双链dna产物的3个拷贝。纳米粒文库中的每个纳米粒可包含线性双链dna产物的4个拷贝。纳米粒文库中的每个纳米粒可不包含线性双链dna产物的多于10个拷贝。纳米粒文库中的每个纳米粒可不包含多联体dna产物。纳米粒文库中的每个纳米粒可不包含含有多个盒的线性双链dna产物。
166、纳米粒可包含复合分子的至少一个拷贝。纳米粒可包含复合分子的至少2、3、4、5、6、7、8、9、10个拷贝。纳米粒文库中的每个纳米粒可包含复合分子的至少一个拷贝。纳米粒文库中的每个纳米粒可包含复合分子的至少2、3、4、5、6、7、8、9、10个拷贝。纳米粒文库中的每个纳米粒可包含复合分子的相同量的拷贝。纳米粒文库中的每个纳米粒可包含复合分子的3个拷贝。纳米粒文库中的每个纳米粒可包含复合分子的4个拷贝。纳米粒文库中的每个纳米粒可以不包含复合分子的多于10个拷贝。
167、文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个纳米粒。例如,文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个纳米粒/ml。
168、纳米粒可以是自组装的纳米粒。优选地,纳米粒可以是可在微流体装置上制造的颗粒。优选地,纳米粒基于例如在天然带电荷的dna分子与带正电荷的阳离子脂质或肽之间的静电相互作用组装。例如,纳米粒可基于自组装生物黏附性聚合物,其可应用于线性双链dna产物的经口递送、静脉内递送和/或经鼻递送。例如,纳米粒可将dna产物递送至癌细胞以阻止肿瘤生长。
169、可通过本领域已知的方法来产生纳米粒。例如,可通过双乳液溶剂蒸发方法将本文中所述的线性双链dna产物或本文中所述的复合分子包封在聚(乳酸-共-乙醇酸)纳米粒中来产生纳米粒。可用阳离子组分(例如生物相容性壳聚糖或环糊精)对纳米粒进一步改进。
170、可通过乙醇负载形成过程来产生纳米粒。在该过程中,在酸性ph(优选ph=4)的水性缓冲液中,将溶解于乙醇中的脂质与本文中所述的线性双链dna产物或本文中所述的复合分子快速混合。在该自组装过程中,静电相互作用驱动了包含dna产物或复合分子或者基本上由dna产物或复合分子组成的反向胶束的形成。
171、纳米粒可以是基于脂质的纳米粒、lnp(脂质纳米粒)、聚合物纳米粒、基于pei的纳米粒、脂质聚合复合物纳米粒(lipopolyplex nanoparticle)(聚合物与脂质的混合物)或固体纳米粒(例如金纳米粒)。
172、优选地,纳米粒(或纳米粒文库)能够转染如本文中所述的细胞。优选地,所述细胞是人细胞。
173、本文中所述的纳米粒(或纳米粒文库)适合用于基因治疗。例如,纳米粒(或纳米粒文库)可用于控制的基因递送过程。纳米粒可以是金纳米粒、纳米金刚石(nanodiamond)或多孔硅纳米粒。适合于基因治疗的纳米粒可以是具有良好稳定性、易于表面功能化和/或易于尺寸控制的任何类型的纳米粒。金纳米粒由于其无毒特性而特别合适。纳米粒可以是基于脂质的纳米粒。
174、基于脂质的纳米粒由于其高生物相容性和与脂质膜的紧密相似性而特别适合于基因递送。与其他已知的纳米粒相比,基于脂质的纳米粒通常具有改善的细胞透性。纳米粒可以是大的单层囊泡纳米粒。例如,已表明lnp对于将sirna递送至肝是高度有效的(tabernero et al.,cancer discovery,2013年4月,第3卷,第4号,第363至470页),并因此被考虑用于将本文中所述的dna产物和复合分子递送至肝。
175、美国专利申请20110293703涉及可用于施用多核苷酸的lipidoid化合物,其可用于递送本发明的dna产物和复合分子。例如,将氨基醇lipidoid化合物与待递送至细胞或对象的药剂组合以形成微粒、纳米粒、脂质体或胶束。待由微粒、纳米粒、脂质体或胶束递送的药剂可以为气体、液体或固体的形式,并且药剂可以是多核苷酸、蛋白质、肽或小分子。氨基醇lipidoid化合物可与其他氨基醇lipidoid化合物、聚合物、表面活性剂、胆固醇、蛋白质、脂质等组合以形成纳米粒。然后,这些纳米粒可任选地与药物赋形剂组合以形成药物组合物。
176、球形核酸(spherical nucleic acid,sna)构建体和其他纳米粒(例如金纳米粒)还适合作为将dna产物和/或复合分子递送至预期靶标的方式。大量数据表明,基于核酸功能化金纳米粒的aurasense therapeutics球形核酸(snatm)构建体优于基于多种关键成功因素的替代平台,所述因素例如:1)高体内稳定性(由于它们的密集负载,大多数载物(dna产物或复合分子)仍然与细胞内的构建体结合,赋予核酸稳定性和对酶促降解的抗性);2)递送性(对于所研究的所有细胞类型(例如神经元、肿瘤细胞系等),在不需要载体或转染剂的情况下,构建体显示出99%的转染效率);3)治疗性靶向(构建体的独特的靶标结合亲和力和特异性允许对于所匹配靶序列的高特异性);4)优异的效力;5)低毒性;6)无显著的免疫应答;以及7)化学可调整性。
177、具有dna产物或复合分子的自组装纳米粒可用聚乙烯亚胺(polyethyleneimine,pei)构建,所述聚乙烯亚胺与arg-gly-asp(rgd)肽聚乙二醇化并在聚乙二醇(polyethylene glycol,peg)远端处连接。纳米复合物可通过混合等体积的阳离子聚合物和核酸的水溶液来制备,以产生净摩尔过量的在2至6的范围内的可电离氮(聚合物)与磷酸(核酸)。阳离子聚合物与核酸之间的静电相互作用可导致形成平均粒径分布为约100nm的聚合复合物,因此这里称为纳米复合物。
178、纳米粒可包含生物相容性纳米载体。例如,纳米粒可包含聚(β-氨基酯)、低分子量聚乙烯亚胺、聚磷酸酯、二硫交联的聚合物和聚酰胺胺。与常规的基因递送机制相比,这些纳米载体显示出改善的纳米粒制剂稳定性和安全性。
179、纳米粒可与另外的组分连接。例如,另外的组分可确保纳米粒在基因治疗中的特异性和选择性。例如,纳米粒可与肽连接。肽可改善纳米粒的靶向能力,降低生物毒性并改善治疗作用。纳米粒可与脂质体(优选融合脂质体)连接。纳米粒可另外地或替代地与归巢肽的外鞘(outer sheath)连接。
180、纳米粒可以是磁性纳米粒。纳米粒可以是基于肽的纳米粒。纳米粒可以是适合于基因治疗的纳米材料的一部分。例如,纳米材料可包含小分子、纳米粒和聚合物。
181、纳米粒可包含在此所述的线性双链dna产物,其与功能部分连接或结合。因此,纳米粒可包含如本文中所述的复合分子。复合分子的功能部分可促进纳米粒的检测。检测可在体内或体外进行。例如,功能部分可以是荧光标记,其可在体内跟踪或在体外成像。
182、功能部分可以是探针或靶向序列。靶向序列可以是可变长度的dna或rna的片段,其用于将dna产物靶向至细胞中的特定位置。靶向序列可用于由于增强的dna产物核输入而提高的非病毒基因递送的转染效率。
183、功能部分可以是结合分子。功能部分可以是蛋白质或肽。功能部分可以是抗体或酶。功能部分可通过与捕获分子(例如通过蛋白质-蛋白质相互作用结合的捕获抗体)结合来促进纳米粒的检测。功能部分可与细胞靶标(例如,细胞受体)结合。
184、为了促进纳米粒的检测和/或定量,功能部分可包含荧光团、放射性化合物或条码。
185、可使用条码来测量与纳米粒中线性双链dna产物的存在、不存在和/或水平相对应的信号。条码可包含至少一个与条码化部分连接的结合部分,其中条码化部分包含至少一个核苷酸(即其中条码化部分包含长度为至少一个核苷酸的核苷酸序列),并且其中结合部分能够与线性双链dna产物的3’突出端、5’突出端或平端结合。结合部分能够与线性双链dna产物的3’和/或5’末端结合。可通过确定条码的条码化部分的存在、不存在和/或水平(例如通过测序或pcr)来测量信号。条码化部分可包含至少2、3、4、5、6、7、8、9或10个核苷酸。条码可包含至少2个结合部分(例如第一结合部分和第二结合部分)。例如,与第一条码化部分连接的第一结合部分可与线性双链dna产物的3’末端连接,并且与第二条码化部分连接的第二结合部分可与线性双链dna产物的5’末端连接。3’末端和5’末端可包含3’突出端、5’突出端或平端。
186、可使用荧光团(即经荧光标记的分子)来测量与纳米粒中dna产物的存在、不存在和/或水平相对应的信号,所述荧光团与线性双链dna产物的3’突出端、5’突出端或平端连接或结合。可通过流式细胞术和/或荧光激活细胞分选来测量信号。
187、4.文库
188、本发明提供了文库,其包含至少两种本文中所述的线性双链dna产物或至少两种本文中所述的复合分子。因此,本发明提供了包含至少两种线性双链dna产物的文库,其中每种线性双链dna产物均包含有义链和反义链,其中每种线性双链dna产物均包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处处的一个或更多个硫代磷酸酯核苷酸可选自:
189、(a)盒的5’末端核苷酸;
190、(b)盒的3’末端核苷酸;和
191、(c)盒外的一个或更多个核苷酸。
192、本发明提供了包含至少两种线性双链dna产物的文库,其中每种线性双链dna产物均包含有义链和反义链,其中每种线性双链dna产物均包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
193、(a)盒的5’末端核苷酸;
194、(b)盒的3’末端核苷酸;和
195、(c)盒外的一个或更多个核苷酸;并且
196、其中盒包含编码序列。
197、文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个线性双链dna产物。例如,文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个线性双链dna产物/ml。优选地,文库包含至少1010个线性双链dna产物(或分子)。例如,文库包含至少1010个线性双链dna产物(或分子)/ml。文库可包含106至1016个线性双链dna产物,优选1013至1016个线性双链dna产物。文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个复合分子。例如,文库可包含至少2、3、4、5、10、15、20、30、40、50、60、70、80、90、100、103、104、105、106、107、108、109、1010、1011、1012、1013、1014、1015、1016或1017个复合分子/ml。优选地,文库包含至少1010个复合分子。例如,文库包含至少1010个复合分子/ml。文库可包含106至1016个复合分子,优选1013至1016个复合分子。每个线性双链dna产物或复合分子可编码不同的目的基因或相同的目的基因(或相同目的基因的集合)。
198、线性双链dna产物或复合分子的文库可以是单分散的。线性双链dna产物或复合分子的文库可具有低分散性。术语“单分散性”和“低分散性”在文库的背景下旨在涵盖具有基本上相同尺寸(即多核苷酸链中碱基的数目)的线性双链dna产物或复合分子。dna产物或复合分子的单分散的文库(或具有低分散性的文库)可用于例如纳米粒的形成。这是因为起始物质(即线性双链dna产物或复合分子)的分散性越低,所产生的纳米粒的分散性就越低(且均匀性越高)。
199、在文库中,相对于文库中其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%,优选小于5%。在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%。优选地,在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)变化小于5%。
200、在文库中,相对于文库中其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%,优选小于5%。在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%。优选地,在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)变化小于5%。
201、在文库中,相对于文库中其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于1000、500、250、100或50个核苷酸,优选小于50个核苷酸。在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于500个核苷酸。在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于250个核苷酸。在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于100个核苷酸。优选地,在文库中,相对于文库中至少1010个其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)变化小于50个核苷酸。
202、在文库中,相对于文库中其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于1000、500、250、100或50个核苷酸,优选小于50个核苷酸。在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于500个核苷酸。在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于250个核苷酸。在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于100个核苷酸。优选地,在文库中,相对于文库中至少1010个其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)变化小于50个核苷酸。
203、文库中的大多数线性双链dna产物或复合分子可具有基本上相同的尺寸(即多核苷酸链中碱基的数目)。换言之,文库可包含至少80%、85%、90%、95%或100%的基本上相同尺寸(即多核苷酸链中碱基的数目)的线性双链dna产物。例如,在1010个线性双链dna产物的文库中,至少90%(即至少109个)线性双链dna产物可具有基本上相同的尺寸(即多核苷酸链中碱基的数目)。文库可包含至少80%、85%、90%、95%或100%的具有基本上相同尺寸(即多核苷酸链中碱基的数目)的复合分子。例如,在1010个复合分子的文库中,至少90%(即至少109个)复合分子可具有基本上相同的尺寸(即多核苷酸链中碱基的数目)。
204、在文库中,相对于文库中至少80%、85%、90%、95%或100%的其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%,优选小于5%。在文库中,相对于文库中至少90%的其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)可变化小于10%。优选地,在文库中,相对于文库中至少90%的其他线性双链dna产物,各线性双链dna产物的尺寸(即多核苷酸链中碱基的数目)变化小于5%。
205、在文库中,相对于文库中至少80%、85%、90%、95%或100%的其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于30%、20%或10%,优选小于5%。在文库中,相对于文库中至少90%的其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)可变化小于10%。优选地,在文库中,相对于文库中至少90%的其他复合分子,各复合分子的尺寸(即多核苷酸链中碱基的数目)变化小于5%。
206、文库的线性双链dna产物或复合分子可基本上相同。换言之,文库中的各线性双链dna产物或复合分子基本上相同,即包含相同或基本上相同的多核苷酸序列。例如,文库可包含具有至少80%、85%、90%、92%、94%、96%、97%、98%、99%或100%序列相似性的线性双链dna产物。例如,文库可包含具有至少80%、85%、90%、92%、94%、96%、97%、98%、99%或100%序列相似性的复合分子。例如,文库可包含具有至少80%、85%、90%、92%、94%、96%、97%、98%、99%或100%序列同一性的线性双链dna产物。例如,文库可包含具有至少80%、85%、90%、92%、94%、96%、97%、98%、99%或100%序列同一性的复合分子。优选地,文库包含具有至少95%序列相似性的线性双链dna产物。还更优选地,文库包含具有至少95%序列同一性的线性双链dna产物。优选地,文库包含具有至少95%序列相似性的复合分子。还更优选地,文库包含具有至少95%序列同一性的复合分子。
207、尽管文库中的各线性双链dna产物或复合分子可基本上相同(即可包含相同或基本上相同的多核苷酸序列),但文库中一些(或所有)线性双链dna产物或复合分子中的受保护核苷酸(例如硫代磷酸酯核苷酸)的位置和/或分布可不同。
208、在线性双链dna产物的文库中,至少80%、85%、90%、95%、96%、97%、98%、99%或100%的线性双链dna产物可具有不同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。优选地,文库中至少99%的线性双链dna产物具有不同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。换言之,文库中至少80%、85%、90%、95%、96%、97%、98%、99%或100%的线性双链dna产物可不具有与文库中任何其他线性双链dna产物相同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。优选地,文库中至少99%的线性双链dna产物不具有与文库中任何其他线性双链dna产物相同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。
209、在复合分子的文库中,至少80%、85%、90%、95%、96%、97%、98%、99%或100%的复合分子可具有不同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。优选地,文库中至少99%的复合分子具有不同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。换言之,文库中至少80%、85%、90%、95%、96%、97%、98%、99%或100%的复合分子可不具有与文库中任何其他复合分子相同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。优选地,文库中至少99%的复合分子不具有与文库中任何其他复合分子相同的受保护核苷酸(例如硫代磷酸酯核苷酸)分布。
210、本文中使用的表述“不同的受保护核苷酸分布”意指涵盖不具有所有受保护核苷酸分布相同的线性双链dna产物或复合分子。例如,在第2、3、7和8位处包含受保护核苷酸的分子与在第2、3、7和9位处包含受保护核苷酸的分子具有不同的受保护核苷酸分布。
211、文库中的各线性双链dna产物可为至少100、200、300、400、500、600、700、800、900、1000、2000、3000、4000、5000、6000、7000、8000、9000、10000、11000、12000、13000、14000或15000个碱基对长。优选地,文库中的各线性双链dna产物为至少500或至少1000个碱基对长。
212、文库中的各复合分子可为至少100、200、300、400、500、600、700、800、900、1000、2000、3000、4000、5000、6000、7000、8000、9000、10000、11000、12000、13000、14000或15000个碱基对长。优选地,文库中的各复合分子为至少500或至少1000个碱基对长。
213、文库中复合分子的功能部分可相同或不同。例如,文库可包含具有不同功能部分并且与复合分子的线性双链dna产物部分的序列具有至少80%、85%、90%、92%、94%、96%、97%、98%、99%或100%序列同一性或相似性的复合分子。
214、本发明的文库可用于筛选在细胞过程以及疾病中的基因功能。文库可用于基因测序。
215、本发明还提供了这样的文库,其包含通过本文中所述的方法产生的经转染细胞的群体。细胞可包含本发明的线性双链dna产物或复合分子。例如,细胞可包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。
216、细胞可包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
217、(a)盒的5’末端核苷酸;
218、(b)盒的3’末端核苷酸;和
219、(c)盒外的一个或更多个核苷酸;并且
220、其中盒包含编码序列。
221、5.组合物
222、本发明还提供了组合物,其包含本文中所述的线性双链dna产物、复合分子、纳米粒或文库。组合物可以是药物组合物。组合物或药物组合物还可包含可药用稀释剂。
223、本发明提供了组合物,其包含本文中所述的线性双链dna产物。因此,本发明提供了组合物,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
224、(a)盒的5’末端核苷酸;
225、(b)盒的3’末端核苷酸;和
226、(c)盒外的一个或更多个核苷酸。
227、本发明还提供了组合物,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
228、(a)盒的5’末端核苷酸;
229、(b)盒的3’末端核苷酸;和
230、(c)盒外的一个或更多个核苷酸;并且
231、其中盒包含编码序列。
232、可药用稀释剂可以是盐水、缓冲溶液(例如缓冲水溶液)或另外的赋形剂。
233、例如,组合物可配制为与一种或更多种可药用固体载体组合的丸剂、片剂或胶囊剂,或者配制为在一种或更多种可药用溶剂中的溶液剂,或者配制为在一种或更多种可药用溶剂或载体中的乳剂、混悬剂或分散体。制剂还可包含另一些可药用赋形剂,例如稳定剂、抗氧化剂、黏合剂、着色剂或乳化剂或味道改变剂和延长释放制剂。
234、组合物可经口、表面、肠胃外或经皮或通过吸入施用。可使用合适的无菌溶液通过注射或静脉内输注来施用组合物。表面剂型可以是适合于经皮和表面剂型的乳膏剂、软膏剂、贴剂或类似载剂。
235、组合物可溶解或混悬于液体载剂中,或者配制为颗粒剂(小颗粒或晶粒(grain))、丸粒剂(在有或没有赋形剂的情况下,由高度纯化的组合物组成的小的无菌固体块,其通过形成颗粒剂或通过压缩和成型制成)、或经包衣延长释放的丸粒剂(其中组合物本身为已施加不同量的包衣的颗粒剂形式的固体剂型,并且其以这样的方式释放组合物:与呈现为常规剂型的组合物相比,允许降低给药频率)。
236、另一些形式包括丸剂(包含旨在经口施用的组合物的小、圆的固体剂型)、散剂(干燥、细碎的组合物与一种或更多种可药用添加剂的紧密混合物,其旨在可内部或外部使用)、酏剂(包含经溶解的组合物的透明、有令人愉快的风味、甜的水醇液体;其旨在经口使用)、口香糖(chewing gum)(多种形状的甜的和矫味的不溶性塑料物质,其在被咀嚼时将组合物释放到口腔中)、糖浆剂(包含组合物和高浓度的蔗糖或其他糖的经口溶液剂;所述术语还用于包括在甜且黏的载剂中制备的任何其他液体剂型,包括经口混悬剂)、片剂(包含组合物、有或没有合适的稀释剂的固体剂型)、可咀嚼片剂(包含组合物、有或没有合适的稀释剂的固体剂型,其旨在用于咀嚼,在口腔中产生令人愉快的味道残留,易于吞咽且不留下苦涩或不愉快的余味)、包衣片剂或延迟释放片剂、分散片剂、泡腾片剂、延长释放片剂、膜包衣片剂、或膜包衣延长释放片剂,其中所述片剂以这样的方式配制:使得所包含的组合物在摄入之后在延长的时间段内可用。
237、在其他形式中,可提供用于溶液剂的片剂、用于混悬剂的片剂、多层片剂、延长释放多层片剂,其中所述片剂以这样的方式配制:与呈现为常规剂型的组合物相比,使得允许至少降低给药频率。经口崩解片剂、延迟释放经口崩解片剂、可溶性片剂、糖包衣片剂、渗透片剂等也是合适的。
238、除组合物之外,经口剂型组合物还可包含一种或更多种非活性药物成分,例如稀释剂、增溶剂、醇类、黏合剂、控制释放聚合物、肠溶聚合物、崩解剂、赋形剂、着色剂、矫味剂、甜味剂、抗氧化剂、防腐剂、颜料(pigment)、添加剂、填充剂、助悬剂、表面活性剂(例如,阴离子的、阳离子的、两性的和非离子的)等。多种经fda批准的表面非活性成分存在于fda的“非活性成分数据库(the inactive ingredients database)”中,其包含如由制造商特别指定的非活性成分。
239、本文中使用的可注射和输注剂型包括但不限于脂质体可注射剂型,其由脂质体(通常由磷脂构成的脂质双层囊泡,用于包封组合物)组成或形成脂质体;注射剂,其包含旨在肠胃外使用的无菌制剂;乳剂注射剂,其包含旨在肠胃外施用的由无菌、无热原制剂组成的乳剂;或脂质复合物注射剂。
240、例如,本文中所述的线性双链dna产物、复合分子、纳米粒或文库可通过鼓室内注射(例如注射到中耳中)和/或注射到外耳、中耳和/或内耳中来施用。这样的方法是在本领域中常规使用的,例如,用于将类固醇和抗生素施用到人耳中。例如,可通过耳的圆窗或通过耳蜗囊进行注射。
241、其他形式包括用于溶液注射剂的散剂,其是旨在重构以形成用于肠胃外使用的溶液的无菌制剂;用于混悬注射剂的散剂,其是旨在重构以形成用于肠胃外使用的混悬液的无菌制剂;用于脂质体混悬注射剂的冻干散剂,其是旨在重构以用于肠胃外使用的无菌冷冻干燥制剂,所述无菌冷冻干燥制剂已以允许在重构时形成脂质体(通常由磷脂构成的脂质双层囊泡,用于将组合物包封在脂质双层内或水性空间中)的方式配制;或者用于溶液注射剂的冻干散剂,其中冻干(“冷冻干燥”)是涉及在极低压力下从冷冻状态下的产物中除去水的过程。
242、混悬注射剂包含适合于注射的液体制剂,其由分散在整个液相中的固体颗粒组成(所述颗粒在液相中不可溶),还可还由分散在整个水相中的油相组成,反之亦然。混悬脂质体注射剂包含适合于注射的液体制剂,其由以形成脂质体(通常由磷脂构成的脂质双层囊泡,用于将组合物包封在脂质双层内或水性空间中)的这样的方式分散在整个水相中的油相组成。声处理的混悬注射剂包含适合于注射的液体制剂,其由分散在整个液相中的固体颗粒组成,所述颗粒在液相中不可溶。另外,对产品进行声处理,同时使气体鼓泡通过混悬液,并且这导致由固体颗粒形成微球。
243、在另一施用模式中,可通过导管或泵原位施用组合物。例如,导管或泵可例如引导组合物进入靶位置中。
244、肠胃外载体系统包括一种或更多种药学上合适的赋形剂,例如溶剂和共溶剂、增溶剂、润湿剂、助悬剂、增稠剂、乳化剂、螯合剂、缓冲剂、ph调节剂、抗氧化剂、还原剂、抗微生物防腐剂、填充剂、保护剂、张度调节剂和特殊添加剂。适合于肠胃外施用的制剂方便地包含组合物的无菌油性或水性制剂,其优选与接受者的血液等张,但这不是必需的。
245、本文中使用的吸入剂型包括但不限于气雾剂(在压力下被包装并且包含组合物的产品,所述组合物在启动合适的阀系统之后被释放,旨在表面施加于皮肤以及局部施加到鼻(鼻气雾剂)、口(舌和舌下气雾剂)或肺(吸入气雾剂)中)。泡沫气雾剂是包含组合物、表面活性剂、水性或非水性液体和抛射剂的剂型,因此如果抛射剂在内(非连续的)相(即水包油型的)中,则排出稳定的泡沫,如果抛射剂在外(连续的)相(即油包水型的)中,则排出喷雾或快速破裂的泡沫。计量气雾剂是由计量剂量阀组成的加压剂型,其允许在每次启动之后递送均匀量的喷雾。粉末气雾剂是在压力下包装并且包含散剂形式的组合物的产品,所述组合物在启动合适的阀系统之后被释放。气溶胶喷雾剂是气雾剂产品,其利用压缩气体作为抛射剂以提供必要的力以将产品作为湿喷雾喷出,并且适用于在水性溶剂中的组合物溶液剂。
246、本文中使用的经皮剂型包括但不限于贴剂,即通常包含通常施加于身体上的外部部位的黏着背衬(adhesive backing)的药物递送系统,其中成分(包含组合物)从贴剂的一些部分被动扩散或主动运输,并从而凭借贴剂,成分(包含组合物)被递送至身体的外表面或身体中。多种类型的经皮贴剂例如基质、储库和其他是本领域已知的。
247、本文中使用的表面剂型包括本领域已知的多种剂型,例如洗剂(乳剂、液体剂型,其中该剂型通常用于外部施加于皮肤)、增强洗剂(增强组合物递送的洗剂剂型,其中增强不是指剂型中组合物的强度)、凝胶剂(半固体剂型,其包含胶凝组合物以为溶液或胶体分散体提供挺度,其中凝胶剂可包含悬浮颗粒)和软膏剂(半固体剂型,通常包含小于20%水和挥发物以及大于50%碳氢化合物,蜡或多元醇作为载剂,其中该剂型通常用于外部施加于皮肤或黏膜)。另一些实施方案包括增强软膏剂(增强组合物递送的软膏剂型,其中增强不是指剂型中组合物的强度)、乳膏剂(乳剂,半固体剂型,通常包含大于20%水和挥发物和/或小于50%碳氢化合物,蜡或多元醇也可用作载剂,其中该剂型通常用于外部施加于皮肤或黏膜)和增强乳膏剂(增强组合物递送的乳膏剂型,其中增强不是指剂型中组合物的强度)。本文中使用的“乳剂”是指由两相系统组成的剂型,所述两相系统包含至少两种不混溶的液体,其中一种作为液滴、内相或分散相分散在另一种液体内,外相或连续相通常用一种或更多种乳化剂稳定,其中乳剂用作剂型术语,除非更具体的术语是适用的(例如乳膏剂、洗剂、软膏剂)。另一些实施方案包括混悬剂(液体剂型,其包含分散于液体载剂中的固体颗粒)、延长释放的混悬剂、糊剂(半固体剂型,包含细分散于脂肪载剂中的大比例(20%至50%)固体,其中该剂型通常用于外部施加于皮肤或黏膜)、溶液剂(澄清均质液体剂型,其包含溶解于溶剂或相互混溶的溶剂的混合物中的一种或更多种化学物质)以及散剂。
248、表面剂型组合物包含组合物和一种或更多种非活性药物成分,例如赋形剂、着色剂、颜料、添加剂、填充剂、软化剂、表面活性剂(例如,阴离子、阳离子、两性和非离子表面活性剂)、渗透促进剂(例如,醇、脂肪醇、脂肪酸、脂肪酸酯和多元醇)等。多种fda批准的表面非活性成分可存在于fda的“非活性成分数据库”中,其包含如由制造商特别指定的非活性成分。
249、6.细胞转染
250、本发明提供了细胞转染组合物,其包含本发明的线性双链dna产物或复合分子。
251、本发明提供了细胞转染组合物,其包含本文中所述的线性双链dna产物。因此,本发明提供了细胞转染组合物,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
252、(a)盒的5’末端核苷酸;
253、(b)盒的3’末端核苷酸;和
254、(c)盒外的一个或更多个核苷酸。
255、本发明还提供了细胞转染组合物,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
256、(a)盒的5’末端核苷酸;
257、(b)盒的3’末端核苷酸;和
258、(c)盒外的一个或更多个核苷酸;并且
259、其中盒包含编码序列。
260、细胞转染组合物可包含或可不包含载体,例如药剂或制剂。优选地,载体促进线性双链dna产物或复合分子在靶部位处的积累,和/或保护线性双链dna产物或复合分子免受与生物环境组分的不期望的相互作用,和/或保护线性双链dna产物或复合分子免受代谢和/或降解。
261、本发明还提供了细胞转染方法,其包括使待转染细胞与本发明的线性双链dna产物、复合分子、纳米粒或文库接触(体外),并且其中线性双链dna产物、复合分子、纳米粒或文库被转染至细胞的胞质溶胶中。
262、可使细胞在存在或不存在载体(例如药剂或制剂)的情况下与线性双链dna产物、复合分子、纳米粒或文库接触。优选地,载体促进线性双链dna产物、复合分子、纳米粒或文库在靶部位处的积累,和/或保护线性双链dna产物、复合分子、纳米粒或文库免受与生物环境组分的不期望的相互作用,和/或保护线性双链dna产物、复合分子、纳米粒或文库免受代谢和/或降解。
263、可将待转染的一种或更多种细胞提供于细胞培养基(例如petri皿、培养容器或孔等)中。可将线性双链dna产物、复合分子、纳米粒或文库分子直接添加至细胞培养基,或者可将细胞添加至包含线性双链dna产物、复合分子、纳米粒或文库的溶液,例如盐水、缓冲溶液或细胞培养基。
264、载体可以是病毒载体或非病毒载体。病毒载体包括用于递送线性双链dna产物或复合分子的慢病毒载体或腺病毒载体。非病毒载体(或载体)包括将线性双链dna产物或复合分子与以下复合:阳离子剂例如阳离子细胞穿透肽(cell penetrating peptide,cpp);阳离子聚合物或树枝状聚合物例如聚乙烯亚胺(pei)和聚-d,l-丙交酯-共-乙交酯(poly-d,l-lactide-co-glycolide,plga);和/或阳离子脂质(例如lipofectamine)。
265、载体可以是与线性双链dna产物或复合分子缀合的小分子(例如,胆固醇、胆汁酸和/或脂质)、聚合物、蛋白质(例如抗体)和/或适配体(例如rna)。载体可以是用于包封线性双链dna产物或复合分子的纳米粒制剂。
266、载体可以是用靶向配体(例如抗体)、肽、小分子(例如叶酸和/或生物素)或存在于胞外基质中的聚合物(例如透明质酸和/或硫酸软骨素)对线性双链dna产物的修饰,或者对双链核酸分子的疏水修饰(例如使用胆固醇和/或α-生育酚)。
267、细胞转染组合物可包含或可不包含选自光敏剂和/或自由基引发剂(例如光引发剂)的药剂。优选地,该药剂改善线性双链dna产物或复合分子在靶部位处的功能,和/或保护线性双链dna产物或复合分子免受代谢和/或降解。
268、本发明还提供了可通过本发明方法获得的细胞。因此,细胞可包含本发明的线性双链dna产物、复合分子、纳米粒或文库。
269、本发明还提供了用本发明的线性双链dna产物、复合分子、纳米粒或文库转染的细胞。
270、细胞可以是动物细胞,例如哺乳动物细胞(例如人细胞)、真菌细胞、微生物的细胞(例如原核细胞或真核细胞)或植物细胞。优选地,细胞是人细胞。
271、使细胞与线性双链dna产物、复合分子、纳米粒或文库接触的步骤可在体内进行。例如,可将线性双链dna产物、复合分子、纳米粒或文库施用于有此需要的生物体(例如对象)。生物体(例如对象)可以是动物(例如哺乳动物(例如人))、真菌、微生物或植物。
272、本文中所述的任何或所有线性双链dna产物或复合分子均可通过递送颗粒(例如脂质体、纳米粒、外排体、巨室微脂粒(macrovesicle)、病毒或非病毒载体)递送至细胞。本文中所述的任何或所有线性双链dna产物或复合分子均可使用基因枪递送至细胞。本文中所述的线性双链dna产物或复合分子可在没有载体的情况下递送至细胞。
273、7.用途和应用
274、与本领域已知的扩增产物相比,本发明的线性双链dna产物具有许多益处。例如,与通常用于目的基因转录的质粒dna不同,线性双链dna产物不包含细菌骨架、抗生素抗性基因和细菌污染物。另外,线性双链dna产物可在无细胞系统中大量产生,这显著加快了制备过程。重要的是,线性双链dna产物可包含可含有编码序列的单个盒。这意指产生的产物具有低分散性(或是基本上单分散的),即具有基本上相同的长度和尺寸,这在纳米粒、病毒或非病毒递送系统和疫苗的产生中高度有益。线性双链dna产物还可具有提高的对外切核酸酶消化的抗性,这提供了产物的较长半衰期(和延长的体内表达)。出于上述原因,本文中所述的线性双链dna产物适合于许多应用,其中的一些在本文中讨论。
275、包含本文中所述受保护核苷酸的产物的用途可以是体内用途或体外用途。
276、rna和蛋白质的产生
277、本发明提供了线性双链dna产物、复合分子、纳米粒或文库在rna(例如mrna)的产生中的用途。
278、本发明提供了用于体外转录的方法,其包括:
279、(a)使本文中所述的线性双链dna产物与聚合酶接触;以及
280、(b)产生转录产物。
281、本发明提供了用于体外转录的方法,其包括(a)使本文中所述的复合分子与聚合酶接触;以及(b)产生转录产物。本发明提供了用于体外转录的方法,其包括(a)使本文中所述的纳米粒与聚合酶接触;以及(b)产生转录产物。本发明还提供了用于体外转录的方法,其包括(a)使本文中所述的文库与聚合酶接触;以及(b)产生转录产物。
282、本发明还提供了用于体内转录的方法,其包括:(a)在细胞中使本文中所述的线性双链dna产物与聚合酶接触;以及(b)在细胞中产生转录产物。
283、细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
284、线性双链dna产物可包含单个盒。盒可包含编码序列。盒可包含启动子和编码序列。编码序列可编码期望的蛋白质。因此,转录产物可包含期望蛋白质的mrna序列。
285、转录可包括使用聚合酶。优选rna聚合酶。rna聚合酶可以是t7rna聚合酶、t3 rna聚合酶或sp6 rna聚合酶。
286、转录可包括并入受保护核苷酸例如硫代磷酸酯核苷酸的步骤。
287、体外转录可在无细胞表达系统中进行。无细胞表达系统可来源于原核细胞或真核细胞。例如,无细胞表达系统可来源于兔网织红细胞、麦胚或大肠杆菌(escherichiacoli)。
288、转录产物可用于病毒rna合成和转染。例如,转录产物可用于开始复制。转录产物可用于体外和/或体内mrna合成。转录产物可用于rna结构研究。转录产物可用于rna适配体合成,例如用于通过指数富集的配体的系统进化(systematic evolution of ligands byexponential enrichment,selex)。转录产物可用于dsrna或shrna合成,例如,用于rnai技术。转录产物可用于crisprgrna合成,例如,用于rnp介导的基因编辑。转录产物可用于核糖核酸探针合成,例如,用于northern印迹或原位杂交。转录产物可用于rna扩增。转录产物可用于mirna合成。转录产物可用于反义rna合成。
289、本发明提供了用于蛋白质表达的方法,所述方法包括将本文中所述的线性双链dna产物引入到原核细胞或真核细胞或无细胞蛋白质表达系统中以产生期望的rna或蛋白质。
290、本发明还提供了用于体外产生期望蛋白质的方法,其包括:
291、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物在每条链中内部位置处包含一个或更多个硫代磷酸酯核苷酸;以及
292、(b)在无细胞表达系统中从线性双链dna产物表达蛋白质。
293、无细胞表达系统可来源于原核细胞或真核细胞。例如,无细胞表达系统可来源于兔网织红细胞、麦胚或大肠杆菌。
294、本发明还提供了用于体内产生期望蛋白质的方法,其包括:
295、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物在每条链中内部位置处包含一个或更多个硫代磷酸酯核苷酸;以及
296、(b)在细胞中从线性双链dna产物表达蛋白质。
297、细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
298、期望的蛋白质可由盒编码。本发明还提供了用于在体外产生期望蛋白质的方法,其包括:
299、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸;以及
300、(b)在无细胞表达系统中从盒表达蛋白质。
301、本发明还提供了用于在体内产生期望蛋白质的方法,其包括:
302、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸;以及
303、(b)在细胞中从盒表达蛋白质。
304、线性双链dna产物可在每条链中内部位置处包含至少2、3、4、5、6、7、8、9、10个硫代磷酸酯核苷酸。优选地,线性双链dna产物在每条链中内部位置处包含至少2个硫代磷酸酯核苷酸。
305、本发明还提供了用于在体外产生期望蛋白质的方法,其包括:
306、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
307、(i)盒的5’末端核苷酸;
308、(ii)盒的3’末端核苷酸;和
309、(iii)盒外的一个或更多个核苷酸;并且
310、其中盒包含编码序列;以及
311、(b)在无细胞表达系统中从盒表达蛋白质。
312、本发明还提供了用于在体内产生期望蛋白质的方法,其包括:
313、(a)提供包含有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
314、(i)盒的5’末端核苷酸;
315、(ii)盒的3’末端核苷酸;和
316、(iii)盒外的一个或更多个核苷酸;并且
317、其中盒包含编码序列;以及
318、(b)在细胞中从盒表达蛋白质。
319、本发明提供了用于在体内转录和翻译线性双链dna产物的方法。本发明还提供了用于在体外转录和翻译线性双链dna产物的方法。线性双链dna产物可具有提高的或增强的对外切核酸酶(例如外切核酸酶iii)消化的抗性。线性双链dna产物可对外切核酸酶(例如外切核酸酶iii)消化具有抗性。因此,本文中所述的表达(即转录和/或翻译)方法,其使用对外切核酸酶消化具有增强的抗性的dna产物,允许在细胞中(或在无细胞系统中)延长目的基因表达。
320、纳米粒或纳米粒文库的产生
321、本发明提供了线性双链dna产物、复合分子或文库在产生纳米粒或纳米粒文库中的用途。
322、病毒载体
323、产生病毒载体(例如avv载体)的方法是本领域已知的。最广泛使用的方法涉及通过三种细菌质粒共转染hek293。第一质粒编码rep和cap元件,第二质粒是辅助质粒,而第三质粒编码具有反向末端重复(inverted terminal repeat,itr)的遗传目的载荷。围绕用于病毒制备(例如avv)使用的质粒存在数个问题,即:1)质粒的产生耗时且昂贵,2)在大肠杆菌(e.coli)中itr序列的增殖存在困难;3)将质粒骨架并入病毒衣壳(例如avv衣壳)中可能是挑战性的(例如关于抗生素抗性标志物的问题)。这些一起代表了病毒载体产生(例如avv产生)中的主要瓶颈。因此,本发明提供了适合用于产生病毒载体的线性双链dna产物。本发明的线性双链dna产物克服了关于质粒载体的以上问题。
324、本发明提供了本文中所述的线性双链dna产物、复合分子或文库在产生病毒载体中的用途。
325、本发明提供了本文中所述的线性双链dna产物在产生病毒载体中的用途。因此,本发明提供了包含有义链和反义链的线性双链dna产物在产生病毒载体中的用途,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
326、(a)盒的5’末端核苷酸;
327、(b)盒的3’末端核苷酸;和
328、(c)盒外的一个或更多个核苷酸。
329、本发明还提供了包含有义链和反义链的线性双链dna产物在产生病毒载体中的用途,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
330、(a)盒的5’末端核苷酸;
331、(b)盒的3’末端核苷酸;和
332、(c)盒外的一个或更多个核苷酸;并且
333、其中盒包含编码序列。
334、本发明提供了产生病毒载体的方法,所述方法包括在使得产生病毒载体的条件下将本文中所述的线性双链dna产物、复合分子或文库引入到细胞中。线性双链dna产物、复合分子或文库可编码产生病毒载体所需的至少一种元件。例如,线性双链dna产物、复合分子或文库可编码rep和/或cap元件。线性双链dna产物、复合分子或文库可编码辅助质粒元件。线性双链dna产物、复合分子或文库可编码rep、cap和辅助质粒元件。所述方法可以是体内或体外方法。所述细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞(例如hek293t、hek293、cap、cap-t或cho)。细胞可以是在组织培养细胞系中在体外培养的细胞。
335、优选地,载体是avv载体或慢病毒载体。
336、本发明还提供了将病毒载体递送至细胞的方法,其包括使通过本文中所述方法产生的病毒载体与细胞接触。细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
337、本发明还提供了可通过本文中所述方法获得的细胞。
338、非病毒载体
339、产生非病毒载体的方法是本领域已知的。与病毒载体相比,使用非病毒载体具有数个优点,包括由于其非免疫原性而重复给药的机会、无限制的包装能力和低相关毒性。大多数用于产生非病毒载体的方法均使用质粒dna。因此,本发明提供了适用于产生非病毒载体的线性双链dna产物。本发明的线性双链dna产物克服了在非病毒载体制备中使用质粒载体的问题。例如,与质粒dna不同,本发明的线性双链dna不包含细菌骨架,允许每mg dna更多的转基因拷贝。另外,本发明不包含抗生素抗性基因和细菌污染物。此外,本发明的线性双链dna产物提供了延长的转基因表达(由于外切核酸酶抗性核苷酸的存在)和非病毒载体产生的更加成本有效的方法。
340、本发明提供了本文中所述的线性双链dna产物在产生非病毒载体中的用途。本发明提供了包含有义链和反义链的线性双链dna产物在产生非病毒载体中的用途,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
341、(a)盒的5’末端核苷酸;
342、(b)盒的3’末端核苷酸;和
343、(c)盒外的一个或更多个核苷酸。
344、本发明还提供了包含有义链和反义链的线性双链dna产物在产生非病毒载体中的用途,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
345、(a)盒的5’末端核苷酸;
346、(b)盒的3’末端核苷酸;和
347、(c)盒外的一个或更多个核苷酸;并且
348、其中盒包含编码序列。
349、本发明还提供了本文中所述的复合分子在产生非病毒载体中的用途。
350、本发明提供了将非病毒载体递送至细胞的方法,其包括使包含线性双链dna产物、复合分子、文库或组合物的非病毒载体与细胞接触。细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
351、本发明还提供了可通过本文中所述的方法获得的细胞。
352、一般的治疗和诊断用途
353、线性双链dna产物、复合分子、纳米粒、组合物或文库特别适合用于治疗。这些分子可编码治疗性蛋白质的序列、疫苗的一部分或遗传改造机制的元件,其用于在对象中治疗疾病或感染。
354、本发明提供了线性双链dna产物、复合分子、纳米粒、组合物或文库在治疗中的用途。
355、本发明提供了本文中所述的线性双链dna产物在治疗中的用途。因此,本发明提供了包含有义链和反义链的线性双链dna产物在治疗中的用途,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
356、(a)盒的5’末端核苷酸;
357、(b)盒的3’末端核苷酸;和
358、(c)盒外的一个或更多个核苷酸。
359、本发明提供了包含有义链和反义链的线性双链dna产物,其用于治疗,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
360、(a)盒的5’末端核苷酸;
361、(b)盒的3’末端核苷酸;和
362、(c)盒外的一个或更多个核苷酸;并且
363、其中盒包含编码序列。
364、本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库,其用作药物。本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库在制备用于治疗疾病的药物中的用途。
365、本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库,其用于治疗疾病。
366、本发明还提供了在对象中治疗疾病的方法,其包括向对象施用本发明的线性双链dna产物、复合分子、纳米粒、组合物或文库。优选地,向对象施用的线性双链dna产物、复合分子、纳米粒、组合物或文库的量是治疗活性量。
367、线性双链dna产物、复合分子、纳米粒、组合物或文库可用于治疗任何疾病或病症。例如,线性双链dna产物、复合分子、纳米粒、组合物或文库可用于治疗一种或更多种选自以下中的疾病和/或病症:遗传病症(例如单基因病症)、癌症、hiv、其他病毒感染(例如由冠状病毒(例如covid-19)、甲型肝炎、乙型肝炎、单纯疱疹病毒2型、流感、麻疹和/或呼吸道合胞病毒引起的感染)、神经退行性疾病(例如帕金森病(parkinson’s disease)和/或多聚谷氨酰胺病(例如亨廷顿病(huntington’s disease))、眼部疾病(例如黄斑变性)和肝衰竭。优选地,线性双链dna产物、复合分子、纳米粒、组合物或文库用于治疗遗传病症。还更优选地,线性双链dna产物、复合分子、纳米粒、组合物或文库用于治疗单基因病症。例如,线性双链dna产物、复合分子、纳米粒、组合物或文库可用于治疗镰状细胞贫血、囊性纤维化、亨廷顿病和迪谢内肌营养不良(duchenne’s muscular dystrophy)、血友病a、α1-抗胰蛋白酶缺乏症、原发性纤毛运动不良症或早产儿呼吸窘迫综合征。
368、用线性双链dna产物、复合分子、纳米粒、组合物或文库治疗的对象可接受线性双链dna产物、复合分子、纳米粒或文库与用于相关病症的其他治疗形式(包括用通常用于治疗病症的药物的治疗)的组合。药物可以以一个或数个剂量单位施用。技术人员(例如医学实践者)根据对象的具体情况能够很好地确定用于对象的合适剂量方案。
369、线性双链dna产物、复合分子、纳米粒、组合物或文库优选作为如本文中所述的组合物或药物组合物施用于对象。
370、本文中使用的“施用”意指将线性双链dna产物、复合分子、纳米粒、组合物或文库引入到对象的身体中,如以上更详细描述的(参见“组合物”)。实例包括但不限于经口、表面、经颊、舌下、经肺、经皮、经黏膜、以及皮下、腹膜内、静脉内和肌内注射、或者通过消化管以液体或固体剂量的形式。
371、本文中使用的短语“治疗活性量”意指当施用于对象以用于治疗疾病时足以实现对该疾病的这样的治疗的线性双链dna产物、复合分子、纳米粒、组合物或文库的量。“治疗活性量”将变化,例如,取决于因素例如:使用的特定产品、对象疾病的严重程度、对象的年龄和相对健康以及施用的途径和形式。基于这样的因素确定用于特定对象的相关治疗活性量对于本领域技术人员(例如主治医学实践者)而言是常规的。如本文中所述的疾病治疗应理解为意指改善一种或更多种疾病症状。
372、本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库在诊断疾病和/或病症的方法中的用途。
373、本发明提供了线性双链dna产物、复合分子、纳米粒、组合物或文库在“体外”诊断疾病中的用途。
374、本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库,其用于“体外”诊断疾病的方法。
375、所述方法可用于诊断任何疾病和/或病症。例如,疾病和/或病症可选自遗传病症(例如单基因病症)、癌症、hiv、其他病毒感染(例如由冠状病毒(例如covid-19)、甲型肝炎、乙型肝炎、单纯疱疹病毒2型、流感、麻疹和/或呼吸道合胞病毒引起的感染)、神经退行性疾病(例如帕金森病和/或多聚谷氨酰胺疾病(例如亨廷顿病))、眼部疾病(例如黄斑变性)和肝衰竭。优选地,线性双链dna产物、复合分子、纳米粒、组合物或文库用于诊断遗传病症。还更优选地,线性双链dna产物、复合分子、纳米粒、组合物或文库用于诊断单基因遗传病症。例如,线性双链dna产物、复合分子、纳米粒、组合物或文库可用于诊断镰状细胞贫血、囊性纤维化、亨廷顿病和迪谢内肌营养不良、血友病a、α1-抗胰蛋白酶缺乏症、原发性纤毛运动不良症或早产儿呼吸窘迫综合征。
376、本文中所述的诊断和治疗方法可以是体外方法或体内方法。
377、诊断方法可依赖于线性双链dna产物、复合分子、纳米粒、组合物或文库的检测和/或定量。
378、为了促进线性双链dna产物的检测和/或定量,可将线性双链dna产物与功能部分连接或结合。功能部分可以是本文中所述的任何功能部分。例如,功能部分可以是探针。功能部分可包含荧光团、放射性化合物或条码。功能部分可以是蛋白质,例如抗体。
379、诊断可依赖于与dna产物的存在、不存在和/或水平相对应的信号的检测。例如,可通过对与荧光探针连接的线性双链dna产物进行流式细胞术和/或荧光激活细胞分选来测量信号。
380、线性双链dna产物可例如在测向流测定中通过与捕获分子结合来检测。在该实例中,功能部分是蛋白质,例如对捕获部分具有特异性的抗体。对与线性双链dna产物连接的抗体的捕获可产生视觉信号(例如不同颜色的条带)。
381、本发明还提供了将疾病诊断与疾病治疗组合的方法。
382、细胞治疗
383、如上所述,与质粒dna相比,本发明的产物可以是显著更少污染的。另外,本发明的产物本质上非常简单(例如无细菌骨架),这意味着它们通常易于处理。由于本发明的产物至少包含目的基因,因此每反应体积(或每质量的最终产物)可获得目的基因的更多拷贝。本文中所述产物的纯的和简单性质使其特别适用于细胞治疗。例如,可将包含本文中所述的线性双链dna产物、复合分子、纳米粒、组合物和文库的细胞注射或以其他方式移植入患者中以引起期望的作用。在免疫治疗的过程中,一个细胞(或更多个细胞)可以能够例如通过细胞介导的免疫来对抗癌细胞。一个细胞(或更多个细胞)可被移植以再生患病组织。
384、本发明提供了线性双链dna产物、复合分子、纳米粒、组合物或文库,其用于细胞治疗。
385、本发明提供了本文中所述的线性双链dna产物,其用于细胞治疗。因此,本发明提供了包含有义链和反义链的线性双链dna产物,其用于细胞治疗,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
386、(a)盒的5’末端核苷酸;
387、(b)盒的3’末端核苷酸;和
388、(c)盒外的一个或更多个核苷酸。
389、本发明还提供了包含有义链和反义链的线性双链dna产物,其用于细胞治疗,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
390、(a)盒的5’末端核苷酸;
391、(b)盒的3’末端核苷酸;和
392、(c)盒外的一个或更多个核苷酸;并且
393、其中盒包含编码序列。
394、本发明还提供了线性双链dna产物、复合分子、纳米粒、组合物或文库在产生细胞治疗中的用途。本发明提供了细胞治疗的方法,其包括使线性双链dna产物、复合分子、纳米粒、文库、病毒或非病毒载体、或者组合物与细胞接触。优选地,细胞治疗是离体细胞治疗。细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
395、本发明还提供了可通过本文中所述的任何方法获得的细胞。例如,所述细胞可适用于细胞治疗。
396、疫苗
397、本发明的产物特别适合用于疫苗产生。疫苗可包含本文中所述的线性双链dna产物、复合分子或文库。或者,本文中所述的线性双链dna产物、复合分子或文库可用于产生疫苗,优选基于mrna的疫苗。例如,疫苗例如针对covid-19的biontech和moderna mrna疫苗。
398、因此,本发明提供了本文中所述的线性双链dna产物、复合分子、纳米粒、组合物或文库在产生疫苗中的用途。
399、本发明提供了本文中所述的线性双链dna产物在产生疫苗中的用途。本发明提供了包含有义链和反义链的线性双链dna产物在产生疫苗中的用途,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)。优选地,在每条链中内部位置处的一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)可选自:
400、(a)盒的5’末端核苷酸;
401、(b)盒的3’末端核苷酸;和
402、(c)盒外的一个或更多个核苷酸。
403、本发明还提供了包含有义链和反义链的线性双链dna产物在产生疫苗中的用途,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
404、(a)盒的5’末端核苷酸;
405、(b)盒的3’末端核苷酸;和
406、(c)盒外的一个或更多个核苷酸;并且
407、其中盒包含编码序列。
408、优选地,疫苗是mrna疫苗。
409、本发明还提供了疫苗,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)。优选地,在每条链中内部位置处的一个或更多个受保护核苷酸(例如硫代磷酸酯核苷酸)可选自:
410、(a)盒的5’末端核苷酸;
411、(b)盒的3’末端核苷酸;和
412、(c)盒外的一个或更多个核苷酸。
413、本发明提供了疫苗,其包含含有有义链和反义链的线性双链dna产物,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
414、(d)盒的5’末端核苷酸;
415、(e)盒的3’末端核苷酸;和
416、(f)盒外的一个或更多个核苷酸;并且
417、其中盒包含编码序列。
418、线性双链dna产物可编码抗原,其可在对象中引起免疫应答。对象可以是人。优选地,抗原在盒上编码。
419、car-t细胞
420、本发明提供了本文中所述的线性双链dna产物、复合分子、纳米粒、组合物或文库在产生car-t细胞中的用途。
421、本发明提供了本文中所述的线性双链dna产物在产生car-t细胞中的用途。本发明提供了包含有义链和反义链的线性双链dna产物在产生car-t细胞中的用途,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸。优选地,在每条链中内部位置处的一个或更多个硫代磷酸酯核苷酸可选自:
422、(a)盒的5’末端核苷酸;
423、(b)盒的3’末端核苷酸;和
424、(c)盒外的一个或更多个核苷酸。
425、本发明还提供了包含有义链和反义链的线性双链dna产物在产生car-t细胞中的用途,其中线性双链dna产物包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
426、(a)盒的5’末端核苷酸;
427、(b)盒的3’末端核苷酸;和
428、(c)盒外的一个或更多个核苷酸;并且
429、其中盒包含编码序列。
430、本发明提供了用于产生经遗传改造car-t细胞的方法,其包括:(a)将本文中所述的线性双链dna产物、复合分子、纳米粒、组合物或文库引入到t细胞中;以及(b)表达目的基因。优选地,目的基因是肿瘤特异性car。
431、本发明提供了用于产生经遗传改造car-t细胞的方法,其包括:(a)将包含有义链和反义链的线性双链dna产物引入到t细胞中,其中线性双链dna产物包含单个盒,并在每条链中的内部位置处包含一个或更多个硫代磷酸酯核苷酸;以及(b)表达目的基因。优选地,目的基因是肿瘤特异性car。
432、在步骤(a)之前,所述方法还可包括从患者中取出单个核细胞的步骤。优选地,所述取出步骤使用白细胞去除术进行。优选地,单个核细胞是t细胞。在步骤(b)之后,所述方法还可包括使经遗传改造的细胞返回患者的步骤。
433、本发明还提供了可通过本文中所述的任何方法获得的经改造t细胞。所述经改造t细胞可适用于car t细胞治疗。
434、crispr递送
435、本发明的产物特别适用于例如在细胞治疗或体内治疗中将crispr机制递送至细胞。
436、使用通常用于递送crispr机制的多种不同的载物和递送载剂,包括物理递送方法(例如显微注射;电穿孔)、病毒递送方法(例如腺相关病毒(adeno-associated virus,aav);全尺寸腺病毒和慢病毒)和非病毒递送方法(例如脂质体;聚合复合物;金颗粒)。如上所讨论的,本发明提供了具有低分散性的线性双链dna产物。因此,包含线性双链dna的纳米粒(或纳米粒文库)或病毒或非病毒递送载体是较低分散的(即更均匀),这提高了细胞递送的效率。
437、线性双链dna产物可包含编码cripsr机制的任何组分的基因序列。线性双链dna产物可编码cripsr机制的所有组分。
438、线性双链dna产物可包含(或编码)修复模板(或编辑模板)。修复模板(或编辑模板)可用于编辑基因组,例如使用crispr-cas系统进行。修复模板(或编辑模板)可包含与期望的dna区(即靶分子)同源的同源区(例如同源臂),或由与期望的dna区(即靶分子)同源的同源区(例如同源臂)组成。修复模板(或编辑模板)可用于crispr-cas介导的同源定向修复(hdr)。修复模板(或编辑模板)可用于修复具有链断裂(例如单链断裂或双链断裂)的靶分子。链断裂可由crispr系统(例如cas9、cpf1或mad7)的核酸酶产生。修复模板(或编辑模板)可在期望的dna区(即靶分子)中引入至少一个突变(例如插入、缺失和/或替换)。修复模板(或编辑模板)可为至少10、20、30、40、50、100、200、300、400、500、600、700、800、900、1000、1500、2000、2500、3000、3500、4000、4500、5000、5500、6000、6500、7000、7500、8000、8500、9000、9500或10000个碱基对长。编码修复模板的线性双链dna产物可通过纳米粒、非病毒载体或病毒载体或者在没有任何载体的帮助下递送至细胞。
439、线性双链dna产物可包含编码crispr系统的核酸酶蛋白(例如cas9、cpf1或mad7)和/或指导rna的基因序列。线性双链dna产物可包含编码crispr系统的核酸酶蛋白(例如cas9、cpf1或mad7)的基因序列。线性双链dna产物可包含编码指导rna的基因序列。线性双链dna产物可包含编码crispr系统的核酸酶蛋白(例如cas9、cpf1或mad7)和指导rna的基因序列。线性双链dna产物可包含编码待修饰基因组靶标(例如间隔区)的基因序列。线性双链dna产物可与载体连接。载体可包含cripsr系统的一些组分的序列。载体可包含指导rna的序列或指导rna的一部分的序列。如果载体包含指导rna的一部分的序列,则线性双链dna产物可包含指导rna的缺失序列部分,使得在连接之后,经连接的载体包含指导rna的完整序列。crispr系统的核酸酶和指导rna可在单个载体上或在两个不同载体上被编码。线性双链dna产物可编码crispr系统的核酸酶和指导rna。一个线性双链dna产物可编码crispr系统的核酸酶,并且另一个线性双链dna产物可编码指导rna。
440、线性双链dna产物可用于crispr-cas介导的重组修复、同源定向修复或非同源末端连接。
441、如果crispr系统的核酸酶和指导rna由不同线性双链dna产物编码,则它们可以是不同或相同递送机制的一部分。例如,编码crispr系统的核酸酶的线性双链dna产物可通过第一纳米粒、非病毒载体或病毒载体递送至细胞,而编码指导rna的线性双链dna产物可通过第二纳米粒、非病毒载体或病毒载体递送至细胞。例如,编码crispr系统的核酸酶的线性双链dna产物和编码指导rna的线性双链dna产物可通过同一纳米粒、非病毒载体或病毒载体递送至细胞。
442、如果crispr系统的核酸酶和指导rna由同一线性双链dna产物编码(或由包含线性双链dna产物的载体编码),则它们可以是同一递送机制的一部分。例如,编码crispr系统的核酸酶和指导rna的线性双链dna产物(或载体)可通过纳米粒、非病毒载体或病毒载体递送至细胞。
443、因此,本发明提供了线性双链dna产物、复合分子、组合物、文库或纳米粒,其用于将crispr系统递送至细胞。本发明提供了将crispr系统递送至细胞的方法,其包括使线性双链dna产物、复合分子、纳米粒、文库或组合物与细胞接触。
444、细胞可以是动物细胞,优选哺乳动物细胞,例如人细胞。
445、本发明还提供了可通过本文中所述方法获得的细胞。所述细胞特别适用于细胞治疗和/或体内治疗。
446、本发明的线性双链dna产物、复合分子、纳米粒或文库可用于体外或体内转录以产生rna,优选mrna。
447、8.产生线性双链dna产物及其文库的方法
448、双链线性dna产物或其文库可以是任何扩增过程的产物。扩增过程可以是体外或体内扩增过程。优选地,扩增过程是体外扩增过程。例如,扩增过程可通过以下进行:滚环扩增(rolling circle amplification,rca)、malbac方法、传统聚合酶链反应(polymerasechain reaction,pcr)、基于核酸序列的扩增(nucleic acid sequence-basedamplification,nasba)、环介导等温扩增(loop-mediated isothermal amplification,lamp)、解旋酶依赖性扩增(helicase-dependent amplification,hda)、多重置换扩增(multiple displacement amplification,mda)和重组酶聚合酶扩增(recombinasepolymerase amplification,rpa)。优选地,扩增过程通过滚环扩增进行。优选地,双链dna产物是滚环扩增的产物。双链dna产物可由线性rca、指数rca或多引物rca产生。滚环扩增可在没有任何引物的情况下或在存在一个引物或多个引物的情况下进行。例如,所述引物可以是合成引物。所述引物可以是随机引物。滚环扩增可在存在引发酶的情况下进行。引发酶可以是tthprimpol。优选地,如果滚环扩增在没有任何引物的情况下进行,则其在存在引发酶例如tthprimpol的情况下进行。类似地,如果在扩增反应期间使用引物,则不使用引发酶。可通过使用合适的核酸聚合酶例如phi29 dna聚合酶在等温条件下进行体外滚环扩增来产生双链dna产物。滚环扩增可在存在受保护核苷酸例如硫代磷酸酯核苷酸的情况下进行。
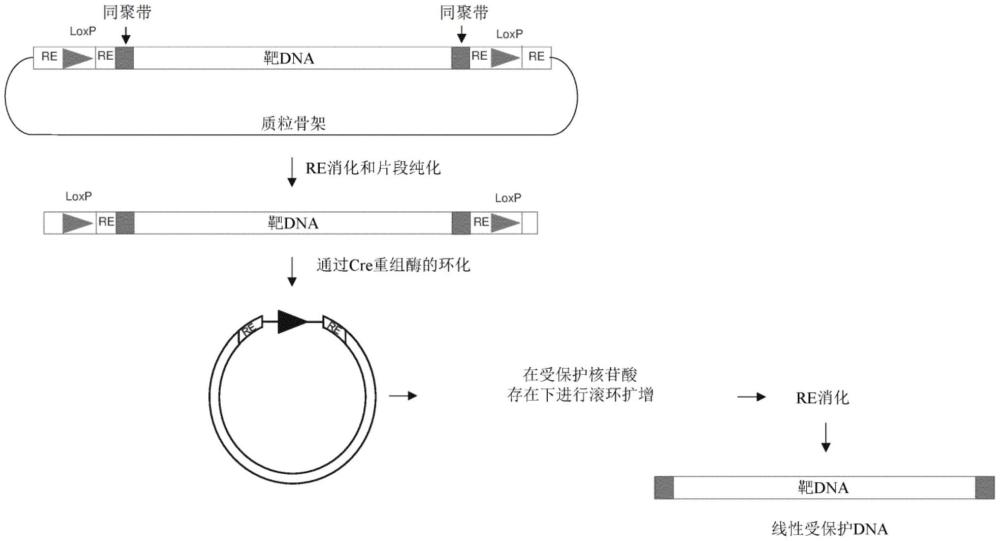
449、本技术的发明人出乎意料地发现了切割滚环扩增产物的方法,使得在单个线性双链dna产物中仅存在盒的单个拷贝(其可包含目的基因)。与已知的扩增产物相比,盒的单个拷贝/单个dna产物提供了许多益处。例如,盒的单个拷贝/单个dna产物确保dna产物尽可能小,这在例如细胞递送方法和/或细胞递送系统的有效性中发挥关键作用。
450、本文中所述的线性双链dna产物或其文库可通过切割扩增产物产生。切割可以是酶促切割,例如内切核酸酶消化,例如限制酶消化。在切割之后,线性双链dna产物可包含单个盒(例如包含单个编码序列的盒)。换言之,在切割之后,线性双链dna产物可不包含多个串联重复序列或多联体dna或者不由多个串联重复序列或多联体dna组成。在切割之后,线性双链dna产物可不包含以下或者不由以下组成:通过已知方法(例如如在美国专利us10350307 b2中所述)产生的多联体dna。在切割之后,线性双链dna产物可包含目的dna序列的单个拷贝,例如,编码序列的单个拷贝。
451、因此,本发明提供了用于产生本文中所述的线性双链dna产物或线性双链dna产物文库的方法,其包括:
452、(a)在存在至少一种类型的受保护核苷酸的情况下,对包含至少一个可切割序列的dna模板分子进行扩增以产生双链dna产物;以及
453、(b)使双链dna产物与至少一种酶接触以产生线性双链dna产物或其文库,优选地,其中线性双链dna产物具有提高的对核酸酶的抗性。
454、扩增方法可采用滚环扩增方法。因此,产生本文中所述的线性双链dna产物或线性双链dna产物文库的方法可包括:
455、(a)在存在至少一种类型的受保护核苷酸的情况下,对包含至少一个可切割序列的dna模板分子进行滚环扩增以产生双链dna产物;以及
456、(b)使双链dna产物与至少一种酶接触以产生线性双链dna产物或其文库,优选地其中线性双链dna产物具有提高的对核酸酶的抗性。
457、可切割序列可以是被酶切割的序列。优选地,可切割序列是被内切核酸酶(例如限制性内切核酸酶)切割的序列。产生本文中所述的线性双链dna产物或线性双链dna产物文库的方法可包括:
458、(a)在存在至少一种类型的受保护核苷酸的情况下,对包含至少一个内切核酸酶靶序列的dna模板分子进行滚环扩增以产生双链dna产物;以及
459、(b)使双链dna产物与至少一种酶接触以产生线性双链dna产物或其文库,优选地其中线性双链dna产物具有提高的对核酸酶的抗性。
460、优选地,线性双链dna产物对外切核酸酶消化例如外切核酸酶iii消化具有抗性。因此,所述方法可使用提供针对外切核酸酶消化的保护的核苷酸,例如硫代磷酸酯核苷酸或moe核苷酸。因此,本发明提供了用于产生本文中所述的线性双链dna产物或线性双链dna产物文库的方法,其包括:
461、(a)在存在至少一种类型的硫代磷酸酯核苷酸的情况下,对包含至少一个内切核酸酶靶序列的dna模板分子进行滚环扩增以产生双链dna产物;以及
462、(b)使双链dna产物与至少一种内切核酸酶接触以产生线性双链dna产物,其中线性双链dna产物具有提高的对外切核酸酶的抗性。
463、如本文中所述,线性双链dna产物可包含盒。因此,用于在体外产生具有提高的对外切核酸酶的抗性的线性双链dna产物或线性双链dna产物文库的方法可包括以下步骤:
464、(a)在存在至少一种类型的硫代磷酸酯核苷酸的情况下,对包含至少一个内切核酸酶靶序列的dna模板分子进行滚环扩增以产生双链dna产物,
465、其中双链dna产物包含单个盒;以及
466、(b)使双链dna产物与至少一种内切核酸酶接触以产生包含单个盒的线性双链dna产物或这样的双链dna产物的文库,优选地,其中线性双链dna产物具有提高的对外切核酸酶的抗性。
467、在本文中所述方法中使用的硫代磷酸酯核苷酸与总核苷酸之比可以为至少0.0001、至少0.0025、至少0.01、至少0.025、至少0.05、至少0.075、至少0.10、至少0.12、至少0.15、至少0.25、至少0.35、至少0.5或至少0.75。在本文中所述方法中使用的硫代磷酸酯核苷酸与总核苷酸之比可小于1、小于0.9、小于0.8、小于0.65、小于0.5、小于0.4、小于0.3、小于0.2、小于0.1、小于0.075或小于0.05。硫代磷酸酯核苷酸与总核苷酸之比可以为0.0001至1、0.0025至0.75、0.025至0.65、0.025至0.15或0.25至0.50。优选地,硫代磷酸酯核苷酸与总核苷酸之比为0.025至0.15。线性双链dna产物可以以下的硫代磷酸酯核苷酸与总核苷酸之比包含硫代磷酸酯核苷酸:0.005至0.3、0.0075至0.2、0.01至0.15、0.01至0.10、0.02至0.08、0.03至0.07、0.04至0.06或0.05至0.075。优选地,硫代磷酸酯核苷酸与总核苷酸之比为0.01至0.10。优选地,硫代磷酸酯核苷酸与总核苷酸之比为约0.025、约0.05、约0.075、约0.10、约0.12、约0.15或约0.25。还更优选地,硫代磷酸酯核苷酸与总核苷酸之比为约0.025或约0.05。如在实施例中所示,硫代磷酸酯核苷酸与总核苷酸之比为约0.025足以提供增强的对外切核酸酶消化的抗性。如在实施例中所示,硫代磷酸酯核苷酸与总核苷酸之比为约0.05或约0.075在提供增强的对外切核酸酶消化的抗性中特别有效(如由表达水平所示;参见实施例7和8)。此外,如在实施例中所示,比率为约0.05特别适合于目的基因在体内表达(参见实施例10)。
468、用于产生本文中所述的线性双链dna产物或双链dna产物文库的方法可包括:
469、(a)在存在至少一种类型的moe核苷酸的情况下,对包含至少一个内切核酸酶靶序列的dna模板分子进行滚环扩增以产生双链dna产物;以及
470、(b)使双链dna产物与至少一种内切核酸酶接触以产生线性双链dna产物或其文库,其中线性双链dna产物具有提高的对外切核酸酶的抗性。
471、尽管至少一种类型的受保护核苷酸足以提供针对外切核酸酶消化的保护,但用于产生本文中所述线性双链dna产物的方法可使用至少两种、至少三种或至少四种不同的受保护核苷酸,例如硫代磷酸酯核苷酸。
472、在本文中所述的方法中,dna模板分子可包含至少一个可切割序列。可切割序列可以是内切核酸酶靶序列。因此,dna模板分子可包含至少一个内切核酸酶靶序列。优选地,dna模板分子包含至少两个内切核酸酶靶序列。内切核酸酶靶序列可相同或不同。优选地,至少一个内切核酸酶靶序列是限制性内切核酸酶靶序列。不同的限制性内切核酸酶靶序列对于技术人员是已知的。例如,限制性内切核酸酶靶序列可以是bsai、ndei、smai、nsii和/或xbai靶序列。至少一个可切割序列(例如内切核酸酶靶序列)可以是天然可切割序列(即存在于模板分子中的可切割序列)。或者,至少一个可切割序列(例如内切核酸酶靶序列)可在产生线性双链dna产物之前被引入至dna模板分子。
473、因此,用于产生本文中所述的线性双链dna产物或线性双链dna产物文库的方法可包括:
474、(a)将至少一个可切割序列(例如限制性内切核酸酶靶序列)引入至dna模板分子;
475、(b)在存在至少一种类型的受保护核苷酸(例如硫代磷酸酯核苷酸)的情况下,对包含至少一个可切割序列的dna模板分子进行扩增(例如滚环扩增)以产生双链dna产物;以及
476、(c)使双链dna产物与至少一种酶(例如限制性内切核酸酶)接触以产生线性双链dna产物或其文库,优选地其中线性双链dna产物具有增强的对核酸酶(例如外切核酸酶iii)的抗性。
477、本技术的发明人已出乎意料地发现,如果将至少一种受保护核苷酸并入到双链dna产物的可切割序列中,则能够切割可切割序列的酶在切割时的效率低得多。换言之,为了实现对可切割序列的基本上完全消化(即释放基本上所有线性双链dna产物),因此至少一种类型的受保护核苷酸可不并入到双链dna产物的可切割序列中。因此,在所述方法中使用的至少一种类型的受保护核苷酸(例如硫代磷酸酯核苷酸)可选择为使得其不形成可切割序列的一部分。例如,smai限制酶识别可切割序列:5’-cccggg-3’(和互补的3’-gggccc-5’),因此,优选地,在所述方法中使用的至少一种类型的受保护核苷酸可以是例如α-s-datp。仅使用α-s-datp作为该实例中的受保护核苷酸将确保可切割序列不含受保护核苷酸。然而,一些类型的可切割序列可包含至少4种类型的核苷酸。例如,bsai限制酶识别5’-ggtctc(n)-3’和互补的3’-ccagag(n)-5’。本技术的发明人还已发现可使用任何类型的受保护核苷酸,只要受保护核苷酸与总核苷酸之比小于0.5即可。优选地,所使用的受保护(例如硫代磷酸酯)核苷酸与总核苷酸之比小于0.5、0.4、0.3、0.2或0.1,还更优选地,比率小于0.3。
478、产生线性双链dna产物或其文库的步骤可释放至少80%、85%、90%、95%或100%的线性双链dna产物或其文库。优选地,产生线性双链dna产物或其文库的步骤释放至少90%的线性双链dna产物或其文库。
479、所释放的线性双链dna产物优选包含单个盒和/或单个目的基因。因此,所述方法可包括以下步骤:
480、(a)将至少一个可切割序列(例如限制性内切核酸酶靶序列)引入至dna模板分子;
481、(b)在存在至少一种类型的硫代磷酸酯核苷酸的情况下,对包含至少一个可切割序列(例如限制性内切核酸酶靶序列)的dna模板分子进行滚环扩增以产生双链dna产物,
482、其中双链dna产物包含单个盒;以及
483、(c)使双链dna产物与至少一种酶(例如限制性内切核酸酶)接触以产生包含单个盒的线性双链dna产物或这样的线性双链dna产物的文库。
484、产生包含单个盒的线性双链dna产物的步骤可释放至少80%、85%、90%、95%或100%的线性双链dna产物。优选地,产生线性双链dna产物的步骤释放至少90%的线性双链dna产物。优选地,所释放的线性双链dna产物包含单个盒(或目的基因)。
485、在切割之后,线性双链dna产物的文库可具有低分散性(即是基本上单分散的)。本文中使用的术语“低分散性”和“单分散性”在线性双链dna产物的背景下旨在涵盖具有基本上相同尺寸(即相同的多核苷酸链长度)的线性双链dna产物拷贝的集合。换言之,相对于文库中其他线性双链dna产物,文库中每个线性双链dna产物的尺寸(即多核苷酸链的碱基数目)可变化小于10%,优选小于5%。这与多分散性线性双链dna产物文库相反,所述多分散性线性双链dna产物文库是指具有不一致的尺寸(即不一致的多核苷酸链长度)的dna产物拷贝的集合。
486、本技术的发明人已发现了产生基本上单分散的线性双链dna产物文库的方法,所述线性双链dna产物文库优选地对外切核酸酶消化具有抗性。与已知的dna产物相比,本文中所述的线性双链dna产物文库的基本上单分散的性质提供了益处,因为其适合于纳米粒和病毒或非病毒载体的产生。所产生的纳米粒、病毒和/或非病毒载体将具有基本上均匀的尺寸,这促进了转化和/或转染并在内化和药物释放过程中发挥关键作用。
487、在本文中所述的方法中使用的dna模板分子可以是单链的或双链的。优选地,dna模板分子是双链的。dna模板分子可以是天然环状dna分子。例如,dna模板分子可以是(i)质粒、(ii)微环、(iii)黏粒或(iv)细菌人工染色体(bacterial artificial chromosome,bac)。dna模板分子可以是酶促产生的环状dna分子。例如,dna模板分子可以是(i)获自重组酶反应(优选cre重组酶反应)的环状dna分子,或(ii)获自连接酶反应(优选使用goldengate assembly)的环状dna分子。dna模板分子可以是酶促产生的共价闭合的线性dna分子。例如,dna模板分子可以是(i)用teln前端粒酶处理的dna分子;或(ii)通过dna末端与适配体的连接产生的dna分子。dna模板分子可包含为双链的元件和为单链的元件。例如,模板dna分子可包含双链dna和单链发夹环。
488、dna模板分子可与线性双链dna产物至少70%、80%、90%、95%、96%、97%、98%、99%或100%互补。优选地,dna模板与线性双链dna产物至少99%互补。
489、dna模板分子可以是线性的。如果dna模板分子是线性的,则在扩增(例如滚环扩增)之前,可将dna模板分子环化以产生适用于本文中所述方法的dna模板分子。
490、模板dna分子可包含盒。盒可以是哺乳动物表达盒。盒还可包含启动子。启动子可以是cmv启动子。盒还可包含增强子。盒还可包含报道基因,例如egfp报道基因或萤光素酶报道基因。盒还可包含同聚序列。盒还可包含loxp序列,优选两个loxp序列。
491、dna模板分子可在5’末端或3’末端或者5’末端和3’末端二者处包含同聚序列。同聚序列可在环化之前添加至dna模板分子。同聚序列可以是polya、polyc、polyg或polyt序列。同聚序列的长度可为3至200个核苷酸。同聚序列可用于促进线性双链dna产物的纯化,在这种情况下,同聚序列的长度可为4至12个核苷酸或长度可为5至10个核苷酸。同聚序列可用于提高mrna表达,在这种情况下,同聚序列的长度可为10至200个核苷酸,优选长度为80至150个核苷酸。同聚序列的长度可为至少10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190或200个核苷酸。优选地,同聚序列的长度为至少100个核苷酸。还更优选地,同聚序列的长度为至少120个核苷酸。例如,同聚序列可包含至少120个核苷酸的polya序列。
492、在本文中所述的方法中,使用的受保护核苷酸类型(例如硫代磷酸酯核苷酸)可与dna模板分子的同聚序列的至少一个核苷酸互补或相同。优选地,受保护核苷酸与同聚序列的核苷酸互补。例如,如果同聚序列是polya序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dttp。如果同聚序列是polyc序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dgtp。如果同聚序列是polyg序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dctp。如果同聚序列是polyt序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-datp。本文中所述的方法可在单个反应中使用不同类型的受保护核苷酸。因此,例如,尽管同聚序列是polya序列,但在所述方法中可使用至少两种、三种或四种不同类型的受保护核苷酸。优选地,在所述方法中使用α-s-datp、α-s-dctp、α-s-dgtp和α-s-dttp的所有四者。
493、dna模板可包含两个不同的同聚序列。例如,在dna模板环化之前,dna模板可在链的每个末端处包含不同的同聚序列。例如,dna模板的3’末端可包含polya序列,并且dna模板的5’末端可包含polyt序列。
494、如本文中所述的,通过本文中所述方法产生的线性双链dna产物可包含单个盒,并在每条链中内部位置处包含至少两个硫代磷酸酯核苷酸,其中在每条链中内部位置处的至少两个硫代磷酸酯核苷酸选自:
495、(a)盒的5’末端核苷酸;
496、(b)盒的3’末端核苷酸;和
497、(c)盒外的一个或更多个核苷酸。
498、线性双链dna产物可通过本文中提供的任何方法获得。
499、本发明提供了用于产生具有受保护末端的线性双链dna产物或这样的线性双链dna产物的文库的方法。所述方法可包括以下步骤:
500、(a)将至少一个同聚序列添加至dna模板分子
501、(b)在存在至少一种类型的受保护核苷酸的情况下,对包含至少一个内切核酸酶靶序列和至少一个同聚序列的dna模板分子进行扩增以产生双链dna产物,
502、(c)使双链dna产物与至少一种内切核酸酶接触以产生线性双链dna产物,以及
503、(d)使线性双链dna产物与外切核酸酶接触以产生具有受保护末端的线性双链dna产物或这样的线性双链dna产物的文库。
504、本文中所述的任何dna模板分子均适用于产生具有受保护末端的线性双链dna产物的方法。
505、将至少一个同聚序列添加至dna模板分子可在dna模板分子环化之前进行。优选地,将两个同聚序列添加至dna模板分子。两个同聚序列可不同或相同。同聚序列可添加至dna模板分子的5’末端或3’末端或者5’末端和3’末端二者。同聚序列可以是polya、polyc、polyg或polyt序列。例如,在dna模板环化之前,可将两个不同的同聚序列添加至dna模板分子。例如,polyc序列可添加至dna模板的3’末端,并且polyg序列可添加至dna模板的5’末端。
506、同聚序列的长度可为3至200个核苷酸。同聚序列可用于促进线性双链dna产物的纯化,在这种情况下,同聚序列的长度可为4至12个核苷酸或长度可为5至10个核苷酸。同聚序列可用于提高mrna表达,在这种情况下,同聚序列的长度可为10至200个核苷酸,优选长度为80至150个核苷酸。同聚序列的长度可为至少10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190或200个核苷酸。优选地,同聚序列的长度为至少100个核苷酸。还更优选地,同聚序列的长度为至少120个核苷酸。例如,同聚序列可包含至少120个核苷酸的polya序列。
507、将至少一个同聚序列添加至dna模板分子的步骤可通过本领域已知的任何常规方法进行。例如,可使用dna连接酶将同聚序列与dna模板分子连接。可使用限制酶方法将同聚序列与dna模板分子连接。可使用任何合成生物学方法(例如连续杂交组装(successivehybridization assembling,sha))将同聚序列与dna模板分子连接。
508、优选地,扩增是滚环扩增。滚环扩增通常需要环状模板分子。因此,在将至少一个同聚序列添加至dna模板分子的步骤之后,所述方法还可包括dna模板分子环化的步骤。环化可通过本领域已知的任何方法进行。例如,环状dna模板分子可从重组酶反应(优选cre重组酶反应)或从连接酶反应(优选使用golden gate assembly)获得。环状dna模板分子可通过共价闭合的线性dna分子获得。例如,dna模板分子可以是用teln前端粒酶处理的dna分子,或通过dna末端与适配体的连接产生的dna分子。
509、使线性双链dna产物与外切核酸酶接触以产生具有受保护末端的线性双链dna产物的步骤可使用外切核酸酶iii。外切核酸酶从多核苷酸链的5’末端或3’末端切割未受保护的核苷酸。因此,外切核酸酶可消化线性双链dna产物,直至遇到链中受保护核苷酸(例如硫代磷酸酯核苷酸)的位点。一旦线性双链dna产物的末端受保护以免进一步的外切核酸酶消化(优选外切核酸酶iii消化),就可将外切核酸酶从反应去除。因此,所述方法还可包括去除外切核酸酶的步骤。
510、优选地,线性双链dna产物还在至少一条链中(优选在两条链中)的内部位置处包含一个或更多个受保护核苷酸。
511、所使用的至少一种类型的受保护核苷酸(例如硫代磷酸酯核苷酸)可与dna模板分子的同聚序列的至少一个核苷酸互补或相同。优选地,受保护核苷酸与同聚序列的核苷酸互补。优选地,受保护核苷酸是硫代磷酸酯核苷酸。例如,如果同聚序列是polya序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dttp。如果同聚序列是polyc序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dgtp。如果同聚序列是polyg序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-dctp。如果同聚序列是polyt序列,则在所述方法中使用的并且优选地被并入到双链dna产物中的硫代磷酸酯核苷酸可以是α-s-datp。所述方法可在单个反应中使用不同类型的受保护核苷酸。因此,例如,尽管同聚序列是polya序列,但在所述方法中可使用至少两种、三种或四种不同类型的受保护核苷酸。优选地,在所述方法中使用α-s-datp、α-s-dctp、α-s-dgtp和α-s-dttp的所有四者。
512、将同聚序列添加至模板dna分子确保了一个受保护核苷酸将被添加至dna产物的互补链。例如,如果将polyt序列并入到模板dna分子中,并且将所有datp用受保护α-s-datp替换并在扩增期间使用,则所得产物将包含受保护poly-α-s-datp末端。类似地,如果将8个核苷酸的polya序列并入到模板dna分子中,并且将所有dttp中的25%用受保护α-s-dttp替换并在扩增期间使用,则所得产物将在dna产物的末端区中包含平均两个α-s-dttp。
513、对dna产物的5’末端的保护可通过本文中所述的任何方法实现。类似地,对dna产物的3’末端的保护可通过本文中所述的任何方法实现。然而,用于产生具有受保护3’末端的线性双链dna产物的方法不需要依赖于将同聚序列并入至模板dna分子。例如,dna模板分子的扩增可在不存在受保护核苷酸的情况下进行以产生双链dna产物。可将双链dna产物消化以产生目的dna盒的单个单元。可对该dna盒进行酶促修饰以在3’末端处并入受保护核苷酸。
514、因此,在一个实例中,所述方法可包括:(1)用产生3’隐性端的限制酶对双链dna产物进行消化;以及(2)通过dna聚合酶(例如t4 dna聚合酶或dna聚合酶i大(klenow)片段)将受保护核苷酸并入到3’隐性端中以产生具有受保护3’末端的双链dna产物。
515、在另一个实例中,所述方法可包括:(1)用产生平端的限制酶消化双链dna产物,以及(2)使用受保护核苷酸通过末端转移酶(terminal transferase,tdt)来延伸3’平端。
516、用于产生具有受保护末端的线性双链dna产物或线性双链dna产物文库的方法可依赖于本文中所述方法的组合。例如,在5’末端处的保护可通过在模板分子中使用同聚序列来实现,而在3’末端处的保护可通过dna聚合酶将受保护核苷酸并入到3’隐性端中来实现(在限制酶消化之后)。
517、用于产生线性dna的基于细胞的常规方法是昂贵的而且具有相当大的制备足迹,需要使用大体积的在发酵罐中无菌条件下培养的细菌培养物。从细菌获得经扩增的dna需要细胞裂解,释放对哺乳动物细胞具有毒性的内毒素。因此,必须对dna产物进行纯化以去除这些细菌污染物,特别是用作治疗剂。宿主细菌细胞的复杂生物化学环境可导致批次之间的可重复性问题,以及不同的dna产率和品质。因此,本发明提供了制备具有提高的对核酸酶消化(例如外切核酸酶消化)的抗性的线性双链dna产物的改进方法。所述制备方法可以是无细胞的,使得所述方法耗时较少且更经济。
518、 序列表
519、<110> 4basebio, s.l.u.
520、 4basebio uk ltd
521、<120> 具有增强的针对外切核酸酶的抗性的线性dna
522、<130> p220979wo00
523、<160> 10
524、<170> patentin version 3.5
525、<210> 1
526、<211> 13
527、<212> dna
528、<213> 人工序列
529、<220>
530、<223> 人工序列
531、<400> 1
532、aaaaaacata aaa 13
533、<210> 2
534、<211> 15
535、<212> dna
536、<213> 人工序列
537、<220>
538、<223> 人工序列
539、<400> 2
540、gatcacagtg agtac 15
541、<210> 3
542、<211> 28
543、<212> dna
544、<213> 人工序列
545、<220>
546、<223> 人工序列
547、<400> 3
548、agaagtgtat ctggtactca ctgtgatc 28
549、<210> 4
550、<211> 34
551、<212> dna
552、<213> 噬菌体p1
553、<400> 4
554、ataacttcgt ataatgtatg ctatacgaag ttat 34
555、<210> 5
556、<211> 204
557、<212> dna
558、<213> 人巨细胞病毒
559、<400> 5
560、gtgatgcggt tttggcagta catcaatggg cgtggatagc ggtttgactc acggggattt 60
561、ccaagtctcc accccattga cgtcaatggg agtttgtttt ggcaccaaaa tcaacgggac 120
562、tttccaaaat gtcgtaacaa ctccgcccca ttgacgcaaa tgggcggtag gcgtgtacgg 180
563、tgggaggtct atataagcag agct 204
564、<210> 6
565、<211> 304
566、<212> dna
567、<213> 人巨细胞病毒
568、<400> 6
569、cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc cccgcccatt 60
570、gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc attgacgtca 120
571、atgggtggag tatttacggt aaactgccca cttggcagta catcaagtgt atcatatgcc 180
572、aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt atgcccagta 240
573、catgacctta tgggactttc ctacttggca gtacatctac gtattagtca tcgctattac 300
574、catg 304
575、<210> 7
576、<211> 720
577、<212> dna
578、<213> 维多利亚多管发光水母(aequorea victoria)
579、<400> 7
580、atggtgagca agggcgagga gctgttcacc ggggtggtgc ccatcctggt cgagctggac 60
581、ggcgacgtaa acggccacaa gttcagcgtg tccggcgagg gcgagggcga tgccacctac 120
582、ggcaagctga ccctgaagtt catctgcacc accggcaagc tgcccgtgcc ctggcccacc 180
583、ctcgtgacca ccctgaccta cggcgtgcag tgcttcagcc gctaccccga ccacatgaag 240
584、cagcacgact tcttcaagtc cgccatgccc gaaggctacg tccaggagcg caccatcttc 300
585、ttcaaggacg acggcaacta caagacccgc gccgaggtga agttcgaggg cgacaccctg 360
586、gtgaaccgca tcgagctgaa gggcatcgac ttcaaggagg acggcaacat cctggggcac 420
587、aagctggagt acaactacaa cagccacaac gtctatatca tggccgacaa gcagaagaac 480
588、ggcatcaagg tgaacttcaa gatccgccac aacatcgagg acggcagcgt gcagctcgcc 540
589、gaccactacc agcagaacac ccccatcggc gacggccccg tgctgctgcc cgacaaccac 600
590、tacctgagca cccagtccgc cctgagcaaa gaccccaacg agaagcgcga tcacatggtc 660
591、ctgctggagt tcgtgaccgc cgccgggatc actctcggca tggacgagct gtacaagtaa 720
592、<210> 8
593、<211> 135
594、<212> dna
595、<213> 恒河猴多瘤病毒1
596、<400> 8
597、gatccagaca tgataagata cattgatgag tttggacaaa ccacaactag aatgcagtga 60
598、aaaaaatgct ttatttgtga aatttgtgat gctattgctt tatttgtaac cattataagc 120
599、tgcaataaac aagtt 135
600、<210> 9
601、<211> 19
602、<212> dna
603、<213> 噬菌体t7
604、<400> 9
605、taatacgact cactatagg 19
606、<210> 10
607、<211> 1653
608、<212> dna
609、<213> 北美萤火虫(photinus pyralis)
610、<400> 10
611、atggaagacg ccaaaaacat aaagaaaggc ccggcgccat tctatcctct agaggatgga 60
612、accgctggag agcaactgca taaggctatg aagagatacg ccctggttcc tggaacaatt 120
613、gcttttacag atgcacatat cgaggtgaac atcacgtacg cggaatactt cgaaatgtcc 180
614、gttcggttgg cagaagctat gaaacgatat gggctgaata caaatcacag aatcgtcgta 240
615、tgcagtgaaa actctcttca attctttatg ccggtgttgg gcgcgttatt tatcggagtt 300
616、gcagttgcgc ccgcgaacga catttataat gaacgtgaat tgctcaacag tatgaacatt 360
617、tcgcagccta ccgtagtgtt tgtttccaaa aaggggttgc aaaaaatttt gaacgtgcaa 420
618、aaaaaattac caataatcca gaaaattatt atcatggatt ctaaaacgga ttaccaggga 480
619、tttcagtcga tgtacacgtt cgtcacatct catctacctc ccggttttaa tgaatacgat 540
620、tttgtaccag agtcctttga tcgtgacaaa acaattgcac tgataatgaa ttcctctgga 600
621、tctactgggt tacctaaggg tgtggccctt ccgcatagaa ctgcctgcgt cagattctcg 660
622、catgccagag atcctatttt tggcaatcaa atcattccgg atactgcgat tttaagtgtt 720
623、gttccattcc atcacggttt tggaatgttt actacactcg gatatttgat atgtggattt 780
624、cgagtcgtct taatgtatag atttgaagaa gagctgtttt tacgatccct tcaggattac 840
625、aaaattcaaa gtgcgttgct agtaccaacc ctattttcat tcttcgccaa aagcactctg 900
626、attgacaaat acgatttatc taatttacac gaaattgctt ctgggggcgc acctctttcg 960
627、aaagaagtcg gggaagcggt tgcaaaacgc ttccatcttc cagggatacg acaaggatat 1020
628、gggctcactg agactacatc agctattctg attacacccg agggggatga taaaccgggc 1080
629、gcggtcggta aagttgttcc attttttgaa gcgaaggttg tggatctgga taccgggaaa 1140
630、acgctgggcg ttaatcagag aggcgaatta tgtgtcagag gacctatgat tatgtccggt 1200
631、tatgtaaaca atccggaagc gaccaacgcc ttgattgaca aggatggatg gctacattct 1260
632、ggagacatag cttactggga cgaagacgaa cacttcttca tagttgaccg cttgaagtct 1320
633、ttaattaaat acaaaggata tcaggtggcc cccgctgaat tggaatcgat attgttacaa 1380
634、caccccaaca tcttcgacgc gggcgtggca ggtcttcccg acgatgacgc cggtgaactt 1440
635、cccgccgccg ttgttgtttt ggagcacgga aagacgatga cggaaaaaga gatcgtggat 1500
636、tacgtcgcca gtcaagtaac aaccgcgaaa aagttgcgcg gaggagttgt gtttgtggac 1560
637、gaagtaccga aaggtcttac cggaaaactc gacgcaagaa aaatcagaga gatcctcata 1620
638、aaggccaaga agggcggaaa gtccaaattg taa 1653
- 还没有人留言评论。精彩留言会获得点赞!