KRAS突变蛋白的小分子抑制剂的制作方法
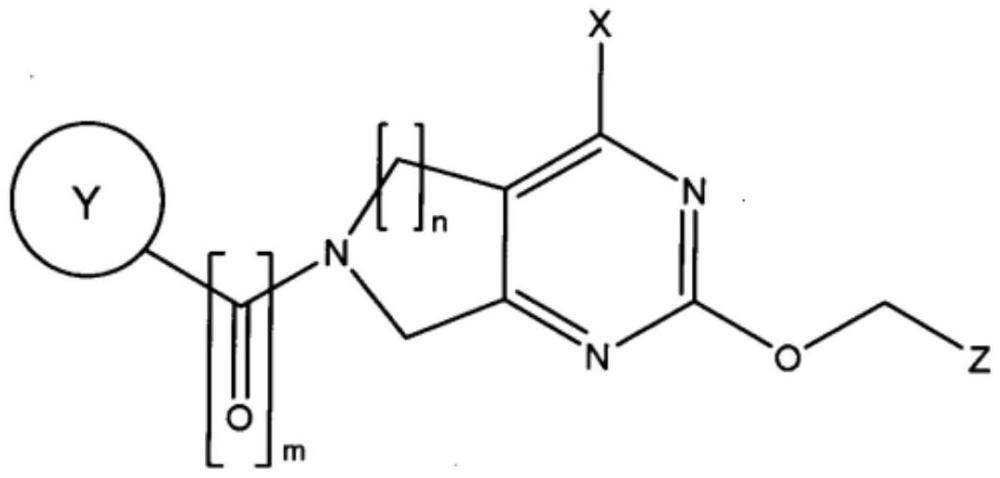
本发明涉及抑制例如kirsten大鼠肉瘤(kras)蛋白的g12c突变体、g12d突变体和g12v突变体的kras小分子抑制剂,并且涉及包含式(i)的化合物的药物组合物以及使用此类化合物治疗包括癌症在内的疾病的方法。
背景技术:
1、ras是分子量约为21kda的小单体gtp结合蛋白,充当分子开/关转换。ras可以通过与鸟嘌呤核苷酸交换因子(gef)(例如,sos1)的蛋白质结合来与gtp结合,从而迫使释放结合的核苷酸,并释放gdp。当ras与gtp结合时,它会被激活(打开)并招募和激活其他受体信号传播所需的蛋白质,例如c-raf和pi 3-激酶。ras还具有酶活性,可切割gtp核苷酸的末端磷酸并将核苷酸转化为gdp。转化速度通常很慢,但可以通过gtp酶激活蛋白(gap)类蛋白质(例如rasgap)显著加快。当gtp转换为gdp时,ras被失活(关闭)。
2、ras亚家族的公知成员包括hras、kras和nras。其中,kras突变在许多恶性肿瘤中观察到:86%的胰腺导管腺癌(pdac)、41%的结直肠癌(crc)和32%的肺腺癌(luad;非小细胞肺癌(nsclc)的一种亚型)。突变通常发生在kras12位甘氨酸残基(“g12”);g12突变分别占kras突变总数的91%(pdac)、68%(crc)和85%(luad)。g12氨基酸取代的分布因组织类型而异。luad中最常见的突变是半胱氨酸(“g12c”)(46%)的突变,而pdac(45%)和crc(45%)中的主要突变是天冬氨酸(“g12d”)的突变。在所有pdac(35%)、crc(30%)和luad(23%)的g12突变中,很大一部分都观察到g12突变为缬氨酸(“g12v”)。(nature reviewsdrug discovery,19,533-552,2020)。
3、正在大力开发kras-g12c抑制剂。目前已经报道了几种针对半胱氨酸残基的共价抑制剂,其中一些已经进行了临床研究,例如amg510(nct03600883)、mrtx849(nct03785249)和jnj-74699157(nct04006301)。然而,kras-g12c突变仅占所有kras突变的一小部分,并且主要发现于luad中。为了有效抑制其他常见的kras突变蛋白,例如kras-g12d和kras-g12v,需要采取不同的方法,因为这些突变体在活性位点缺乏反应性半胱氨酸(nature reviews drug discovery,19,533-552,2020)。
技术实现思路
1、本公开提供了调节突变型kras、hras和/或nras蛋白的小分子抑制剂,并且可以是用于治疗癌症的有价值的药物活性化合物。在一些实施方案中,所公开的化合物选择性抑制kras-g12c、kras-g12d和/或kras-g12v蛋白。式(i)的化合物:
2、
3、及其药学上可接受的盐可以调节kras、hras和/或nras活性的活性,从而影响调节与肿瘤病症相关的细胞生长、分化和增殖的信号传导途径。在某些实施方案中,式(i)的化合物可以抑制kras-g12c、kras-g12d和/或kras-g12v蛋白。本公开还提供了制备式(i)的化合物的方法、使用此类化合物治疗肿瘤病症的方法、以及包含式(i)的化合物的药物组合物。
技术特征:
1.一种式(i)的化合物或其药学上可接受的盐
2.如权利要求1所述的化合物或其药学上可接受的盐,其中环y是
3.如权利要求2所述的化合物或其药学上可接受的盐,其中环y是
4.如权利要求1所述的化合物或其药学上可接受的盐,其中x是
5.如权利要求4所述的化合物或其药学上可接受的盐,其中x被1至4个选自由以下组成的组的rx取代基取代:卤素、羟基、c1-c6烷基、c1-c3羟烷基、c1-c6氟烷基、羧基、氨基甲酰基、c1-c3羧烷基、氧代、氰基、氰基甲基、氨基、吡唑基、噁二唑基、-nhc(o)c1-c3烷氧基c1-c3烷基、-nhc(o)c1-c3烷氧基c6-c10芳基和nhc(o)c5-c10杂芳基,其中杂芳基可被c1-c3烷基取代。
6.如权利要求5所述的化合物或其药学上可接受的盐,其中x是
7.如权利要求1所述的化合物或其药学上可接受的盐,其中x是其中下标p是0、1或2。
8.如权利要求1所述的化合物或其药学上可接受的盐,
9.如权利要求1所述的化合物或其药学上可接受的盐,其中z是
10.如权利要求1所述的化合物或其药学上可接受的盐,其中下标m是1。
11.如权利要求1所述的化合物或其药学上可接受的盐,其中下标n是1。
12.如权利要求1所述的化合物或其药学上可接受的盐,其中下标n是2。
13.如权利要求1所述的化合物,选自实施例1-151,或其药学上可接受的盐。
14.一种药物组合物,其包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐,以及药学上可接受的载剂。
15.一种药物组合物,其包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐、另外的抗癌剂和药学上可接受的载剂。
16.一种抑制kras-g12d蛋白的方法,所述方法包括使kras-g12d蛋白与如权利要求1-13中任一项所述的化合物或其药学上可接受的盐接触以抑制所述kras-g12d蛋白的活性。
17.一种抑制kras-g12c蛋白的方法,所述方法包括使kras-g12c蛋白与如权利要求1-13中任一项所述的化合物或其药学上可接受的盐接触以抑制所述kras-g12c蛋白的活性。
18.一种抑制kras-g12v蛋白的方法,所述方法包括使kras-g12v蛋白与如权利要求1-13中任一项所述的化合物或其药学上可接受的盐接触以抑制所述kras-g12v蛋白的活性。
19.一种治疗癌症的方法,所述方法包括向需要此类治疗的受试者施用治疗有效量的如权利要求1-13中任一项所述的化合物或其药学上可接受的盐。
20.如权利要求19所述的方法,其进一步包括向所述受试者施用另外的活性剂。
21.如权利要求1-13中任一项所述的化合物或其药学上可接受的盐,其用于在疗法中使用,或者如权利要求1-13中任一项所述的化合物或其药学上可接受的盐在疗法中的用途。
22.如权利要求1-13中任一项所述的化合物或其药学上可接受的盐,其用于在治疗癌症中使用,或者如权利要求1-13中任一项所述的化合物或其药学上可接受的盐用于治疗癌症的用途。
23.如权利要求1-13中任一项所述的化合物或其药学上可接受的盐,其用于制备用于治疗癌症的药物,或者如权利要求1-13中任一项所述的化合物或其药学上可接受的盐用于制备用于治疗癌症的药物的用途。
24.如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂,其用于在治疗癌症中使用,或如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂用于治疗癌症的用途。
25.如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂,其用于制备用于治疗癌症的药物,或如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂用于制备用于治疗癌症的药物的用途。
26.包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐的药物组合物,所述药物组合物用于治疗癌症,或者包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐的药物组合物用于治疗癌症的用途。
27.包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂的药物组合物,所述药物组合物用于治疗癌症,或者包含如权利要求1-13中任一项所述的化合物或其药学上可接受的盐和另外的抗癌剂的药物组合物用于治疗癌症的用途。
技术总结
式(I)的化合物或其药学上可接受的盐可以抑制Kirsten大鼠肉瘤(KRAS)蛋白的G12C、G12D和/或G12V突变体并且预期具有作为治疗剂的效用,例如用于治疗癌症。本公开还提供了包含式(I)的化合物或其药学上可接受的盐的药物组合物。本公开还涉及使用所述化合物或其药学上可接受的盐治疗和预防癌症的方法以及制备用于此目的的药物的方法。
技术研发人员:小早川优,大岛豪,伊藤智,P·施奥夫
受保护的技术使用者:大鹏药品工业株式会社
技术研发日:
技术公布日:2024/3/27
- 还没有人留言评论。精彩留言会获得点赞!