一种CD45基因分型检测的引物组合及检测试剂盒和应用
本发明属于基因分型检测,具体涉及一种cd45基因分型检测的引物组合及检测试剂盒和应用。
背景技术:
1、跨膜受体酪氨酸磷酸酶蛋白cd45(ly5,ptprc)是一种在所有有核造血细胞上表达的蛋白,是调控环境信号整合到细胞反应中的关键控制蛋白。对cd45突变细胞系、cd45缺陷小鼠和cd45缺陷人类的研究,初步证实了cd45在抗原受体、细胞因子受体信号转导和淋巴细胞发育中的重要作用。
2、有研究报道在sjl小鼠中鉴定出ptprc位点(编码cd45,也称为ly5)的遗传变异,即ptprca等位基因(编码cd45.1)。cd45常见的形式是cd45.2,在c57bl/6小鼠表达;而sjl小鼠则表达cd45.2。cd45.1和cd45.2等位基因在细胞外结构域只存在5个氨基酸的差异,并且这种编码变异不影响其功能,但其独特的表位变化可以通过单克隆抗体进行特异性识别。为了使用cd45的突变作为实验工具,研究人员将sjl小鼠的ptprca等位基因反交至c57bl/6小鼠,以产生b6.sjl-ptprcapepcb小鼠(即b6.sjl-cd45.1小鼠)。b6.sjl-cd45.1小鼠广泛应用于竞争性移植模型、混合骨髓嵌合体实验等免疫研究中,通过使用cd45.2或cd45.1特异性的单克隆抗体可以示踪移植的细胞。
3、鉴定cd45.1是b6.sjl-cd45.1小鼠应用的重要环节。近年来已发展出单克隆抗体、荧光探针,sanger测序等方法。其中,sanger测序法的优点是准确度高,但存在设备要求高、耗时长、成本高等缺点,多数实验室不具备自行检测的条件。单克隆抗体法常使用小鼠眼眶取血,采样困难、要求相对较多的活细胞才能用于后续检测,且样本前处理步骤繁琐、需要流式检测、成本昂贵、准确度不高,重复性差。荧光探针法同样存在样本前处理步骤繁琐、成本昂贵、特异性不强、耗时长等缺点。
4、因此,开发一种新型简单、高效、准确、经济的cd45.1鉴定方法对b6.sjl-cd45.1小鼠的广泛应用具有重大意义。
技术实现思路
1、针对现有技术存在的不足,本发明的目的在于提供一种cd45基因分型检测的引物组合及检测试剂盒和应用。本发明提供了一种经济、简单、高效、准确的b6.sjl-cd45.1小鼠(以下简称cd45.1小鼠)鉴定手段,通过截取小鼠少量组织提取小鼠dna,取dna样品用特异性引物进行pcr扩增,最后将pcr产物进行琼脂糖凝胶电泳,通过凝胶成像系统拍照即可得到鉴定结果。所述方法操作简便,成本低廉,结果准确且耗时极短,可极大地降低b6.sjl-cd45.1小鼠的鉴定难度,在保证其鉴定结果准确性的同时,节约成本以及人力物力。
2、为达到此发明目的,本发明采用以下技术方案:
3、第一方面,本发明提供一种cd45基因分型检测的引物组合,所述引物组合包括检测cd45.1的引物和阳性对照引物;
4、所述检测cd45.1的引物包括seq id no:3和seq id no:6所示的核苷酸序列。
5、本发明中,所述检测cd45.1的引物可扩增cd45.1序列,而无法扩增cd45.2序列,所述阳性对照引物对cd45.1和cd45.2序列均可有效扩增,用于判定pcr扩增反应及实验流程是否成功。
6、优选地,所述阳性对照引物包括seq id no:1和seq id no:6所示的核苷酸序列。
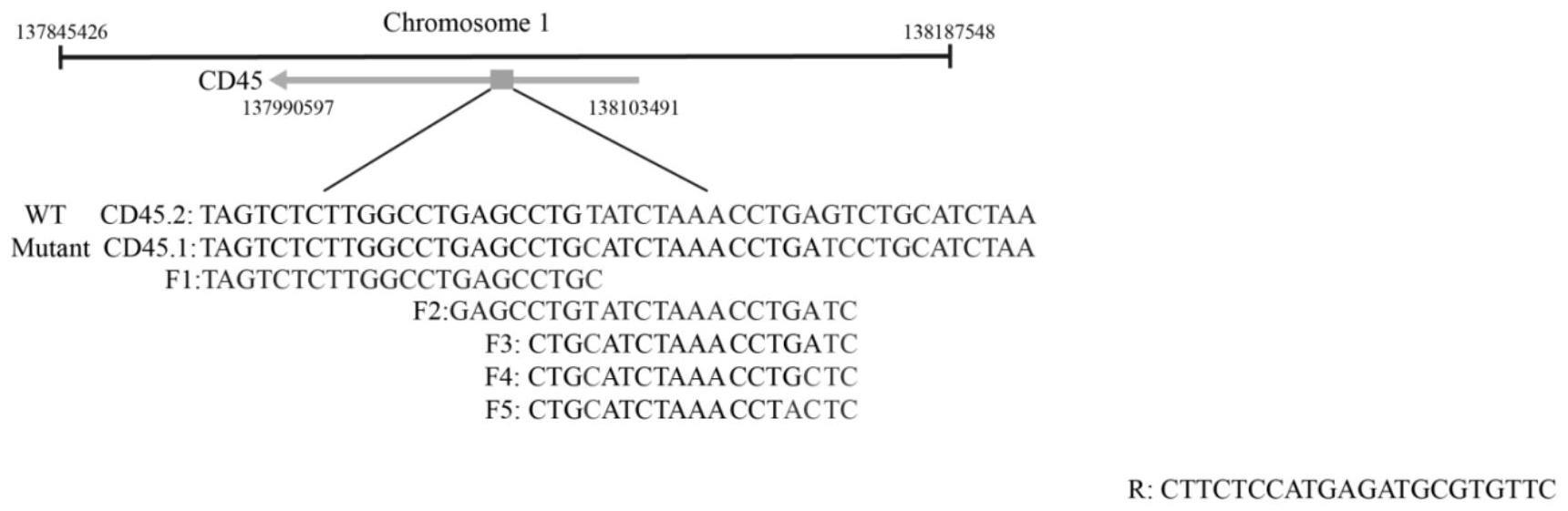
7、f3:seq id no:3:ctgcatctaaacctgatc;
8、r:seq id no:6:cttctccatgagatgcgtgttc;
9、f1:seq id no:1:tagtctcttggcctgagcctgc;
10、r:seq id no:6:cttctccatgagatgcgtgttc。
11、本发明中,f1+r引物在同样的pcr条件下,既可以扩增突变型cd45.1小鼠的dna,又可以扩增出与f1引物3’端不匹配的野生型cd45.2小鼠的dna,不具有任何特异性。因此,将f1+r引物设置为试剂盒中的阳性对照引物,用于判定pcr扩增反应及实验流程是否成功。
12、本发明中,合成了与cd45.1匹配较高,但与cd45.2具有更多碱基错配的引物f3,f3+r引物可以在退火温度62-64℃的情况下有效识别cd45.1小鼠的dna,而cd45.2小鼠的dna则无法扩增,因此,以f3+r引物作为检测cd45.1的引物。
13、第二方面,本发明提供一种cd45基因分型检测的试剂盒,所述试剂盒中含有第一方面所述的cd45基因分型检测的引物组合。
14、优选地,所述试剂盒中还含有dna快速提取试剂和/或保真扩增酶体系。
15、优选地,所述dna快速提取试剂中包含消化液和中止液。
16、优选地,所述消化液为30-100mm的naoh溶液,例如可以是30mm、50mm、80mm或100mm等。
17、优选地,所述中止液为0.5-2m的tris-hcl溶液,例如可以是0.5m、0.6m、1.0m或2.0m等,ph为6-7.5,例如可以是6、6.5、7、7.3或7.5等。
18、优选地,所述保真扩增酶体系为:primestar max dna polymerase体系。
19、第三方面,本发明提供一种cd45基因分型检测方法,所述检测方法包括:
20、(1)采用第二方面所述的cd45基因分型检测的试剂盒提取小鼠dna;
21、(2)基于提取的小鼠dna,利用第一方面所述的cd45基因分型检测的引物组合进行pcr扩增;
22、(3)将pcr产物进行琼脂糖凝胶电泳,根据电泳结果判断cd45基因的基因型。
23、优选地,步骤(2)中,所述pcr扩增实验中的扩增体系按终浓度计包括:检测cd45.1的引物或阳性对照引物0.5-2μm(例如可以是0.5μm、0.8μm、1μm、1.2μm、1.5μm、1.8μm或2μm等),1×primestar max dna polymerase。
24、优选地,步骤(2)中,所述pcr扩增实验中的扩增程序为:
25、预变性:95-98℃,20-40s;变性:95-98℃,8-15s;退火:62-64℃,8-15s;延伸:70-72℃,10-30s;变性-延伸:32-35个循环;补充延伸:70-72℃,2-5min。
26、本发明所述扩增程序中,预变性:95-98℃,20-40s;预变性的温度例如可以是95℃、96℃、97℃或98℃等,预变性的时间例如可以是20s、30s或40s等;
27、变性:95-98℃,8-15s;变性的温度例如可以是95℃、96℃、97℃或98℃等,变性的时间例如可以是8s、10s或15s等;
28、退火:62-64℃,8-15s;退火的温度例如可以是62℃、63℃或64℃等,退火的时间例如可以是8s、10s或15s等;
29、延伸:70-72℃,10-30s;延伸的温度例如可以是70℃、71℃或72℃等,延伸的时间例如可以是10s、20s或30s等;
30、变性-延伸:32-35个循环(例如可以是32、33、34或35),补充延伸:70-72℃,2-5min,补充延伸的温度例如可以是70℃、71℃或72℃等,补充延伸的时间例如可以是2min、3min或5min等。
31、优选地,步骤(3)中,所述判断cd45基因的基因型的标准包括:
32、在阳性对照引物成功扩增出产物前提下;若检测cd45.1的引物成功扩增出pcr产物,则样品为cd45.1突变型基因型;若检测cd45.1的引物无法扩增出pcr产物,则样品为cd45.2野生型基因型。
33、第四方面,本发明提供第一方面所述的cd45基因分型检测的引物组合、第二方面所述的cd45基因分型检测的试剂盒或第三方面所述的cd45基因分型检测方法中任意一种或至少两种的组合在cd45基因分型检测中的应用。
34、本发明所述的数值范围不仅包括上述列举的点值,还包括没有列举出的上述数值范围之间的任意的点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
35、相对于现有技术,本发明具有以下有益效果:
36、(1)提升检测速度、降低操作难度。应用本发明所提供的试剂盒,将鉴定cd45.1突变的时间降低至1.5小时,且操作简单,无复杂精密的操作,极大地节约了时间和人力成本。
37、(2)降低检测成本、减少对贵重仪器的依赖。应用本发明所提供的试剂盒,单次样本检测成本低至1.78元,且无需依赖贵重仪器,仅需普通pcr仪即可完成检测,所需成本大幅降低,常规实验室均能自行完成cd45.1突变小鼠的基因型鉴定。
38、(3)提高检测灵敏度。应用本发明所提供的试剂盒,检测限可低至0.0001ng/μl,仅需微量dna即可鉴定,提高了检测灵敏度,克服了现有鉴定技术对样本收集要求高的困难。
- 还没有人留言评论。精彩留言会获得点赞!