SynNotch受体及其用途的制作方法
本领域属于生物,具体地,本发明涉及一种synnotch受体及其用途,更具体地,本发明涉及一种分离的多肽在制备synnotch合成受体中的用途、嵌合多肽、第一核酸分子、第一表达载体、重组细胞、药物组合物及其用途、激活免疫细胞的方法、追踪第一细胞-第二细胞接触的方法。
背景技术:
1、随着合成生物学的发展,通过改造细胞使之可以识别细胞外特定的信号,并在改造的细胞中传递识别到的信号,进而做出人工设计的反应已经成为现实,并已经逐渐在生物医疗领域展开了应用。如嵌合抗原受体(car)技术在临床治疗中的应用,除此之外,在2016年,wend ell a.lim团队基于notch信号通路开发出了一套synnotch受体系统,该系统同样可以识别细胞膜表面配体,并且其信号输出并不局限于单纯的免疫细胞激活信号,可以实现多种不同的信号输出类型,如特定基因的表达激活与抑制等。该受体系统可以实现不同输入信号与输出信号的多种组合,且同一体系(细胞)内的多组系统间具有正交性;同时在众多细胞中均可运行,具有普适性;同时具有简易性和可调控性等诸多优秀特征,是应用合成生物学对细胞进行改造的一个强力工具。
2、生物学中,传统的notch信号通路(系统)包括notch对应的配体、notch分子和notch调控的下游基因。其中notch分子是一个跨膜分子,其可以分为胞外结构、跨膜结构域和胞内结构域3个部分。其胞外结构域与对应的notch配体结合后,配体所在的细胞出现胞吞活动,拉扯notch分子,使notch分子的胞外结构域上的s2蛋白酶切割位点暴露出来,被金属蛋白酶adams家族成员等切割;进一步的,伴随着胞外结构域的切割断裂,notch分子的胞内结构域被γ-分泌酶切割后释放到细胞内,随后入核作为转录因子调控下游相关基因的表达。wend ell a.lim团队改造了鼠的notch1受体,将其胞外域用单链抗体或者纳米抗体替换,胞内域用转录激活或转录抑制的结构域替换,仅保留了可以被蛋白酶识别切割的跨膜结构域,还配备了下游被调控的基因元件。针对不同靶标,胞外域采用特异识别该抗原的抗体单链,而胞内域调控预先设定的目标基因或因子的表达。在同一细胞中可以设计由不同抗原启动的基因调控环路,并具有很好的正交性。synnotch系统可以被应用到许多细胞类型中,包括神经细胞、肿瘤细胞、表皮细胞和免疫细胞等。car技术和synnotch系统组合应用到免疫细胞改造中,可以实现免疫细胞的“与门”激活,即只有当细胞同时表达两种特定的表面抗原时,才能将免疫细胞激活。改变synnotch下游调控的基因元件,免疫细胞可以在接触特定抗原后,分泌单链抗体、细胞因子等等具有治疗作用的因子,并且在体外、体内都具有抗肿瘤的作用。可见synnotch受体系统,在细胞改造中具有极大的技术优势。
技术实现思路
1、本发明旨在至少在一定程度上解决现有技术中存在的技术问题至少之一。为此,本发明提供了一种synnotch受体,该synnotch受体可增强其对下游基因的激活能力和减少本底泄露激活水平。
2、本发明是基于发明人的下列发现而完成的:
3、synnotch系统功能十分强大,但是目前常用的初始版本synnotch系统(又称synnotch合成受体、synnotch)具有如下缺点:第一,初始版本synnotch被激活后,其下游转录表达调控能力并不是很强,即激活下游基因的表达量并不很高,会局限synnotch的使用,特别是针对需要下游基因有较高的表达量才能发挥效用的情况。第二,初始版本synnotch的本底泄露水平较高,对于下游需要严谨调控的基因,其较高水平的泄露表达可能会导致synnotch分子开关的失效,分子表达线路会直接越过synnotch分子开关实现表达。
4、然而,发明人经过试验意外发现,上述问题的关键点在于synnotch分子的跨膜结构域存在不足。初始版本synnotch合成受体选择了小鼠来源notch分子的跨膜结构域来作为synnotch合成受体的跨膜结构域。考虑到不同种属来源的notch跨膜结构域上所携带的s2和s3切割序列存在差异,以及不同物种来源的s2和s3切割酶存在的构象和序列偏好性,在不同物种的细胞中,使用不同的跨膜结构域所构建的synnotch合成受体其激活效率和泄露效率必然有所差异。发明人以用synnotch合成受体改造人源细胞为最终目的,在试验过程中意外发现选择热带爪蟾的notch跨膜结构域,可以提高synnotch合成受体对下游基因转录激活的能力和效率,以及降低synnotch合成受体的本底泄露激活,使synnotch合成受体能够更加有效的发挥作用。
5、因此,在本发明的一个方面,本发明提出了一种分离的多肽在制备synnotch合成受体中的用途,所述分离的多肽与来源于热带爪蟾(xenopus tropicalis)的notch受体蛋白的跨膜区具有至少80%的同一性。发明人发现,选择热带爪蟾的notch受体蛋白的跨膜区制备的synnotch合成受体,可以提高其对下游基因转录激活的能力和效率,降低synnotch合成受体的本底泄露。
6、本发明的另一方面,本发明提出了一种嵌合多肽。根据本发明的实施例,所述嵌合多肽包括:胞外区,所述胞外区具有结合第一分子活性;跨膜区,所述跨膜区的n端与所述胞外区的c端相连;胞内区,所述胞内区的n端与所述跨膜区的c端相连;其中,所述跨膜区包括分离的多肽,所述分离的多肽与来源于热带爪蟾的notch受体蛋白的跨膜区具有至少80%的同一性。本发明的嵌合多肽选择热带爪蟾的notch受体蛋白的跨膜区作为嵌合多肽(即为synnotch合成受体)的跨膜区,可以提高嵌合多肽对下游基因转录激活的能力和效率,以及降低嵌合多肽的本底泄露。
7、在本发明的又一方面,本发明提出了一种第一核酸分子。根据本发明的实施例,所述第一核酸分子编码权利要求前述的嵌合多肽。根据本发明实施例的第一核酸分子所编码前述的嵌合多肽。
8、在本发明的又一方面,本发明提出了一种第一表达载体。根据本发明的实施例,所述第一表达载体携带前述的第一核酸分子。本发明的第一表达载体导入合适的接收细胞后,可实现前述的嵌合多肽的表达。
9、在本发明的又一方面,本发明提出了一种重组细胞。根据本发明的实施例,所述重组细胞包括:携带前述的第一核酸分子或前述的第一表达载体;或,表达前述的嵌合多肽。本发明的重组细胞可有效地表达前述的嵌合多肽。
10、在本发明的又一方面,本发明提出了一种药物组合物。根据本发明的实施例,所述药物组合物包括前述的嵌合多肽、前述的第一核酸分子、前述的第一表达载体或前述的重组细胞。由前可知,表达上述嵌合多肽的细胞可识别第一分子,其在结合第一分子后可以实现多种不同的信号输出类型,如特定基因的表达激活与抑制等,或者采用表达嵌合多肽的免疫细胞在接触第一分子后,可分泌具有治疗作用的因子(如单链抗体、细胞因子等),用于抗肿瘤;并且,第一核酸分子和第一表达载体可在细胞(例如免疫细胞)表达嵌合多肽,前述的重组细胞上可表达嵌合多肽。因此,采用含有前述的嵌合多肽、第一核酸分子、第一表达载体或重组细胞的药物组合物可靶向第一分子,用于预防和/或治疗相关疾病,例如用于治疗癌症等。
11、在本发明的又一方面,本发明提出了一种前述的嵌合多肽、前述的第一核酸分子、前述的第一表达载体、前述的重组细胞或前述的药物组合物在制备药物中用途,所述药物用于预防和/或治疗疾病。由前可知,表达上述嵌合多肽的细胞可识别第一分子,其在结合第一分子后可以实现多种不同的信号输出类型,如特定基因的表达激活与抑制等,或者采用表达嵌合多肽的免疫细胞在接触第一分子后,可分泌具有治疗作用的因子(如单链抗体、细胞因子等),用于抗肿瘤;并且,第一核酸分子和第一表达载体可在细胞(例如免疫细胞)表达嵌合多肽,前述的重组细胞上可表达嵌合多肽,以及药物组合物包含前述的嵌合多肽、第一核酸分子、第一表达载体或重组细胞。由此,含有嵌合多肽、第一核酸分子、第一表达载体、重组细胞或药物组合物的药物可靶向第一分子,用于预防和/或治疗相关疾病,例如用于治疗癌症等。
12、在本发明的又一方面,本发明提出了一种激活免疫细胞的方法。根据本发明的实施例,所述方法包括:将所述免疫细胞与第一分子进行第一接触,其中,所述免疫细胞表达前述的嵌合多肽。由此,表达上述嵌合多肽的免疫细胞可识别第一分子,其在结合第一分子后可以实现激活免疫细胞。
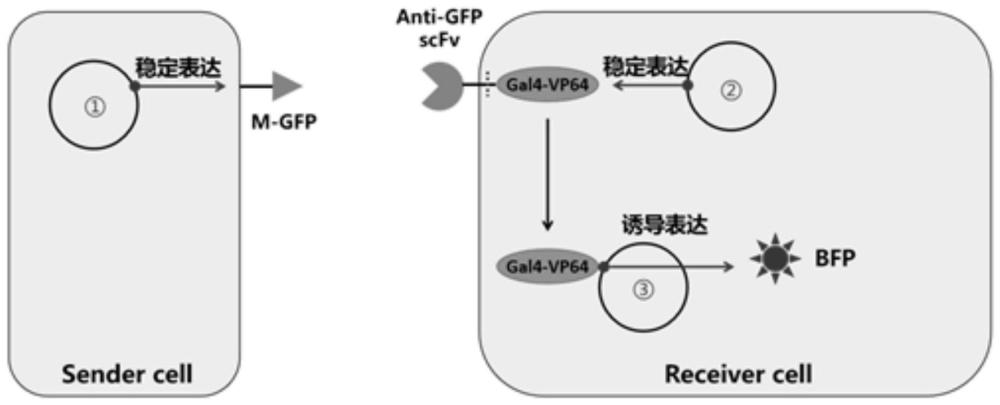
13、在本发明的又一方面,本发明提出了一种追踪第一细胞-第二细胞接触的方法。根据本发明的实施例,所述方法包括:将所述第一细胞和所述第二细胞进行第二接触,其中,所述第一细胞表达前述的嵌合多肽和报告基因蛋白,所述嵌合多肽的胞内区为转录激活蛋白,编码所述报告基因蛋白的第三核酸分子的5’端与诱导表达核酸序列与诱导表达核酸序列相连,所述诱导表达核酸序列用于结合所述转录激活蛋白,所述第二细胞表达所述第一分子;基于所述第一细胞中所述报告基因蛋白的检测结果,确定第一细胞和第二细胞的接触情况。由此,采用上述方法可基于报告基因蛋白的检测结果,确定第一细胞和第二细胞之间是否接触。
14、本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
- 还没有人留言评论。精彩留言会获得点赞!