拮抗性抗肿瘤坏死因子受体超家族抗体的制作方法
发明领域本发明涉及能够拮抗肿瘤坏死因子受体2的多肽,如抗体及其抗原结合片段。本发明的多肽可用于调节调控性t细胞的活性,以及上调t效应细胞的活性并直接调节表面致癌基因,如用于治疗细胞增殖病症和感染性疾病的免疫疗法领域中。
背景技术:
0、发明背景
1、使用天然存在的和遗传工程化的t淋巴细胞是用于改善各种人类病理的突出范式。例如,虽然用于治疗癌症的传统治疗平台包括手术切除肿瘤块、放射疗法和施用化学治疗剂(shewach,chem.rev.,109:2859-2861,2009),但是过去十年见证了过继性免疫疗法应用于癌症治疗方案中的再现。随着嵌合抗原受体(car-t)疗法的出现,已经出现了向患者输注自体和同种异体肿瘤反应性t细胞的新方法(june,j.clin.invest.,117:1466-1476,2007)。car-t疗法利用适应性免疫响应的资源以促进癌细胞细胞毒性并根除肿瘤物质。过继性免疫疗法中的常见基序是使用t细胞,所述t细胞表现出在展示不同肿瘤抗原的细胞中选择性地加强细胞毒性的能力。这种技术的实例包括施用肿瘤浸润性淋巴细胞(dudley等人,j.immunother.,26:332-342,2003),以及已经遗传重新工程化以便表现出与肿瘤特异性抗原的反应性的自体或同种异体t细胞(yee等人,pnas.,99:16168-16173,2002)。
2、尽管基于t淋巴细胞的癌症免疫疗法具有前景,但这种治疗平台的开发一直受免疫系统遏制自身细胞上固定的免疫攻击的自然倾向阻碍。与所有有核人细胞一样,癌细胞表达i类主要组织相容性复合物(mhc)蛋白,所述蛋白将这些细胞与外来细胞区分开来。为了防止细胞自相残杀,已经进化出调控性t细胞(t-reg细胞),所述调控t细胞遏制表现出针对“自身”mhc抗原的反应性的t细胞的活性。t-reg细胞代表异质类t细胞,所述t细胞可基于其独特的表面蛋白呈递来区分。最容易理解的t-reg细胞群体包括cd4+、cd25+、foxp3+t-reg细胞和cd17+t-reg细胞。这些细胞介导自身反应性t细胞的遏制的确切机制是正在进行的研究的主题,但是已经显示某些类别的t-reg细胞抑制靶t细胞中诱导增殖的细胞因子il-2的产生,并且可另外地凭借cd25(il-2受体的亚结构域)对il-2的亲和力螯合来自自身反应细胞的il-2(josefowicz等人,ann.rev.immun.,30:531-564,2012)。
3、虽然t-reg细胞在维持外周耐受中起重要作用,但构成这些细胞调节自身反应性t细胞活性的能力的基础的相同生物化学特征也用于通过遏制肿瘤反应性t淋巴细胞的活性来破坏过继性免疫疗法和天然免疫响应。t-reg细胞活性的化学调节剂的开发已经成为许多药理学研究的主题,因为获得能够抑制t-reg介导的t细胞遏制的剂可极大地提高过继性癌症免疫疗法的范围和功效,以及提高免疫系统根除引起感染性疾病的病原生物体的能力。
4、已经在t-reg细胞表面上鉴定了肿瘤坏死因子受体(tnfr)亚型1和2作为决定细胞命运的信号转导分子。例如,tnfr1的活化加强了半胱天冬酶信号传导级联并终止于t-reg细胞凋亡,而tnfr2的活化通过有丝分裂原活化的蛋白激酶(mapk)信号传导途径诱导信号传导,其协调通过traf2/3信号传导和nfκb介导的促进逃避细胞凋亡和细胞增殖的基因的转录。由于其在指导细胞存活和生长中的作用,tnfr2代表了用于防止肿瘤反应性t淋巴细胞的免疫检测的有吸引力的靶标。因此,目前需要用于靶向细胞增殖病症(如癌症)和多种感染性疾病的治疗中的能够阻止t-reg细胞存活和增殖的疗法。
技术实现思路
1、本发明提供了拮抗性肿瘤坏死因子受体2(tnfr2)多肽,如单链多肽、抗体以及其抗原结合片段。本发明的拮抗性tnfr2多肽特异性地结合人tnfr2内含有kcrpg序列(seq idno:19)的一个或多个残基的表位或非人灵长类动物(例如,野牛或牛,如本文所描述)的tnfr2中的等效表位,并且不会特异性地结合人tnfr2内的kcspg基序(seq id no:12)的残基或非人灵长类动物的tnfr2中的等效表位。本文所述的多肽(例如,单链多肽、抗体以及其抗原结合片段)可用于治疗多种病理,包括癌症和感染性疾病。
2、本发明的拮抗性tnfr2多肽如此描述,因为它们表现出抑制t-reg细胞的增殖和/或促进t-reg细胞的死亡的能力。本发明的拮抗性tnfr2多肽可抑制表达tnfr2和致癌基因的癌细胞的增殖和/或促进所述癌细胞的死亡。本发明的拮抗性tnfr2多肽可允许t效应细胞(如细胞毒性cd8+t细胞)的相互扩增。例如,这可能由于t-reg细胞增殖和活性的减弱而发生。本发明的拮抗性tnfr2多肽可直接扩增t效应细胞,如cd8+细胞毒性t细胞。因此,本发明的tnfr2多肽作为拮抗剂的名称是指它们减弱表达t-reg和tnfr2的癌细胞的增殖和活性的能力,并且为清楚起见不表示t效应细胞响应的拮抗作用。
3、本文公开了能够特异性地结合人tnfr2的多肽,如单链多肽、抗体或其抗原结合片段,所述多肽含有互补决定区-重链1(cdr-h1)和源自tnfr2抗体的cdr-h2以及具有氨基酸序列jz1jz2z4jz3jz5(j)2z5z2z5、jz1jz2z4z3z5(j)2z5z2z5(j)2、jrjdgjsjy(j)2fdj(seq id no:278)、jrjdgsy(j)2fd(j)3(seq id no:279)、qz1vz2z4yz3sz5wyz5z2z5(seq id no:265)或az1dz2z4z3z5spz5z2z5wg(seq id no:266)的cdr-h3,其中
4、每个j独立地是天然存在的氨基酸;
5、每个z1独立地是含有在生理ph下的阳离子侧链的天然存在的氨基酸,如赖氨酸、精氨酸和组氨酸;
6、每个z2独立地是含有在生理ph下的阴离子侧链的天然存在的氨基酸,如天冬氨酸和谷氨酸;
7、每个z3独立地是含有在生理ph下的极性不带电荷的侧链的天然存在的氨基酸,如丝氨酸、苏氨酸、天冬酰胺和谷氨酰胺;
8、每个z4独立地是甘氨酸或丙氨酸;并且
9、每个z5独立地是含有疏水性侧链的天然存在的氨基酸,如丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸和甲硫氨酸、色氨酸、苯丙氨酸以及酪氨酸。如本文在多肽式的上下文中所使用的,下标符号中的数字字符表示所述式中存在的在前的氨基酸的量,并且上标符号中的数字字符表示所述式中存在的前述氨基酸的类型。
10、在第一方面,本发明的特征是一种能够特异性地结合人肿瘤坏死因子受体2(tnfr2)的多肽,如单链多肽、抗体或其抗原结合片段,其中所述单链多肽、抗体或其抗原结合片段含有cdr-h3,所述cdr-h3具有以下氨基酸序列:
11、(a)jrjdgsy(j)2fd(j)3(seq id no:279);
12、(b)az1dz2z4z3z5spz5z2z5wg(seq id no:266);或
13、(c)arddgsyspfdywg(seq id no:259),或者相对于所述序列具有至多两个氨基酸取代的氨基酸序列;
14、其中每个j独立地是天然存在的氨基酸;
15、每个z1独立地是包含在生理ph下的阳离子侧链的天然存在的氨基酸,如赖氨酸、精氨酸和组氨酸;
16、每个z2独立地是包含在生理ph下的阴离子侧链的天然存在的氨基酸,如天冬氨酸和谷氨酸;
17、每个z3独立地是包含在生理ph下的极性不带电荷的侧链的天然存在的氨基酸,如丝氨酸、苏氨酸、天冬酰胺和谷氨酰胺;
18、每个z4独立地是甘氨酸或丙氨酸;并且
19、每个z5独立地是包含疏水性侧链的天然存在的氨基酸,如丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸和甲硫氨酸、色氨酸、苯丙氨酸以及酪氨酸。
20、在一些实施方案中,在以上cdr-h3存在下,所述抗体或其抗原结合片段能够特异性地结合包含lrkcrpgfgva(seq id no:285)或vvckpcapgtfsn(seq id no:286)的氨基酸序列的肽。在一些实施方案中,在以上cdr-h3存在下,所述抗体或其抗原结合片段能够特异性地结合seq id no:7的氨基酸142-149(kcrpgfgv)或氨基酸161-169(ckpcapgtf)内的表位。
21、在一些实施方案中,所述cdr-h3具有氨基酸序列arddgsyspfdywg(seq id no:259)。在一些实施方案中,所述cdr-h3具有氨基酸序列arddgsyspfdyfg(seq id no:284)。
22、在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有以下区(cdr)中的一个或多个或全部:
23、(a)cdr-h1,所述cdr-h1具有氨基酸序列gjtf(j)2yj(seq idno:277);
24、(b)cdr-h2,所述cdr-h2具有氨基酸序列(j)5gsj;
25、(c)cdr-l1,所述cdr-l1具有氨基酸序列(j)5y;
26、(d)cdr-l2,所述cdr-l2具有氨基酸序列(j)2s;以及
27、(e)cdr-l3,所述cdr-l3具有氨基酸序列(j)3y(j)4t。
28、其中每个j独立地是天然存在的氨基酸。
29、在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有以下区(cdr)中的一个或多个或全部:
30、(a)cdr-h1,所述cdr-h1具有氨基酸序列z4yz3z5tdz5x;
31、(b)cdr-h2,所述cdr-h2具有氨基酸序列vdpeyz4z3t(seq id no:264);
32、(c)cdr-l1,所述cdr-l1具有氨基酸序列qninkz5(seq id no:268);
33、(d)cdr-l2,所述cdr-l2具有氨基酸序列tyz3或ytz3;以及
34、(e)cdr-l3,所述cdr-l3具有氨基酸序列clqz5vnlxz3(seq id no:271);
35、其中每个z1独立地是包含在生理ph下的阳离子侧链的氨基酸;
36、每个z2独立地是包含在生理ph下的阴离子侧链的氨基酸;
37、每个z3独立地是包含在生理ph下的极性不带电荷的侧链的氨基酸;
38、每个z4独立地是甘氨酸或丙氨酸;
39、每个z5独立地是包含疏水性侧链的氨基酸;以及
40、每个x独立地是亮氨酸或异亮氨酸。
41、在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有以下区(cdr)中的一个或多个或全部:
42、(a)cdr-h1,所述cdr-h1具有氨基酸序列gytftdyx(seq id no:257)或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;
43、(b)cdr-h2,所述cdr-h2具有氨基酸序列vdpeygst(seq id no:258)或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;
44、(c)cdr-l1,所述cdr-l1具有氨基酸序列qninky(seq id no:260)或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;
45、(d)cdr-l2,所述cdr-l2具有氨基酸序列tys或yts;以及
46、(e)cdr-l3,所述cdr-l3具有氨基酸序列clqyvnlxt(seq id no:261)或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;
47、其中每个x独立地是亮氨酸或异亮氨酸。
48、在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有以下区(cdr)中的一个或多个或全部:
49、(a)cdr-h1,所述cdr-h1具有氨基酸序列gytftdyx(seq id no:257);
50、(b)cdr-h2,所述cdr-h2具有氨基酸序列vdpeygst(seq id no:258);
51、(c)cdr-l1,所述cdr-l1具有氨基酸序列qninky(seq id no:260);
52、(d)cdr-l2,所述cdr-l2具有氨基酸序列tys或yts;以及
53、(e)cdr-l3,所述cdr-l3具有氨基酸序列clqyvnlxt(seq id no:261)。
54、其中每个x独立地是亮氨酸或异亮氨酸。
55、在一些实施方案中,所述cdr-h1具有氨基酸序列gytftdyl(seq id no:274)。在一些实施方案中,所述cdr-h1具有氨基酸序列gytftdyi(seq id no:275)。
56、在一些实施方案中,所述cdr-l2具有氨基酸序列tys。在一些实施方案中,所述cdr-l2具有氨基酸序列yts。
57、在一些实施方案中,所述cdr-l3具有氨基酸序列clqyvnllt(seq id no:272)。在一些实施方案中,所述cdr-l3具有氨基酸序列clqyvnlit(seq id no:273)。
58、在一些实施方案中,所述cdr-h1具有氨基酸序列gytftdyl(seq id no:274),并且所述cdr-l3具有氨基酸序列clqyvnlit(seq id no:273)。
59、在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有含与cdr-l2的n-末端结合的氨基酸序列llir(seq id no:262)的框架区。在一些实施方案中,所述单链多肽、抗体或其抗原结合片段含有含与cdr-l2的c-末端结合的氨基酸序列tle的框架区。
60、在一些实施方案中,所述单链多肽、抗体或抗原结合片段不包含以下cdr中的一个或多个:
61、(a)cdr-h1,所述cdr-h1具有氨基酸序列gftfssy(seq id no:23);
62、(b)cdr-h2,所述cdr-h2具有氨基酸序列ssggsy(seq id no:24);以及
63、(c)cdr-l1,所述cdr-l1具有氨基酸序列sasssvyymy(seq id no:26);
64、(d)cdr-l2,所述cdr-l2具有氨基酸序列stsnlas(seq id no:27);
65、(e)cdr-l3,所述cdr-l3具有氨基酸序列qqrrnypyt(seq id no:28);
66、(f)cdr-l1,所述cdr-l1含有氨基酸序列rasksvstsgysymh(seq id no:29);
67、(g)cdr-l2,所述cdr-l2含有氨基酸序列lasnles(seq id no:30);以及
68、(h)cdr-l3,所述cdr-l3含有氨基酸序列qhsrelprt(seq id no:31)。
69、在一些实施方案中,所述抗体或其抗原结合片段含有非天然恒定区(如人恒定区),缺乏fc结构域的全部或一部分,缺乏天然fc结构域的全部或一部分,或者完全缺乏fc结构域。
70、在另一方面,本发明提供含有第一多肽结构域和第二多肽结构域的构建体,所述结构域各自含有本发明的单链多肽。所述第一多肽结构域和第二多肽结构域可以是相同的。在一些实施方案中,所述第一多肽结构域和第二多肽结构域可以是不同的。所述第一多肽结构域和第二多肽结构域可通过接头结合,所述接头如含有酰胺键或二硫桥键的接头。所述构建体可缺乏鼠类fc结构域。
71、本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可以小于约100nm的kd特异性地结合至含有seq id no:11、19、20和34-117中任一者的氨基酸序列的肽,并且不结合含有seq id no:7的氨基酸56-60(kcspg)的肽。类似地,本发明的多肽(如单链多肽、抗体或其抗原结合片段)可特异性地结合含有seq id no:7的氨基酸142-146(kcrpg)中的一个或多个的肽,并且不结合含有seq id no:7的氨基酸56-60(kcspg)的肽。
72、本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可抑制tnfr2信号传导。在一些实施方案中,所述单链多肽、抗体或其抗原结合片段降低或抑制选自由chuk、nfkbie、nfkbia、map3k11、traf2、traf3、relb以及ciap2/birc3组成的组的一种或多种基因的表达。在一些实施方案中,所述单链多肽、抗体或其抗原结合片段抑制nfκb活化。例如,本发明的拮抗性tnfr2单链多肽、抗体或其抗原结合片段可使chuk、nfkbie、nfkbia、map3k11、traf2、traf3、relb或ciap2/birc3中的一种或多种的表达或翻译后修饰(例如,磷酸化)相对于从未用本发明的拮抗性tnfr2单链多肽、抗体或其抗原结合片段处理的样品中分离的这些分子中的一种或多种的表达或翻译后修饰(例如,磷酸化)降低或抑制例如1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。可用于测定表达水平和磷酸化状态的示例性测定是本领域中已知的,并且包括用于测定蛋白质含量的蛋白质印迹测定和用于测定mrna含量的定量逆转录聚合酶链式反应(rt-pcr)实验。在优选的实施方案中,抗tnfr2多肽(例如,单链多肽、抗体或其抗原结合片段)是显性tnfr2拮抗剂并且因此即使在tnfr2激动剂(如tnfα)或生长促进剂(如il-2)存在下也能够抑制tnfr2活化。
73、拮抗性tnfr2多肽(例如,本发明的单链多肽、抗体、其抗原结合片段和构建体)可表现出以下性质中的一种或多种或全部:
74、a.例如通过结合t-reg细胞表面上的tnfr2并使所述tnfr2失活来遏制t-reg细胞增殖;
75、b.例如通过结合mdsc表面上的tnfr2并使所述tnfr2失活来遏制mdsc增殖;
76、c.促进t效应细胞(如cd8+t细胞)的扩增;和/或
77、d.遏制表达tnfr2的癌细胞,如t细胞淋巴瘤细胞(例如,霍奇金氏淋巴瘤细胞和皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞和肾细胞癌细胞的增殖。
78、例如,本发明的拮抗性tnfr2多肽(如单链多肽、抗体或其抗原结合片段)可减少患者(如人患者)体内或样品(例如,从患者分离的样品,所述患者如正在经历如本文所述的癌症或感染性疾病的治疗的人患者,相对于未用所述拮抗剂治疗的患者或样品)内的t-reg或癌细胞的总量。
79、在一些实施方案中,所述拮抗性tnfr2多肽(例如,单链多肽、抗体或其抗原结合片段)降低例如t-reg细胞或癌细胞(如t细胞淋巴瘤(例如,霍奇金氏或皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞或肾细胞癌细胞)表达tnfr2和/或这些细胞分泌可溶性tnfr2。
80、本发明的拮抗性tnfr2多肽(例如,单链多肽、抗体以及其抗原结合片段)可抑制患者(例如,人患者)体内或样品(例如,从正在经历如本文所述的癌症或感染性疾病的治疗的人患者中分离的样品)中的t-reg细胞的增殖或减少所述t-reg细胞的总量。
81、本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可能能够减少或抑制t-reg细胞和/或表达tnfr2的癌细胞的增殖。例如,所述癌细胞可选自由以下组成的组t细胞淋巴瘤细胞(例如,霍奇金氏和皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞和肾细胞癌细胞。结合癌细胞上的tnfr2可抑制或减少癌细胞的增殖或可促进癌细胞的凋亡。
82、本发明的拮抗性tnfr2多肽(例如,单链多肽、抗体或其抗原结合片段)可结合骨髓源性抑制细胞(mdsc;例如,表达选自由以下组成的组的蛋白质和小分子的全部或子集的细胞:b7-1(cd80)、b7-h1(pd-l1)、ccr2、cd1d、cd1d1、cd2、cd31(pecam-1)、cd43、cd44、补体组分c5a r1、f4/80(emr1)、fcγriii(cd16)、fcγrii(cd32)、fcγriia(cd32a)、fcγriib(cd32b)、fcγriib/c(cd32b/c)、fcγriic(cd32c)、fcγriiia(cd16a)、fcγriiib(cd16b)、半乳糖凝集素-3、gp130、gr-1(ly-6g)、icam-1(cd54)、il-1ri、il-4rα、il-6rα、整联蛋白α4(cd49d)、整联蛋白αl(cd11a)、整联蛋白αm(cd11b)、m-csfr、mgl1(cd301a)、mgl1/2(cd301a/b)、mgl2(cd301b)、一氧化氮、psgl-1(cd162)、l-选择蛋白(cd62l)、siglec-3(cd33)、转铁蛋白受体(tfr)、vegfr1(flt-1)以及vegfr2(kdr或flk-1))表面上的tnfr2。特别地,mdsc不表达选自由b7-2(cd86)、b7-h4、cd11c、cd14、cd21、cd23(fcεrii)、cd34、cd35、cd40(tnfrsf5)、cd117(c-kit)、hla-dr以及sca-1(ly6)组成的组的蛋白质。结合mdsc上的tnfr2可抑制或减少mdsc的增殖或可促进mdsc的凋亡。本发明的多肽(如单链多肽、抗体以及其抗原结合片段)不需要tnfα来减少或抑制t-reg细胞、癌细胞(例如,表达tnfr2的癌细胞)和/或mdsc的增殖。
83、在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于未患癌症的受试者在患有癌症的患者中以更大的效力减少或抑制t-reg细胞的增殖。在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)在肿瘤的微环境中以更大的效力减少或抑制t-reg细胞的增殖。
84、例如,在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)减少或抑制t-reg细胞的增殖,其效力在肿瘤微环境中比在不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)中更大。例如,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可表现出用于抑制肿瘤微环境中t-reg细胞的增殖的ic50比所述多肽用于抑制不含癌细胞的部位中t-reg细胞的增殖的ic50小例如1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、25倍、30倍、35倍、40倍、45倍、50倍、100倍、1,000倍、10,000倍或更多。本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可减少或抑制t-reg细胞的增殖,其效力在含有t细胞淋巴瘤细胞(例如,霍奇金氏或皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞或肾细胞癌细胞的肿瘤的微环境中比在不含此类癌细胞的部位(如患有前述癌症中的一种或多种的患者中远离肿瘤的部位或未患癌症的受试者中的部位)中更大。
85、在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于未患癌症的受试者在患有癌症的患者中以更大的效力减少或抑制mdsc的增殖。在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)在肿瘤的微环境中以更大的效力减少或抑制mdsc的增殖。
86、例如,本发明的拮抗性tnfr2多肽(例如,单链多肽、抗体或其抗原结合片段)可结合肿瘤的微环境内存在的mdsc表面上的tnfr2,并且可抑制或减少所述mdsc的增殖或者可促进mdsc的细胞凋亡,其效力在肿瘤微环境中比在不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)更大。例如,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可表现出用于抑制肿瘤微环境中mdsc的增殖的ic50比所述多肽用于抑制不含癌细胞的部位中mdsc的增殖的ic50小例如1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、25倍、30倍、35倍、40倍、45倍、50倍、100倍、1,000倍、10,000倍或更多。本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可减少或抑制mdsc的增殖或者可促进mdsc的细胞凋亡,其效力在含有t细胞淋巴瘤细胞(例如,霍奇金氏或皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞或肾细胞癌细胞的肿瘤的微环境中比在不含此类癌细胞的部位(如患有前述癌症中的一种或多种的患者中远离肿瘤的部位或未患癌症的受试者中的部位)中更大。
87、在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于未患癌症的受试者在患有癌症的患者中以更大的效力扩增t效应细胞,如cd8+细胞毒性t细胞。在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)相对于不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)在肿瘤的微环境中以更大的效力扩增t效应细胞,如cd8+细胞毒性t细胞。
88、例如,在一些实施方案中,本发明的多肽(如单链多肽、抗体以及其抗原结合片段)直接扩增t效应细胞,如cd8+细胞毒性t细胞,其效力在肿瘤微环境中比在不含癌细胞的部位(如患有癌症的患者中远离肿瘤的部位或未患癌症的受试者中的部位)中更大。例如,本发明的多肽可具有的用于扩增癌症患者中的t效应细胞的ec50比所述多肽用于扩增未患癌症的受试者中的t效应细胞的ec50小例如1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、25倍、30倍、35倍、40倍、45倍、50倍、100倍、1,000倍、10,000倍或更多。本发明的多肽(如单链多肽、抗体以及其抗原结合片段)可直接扩增t效应细胞,如cd8+细胞毒性t细胞,其效力在含有t细胞淋巴瘤细胞(例如,霍奇金氏或皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞或肾细胞癌细胞的肿瘤的微环境中比在不含此类癌细胞的部位(如患有前述癌症中的一种或多种的患者中远离肿瘤的部位或未患癌症的受试者中的部位)中更大。在一些实施方案中,所述t效应细胞(例如,cd8+细胞毒性t细胞)与存在于一种或多种癌细胞(如霍奇金氏淋巴瘤细胞、皮肤非霍奇金氏淋巴瘤细胞、t细胞淋巴瘤细胞、卵巢癌细胞、结肠癌细胞、多发性骨髓瘤细胞或肾细胞癌细胞)上的抗原特异性地反应。
89、在另一方面,本发明的特征是一种通过以下方式鉴别tnfr2拮抗剂抗体或其抗原结合片段的方法:
90、(a)使抗体或其片段的异质混合物暴露于肽,所述肽具有id no:285或286的氨基酸序列,或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;以及
91、(b)保留特异性地结合所述肽的抗体或其片段并除去不特异性地结合所述肽的抗体或其片段,从而产生含有至少一种所述tnfr2拮抗剂抗体或其抗原结合片段的富集的抗体混合物。在一些实施方案中,所述方法包括确定所述富集的抗体混合物中的抗体或其抗原结合片段中的一种或多种的氨基酸序列。
92、在一些实施方案中,所述肽结合至表面。所述抗体或其抗原结合片段可在病毒颗粒或细胞的表面(如噬菌体、细菌细胞或酵母细胞的表面)上表达。所述抗体或其抗原结合片段可表达为与核糖体非共价结合或与mrna或cdna共价结合的一条或多条多肽链。在一些实施方案中,所述肽与可检测标记,如选自由以下组成的组的可检测标记缀合:荧光分子(例如,绿色荧光蛋白、青色荧光蛋白、黄色荧光蛋白、红色荧光蛋白、藻红蛋白、别藻蓝蛋白、赫斯特、4',6-二脒基-2-苯基吲哚(dapi)、碘化丙啶、荧光素、香豆素、罗丹明、四甲基罗丹明和花菁)、表位标签(例如,麦芽糖结合蛋白、谷胱甘肽-s-转移酶、聚-组氨酸标签、flag-标签、myc-标签、人流感血凝素(ha)标签、生物素和链霉亲和素)和放射性标记。在一些实施方案中,所述方法的步骤(a)和(b)顺序地重复一次或多次。
93、在另一方面,本发明的特征是一种通过以下方式产生tnfr2拮抗剂抗体或其抗原结合片段的方法:用肽免疫非人哺乳动物,所述肽含有seq id no:285或286的序列,或相对于所述序列具有至多两个氨基酸取代的氨基酸序列;以及收集含有所述tnfr2拮抗剂抗体或其抗原结合片段的血清。非人哺乳动物可选自由以下组成的组:兔、小鼠、大鼠、山羊、豚鼠、仓鼠、马和绵羊。
94、在另一方面,本发明的特征是一种通过以上实施方案中的任一个的方法产生的抗体或其抗原结合片段。
95、本发明的抗体或其抗原结合片段可以是全长抗体或抗体片段,如单克隆抗体或其抗原结合片段、多克隆抗体或其抗原结合片段、人源化抗体或其抗原结合片段、灵长类化抗体或其抗原结合片段、双特异性抗体或其抗原结合片段、多特异性抗体或其抗原结合片段、双重可变免疫球蛋白结构域、单价抗体或其抗原结合片段、嵌合抗体或其抗原结合片段、单链fv分子(scfv)、双抗体、三抗体、纳米抗体、抗体样蛋白支架、结构域抗体、fv片段、fab片段、f(ab’)2分子以及串联scfv(tafv)。在一些实施方案中,所述抗体或其抗原结合片段含有例如通过酰胺键、硫醚键、碳-碳键或二硫桥键或通过接头(如本文所述的接头)彼此共价结合的两个或更多个cdr。在一些实施方案中,所述抗体或其抗原结合片段具有选自由igg、iga、igm、igd和ige组成的组的同种型。所述抗体或其抗原结合片段可例如缀合至治疗剂,如本文所述的细胞毒性剂。
96、本发明的特征是一种编码本发明的单链多肽、构建体、抗体或其抗原结合片段的多核苷酸,以及一种含有这种多核苷酸的载体。所述载体可以是表达载体,如真核表达载体,或病毒载体,如腺病毒(ad,如血清型5、26、35或48腺病毒)、逆转录病毒(如γ-逆转录病毒或慢病毒)、痘病毒、腺相关病毒、杆状病毒、单纯疱疹病毒或牛痘病毒(如修饰的牛痘安卡拉(mva))。本发明的特征还是宿主细胞,如含有本发明地载体的原核细胞和真核细胞(例如,哺乳动物细胞)。
97、在另一方面,本发明的特征是一种药物组合物,所述药物组合物含有本发明的抗体或其抗原结合片段、单链多肽、构建体、多核苷酸、载体或宿主细胞(例如,tnfr2拮抗剂抗体或其抗原结合片段)和药学上可接受的载体或赋形剂。所述药物组合物可含有例如另外的治疗剂,如免疫治疗剂。在一些实施方案中,所述免疫治疗剂是抗ctla-4剂、抗pd-1剂、抗pd-l1剂、抗pd-l2剂、tnf-α交联剂、trail交联剂、抗cd27剂、抗cd30剂、抗cd40剂、抗4-1bb剂、抗gitr剂、抗ox40剂、抗trailr1剂、抗trailr2剂或抗tweakr剂。例如,所述免疫治疗剂可以是抗ctla-4抗体或其抗原结合片段、抗pd-1抗体或其抗原结合片段、抗pd-l1抗体或其抗原结合片段、抗pd-l2抗体或其抗原结合片段、tnf-α交联抗体或其抗原结合片段、trail交联抗体或其抗原结合片段、抗cd27抗体或其抗原结合片段、抗cd30抗体或其抗原结合片段、抗cd40抗体或其抗原结合片段、抗4-1bb抗体或其抗原结合片段、抗gitr抗体或其抗原结合片段、抗ox40抗体或其抗原结合片段、抗trailr1抗体或其抗原结合片段、抗trailr2抗体或其抗原结合片段或抗tweakr抗体或其抗原结合片段。所述免疫治疗剂可能能够特异性地结合mahoney等人,cancer immunotherapy,14:561-584(2015)的表1中描述的一种或多种免疫靶标,所述文献的公开内容以引用的方式整体并入本文。例如,所述免疫治疗剂可以是特异性地结合以下中的一种或多种的剂,如抗体或其抗原结合片段:ox40l、tl1a、cd40l、light、btla、lag3、tim3、singlecs、icos、b7-h3、b7-h4、vista、tmigd2、btnl2、cd48、kir、lir、lir抗体、ilt、nkg2d、nkg2a、mica、micb、cd244、csf1r、ido、tgfβ、cd39、cd73、cxcr4、cxcl12、sirpa、cd47、vegf或神经纤毛蛋白。特别地,所述药物组合物含有tnfr2拮抗剂抗体或其抗原结合片段和抗pd-1或抗pdl1抗体。在一些实施方案中,所述免疫治疗剂是塔革雷汀(targretin)、干扰素-α、氯倍他索(clobestasol)、peg干扰素(例如,)、泼尼松、罗米地辛(romidepsin)、贝沙罗汀、甲氨蝶呤、曲安西龙乳膏、抗趋化因子、伏立诺他、加巴喷丁、针对淋巴细胞表面受体和/或淋巴因子的抗体、针对表面癌蛋白的抗体和/或小分子疗法如伏立诺他。
98、在一些实施方案中,另外的治疗剂是化学治疗剂,如本文所描述的化学治疗剂。本发明的抗体或其抗原结合片段、单链多肽、构建体、多核苷酸、载体或宿主细胞(例如,tnfr2拮抗剂抗体或其抗原结合片段)可例如通过将所述抗体或其抗原结合片段、单链多肽、构建体、多核苷酸、载体或宿主细胞与化学治疗剂掺混而被配制用于与化学治疗剂共同施用。在一些实施方案中,所述抗体或其抗原结合片段、单链多肽、构建体、多核苷酸、载体或宿主细胞被配制用于与化学治疗剂分开施用。在一些实施方案中,例如使用本文所述的或本领域中已知的键形成技术使所述化学治疗剂与所述抗体或其抗原结合片段、单链多肽、构建体、多核苷酸、载体或宿主细胞直接缀合。
99、本发明的特征还是一种通过以下方式产生本发明的多肽(例如,单链多肽、构建体、抗体或抗原结合片段)的方法:在宿主细胞中表达编码所述单链多肽、构建体、抗体或其抗原结合片段的多核苷酸以及从宿主细胞培养基回收所述单链多肽、抗体或其抗原结合片段。
100、本发明另外地特征是一种通过以下方式抑制人中由调控性t细胞介导的免疫响应的方法以及一种通过以下方式治疗人的细胞增殖病症的方法:向需要治疗的人施用本发明的单链多肽、构建体、抗体或其抗原结合片段、多核苷酸、载体、宿主细胞或药物组合物(例如,含有tnfr2拮抗剂抗体或其抗原结合片段和任选的免疫治疗剂如抗pd-1或抗pdl1抗体的药物组合物)。另外地,本发明的特征是一种用于抑制人中由调控性t细胞介导的免疫响应以及用于治疗人的细胞增殖病症的组合物,所述组合物含有本发明的单链多肽、构建体、抗体或其抗原结合片段、多核苷酸、载体或宿主细胞。
101、在一些实施方案中,所述细胞增殖病症可以是癌症,如白血病、淋巴瘤、肝癌、骨癌、肺癌、脑癌、膀胱癌、胃肠癌、乳腺癌、贲门癌、宫颈癌、子宫癌、头颈癌、胆囊癌、喉癌(laryngeal cancer)、唇癌和口腔癌、眼癌、黑色素瘤、胰腺癌、前列腺癌、结肠直肠癌、睾丸癌或喉癌(throat cancer)。在特定情况下,所述细胞增殖病症可以是选自由以下组成的组的癌症:急性成淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、慢性淋巴细胞性白血病(cll)、慢性骨髓性白血病(cml)、肾上腺皮质癌、aids相关淋巴瘤、原发性cns淋巴瘤、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎瘤/横纹肌样瘤、基底细胞癌、胆管癌、肝外癌、尤文肉瘤家族、骨肉瘤和恶性纤维组织细胞瘤、中枢神经系统胚胎肿瘤、中枢神经系统生殖细胞肿瘤、颅咽管瘤、室管膜瘤、支气管肿瘤、伯基特淋巴瘤、类癌肿瘤、原发性淋巴瘤、脊索瘤、慢性骨髓增生性肿瘤、结肠癌、肝外胆管癌、原位导管癌(dcis)、子宫内膜癌、室管膜瘤、食道癌、成感觉神经母细胞瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、输卵管癌、骨纤维组织细胞瘤、胃肠类癌肿瘤、胃肠间质肿瘤(gist)、睾丸生殖细胞肿瘤、妊娠滋养细胞疾病、神经胶质瘤、儿童脑干神经胶质瘤、毛细胞白血病、肝细胞癌、朗格汉斯细胞组织细胞增生症、霍奇金淋巴瘤、下咽癌、胰岛细胞肿瘤、胰腺神经内分泌肿瘤、威尔姆斯肿瘤和其他儿童肾脏肿瘤、朗格汉斯细胞组织细胞增生症、小细胞肺癌、皮肤t细胞淋巴瘤、眼内黑色素瘤、梅克尔细胞癌、间皮瘤、转移性鳞状颈癌、中线道癌、多发性内分泌瘤形成综合征、多发性骨髓瘤/浆细胞肿瘤、骨髓增生异常综合征、鼻腔和副鼻窦癌、鼻咽癌、成神经细胞瘤、非霍奇金淋巴瘤(nhl)、非小细胞肺癌(nsclc)、上皮性卵巢癌、生殖细胞卵巢癌、低恶性潜能卵巢癌、胰腺神经内分泌肿瘤、乳头瘤病、副神经节瘤、副鼻窦和鼻腔癌、甲状旁腺癌、阴茎癌、咽癌、嗜铬细胞瘤、垂体肿瘤、胸膜肺母细胞瘤、原发性腹膜癌、直肠癌、成视网膜细胞瘤、横纹肌肉瘤、唾液腺癌、卡波济肉瘤、横纹肌肉瘤、塞扎里综合征(sézary syndrome)、小肠癌、软组织肉瘤、喉癌、胸腺瘤和胸腺癌、甲状腺癌、肾盂和输尿管移行细胞癌、尿道癌、子宫内膜子宫癌、子宫肉瘤、阴道癌、外阴癌以及瓦尔登斯特伦巨球蛋白血症。
102、本发明的特征还是通过向患者(例如,哺乳动物患者,如人患者)施用本发明的拮抗性tnfr2多肽(例如,单链多肽、构建体、抗体或其抗原结合片段)、多核苷酸、载体或宿主细胞来治疗t细胞淋巴瘤(例如,霍奇金氏或皮肤非霍奇金氏淋巴瘤细胞)、卵巢癌、结肠癌、多发性骨髓瘤或肾细胞癌的方法。例如,本发明提供了一种通过向患者(例如,哺乳动物患者,如人患者)施用本发明的拮抗性tnfr2抗体或其抗原结合片段来治疗卵巢癌的方法。本发明另外地特征是一种用于治疗患者(例如,人患者)的霍奇金氏或皮肤非霍奇金氏淋巴瘤、t细胞淋巴瘤、卵巢癌、结肠癌、多发性骨髓瘤或肾细胞癌的组合物,所述组合物含有本发明的单链多肽、构建体、抗体或其抗原结合片段、多核苷酸、载体或宿主细胞。
103、本发明的特征还是一种通过向需要治疗的人施用本发明的单链多肽、构建体、抗体或其抗原结合片段、多核苷酸、载体或宿主细胞来治疗患者(例如,人患者)的感染性疾病的方法,以及一种用于治疗患者(例如,人患者)的感染性疾病的组合物,所述组合物含有本发明的单链多肽、构建体、抗体或其抗原结合片段、多核苷酸、载体或宿主细胞。在一些实施方案中,所述感染性疾病由病毒、细菌、真菌或寄生虫引起。例如,可根据本发明的方法治疗的病毒感染包括丙型肝炎病毒、黄热病病毒、凯丹姆病毒、科萨努尔森林病病毒、兰加特病毒、鄂木斯克出血热病毒、波瓦森病毒、皇家农场病毒、喀什病毒、蜱传脑炎病毒、纽多佛病毒、索夫吉病毒、跳跃病病毒、根岸病毒、米班病毒、索马里兹礁病毒、秋列尼病毒、阿罗阿病毒、登革病毒、凯杜古病毒、卡西帕科利病毒、库坦戈病毒、日本脑炎病毒、墨累谷脑炎病毒、圣路易斯脑炎病毒、乌苏图病毒、西尼罗河病毒、雅温德病毒、科科贝拉病毒、巴加扎病毒、伊利乌斯病毒、以色列火鸡脑脊膜脑脊髓炎病毒、恩塔亚病毒、坦布苏病毒、寨卡病毒、班齐病毒、博博衣病毒、边山病毒、朱格拉病毒、萨沃亚病毒,赛皮克病毒、乌干达s病毒、韦塞尔斯布朗病毒、黄热病毒、恩德培蝙蝠病毒、横须贺病毒、阿波依病毒、牛骨山脊病毒、胡蒂亚帕病毒、摩多克病毒、萨尔别霍病毒、圣帕利塔病毒,布卡拉沙蝙蝠病毒、凯里岛病毒、达卡尔蝙蝠病毒、蒙大拿鼠耳蝙蝠脑白质炎病毒、金边蝙蝠病毒、里约布拉沃病毒、塔马纳蝙蝠病毒、细胞融合因子病毒、伊皮病毒、拉沙病毒、淋巴细胞性脉络丛脑膜炎病毒(lcmv)、莫巴拉病毒、莫佩亚病毒、阿马帕里病毒、弗莱克索病毒、瓜纳里托病毒、胡宁病毒、拉蒂诺病毒、马邱波病毒、奥利华斯病毒、巴拉那病毒、皮钦德病毒、皮里陶病毒、萨比亚病毒、塔卡里伯病毒、太米阿米病毒、怀特沃特阿罗约病毒、查帕雷病毒、卢约病毒、汉坦病毒、辛诺柏病毒、道格比病毒、布尼奥罗病毒、裂谷热病毒、拉克罗斯病毒、加利福尼亚脑炎病毒、克里米亚-刚果出血热(cchf)病毒、埃博拉病毒、马尔堡病毒、委内瑞拉马脑炎病毒(vee)、东方马脑炎病毒(eee)、西方马脑炎病毒(wee)、辛德毕斯病毒、风疹病毒、塞姆利基森林病毒、罗斯河病毒、巴马森林病毒、阿尼昂-尼昂病毒(o’nyong’nyong virus)和基孔肯雅病毒、天花病毒、猴痘病毒、牛痘病毒、单纯疱疹病毒、人疱疹病毒、巨细胞病毒(cmv)、爱泼斯坦-巴尔病毒(ebv)、水痘-带状疱疹病毒、卡波西氏肉瘤相关疱疹病毒(kshv)、流感病毒、严重急性呼吸综合征(sars)病毒、狂犬病毒、水疱性口炎病毒(vsv)、人呼吸道合胞病毒(rsv)、新城疫病毒、亨德拉病毒、尼帕病毒、麻疹病毒、牛瘟病毒、犬瘟热病毒、仙台病毒、人副流感病毒(例如,1、2、3和4)、鼻病毒、腮腺炎病毒、脊髓灰质炎病毒、人肠道病毒(a、b、c和d)、甲型肝炎病毒、柯萨奇病毒、乙型肝炎病毒、人乳头状瘤病毒、腺相关病毒、星状病毒、jc病毒、bk病毒、sv40病毒、诺沃克病毒、轮状病毒、人免疫缺陷病毒(hiv)、人t-嗜淋巴细胞病毒i型和ii型以及传染性海绵状脑病如慢性耗竭疾病。
104、在一些实施方案中,可根据本发明的方法治疗的细菌感染包括由属于选自由以下组成的组的属的细菌引起的细菌感染:沙门氏菌属、链球菌属、芽孢杆菌属、李斯特菌属、棒状杆菌属、诺卡氏菌属、奈瑟氏菌属、放线杆菌属、莫拉氏菌属、肠杆菌属(例如,大肠杆菌,如o157:h7)、假单胞菌属、埃希氏菌属、克雷伯氏菌属、沙雷氏菌属、肠杆菌属、变形杆菌属、沙门氏菌属、志贺氏菌属、耶尔森氏菌属、嗜血杆菌属、博德特氏菌属、军团菌属、巴斯德氏菌属、弗朗西斯氏菌属、布鲁氏菌属、巴尔通氏体属、梭菌属、弧菌属、弯曲杆菌属和葡萄球菌属。此外,可根据本发明的方法治疗的寄生虫感染包括由以下引起的寄生虫感染:溶组织内阿米巴、兰伯氏贾第虫、鼠型隐孢子虫、冈比亚锥虫、罗德西亚锥虫、克氏锥虫、墨西哥利什曼原虫、巴西利什曼原虫、热带利什曼原虫、杜氏利什曼原虫、刚地弓形虫、间日疟原虫、卵形疟原虫、三日疟原虫、镰状疟原虫、阴道毛滴虫和火鸡组织滴虫。示例性蠕虫寄生虫包括毛首鞭形线虫、豚蛔虫、蛲虫、十二指肠钩虫、美洲钩虫、粪类圆线虫、班氏丝虫和麦地那龙线虫、曼氏血吸虫、住血吸虫、日本血吸虫、肝片吸虫、大片吸虫、异形吸虫、卫氏并殖吸虫、猪带绦虫、牛带绦虫、短膜壳绦虫或细粒棘球绦虫。
105、本发明的特征还是试剂盒,如含有本发明的单链多肽、构建体、抗体或抗原结合片段(例如,拮抗剂tnfr2抗体)、本发明的多核苷酸、本发明的载体或本发明的宿主细胞的试剂盒。在一些情况下,本发明的试剂盒可含有用于将本发明的载体转染到本发明的宿主细胞中的说明书。任选地,试剂盒可含有用于在本发明的宿主细胞中表达本发明的单链多肽、抗体或抗原结合片段的说明书(和任选地,可用于在本发明的宿主细胞中表达本发明的单链多肽、抗体或抗原结合片段的试剂)。本发明的试剂盒还可含有用于将本发明的单链多肽、构建体、抗体或抗原结合片段、本发明的多核苷酸、本发明的载体或本发明的宿主细胞施用于人患者的说明书。任选地,试剂盒可含有用于制备或使用本发明的抗体或抗原结合片段、本发明的多核苷酸、本发明的载体或本发明的宿主细胞的说明书。
106、定义
107、如本文所用,术语“约”是指高于或低于所描述值的不超过10%的值。例如,术语“约5nm”指示4.5nm至5.5nm的范围。
108、如本文所用,术语“抗体”(ab)是指特异性地结合至特定抗原或与特定抗原免疫反应的免疫球蛋白分子,并且包括多克隆、单克隆、遗传工程化和以其他方式修饰形式的抗体,包括但不限于嵌合抗体、人源化抗体、异缀合物抗体(例如,双-、三-和四-特异性抗体、双抗体、三抗体和四抗体)以及抗体的抗原结合片段,包括例如fab'、f(ab')2、fab、fv、rlgg和scfv片段。此外,除非另外说明,否则术语“单克隆抗体”(mab)是指包括完整分子以及能够特异性地结合至靶蛋白的抗体片段(例如像,fab和f(ab')2片段)两者。fab和f(ab')2片段缺乏完整抗体的fc片段,从动物的循环中更快地清除,并且可具有比完整抗体更少的非特异性组织结合(参见wahl等人,j.nucl.med.24:316,1983;以引用的方式并入本文)。
109、如本文所用的术语“抗原结合片段”是指抗体的保留特异性地结合至靶抗原的能力的一个或多个片段。抗体的抗原结合功能可由全长抗体的片段执行。抗体片段可以是fab、f(ab’)2、scfv、smip、双抗体、三抗体、亲和体、纳米抗体、适体或结构域抗体。涵盖于术语抗体的“抗原结合片段”中的结合片段的实例包括但不限于:(i)fab片段,一种由vl、vh、cl和ch1结构域组成的单价片段;(ii)f(ab')2片段,一种包含在铰链区处通过二硫桥连接的两个fab片段的二价片段;(iii)由vh和ch1结构域组成的fd片段;(iv)由抗体单臂的vl和vh结构域组成的fv片段;(v)包含vh和vl结构域的dab;(vi)dab片段(ward等人,nature 341:544-546,1989),其由vh结构域组成;(vii)由vh或vl结构域组成的dab;(viii)分离的互补决定区(cdr);以及(ix)两个或更多个分离的cdr的组合,所述cdr可任选地通过合成接头连接。此外,尽管fv片段的两个结构域vl和vh由单独基因编码,但它们可使用重组方法通过接头连接,所述接头使它们能够制成其中vl和vh区配对以形成单价分子的单一蛋白质链(称为单链fv(scfv);参见例如,bird等人,science 242:423-426,1988和huston等人,proc.natl.acad.sci.usa85:5879-5883,1988)。可使用本领域技术人员已知的常规技术来获得这些抗体片段,并且可以与完整抗体相同的方式筛选所述片段的效用。抗原结合片段可通过重组dna技术、完整免疫球蛋白的酶促或化学裂解或者在一些实施方案中通过本领域中已知的化学肽合成程序而产生。
110、如本文所用,术语“抗肿瘤坏死因子受体2抗体”、“tnfr2抗体”、“抗tnfr2抗体部分”和/或“抗tnfr2抗体片段”等包括能够特异性地结合至tnfr2的任何含蛋白质或肽的分子,所述分子包含免疫球蛋白分子的至少一部分,如但不限于重链或轻链的至少一个互补决定区(cdr)或其配体结合部分、重链或轻链可变区、重链或轻链恒定区、框架区或其任何部分。例如,免疫球蛋白分子的两个或更多个部分可例如通过酰胺键、硫醚键、碳-碳键、二硫桥键或通过接头(如本文描述或本领域中已知的接头)彼此共价结合。tnfr2抗体还包括抗体样蛋白支架,如第十纤连蛋白iii型结构域(10fn3),其含有在结构以及对抗体cdr的溶剂可及性方面相似的bc、de和fg结构环。10fn3结构域的三级结构类似于igg重链的可变区的三级结构,并且本领域技术人员可通过用来自tnfr2单克隆抗体的cdr-h1、cdr-h2或cdr-h3区的残基替代10fn3的bc、de和fg环的残基来将例如tnfr2单克隆抗体的cdr移植到纤连蛋白支架上。
111、如本文所用,术语“拮抗剂tnfr2抗体”和“拮抗性tnfr2抗体”是指能够抑制或降低tnfr2的活化和/或减弱由tnfr2介导的一种或多种信号转导途径的tnfr2抗体。例如,拮抗性tnfr2抗体可抑制或减少调控性t细胞的生长和增殖。拮抗性tnfr2抗体可通过阻断tnfr2结合tnfα来抑制或降低tnfr2活化。以这种方式,拮抗性tnfr2抗体可阻断tnfr2的三聚化,否则所述tnfr2的三聚化将通过与tnfα相互作用诱导、从而导致tnfr2活性的遏制。
112、如本文所用,术语“双特异性抗体”是指对至少两种不同的抗原具有结合特异性的单克隆抗体,通常是人或人源化抗体。在本发明中,结合特异性中的一种可针对tnfr2,并且另一种可针对任何其他抗原,例如,针对细胞表面蛋白、受体、受体亚基、组织特异性抗原、病毒源性蛋白、病毒编码包膜蛋白、细菌源性蛋白或细菌表面蛋白等。
113、如本文所用,短语“化学治疗剂”是指在治疗癌症(如本文所述的癌症)中具有治疗有用性的任何化学试剂。化学治疗剂涵盖化学剂和生物剂两者。这些剂可起到抑制细胞活性的作用,癌细胞依赖于细胞活性以继续存活。化学治疗剂的类别包括烷化/生物碱剂、抗代谢物、激素、激素类似物和抗肿瘤药物。适合与本文所述的组合物和方法结合使用的示例性化学治疗剂包括但不限于slapak和kufe,principles of cancer therapy,chapter86in harrison's principles ofinternal medicine,第14版;perry等人,chemotherapeutic,chapter 17in abeloff,clinical oncology第2版,2000;baltzer l.和berkery r.(编):oncologypocket guide to chemotherapeutic,第2版st.luois,mosby-yearbook,1995;fischer d.s.,knobf m.f.,durivage h.j.(编):the cancerchemotherapeutic handbook,第4版st.luois,mosby-year handbook中列出的那些,其各自的公开内容均以引用的方式并入本文,因为它们属于化学治疗剂。
114、如本文所用,术语“嵌合”抗体是指具有源自一种来源生物(如大鼠或小鼠)的免疫球蛋白的可变结构域序列(例如,cdr序列)和源自不同生物体(例如,人、另一种灵长类动物、猪、山羊、兔、仓鼠、猫、狗、豚鼠、牛科的成员(如牛、野牛、水牛、麋鹿和牦牛等)、奶牛、绵羊、马或野牛等)的免疫球蛋白的恒定区的抗体。用于产生嵌合抗体的方法是本领域中已知的。参见例如,morrison,1985,science229(4719):1202-7;oi等人,1986,biotechniques4:214-221;gillies等人,1985,j.immunol.methods 125:191-202;美国专利号5,807,715;4,816,567;和4,816,397;其以引用的并入本文。
115、如本文所用,术语“互补决定区”(cdr)是指在轻链和重链可变结构域中发现的高变区。可变结构域的更高度保守的部分被称为框架区(fr)。如本领域所理解的,描绘抗体的高变区的氨基酸位置可根据上下文和本领域中已知的各种定义而变化。可变结构域内的一些位置可被视为杂合高变位置,因为这些位置可被认为是在一组标准下的高变区内,同时被认为是在不同组标准下的高变区之外。这些位置中的一个或多个也可在扩增的高变区中找到。本发明包括在这些杂合高变位置中包含修饰的抗体。天然重链和轻链的可变结构域各自包含通过三个cdr连接的四个框架区,所述框架区主要采用β-折叠构型,所述cdr形成连接β-折叠结构并且在一些情况下形成β-折叠结构的一部分的环。每条链中的cdr通过fr区按顺序fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4紧密靠近地保持在一起,并且与来自其他抗体链的cdr一起有助于抗体的靶结合位点的形成(参见kabat等人,sequences of proteinsof immunological interest(national institute ofhealth,bethesda,md.1987;其以引用的并入本文)。如本文所用,除非另有说明,否则根据kabat等人的免疫球蛋白氨基酸残基编号系统进行免疫球蛋白氨基酸残基的编号。
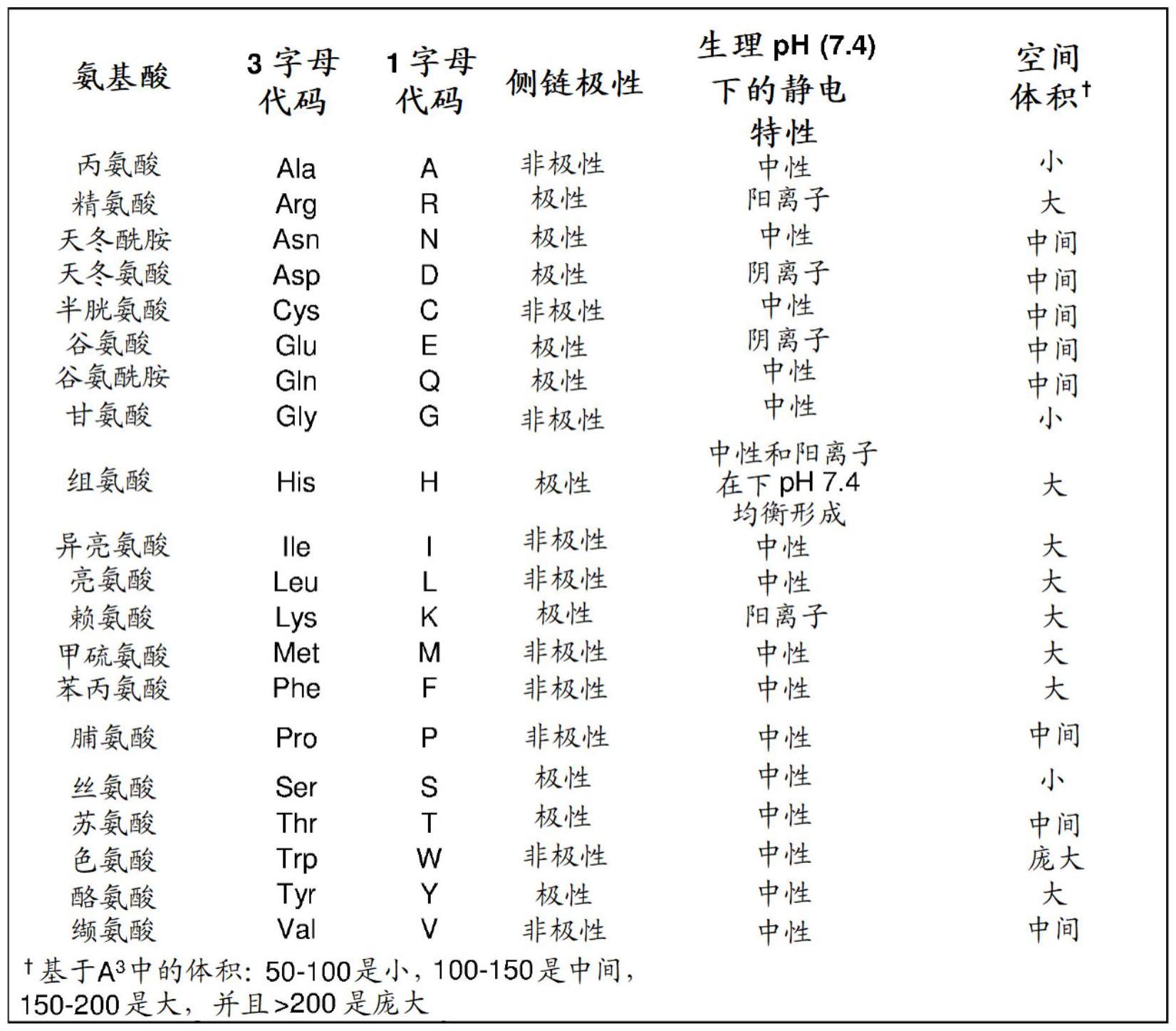
116、如本文所用,术语“保守突变”、“保守取代”或“保守氨基酸取代”是指一个或多个氨基酸取代表现出类似物理化学性质(如极性、静电荷和空间体积)的一个或多个不同的氨基酸。对于以下表1中的20种天然存在的氨基酸中的每一种,总结了这些性质。
117、表1.天然存在的氨基酸的代表性物理化学性质
118、
119、从此表可以看出,保守氨基酸家族包括例如(i)g、a、v、l、i、p和m;(ii)d和e;(iii)c、s和t;(iv)h;k和r;(v)n和q;以及(vi)f、y;并且w.a保守突变或取代因此是一种氨基酸取代相同氨基酸家族的成员的突变或取代(例如,ser取代thr或lys取代arg)。
120、如本文所用,术语“缀合物”是指通过一个分子的反应性官能团与另一个分子的适当反应性官能团的化学键合形成的化合物。
121、如本文在tnfr2拮抗剂的背景下所用,术语“构建体”是指含有与第二多肽结构域结合的第一多肽结构域的融合蛋白。多肽结构域可各自独立地为拮抗性tnfr2单链多肽,例如,如本文所述。第一多肽结构域可例如通过接头如肽接头或二硫桥等与第二多肽结构域共价结合。可用于连接拮抗性tnfr2构建体的多肽结构域的示例性接头包括但不限于在leriche等人,bioorg.med.chem.,20:571-582(2012)中描述的那些,其公开内容以引用的方式整体并入本文。
122、如本文所用,术语“衍生化抗体”是指通过化学反应进行修饰以便裂解残基的抗体或添加对分离的抗体不是天然的化学部分。衍生化抗体可通过糖基化、乙酰化、聚乙二醇化、磷酸化、酰胺化、通过添加已知的化学保护/封闭基团衍生化、蛋白水解裂解、与细胞配体或其他蛋白质的键联来获得。可通过已知技术进行多种化学修饰中的任一种,所述技术包括但不限于使用已建立的程序的特异性化学裂解、乙酰化、甲酰化、衣霉素的代谢合成等。另外,衍生物可含有一种或多种非天然氨基酸,例如使用琥珀抑制技术(参见例如,美国专利号6,964,859;以引用的方式并入本文)。
123、如本文所用,术语“双抗体”是指包含两条多肽链的二价抗体,其中每条多肽链包含通过太短的接头(例如,由五个氨基酸组成的接头)连接的vh和vl结构域以允许同一肽链上的vh和vl结构域的分子内缔合。这种构型迫使每个结构域与另一条多肽链上的互补结构域配对,以便形成同二聚体结构。因此,术语“三抗体”是指包含三条肽链的三价抗体,所述肽链各自含有通过极短的接头(例如,由1-2个氨基酸组成的接头)连接的一个vh结构域和一个vl结构域以允许同一肽链内的vh和vl结构域的分子内缔合。为了折叠成它们的天然结构,以这种方式配置的肽通常是三聚化以便将相邻肽链的vh和vl结构域定位成在空间上彼此接近以允许适当的折叠(参见holliger等人,proc.natl.acad.sci.usa 90:6444-48,1993;以引用的方式并入本文)。
124、如本文所用,tnfr2的“显性拮抗剂”是即使在tnfr2激动剂如tnfα或il-2存在下也能够抑制tnfr2活化的拮抗剂(例如,拮抗性多肽,如单链多肽、抗体或其抗原结合片段)。例如,如果在tnfr2激动剂(例如,tnfα)或il-2存在下拮抗剂的ic50相对于如在tnfr2激动剂(如tnfα或il-2)不存在下在相同测定中测量的拮抗剂的ic50增加小于200%(例如,小于200%、100%、50%、45%、40%、35%、30%、25%、20%、15%、10%、5%、1%或更少),则tnfr2拮抗剂是显性拮抗剂。可例如通过测量tnfr2+细胞(如t-reg细胞,表达tnfr2的癌细胞,或骨髓源性抑制细胞)的增殖的抑制以及通过测量nfκb信号传导的抑制(例如,通过在常规基因表达测定中监测选自由chuk、nfkbie、nfkbia、map3k11、traf2、traf3、relb以及ciap2/birc3组成的组的一种或多种基因的表达降低)来评估tnfr2活化的抑制。本文描述了可用于监测tnfr2活化的细胞增殖测定和基因表达测定(例如分别在实施例9和12中)。
125、如本文所用,“双重可变结构域免疫球蛋白”(“dvd-ig”)是指通过接头组合两种单克隆抗体的靶结合可变结构域以产生四价双重靶向单一剂的抗体。(gu等人,meth.enzymol.,502:25-41,2012;以引用的方式并入本文)。用于本发明的dvd的轻链的合适接头包括gu等人的第30页上表2.1中鉴定的那些:短k链接头adaap(seq id no:118)(鼠类)和tvaap(seq id no:119)(人);长κ链接头adaaptvsifp(seq id no:120)(鼠类)和tvaapsvfifpp(seq id no:121)(人);短λ链接头qpkaap(seq id no:122)(人);长λ链接头qpkaapsvtlfpp(seq id no:123)(人);gs-短接头ggsgg(seq id no:124),gs-培养基接头ggsggggsg(seq id no:125)和gs-长接头ggsggggsggggs(seq id no:126)(所有gs接头都是鼠类和人)。用于dvd的重链的合适接头包括在gu&ghayur,2012,methods in enzymology502:25-41的第30页上的表2.1中鉴定的那些,所述文献以引用的方式并入本文:短接头akttap(seq id no:127)(鼠类)和astkgp(seq id no:128)(人);长接头akttapsvyplap(seq id no:129)(鼠类)和astkgpsvfplap(seq id no:130)(人);gs-短接头ggggsg(seqid no:131),gs-培养基接头ggggsggggs(seq id no:132)和gs-长接头ggggsggggsgggg(seq id no:133)(所有gs接头都是鼠类和人)。
126、如本文所用,术语“内源性”描述天然存在于特定生物体(例如人)中或生物体内的特定位置(例如,器官、组织或细胞,如人细胞)中的分子(例如,多肽、核酸或辅因子)。
127、如本文所用,术语“外源性”描述不天然存在于特定生物体(例如人)中或生物体内的特定位置(例如,器官、组织或细胞,如人细胞)中的分子(例如,多肽、核酸或辅因子)。外源性物质包括从外部来源提供给生物体或从其提取的培养物质的那些。
128、如本文所用,术语“框架区”或“fw区”包括与cdr相邻的氨基酸残基。fw区残基可存在于例如人抗体、啮齿动物来源的抗体(例如鼠类抗体)、人源化抗体、灵长类化抗体、嵌合抗体、抗体片段(例如fab片段)、单链抗体片段(例如,scfv片段)、抗体结构域和双特异性抗体等。
129、如本文所用,术语“融合蛋白”是指通过共价键与另一分子连接的蛋白质。融合蛋白可通过例如一种蛋白质的n-末端与另一种蛋白质的c-末端之间的形成酰胺键的反应来化学合成。或者,可通过例如从载体或细胞的基因组表达编码融合蛋白的多核苷酸来在细胞(例如,真核细胞或原核细胞)中重组表达含有与另一种蛋白质共价结合的一种蛋白质的融合蛋白。融合蛋白可含有与接头共价结合的一种蛋白质,所述接头进而与另一分子共价结合。可用于形成融合蛋白的接头的实例包括含肽的接头,如含有天然存在的或非天然存在的氨基酸的接头。在一些实施方案中,可能需要在接头中包含d-氨基酸,因为这些残基不存在于天然存在的蛋白质中并且因此对内源性蛋白酶的降解更具抗性。接头可使用本领域中熟知的各种策略来制备,并且取决于接头的反应性组分可通过酶水解、光解、在酸性条件下的水解、在碱性条件下的水解、氧化、二硫化物还原、亲核裂解或有机金属裂解而裂解(leriche等人,bioorg.med.chem.,20:571-582,2012)。
130、如本文所用,术语“异种特异性抗体”是指对至少两种不同的抗原具有结合特异性的单克隆抗体,优选人或人源化抗体。传统上,异种特异性抗体的重组产生是基于两个免疫球蛋白重链-轻链对的共表达,其中两条重链具有不同特异性(milstein等人,nature 305:537,1983)。类似的程序公开于例如wo 93/08829;美国专利号6,210,668;6,193,967;6,132,992;6,106,833;6,060,285;6,037,453;6,010,902;5,989,530;5,959,084;5,959,083;5,932,448;5,833,985;5,821,333;5,807,706;5,643,759;5,601,819;5,582,996;5,496,549;4,676,980;wo 91/00360;wo 92/00373;ep 03089;traunecker等人,embo j.10:3655(1991);suresh等人,methods in enzymology 121:210(1986)中;其以引用的方式并入本文。异种特异性抗体可包含在多特异性抗体中强制正确链结合的fc突变,如klein等人,mabs 4(6):653-663,2012所描述;其以引用的方式并入本文。
131、如本文所用,术语“人抗体”是指其中蛋白质的基本上每个部分(例如,cdr、框架、cl、ch结构域(例如,ch1、ch2、ch3)、铰链、(vl,vh))在人中是基本上非免疫原性、只有微小序列变化或变异的抗体。人抗体可在人细胞中(例如,通过重组表达)产生或者由能够表达功能重排的人免疫球蛋白(例如,重链和/或轻链)基因的非人动物或原核或真核细胞产生。此外,当人抗体是单链抗体时,它可包括不存于天然人抗体中的接头肽。例如,fv可包含接头肽,如2至约8个甘氨酸或其他氨基酸残基,所述接头肽连接重链的可变区和轻链的可变区。此类接头肽被认为具有人源。人抗体可通过本领域已知的多种方法来制备,所述方法包括使用源自人免疫球蛋白序列的抗体文库的噬菌体展示方法。参见美国专利号4,444,887和4,716,111;以及pct公布wo 1998/46645;wo 1998/50433;wo 1998/24893;wo 1998/16654;wo 1996/34096;wo 1996/33735;和wo 1991/10741;其以引用的方式并入本文。人抗体还可使用不能表达功能性内源免疫球蛋白、但可表达人免疫球蛋白基因的转基因小鼠来产生。参见例如,pct公布wo 98/24893;wo 92/01047;wo 96/34096;wo 96/33735;美国专利号5,413,923;5,625,126;5,633,425;5,569,825;5,661,016;5,545,806;5,814,318;5,885,793;5,916,771;以及5,939,598;其以引用的方式并入本文。
132、如本文所用,术语“人源化”抗体是指非人(例如,鼠类)抗体的形式,所述形式是嵌合免疫球蛋白、免疫球蛋白链或其片段(如fv、fab、fab'、f(ab')2或抗体的其他靶结合亚结构域),其含有源自非人免疫球蛋白的最小序列。通常,所述人源化抗体将包含至少一个且通常两个可变结构域的基本全部,其中全部或基本全部的cdr区对应于非人免疫球蛋白的那些。全部或基本全部的fr区也可以是人免疫球蛋白序列的那些。人源化抗体还可包含免疫球蛋白恒定区(fc)的至少一部分,通常是人免疫球蛋白共有序列的至少一部分。抗体人源化的方法是本领域中已知的。参见例如,riechmann等人,nature 332:323-7,1988;queen等人的美国专利号5,530,101;5,585,089;5,693,761;5,693,762;以及6,180,370;ep239400;pct公布wo 91/09967;美国专利号5,225,539;ep592106;以及ep519596;其以引用的方式并入本文。
133、如本文所用,术语“疏水性侧链”是指由于例如侧链内存在的化学部分的空间或电子性质而在水中表现出低溶解度的氨基酸侧链。含有疏水性侧链的氨基酸的实例包括含有不饱和脂族烃的那些,如丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸和甲硫氨酸;以及含有在生理ph下静电中性的芳环系统的氨基酸,如色氨酸、苯丙氨酸和酪氨酸。
134、如本文所用,术语“免疫治疗剂”是指如本文所述的化合物,如抗体、其抗原结合片段、单链多肽或构建体,所述化合物特异性地结合免疫检查点受体或配体并且对受体或配体发挥拮抗性作用,从而减少或抑制受体或配体的信号转导,所述受体或配体的信号转导否则会导致免疫响应的下调。免疫治疗剂包括化合物,如抗体、抗原结合片段、单链多肽和的构建体,所述化合物能够特异性地结合在造血细胞如淋巴细胞(例如t细胞)表面上表达的受体,并且遏制由受体或配体诱导的信号传导,所述信号传导否则将导致针对内源性(“自身”)抗原(如肿瘤相关抗原)的耐受性。免疫治疗剂可使由受体或配体诱导的信号传导相对于在所述免疫治疗剂不存在下表现出的由所述受体或配体诱导的信号传导降低例如1%、2%、3%、4%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、96%、97%、98%、99%、99.9%或100%。可用于测量受体或配体信号传导的程度的示例性测定包括例如,用于测量与特定信号转导途径相关的蛋白质表达改变的酶联免疫吸附测定(elisa)技术,以及基于聚合酶链式反应(pcr)的技术,如可用于确定与特定信号转导途径相关的基因表达的变化的定量pcr、逆转录pcr和实时pcr实验等。可用于确定剂是否是“免疫治疗剂”的示例性方法包括mahoney等人,cancer immunotherapy,14:561-584(2015)中描述的测定,其公开内容以引用的方式整体并入本文。免疫治疗剂的实例包括例如,特异性地结合以下中的一种或多种的抗体或其抗原结合片段:ox40l、tl1a、cd40l、light、btla、lag3、tim3、singlecs、icos、b7-h3、b7-h4、vista、tmigd2、btnl2、cd48、kir、lir、lir抗体、ilt、nkg2d、nkg2a、mica、micb、cd244、csf1r、ido、tgfβ、cd39、cd73、cxcr4、cxcl12、sirpa、cd47、vegf和神经纤毛蛋白。免疫治疗剂的另外实例包括塔革雷汀、干扰素-α、氯倍他索、peg干扰素(例如,)、泼尼松、罗米地辛、贝沙罗汀、甲氨蝶呤、曲安西龙乳膏、抗趋化因子、伏立诺他、加巴喷丁、针对淋巴细胞表面受体和/或淋巴因子的抗体、针对表面癌蛋白的抗体和/或小分子疗法如伏立诺他。
135、如本文所用,术语“单克隆抗体”是指来源于单一克隆(包括任何真核、原核或噬菌体克隆)的抗体,而不是指产生所述抗体的方法。
136、如本文所用,术语“多特异性抗体”是指对多于一种靶抗原表现出亲和力的抗体。多特异性抗体可具有与完整免疫球蛋白分子相似的结构,并且包括fc区,例如igg fc区。此类结构可包括但不限于igg-fv、igg-(scfv)2、dvd-ig、(scfv)2-(scfv)2-fc和(scfv)2-fc-(scfv)2。在igg-(scfv)2的情况下,scfv可连接至重链或轻链的n-末端或c-末端。包含fc区并且抗tnfr2抗体或其抗原结合片段可掺入其中的示例性多特异性分子已由kontermann,2012,mabs 4(2):182-197;yazaki等人,2013,protein engineering,design&selection26(3):187-193和grote等人,2012,在proetzel&ebersbach(eds.),antibody methods andprotocols,methods in molecular biology第901卷,第16章:247-263中进行了综述;其以引用的方式并入本文。在一些实施方案中,基于igg或dvd或scfv的片段,抗体片段可以是无fc区的多特异性分子的组分。缺乏fc区并且抗体或抗体片段可掺入其中的示例性多特异性分子包括scfv二聚体(双抗体)、三聚体(三抗体)和四聚体(四抗体),fab二聚体(通过粘附多肽或蛋白质结构域缀合)和fab三聚体(化学缀合的)由hudson和souriau,2003,naturemedicine 9:129-134描述;所述文献以引用的方式并入本文。
137、如本文所用,术语“骨髓源性抑制细胞”或“mdsc”是指免疫系统的调节多种效应细胞和抗原呈递细胞的活性的细胞,如t细胞、nk细胞、树突细胞和巨噬细胞等。骨髓源性抑制细胞通过它们的基因表达谱区分,并且表达选自由以下组成的组的蛋白质和小分子的全部或子集:b7-1(cd80)、b7-h1(pd-l1)、ccr2、cd1d、cd1d1、cd2、cd31(pecam-1)、cd43、cd44、补体组分c5ar1、f4/80(emr1)、fcγriii(cd16)、fcγrii(cd32)、fcγriia(cd32a)、fcγriib(cd32b)、fcγriib/c(cd32b/c)、fcγriic(cd32c)、fcγriiia(cd16a)、fcγriiib(cd16b)、半乳糖凝集素-3、gp130、gr-1(ly-6g)、icam-1(cd54)、il-1ri、il-4rα、il-6rα、整联蛋白α4(cd49d)、整联蛋白αl(cd11a)、整联蛋白αm(cd11b)、m-csfr、mgl1(cd301a)、mgl1/2(cd301a/b)、mgl2(cd301b)、一氧化氮、psgl-1(cd162)、l-选择蛋白(cd62l)、siglec-3(cd33)、转铁蛋白受体(tfr)、vegfr1(flt-1)以及vegfr2(kdr或flk-1))。特别地,mdsc不表达选自由b7-2(cd86)、b7-h4、cd11c、cd14、cd21、cd23(fcεrii)、cd34、cd35、cd40(tnfrsf5)、cd117(c-kit)、hla-dr以及sca-1(ly6)组成的组的蛋白质。
138、如本文所用,术语“中性tnfr2多肽”和“表型-中性tnfr2多肽”是指结合tnfr2并且不发挥对tnfr2活化的拮抗或激动作用的多肽(如单链多肽、抗体或抗体片段)。例如,如果tnfr2多肽结合tnfr2并且既不加强也不遏制tnfr2活化,例如,如通过测量表达tnfr2的细胞(例如,t-reg细胞、tnfr2+癌细胞和/或mdsc)和/或通过测量一种或多种nfκb靶基因(如chuk、nfkbie、nfkbia、map3k11、traf2、traf3、relb和/或ciap2/birc3)的表达,则所述多肽是中性tnfr2多肽。用于测量细胞增殖和基因表达的示例性测定分别描述于例如实施例9和12中。
139、如本文所用,术语“非天然恒定区”是指抗体恒定区,源自不同于抗体可变区的来源或者是具有不同于天然抗体恒定区序列的氨基酸序列的人源合成多肽的抗体恒定区。例如,含有非天然恒定区的抗体可具有源自非人来源(例如,小鼠、大鼠或兔)的可变区和源自人来源的恒定区(例如,人抗体恒定区),或者源自另一种灵长类动物、猪、山羊、兔、仓鼠、猫、狗、豚鼠、牛科动物的成员(如牛、野牛、水牛、麋鹿和牦牛等)、奶牛、绵羊、马或野牛等的恒定区。
140、如本文所用,术语“序列同一性百分比(%)”是指在比对序列并且(必要时)引入空位以获得最大序列同一性百分比(例如,为了进行最佳比对,可将空位引入候选序列和参考序列中的一个或两个,并且为了比较目的,可忽略非同源序列)之后,候选序列中与参考序列的氨基酸(或核酸)残基相同的氨基酸(或核酸)残基的百分比。用于确定序列同一性百分比的目的的比对可以本领域技术范围内的各种方式实现,所述方式例如使用可公开获得的计算机软件,如blast、align或megalign(dnastar)软件。本领域技术人员可确定用于测量比对的适当参数,包括为在所比较序列的全长上实现最大比对所需的任何算法。例如,出于比较与候选序列进行比对的参考序列可显示,候选序列在候选序列的全长或在候选序列的连续氨基酸(或核酸)残基的选定部分上表现出50%至100%的序列同一性。出于比较目的而比对的候选序列的长度可以是例如,参考序列的长度的至少30%(例如,30%、40、50%、60%、70%、80%、90%或100%)。当候选序列中的位置由与参考序列中的相应位置相同的氨基酸残基占据时,则在所述位置处的分子是相同的。
141、如本文所用,术语“灵长类化抗体”是指包含来自灵长类动物来源的抗体的框架区和来自非灵长类动物来源的抗体的其他区(如cdr和/或恒定区)的抗体。用于产生灵长类化抗体的方法是本领域中已知的。参见例如,美国专利号5,658,570;5,681,722;和5,693,780;所述专利以引用的方式并入本文。例如,本发明的灵长类化抗体或其抗原结合片段可通过将非灵长类动物抗体或其抗原结合片段的cdr插入含有灵长类动物的一个或多个框架区的抗体或其抗原结合片段中来产生。
142、如本文所用,在多核苷酸片段的背景下术语“可操作地连接”意图指将两个多核苷酸片段连接以使得由所述两个多核苷酸片段编码的氨基酸序列保持在框内。
143、如本文所用,术语“药物代谢动力学概况”是指在将药物施用至患者后药物随时间推移的吸收、分布、代谢和清除。
144、如本文所用,tnfr2的“隐性拮抗剂”是在诸如tnfα或il-2的tnfr2激动剂存在下将tnfr2活化抑制至相对于如在诸如tnfα或il-2的tnfr2激动剂不存在下测量的相同拮抗剂的抑制程度显著更低程度的拮抗剂(例如,拮抗性多肽,如单链多肽、抗体或其抗原结合片段)。例如,如果在tnfr2激动剂(例如,tnfα)或il-2存在下拮抗剂的ic50相对于如在tnfr2激动剂(如tnfα或il-2)不存在下在相同测定中测量的拮抗剂的ic50增加例如10倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍或更多倍,则tnfr2拮抗剂是隐性拮抗剂。可例如通过测量tnfr2+细胞(如t-reg细胞,表达tnfr2的癌细胞,或骨髓源性抑制细胞)的增殖的抑制以及通过测量nfκb信号传导的抑制(例如,通过在常规基因表达测定中监测选自由chuk、nfkbie、nfkbia、map3k11、traf2、traf3、relb以及ciap2/birc3组成的组的一种或多种基因的表达降低)来评估tnfr2活化的抑制。本文描述了可用于监测tnfr2活化的细胞增殖测定和基因表达测定(例如分别在实施例9和12中)。
145、如本文所用,术语“调控序列”包括控制抗体链基因的转录或翻译的启动子、增强子和其他表达控制元件(例如,聚腺苷酸化信号)。此类调控序列描述于例如goeddel,geneexpression technology:methods in enzymology 185(academic press,san diego,ca,1990)中;所述文献以引用的方式并入本文。
146、如本文所用,术语“scfv”是指单链fv抗体,其中来自抗体的重链和轻链的可变结构域已经连接以形成一条链。scfv片段含有单条多肽链,所述多肽链包含通过接头隔开的抗体轻链(vl)的可变区(例如,cdr-l1、cdr-l2和/或cdr-l3)和抗体重链(vh)的可变区(例如,cdr-h1、cdr-h2和/或cdr-h3)。连接scfv片段的vl和vh区的接头可以是由蛋白原氨基酸组成的肽接头。可使用替代接头以便增加scfv片段对蛋白水解降解的抗性(例如,含有d-氨基酸的接头),以便增强scfv片段的溶解度(例如,亲水性接头如含有重复甘氨酸和丝氨酸残基的含聚乙二醇的接头或多肽),以改善分子的生物物理稳定性(例如,含有形成分子内或分子间二硫键的半胱氨酸残基的接头),或者以减弱scfv片段的免疫原性(例如,含有糖基化位点接头)。scfv分子是本领域中已知的并且描述于例如美国专利5,892,019;flo等人,(gene 77:51,1989);bird等人,(science 242:423,1988);pantoliano等人,(biochemistry 30:10117,1991);milenic等人,(cancer research51:6363,1991);以及takkinen等人,(protein engineering 4:837,1991)中。scfv分子的vl和vh结构域可源自一种或多种抗体分子。本领域普通技术人员还将理解,可修饰本发明的scfv分子的可变区,以使得它们的氨基酸序列与它们所源自的抗体分子不同。例如,在一个实施方案中,可(例如,在cdr和/或框架残基中)进行导致氨基酸残基的保守取代或改变的核苷酸或氨基酸取代。或者或另外,使用本领域公认的技术对cdr氨基酸残基进行突变以优化抗原结合。scfv片段描述于例如wo 2011/084714中;其以引用的方式并入本文。
147、如本文所用,短语“特异性地结合”是指以特殊性决定蛋白质和其他生物分子的异源群体中抗原的存在的结合反应,所述蛋白质和其他生物分子例如通过抗体或其抗原结合片段识别。特异性地结合至抗原的抗体或其抗原结合片段将以小于100nm的kd结合至抗原。例如,特异性地结合至抗原的抗体或其抗原结合片段将以达100nm(例如,1pm与100nm之间)的kd结合至抗原。未表现出与特定抗原或其表位的特异性结合的抗体或其抗原结合片段将对所述特定抗原或其表位表现出大于100nm(例如,大于500nm、1μm、100μm、500μm或1mm)的kd。可使用多种免疫测定形式来选择与特定蛋白质或碳水化合物特异性免疫反应的抗体。例如,固相elisa免疫测定常规地用于选择与蛋白质或碳水化合物特异性免疫反应的抗体。关于可用于确定特异性免疫反应性的免疫测定形式和条件的描述,参见harlow和lane,antibodies,a laboratory manual,cold spring harbor press,new york(1988)以及harlow和lane,using antibodies,a laboratory manual,cold spring harborpress,newyork(1999)。
148、如本文所用,术语“受试者”和“患者”是指接受针对如本文所述的特定疾病或病状(如癌症或感染性疾病)的治疗的生物体。受试者和患者的实例包括接受针对疾病或病状(例如,诸如癌症或感染性疾病的细胞增殖病症)的治疗的哺乳动物,如人、灵长类动物、猪、山羊、兔、仓鼠、猫、狗、豚鼠、牛科的成员(如牛、野牛、水牛、麋鹿和牦牛等)、奶牛、绵羊、马和野牛等。
149、如本文所用,术语“转染”是指通常用于将外源dna引入原核或真核宿主细胞中的多种技术中的任一种,例如电穿孔、脂质转染、磷酸钙沉淀、deae-葡聚糖转染等。
150、如本文所用,术语“治疗(treat)”或“治疗(treatment)”是指目的是预防或减缓(减轻)不希望的生理变化或病症,如细胞增殖病症(如癌症或感染性疾病)的进展的治疗性治疗。有益或所需的临床结果包括但不限于症状减轻、疾病程度减轻、疾病状态稳定化(即未恶化)、疾病进展延迟或减缓、疾病状态改善或缓和以及缓解(无论是部分缓解还是全部缓解),无论是可检测的还是不可检测的。需要治疗的那些包括已患有病状或病症的那些以及易于患上病状或病症的那些或有待预防病状或病症的那些。
151、如本文所用,术语“肿瘤微环境”是指形成肿瘤的癌细胞以及肿瘤内或肿瘤边界或围绕癌细胞的非癌细胞、分子和/或血管的群体。
152、如本文所用,术语“肿瘤坏死因子受体超家族”、“tnfr超家族”或“tnfrs”是指特征在于常见富含半胱氨酸的结构域(crd)的具有羧基末端细胞内结构域和氨基末端细胞外结构域的一组i型跨膜蛋白。tnfr超家族包括由于与tnf超家族中的一种或多种配体结合而介导细胞信号传导的受体。tnfr超家族可分成两个亚组:含有细胞内死亡结构域的受体和缺乏这种结构域的那些受体。死亡结构域是80个氨基酸的基序,所述基序在受体活化后传播细胞凋亡信号转导级联。含有细胞内死亡结构域的示例性tnfr超家族成员包括tnfr1,而tnfr2表示不含这种结构域的tnfr超家族蛋白。tnfr超家族的成员包括tnfr1、tnfr2、rank、cd30、cd40、淋巴毒素β受体(lt-βr)、ox40、fas受体、诱饵受体3(dcr3)、cd27、4-1bb、死亡受体4(dr4)、死亡受体5(dr5)、诱饵受体1(dcr1)、诱饵受体2(dcr2)、骨保护素、tweak受体、taci、baff受体、疱疹病毒进入介质、神经生长因子受体、b细胞成熟抗原、糖皮质激素诱导的tnfr-相关的troy、死亡受体6(dr6)、死亡受体3(dr3)和外异蛋白a2受体。
153、如本文所用,术语“可变区cdr”包括如使用基于序列或结构的方法鉴定的cdr或互补决定区中的氨基酸。如本文所用,术语“cdr”或“互补决定区”是指在重链和轻链多肽两者的可变区内发现的非连续抗原结合位点。这些特定区已由以下文献描述:kabat等人,j.biol.chem.252:6609-6616,1977和kabat,等人,sequences of proteins ofimmunological interest,第五版,美国卫生和公共服务部,nih出版号91-3242,1991;chothia等人,(j.mol.biol.196:901-917,1987)以及maccallum等人,(j.mol.biol.262:732-745,1996),其中定义包括当彼此比较时氨基酸残基的重叠或子集。在某些实施方案中,术语“cdr”是由kabat基于序列比较定义的cdr。
154、如本文所用,术语“载体”包括核酸载体,例如dna载体,如质粒、rna载体、病毒或其他合适的复制子(例如,病毒载体)。已经开发了多种载体用于将编码外源蛋白质的多核苷酸递送到原核或真核细胞中。此类表达载体的实例公开于例如wo 1994/11026中;其以引用的方式并入本文。本发明的表达载体含有多核苷酸序列以及例如用于表达蛋白质和/或将这些多核苷酸序列整合到哺乳动物细胞的基因组中的另外序列元件。可用于表达本发明的抗体和抗体片段的某些载体包括含有调控序列的质粒,如指导基因转录的启动子和增强子区。用于表达抗体和抗体片段的其他有用载体含有多核苷酸序列,所述多核苷酸序列增强这些基因的翻译速率或改善由基因转录产生的mrna的稳定性或核输出。这些序列元件包括例如5'和3'非翻译区、内部核糖体进入位点(ires)和聚腺苷酸化信号位点,以便指导表达载体上携带的基因的有效转录。本发明的表达载体还可含有编码用于选择含有这种载体的细胞的标记的多核苷酸。合适的标记的实例包括编码对抗生素(如氨苄青霉素、氯霉素、卡那霉素或诺尔丝菌素)的抗性的基因。
155、如本文所用,术语“vh”是指抗体的免疫球蛋白重链的可变区,包括fv、scfv或fab的重链。提及“vl”是指免疫球蛋白轻链的可变区,包括fv、scfv、dsfv或fab的轻链。抗体(ab)和免疫球蛋白(ig)是具有相同结构特征的糖蛋白。虽然抗体表现出对特定靶标的结合特异性,但免疫球蛋白包括抗体和缺乏靶标特异性的其他抗体样分子两者。天然抗体和免疫球蛋白通常是约150,000道尔顿的异四聚体糖蛋白,其由两条相同的轻(l)链和两条相同的重(h)链组成。天然抗体的每条重链在氨基末端具有可变结构域(vh),随后是许多恒定结构域。天然抗体的每条轻链在氨基末端(vl)具有可变结构域,并且在羧基末端具有恒定结构域。
- 还没有人留言评论。精彩留言会获得点赞!