试剂盒及其制备方法和使用方法以及即用型测定培养基的制备方法与流程
本发明涉及培养基领域,具体而言,涉及一种试剂盒及其制备方法和使用方法以及即用型测定培养基的制备方法。
背景技术:
1、现有技术中,水溶性b维生素的检测在国标方法中多采用微生物方法,以叶酸为例,作为鼠李糖乳杆菌lactobacillus rhamnosus(atcc 7469)生长所必需的营养素,在一定控制条件下,将鼠李糖乳杆菌接种至含有试样液的培养液中,培养一段时间后测定透光率(或吸光度值),根据叶酸含量与透光率(或吸光度值)的标准曲线计算出试样中叶酸的含量。此方法中,维生素检测培养基的性能对最终检测结果有着关键影响。该培养基成分复杂、微量成分繁多、保质期短,对于维生素快速检测产品——即用型试剂盒而言,培养基的处理方式一直是一个难点。
技术实现思路
1、本发明的主要目的在于提供一种试剂盒及其制备方法和使用方法以及即用型测定培养基的制备方法,以解决现有技术中即用型测定培养基的稳定性差、保质期短的问题。
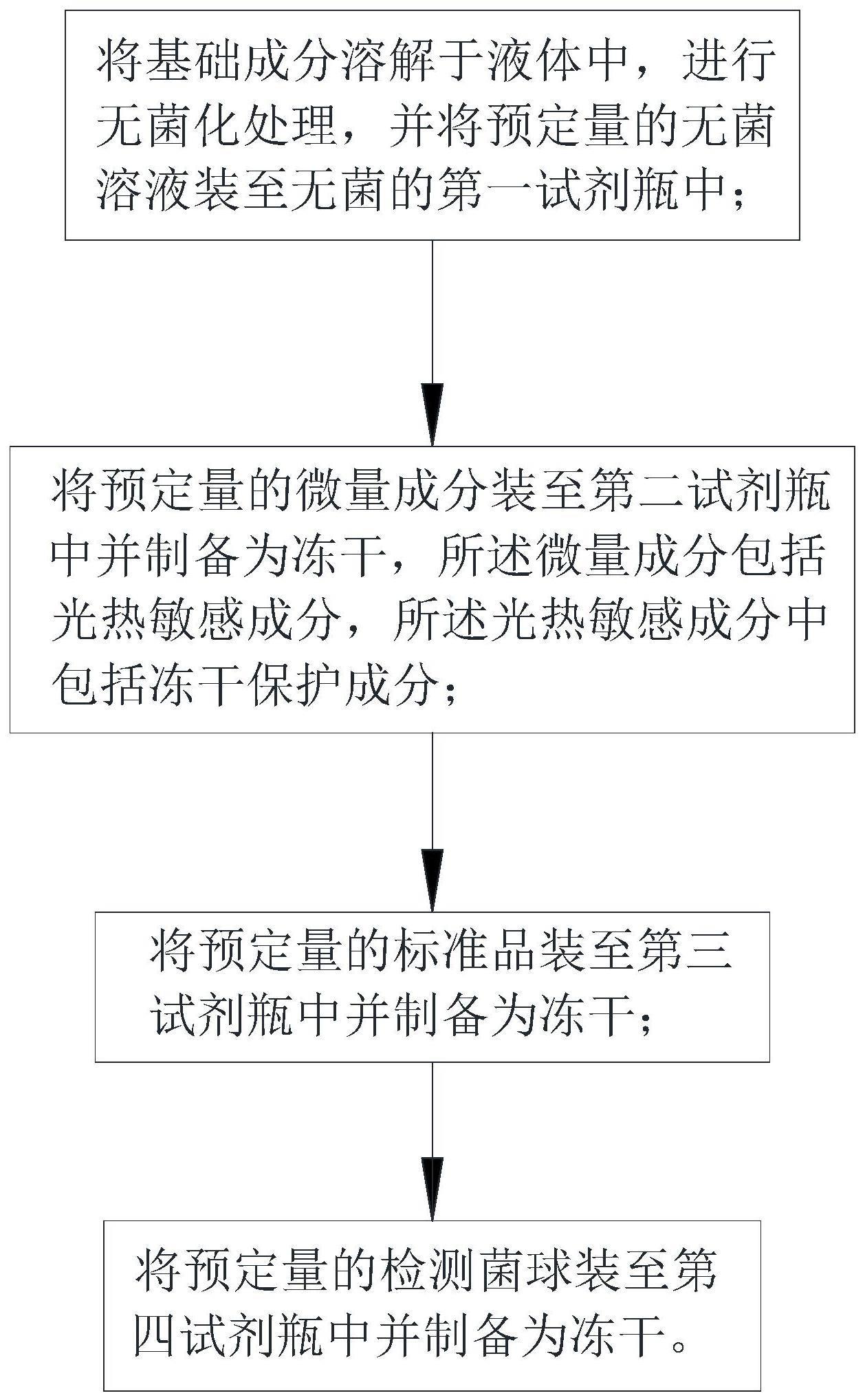
2、为了实现上述目的,根据本发明的一个方面,提供了一种试剂盒的制备方法,试剂盒用以制备即用型测定培养基,即用型测定培养基为叶酸即用型测定培养基、维生素b12即用型测定培养基、生物素即用型测定培养基与泛酸即用型测定培养基中的任一种,试剂盒的制备方法包括:将基础成分溶解于液体中,进行无菌化处理,并将预定量的无菌溶液装至无菌的第一试剂瓶中;将预定量的微量成分装至第二试剂瓶中并制备为冻干,微量成分包括光热敏感成分,光热敏感成分中包括冻干保护成分;其中,在即用型测定培养基为叶酸即用型测定培养基的情况下,基础成分包括:酸水解无维生素酪蛋白、无水葡萄糖、三水合乙酸钠、磷酸氢二钾以及磷酸二氢钾,微量成分包括:葡萄糖、l-色氨酸、l-盐酸半胱氨酸、l-天冬氨酸、硫酸腺嘌呤、盐酸鸟嘌呤、尿嘧啶、黄嘌呤、聚山梨酯-80、还原型谷胱甘肽、七水合硫酸镁、氯化钠、七水合硫酸亚铁、一水合硫酸锰、核黄素、对氨基苯甲酸、盐酸吡哆醇、盐酸硫胺素、泛酸钙、尼克酸以及生物素;在即用型测定培养基为维生素b12即用型测定培养基的情况下,基础成分包括:酸水解无维生素酪蛋白、无水葡萄糖、乙酸钠、抗坏血酸、磷酸氢二钾以及磷酸二氢钾,微量成分包括:葡萄糖、天门冬酰胺、l-胱氨酸、dl-色氨酸、硫酸腺嘌呤、盐酸鸟嘌呤、尿嘧啶、黄嘌呤、核黄素、盐酸硫胺素、生物素、烟酸、ρ-氨基苯甲酸、泛酸钙、盐酸吡哆醇、盐酸吡哆醛、烟酸吡哆胺、叶酸、硫酸镁、氯化钠、硫酸亚铁、硫酸锰以及聚山梨糖单油酸酯;在即用型测定培养基为生物素即用型测定培养基的情况下,基础成分包括:酸水解无维生素酪蛋白、无水葡萄糖、乙酸钠、磷酸氢二钾以及磷酸二氢钾,微量成分包括:无水葡萄糖、l-胱氨酸、dl-色氨酸、硫酸腺嘌呤、盐酸鸟嘌呤、尿嘧啶、盐酸硫胺素、核黄素、烟酸、泛酸钙、盐酸吡哆醇、ρ-氨基苯甲酸、硫酸镁、氯化钠、硫酸亚铁以及硫酸锰;在即用型测定培养基为泛酸即用型测定培养基的情况下,基础成分包括:酸水解无维生素酪蛋白、无水葡萄糖、乙酸钠、磷酸氢二钾以及磷酸二氢钾,微量成分包括:无水葡萄糖、l-胱氨酸、l-色氨酸、硫酸镁、氯化钠、硫酸亚铁、硫酸锰、硫酸腺嘌呤、盐酸鸟嘌呤、尿嘧啶、核黄素、盐酸硫胺素、生物素、ρ-氨基苯甲酸、烟酸、盐酸吡哆醇以及聚山梨糖单油酸酯。
3、在一个实施方式中,试剂盒用以进行维生素测定,试剂盒的制备方法还包括:将预定量的标准品装至第三试剂瓶中并制备为冻干;和/或,将预定量的检测菌球装至第四试剂瓶中并制备为冻干;其中,在即用型测定培养基为叶酸即用型测定培养基的情况下,标准品为叶酸标准品,检测菌球为叶酸检测菌球;在即用型测定培养基为维生素b12即用型测定培养基的情况下,标准品为维生素b12标准品,检测菌球为维生素b12检测菌球;在即用型测定培养基为生物素即用型测定培养基的情况下,标准品为生物素标准品,检测菌球为生物素检测菌球;在即用型测定培养基为泛酸即用型测定培养基的情况下,标准品为泛酸标准品,检测菌球为泛酸检测菌球。
4、在一个实施方式中,将预定量的微量成分装至第二试剂瓶中并制备为冻干,微量成分包括光热敏感成分,光热敏感成分中包括冻干保护成分,包括:将微量成分按配方配置成浓缩50倍的浓缩溶液并将预定量的浓缩溶液装入第二试剂瓶中,微量成分包括光热敏感成分,光热敏感成分中包括冻干保护成分;将第二试剂瓶放入设备中以进行冻干操作;密封第二试剂瓶。
5、在一个实施方式中,在即用型测定培养基为叶酸即用型测定培养基的情况下,配置1000ml的浓缩液的基础成分的配方为:酸水解无维生素酪蛋白10g、无水葡萄糖39g、三水合乙酸钠40g、磷酸氢二钾2g以及磷酸二氢钾2g;配置1000ml的浓缩液的微量成分的配方为:葡萄糖1g、l-色氨酸0.4g、l-盐酸半胱氨酸0.4g、l-天冬氨酸0.6g、硫酸腺嘌呤20mg、盐酸鸟嘌呤20mg、尿嘧啶20mg、黄嘌呤20mg、聚山梨酯-80 0.1g、还原型谷胱甘肽5mg、七水合硫酸镁0.4g、氯化钠20mg、七水合硫酸亚铁20mg、一水合硫酸锰20mg、核黄素1mg、对氨基苯甲酸2mg、盐酸吡哆醇4mg、盐酸硫胺素400μg、泛酸钙800μg、尼克酸800μg以及生物素20μg;在即用型测定培养基为维生素b12即用型测定培养基的情况下,配置1000ml的浓缩液的基础成分的配方为:酸水解无维生素酪蛋白15g、无水葡萄糖39g、乙酸钠20g、抗坏血酸4.0g、磷酸氢二钾1.0g以及磷酸二氢钾1.0g;配置1000ml的浓缩液的微量成分的配方为:葡萄糖1.0g、天门冬酰胺0.2g、l-胱氨酸0.4g、dl-色氨酸0.4g、硫酸腺嘌呤20.0mg、盐酸鸟嘌呤20.0mg、尿嘧啶20.0mg、黄嘌呤20.0mg、核黄素1.0mg、盐酸硫胺素1.0mg、生物素10.0μg、烟酸2.0mg、ρ-氨基苯甲酸2.0mg、泛酸钙1.0mg、盐酸吡哆醇4.0mg、盐酸吡哆醛4.0mg、烟酸吡哆胺800μg、叶酸200μg、硫酸镁0.4g、氯化钠20.0mg、硫酸亚铁20.0mg、硫酸锰20mg以及聚山梨糖单油酸酯2.0g;在即用型测定培养基为生物素即用型测定培养基的情况下,配置1000ml的浓缩液的基础成分的配方为:酸水解无维生素酪蛋白12g、无水葡萄糖39g、乙酸钠20g、磷酸氢二钾1.0g以及磷酸二氢钾1.0g;配置1000ml的浓缩液的微量成分的配方为:无水葡萄糖1.0g、l-胱氨酸0.2g、dl-色氨酸0.2g、硫酸腺嘌呤20.0mg、盐酸鸟嘌呤20.0mg、尿嘧啶20.0mg、盐酸硫胺素2.0mg、核黄素2.0mg、烟酸2.0mg、泛酸钙2.0mg、盐酸吡哆醇4.0mg、ρ-氨基苯甲酸200.0μg、硫酸镁0.4g、氯化钠20.0mg、硫酸亚铁20.0mg以及硫酸锰20mg;在即用型测定培养基为泛酸即用型测定培养基的情况下,配置1000ml的浓缩液的基础成分的配方为:酸水解无维生素酪蛋白5g、无水葡萄糖39g、乙酸钠33g、磷酸氢二钾1.0g以及磷酸二氢钾1.0g;配置1000ml的浓缩液的微量成分的配方为:无水葡萄糖1.0g、l-胱氨酸0.4、l-色氨酸0.1g、硫酸镁0.4g、氯化钠20.0mg、硫酸亚铁20.0mg、硫酸锰20mg、硫酸腺嘌呤20.0mg、盐酸鸟嘌呤20.0mg、尿嘧啶20.0mg、核黄素400μg、盐酸硫胺素200μg、生物素0.8μg、ρ-氨基苯甲酸200.0μg、烟酸1.0mg、盐酸吡哆醇800μg以及、聚山梨糖单油酸酯0.1g。
6、在一个实施方式中,设备为真空冷冻干燥仪,真空冷冻干燥仪的固定化干燥冻干程序包括:预冻阶段、一次升华干燥阶段、二次升华干燥阶段以及解析干燥阶段。
7、在一个实施方式中,当真空冷冻干燥仪执行预冻阶段的程序时,真空冷冻干燥仪内的温度为-65℃并保持1.0h;和/或,当真空冷冻干燥仪执行一次升华干燥阶段的程序时,真空冷冻干燥仪内的温度为-55℃,真空度为0.22mbar并保持8h;和/或,当真空冷冻干燥仪执行二次升华干燥阶段的程序时,真空冷冻干燥仪内的温度在-55℃-0℃之间并保持12h;和/或,当真空冷冻干燥仪执行解析干燥阶段的程序时,真空冷冻干燥仪内的温度在25℃,真空度控制在0.010mbar,并保持8h。
8、在一个实施方式中,将预定量的无菌溶液装至无菌的第一试剂瓶中包括:将无菌化处理后的基础成分溶液分装至两种规格的第一试剂瓶中,第一种规格和第二种规格的第一试剂瓶中分别装有250ml和20ml的基础成分溶液;将预定量的浓缩溶液装入第二试剂瓶中包括:将浓缩50倍的浓缩溶液分装至两种规格的第二试剂瓶中,第一种规格和第二种规格的第二试剂瓶中在进行冻干操作之前分别装有5ml和0.4ml的浓缩溶液。
9、在一个实施方式中,将基础成分溶解于液体中,进行无菌化处理,并将预定量的无菌溶液装至无菌的第一试剂瓶中包括:将基础成分溶解于去离子水或蒸馏水中,完全溶解后,使用孔径为0.22μm~0.45μm无菌滤膜过滤除菌设备将溶解后的溶液过滤装至无菌的第一试剂瓶中。
10、根据本发明的另一方面,提供了一种即用型测定培养基的制备方法,制备即用型测定培养基所使用的试剂盒为通过上述的即用型测定培养基的试剂盒的制备方法获得的试剂盒,即用型测定培养基的制备方法包括:将第二试剂瓶中的试剂溶解并加入第一试剂瓶中的试剂中,混匀。
11、根据本发明的又一方面,提供了一种试剂盒的使用方法,试剂盒为上述的试剂盒,使用方法包括:制备即用型测定培养基,将第二试剂瓶中的试剂溶解并加入第一试剂瓶中的试剂中,混匀,再将第四试剂瓶中的检测菌球全部加入至第一试剂瓶中,混匀;制备标准溶液,将预定量的无菌水加入至第三试剂瓶中混匀,再将混匀后的液体取预定量加入至预定量的无菌水中。
12、根据本发明的再一方面,提供了一种试剂盒,试剂盒采用上述的即用型测定培养基的试剂盒的制备方法获得。
13、根据本发明的最后一方面,提供了一种试剂盒,试剂盒采用上述的即用型测定培养基的试剂盒的制备方法获得,试剂盒具有两种规格,其中一种规格的试剂盒包括第一种规格的第一试剂瓶与第一种规格的第二试剂瓶,另一种规格的试剂盒包括第二种规格的第一试剂瓶与第二种规格的第二试剂瓶。
14、应用本发明的技术方案,将即用型测定培养基所需要的成分按照其特性分为稳定性主成分(即基础成分)与敏感成分(即光热敏感成分)两大类,其中稳定成分可以以液体形式稳定存放,将这些成分单独溶解,通过无菌过滤形式分装至无菌试剂瓶中,作为测定培养基基础可在冷藏避光条件下保存1年以上;敏感成分是培养基的重要组成部分,化学活性较强,为了不影响培养基的检测效果,将其通过先进的真空冻干工艺制备成冻干状态,敏感成分以冻干形式也可稳定保存1年,在1年保质期内性能良好。因此采用本实施例所制得的基础成分溶液与冻干均可稳定保存,为后续制备稳定性良好的即用型测定培养基打下良好的基础,最终实现保障培养基的检测效果,增加培养基的稳定性的目的。此外,应用实施例一的技术方案,使用时以培养基添加剂形式溶解后加入基础成分溶液中,简化了配制过程,即开即用,为微生物法检测维生素提供高效、稳定、准确的解决方案。最后,应用实施例一的技术方案,由于即用型测定培养基所需的光热敏感成分本身还包括葡萄糖、天冬氨酸和色氨酸等氨基酸(低分子量化合物保护剂,防止活性成分变性)、氯化钠(使溶液具有一定的离子强度)或聚山梨酯-80(一种表面活性剂)等能够在冻干过程中起到一定的保护作用的成分,因此无需额外添加其他成分的保护剂,简化了制备过程,提高了制备效率。
15、除了上面所描述的目的、特征和优点之外,本发明还有其它的目的、特征和优点。下面将参照图,对本发明作进一步详细的说明。
- 还没有人留言评论。精彩留言会获得点赞!